生物催化制备(S)-2-(2,5-二氟苯基)吡咯烷的方法与流程
本发明涉及一种医药中间体制备方法,尤其涉及一种生物酶催化制备(s)-2-(2,5-二氟苯基)吡咯烷的方法。
背景技术:
larotrectinib是由loxooncology公司和拜耳公司研发的一款广谱肿瘤药,用于所有表达有原肌球蛋白受体激酶(tropomyosinreceptorkinase,trk)的肿瘤患者,该药是一款针对特定基因突变,而不针对特定癌症种类的抗癌新药。其所能治疗的ntrk基因融合实体瘤包括乳腺癌、结直肠癌、肺癌、甲状腺癌等癌症类型。因此,larotrectinib(loxo-101)在美国获批被认为是癌症疗法从“基于癌症在体内的起源”转向“基于肿瘤的遗传特征”这一演变过程中的重要里程碑。
larotrectinib通用名为拉罗替尼,商品名为vitrakvi,结构式如式i。该药物在2016年7月13日被fda授予突破性药物资格,用于trk融合基因突变阳性的成人及儿童的不可手术切除或转移性实体瘤,2018年11月26日,被fda批准在美国上市。根据国家药监局药品审评中心(cde)网站公开信息可知,该药品以“硫酸larotrectinib胶囊”为名称的ind申请由拜耳公司申报,且已经于2019年1月14日获受理,该药在中国申报临床并获得受理,是该药在全球进行注册的又一大进展。
随着对拉罗替尼药理学研究的进一步推进,拉罗替尼的光学异构体也具备一定的市场需求。在工业化生产过程中,拉罗替尼光学异构体作为标准对照品将具备广泛的应用市场。目前拉罗替尼光学异构体并无专门的生产路线,而是作为拉罗替尼的拆分纯化副产品制备。但随着手性合成技术研究的不断伸入,作为副产物的拉罗替尼光学异构体产出逐步降低,难以满足市场需求。根据中国专利cn107987082(a)公开的一种合成拉罗替尼的工艺路线scheme1分析可知,(s)-2-(2,5-二氟苯基)吡咯烷将成为制备拉罗替尼光学异构体的关键中间体。
同时,(s)-2-(2,5-二氟苯基)吡咯烷也可以应用于其他化合物的合成过程中。
整合应激反应指细胞在氧化应激、氨基酸剥夺和内质网应激等情况下,通过真核细胞起始因子2(eif2α)/活化转录因子4(atf4)所介导的细胞适应反应。主要由内质网应激反应的perk途径介导,并通过整合调控蛋白质合成、折叠、细胞自噬与凋亡。可能会引起脑白质营养不良,癌症,炎性疾病,肌肉骨骼疾病,代谢疾病,或与eif2b功能受损或isr途径中的组分相关的疾病或病症。
专利wo2019090088(a1)报道一种化合物通式能够用在治疗此类疾病中,其中包含了结构式ii的化合物,含有片段(s)-2-(2,5-二氟苯基)吡咯烷。此化合物目前仍然处于临床实验过程中。
综上所述,(s)-2-(2,5-二氟苯基)吡咯烷不仅应用于拉罗替尼药物研究及生产领域,也会被用于一些新药研究中,因此未来将具有广泛的市场需求。
目前,仅专利cn108101820(a)报道一种制备(s)-2-(2,5-二氟苯基)吡咯烷的化学合成法,路线如scheme2所示。
此路线以2,5-二氟溴苯和n-甲氧基-n-甲基-4-氯丁酰胺为原料,经四步反应得到(s)-2-(2,5-二氟苯基)吡咯烷,需要用到格氏试剂参与反应,且需要柱层析纯化,收率较低,不适合工业化生产。
技术实现要素:
本发明的目的在于针对现有技术的不足,运用亚胺还原酶催化5-(2,5-二氟苯基)-3,4-二氢-2h-吡咯为(s)-2-(2,5-二氟苯基)吡咯烷,提高收率。
本发明采用的技术方案如scheme3所示:
进一步,生物催化制备(s)-2-(2,5-二氟苯基)吡咯烷的方法,其特征在于:将5-(2,5-二氟苯基)-3,4-二氢-2h-吡咯、亚胺还原酶酶粉或含有亚胺还原酶的细胞、辅酶、缓冲溶液配制成混合溶液,反应得到产物。
进一步,所述的亚胺还原酶的氨基酸序列如seqidno.1所示。
进一步,所述的亚胺还原酶的基因核苷酸序列如seqidno.2所示。
进一步,所述反应的反应时间为12~36h,优选为24h。
进一步,所述5-(2,5-二氟苯基)-3,4-二氢-2h-吡咯浓度为1~400g/l;亚胺还原酶酶粉浓度为1~10g/l,或含有亚胺还原酶的细胞的浓度为10~100g/l。
进一步,反应体系中可以加入辅酶促进反应,当采用含亚胺还原酶的细胞时,细胞内部含有少量辅酶,此时也可以不加入辅酶;某些情况下制备的亚胺还原酶酶粉中亦含有少量辅酶,此时也可以不加入辅酶。但反应体系中也可以加入辅酶进一步促进反应进行,当反应体系中加入辅酶促进反应时,所述辅酶选自nad+、nadh、nadp+、nadph或它们的组合物,优选nadp+。
更进一步,添加辅酶的浓度为0.02~0.4g/l,优选为0.05~0.10g/l。
更进一步,本技术方案中所采用的辅酶,均选自尚科生物医药(上海)有限公司对外销售的辅酶产品。
进一步,所述缓冲液为磷酸钾缓冲液。
进一步,本技术方案中,所述亚胺还原酶为来源于streptomycessp.gf3587的野生型亚胺还原酶。
进一步,所述含有亚胺还原酶的细胞由基因工程菌发酵得到,所述基因工程菌为基因工程改造的大肠杆菌或酵母菌。
附图说明
图1为底物标品的常规hplc分析谱图
图2为产物标品的常规hplc分析谱图
图3为实施例3的反应液常规hplc分析谱图
图4为消旋产物标品的手性hplc分析谱图
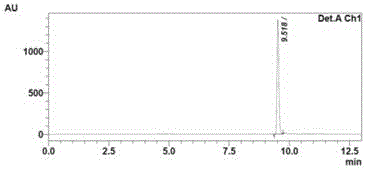
图5为r型产物标品的手性hplc分析谱图
图6为实施例3的反应液手性hplc分析谱图
具体实施方式
下面结合具体实施例对本发明的技术内容作进一步的阐述,其目的是为了更好的理解本发明的内容,但本发明的保护范围不限于此。
实施例1亚胺还原酶的筛选
使用本公司的亚胺还原酶(ired)酶库对底物进行反应筛选,反应体系组分如下:0.1mph7.0磷酸钾缓冲液,底物1g/l,dmso10%,nadp0.2g/l,葡萄糖10g/l,gdh(葡萄糖脱氢酶)5g/l,ired酶粉10g/l。于30℃反应24h,进行hplc检测。结果显示,筛到的效果最好的酶为来自于streptomycessp.gf3587的亚胺还原酶,转化率为98.2%,手性hplc检测显示产物手性纯度为96.6%,s构型为优势构型。
实施例2亚胺还原酶细胞的制备
将含有亚胺还原酶的编码基因(seqidno.2)的基因工程菌(载体pet24a,宿主细胞e.colibl21(de3))接种至5ml含卡那霉素的lb试管培养基中活化培养(37℃培养12h),按1%接种量转接活化培养物至380ml含卡那霉素的lb液体培养基中,37℃培养od至0.6-0.8,加入iptg(终浓度0.1mm)于25℃诱导培养16h。离心收集菌体得到亚胺还原酶细胞。
实施例3使用亚胺还原酶酶粉制备(2s)-2-(2,5-二氟苯基)吡咯烷
向100ml反应体系中加入0.1mph7.0磷酸钾缓冲液,底物10g/l,dmso10%,nadp0.2g/l,葡萄糖10g/l,gdh5g/l,亚胺还原酶细胞50g/l。于30℃反应24h,进行hplc检测。底物标品的常规hplc图谱如图1所示;产物标品的常规hplc图谱如图2所示;反应液的常规hplc图谱如附图3;消旋产物的手性hplc图谱如附图4所示;r型产物标品的手性hplc图谱如附图5所示;反应液的手性hplc图谱如图6所示。底物转化率为90.6%,s型产物手性纯度为96.6%。
序列表
<110>尚科生物医药(上海)有限公司
<120>生物催化制备(s)-2-(2,5-二氟苯基)吡咯烷的方法
<160>2
<170>siposequencelisting1.0
<210>1
<211>295
<212>prt
<213>streptomycessp.gf3587
<400>1
metglyalaalaalathrprovalthrvalileglyleuglyleumet
151015
glyglyalaleualaalaalaproleuglyalaglyhisthrthrthr
202530
valthralaalaseralaglyleualaglyglyleuvalserglygly
354045
alavalglyalaalathrproalaalaalavalalaalaserglyleu
505560
valvalvalcysleuserthrthralaalamethisalavalilegly
65707580
serleuglyglyserleualaglyleuvalilevalalaleuthrser
859095
glyserseralaglyglyalaglythralaalathralaglyleugly
100105110
glyvalglythrleualaglyalailemetilethrproproglyile
115120125
glythrglythralavalleuprothralaglythrglyservalpro
130135140
glyleuthrglyproalaleuleuleuleuglyglyglythrthrthr
145150155160
leuglythralahisglymetproalaleuthralavalserleuleu
165170175
glyleumetthrglythrleualaserproleuhisglyvalalaval
180185190
valglythralaglyvalglyalaglyglyproleuprothralahis
195200205
metthrleuglyalaileleumetprothralaalathralaalagly
210215220
ilealaalaglyalaglyleuproproalaalaalaalathrleugly
225230235240
thrhisleualaalaleuleuhisleuvalhisglyserglyalaleu
245250255
glyilealaalaglyleuproleuthrserglyalaleumetglyala
260265270
valileserglyglyhisalaleualaserthralaalavalleuleu
275280285
alaproalaleuprosergly
290295
<210>2
<211>888
<212>dna
<213>streptomycessp.gf3587
<400>2
atgggcgacaaccgcaccccggtgacggtcatcggcctcggcctcatgggacaggcgctc60
gccgccgcgttcctcgaggccggccacaccacgaccgtgtggaaccgttcggcgggcaag120
gccgagcagctcgtctcgcagggcgcggtgcaggccgccacgcccgccgacgcggtggcc180
gccagtgagctggtcgtggtctgcctgtcgacgtacgacaacatgcacgacgtgatcggt240
tcgctcggcgagtccctccggggcaaggtcatcgtgaacctgacgtccggctcgtcggac300
cagggccgcgagacggccgcttgggccgagaagcagggcgtggagtacctcgacggcgcg360
atcatgatcacgccgcccggcatcggcaccgagaccgccgtcctcttctacgccggtacg420
cagagcgtgttcgagaagtacgagcccgcgctcaagctgctcggcggcggcaccacgtac480
ctcggtaccgaccacggcatgcccgcgctgtacgacgtgtcgctgctcggcctcatgtgg540
ggcacgctcaacagcttcctgcacggtgtcgccgtggtggagaccgcgggcgtcggcgcc600
cagcagttcctgccgtgggcgcacatgtggctggaggcgatcaagatgttcaccgccgac660
tacgcggcccagatcgacgccggcgacggcaagttccccgccaacgacgccacgctggag720
acgcacctggcggcgctcaagcacctggtgcacgagagcgaggcgctgggcatcgacgcc780
gaactgcccaagtactcggaggcgttgatggagcgcgtcatcagccagggtcacgccaag840
aacagctacgcggccgtgctgaaggcgttccgcaagccgtcggagtga888
- 还没有人留言评论。精彩留言会获得点赞!