一种藤黄果果实提取羟基柠檬酸盐的方法与流程
本发明涉及植物提取领域,具体涉及一种藤黄果果实提取羟基柠檬酸盐的方法。
背景技术:
藤黄果(garciniacambogial.)是一种分布在南亚热带地区的藤黄科乔木,其果实的果皮中富含羟基柠檬酸,果实具有酸味,在南亚国家常用作食物调料和传统药物。羟基柠檬酸是atp柠檬酸裂解酶的强竞争性抑制剂,具有抑制脂肪合成和促进糖元异生的作用,使丙酮酸和乳酸的利用率增高,抑制食欲。因此,羟基柠檬酸常作为减肥功能性食品的有效成分加以应用。近年的研究表明,羟基柠檬酸还能抑制肾中草酸钙结晶的生成。
羟基柠檬酸为含有2个羟基和3个游离羧基的有机酸,在分离提取的过程中极易缩合成内酯,使得产品的生物学活性降低。工业制备上从藤黄果中提取羟基柠檬酸主要采用3种方法:水提取法、有机溶剂提取法和离子交换色谱提取法。国内外市场的藤黄果提取物主要采用上述几种方法制备,其产品的主要成分为羟基柠檬酸内酯,而不是游离的羟基柠檬酸。
技术实现要素:
本发明的目的在于克服现有技术中提取的羟基柠檬酸盐中易形成内酯的问题,提供了一种藤黄果果实羟基柠檬酸盐的方法。
本发明的目的通过以下技术方案予以实现:
一种藤黄果果实提取羟基柠檬酸盐的方法,包括以下步骤:
s1.将藤黄果果实粉碎;
s2.在s1中粉碎的藤黄果果实中,按照料液比为1:13~15加入水,并在110~120℃条件下煮沸10~20min,冷却之后过滤保留滤液;
s3.将步骤s2中的滤液浓缩4~6倍,加入浓缩液体积的1~2倍的90%~95%的乙醇;
s4.将步骤s3进行过滤,在滤液中加入90%~95%的乙醇调节酒精度数为58~62;
s5.在步骤s4中加入碱溶液,调节溶液ph至11.5~12.5;
s6.对步骤s5进行过滤、洗涤、蒸发、干燥。
上述藤黄果果实提取柠檬酸盐的方法,是从藤黄果果实中提取羟基柠檬酸,在提取过程中由于加入的碱溶液,最终产物为盐的形态。步骤s2中按照料液比为1:13~15加入水,是指按照质量体积比,每克藤黄果果实中加入13~15ml的水。步骤s2中煮沸的温度为110~120℃,是根据不同的温度需要,通过加压的方式予以实现的。上述通过加入90%~95%的乙醇调节溶液的酒精度数,是用40~70度酒精度计进行测量。另外,步骤s6中,最后形成的为油状沉淀,弃除清液以后,沉淀用95%乙醇洗涤3次,再用无水乙醇洗涤沉淀2次后置于常温下过夜,然后置于60℃减压蒸发,干燥。
优选地,所述步骤s1中藤黄果果实粉碎为30~50目颗粒。
优选地,所述步骤s2中料液比为1:14。
优选地,所述步骤s2中采用115℃的条件煮沸15min。
优选地,所述步骤s3中滤液的浓缩倍数为5倍。
优选地,所述步骤s4中酒精度数为60。
优选地,所述步骤s5中调节溶液的ph为12。
优选地,所述步骤s5中的碱溶液为koh或naoh溶液。优选采用koh溶液,koh的质量百分含量为30%~50%。
与现有技术相比,本发明具有以下技术效果:
本发明提供的藤黄果果实提取羟基柠檬酸盐的方法,采用碱溶液尤其是koh溶液,使待提取物处于适宜的碱性条件,在此碱性条件性下,羟基柠檬酸中的羧基处于碱性氛围下而不是与碱性物质直接形成中性盐。由于羧基不能形成羧基盐,从而不利于酯化反应的进行,有效减少内酯的形成,提高了羟基柠檬酸盐的纯度和生物活性。
附图说明
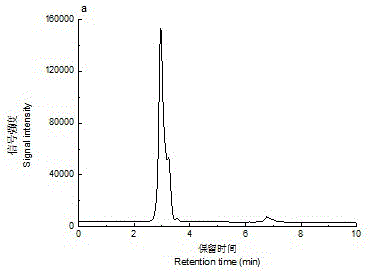
图1羟基柠檬酸标准品的高效液相色谱图;
图2柠檬酸的高效液相色谱图;
图3实施例1制得的产品的高效液相色谱图;
图4nowfoods公司的藤黄果提取物对照品的高效液相色谱图;
图5偏钒酸铵显色反应图;以及
图6薄层层析图。
附图标记说明:
1-羟基柠檬酸标准品,2-柠檬酸,3-实施例1制得的产品,4-nowfoods藤黄果提取物对照品。
具体实施方式
为使本发明的目的、技术方案和优点更加清楚,下面结合具体实施例和对比例将对本发明的技术方案进行详细的描述。显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动的前提下所得到的所有其它实施方式,都属于本发明所保护的范围。
除特殊说明,本实施例、对比例以及实验例中所用的设备均为常规实验设备,所用的材料、试剂均为市售可得。
实施例1
s1.取粉碎至40目的藤黄果果实粉末;
s2.在步骤s1中按照料液比为1:14的比例加入水,再在115℃高压蒸煮15min,冷却后用5层医用纱布过滤挤压出滤液,滤液于4000×g离心15min;
s3.在55℃的条件下减压蒸发浓缩上清液,浓缩倍数为5倍,然后在浓缩液中1:1(v/v)加入95%乙醇沉淀果胶;
s4.将步骤s3所得到的混合物用纱布过滤后4000×g离心15min除去果胶,上清液中加入95%乙醇用40-70度酒精度计(河北武强华鹏仪器厂)在室温下调节溶液酒精度数至60;
s5.然后加入40%koh调节ph至12;
s6.步骤s5中形成油状沉淀后弃上清液,沉淀用95%乙醇洗涤3次,再用无水乙醇洗涤沉淀2次后置于常温下过夜,然后置于60℃减压蒸发,干燥。
实施例2
s1.取粉碎至30目的藤黄果果实粉末;
s2.在步骤s1中按照料液比为1:15的比例加入水,再在110℃高压蒸煮20min,冷却后用5层医用纱布过滤挤压出滤液,滤液于4000×g离心15min;
s3.在55℃的条件下减压蒸发浓缩上清液,浓缩倍数为6倍,然后在浓缩液中1:2(v/v)加入90%乙醇沉淀果胶;
s4.将步骤s3所得到的混合物用纱布过滤后4000×g离心15min除去果胶,上清液中加入95%乙醇用40-70度酒精度计(河北武强华鹏仪器厂)在室温下调节溶液酒精度数至58;
s5.然后加入40%koh调节ph至11.5;
s6.步骤s5中形成油状沉淀后弃上清液,沉淀用95%乙醇洗涤3次,再用无水乙醇洗涤沉淀2次后置于常温下过夜,然后置于60℃减压蒸发,干燥。
实施例3
s1.取粉碎至50目的藤黄果果实粉末;
s2.在步骤s1中按照料液比为1:13的比例加入水,再在120℃高压蒸煮10min,冷却后用5层医用纱布过滤挤压出滤液,滤液于4000×g离心15min;
s3.在55℃的条件下减压蒸发浓缩上清液,浓缩倍数为4倍,然后在浓缩液中1:1(v/v)加入90%乙醇沉淀果胶;
s4.将步骤s3所得到的混合物用纱布过滤后4000×g离心15min除去果胶,上清液中加入95%乙醇用40-70度酒精度计(河北武强华鹏仪器厂)在室温下调节溶液酒精度数至62;
s5.然后加入40%koh调节ph至12.5;
s6.步骤s5中形成油状沉淀后弃上清液,沉淀用95%乙醇洗涤3次,再用无水乙醇洗涤沉淀2次后置于常温下过夜,然后置于60℃减压蒸发,干燥。
对比例1~3
主要步骤与实施例1相同。区别在于:对比例1至对比例3的步骤s5溶液的ph依次为9、11、13。
对比例4~6
主要步骤与实施例1相同。区别在于:对比例4至对比例6的步骤s2中料液比依次为1:6、1:10、1:18。
对比例7~9
主要步骤与实施例1相同。区别在于:对比例7至对比例9的步骤s3中溶液的浓缩倍数依次为1、3、7。
对比例10~12
主要步骤与实施例1相同。区别在于:对比例10至对比例12的步骤s4中溶液的酒精度数依次为40、50、70。
实施例1
按照各实施例和各对比例的方法提取藤黄果果实中的柠檬酸钾,并分别计算得率。结果如表1所示。
得率=(提取获得羟基柠檬酸钾的质量/藤黄果果实质量)×100%
表1得率情况表
从上表可以看出料液比、浓缩倍数、酒精度数以及ph对羟基柠檬酸盐的得率都有较大的影响。只有在料液比在1:13~15,浓缩倍数为4~6倍,酒精度数为58~62,ph为11.5~12.5的范围内,羟基柠檬酸盐才有较好的得率。
实验例2
参照文献(huizf,xiaoh,huiyh,etal.determinationofhydroxycitricacidingarciniacambogiabyrp-hplc[j].northwestpharmaceuticalj,2015,30:371-372.)采用lc-10avpplus(岛津)高效液相色谱仪,色谱柱为wondasilc18(250mm×4.6mm,5μm),流动相为0.05mol/l无水硫酸钠,用硫酸调整ph至2.3,流速为1ml/min。取50mg待测样品溶于40ml3.0%的磷酸溶液中,超声波处理30min后用0.022μm滤膜过滤,上样量为20μl,采用紫外检测器于210nm处检测。利用上述方法分别对羟基柠檬酸标准品(图1),柠檬酸(图2)实施例1制得的产品(图3),nowfoods藤黄果提取物对照品(图4)进行测试。
从图中可以发现,图3在保留时间为2.90min处出现吸收峰,与图1的羟基柠檬酸标准品(2.96min)、图4的nowfoods藤黄果提取物对照品(2.88min)具有相同的峰位置。而图2的柠檬酸在2.90min没有吸收峰。说明实施例1制得的产品为羟基柠檬酸盐。另外,在图4的nowfoods公司的藤黄果提取物对照品在5.63min出还有一个更强的吸收峰,此峰对应的为形成内酯羟基柠檬酸,而图3在5.63min没有吸收峰,说明本发明的方法获得的羟基柠檬酸盐是以纯净的羟基柠檬酸盐存在,其中没有形成内酯。
实验例3
显色反应参照文献(baintolc,dizonei,laurenaac,etal.isolationandquantificationofhydroxycitricacidfrombatuan[garciniabinucao(blanco)choisy]fruit[j].intfoodresj,2018,25:706-711)的方法。称取0.1g待测样品溶于50ml3.0%的磷酸溶液中,超声波处理30min后取1ml上清液,加入3ml1%偏矾酸铵,静置30min后观察。
用偏矾酸铵进行显色反应(如图5),发现羟基柠檬酸标准品1、实施例1的产品3和nowfoods公司的藤黄果提取物4均呈红棕色,而柠檬酸2呈黄色。
实验例4
取0.1g待测样品溶于0.9ml3.0%的磷酸溶液中,超声波处理30min后用0.022μm滤膜过滤,点样在活化后的gf254薄层层析硅胶板上(2.5×7.5cm),以甲醇:水=6:1(v/v)为展开剂。层析完毕后采用5%偏矾酸铵溶液显色。rf值按如下公式计算:
rf=原点至组分点中心的距离÷原点至溶剂前沿的距离
如图6显示,羟基柠檬酸标准品1、柠檬酸2、实施例1制得的产品3和nowfoods藤黄果提取物4的rf值无明显差异,均在0.69-0.71之间,但柠檬酸的rf值稍低。进一步说明所提取物为羟基柠檬酸盐。
最后所应当说明的是,以上实施例仅用以说明本发明的技术方案而非对本发明保护范围的限制,对于本领域的普通技术人员来说,在上述说明及思路的基础上还可以做出其它不同形式的变化或变动,这里无需也无法对所有的实施方式予以穷举。凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明权利要求的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!