人冠状病毒和呼吸道合胞病毒荧光定量PCR检测方法及其应用与流程
本发明涉及人呼吸道病毒检测领域,特别是可用于人冠状病毒和呼吸道合胞病毒所致疾病检测领域的荧光定量pcr方法及其应用。
背景技术:
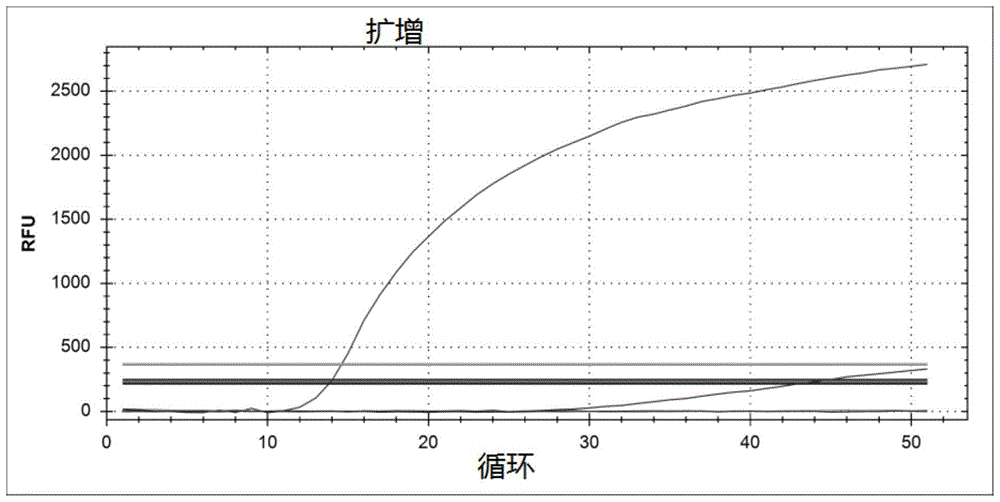
:目前,传染仍是人类健康的重大威胁,尤其是急性呼吸道传染病,由于其种类多、传播快、流行广等特点,发病率和死亡率高,对人类健康、社会稳定和经济发展造成重大威胁。全球疾病、伤害和风险因素负担(gbd)研究发现,2016年下呼吸道感染导致65万5岁以下儿童死亡,108万70岁以上成人死亡,而全世界所有年龄段的人中约有238万死于下呼吸道感染,使下呼吸道感染成为所有年龄段死亡的第六大原因,也是5岁以下儿童死亡的主要原因(参见:gbd2016lowerrespiratoryinfectioncollaborators.estimatesoftheglobal,regional,andnationalmorbidity,mortality,andaetiologiesoflowerrespiratoryinfectionsin195countries,1990-2016:asystematicanalysisfortheglobalburdenofdiseasestudy2016.lancetinfectdis.2018,18(11):1191-1210.)。呼吸道感染一直是全球致死、致残的主要病因。病毒是造成呼吸道感染最主要的原因,50%以上的呼吸道感染是由呼吸道病毒引起。此外,由于呼吸道病毒变异频繁,新的病毒或变异株不断出现,常易引起新发/突发传染病暴发流行。呼吸道病毒成为全球传染病防控和研究的重点,努力减少下呼吸道感染导致的死亡是世界各国优先考虑的事情,因此亟需提高呼吸道感染病原体检测和应对疫情的能力。冠状病毒(coronavirus)属于冠状病毒科,冠状病毒属,可以感染哺乳动物和禽类,引起呼吸系统、消化和中枢神经的各种疾病[参见:hamred,etal.anewvirusisolatedfromthehumanrespiratorytract.procsocexpbiolmed,1966,121(1):190-3.]。根据基因组和血清学差异可以将冠状病毒分成四个不同的属:α、β、γ和δ,目前只有α和β属冠状病毒感染人类。截至目前已鉴定出来自两个属(α和β)的6种人冠状病毒(hcov),α属冠状病毒包括nl63和229e,β属冠状病毒包括oc43、hku1、急性呼吸系统综合征冠状病毒(sars-cov)和中东呼吸综合征冠状病毒(mers-cov)。hcov是引起急性呼吸道感染的重要病原体,可以通过直接接触呼吸道分泌物或经气溶胶飞沫传播,感染呈现的临床表现从轻微感冒到严重的下呼吸道感染。研究发现,我国大约3.36%的急性儿童下呼吸道感染由冠状病毒引起[参见qiany,etal.detectionandclinicalanalysisofacutelowerrespiratorytractinfectionwithhumancoronavirusesinchildreninbeijingarea2007-2015.zhonghuaerkezazhi.2015sep;53(9):707-11]。呼吸道合胞病毒(rsv)为副黏病毒科肺病毒属中单链rna病毒,分为a、b两型,是5岁以下婴幼儿呼吸道感染的最主要病因,此外,rsv还能感染其他各个年龄组的人群,并导致严重的呼吸道疾病,其病情在老年人中尤为严重。我国2岁以下住院和门/急诊病例中,rsv检出率高居榜首,达33.3%[参见yuj,etal.comparisonoftheprevalenceofrespiratoryvirusesinpatientswithacuterespiratoryinfectionsatdifferenthospitalsettingsinnorthchina,2012-2015.bmcinfectdis.2018feb8;18(1):72]。人冠状病毒和呼吸道合胞病毒造成严重的临床疾病负担,迫切需要开发灵敏、快速、特异、稳定和便于使用的诊断方法,在临床应用中能够为明确病原、早期诊断提供依据,促进早期合理治疗,减少经验性抗生素使用增加的耐药负担,及时控制病情。对呼吸道病毒的检测方法主要包括病毒分离、抗原检测、抗体检测(如酶联免疫吸附、免疫荧光分析)、传统的聚合酶链反应(polymerasechainreaction,pcr)方法以及荧光定量pcr(real-timepcr)方法等。pcr是一种分子生物学技术,在生物体外扩增特定的dna片段,不必依赖大肠杆菌或酵母菌等生物体。它是一种简单可靠的复制dna片段方法,适用于现代生物学和相关科学的许多领域。pcr检测方法快速、灵敏,对于不能培养、难于培养或培养时间较长的病毒,以及由于抗原的多样性或临床样本抗原含量过低而难于进行抗原检测时,pcr检测显示出强大的优势,特别适用于病毒的急性期感染的检测。而荧光定量pcr技术是一种在dna扩增反应中,使用5’端带有荧光物质(如:fam、hex、rox、cy5等),3’端带有淬灭物质(如:tamra等)修饰的寡核苷酸检测pcr循环后产物总量的方法。进行pcr反应时,向pcr反应液中加入荧光探针,在pcr反应的退火过程中,荧光探针与模板杂交,5’端的荧光物质受到3’端淬灭物质的制约,不能发出荧光。在进一步pcr反应的延伸过程中,taqdna聚合酶的5’→3’外切核酸酶(exonuclease)活性分解与模板杂交的荧光探针,使游离荧光物质发出荧光。通过检测反应体系中的荧光强度,达到检测pcr产物扩增量的目的。荧光定量pcr技术在核酸检测中具有独特的优势,如易于操作、精确度高,灵敏度高,特异性强,检测时间快,通量高,不易污染等,因此广泛应用于临床和科研实验室的检测。传统的pcr方法针对每种病原体设计相应的引物,一个反应检测一种病原体,当需要检测多种病原体时就会受到限制。鉴于此,多重pcr(multiplexpcr)技术应运而生,在一个体系内可以同时扩增多个目的基因,从而实现多种病毒病原体的同时检测,满足临床的需求。仍然需要设计性能更优的引物,以快速、特异、灵敏、精确检测多种呼吸道病毒。技术实现要素:在本发明中,我们成功设计了针对oc43、hku1和rsvb基因的特异性引物和探针,利用急性呼吸道病毒感染患者的呼吸道样本提取核酸后进行检测,分别可以成功检测出呼吸道病毒oc43、hku1,rsvb。进一步把三种呼吸道感染病原体的引物和探针进行组合,可以在急性呼吸道感染样本中同时检测oc43、hku1和rsvb。检测体系中引物和探针具有较好的灵敏度和特异度,检测体系具有较好的可重复性。第一方面,本发明提供了用于通过荧光定量pcr方法检测样品中人冠状病毒oc43的引物和探针,所述引物用于特异性扩增oc43n蛋白基因序列,所述探针特异性结合oc43n蛋白基因内部序列。第二方面,本发明提供了用于通过荧光定量pcr方法检测样品中人冠状病毒hku1的引物和探针,所述引物用于特异性扩增hku1n蛋白基因序列,所述探针特异性结合hku1n蛋白基因内部序列。第三方面,本发明提供了用于通过荧光定量pcr方法检测样品中呼吸道合胞病毒rsvb的引物和探针,所述引物用于特异性扩增rsvbn蛋白基因序列,所述探针特异性结合rsvbn蛋白基因内部序列。第四方面,本发明提供了用于通过荧光定量pcr方法同时检测样品中人冠状病毒oc43、人冠状病毒hku1和/或呼吸道合胞病毒rsvb的引物和探针组合,所述引物和探针组合由第一方面和第二方面的引物和探针组成,或由第二方面和第三方面的引物和探针组成,或由第一方面和第三方面的引物和探针组成,或由第一方面、第二方面和第三方面的引物和探针组成。第五方面,本发明提供了一种荧光定量pcr试剂盒,所述试剂盒包括第一方面至第三方面中任一项的引物和探针,或第四方面的引物和探针组合。第六方面,本发明提供了第一方面至第三方面中任一项的引物和探针,或第四方面的引物和探针组合用于制备检测样品中人冠状病毒oc43、人冠状病毒hku1和/或呼吸道合胞病毒rsvb的试剂的用途。附图说明图1表示荧光定量pcr方法检测oc43。图2表示荧光定量pcr方法检测hku1。图3表示荧光定量pcr方法检测rsvb。图4表示荧光定量pcr方法同时检测检测oc43、hku1和rsvb。图5表示荧光定量pcr方法的检测限分析:(a)oc43;(b)hku1;(c)rsvb。具体实施方式本发明提供了一组用于通过荧光定量pcr方法检测样品中人冠状病毒oc43的引物和探针,所述引物用于特异性扩增oc43n蛋白基因序列,所述探针特异性结合oc43n蛋白基因内部序列;优选地,所述引物和探针的核苷酸序列如seqidnos:1-3所示。本发明还提供了一组用于通过荧光定量pcr方法检测样品中人冠状病毒hku1的引物和探针,所述引物用于特异性扩增hku1n蛋白基因序列,所述探针特异性结合hku1n蛋白基因内部序列;优选地,所述引物和探针的核苷酸序列如seqidnos:4-6所示。本发明还提供了一组用于通过荧光定量pcr方法检测样品中呼吸道合胞病毒rsvb的引物和探针,所述引物用于特异性扩增rsvbn蛋白基因序列,所述探针特异性结合rsvbn蛋白基因内部序列;优选地,所述引物和探针的核苷酸序列如seqidnos:7-9所示。本发明还提供了用于通过荧光定量pcr方法同时检测样品中人冠状病毒oc43、人冠状病毒hku1和/或呼吸道合胞病毒rsvb的引物和探针组,所述引物和探针组由上述特异性引物和探针中任意两组组成,或由上述三组特异性引物和探针组成;优选地,所述引物和探针组的序列如seqidnos:1-6、或seqidnos:4-9、或seqidnos:1-3和7-9、或seqidnos:1-9所示。本发明还提供了一种荧光定量pcr试剂盒,所述试剂盒包括上述任一组的引物和探针,或上述任意两组的引物和探针,或上述三组引物和探针。在一个具体实施方案中,所述试剂盒还包括酶混合物、pcr缓冲液和无核酸酶的水。本发明还提供了上述各组引物和探针或其组合用于制备检测样品中人冠状病毒oc43、人冠状病毒hku1和/或呼吸道合胞病毒rsvb的试剂的用途。在一个具体实施方案中,所述样品为呼吸道感染患者临床样品;优选地,所述样品包括痰液、鼻咽拭子、肺泡灌洗液。下面结合优选实施例进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。下列实施例中未注明具体的实验方法,通常按照常规条件和方法,如分子克隆实验室手册(sambrook,etal.newyork:coldspringharborlaboratorypress,1989)中所述方法或试剂制造商提供的方法。实施例1荧光定量pcr方法检测人冠状病毒oc431.1核酸的提取取急性呼吸道感染患者临床样品,如痰液、鼻咽拭子、肺泡灌洗液等,按照常规方法提取核酸。将所得核酸溶于50μl洗脱液,按照常规方法对提取的核酸进行定量和纯度检测。将提取的核酸分装成小份,冻存于-80℃冰箱。1.2特异性引物和探针的设计及合成利用primer3软件,针对oc43n蛋白基因序列分别设计荧光定量pcr正向引物和反向引物,并在基因内部设计探针。设计方法如下:针对靶向的目标基因,使用滑动窗口法设计taqman探针,窗口宽度设置为120个核苷酸,步长为1个核苷酸,穷举全部可能的探针序列。使用以下条件筛选探针:1)探针序列长度20-35个核苷酸;2)探针序列tm值为70±2℃;3)探针不与病毒基因形成发卡结构;4)探针序列的gc含量40%-70%。确定taqman探针后,使用软件设计与之匹配的引物,引物需满足以下条件:1)长度18-35个核苷酸,上、下游引物长度相差不超过4个核苷酸;2)引物tm值为60±2℃,上、下游引物tm相差不超过2℃;3)引物自身不形成环状发卡结构;4)引物自身不形成二聚体;5)上下游引物间不形成二聚体;6)引物的3’端不为g或c;7)上下游引物的扩增子大小为80-180个核苷酸。设计多对引物与设计好的探针进行匹配实验,选择所得ct值最低的引物对。按照常规方法合成引物和探针,在探针5’端加入fam荧光基团。正向引物、反向引物和探针分别命名为oc43nfor、oc43nrev、oc43nfam。将引物和探针用无dna酶和rna酶的无菌水配制成10μm浓度,分装成小份,冻存于-20℃冰箱。1.3荧光定量pcr体系的配制以abilifetechnologies公司的agpath-idtmone-steprt-pcrkit为例,进行荧光定量pcr体系的配制。将agpath-idtmone-steprt-pcrkit试剂、引物和探针从-20℃冰箱取出,溶解后置于冰上,在pcr管中配制rt-pcrmastermix体系:从-80℃冰箱取出核酸,调整核酸浓度,向上述pcr管内加入2μl(1-50ng)核酸。1.4荧光定量pcr反应程序配制的荧光定量pcr反应体系,放入荧光定量pcr仪,执行下列程序:1.5结果判定判定标准:阴性对照无扩增曲线;样品ct<35且具典型的“s”型扩增曲线。结果表明,急性呼吸道感染样本中可以特异性检测出oc43阳性样本,如图1所示。实施例2荧光定量pcr方法检测人冠状病毒hku12.1核酸的提取取急性呼吸道感染患者临床样品,如痰液、鼻咽拭子、肺泡灌洗液等。按照常规方法提取核酸,将所得核酸溶于50μl洗脱液。按照常规方法对提取的核酸进行定量和纯度检测。将提取的核酸分装成小份,冻存于-80℃冰箱。2.2特异性引物和探针的设计及合成利用primer3软件,针对hku1n蛋白基因序列分别设计荧光定量pcr正向引物和反向引物,并在基因内部设计探针。方法如1.2中所述。按照常规方法合成引物和探针,在探针5’端加入rox荧光基团。正向引物、反向引物和探针分别命名为hku1nfor、hku1nrev、hku1nfam。将引物和探针用无dna酶和rna酶的无菌水配制成10μm浓度,分装成小份,冻存于-20℃冰箱。2.3荧光定量pcr体系的配制以abilifetechnologies公司的agpath-idtmone-steprt-pcrkit为例,进行荧光定量pcr体系的配制。将agpath-idtmone-steprt-pcrkit试剂、引物和探针从-20℃冰箱取出,溶解后置于冰上,在pcr管配制rt-pcrmastermix体系:组成1×25(μl)无核酸酶的水82×rt-pcr缓冲液12.5hku1for0.5hku1rev0.5hku1rox0.5rt-pcr酶混合物1合计23从-80℃冰箱取出核酸,调整核酸浓度,向上述pcr管内加入2μl(1-50ng)核酸。2.4荧光定量pcr反应程序配制的荧光定量pcr反应体系,放入荧光定量pcr仪,执行下列程序:2.5结果判定判定标准:阴性对照无扩增曲线;样品ct<35且具典型的“s”型扩增曲线。结果表明,急性呼吸道感染样本中可以特异性检测出hku1阳性样本,如图2所示。实施例3荧光定量pcr方法检测呼吸道合胞病毒rsvb3.1核酸的提取取急性呼吸道感染患者临床样品如痰液、鼻咽拭子、肺泡灌洗液等,按照常规方法提取核酸,将所得核酸溶于50μl洗脱液。按照常规方法对提取的核酸进行定量和纯度检测。将提取的核酸分装成小份,冻存于-80℃冰箱。3.2特异性引物和探针的设计及合成利用primer3软件,针对rsvbn蛋白基因序列分别设计荧光定量pcr正向引物和反向引物,并在基因内部设计探针。方法如1.2中所述。按照常规方法合成引物和探针,在探针5’端加入cy5荧光基团。正向引物、反向引物和探针分别命名rsvbnfor、rsvbnrev、rsvbncy5。将引物和探针用无dna酶和rna酶的无菌水配制成10μm浓度,分装成小份,冻存于-20℃冰箱。3.3荧光定量pcr体系的配制以abilifetechnologies公司的agpath-idtmone-steprt-pcrkit为例,进行荧光定量pcr体系的配制。将agpath-idtmone-steprt-pcrkit试剂、引物和探针从-20℃冰箱取出,溶解后置于冰上,在pcr管配制rt-pcrmastermix体系:组成1×25(μl)无核酸酶的水82×rt-pcr缓冲液12.5rsvbfor0.5rsvbrev0.5rsvbcy50.525×rt-pcr酶混合物1合计23从-80℃冰箱取出核酸,调整核酸浓度,向上述pcr管内加入2μl(1-50ng)核酸。3.4荧光定量pcr反应程序将配制的荧光定量pcr反应体系放入荧光定量pcr仪,执行下列程序:3.5结果判定判定标准:阴性对照无扩增曲线;样品ct<35且具典型的“s”型扩增曲线。结果表明,急性呼吸道感染样本中可以特异性检测出rsvb阳性样本,如图3所示。实施例4荧光定量pcr方法同时检测oc43、hku1和rsvb4.1核酸的提取取急性呼吸道感染患者临床样品,如痰液、鼻咽拭子、肺泡灌洗液等,按照常规方法提取核酸。将所得核酸溶于50μl洗脱液。按照常规方法对提取的核酸进行定量和纯度检测。将提取的核酸分装成小份,冻存于-80℃冰箱。4.2oc43、hku1和rsvb特异性引物和探针oc43、hku1和rsvb特异性引物和探针序列分别为实施例1、实施例2和实施例3中的对应的引物和探针序列,合成后用无dna酶和rna酶的无菌水溶解,将所有引物和探针混合,调整引物-探针混合液中各引物或探针的终浓度为10μm。将混合液分装成小份,冻存于-20℃冰箱。4.3荧光定量pcr体系的配制以abilifetechnologies公司的agpath-idtmone-steprt-pcrkit为例,进行荧光定量pcr体系的配制。将agpath-idtmone-steprt-pcrkit试剂、引物和探针从-20℃冰箱取出,溶解后置于冰上,在pcr管配制rt-pcrmastermix体系:组成1×25(μl)无核酸酶的水8.52×rt-pcr缓冲液12.5引物-探针混合液125×rt-pcr酶混合物1合计23从-80℃冰箱取出核酸,调整核酸浓度,向上述pcr管内加入2μl(1-50ng)核酸。4.4荧光定量pcr反应程序将配制的荧光定量pcr反应体系放入荧光定量pcr仪,执行下列程序:4.5结果判定判定标准:阴性对照无扩增曲线;样品ct<35且具典型的“s”型扩增曲线。结果表明,在同一检测体系中,急性呼吸道感染样本可以同时特异性检测出oc43、hku1和rsvb阳性样本,如图4所示。实施例5荧光定量pcr方法检测oc43、hku1和rsvb的特异度和灵敏度分析以国家科技重大专项传染病监测平台网络实验室发热呼吸道症候群病毒核酸检测方案的巢式pcr方法(以下称巢式pcr)作为金标准,本发明中oc43、hku1和rsvb荧光定量pcr方法与之相比较。以经金标准巢式pcr检测阳性且测序正确的样本为阳性参照,再随机挑选检测阴性样本共500份进行分析。结果提示,以巢式pcr作为金标准,oc43荧光定量pcr方法的特异度为100%,灵敏度为100%(表1);hku1荧光定量pcr方法的特异度为100%,灵敏度为100%(表2);rsvb荧光定量pcr方法的特异度为99.6%,灵敏度为98%(表3)。表1.oc43荧光定量pcr方法的特异度和灵敏度分析注:灵敏度=a/(a+b);特异度=d/(c+d)表2.hku1荧光定量pcr方法的特异度和灵敏度分析注:灵敏度=a/(a+b);特异度=d/(c+d)表3.rsvb荧光定量pcr方法的特异度和灵敏度分析注:灵敏度=a/(a+b);特异度=d/(c+d)实施例6oc43、hku1和rsvb荧光定量pcr检测方法的重复性(精密度)分析随机抽oc43、hku1和rsvb病毒阳性的急性呼吸道感染样本,提取核酸后进行定量,取106拷贝/反应在同一试验日并在同一台仪器上重复5孔进行荧光定量pcr分析,检测其循环阈值(ct值);随机抽取oc43、hku1和rsvb病毒阳性的急性呼吸道感染标本,提取核酸后提取核酸后进行定量,取106拷贝/反应分别在不同试验日进行荧光定量pcr分析,检测其ct,共进行5次重复检测。分别计算均数和标准差,根据标准差/均数计算批内和批间变异系数(cv)。结果表明,oc43、hku1和rsv批内cv分别为0.18%、0.09%和0.25%,批间cv值分别为0.15%、0.17%和0.24%,批内和批间cv值均小于1%,说明重复性良好(表4)。表4.oc43、hku1和rsvb荧光定量pcr检测方法的重复性(精密度)分析实施例7oc43、hku1和rsvb荧光定量pcr检测方法的检测限分析pcr扩增oc43、hku1和rsv目的片段,分别克隆到含t7启动子的质粒,进一步体外转录成rna,用dnase消化残余dna,根据rna浓度和片段大小分别计算相应的拷贝数。对rna进行梯度稀释,作为模板分别做荧光定量pcr分析,根据梯度拷贝数与相应ct值做标准曲线。将oc43、hku1和rsvb阳性样品分别进行荧光定量pcr分析,将样品ct值套入标准曲线获得病毒rna拷贝数。然后将108拷贝/反应的oc43、hku1和rsvb阳性样品进行10倍梯度稀释作为模板进行荧光定量pcr分析,获取反应体系对oc43、hku1和rsvb的最低检出拷贝数分别为3、2和5。结果如图sa-c所示。序列表<110>中国医学科学院病原生物学研究所<120>人冠状病毒和呼吸道合胞病毒荧光定量pcr检测方法及其应用<130>cp1190741/cb<141>2019-10-22<160>9<170>siposequencelisting1.0<210>1<211>19<212>dna<213>人工序列(syntheticsequence)<400>1gagcgtcctctggaaatcg19<210>2<211>23<212>dna<213>人工序列(syntheticsequence)<400>2ctacccctggtttgaacatttct23<210>3<211>23<212>dna<213>人工序列(syntheticsequence)<400>3tctggtaatggcatcctcaagtg23<210>4<211>20<212>dna<213>人工序列(syntheticsequence)<400>4atctcggtaccggcccatat20<210>5<211>23<212>dna<213>人工序列(syntheticsequence)<400>5catcggagggagtagaagtgtca23<210>6<211>23<212>dna<213>人工序列(syntheticsequence)<400>6gaaggggtcttctgggttgctaa23<210>7<211>27<212>dna<213>人工序列(syntheticsequence)<400>7ctgaagatgcaaatcataaattcacag27<210>8<211>33<212>dna<213>人工序列(syntheticsequence)<400>8catgatatccagcatctttaagtatctttatag33<210>9<211>24<212>dna<213>人工序列(syntheticsequence)<400>9tgtccaggttaggaagggaagaca24当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1