一种钯催化合成的芳基吖啶衍生物及其制备方法与流程
本发明涉及有机合成领域,更具体的说是涉及一种钯催化合成的芳基吖啶衍生物及其制备方法。
背景技术:
芳基吖啶及其衍生物是一类重要的有机化合物,在生物医药、食品、化妆品及其有机电子材料领域都具有着很大的应用价值和广泛的应用前景。
在现有技术中,芳基吖啶及其衍生物主要通过以下方法制备得到:1、通过钯催化2-氨基二苯甲酮和环己酮进行环化反应制备得到芳基吖啶衍生物(eur.j.org.chem.2017,577-581);2、以9-氯吖啶和芳基硼酸为原料,在100℃下,以甲苯为溶剂,发生取代反应制备得到芳基吖啶化合物(chem.commun.2017,53,13063)。但上述方法都存在着一定的缺陷,其中方法1的反应条件十分苛刻,需要在160℃下的氧气氛围下进行,而且所采用的溶剂是tce,tce是一种有毒溶剂,低剂量吸入就可能会出现类似酒精样的酒醉。而方法2中在合成9-氯吖啶时需要用到有毒的pocl3或socl2,二者都具有刺激性气味而且具有一定毒性,容易对实验人员的健康造成影响,反应存在较大的危险性,不符合绿色化学发展;由于这些缺陷的存在,使得这些方法的实用性和适用性受到了较大的限制,无法真正大规模的推广。
技术实现要素:
针对现有技术存在的不足,本发明的目的在于提供一种钯催化合成的芳基吖啶衍生物及其制备方法,该制备方法所用原料毒性小,反应过程简单,安全。为实现上述目的,本发明提供了如下技术方案:
一种钯催化合成的芳基吖啶衍生物,其结构式为
其中-r1是氢、甲基、甲氧基、卤素、三氟甲基中的任意一种;
-r2是氢、甲基、甲氧基、卤素、三氟甲基中的任意一种;
ar是苯基,间氯苯基,对溴苯基,对叔丁基苯基,对甲氧基苯基中的任意一种。
作为本发明的进一步改进,所述芳基吖啶衍生物是由2-(芳氨基)苯甲腈衍生物和芳基硼酸反应而成;
其中2-(芳氨基)苯甲腈衍生物的结构式为
所述芳基硼酸的结构式为
arb(oh)2;
其反应式为
其中2-(芳氨基)苯甲腈衍生物与芳基吖啶衍生物中的-r1相同,均为氢、甲基、甲氧基、卤素、三氟甲基中的任意一种;
2-(芳氨基)苯甲腈衍生物与芳基吖啶衍生物中的-r2相同,均为氢、甲基、甲氧基、卤素、三氟甲基中的任意一种;
芳基硼酸与芳基吖啶衍生物中的ar相同,均为是苯基,间氯苯基,对溴苯基,对叔丁基苯基,对甲氧基苯基中的任意一种。
作为本发明的进一步改进,所述2-(芳氨基)苯甲腈衍生物和芳基硼酸反应在溶剂中进行,所述溶剂为水。
作为本发明的进一步改进,所述2-(芳氨基)苯甲腈衍生物和芳基硼酸在溶剂中反应时,还向溶剂中加入了钯催化剂、添加剂和配体。
作为本发明的进一步改进,所述钯催化剂为氯化钯、乙酸钯、三氟乙酸钯和乙酰丙酮钯中的任意一种。
作为本发明的进一步改进,所述添加剂为甲基磺酸。
作为本发明的进一步改进,所述配体为2,2`-联吡啶。
作为本发明的进一步改进,一种钯催化合成的芳基吖啶衍生物的制备方法,其特征在于:在空气氛围下,向反应容器中加入2-(芳氨基)苯甲腈衍生物、芳基硼酸、钯催化剂、配体、添加剂和溶剂进行搅拌混合,混合均匀后,在温度为90-110℃的条件下反应20-25h,制得芳基吖啶衍生物。
作为本发明的进一步改进,向反应容器中加入的2-(芳氨基)苯甲腈衍生物与芳基硼酸的物质的量之比为1:1.5-2.5。
作为本发明的进一步改进,向反应容器中加入的2-(芳氨基)苯甲腈衍生物、钯催化剂、配体和添加剂之间的物质的量之比为1:0.05:0.06:2。
本发明的有益效果:原料容易制得,来源广泛,成本相对较低;可以直接合成目标产物,无需分离中间产物;反应条件温和产率最高可达到94%,大大简化了工艺工程,降低了能量消耗,具有高产率的优点;且反应过程中废弃溶液较少,也未排放出其它污染气体和液体,因此本发明减少了废弃溶液的排放,具有保护环境和保障操作人员健康的优点;在本发明中所使用的的物质毒性较低,保证了操作人员的健康;此外,可以制备一系列的芳基吖啶衍生物,该方法具有较强的底物普适性,为开发有关芳基吖啶衍生物的有机化合物提供了较好的保证
附图说明
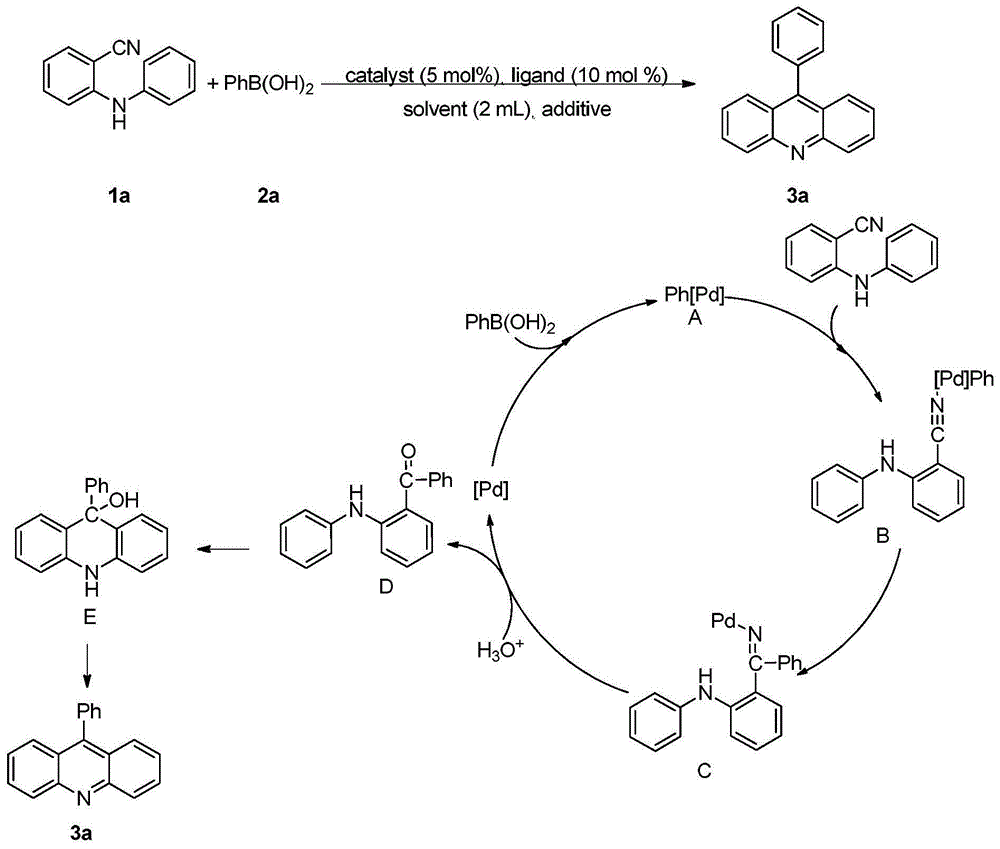
图1为本发明实施例1的反应机理图;
具体实施方式
实施例1
在空气氛围下,向反应容器中加入原料2-(苯基氨基)苯甲腈(0.5mmol)、苯硼酸(0.75mmol)、钯催化剂乙酸钯(5mol%),2,2`-联吡啶(6mol%),甲基磺酸(1.0mmol)和溶剂水(2ml)进行搅拌混合;混合均匀后,在100℃的条件下反应24h,制得9-苯基吖啶;产物收率为94%;
表征数据:1hnmr(400mhz,cdcl3)δ8.34(d,j=8.8hz,2h),7.82(t,j=7.9hz,2h),7.77-7.75(m,2h),7.76-7.63(m,3h),7.50-7.45(m,4h);13cnmr(100mhz,cdcl3)δ148.8,147.2,136.0,130.4,130.0,129.6,128.5,128.4,126.9,125.6,125.2.9-苯基吖啶的结构式为
其反应式为
实施例2
在空气氛围下,向反应容器中加入原料2-(苯基氨基)苯甲腈(0.5mmol)、3-氯苯硼酸(0.75mmol)、钯催化剂乙酸钯(5mol%),配体2,2`-联吡啶(6mol%),添加剂甲基磺酸(1.0mmol)和溶剂水(2ml)进行搅拌混合;混合均匀后,在100℃的条件下反应24h,制得9-(3-氯苯基)吖啶;最终产物的收率为96%。
表征数据:
1hnmr(400mhz,cdcl3)δ8.30(d,j=8.8hz,2h),7.81-7.77(m,2h),7.67(d,j=8.7hz,1h),7.48-7.44(m,3h),7.36-7.32(m,1h);13cnmr(125mhz,cdcl3)δ148.8,145.6,130.8,134.0,134.8,130.6,130.3,130.0,129.8,128.8,127.8,126.6,126.2,125.1.
9-(3-氯苯基)吖啶的结构式如下:
其反应式为:
实施例3
在空气氛围下,向反应容器中加入原料2-(苯基氨基)苯甲腈(0.5mmol)、4-甲氧基苯硼酸(0.75mmol)、钯催化剂乙酸钯(5mol%),配体2,2`-联吡啶(6mol%),添加剂甲基磺酸(1.0mmol)和溶剂水(2ml)进行搅拌混合;混合均匀后,在100℃的条件下反应24h,制得9-(4-甲氧基苯基)吖啶;最终产物的收率为90%。
表征数据:1hnmr(500mhz,cdcl3)δ8.27(d,j=8.9hz,2h),7.77-7.76(m,4h),7.13(d,j=8.3hz,2h),3.94(s,3h);13cnmr(125mhz,cdcl3)δ159.9,149.1,147.3,131.9,130.0,129.8,128.2,127.1,125.7,125.6,114.1,55.6.
9-(4-甲氧基苯基)吖啶的结构式如下:
其反应式:
实施例4
在空气氛围下,向反应容器中加入原料2-(苯基氨基)苯甲腈(0.5mmol)、4-异丙基苯硼酸(0.75mmol)和钯催化剂乙酸钯(5mol%),配体2,2`-联吡啶(6mol%),添加剂甲基磺酸(1.0mmol)和溶剂水(2ml)进行搅拌混合;混合均匀后,在100℃的条件下反应24h,制得9-(4-异丙基苯基)吖啶;最终产物的收率为91%。
表征数据:1hnmr(500mhz,cdcl3)δ8.28(d,j=8.28hz,2h),7.79-7.75(m,4h),7.47-7.40(m,4h),7.37-7.35(m,2h),3.12-3.05(m,1h),1.40(d,j=6.9hz,6h);13cnmr(125mhz,cdcl3)δ149.2,148.9,147.8,133.3,130.6,130.1,129.7,127.2,126.6,125.6,125.5,34.2,24.2.
9-(4-异丙基苯基)吖啶的结构式如下:
其反应式:
实施例5
在空气氛围下,向反应容器中加入原料2-(苯基氨基)苯甲腈(0.5mmol)、4-溴苯硼酸(0.75mmol)和钯催化剂乙酸钯(5mol%),配体2,2`-联吡啶(6mol%),添加剂甲基磺酸(1.0mmol)和溶剂水(2ml)进行搅拌混合;混合均匀后,在110℃的条件下反应22h,制得9-(4-溴苯基)吖啶;最终产物的收率为90%。表征数据:1hnmr(500mhz,cdcl3)δ8.29(d,j=8.8hz,2h),7.80-7.74(m,4h),7.67(d,j=8.7hz,2h),7.44(t,j=7.4hz,2h),7.32(d,j=8.2hz,2h);13cnmr(125mhz,cdcl3)δ148.8,145.9,135.0,132.3,131.9,130,3,129.8,126.6,126.1,125.1,123.0.
9-(4-溴苯基)吖啶的结构式如下:
其反应式:
实施例6
在空气氛围下,向反应容器中加入原料2-(苯基氨基)苯甲腈(0.5mmol)、4-叔丁基苯硼酸(0.75mmol)和钯催化剂乙酸钯(5mol%),配体2,2`-联吡啶(6mol%),添加剂甲基磺酸(1.0mmol)和溶剂水(2ml)进行搅拌混合;混合均匀后,在110℃的条件下反应25h,制得9-(4-叔丁基基苯基)吖啶;最终产物的收率为86%。
表征数据:1hnmr(400mhz,cdcl3)δ8.32-8.28(m,2h),7.80-7.75(m,4h),7.63-7.60(m,2h),7.45-7.36(m,4h),1.46(s,9h);13cnmr(125mhz,cdcl3)δ151.5,148.9,147.8,133.0,130.4,130.1,129.7,127.2,125.6,125.5,125.4,35.0,31.6.
9-(4-叔丁基基苯基)吖啶的结构式如下:
其反应式:
实施例7
在空气氛围下,向反应容器中加入2-(间甲基苯氨基)苯甲腈(0.5mmol)、苯硼酸(0.75mmol)、钯催化剂乙酸钯(5mol%),配体2,2`-联吡啶(6mol%),添加剂甲基磺酸(1.0mmol)和溶剂水(2ml)进行搅拌混合;混合均匀后,在90℃的条件下反应20h,制得3-甲基-9-苯基吖啶;最终产物的收率为88%。表征数据:1hnmr(400mhz,cdcl3)δ8.20-8.18(m,2h),7.74-7.69(m,1h),7.65-7.63(m,1h),7.58-7.52(m,4h),7.49-7.48(m,1h),7.40-7.38(m,2h),7.35-7.31(m,1h),7.08-7.05(m,1h),3.99(s,3h);13cnmr(125mhz,cdcl3)δ161.4,150.6,149.0,147.1,136.1,130.4,130.0,128.9,128.5,128.4,128.1,126.9,124.6,124.2,121.3,121.0,105.3,55.6.
3-甲基-9-苯基吖啶的结构式如下:
其反应式为
实施例8
在空气氛围下,向反应容器中加入2-(间甲氧基苯氨基)苯甲腈(0.5mmol)、苯硼酸(0.75mmol)、钯催化剂乙酸钯(5mol%),配体2,2`-联吡啶(6mol%),添加剂甲基磺酸(1.0mmol)和溶剂水(2ml)进行搅拌混合;混合均匀后,在100℃的条件下反应24h,制得3-甲氧基-9-苯基吖啶;最终产物的收率为85%。表征数据:1hnmr(cdcl3,400mhz,ppm):δ8.19(d,j=8.5hz,1h),7.74-7.73(m,1h),7.65-7.63(m,1h),7.58-7.52(m,4h),7.49(d,j=2.9hz,1h),7.40-7.38(m,2h),7.35-7.31(m,1h),7.07(dd,j=2.5hz,j=9.5hz,1h),3.99(s,3h);13cnmr(cdcl3,125mhz,ppm):δ161.2,150.7,149.0,147.1,136.1,130.4,130.0,129.0,128.5,128.4,128.1,127.0,124.7,124.3,121.4,121.0,105.3,55.7.
3-甲氧基-9-苯基吖啶的结构式如下:
其反应式为
实施例9
在空气氛围下,向反应容器中加入2-(邻甲基苯氨基)苯甲腈(0.5mmol)、苯硼酸(0.75mmol)、钯催化剂乙酸钯(5mol%),配体2,2`-联吡啶(6mol%),添加剂甲基磺酸(1.0mmol)和溶剂水(2ml)进行搅拌混合;混合均匀后,在90℃的条件下反应23h,制得2-甲基-9-苯基吖啶;最终产物的收率为92%。表征数据:1hnmr(cdcl3,400mhz,ppm):δ8.33(d,j=8.8hz,1h),7.77-7.73(m,1h),7.69-7.66(m,1h),7.62-7.54(m,5h),7.45-7.40(m,3h),7.33-7.29(m,1h),3.01(s,3h);13cnmr(cdcl3,125mhz,ppm):δ148.5,148.2,147.0,137.5,136.7,130.6,130.4,129.5,129.3,128.5,128.3,126.8,125.6,125.5,125.2,125.1,125.0,18.8;
2-甲基-9-苯基吖啶的结构式如下:
其反应式为
实施例10
在空气氛围下,向反应容器中加入2-(间叔丁基苯氨基)苯甲腈(0.5mmol)、苯硼酸(0.75mmol)、钯催化剂乙酸钯(5mol%),配体2,2`-联吡啶(6mol%),添加剂甲基磺酸(1.0mmol)和溶剂水(2ml)进行搅拌混合;混合均匀后,在100℃的条件下反应22h,制得3-甲氧基-9-苯基吖啶;最终产物的收率为85%。表征数据:1hnmr(cdcl3,400mhz,ppm):δ8.27(d,j=8.7hz,1h),8.22-8.21(m,1h),7.77-7.73(m,1h),7.70(d,j=8.7hz,1h),7.65(d,j=9.2hz,1h),7.60-7.56(m,3h),7.54-7.51(m,1h),7.44-7.37(m,3h),1.46(s,9h);13cnmr(cdcl3,125mhz,ppm):δ153.3,149.3,149.0,146.8,136.2,130.6,129.9,129.5,128.5,128.4,126.9,126.5,125.3,125.1,124.2,123.6,35.4,31.0
3-叔丁基-9-苯基吖啶的结构式如下:
其反应式为
图1为本发明实施例1的反应机理图:
机理说明,以实施例1为例:底物2-(苯氨基)苯甲腈1a和苯硼酸的反应生成9-苯基吖啶为例,提出了反应可能的机理。首先苯硼酸和钯催化剂反应生成活性苯基钯物种a,与底物2-(苯氨基)苯甲腈配位形成中间体b,再进一步将苯基-钯键插入到c≡n,形成中间体c。在酸性条件下水解形成中间体d并形成钯物种。中间体d可以进一步发生分子内的傅克酰基化反应,生成中间体e。最后e再进一步脱水,形成目标产物9-苯基吖啶。
本发明的一种钯催化合成的芳基吖啶衍生物及其制备方法,通过以2-(芳氨基)苯甲腈衍生物和芳基硼酸作为反应物反应制得;其中2-(芳氨基)苯甲腈衍生物的结构式为
本发明方法可以直接一步合成目标产物,无需分离中间产物,只需在常压下搅拌反应既可获得目标物,产率最高可达到94%,大大简化了工艺工程,降低了能量消耗,具有高产率的优点;且反应过程中废弃溶液较少,也未排放出其它污染气体和液体,因此本发明减少了废弃溶液的排放,具有保护环境和保障操作人员健康的优点;在本发明中所使用的的物质毒性较低,保证了操作人员的健康;此外,可以制备一系列的芳基吖啶衍生物,该方法具有较强的底物普适性,为开发有关芳基吖啶衍生物的有机化合物提供了较好的保证。
以上所述仅是本发明的优选实施方式,本发明的保护范围并不仅局限于上述实施例,凡属于本发明思路下的技术方案均属于本发明的保护范围。应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理前提下的若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!