一种基于分子异构化机理的可用于铁离子特异性检测的新型荧光探针的制备方法及应用与流程
1.本发明涉及荧光探针,基于分子异构化机理的可用于铁离子特异性检测的新型荧光探针的制备方法,特别还涉及该荧光分子探针在环境和生物体内的铁离子检测方面的应用,属于化学分析、生物分析检测技术领域。
2.
背景技术:
3.铁是人体必要的微量元素之一,在氧气吸收代谢、电子转移、酶催化、神经传导等生物体内的生理过程中均有着至关重要的作用。人体内铁元素的含量过高,可能会引起一系列严重疾病,如肝脏,心脏和胰腺等器官功能障碍、肝炎、甚至癌症。而体内如果铁含量过低,则有可能出现免疫力下降、抗感染力降低、体温调节能力减弱,神经紊乱等疾病。最近有研究表明,fe
3+
离子与阿兹海默、帕金森等神经退行性疾病也息息相关。因此,开发高灵敏的的fe
3+
离子检测技术是非常有意义的。
4.目前,已有原子吸收法、电感耦合等离子发射光谱法、分光光度法、电化学法等传统方法可用于fe
3+
的检测,但这些方法均存在选择性差、操作复杂、成本高昂等问题,限制了其进一步使用。与之相比,荧光检测法具有许多优势,如灵敏度高、选择性好、成本低廉、无创性和易于实现实时监测。因此,已经有许多可用于fe
3+
离子检测的荧光分子探针被开发报道出来。然而,这些荧光分子探针大多数基于荧光猝灭机制,这限制了它们在生物系统中的应用。近年来,也有用于检测fe
3+
离子“turn-on”型荧光探针被报道,这些探针大多是基于罗丹明荧光母核,通过fe
3 +
诱导的从螺环形式(无荧光)向开环形式(有荧光)的转变而产生荧光变化。然而罗丹明母核结构的变化易受到多种因素的影响,如ph等,导致探针的稳定性差、特异性较差。因此,开发一种稳定性好、特异性强,灵敏度高的新型fe
3+
荧光分子探针具有较强的实际应用价值。
技术实现要素:
5.针对现有fe
3+
荧光分子探针存在的不足,本发明的目的在于提供一种稳定性好、特异性强、灵敏度高的fe
3+
荧光分子探针。
6.本发明的第二个目的在于提供上述荧光分子探针的高效制备方法。
7.本发明的第三个目的在于提供上述荧光分子探针在检测溶液和生物体内fe
3+
的检测应用。
8.为了实现上述目的,本发明提供了一种荧光分子探针,具有式i结构:
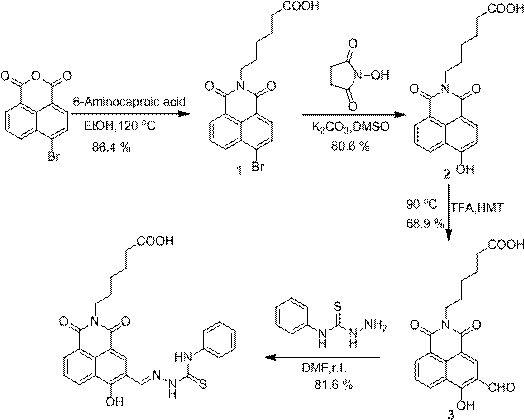
式(i)所述荧光探针的制备方法优选为:以4-溴-1,8-萘二甲酸酐、6-氨基己酸为原料,溶于无水乙醇,120℃下加热回流至反应完成,倒入冰水中,抽滤洗涤滤饼,柱层析干燥后可得淡黄色粉末。将其溶解于dmso中,加入n-羟基琥珀酰亚胺和无水碳酸钾,90 o
c下加热回流至反应完全,倒入冰水中并调节ph至近中性,用乙酸乙酯萃取、合并、干燥后硅胶柱层析纯化。将纯化后的产物溶解于三氟乙酸中,加入六次甲基四胺,90 o
c下加热回流至反应完全,冷却至室温,逐滴滴入冰水中并用调节ph至近中性,抽滤干燥后硅胶柱层析纯化。将纯化后的产物加入dmf溶液中,加入4-苯基-3-氨基硫脲,室温下反应完全,经硅胶柱层析纯化后可得目标分子探针。
9.本发明的合成如下所示:本发明提供了一种所述荧光探针的应用,可应用于环境和生物体内fe
3+
的定量检测,检测原理为:由于分子的荧光量子产率与分子的结构特征有密切关系,分子刚性越强,分子振动少,与其他分子碰撞失活的几率下降,荧光梁子效率提高。本发明荧光分子探针由于含
有c=n双键,在受光激发的情况下会导致双键顺反异构化,这种异构化作用将大大增加分子内的非辐射衰减途径,导致荧光量子产率降低,探针在483 nm处无荧光发射。而当fe
3+
与探针反应后,阻止了c=n双键的翻转,整个分子的刚性增加,483 nm处荧光显著增强。其他金属离子的加入则不会引起如此明显的荧光变化,从而实现了探针对fe
3+
的特异性识别。检测机理如图所示:本发明提供了一种所述荧光探针测定fe
3+
的方法。具体测定方法是:在室温条件下,所述荧光探针溶解于pbs缓冲溶液,乙腈、二氯甲烷或二甲基亚砜与pbs缓冲溶液按照一定比例配置的溶液中,将其浓度配置成10 μm-40 μm。向体系中加入不同浓度的fecl3水溶液,分别测定荧光强度,通过荧光强度与fe
3+
浓度的线性关系实现对fe
3+
的定量检测。
10.上述检测方法,优选的,溶剂体系为pbs:ch3cn= 1:1 (v/v)。
11.上述检测方法,优选的,ph为7.4。
12.上述检测方法,优选的,荧光探针浓度为10 μm。
13.本发明所述荧光探针可以应用于细胞内fe
3+
的检测。具体检测方法为:在hela培养基中加入10 μm的荧光探针溶液,置于 37 o
c,5%的co2下在培养箱中孵育30分钟后,用0.1 m的pbs 缓冲液(10 mm,ph=7.4)洗涤三次,除去未进入细胞的探针分子,然后更换培养基,再由fecl3缓冲溶液(35 μm)培养30分钟,细胞发出强烈的红色荧光。实验表明,荧光探针对细胞中的fe
3+
有良好的成像作用,可用于检测生物体内的fe
3+
。
14.相对现有技术,本发明的技术方案带来的有益技术效果:(1)本发明所涉及的一种检测fe
3+
的荧光分子探针,合成只需要3步,并且后处理过程简单,易于操作,产物易得,有利于大规模推广;(2)本发明所涉及的一种检测fe
3+
的荧光分子探针,具有响应快速、灵敏度高、特异性高的优点,能够避免其他金属离子的干扰,有利于环境和活细胞中fe
3+
的快速检测,在环境和生命科学领域具有较强的实际应用价值。
15.附图说明
16.【图1】本发明实施中荧光探针的荧光强度随fe
3+
浓度变化的发射光谱图;【图2】本发明实施中荧光探针对fe
3+
的选择性图;【图3】本发明实施中荧光探针在hela细胞内荧光共聚焦成像图。
具体实施方式
17.以下实施方式旨在进一步阐释说明本发明而不是对本发明的限定。
18.实施例1化合物1的合成:称取4-溴-1,8-萘二甲酸酐(2770 mg,10 mmol)溶于30 ml无水乙醇,向体系中加入6-氨基己酸(1637.5 mg,12.5 mmol)120℃加热反应,tlc监测至反应完全。将反应体系倒入冰水中,有黄色絮状物析出,抽滤并收集、洗涤滤饼,硅胶柱层析纯化,旋蒸除去溶剂后得到淡黄色粉末3369.6 mg,产率86.4 %。
19.化合物2的合成:分别向圆底烧瓶中加入化合物1(3120 mg, 8 mmol)、n-羟基琥珀酰亚胺(1012mg,8.8 mmol)和无水碳酸钾(3864 mg,4 mmol),并加入适量dmso溶液溶解,90℃下反应,tlc监测至反应完全。将体系倒入冰水中,用稀hcl溶液调节ph至近中性,用乙酸乙酯萃取,干燥后硅胶柱层析纯化,旋蒸除去溶剂后得到淡黄色固体2108.5 mg,产率80.6 %。
20.化合物3的合成分别向圆底烧瓶中加入化合物2(1962 mg,6 mmol),以及六次甲基四胺(4200 mg,30 mmol),加入15 ml三氟乙酸溶解溶解,90℃回流反应,tlc监测至反应完全。将体系倒入冰水中,用naoh溶液调节ph至近中性,抽滤、干燥后,硅胶柱层析纯化,旋蒸除去溶剂后得到黄色固体1467.6 mg,产率68.9 %。1h-nmr (400 mhz, dmso-d6, tms): δ = 1.29 (m, 2h), 1.52 (m, 2h), 1.67 (m, 2h), 2.30 (t, 2h, j=7.40 hz), 3.14 (t, 2h, j=7.56 hz), 7.86 (t, 1h, j=7.81 hz), 8.39 (s, 1h), 8.44 (d, 1h, j=7.42 hz), 8.49 (d, 1h, j=7.39 hz). hr-ms (esi, negative), calculated [m-h]: 354.2135, found [m-h]: 354.3415.目标分子探针的合成分别向圆底烧瓶中加入化合物3(1420 mg,4 mmol)和4-苯基-3-氨基硫脲(668.92 mg, 4 mmol),加入10 mln,n-二甲基甲酰胺(dmf)溶液溶液后,室温下反应,tlc监测至反应完全。将反应体系浓缩后,经硅胶柱分离纯化可得目标分子探针1645 mg,产率81.6 %。1h-nmr (400 mhz, dmso-d6, tms): δ = 1.30 (m, 2h), 1.51 (m, 2h), 1.70 (m, 2h), 2.20(s, 1h),2.28 (t, 2h, j=7.39 hz), 3.16 (t, 2h, j=7.48 hz), 6.81(t,1h, j=7.64), 7.20-7.22(m, 2h), 7.69-7.72(m, 2h), 7.85 (t, 1h, j=7.80 hz),8.44 (d, 1h, j=7.52 hz ), 8.48-8.50 (m, 2h), 8.74 (s, 1h). hr-ms (esi, negative), calculated [m-h]: 503.2319, found [m-h]: 503.2376。
[0021]
实施例2荧光探针母液的制备将上述分离得到的纯度在99 %以上的产物,准确称量5.04 mg并小心转移于50 ml的容量瓶中,室温下加入ch3cn溶液并使之完全溶解,定容至刻度线,得浓度为1 mm的探针母液。在测试过程中,每次用微量进样器量取20 μl的上述溶液,将其溶于测试体系中,使得每次测试总体积为2 ml,此时荧光探针的浓度为10 μm。
[0022]
实施例3fe
3+
母液的制备
fe
3+
用pbs缓冲溶液配制成5 ml不同的浓度梯度(0.1 mm、0.2 mm、0.4 mm、0.7 mm、1.0 mm、1.5 mm、2.0 mm、3.0 mm、4.0 mm)的母液。其余测试需要使用的金属离子则分别用pbs缓冲溶液配制成浓度为3 mm的母液。
[0023]
实施例4荧光探针荧光强度与fe
3+
浓度的关系量取4.900 ml pbs缓冲溶液,将50 μl浓度为1 mm的探针母液溶解其中,再移取50 μl不同浓度的fe
3+
母液中,使得最终整个检测体系探针的浓度为10 μm,而fe
3+
的浓度则分别为1 μm、2 μm、4 μm、7 μm、10 μm、15 μm、20 μm、30 μm、40 μm。室温孵育20 min后,分别在10 mm的比色皿中测试不同体系的荧光光谱(附图1)。结果表明,随着fe
3+
浓度逐渐增加,体系在487 nm处的荧光发射强度逐渐增强。
[0024]
实施例5荧光探针对fe
3+
检测的选择性将浓度为1 mm探针母液50 μl溶解于4.900 ml pbs缓冲溶液,再移取50 μl浓度为3 mm的nacl,kcl,mgcl2,cacl2,bacl2,mncl2,zncl2,pb(no3)2,fecl2,cucl2,agno3母液分别加入体系中,室温孵育20 min,分别测定其荧光光谱,记录487 nm的荧光强度值。如图所示,结果表明只有加入fe
3+
时,荧光探针的荧光明显加强,而加入其它测试金属离子时,均没有或只有微弱的荧光变化。表明该荧光探针具有良好的选择性。
[0025]
实施例6荧光探针对细胞中fe
3+
的响应在hela培养基中加入10 μm的荧光探针溶液,置于 37 o
c,5 %的co2下在培养箱中孵育30分钟后,用0.1 m的pbs 缓冲液(10 mm,ph=7.4)洗涤三次,除去未进入细胞的探针分子,然后更换培养基,再由fecl3缓冲溶液(35 μm)培养30分钟,用0.1 m的pbs 缓冲液(10 mm,ph=7.4)洗涤三次,置于荧光显微镜下观察其荧光变化,结果如附图3所示。实验表明进入细胞体内的探针分子和fe
3+
反应,发出强烈的红色荧光,因此该荧光探针对细胞中的fe
3+
有良好的成像作用,可用于检测生物体内的fe
3+
。
[0026]
上述虽然结合附图对本发明的具体实施方式进行了描述,但并非对发明范围的限制,本领域的相关技术人员能从发明公开的内容不需要付出创造性劳动即可做出的各种修改或变形仍在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1