一种基于心型弧状凹槽的高效循环肿瘤细胞分选芯片装置的制作方法
本发明涉及一种可用于进行循环肿瘤细胞分选实验的实验装置,本发明属于微流控技术研究领域。
背景技术:
微流控技术(microfluidics)是利用微通道(微米级)操控或处理微小流体(纳升到微升)的新兴科学技术,因具有精准化、微型化、可集成等颠覆性特点被应用于新一代医疗诊断、药品检测等领域。通过运用微流控技术的即时检测技术(poct)实现重大疾病早期排查、疗效检测、预后复诊等功能,成为贯彻医疗设备便民化、发展社区医疗的重要途径,其中循环肿瘤细胞(ctcs,circulatingtumorcells)检测作为新兴“液体活检”技术的一种,对肿瘤早期诊断治疗至关重要。然而,肿瘤患者血液中的ctcs含量极低,每毫升全血中仅含有1-10个ctcs,要实现血液中ctcs检测极具挑战性,关键在于如何将其准确、高效的分选出来。
利用惯性微流控技术通过微凹槽芯片实现对目标细胞分选成为新一代被动式循环肿瘤细胞分选技术,具备高通量、高分离纯度、高存活率等技术优势和操作简单、成本低廉等应用优势,为肿瘤疾病早期诊断、疗效评估和药品研制等提供了突破方向。
技术实现要素:
本发明目的是将循环肿瘤细胞(ctcs)从血液中分选出来。设计一种基于心型弧状凹槽的高效循环肿瘤细胞分选芯片装置,该装置可以实现ctcs高效率、高纯度的捕获和收集,其操作简单,应用范围广,具有较高的科研和临床应用价值。
本发明采用的技术方案为一种基于心型弧状凹槽的高效循环肿瘤细胞分选芯片装置,该分选芯片装置包括主体固体结构1、入口2、溶液主通道结构3、心型弧状凹槽结构4、出口5和下底板6。
具体而言,入口2、溶液主通道结构3、心型弧状凹槽结构4、出口5为主体固体结构1上凹槽或孔洞结构,且各凹槽或孔洞结构为芯片工作时流体流动区域;入口2和出口5处于溶液主通道3的两端位置,心型弧状捕获凹槽结构4位于溶液主通道3上靠近出口5的位置。心型弧状凹槽捕获结构4由半径为200微米的半圆和半径为400微米的四分之一圆组合而成,如图1所示,其与矩形捕获凹槽对称边的主要区别为心型弧形凹槽结构4为非对称非均匀弧,靠近入口2的一端较宽,靠近出口5的一端较窄,相比之下,不对称结构更有利于凹槽内捕获流场的形成,且充分利用心型弧状的壁面结构,促进凹槽内微涡胞结构的形成,使得捕获流量的控制更为精确,捕获细胞的尺寸分离度更高,更易实现ctcs的精准及高效率捕获,凹槽内用于捕获ctcs的涡胞结构如图2所示;心型弧状凹槽捕获结构4位于主通道的两侧位置处,利用惯性升力作用和碰撞捕获机理,将循环肿瘤细胞捕获进凹槽内部,由于心型弧状凹槽有利于微涡胞的形成,可以通过调节流速进行更加精准的ctcs的按尺度捕获。
所述主体结构1和下底板6均由聚二甲基硅氧烷制作,并通过氧离子上下键合固定,下底板6置于主体结构1底部,以支撑芯片主体结构并提供流动空间;
本发明总体工作过程如下:
含ctcs血液从入口2进入主通道结构3中,血液中的ctcs在流至心型弧状凹槽捕获结构4被捕获。由于ctcs尺寸略大于血液中其他细胞,故其在凹槽入口处获得相同的惯性升力后,更加容易被凹槽内的涡胞捕获,其他尺寸较小的血细胞则会随着主通道流体流出。相比于矩形凹槽,在相同的入口流速下,凹槽内形成结构更加稳定、高速的微涡胞,从而提供了更高的捕获效果,实现ctcs的分选。ctcs被凹槽捕获后可通过降低入口流速使细胞排出,以进行后续检测。
附图说明
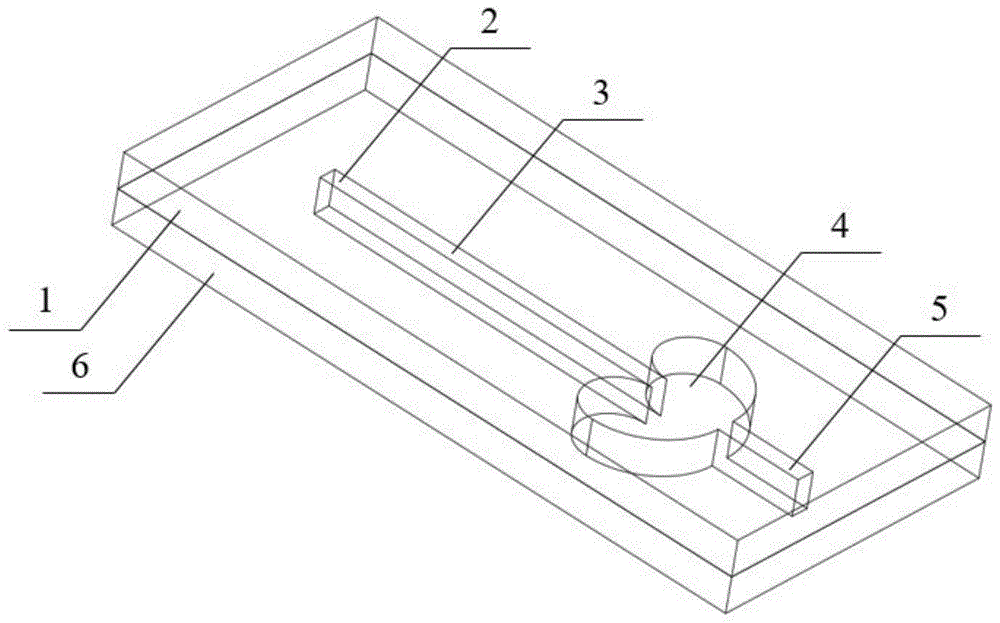
图1是本发明芯片的三维结构示意图。
图2是凹槽内涡胞结构流线图。
图3是芯片的平面结构示意图。
注释:
1.主体固体结构,2.入口,3.溶液主通道结构,4.心型弧状凹槽捕获结构,5.出口,6.下底板。
具体实施方式
下面结合结构附图对发明的工作过程和效果进行进一步的说明。
图1为一种基于心型弧状凹槽的高效循环肿瘤细胞分选芯片装置的结构示意图。
一种用于实现循环肿瘤细胞分选实验的微流控芯片装置。该通道包括主体固体结构1、入口2、溶液主通道结构3、心型弧状凹槽捕获结构4、出口5、和下底板6。入口2、溶液主通道结构3、心型弧状凹槽捕获结构4、出口5和下底板6为主体固体结构1上凹槽或孔洞结构,且各结构为芯片工作时流体流动区域;入口2和出口5处于溶液主通道3的两端位置,心型弧状捕获凹槽结构4位于溶液主通道3上靠近出口5的位置。心型弧状凹槽捕获结构4由半径为200微米的半圆和半径为400微米的四分之一圆组合而成,如图1所示,其与矩形捕获凹槽对称边的主要区别为心型弧形凹槽结构4为非对称非均匀弧,靠近入口2的一端较宽,靠近出口5的一端较窄,相比之下,不对称结构更有利于凹槽内捕获流场的形成,且充分利用心型弧状的壁面结构,促进凹槽内微涡胞结构的形成,使得捕获流量的控制更为精确,捕获细胞的尺寸分离度更高,更易实现ctcs的精准及高效率捕获,凹槽内用于捕获ctcs的涡胞结构如图2所示;心型弧状凹槽捕获结构4位于主通道的两侧位置处,利用惯性升力作用和碰撞捕获机理,将循环肿瘤细胞捕获进凹槽内部,由于心型弧状凹槽有利于微涡胞的形成,可以通过调节流速进行更加精准的ctcs的按尺度捕获。
所述主体结构1和下底板6由聚二甲基硅烷制成。
所述流体入口为设置在主体结构1上的上下贯通的孔洞结构。
本装置的工作过程如下:含ctcs血液从入口2进入主通道结构3中,血液中的ctcs在流至心型弧状凹槽捕获结构4被捕获。由于ctcs尺寸略大于血液中其他细胞,故其在凹槽入口处获得相同的惯性升力后,更加容易被凹槽内的涡胞捕获,其他尺寸较小的血细胞则会随着主通道流体流出。相比于矩形凹槽,在相同的入口流速下,凹槽内形成结构更加稳定、高速的微涡胞,从而提供了更高的捕获效果,实现ctcs的分选。ctcs被凹槽捕获后可通过降低入口流速使细胞排出,以进行后续检测。
注:由于微通道尺寸较小,用实际尺寸表示微流控芯片时不能有效表征微流控芯片流道部分的结构,因此附图使用的是微流道结构相对放大的芯片示意图。
- 还没有人留言评论。精彩留言会获得点赞!