尿路上皮癌的风险的判定方法与流程
本发明涉及一种尿路上皮癌的风险的判定方法。
背景技术:
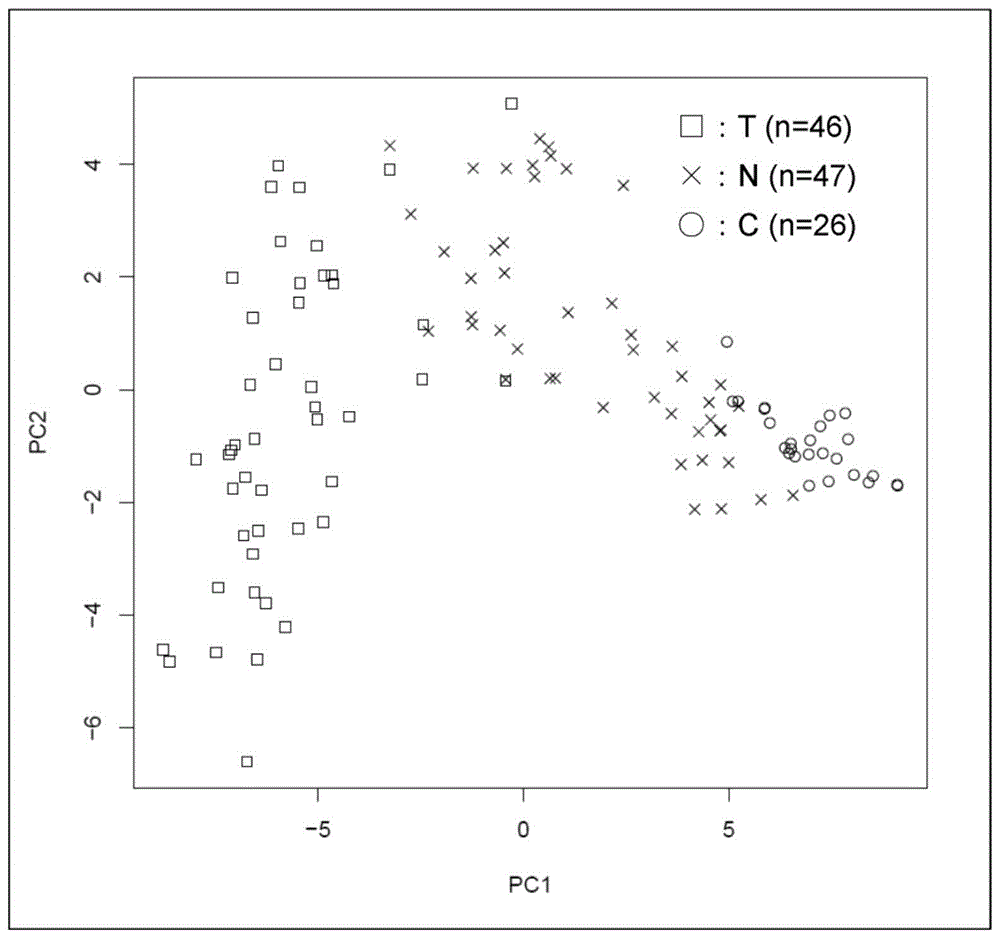
:尿路上皮癌以时间和空间多发性、即肾盂、输尿管和膀胱的多个位置或广范围的同时性和异时性的病变的发生为临床病理学特征。作为空间多发性的显著的例子,有从肾盂到尿道广泛发展至整个尿路的高异型度扁平上皮内癌。高异型度扁平上皮内癌被认为是恶性度高且预后不良的非乳头状(结节状)的浸润性尿路上皮癌的前期病变。与此相对,低异型度的浅表性乳头状尿路上皮癌虽然反复频繁复发(异时多发性),但预后良好。但是,低异型度的乳头状尿路上皮癌反复复发后使异型度增加,有时经过高异型度的乳头状尿路上皮癌发展至非乳头状(结节状)的浸润性尿路上皮癌。在尿路中,可以使用膀胱镜来观察病变,另外可以非侵害性地反复施行细胞诊断,更重要地,全膀胱切除术明显限制qol,因此,作为尿路上皮癌的治疗法,首先选择经尿道切除术(tur)、基于bcg注入的保守疗法。另一方面,尿路上皮癌由于其多发性,即使看起来手术疗法成功也不容易成为终诊,需要长期的慎重的后续观察。为了更良好地保持患者的qol和生命预后,对医生要求关于手术疗法的适用时期和手术方式进行适当判断。近年来,明确了dna的甲基化的异常与癌化密切相关,受到瞩目。作为癌细胞中的特征性的表观遗传异常,已知有一部分基因启动子区域中的cpg岛的异常的dna甲基化。cpg岛是介由磷酸二酯键(p)的胞嘧啶(c)-鸟嘌呤(g)这2碱基序列以高频率出现的区域,多存在于基因上游的启动子区域。cpg岛的dna甲基化的异常通过癌抑制基因的失活等而参与致癌。结肠癌、胃癌、肾细胞癌等中,报告了与临床病理学因子相关的cpg岛的dna甲基化亢进(非专利文献1~4、专利文献1~4)。关于尿路上皮癌,报告了通过测定临床试样的dna甲基化率来预测尿路上皮癌的发生风险等(非专利文献5)。进而,报告了由尿路上皮癌症例得到的非癌尿路上皮显示与正常尿路上皮不同的dna甲基化谱,表明dna甲基化异常参与尿路上皮癌的时间和空间多发性(非专利文献6)。另外,虽然未必着眼于尿路上皮癌的时间和空间多发性,但报告了同源异型基因hox基因组、编码转录因子的tbx2·gata2、受体型酪氨酸激酶fgfr3、组蛋白甲基化酶ezh2的dna甲基化亢进和重复序列line-1的dna甲基化减弱等与尿路上皮癌的关联(非专利文献7)。作为甲基化dna的解析方法,已经建立了利用亚硫酸氢盐(bisulfite)法的方法,并被广泛使用。作为以亚硫酸氢盐法为基本原理的甲基化dna解析方法,经常使用methylation-specificpcr(msp)法、combinedbisulfiterestrictionanalysis(cobra)法、基于bac阵列的甲基化cpg岛扩增法(bamca法)。在专利文献1中公开了通过bamca法来检测特定的基因的cpg位点的甲基化水平,从而对尿路上皮癌的发生风险和预后不良风险等进行检测的方法。然而,在该方法中,通过bac整体的杂交来测定bac克隆上的多个cpg位点的dna甲基化率的平均量,诊断精度高的cpg位点不明确,此外,测定方法繁杂,难以医疗实施。在专利文献2中公开了通过微珠阵列法、质谱分析(massarray法)、焦磷酸测序、甲基化敏感性高分辨率熔解曲线分析、定量pcr、亚硫酸氢盐处理物的直接测序、cobra法等来检测特定基因的cpg位点的甲基化水平,从而对肾细胞癌的预后不良风险进行检测的方法。在专利文献3、4中公开了基于离子交换色谱的保留时间的不同来检测特定基因的cpg位点的甲基化水平,从而判定癌的预后的方法。现有技术文献专利文献专利文献1:日本特开2010-207162号公报专利文献2:国际公开公报第2013/168644号专利文献3:国际公开公报第2015/129916号专利文献4:国际公开公报第2017/038983号非专利文献非专利文献1:nat.rev.cancer,4,988-993(2004)非专利文献2:proc.natl.acad.sci.usa,96,8681-8686(1999)非专利文献3:proc.natl.acad.sci.usa,104,18654-18659(2007)非专利文献4:cancerres.,59,5438-5442(1999)非专利文献5:cancersci.,101(1),231-240(2010)非专利文献6:病理和临床,35(9),852-857(2017)非专利文献7:methodsmol.biol.,1238.,183-215(2015)技术实现要素:本发明提供一种以dna的甲基化水平为基准来判定尿路上皮癌的风险的方法。本发明人等鉴定了在尿路上皮癌患者的尿路上皮组织中与正常组织相比更高度地甲基化了的基因。进而,发现能够通过测定这些基因的dna甲基化水平来判定尿路上皮癌的发病风险。因此,本发明提供以下方案。〔1〕一种尿路上皮组织的癌化风险的判定方法,包括:对来自尿路上皮细胞或含有该尿路上皮细胞的组织的基因组dna中的选自tenm3、hoxc4、tlr1、cpvl和prdm16中的至少1个基因的cpg位点的dna甲基化水平进行检测,以及由检测的dna甲基化水平判定该尿路上皮组织的癌化风险。〔2〕根据〔1〕所述的方法,其中,所述dna甲基化水平的检测包括使用经亚硫酸氢盐处理的所述基因组dna对所述至少1个基因的cpg位点的dna甲基化水平进行检测。〔3〕根据〔2〕所述的方法,其中,所述dna甲基化水平的检测使用焦磷酸测序法、质谱分析、微珠阵列法或离子交换色谱进行。〔4〕根据〔1〕~〔3〕中任一项所述的方法,其中,所述tenm3的cpg位点为选自由序列号1所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点,所述hoxc4的cpg位点为选自由序列号2所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点,所述tlr1的cpg位点为选自由序列号3所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点,所述cpvl的cpg位点为选自由序列号4所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点,所述prdm16的cpg位点为选自由序列号5所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点。〔5〕根据〔1〕~〔3〕中任一项所述的方法,其中,基于ncbi数据库基因组版本(genomebuild)37,所述tenm3的cpg位点为选自第4染色体的183,710,473位、183,710,455位、183,710,441位、183,710,349位、183,710,344位、183,710,318位和183,710,311位中的至少1个位置,所述hoxc4的cpg位点为选自第12染色体的54,438,419位和54,438,426位中的至少1个位置,所述tlr1的cpg位点为第4染色体的38,807,259位,所述cpvl的cpg位点为第7染色体的29,187,019位,所述prdm16的cpg位点为第1染色体的3,078,013位。〔6〕一种用于尿路上皮癌的风险判定的引物或探针,具有至少12个碱基的链长且与经亚硫酸氢盐处理后的选自tenm3、hoxc4、tlr1、cpvl和prdm16中的至少1个基因所含的cpg位点杂交。〔7〕根据〔6〕所述的引物或探针,其中,所述tenm3的cpg位点为选自由序列号1所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点,所述hoxc4的cpg位点为选自由序列号2所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点,所述tlr1的cpg位点为选自由序列号3所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点,所述cpvl的cpg位点为选自由序列号4所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点,所述prdm16的cpg位点为选自由序列号5所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点。〔8〕根据〔6〕所述的引物或探针,其中,基于ncbi数据库基因组版本37,所述tenm3的cpg位点为选自第4染色体的183,710,473位、183,710,455位、183,710,441位、183,710,349位、183,710,344位、183,710,318位和183,710,311位中的至少1个位置,所述hoxc4的cpg位点为选自第12染色体的54,438,419位和54,438,426位中的至少1个位置,所述tlr1的cpg位点为第4染色体的38,807,259位,所述cpvl的cpg位点为第7染色体的29,187,019位,所述prdm16的cpg位点为第1染色体的3,078,013位。〔9〕根据〔6〕~〔8〕中任一项所述的引物或探针,选自由序列号6~15所示的核苷酸序列构成的多核苷酸和其互补链。〔10〕根据〔9〕所述的引物或探针,是由序列号6和7所示的多核苷酸、序列号8和9的多核苷酸、序列号10和11的多核苷酸、序列号12和13的多核苷酸、序列号14和15的多核苷酸、或者它们的互补链的组合构成的引物组。〔11〕一种受验体的尿路上皮癌的风险的判定方法,包括:对来自受验体的尿路上皮细胞或含有该尿路上皮细胞的组织的基因组dna中的选自tenm3、hoxc4、tlr1、cpvl和prdm16中的至少1个基因的cpg位点的dna甲基化水平进行检测,以及由检测的dna甲基化水平来判定该受验体的尿路上皮癌的风险。〔12〕根据〔11〕所述的方法,其中,所述dna甲基化水平的检测包括使用经亚硫酸氢盐处理的所述基因组dna对所述至少1个基因的cpg位点的dna甲基化水平进行检测。〔13〕根据〔12〕所述的方法,其中,所述dna甲基化水平的检测使用焦磷酸测序法、质谱分析、微珠阵列法或离子交换色谱进行。〔14〕根据〔11〕~〔13〕中任一项所述的方法,其中,所述tenm3的cpg位点为选自由序列号1所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点,所述hoxc4的cpg位点为选自由序列号2所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点,所述tlr1的cpg位点为选自由序列号3所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点,所述cpvl的cpg位点为选自由序列号4所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点,所述prdm16的cpg位点为选自由序列号5所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点。〔15〕根据〔11〕~〔13〕中任一项所述的方法,其中,基于ncbi数据库基因组版本37,所述tenm3的cpg位点为选自第4染色体的183,710,473位、183,710,455位、183,710,441位、183,710,349位、183,710,344位、183,710,318位和183,710,311位中的至少1个位置,所述hoxc4的cpg位点为选自第12染色体的54,438,419位和54,438,426位中的至少1个位置,所述tlr1的cpg位点为第4染色体的38,807,259位,所述cpvl的cpg位点为第7染色体的29,187,019位,所述prdm16的cpg位点为第1染色体的3,078,013位。根据本发明,能够以简便且高灵敏度和特异性判定尿路上皮癌的风险。本发明提供用于防止检诊受诊者等将来发生尿路上皮癌的生活习惯改善等的预防干预的指南,或者使实际发病时的早期诊断成为可能,进而有助于提高患者的qol和存活率。附图说明图1是用于解析dna甲基化水平的变化的、infinium(注册商标)测定中的使用2750个探针的主成分分析。(c):来自正常组织的检体(n=26),(n):来自尿路上皮癌患者的非癌组织的检体(n=47),(t):来自尿路上皮癌组织的检体(n=46)。图2是正常组织(c)和尿路上皮癌患者的非癌组织(n)中的满足诊断阈值的cpg位点数的直方图。图3是infinium(注册商标)测定与焦磷酸测序或massarray(注册商标)间的dna甲基化水平检测值的相关。具体实施方式本说明书中,“尿路上皮癌”是指在包含肾盂、输尿管、尿道的尿路的上皮细胞发生的癌。尿路上皮癌由于异时性或同时性多发,因此,本说明书中的“尿路上皮癌”包含原发癌和已在组织内转移的癌。另外,在本说明书中,作为“受验体”,可举出人类,例如需要判定尿路上皮癌的风险的人(例如检诊受诊者)、怀疑患有尿路上皮癌的患者等。在本说明书中,“癌的风险”是指患癌或者将来患癌的风险。另外,在本说明书中,“组织的癌化风险”是指组织具有癌或者将来具有癌的风险。作为该“组织”,可举出以前没有观察到癌的组织和怀疑具有癌的组织。在本说明书中,“cpg位点”是指在dna中胞嘧啶(c)与鸟嘌呤(g)之间进行磷酸二酯键合(p)的部位。cpg位点以高频率出现的区域被称为cpg岛。cpg岛多存在于接近基因的编码区域的位置、例如启动子区域,因此,基因的cpg位点大量存在于cpg岛或该基因的启动子区域,所述cpg岛存在于接近该基因的编码区域的位置。在本说明书中,在没有另行定义时,“(某)基因的cpg位点”优选是指存在于接近该基因的编码区域的位置的cpg岛中所含的cpg位点,更优选是指存在于该基因的启动子区域的cpg位点。在本说明书中,“dna甲基化”是指在dna中,胞嘧啶的5位的碳被甲基化的状态。另外,在本说明书中,某cpg位点的“dna甲基化水平”是指在该cpg位点中dna被甲基化的比例。在本说明书中,dna甲基化水平高和低分别是指dna被甲基化的比例高和低。在本说明书中,有关氨基酸序列和核苷酸序列的“至少95%同源性”是指95%以上的同源性、优选96%以上的同源性、更优选97%以上的同源性、进一步优选98%以上的同源性、进一步优选99%以上的同源性。本发明提供一种尿路上皮组织的癌化风险的判定方法,包括:对来自受验体的尿路上皮细胞或含有该尿路上皮细胞的组织的基因组dna中的选自tenm3、hoxc4、tlr1、cpvl和prdm16中的至少1个基因的cpg位点的dna甲基化水平进行检测,以及由检测的dna甲基化水平来判定该尿路上皮组织的癌化风险。另外,本发明提供一种受验体的尿路上皮癌的风险的判定方法,包括:对来自受验体的尿路上皮细胞或含有该尿路上皮细胞的组织的基因组dna中的选自tenm3、hoxc4、tlr1、cpvl和prdm16中的至少1个基因的cpg位点的dna甲基化水平进行检测,以及由检测的dna甲基化水平来判定该受验体的尿路上皮癌的风险。作为本发明的方法中使用的来自尿路上皮细胞或含有该尿路上皮细胞的组织的基因组dna,可举出由尿路上皮细胞或含有该尿路上皮细胞的组织制备的基因组dna、来自尿中的尿路上皮细胞的dna或无细胞dna等。作为该尿路上皮细胞或含有该尿路上皮细胞的组织,例如可举出在外科手术、活检中采取的新鲜尿路上皮组织、采取后冷冻的冷冻尿路上皮组织、采取后实施福尔马林固定和石蜡包埋而得的尿路上皮组织、由尿浓缩而得的尿路上皮细胞等。其中,从抑制组织中的基因组dna的分解等,能够更高效地进行dna甲基化水平的检测的观点考虑,优选冷冻尿路上皮组织。作为由尿路上皮组织或尿路上皮细胞制备样品dna的方法,没有特别限制,可以适当选择使用公知的方法。作为制备dna的公知的方法,可举出苯酚氯仿法或使用市售的dna提取试剂盒例如后述的qiaampdnaminikit(qiagen公司制)、cleancolumns(nextec公司制)、aquapure(bio-rad公司制)、zrplant/seeddnakit(zymoresearch公司制)、prepgem(zygem公司制)、buccalquick(trimgen公司制)的dna提取方法等。另外,来自尿中的尿路上皮细胞的dna或无细胞dna也可以使用市售的来自尿中的细胞的dna或无细胞dna纯化用试剂盒来制备。优选所制备的基因组dna进行亚硫酸氢盐处理。作为dna的亚硫酸氢盐处理的方法,没有特别限制,可以适当选择公知的方法而使用。作为用于亚硫酸氢盐处理的公知的方法,例如可举出使用后述的epitectbisulfitekit(48)(qiagen公司制)、methyleasy(humangeneticsignaturespty公司制)、cells-to-cpgbisulfiteconversionkit(appliedbiosystems公司制)、cpgenometurbobisulfitemodificationkit(merckmillipore公司制)等市售的试剂盒的方法。进而,优选将上述经亚硫酸氢盐处理的dna进行扩增。扩增的方法没有特别限制,优选可利用pcr。扩增的方法和条件可以根据扩增对象的dna的序列、长度、量等适当选择公知的方法和条件而使用。如后述的实施例所示,本发明人等明确了5个基因(tenm3、hoxc4、tlr1、cpvl和prdm16)的cpg位点的dna甲基化水平在正常尿路上皮组织和来自尿路上皮癌患者的尿路上皮组织中不同。因此,在本发明的方法中,作为检测dna甲基化水平的对象的cpg位点为选自该5个基因(即,tenm3、hoxc4、tlr1、cpvl和prdm16)中的至少1个基因的cpg位点。优选在本发明的方法中作为检测dna甲基化水平的对象的cpg位点为选自tenm3、hoxc4、tlr1和cpvl中的至少1个基因的cpg位点。因此,如上所述将经亚硫酸氢盐处理的dna通过pcr等进行扩增时,将包含选自该5个基因、优选tenm3、hoxc4、tlr1和cpvl中的至少1个基因的cpg位点的区域进行扩增。优选将包含选自该5个基因中的至少1个基因的cpg岛或启动子区域的一部分或全部的dna区域进行扩增。更优选将包含选自tenm3、hoxc4、tlr1和cpvl中的至少1个基因的cpg岛或启动子区域的一部分或全部的dna区域进行扩增。进一步优选将包含由序列号1~5中的任一者所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸的dna区域进行扩增。进一步优选将包含由序列号1~4中的任一者所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸的dna区域进行扩增。tenm3是对由refseqid:np_001073946确定的蛋白质进行编码的基因,hoxc4是对由refseqid:np_705897确定的蛋白质进行编码的基因,tlr1是对由refseqid:np_003254确定的蛋白质进行编码的基因,cpvl是对由refseqid:np_001334981确定的蛋白质进行编码的基因,prdm16是对由refseqid:np_071397确定的蛋白质进行编码的基因。优选本发明中使用的tenm3的cpg位点为选自由序列号1所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点。优选本发明中使用的tenm3的cpg位点是存在于选自第4染色体的183,710,473位、183,710,455位、183,710,441位、183,710,349位、183,710,344位、183,710,318位、和183,710,311位中的至少1个位置的cpg位点。优选本发明中使用的hoxc4的cpg位点为选自由序列号2所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点。优选本发明中使用的hoxc4的cpg位点存在于第12染色体的54,438,419位、和54,438,426位。优选本发明中使用的tlr1的cpg位点为选自由序列号3所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点。优选本发明中使用的tlr1的cpg位点存在于第4染色体的38,807,259位。优选本发明中使用的cpvl的cpg位点为选自由序列号4所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点。优选本发明中使用的cpvl的cpg位点存在于第7染色体的29,187,019位。优选本发明中使用的prdm16的cpg位点为选自由序列号5所示的核苷酸序列或与该序列具有至少95%同源性的核苷酸序列构成的多核苷酸所含的cpg位点中的至少1个cpg位点。优选本发明中使用的prdm16的cpg位点存在于第1染色体的3,078,013位。在本说明书中,cpg位点的染色体上的位置以作为基准人类基因组序列的ncbi数据库基因组版本37上的位置为基准来表示。将本发明中使用的优选的cpg位点记载于表1。[表1]在本发明的方法中,检测dna甲基化水平的cpg位点优选为选自存在于表1中记载的染色体上的位置的cpg位点中的至少1个。更优选本发明的方法中检测dna甲基化水平的cpg位点为选自存在于第4染色体的183,710,473位、183,710,455位、183,710,441位、183,710,349位、183,710,344位、183,710,318位和183,710,311位(以上为tenm3的基因区域)、第12染色体的54,438,419位和54,438,426位(以上为hoxc4的基因区域)、第4染色体的38,807,259位(以上为tlr1的基因区域)以及第7染色体的29,187,019位(以上为cpvl的基因区域)的cpg位点中的至少1个。从能够进一步提高dna甲基化水平的检测的灵敏度或特异性的观点考虑,也可以将上述的cpg位点组合而作为检测对象。作为该组合的优选的例子,可举出表1所示的tenm3的cpg位点的任1个以上与表1所示的其它cpg位点的任1个以上的组合、表1所示的tenm3的cpg位点的任2个以上的组合等。作为该组合的更优选的例子,可举出选自下述表2中记载的cpg位点的组合中的至少1个。[表2]在本发明的方法中,作为对cpg位点的dna甲基化水平进行检测的方法,只要是能够对给定的cpg位点中的dna甲基化水平进行定量的方法即可,可以适当选择公知的方法。作为该公知的方法,例如可举出以下所示的第1~第8方法。第1方法是利用使用了以在3’末端具有与甲基化胞嘧啶或非甲基化胞嘧啶互补的碱基的方式构建的探针的单碱基伸长反应对cpg位点中的dna的甲基化进行定量的方法。例如,第1方法是基于以下原理的方法。首先,对上述基因组dna实施亚硫酸氢盐处理。应予说明,通过该亚硫酸氢盐处理,非甲基化胞嘧啶残基被转换成尿嘧啶,但甲基化胞嘧啶残基未被转换(参照clarksj等、nucleicacidsres、1994年、22卷、2990~7页)。接着,以如此进行了亚硫酸氢盐处理的基因组dna为模板进行全基因组扩增,利用酶进行片段化(通常300~600bp左右的片段化),解离成单链。在第1方法中,制备一种与通过亚硫酸氢盐处理而转换的基因组dna杂交的探针,该探针的3’末端的碱基是与上述cpg位点的胞嘧啶互补的碱基。即,该cpg位点被甲基化时,探针的3’末端的碱基成为鸟嘌呤,该cpg位点未被甲基化时,探针的3’末端的碱基成为腺嘌呤。然后,使这样的仅仅与上述cpg位点互补的3’末端的碱基不同的2种探针与上述单链dna片段杂交,在经荧光标记的碱基存在下进行单碱基伸长反应。其结果,该单链片段的cpg位点被甲基化时,在3’末端的碱基为鸟嘌呤的探针(甲基化检测用探针)中通过单碱基伸长反应而掺入经荧光标记的碱基,但在3’末端的碱基为腺嘌呤的探针(非甲基化检测用探针)中,由于3’末端的碱基的错配而未发生单碱基伸长反应,从而经荧光标记的碱基未被掺入。另一方面,该单链片段的cpg位点未被甲基化时,虽然在非甲基化检测用探针中掺入经荧光标记的碱基,但在甲基化检测用探针中未掺入经荧光标记的碱基。因此,可以根据甲基化检测用探针和/或非甲基化检测用探针所发出的荧光的强度来算出dna甲基化水平。另外,在该第1方法中,作为其它方式,可以使用与通过亚硫酸氢盐处理而转换的基因组dna杂交的探针即该探针的3’末端的碱基成为与上述cpg位点的鸟嘌呤互补的碱基的探针代替上述甲基化检测用探针和非甲基化检测用探针。然后,使该探针与上述单链dna片段杂交,在用荧光物质标记了的鸟嘌呤和/或利用与该荧光物质不同的荧光色素标记了的腺嘌呤的存在下进行单碱基伸长反应。其结果,上述cpg位点被甲基化时,在该探针掺入经荧光标记的鸟嘌呤,另一方面,上述cpg位点未被甲基化时,在该探针掺入经荧光标记的腺嘌呤,因此,可以根据掺入上述探针的各荧光物质所发出的荧光的强度来算出dna甲基化水平。作为该第1方法的优选的例子,例如可举出微珠阵列法(例如,infinium(注册商标)测定)。第2方法是通过质谱分析对甲基化dna进行定量的方法。例如,第2方法是基于以下原理的方法。首先,对上述基因组dna实施亚硫酸氢盐处理。接着,以经亚硫酸氢盐处理的基因组dna为模板,将含有至少一个上述cpg位点的dna用附加了t7启动子的引物进行扩增。接着,将经扩增的dna转录成rna,利用rnase进行碱基特异性的切割反应。然后,将该切割反应产物施加于质谱分析仪进行质量测定。然后,将通过质量测定而得到的来自甲基化胞嘧啶残基的质量(胞嘧啶的质量)与来自非甲基化胞嘧啶残基的质量(尿嘧啶的质量)进行比较,算出上述cpg位点中的dna甲基化水平。作为该第2方法的优选的例子,例如可举出使用质谱分析仪的dna甲基化解析法(例如,参照massarray(注册商标)、jurinkec等、mutatres、2005年、573卷、83~95页和后述的实施例2)。在massarray(注册商标)中,将亚硫酸氢盐处理后的含有cpg位点的dna进行扩增,转录成rna后,利用rnaase在尿嘧啶的部位进行特异性切割。由此,根据dna的甲基化的有无而生成长度不同的rna片段。将得到的rna片段进行质谱分析,由此将cpg位点被甲基化的片段和非甲基化片段依照分子量的差进行分离并检测。用于含有该cpg位点的dna的扩增的引物可以使用epidesigner(sequenom公司制,massarray用引物设计软件)等进行设计。在rna片段的质谱分析中,可使用能够检测一个碱基的质量的差异的maldi-tofmas(例如,sequenom公司制,massarrayanalyzer4)。根据来自甲基化dna的rna片段与来自非甲基化dna的rna片段的质量的比来算出dna的甲基化水平。第3方法是基于以下原理的方法。首先,对上述基因组dna实施亚硫酸氢盐处理。应予说明,通过该亚硫酸氢盐处理,非甲基化胞嘧啶残基被转换成尿嘧啶,但在下述伸长反应(序列反应)中,尿嘧啶以胸腺嘧啶的形式显示。接着,以如此经亚硫酸氢盐处理的基因组dna为模板,将含有至少一个上述cpg位点的dna进行扩增。然后,使经扩增的dna解离成单链。接着,在经解离的单链dna中,仅分离一条链。然后,从上述cpg位点的碱基的附近1个碱基1个碱基地进行伸长反应,使此时生成的焦磷酸进行酶促发光,并测定发光的强度。将以这样的方式得到的来自甲基化胞嘧啶残基的发光的强度(胞嘧啶的发光强度)与来自非甲基化胞嘧啶残基的发光的强度(胸腺嘧啶的发光强度)进行比较,例如利用下述式算出上述cpg位点中的dna甲基化水平(%)。dna甲基化水平(%)=胞嘧啶的发光强度×100/(胞嘧啶的发光强度+胸腺嘧啶的发光强度)。作为第3方法,例如可举出焦磷酸测序法(注册商标,pyrosequencing)(参照anal.biochem.(2000)10:103-110)等。第4方法是基于以下原理的方法。首先,对上述基因组dna进行亚硫酸氢盐处理。接着,在含有插入到dna双链间时发出荧光的嵌入剂的反应体系中,以上述经亚硫酸氢盐处理的基因组dna为模板,对含有至少1个上述cpg位点的核苷酸进行扩增。接着,改变上述反应体系的温度,并检测上述嵌入剂所发出的荧光的强度的变动。将含有至少1个上述cpg位点的核苷酸的熔解曲线与以甲基化·非甲基化对照检体为模板的扩增产物的熔解曲线相比,算出上述cpg位点中的dna甲基化水平。作为第4方法,例如可举出甲基化敏感性高分辨率熔解曲线分析(methylation-sensitivehighresolutionmelting:ms-hrm,参照wojdacztk等、natprotoc.,2008年、3卷、1903~8页)。第5方法是基于以下原理的方法。首先,对上述基因组dna实施亚硫酸氢盐处理。接着,制备上述cpg位点被甲基化时可扩增的引物组和上述cpg位点未被甲基化时可扩增的引物组。然后,以上述经亚硫酸氢盐处理的基因组dna为模板,将含有至少1个上述cpg位点的核苷酸使用这些引物组分别进行扩增。然后,通过将得到的扩增产物的量、即甲基化cpg位点特异性的扩增产物的量和非甲基化cpg位点特异性的扩增产物的量进行比较,算出上述cpg位点中的dna甲基化水平。进而,在该第5方法中,作为其它方式,首先,对上述基因组dna实施亚硫酸氢盐处理。接着,制备具有在上述cpg位点被甲基化时可杂交的核苷酸且标记了报告荧光色素和猝灭荧光色素的寡核苷酸探针。另外,制备具有在上述cpg位点未被甲基化时可杂交的核苷酸且标记了与上述报告荧光色素不同的报告荧光色素和猝灭荧光色素的寡核苷酸探针。然后,使上述寡核苷酸探针与经亚硫酸氢盐处理的基因组dna杂交,进一步以上述寡核苷酸探针杂交的基因组dna为模板,将含有上述cpg位点的核苷酸进行扩增。然后,通过伴随上述扩增的寡核苷酸探针的分解来检测上述报告荧光色素所发出的荧光。通过将以这样的方式检测的甲基化胞嘧啶cpg位点特异性的报告荧光色素所发出的荧光的强度与非甲基化胞嘧啶cpg位点特异性的报告荧光色素所发出的荧光的强度进行比较而算出上述cpg位点中的dna甲基化水平。作为第5方法,例如可举出使用taqman探针(注册商标)的methylight法等甲基化特异性定量pcr法(methylation-specificpolymerasechainreaction(ms-pcr)usingreal-timequantitativepcr)。第6方法是基于以下原理的方法。首先,对上述基因组dna实施亚硫酸氢盐处理。接着,以经亚硫酸氢盐转换的含有上述cpg位点的核苷酸为模板进行直接测序反应。然后,通过将基于所确定的碱基序列的荧光强度、即来自甲基化胞嘧啶残基的荧光强度(胞嘧啶的荧光强度)与来自非甲基化胞嘧啶残基的荧光强度(胸腺嘧啶的荧光强度)进行比较而算出上述cpg位点中的dna甲基化水平。进而,在该第6方法中,作为其它方式,首先,对上述基因组dna实施亚硫酸氢盐处理。接着,将经亚硫酸氢盐转换的含有上述cpg位点的核苷酸通过pcr反应等进行克隆。然后,分别确定所得到的多个克隆产物的碱基序列,通过将具有甲基化胞嘧啶cpg位点特异性的碱基序列的克隆产物的个数与具有非甲基化胞嘧啶cpg位点特异性的碱基序列的克隆产物的个数进行比较而算出上述cpg位点中的dna甲基化水平。作为第6方法,例如可举出亚硫酸氢盐直接测序(bisulfitedirectsequencing)、亚硫酸氢盐克隆测序(bisulfitecloningsequencing)(参照kristensenls等、clinchem、2009年、55卷、1471~83页)。第7方法是基于以下原理的方法。首先,对上述基因组dna实施亚硫酸氢盐处理。接着,以经亚硫酸氢盐转换的含有上述cpg位点的核苷酸为模板,将含有上述cpg位点的区域利用pcr进行扩增。接着,将经扩增的dna片段用识别在该cpg位点被甲基化时和未被甲基化时序列不同的位置的限制酶进行处理。然后,对通过电泳而分级的、来自甲基化cpg位点的限制酶片段与来自非甲基化cpg位点的限制酶片段的条带浓度进行定量解析,由此能够算出该cpg位点的dna甲基化水平。作为第7方法,例如可举出cobra(通过并用亚硫酸氢盐与限制酶进行的解析)。第8方法是使用离子交换色谱的方法。例如,第8方法是基于以下原理的方法。首先,对上述基因组dna实施亚硫酸氢盐处理。接着,将其片段化而得到含有cpg位点的dna片段。以得到的dna片段为模板,将含有cpg位点的区域利用pcr进行扩增。接着,将经扩增的dna片段施加于离子交换色谱,将cpg位点被甲基化的dna和未被甲基化的dna分离。在第8方法中,pcr的扩增产物的链长可考虑pcr的扩增时间的缩短以及离子交换色谱中的分析时间的缩短、分离性能的维持等要素而适当选择。例如,使用cpg位点多的样品dna时的pcr扩增产物的链长优选为1000bp以下,更优选为700bp以下,进一步优选为500bp以下。另一方面,对于使用cpg位点少的样品dna时的pcr扩增产物的链长,使用避免pcr中的非特异性杂交的15mer附近的引物时的pcr扩增产物的链长即30~40bp成为下限。另一方面,优选以cpg位点的含有率变得丰富的方式设计引物。例如,cpg位点的胞嘧啶相对于pcr扩增产物的链长优选含有2%以上,更优选含有5%以上。在第8方法中,非甲基化胞嘧啶残基通过基因组dna的亚硫酸氢盐处理转换成尿嘧啶后,通过pcr进一步转换成胸腺嘧啶。另一方面,甲基化胞嘧啶残基在亚硫酸氢盐处理和pcr后也是胞嘧啶的状态。根据该碱基的不同,含有甲基化胞嘧啶的片段(甲基化片段)和非甲基化片段在离子交换色谱中作为保留时间不同的不同峰被检测出。即,甲基化片段与非甲基化片段相比,作为保留时间更短的峰被检测出。因此,可以基于离子交换色谱中的峰的保留时间来判定cpg位点的dna是否甲基化。进而,在施加于离子交换色谱的dna中含有多个cpg位点时,越更多个cpg位点被甲基化,峰的保留时间越进一步变短。因此,可以基于该峰的保留时间来算出cpg位点的dna甲基化水平。或者,也可以基于该峰的面积或高度来算出甲基化片段和非甲基化片段各自的存在量、存在比率。优选通过cpg位点的dna甲基化水平与已知的样品(对照)进行比较,或者利用使用dna甲基化水平已知的样品预先制作的校正曲线来判断cpg位点的dna是否被甲基化或者cpg位点的dna甲基化水平。或者使用dna甲基化水平已知的样品来预先确定作为将cpg位点被高度甲基化的甲基化片段的峰的保留时间与甲基化水平低的片段的峰的保留时间分开的基准的保留时间(在本说明书中也称为基准保留时间)。例如,在早于基准保留时间的保留时间检测出的片段可判断为被高度甲基化的dna。第8方法中进行的离子交换色谱优选为阴离子交换色谱。作为柱的填充剂,只要是在表面具有强阳离子性基团的基材粒子就没有特别限定,优选国际公开公报第2012/108516号所示的在填充剂表面具有强阳离子性基团和弱阳离子性基团两者的基材粒子。更优选该基材粒子是含有具有强阳离子性基团(优选为季铵盐)的亲水性聚合物的层共聚于疏水性交联聚合物粒子的表面的被覆聚合物粒子和导入该被覆聚合物粒子表面的弱阳离子性基团(优选为叔氨基)的基材粒子。色谱分析时的柱温优选为30℃以上且小于90℃。以上,例示了能够优选适用于本发明中“检测dna甲基化水平的方法”的方法,但方法并不限定于此。在上述第1~第8方法中,如上所述,由尿路上皮组织制备的基因组dna被进一步供于亚硫酸氢盐处理。因此,在本发明的方法中,cpg位点的dna甲基化水平的检测中使用的基因组dna优选为来自尿路上皮细胞组织或含有该尿路上皮细胞组织的组织的经亚硫酸氢盐处理的基因组dna。在本发明的方法中,由检测出的cpg位点的dna甲基化水平来判定受验尿路上皮组织的癌化风险或受验体的尿路上皮癌的风险。优选判定该受验尿路上皮组织的癌化风险是否高,或者该受验体的尿路上皮癌的风险是否高。更优选判定该受验尿路上皮组织将来保有尿路上皮癌的风险是否高,或者该受验体将来患有尿路上皮癌的风险是否高。用于风险判定的具体的指标可以由本领域技术人员根据检测dna甲基化水平的方法而适当设定。以下对风险判定步骤的实施方式进行描述。在第一实施方式中,首先,关于各dna甲基化水平检测方法,对各个cpg位点进行接收者操作特性(roc)解析,求出灵敏度(阳性率)和特异度(阴性率),将灵敏度和特异度的和达到最大的dna甲基化水平设定为指标(截止值)。在上述第一实施方式中,关于因尿路上皮组织的癌化而使甲基化水平亢进的cpg位点(例如,表1所示tenm3的cpg位点),通过本发明的方法检测出的dna甲基化水平比截止值高时,判断为dna甲基化水平超过诊断阈值,受验组织或受验体被分类为高风险组,但如果检测出的甲基化水平为该截止值以下,则该受验组织或受验体被分类为不是高风险组。另一方面,关于因尿路上皮组织的癌化而甲基化水平降低的cpg位点(例如,表1所示的hoxc4、tlr1、cpvl和prdm16的cpg位点),通过本发明的方法检测出的dna甲基化水平低于截止值时,判断为dna甲基化水平超过诊断阈值,受验组织或受验体被分类为高风险组,但如果检测出的甲基化水平为该截止值以上,则该受验组织或受验体被分类为不是高风险组。在上述第一实施方式中,检测多个cpg位点的甲基化水平时,可以将dna甲基化水平超过上述诊断阈值的cpg位点的个数或比例作为用于风险判定的指标。例如,调查的全部cpg位点的甲基化水平均超过诊断阈值时,可以将受验组织或受验体分类为高风险组。或者,调查的cpg位点中的一定比例以上的甲基化水平超过诊断阈值时,可以将受验组织或受验体分类为高风险组。或者一定数以上的cpg位点的甲基化水平超过诊断阈值时,可以将受验组织或受验体分类为高风险组。另一方面,不满足这些基准的受验组织或受验体可以分类为不是高风险组。在风险判定步骤的第二实施方式中,通过将关于含有来自受验组织或受验体的靶cpg位点的dna(样品)的离子交换色谱解析(上述第8方法)中得到的峰的保留时间与关于含有未甲基化的该靶cpg位点的dna(阴性对照)或含有甲基化的该靶cpg位点的dna(阳性对照)的保留时间进行比较来进行该cpg位点的甲基化水平的确定或尿路上皮癌的风险判定。在上述第二实施方式中,关于因尿路上皮组织的癌化使甲基化水平亢进的cpg位点(例如,表1所示的tenm3的cpg位点),从样品检测出保留时间比阴性对照的峰短的峰时,判定为样品被甲基化,或者受验组织或受验体分类为高风险组。或者,从样品检测出与阳性对照同等的保留时间的峰时,判定为样品被甲基化,或者受验组织或受验体被分类为高风险组。另一方面,关于因尿路上皮组织的癌化使甲基化水平降低的cpg位点(例如,表1所示的hoxc4、tlr1、cpvl和prdm16的cpg位点),从样品检测出保留时间比阳性对照的峰长的峰时,判定为样品未被甲基化,或者受验组织或受验体被分类为高风险组。或者从样品检测出与阴性对照同等的保留时间的峰时,判定为样品未被甲基化,或者受验组织或受验体被分类为高风险组。如此,根据本发明,可以在产生异型增生等组织学上明显的前癌病变等之前通过简单的方法来判定尿路上皮癌的风险。另外,根据本发明,不需要进行组织学观察等需要技术的检査而能够判定受验体的尿路上皮癌的风险。如果能够通过本发明的方法在早期发现尿路上皮癌发生的高风险组患者,则能够进行预防干预而避免尿路上皮癌的发生,或者通过早期的治疗而改善它们的生命预后。或者,如果能够通过本发明的方法来筛选尿路上皮癌发生的风险不高的患者,则能够减少检诊受诊次数等而改善qol。因此,本发明还涉及对通过上述本发明的方法而分类为尿路上皮癌的高风险组的受验体进行预防干预。由此,能够进行该高风险组的受验体的尿路上皮癌的预防、早期诊断或早期治疗。进而,本发明提供一种尿路上皮癌的治疗方法,包括对通过上述本发明的方法而判定为尿路上皮癌的受验体进行治疗。作为治疗手段,可举出外科手术、利用药物或放射射线等的化学疗法等,但没有特别限定。进而,本发明提供用于判定尿路上皮组织的癌化风险或受验体的尿路上皮癌的风险的引物或探针。该引物或探针具有至少12个碱基的链长且与经亚硫酸氢盐处理后的选自5个基因(tenm3、hoxc4、tlr1、cpvl和prdm16)中的至少1个基因所含的至少1个cpg位点杂交。优选该引物或探针与该5个基因(tenm3、hoxc4、tlr1、cpvl和prdm16)的任一个中的至少1个cpg位点杂交。tenm3、hoxc4、tlr1、cpvl和prdm16的cpg位点的例子如上述表1所示。本发明的引物或探针的一个例子为与序列号1~5中的任一者所示的区域、优选序列号1~4中的任一者所示的区域中所含的至少1个cpg位点杂交的引物或探针。本发明的引物的其它例子为将序列号1~5中的任一者所示的区域、更优选序列号1~4中的任一者所示的区域扩增的引物。本发明的引物或探针的优选的一个例子是以与经亚硫酸氢盐处理的上述5个基因的dna的片段中的含有上述cpg位点的区域杂交且在其3’末端具有与甲基化胞嘧啶或非甲基化胞嘧啶互补的碱基的方式构建的引物或探针(例如上述的第1方法中可以使用的引物或探针)。本发明的引物或探针的其它优选的一个例子是从经亚硫酸氢盐处理的上述5个基因的dna的片段中的上述cpg位点的碱基附近可以1个碱基1个碱基地进行伸长反应的引物(测序引物)(例如上述的第3方法中可以使用的引物或探针)。其它优选的一个例子是与经亚硫酸氢盐处理的上述5个基因的dna的片段中的含有上述cpg位点的核苷酸杂交的探针(例如上述的第4方法中可以使用的引物或探针)。本发明的引物或探针的其它优选的一个例子是能够将经亚硫酸氢盐处理的上述5个基因的dna的片段中的含有甲基化或未被甲基化的上述cpg位点的区域进行特异性扩增的引物组(例如上述的第5方法或第8方法的pcr扩增中可以使用的引物组)。本发明的引物或探针的链长只要为至少12个碱基即可,但优选为至少15个碱基,更优选为至少20个碱基,进一步优选为15~40个碱基。另外,本发明的引物或探针可以被标记(例如荧光标记)。另外,本发明的引物或探针优选为上述第1~第8方法的任一方法中可以使用的引物或探针。另外,本发明的引物优选为pcr引物。作为本发明的引物或探针的更优选的例子,可举出由序列号6~15所示的核苷酸序列构成的多核苷酸和其互补链。作为进一步优选的例子,可举出由序列号6和7所示的多核苷酸或它们的互补链的组合、序列号8和9所示的多核苷酸或它们的互补链的组合、序列号10和11所示的多核苷酸或它们的互补链的组合、序列号12和13所示的多核苷酸或它们的互补链的组合或者序列号14和15所示的多核苷酸或它们的互补链的组合构成的引物组。进而,本发明提供用于尿路上皮组织的癌化风险或受验体的尿路上皮癌的风险判定的试剂盒,包括上述本发明的引物或探针。优选本发明的试剂盒用于通过上述第1~第8方法中的任一者来判定尿路上皮组织的癌化风险或受验体的尿路上皮癌的风险。本发明的试剂盒可以包含上述本发明的引物或探针以外的成分。作为这样的成分的例子,可举出亚硫酸氢盐处理所需的试剂(例如,亚硫酸氢钠溶液等)、pcr反应所需的试剂(例如,脱氧核糖核苷酸、耐热性dna聚合酶等)、infinium(注册商标)测定所需的试剂(例如,利用荧光物质标记了的核苷酸)、massarray(注册商标)所需的试剂(例如,用于进行碱基特异性的切割反应的rnase)、焦磷酸测序所需的试剂(例如,用于焦磷酸的检测的atp硫酸化酶、腺苷-5’-磷酰硫酸、荧光素酶、荧光素、用于将单链dna分离的链霉亲和素等)、ms-hrm法所需的试剂(例如,插入到dna双链间时发出荧光的嵌入剂等)、标记的检测所需的试剂(例如底物、酶)、阳性对照或阴性对照样品、试样(来自组织的基因组dna等)的稀释和清洗中使用的缓冲液等等。另外,试剂盒中可以包含其使用说明书。实施例以下,利用实施例对本发明详细地进行说明,但本发明并不限定于以下的实施例。〔患者和组织样品〕将由尿路上皮癌症例得到的非癌尿路上皮组织(n)(n=47)和尿路上皮癌组织(t)(n=46)以及由非尿路上皮癌症例得到的正常尿路上皮组织(c)(n=26)用作样品。组织样品通过国立癌症研究中心医院从接受外科手术的患者得到。从全部患者得到书面的知情同意。另外,本实施例的全部研究是受到国立癌症研究中心的伦理委员会的批准而实施的。采取的组织被冷冻保存。将得到的新鲜冷冻组织样品利用苯酚-氯仿进行处理,接着实施透析,由此提取基因组dna。将提取的dna500ng使用ezdna甲基化-gold(tm)试剂盒(zymoresearch公司制)进行亚硫酸氢盐处理。〔实施例1癌化组织中的cpg位点的甲基化的检测〕(infinium(注册商标)测定)使用infinium(注册商标)humanmethylation450kbeadchip(illumina公司制)以1个cpg位点的分辨率对485764的cpg部位的dna甲基化状态进行解析。一般认为infinium(注册商标)humanmethylation450kbeadchip(illumina公司制)覆盖refseq基因的99%、cpg岛的96%。更详细而言,出于对dna甲基化状态全面地进行解析的目的,在解析对象中包含启动子区域、5’非翻译区域、第1外显子、基因内、3’非翻译区域,一般认为包罗了99%的参照序列基因。使用infinium(注册商标)测定试剂盒(illumina公司制)对经亚硫酸氢盐处理的dna进行全基因组扩增处理(参照bibikova,m.等、epigenomics、2009年、1卷、177~200页)。使经扩增的dna片段与上述芯片上的探针杂交,接着通过单碱基伸长反应对经杂交的dna掺入经荧光标记的碱基。由此,将与含有甲基化cpg的dna片段杂交的甲基化检测用探针和与含有非甲基化cpg的dna片段杂交的非甲基化检测用探针分别进行荧光标记。接着,依照制造公司的说明书,使用iscanreader(illumina公司制)测定荧光信号。得到的数据使用genomestudiomethylationsoftware(illumina公司制)进行解析。(dna甲基化水平的计算)在各cpg位点中,计算来自甲基化检测用探针的信号相对于来自甲基化检测用探针和非甲基化检测用探针的信号的合计的相对比。即,来自各cpg位点的甲基化水平表示为所谓β值(范围:0.00~1.00)。(统计解析)对得到的甲基化水平的数据进行welcht检验,与(c)样品相比,在(n)样品中鉴定出了显示显著的甲基化异常的cpg位点。接着,通过jonckheere-terpstra倾向性检验,鉴定了dna甲基化水平按照(c)、(n)、(t)阶段性地变化的cpg位点。其结果,两个检验均发现2750个显著的cpg位点。这些位点中的dna甲基化异常与正常组织(c)相比,在尿路上皮癌患者的非癌组织(n)中显著多地产生,在癌组织(t)中频率进一步增加,因此,认为参与尿路上皮组织的癌化。(主成分分析)对上述2750个的cpg位点的dna甲基化水平(β值)进行主成分分析。其结果,(c)、(n)、(t)显示明显不同的分布(图1),因此,推测(n)是已经伴有dna甲基化异常的前癌阶段。(roc解析)为了研究是否可以以dna甲基化异常为指标将(n)从(c)区分开,对上述2750个cpg位点进行roc解析。对各位点的甲基化水平制作基于灵敏度和特异度的roc曲线,将灵敏度和特异度的和达到最大时(与roc曲线的图表上的左上角最接近时)的甲基化水平设定为临时诊断阈值(截止值)。即,关于与(c)相比在(n)中dna甲基化亢进的cpg位点,样品的dna甲基化水平大于截止值时,将该样品视作满足诊断阈值(癌化风险高)。相反,关于与(c)相比在(n)中dna甲基化降低的cpg位点,样品的dna甲基化水平小于截止值时,将该样品视作满足诊断阈值(癌化风险高)。进而,对各位点测定roc曲线的曲线下面积(auc)。图2表示横轴取满足诊断阈值的cpg位点数、纵轴取样品数的直方图。确认了直方图显示将(c)和(n)明确分开的双峰性,且显示(c)和(n)明显不同的甲基化谱。因此,认为可以以这些cpg位点的dna甲基化水平为基准将患有尿路上皮癌或患病的可能性高的样品与尿路上皮癌的患病的可能性低的样品进行区别,从而能够进行尿路上皮癌的风险判定。〔实施例2尿路上皮癌标记物的评价〕选择含有实施例1中制作的roc曲线的auc为0.95以上的cpg位点的5个基因(tenm3、hoxc4、tlr1、cpvl和prdm16),利用massarray(注册商标)或焦磷酸测序确认这些基因的cpg位点中的dna甲基化水平。(massarray(注册商标)法)massarray(注册商标)法是将亚硫酸氢盐处理后的dna进行扩增并转录为rna,进一步利用rnaase进行碱基特异性切割后,利用质谱分析仪检测甲基化dna片段与非甲基化dna片段的分子量之差的方法。使用epidesigner(sequenom公司制,massarray用引物设计软件)对tenm3基因的cpg位点进行massarray的引物设计。对设计的每1个引物组平均试验dna聚合酶3种与退火温度4个阶段左右的条件的组合,确定定量性良好的最佳pcr条件。确认了作为解析对象的全部cpg位点在所采用的pcr条件下定量性良好。应予说明,massarray中的pcr靶序列为100~500bp左右,稍长,因此,能够一并评价靶cpg位点周边的多个cpg位点的dna甲基化水平。将本解析中使用的引物的序列和pcr条件示于表3,将靶序列示于表4。[表3][表4]将经亚硫酸氢盐处理的dna通过pcr进行扩增,接着,进行体外转录反应。将得到的rna利用rnaase在尿嘧啶的部位进行特异性切割,生成与各样品的基因组dna的甲基化的有无对应的长度不同的片段。将得到的rna片段施加于能够检测一个碱基的质量差异的maldi-tofmas(sequenom公司制,massarray(注册商标)analyzer4)进行质谱分析。将得到的质谱分析结果使用解析软件(epityper、sequenom公司制)与参照序列进行比对,由来自甲基化dna的rna片段与来自非甲基化dna的rna片段的质量的比算出甲基化水平。(焦磷酸测序)焦磷酸测序以表5所示的条件进行。另外,将靶序列示于表6。[表5][表6]靶基因名_靶序列序列号hoxc45’-tcgtgtaccgcat-3’2tlr15’-tccagtcaaaaccggat-3’3cpvl5’-gcagcccagccaacccgac-3’4prdm165’-cgtgagg-3’5(结果)其结果,对于5个基因中的任一者,均在利用massarray(注册商标)或焦磷酸测序得到的解析结果与通过infinium(注册商标)测定得到的解析结果之间发现强相关性(图3)。因此,表示这5个基因的cpg位点可以作为用于尿路上皮癌的风险判定的标记物使用。使用massarray(注册商标)或焦磷酸测序中测定的dna甲基化水平对5个基因的cpg位点再次进行roc解析。由于一部分cpg位点彼此接近,因此,可以统一作为1个cpg单元进行解析。将结果示于表7。[表7]表7所示的cpg位点或单元的roc曲线的auc均高,表示即使单独也能够以高灵敏度和特异度进行尿路上皮癌风险判定。进而,通过将这些cpg位点或单元组合,可期待能够进一步提高灵敏度和特异度以及再现性。表8示出表7所示的cpg位点或单元中的2个的组合的例子。基于这些组合的风险判定的灵敏度和特异度均为96%以上。[表8]序列表<110>学校法人庆应义塾<120>尿路上皮癌的风险的判定方法<130>dc0117<150>jp2018-051464<151>2018-03-19<160>15<170>patentinversion3.5<210>1<211>314<212>dna<213>智人<220><223>tenm3<400>1gatcgaacaacaaagacagaaaagatctatgacgaccaccgtaaatttctactgaggatc60gcctacgacacgtctgggcacccgactctctggctgccaagcagcaagctgatggccgtc120aatgtcacctattcatccacaggtcaaattgccagcatccagcgaggcaccactagcgag180aaagtagattatgacggacaggggaggatcgtgtctcgggtctttgctgatggtaaaaca240tggagttacacatatttagaaaaggtatgcctgcaaactaagctcaacaatagggaaagg300ataattcacatttt314<210>2<211>13<212>dna<213>智人<220><223>hoxc4<400>2tcgtgtaccgcat13<210>3<211>17<212>dna<213>智人<220><223>tlr1<400>3tccagtcaaaaccggat17<210>4<211>19<212>dna<213>智人<220><223>cpvl<400>4gcagcccagccaacccgac19<210>5<211>7<212>dna<213>智人<220><223>prdm16<400>5cgtgagg7<210>6<211>25<212>dna<213>人工的<220><223>tenm3的引物<400>6ttttagtgttttggatgattgttga25<210>7<211>26<212>dna<213>人工的<220><223>tenm3的引物<400>7acaaaaacctcctttcaattaacttt26<210>8<211>24<212>dna<213>人工的<220><223>hoxc4的引物<400>8tggtagaggggtataggggaattt24<210>9<211>25<212>dna<213>人工的<220><223>hoxc4的引物<400>9caaactacaaaatttcctccattca25<210>10<211>24<212>dna<213>人工的<220><223>tlr1的引物<400>10gggtttataaaaattttggggttt24<210>11<211>24<212>dna<213>人工的<220><223>tlr1的引物<400>11aaaacaattttatcatccccacat24<210>12<211>24<212>dna<213>人工的<220><223>cpvl的引物<400>12tgtaggagtgagtttagggaaatt24<210>13<211>23<212>dna<213>人工的<220><223>cpvl的引物<400>13aatcctcacaacaacccaataaa23<210>14<211>25<212>dna<213>art<213>人工的<220><223>prdm16的引物<400>14gtgtttagggaaaagtttattggaa25<210>15<211>21<212>dna<213>人工的<220><223>prdm16的引物<400>15attttcctacccccaacatct21当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1