用于治疗IVA型粘多糖的腺相关病毒载体
用于治疗iv a型粘多糖的腺相关病毒载体
技术领域
1.本发明涉及可用于表达目的蛋白质及其在基因治疗中的用途的多核苷酸序列和载体。本发明还涉及有助于治疗粘多糖贮积酶(mps)、特别是用于治疗iva型粘多糖贮积症或morquio a综合征的载体和核酸序列。
背景技术:
2.溶酶体是一种在动物细胞的细胞质中发现的细胞器,其中含有50多种水解酶,这些水解酶会在回收破旧的细胞组分过程中或吞噬病毒和细菌后分解生物分子。该细胞器包含几种类型的水解酶,包括蛋白酶、核酸酶、糖苷酶、脂肪酶、磷脂酶、磷酸酶和硫酸酯酶。所有的酶都是酸性水解酶。
3.溶酶体贮积病(lsd)是由影响一种或多种溶酶体酶的遗传缺陷引起的。这些遗传疾病通常是由溶酶体中存在的特定酶活性不足引起的。在较小程度上,这些疾病可能是由于参与溶酶体生物发生的蛋白质缺乏所致。
4.lsds个别罕见,尽管作为一个整体,这些疾病在普通人群中相对普遍。lsd的综合患病率约为每5,000例活产1例。但是,普通人群中的某些群体尤其容易遭受lsd的困扰。例如,犹太中欧和东欧(ashkenazi)个体的后代中的高雪氏病和泰萨克斯氏病的患病率分别为每600例出生1例和每3,900例出生1例。
5.粘多糖酶(mps)是一组七个lsd疾病,其特征是缺乏或缺乏参与糖胺聚糖(gags)代谢的特定溶酶体酶。除具有x染色体连锁遗传的mpsii(亨特病)外,所有mps都具有常染色体隐性遗传模式。
6.在这七个mps中,iv型粘多糖贮积病(mpsiv或morquio综合征)有两个亚型,a和b。morquioa和b都是常染色体隐性遗传,对男性和女性的影响均相同。morquio a或mpsiva是一种罕见病,现有的流行率数据稀缺且易变。报告的估计值范围从北爱尔兰的每76,320个到西澳大利亚的每641,178个。mpsiva是由参与gag硫酸角质素(ks)和6
‑
硫酸软骨素(c6s)降解的一种酶的缺乏引起的。已经鉴定出编码该酶的基因,并且已经报道了各种突变。
7.mpsiva是由于半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的活性不足引起的(galns,ec 3.1.6.4)。galns是一种溶酶体酶,它在硫酸软骨素
‑
6(c6s)的非还原端水解n
‑
乙酰半乳糖胺
‑6‑
硫酸盐的硫酸酯基,在硫酸角质素(ks)的非还原端水解6
‑
硫酸半乳糖的硫酸酯基。由于未降解的c6s和ks持续积累,结果发生了进行性细胞损伤,从而导致了多系统疾病。目前,已在人galns基因中鉴定出约180种不同的突变,导致galns酶活性的不足。
8.ks和c6s的大部分是软骨细胞产生的,因此,未降解的底物主要在软骨细胞和细胞外基质中积累。这直接影响软骨和骨骼发育,导致系统性骨骼发育异常。在患有morquio a的患者中,软骨细胞被空泡化,这导致异常的软骨形成和/或软骨内骨化。大多数mpsiva患者出生时看起来很健康,并且症状逐渐发展。最初的症状可在1
‑
3岁之间发现,诊断时的平均年龄在4.7岁左右。主要的骨骼特征包括:击打躯干侏儒症、齿状突发育不全、肉眼食管、后凸畸形、脊柱侧弯、膝外翻、髋关节外翻、下肋骨张开、关节活动过度和步态不稳而倾向于
掉落。其他潜在的并发症包括肺功能不全、瓣膜性心脏病、听力损失、肝肿大、角膜混浊、面部特征粗大、牙齿间距大、牙釉质异常稀薄和龋齿频繁。mpsiva患者可以保留智力。患者之间疾病进展的速度和表型特征是可变的。在整个年龄段中,如果最终身高低于120cm,则将mpsiva表型定义为严重;如果最终身高在120cm以上和140cm以下,则将mpsiva表型定义为中度;如果最终身高在140cm以上,则定义为mpsiva表型。报告的预期寿命从第二个十年到70岁不等。这种可变性可能与多种因素有关,例如突变的性质、种族或患者所接受的医疗保健方面的差异。
9.直到最近,还没有针对mpsiva综合征的疾病特定的批准疗法。可用的治疗方法是对症治疗,其方法是使用多种非特异性药物来预防和控制疾病并发症。然而,最近几年,mpsiva患者有两种主要的治疗选择:酶替代疗法(ert)和造血干细胞移植(hsct)。基于正常细胞分泌大量甘露糖
‑6‑
磷酸(m6p)标记的可溶性溶酶体酶(例如galns)的事实,这两种治疗策略的设计都依赖于交叉校正的可能性,其随后可以被其他细胞通过质膜上的m6p受体从细胞外区吸收,并靶向溶酶体。另外,存在残余酶活性的阈值,通常非常低,在该阈值之上,该细胞能够应付底物涌入并且该疾病不影响受试者,这表明恢复正常活性不是改变临床过程的必要条件。
10.对于mpsiva,已经在两种不同的小鼠小鼠疾病模型中测试了ert(tomatsu等人,2008,2010a,2015)。在这项研究中,每周向0.5和12周龄的mpsiva小鼠静脉内或腹膜内给予250u/g重组鼠galns(rgalns)剂量。在最后一次给药后一周,mpsiva小鼠显示出内脏器官、骨髓、心脏瓣膜、韧带和结缔组织的窦壁内衬细胞的gag贮藏量显着减少,并且血液ks水平显着降低,表明通过输注rgalns可以进行体细胞校正。
11.2014年,商品名为elosulfase alfa的重组人galns,(biomarin制药公司)被美国食品药品管理局(fda)和欧洲药品管理局(ema)批准用于mpsiva的治疗。每周通过静脉输注以2mg/kg的剂量进行治疗,平均输注时间为3.5
‑
4.5小时。入组患者的年龄为5至57岁。在基线时,所有入组患者在6分钟步行测试(6mwt)中可行走30至325m(sanford and lo,2014)。主要终点被确定为治疗开始后第24周在6mwt中行走距离相对于基线的变化。次要终点包括第3周的3分钟爬楼梯速率(3msct)和第24周的尿ks水平相对于基线的变化。将患者分为两个治疗组:每周接受2mg/kg剂量的的患者,每两周一次接受2mg/kg的患者。每周接受2mg/kg的患者,与开始治疗后24周的安慰剂组相比,在6mwt中行走的距离增加到22.5m。但是,接受的患者的爬楼梯率没有差异。而且,相对于治疗的最初24周,没有观察到步行能力的进一步改善。另一方面,与安慰剂组相比,每两周一次接受2mg/kg的患者在6mwt和3msct方面没有差异。在所有治疗组中,尿中ks水平相对于基线的降低(一种药效学作用)降低的幅度更大(2014年)。最初纳入安慰剂对照试验的患者随后才有资格在开放标签延伸试验(mor
‑
005)中开始使用治疗。
12.由于可能对过敏,因此在产品管理过程中会提供医疗支持。在试验期间,所描述的最严重的不良事件是过敏反应和超敏反应,可以在输注期间的任何时间出现,也可以在给药后3小时内出现。患有急性呼吸系统疾病的患者的风险可能更高,需要进一步监测。这些过敏反应可能会危及患者的生命,包括咳嗽、皮疹、喉咙紧绷、
荨麻疹、潮红、肤色改变、血压低、呼吸急促、胸痛以及胃肠道症状、例如恶心、腹痛、呕吐(http://vimizim.com)。ert的其他缺点包括:1)小儿患者难以进行3.5
‑
4.5小时的静脉内输注,2)每周接受一次2mg/kg治疗的患者中有100%在4周后产生抗药物抗体,3)所有接受测试的患者均研发出中和抗体,该中和抗体能够在试验期间至少一次抑制药物与6
‑
磷酸甘露糖受体的结合,并且4)治疗费用高昂,其中还包括家庭护理费用(2014)。
13.使用骨髓干细胞(骨髓移植,bmt)的造血干细胞移植(hsct)已被证明可有效治疗其他mps患者的躯体和神经病理学。hsct校正表型的主要缺点是治疗对mpsiva患者生长的影响极小(chinen et al.,2014;wang et al.,2016;yabe et al.,2016)。
14.考虑到当前mpsiva治疗方案的局限性,需要其他方法。
15.体内基因治疗为mpsiva和其他遗传性疾病提供一次性治疗的可能性,并具有终身有益的前景。
16.morquio a疾病的基因治疗临床前研究主要基于给予γ
‑
逆转录病毒、慢病毒和腺相关的载体。
17.γ
‑
逆转录病毒衍生的编码人galns基因的载体对mpsiva人淋巴母细胞b细胞、人角质形成细胞、鼠成肌细胞和兔滑膜细胞的体外转导导致galns酶活性增加,导致细胞内gag储存减少(toietta et al。,2001)。
18.对morquio a皮肤成纤维细胞施用编码人galns cdna的慢病毒衍生载体,其酶活性水平比未转导的mpsiva成纤维细胞高7.5倍,但低于人类健康成纤维细胞。慢病毒载体的使用还导致β
‑
己糖胺酶和β
‑
半乳糖苷酶活性的正常化,据报道这是morquio a的次生生物标志物(almeciga等,2013;salazar等,2016)。
19.尤其是腺相关病毒(aav)载体介导的基因转移,由于其高转导效率和缺乏致病性,正在迅速成为许多体内基因治疗应用的选择方法。aav载体可以转导有丝分裂后的细胞,一些临床前和临床研究表明,aav载体介导的基因转移具有潜力,可以有效地驱动治疗性转基因在多种疾病中的持续表达。
20.使用aav载体可以评估galns和硫酸酯酶修饰因子1(sumf1)共表达对酶活性的影响。这种共表达使细胞培养物中的酶活性增加了多达4倍(alm
é
ciga
‑
d
í
az等,2010)。在体内,在morquio a小鼠模型中施用aav
‑
galns载体显示,在单次静脉内给药后12周,血浆中的酶活性恢复到野生型水平的8.5%,而与aav
‑
sumf1载体共同给药导致galns活性提高到野生型水平的19%。在心脏和骨骼中,galns酶的活性也分别增加至野生型的30%和33%(alm
é
ciga javier, adriana,shunji tomatsu,2012年)。
21.为了改善galns酶的骨递送,开发了在病毒衣壳内携带短酸性氨基酸肽以赋予病毒对骨羟基磷灰石亲和力的修饰的aav载体。这种修饰的galns编码aav载体大大提高了mpsiva小鼠模型骨骼中的载体基因组拷贝和转基因表达,并导致galns活性水平达到了野生型的42%(alm
é
ciga javier, adriana,shunji tomatsu,2012;tomatsu et al.,2010b)。
22.上述方法均无法完全恢复半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的活性,不能完全消除胞浆内的内含物,也不能纠正mpsiva的所有临床症状。因此,需要具有更好的功效和安全性的新颖的mpsiva治疗方法。
23.发明概述
24.本发明提供用于治疗粘多糖酶、特别是iva型粘多糖酶或morquio a综合征的新的多核苷酸序列和载体。
25.在第一方面,本发明提供一种新的分离的多核苷酸序列,其与seq id no:1所示的核苷酸序列具有75%至90%的同一性,其中所述序列编码功能性人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶。
26.在另一方面,本发明涉及包含本发明的多核苷酸序列的表达载体。
27.本发明的另一方面涉及药物组合物,包含治疗有效量的本发明的多核苷酸序列或载体。
28.本发明的另一方面还涉及用作药物、特别是用于治疗iva型粘多糖贮积症或morquio a综合征的本文所述的多核苷酸序列或载体或药物组合物。
29.本发明还提供一种制备根据本发明的腺相关病毒载体的方法。
30.附图简述
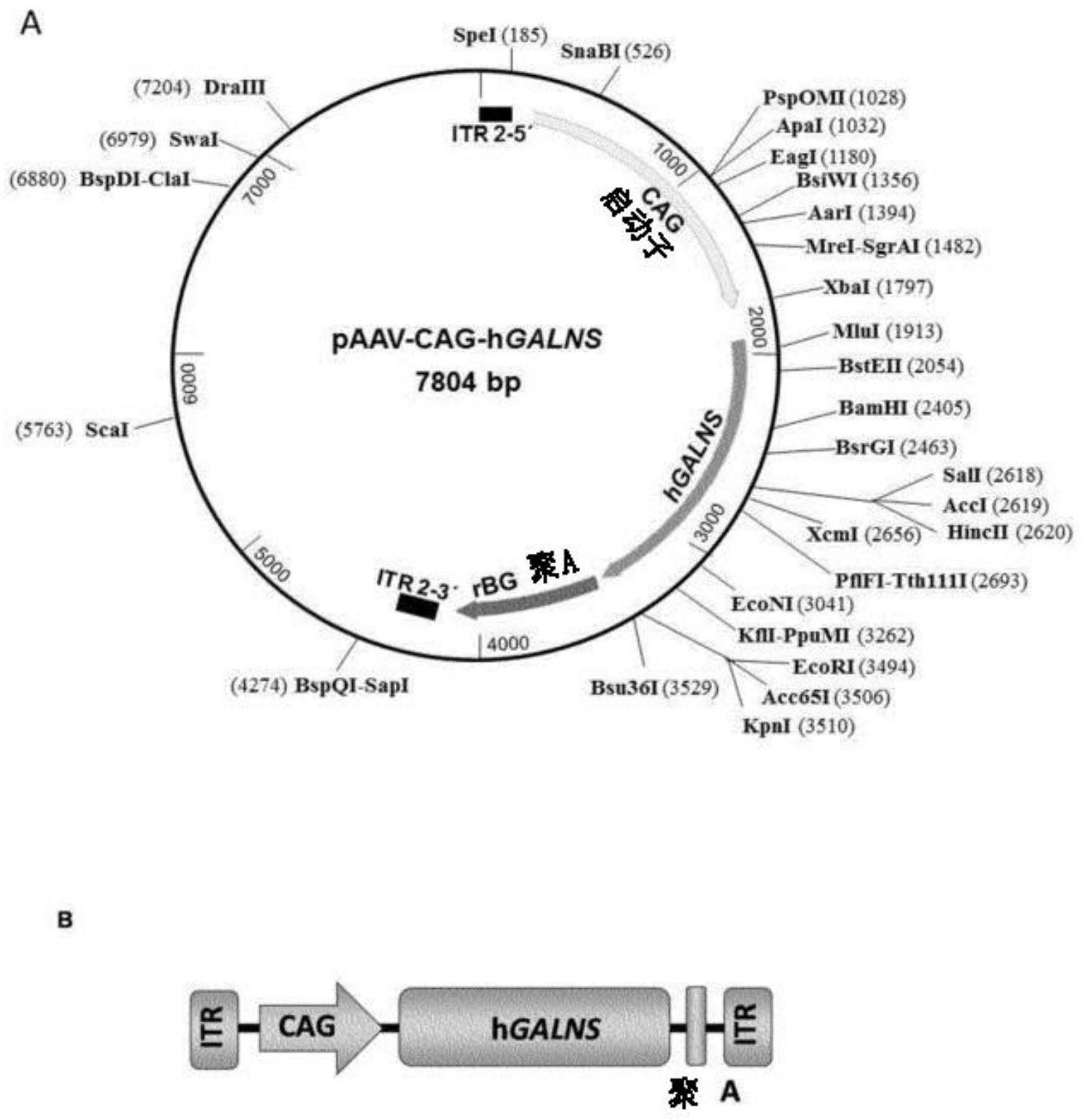
31.图1.产生paav
‑
cag
‑
hgalns和aav9
‑
cag
‑
hgalns。(a)质粒paav
‑
cag
‑
hgalns及其组分的示意图。(b)含有hgalns编码序列的腺相关载体的基因组示意图。
32.图2.paav
‑
cag
‑
ohgalns
‑
v1和aav9
‑
cag
‑
ohgalns
‑
v1的生成。(a)质粒paav
‑
cag
‑
ohgalns
‑
v1及其组分的示意图。(b)含有ohgalns
‑
v1编码序列的腺相关载体的基因组示意图。
33.图3.paav
‑
cag
‑
ohgalns
‑
v2和aav9
‑
cag
‑
ohgalns
‑
v2的生成。(a)质粒paav
‑
cag
‑
ohgalns
‑
v2及其组分的示意图。(b)含有ohgalns
‑
v2编码序列的腺相关载体的基因组示意图。
34.图4.paav
‑
cag
‑
ohgalns
‑
v3和aav9
‑
cag
‑
ohgalns
‑
v3的生成。(a)质粒paav
‑
cag
‑
ohgalns
‑
v3及其组分的示意图。(b)包含ohgalns
‑
v3编码序列的腺相关载体的基因组示意图。
35.图5.paav
‑
cag
‑
omgalns、aav9
‑
cag
‑
omgalns和aav8
‑
cag
‑
omgalns的生成。(a)质粒paav
‑
cag
‑
omgalns及其组分的示意图。(b)含有omgalns编码序列的腺相关载体的基因组示意图。
36.图6.paav
‑
haat
‑
omgalns和aav8
‑
haat
‑
omgalns的生成。(a)质粒paav
‑
haat
‑
omgalns及其组分的示意图。(b)含有omgalns编码序列的腺相关载体的基因组示意图。
37.图7.将编码不同人类galns版本(aav9
‑
cag
‑
hgalns、aav9
‑
cag
‑
ohgalns
‑
v1、aav9
‑
cag
‑
ohgalns
‑
v2和aav9
‑
cag
‑
ohgalns
‑
v3)的aav9载体静脉内递送至雄性小鼠。在2个月大时,野生型(健康)小鼠(wt)、未经处理的galns
‑
/
‑
小鼠和galns
‑
/
‑
小鼠的(a)肝和(b)血清中通过静脉内(iv)注射与每种载体5*10
10
vg全身给药。wt galns活性设置为100%。值是每组4
‑
5只小鼠的平均值
±
sem。
38.图8.将编码优化的鼠galns(aav9
‑
cag
‑
omgalns)的aav9载体静脉内递送至雄性小鼠。在1个月大时,(a)肝、(b)股骨、(c)野生型(健康)小鼠(wt)、未经治疗的galns
‑
/
‑
小鼠和galns
‑
/
‑
小鼠的的脂肪组织中的galns活性通过静脉内(iv)全身注射1x10
12 vg aav9
‑
cagomgalns。(d)在同一群动物中在不同注射后点的血清中galns活性。wt galns活性设置为100%。值是每组4
‑
5只小鼠的平均值
±
sem。*p<0.05,****p<0.0001,对照组为未经处理的galns//小鼠。
39.图9.将编码优化的鼠galns(aav8
‑
cag
‑
omgalns)的aav8载体静脉内递送至雄性小鼠。(a)肝、(b)股骨、(c)野生型(健康)小鼠(wt)、未经治疗的galns
‑
/
‑
小鼠和galns
‑
/
‑
小鼠的脂肪组织中的galns活性在1个月大时通过静脉内(iv)全身注射1x10
12 vg aav8
‑
cagomgalns。(d)在同一群动物中在不同注射后点的血清中galns活性。wt galns活性设置为100%。值是每组4
‑
5只小鼠的平均值
±
sem。*p<0.05,****p<0.0001,相对于未经处理的galns
‑
/
‑
小鼠。
40.图10.将编码优化的鼠galns(aav8
‑
haat
‑
omgalns)的aav8载体静脉内递送至雄性小鼠。(a)肝、(b)股骨、(c)野生型(健康)小鼠(wt)、未经治疗的galns
‑
/
‑
小鼠和galns
‑
/
‑
小鼠的脂肪组织中的galns活性在1个月大时通过静脉内(iv)全身注射1x10
11 vg aav8
‑
haat
‑
omgalns。(d)在同一群动物中在不同注射后点的血清中galns活性。wt galns活性设置为100%。值是每组4
‑
5只小鼠的平均值
±
sem。*p<0.05,****p<0.0001,相对于未经处理的galns
‑
/
‑
小鼠。
41.图11.将编码优化的鼠galns(aav9
‑
cag
‑
omgalns,aav8
‑
cag
‑
omgalns和aav8
‑
haatomgalns)的aav9和aav8载体静脉内递送至雄性小鼠。通过lc
‑
ms/ms分析定量(a)肝脏和(b)血清中的硫酸角质素(ks)。****p<0.0001,与未治疗的galns
‑
/
‑
雄性小鼠相比。
42.图12.将编码优化的鼠galns(aav9
‑
cag
‑
omgalns,aav8
‑
cag
‑
omgalns和aav8
‑
haatomgalns)的aav9和aav8载体静脉内递送至雄性小鼠。胫骨epiphyseal生长板组织切片的甲苯胺蓝染色。原始放大倍率100倍。
43.图13.将编码优化的鼠galns(aav9
‑
cag
‑
omgalns,aav8
‑
cag
‑
omgalns和aav8
‑
haatomgalns)的aav9和aav8载体静脉内递送至雄性galns
‑
/
‑
小鼠。(a)对mowry糖胺聚糖染色后在角膜上皮中获得的染色强度进行定量。(b)野生型(健康)小鼠(wt)、未经处理的galns
‑
/
‑
小鼠和galns
‑
/
‑
小鼠的甲苯胺蓝染色切片的泪腺组织病理学通过静脉内(iv)全身注射。原始放大倍率40倍。***p<0.001,****p<0.0001,相对于未处理的galns
‑
/
‑
雄性小鼠。
44.图14.将编码优化的小鼠galns(aav9
‑
cag
‑
omgalns)的aav9载体静脉内递送至雄性小鼠。通过透射电子显微镜分析从6个月大的健康wt和galns
‑
/
‑
雄性小鼠中收获的齿状回和杏仁状体的超微结构,全身施用1x10
12 vg编码最优化小鼠galns的载体(aav9
‑
cag
‑
omgalns)。箭头指示血管周巨噬细胞(齿状回)、神经周围神经胶质细胞和内皮细胞(杏仁核)中溶酶体增大。
45.发明详述
46.微生物沉积
47.质粒paav
‑
cag
‑
hgalns(seq id no:2)、paav
‑
cag
‑
ohgalns
‑
v1(seq id no:4)、paav
‑
cag
‑
ohgalns
‑
v2(seq id no:6)和paav
‑
cag
‑
ohgalns
‑
v3(seq id no:8)分别于2018年4月19日在dsmz上保藏,登录号为dsm 32791、dsm 32792、dsm 32793和dsm 32794,分别在dsmz
‑
德意志联邦共和国inhoffenstraβe7 b,d
‑
38124不伦瑞克的德意志大学(deutsche sammlung von mikroorganismen und zellkulturen)。
48.定义
49.术语“核苷酸序列”或“分离的核苷酸序列”或“多核苷酸序列”或“多核苷酸”或“分离的多核苷酸序列”在本文可互换使用,并且是指分别含有脱氧核糖核苷酸或核糖核苷酸
的核酸分子,dna或rna。核酸可以是双链的、单链的、或包含双链或单链序列的部分。
50.术语“%序列同一性”、“%同一性”或“%序列同源性”是指在比对序列以获得最大%序列同一性之后,候选序列中与参考序列中的核苷酸或氨基酸相同的核苷酸或氨基酸的百分比。在一个优选的实施方案中,基于两个给定的seq id no的全长或其部分,计算序列同一性。%序列同一性可以通过本领域中建立的任何方法或算法来确定,例如align、blast和blast 2.0算法。参见altschul s,et al.,nuc acids res.1977;25:3389
‑
3402 and altschul s,et al.,j mol biol.1990;215:403
‑
410。
51.在此,将比对序列和候选序列比对后,将相同的核苷酸或氨基酸数除以参考序列中的核苷酸或氨基酸总数,并将结果乘以100,即可计算出“%序列同一性”、“%同一性”或“%序列同源性”。
52.任选地,在确定氨基酸相似性的程度时,技术人员也可以考虑对技术人员显而易见的所谓的“保守”氨基酸取代。保守氨基酸取代是基于具有相似侧链的残基的互换性。例如,具有脂族侧链的氨基酸组包括甘氨酸、丙氨酸、缬氨酸、亮氨酸和异亮氨酸。具有脂族
‑
羟基侧链的氨基酸基团包括丝氨酸和苏氨酸。具有含酰胺侧链的氨基酸组包括天冬酰胺和谷氨酰胺。具有芳族侧链的氨基酸基团包括苯丙氨酸、酪氨酸和色氨酸。具有碱性侧链的氨基酸组包括赖氨酸、精氨酸和组氨酸。具有含硫侧链的氨基酸组包括半胱氨酸和蛋氨酸。本文公开的氨基酸序列的取代变体是其中公开的序列中的至少一个残基已被去除并且在其位置插入了不同残基的那些。优选地,氨基酸变化是保守的。对于每个天然存在的氨基酸优选的保守取代如下:丙氨酸到丝氨酸;精氨酸到赖氨酸;asn到谷氨酰胺或组氨酸;天冬酰胺到谷氨酸;半胱氨酸到丝氨酸或丙氨酸;谷氨酰胺到asn;谷氨酸到天冬酰胺;甘氨酸到脯氨酸;组氨酸到asn或谷氨酰胺;异亮氨酸到亮氨酸或缬氨酸;亮氨酸到异亮氨酸或缬氨酸;赖氨酸到精氨酸;谷氨酰胺到谷氨酸;蛋氨酸到亮氨酸或异亮氨酸;苯丙氨酸到蛋氨酸、亮氨酸或酪氨酸;丝氨酸到苏氨酸;苏氨酸到丝氨酸;色氨酸到酪氨酸;酪氨酸到色氨酸或苯丙氨酸;以及缬氨酸到异亮氨酸或亮氨酸。
53.术语“编码”是指确定核苷酸序列如何翻译成多肽或蛋白质的遗传密码。序列中核苷酸的顺序决定了沿着多肽或蛋白质的氨基酸顺序。
54.术语“蛋白质”是指由一条或多条氨基酸或多肽的线性链组成的大分子。蛋白质可能遭受翻译后修饰,例如半胱氨酸残基向3
‑
氧代丙氨酸的转化、糖基化或金属结合。蛋白质的糖基化是添加与氨基酸链共价连接的不同碳水化合物。
55.如本文所用,术语“转录调节区”是指能够调节一个或多个基因表达的核酸片段。本发明的多核苷酸的调节区可包括启动子,加上响应元件,用于结合转录因子以帮助rna聚合酶结合并促进表达的激活子和增强子序列,以及操纵基因或沉默子序列,阻遏蛋白与之结合,以阻断rna聚合酶的附着并阻止其表达。
56.术语“启动子”必须被理解为具有用于控制一个或多个多核苷酸例如编码序列的转录的功能的核酸片段,其位于多核苷酸序列的5'上游,并且通过dna依赖性rna聚合酶的结合位点、转录起始位点以及但不限于转录因子,阻遏物和本领域已知的任何其他核苷酸序列的结合位点,可直接或间接作用以调节启动子的转录量。
57.当其可以使用合适的测定法,例如rt
‑
qpcr或northern印迹(检测转录本),使用包含与所述目的核苷酸序列可操作地连接的所述启动子的基因构建体,在表达系统中启动所
述核苷酸序列的转录时,启动子被认为是有活性的,或者说是驱动与其有效连接的核苷酸序列表达的启动子。所述启动子的活性也可以在蛋白质水平上使用编码蛋白的合适测定法如蛋白质印迹或elisa来评估。如果可以检测到转录物,或者发现转录物或蛋白质水平的增加与使用构建体的转录相比至少增加5%、10%、15%、20%、30%、40%、50%、60%、70%、80%、90%、100%、200%、300%、500%、1000%、1500%或2000%,则认为该启动子能够启动转录,与使用构建体的转录相比,其区别仅在于其不含所述启动子。
58.术语“组成型”启动子是指在大多数生理和发育条件下具有活性的启动子。“诱导型”启动子是优选根据生理或发育条件调节的启动子。诱导型启动子在药物递送或曝光后可能是有活性的。因此,“组成型”启动子在“诱导型”启动子的意义上不受调控。“组织特异性”启动子优选在特定类型的细胞/组织中具有活性。普遍存在的启动子可以定义为在许多或任何不同组织中有活性的启动子。通常,在此上下文中,“许多”是指大于5或至少6、10、15、20或5、6、7、8、9、10、11、12、13、14、15、16、17、18、19、20种不同的组织。
59.术语“cag”启动子是指包含鸡β
‑
肌动蛋白启动子和巨细胞病毒增强子的启动子(alexopoulou a.等人,bmc cell biology 2008;9(2):1
‑
11)。更精确地,所述cag启动子包含(i)巨细胞病毒(cmv)早期增强子元件,(ii)鸡β
‑
肌动蛋白启动子,(iii)鸡β
‑
肌动蛋白基因的第一内含子,和(iv)内含子2/兔β
‑
珠蛋白基因的第3外显子。
60.术语“haat”启动子是指包含人α1
‑
抗胰蛋白酶启动子和载脂蛋白e的三个拷贝的肝细胞控制区(hcr)增强子的杂合启动子。
61.术语“可操作地连接”是指启动子序列相对于目的基因的功能关系和位置(例如,如果启动子或增强子影响编码序列,则其可操作地连接至编码序列)。通常,可操作地连接的启动子与目的序列相邻。然而,增强子不必与目的序列邻接以控制其表达。
62.如本文所用,术语“转录后调控区”是指促进表达、稳定或定位在盒或所得基因产物中的序列的任何多核苷酸。
63.如本文所用,术语“载体”是指能够将一种或多种目的多核苷酸递送和任选表达到宿主细胞中的构建体。载体的实例包括但不限于病毒载体、裸露的dna或rna表达载体、质粒、粘粒或噬菌体载体、与阳离子缩合剂相关的dna或rna表达载体、封装在脂质体中的dna或rna表达载体,以及某些真核细胞,如生产细胞。载体可以是稳定的并且可以自我复制。对于可以使用的载体类型没有限制。载体可以是适合于繁殖并获得掺入几种异源生物的多核苷酸、基因构建体或表达载体的克隆载体。
64.在一个特定的实施方案中,所述载体是表达载体。如本文所用,术语“表达载体”是指设计用于细胞中基因表达的载体,即,该载体用于将特定基因导入靶细胞以产生由该基因编码的蛋白质。
65.根据本发明的载体可以包含调节序列,其充当增强子和/或启动子区域并导致表达载体上携带的基因的有效转录。合适的载体包括原核表达载体(例如puc18,puc19,bluescript及其衍生物),mpl8、mpl9、pbr322、pmb9、coiel、pcrl、rp4、噬菌体和穿梭载体(例如psa3和pat28),和基于病毒载体的真核表达载体(例如腺病毒,腺相关病毒以及逆转录病毒和慢病毒),以及非病毒载体,例如psilencer 4.1
‑
cmv(life technologies corp.,carslbad,ca,us)、pcdna3、pcdna3.1/hyg phcmv/zeo、pcr3.1、pefl/his、pind/gs、prc/hcmv2、psv40/zeo2、ptracer
‑
hcmv、pub6/v5
‑
his、pvaxl、pzeosv2、pci、
psvl和pksv
‑
10、pbpv
‑
l、pml2d和ptdtl。
66.术语“重组质粒”或“质粒”是指通过基因工程技术获得的小、环状、双链、自我复制dna分子,能够将感兴趣的遗传物质转移到细胞中,从而在靶细胞中产生由所述遗传物质(例如蛋白多肽,肽或功能性rna)编码的产物。此外,术语“重组质粒”或“质粒”还指小的、环状、双链、自我复制的dna分子,其通过在病毒载体的生产过程中使用的基因工程技术获得,所述病毒载体作为重组载体基因组的载体。
67.术语“重组病毒载体”或“病毒载体”是指通过基因工程技术从天然病毒中获得的试剂,该基因工程技术能够将目标遗传物质(例如dna或rna)转移到细胞中,从而导致在靶细胞中产生由所述遗传物质(例如蛋白多肽、肽或功能性rna)编码的产物。
68.在本文中用作同义词的术语“腺相关病毒”、“aav病毒”、“aav病毒体”、“aav病毒颗粒”和“aav颗粒”是指由至少一种aav衣壳蛋白组成的病毒颗粒(优选由特定aav血清型的所有衣壳蛋白和对应于aav基因组的封装多核苷酸组成。野生型aav是指属于细小病毒科的依赖病毒属的病毒。野生型aav基因组的长度约为4.7kb,由可以是阳性或阴性的单链脱氧核糖核酸(ssdna)组成。野生型基因组包括在dna链两端的反向末端重复序列(itr)和三个开放阅读框(orf)。orf rep编码aav生命周期必需的四种rep蛋白。orf帽包含编码衣壳蛋白的核苷酸序列:vp1、vp2和vp3,它们相互作用形成二十面体对称的衣壳。最后,与cap orf重叠的aap orf编码似乎促进衣壳装配的aap蛋白。如果颗粒包含aav itr侧翼的异源多核苷酸(即不同于野生型aav基因组的多核苷酸,例如要传递至哺乳动物细胞的转基因),则通常称为“aav载体颗粒”或“aav病毒载体”或“aav载体”。本发明还包括双链aav的使用,也称为dsaav或scaav。
69.如本文所用,术语“腺相关病毒itr”或“aav itr”是指存在于aav基因组dna链的两端的反向末端重复。itr序列是aav基因组有效繁殖所必需的。这些序列的另一个特性是它们形成发夹的能力,该特征有助于它们的自引发,其允许第二dna链的不依赖于引发酶的合成。还已经证明itr既需要将野生型aav dna整合到宿主细胞基因组中(例如,在人类第19号染色体上的血清型2aav),又需要从itr中解救出来,以及有效地将aav dna衣壳化为完全组装的抗脱氧核糖核酸酶的aav颗粒。itr序列的长度约为145bp。优选地,itr的整个序列用于aav病毒载体的基因组中,尽管可以对这些序列进行一定程度的微小修饰。可以通过插入、缺失或截短来改变野生型itr序列,只要该itr介导期望的功能例如复制、刻痕、病毒打包、集成和/或provirus抢救。修饰这些itr序列的方法是本领域众所周知的。itr可以来自任何野生型aav,包括但不限于血清型1、2、3、4、5、6、7、8、9、10、11或12或任何其他已知或以后发现的aav。aav包含两个相同或不同的itr。此外,两个aav itr可以与aav衣壳来自相同的aav血清型,也可以不同。在优选的实施方案中,5'和3'aav itr衍生自aav1、aav2、aav4、aav5、aav7、aav8和/或aav9。优选地,itr来自aav2、aav8和/或aav9是最优选的aav2。在一个实施方案中,选择aav2 itr以产生假型aav(即具有衣壳和衍生自不同血清型的itr的aav)。
70.如本文所用,表达“重组病毒基因组”是指aav基因组,其中至少一个外源多核苷酸插入天然存在的aav基因组中。根据本发明的aav的基因组通常包含顺式作用的5'和3'反向末端重复序列(itr)和表达盒。
71.术语“基因疗法”是指将感兴趣的遗传物质(例如dna或rna)转移到细胞中以治疗或预防遗传或获得性疾病或病症。目的遗传物质编码需要体内产生的产物(例如蛋白多肽、
肽或功能性rna)。例如,目的遗传物质可以编码具有治疗价值的酶、激素、受体或多肽。
72.如本文所用,术语“转导”或“转导”是指通过病毒载体将外源核苷酸序列引入细胞中的过程。
73.如本文所用,术语“转染”是指通过非病毒方法故意将纯化的核酸引入真核细胞的过程。
74.如本文所用,术语“治疗”是指给予本发明的化合物或组合物以控制疾病的进展。疾病进展的控制应理解为实现有益或期望的临床结果,包括但不限于减轻症状、减少疾病持续时间、稳定病理状态(特别是避免进一步恶化)、疾病进展的延迟、病理状态的改善和缓解(部分和全部)。与不进行治疗的预期生存相比,疾病进展的控制还涉及生存期的延长。
75.术语“有效量”是指足以实现预期目的的物质的量。例如,增加半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶(galns)活性的aav载体的有效量是足以减少糖胺聚糖积聚的量。用于治疗疾病或病症的表达载体的“治疗有效量”是足以减少或消除疾病或病症的信号和症状的表达载体的量。给定物质的有效量将随各种因素而变化,例如物质的性质、给药途径、接受该物质的动物的大小和种类以及给予该物质的目的。每种情况下的有效量可以由技术人员根据本领域中已建立的方法凭经验确定。
76.术语“个体”是指哺乳动物,优选为人或非人哺乳动物,更优选为小鼠、大鼠、其他啮齿动物、兔、狗、猫、猪、牛、马或灵长类动物,进一步优选为人。
具体实施方式
77.本发明提供了用于治疗粘多糖酶,特别是iva型粘多糖酶或morquio a综合征的新的多核苷酸序列和载体。
78.因此,在第一方面,本发明涉及一种分离的多核苷酸序列(以下称为“本发明的多核苷酸”)与seq id no:1中设定的核苷酸序列具有75%至90%的同一性,其中所述序列编码功能性人半乳糖胺(n
‑
乙酰基)
‑
6硫酸酯酶。
79.如上所述,mpsiva是由半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶(galns)的活性不足引起的。galns是一种溶酶体酶,其在硫酸软骨素
‑
6(c6s)的非还原端水解n
‑
乙酰基半乳糖胺
‑6‑
硫酸盐的硫酸酯基团,在硫酸角质素(ks)的非还原端水解n
‑
乙酰半乳糖胺的硫酸酯基团。由于未降解的c6s和ks的持续积累,会发生进行性细胞损伤,从而导致多系统疾病。
80.发明人已经表明,体内施用含有不同版本的人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶(galns)表达盒的载体,其中所述galns编码序列与编码galns核苷酸序列的野生型具有75%至90%的同一性,导致galns活性大大超过mpsiva动物中测得的水平。实际上,包含与野生型具有75%至90%同一性的序列的表达载体达到的人galns活性水平高于由包含野生型序列的载体介导的表达载体。
81.本发明还考虑了与编码野生型galns的核苷酸序列具有75%至90%同一性的多核苷酸序列,如seq id no:1所示,其中所述序列编码本领域已知的功能性人galns变体和片段。因此,本发明应被解释为包括编码功能上等效的galns变体的dna。
82.如本文所用,术语“功能上等同的变体”涉及与由galns的多肽序列编码的酶基本上同源并且保留galns的生物学活性的任何酶。这种功能等效变体的序列可以通过插入、取代或缺失一个或多个氨基酸而从galns的序列获得,并且其基本上保留了galns的生物学活
性。用于确定变体是否保留天然galns的生物学活性的方法是技术人员众所周知的,并且包括在本技术的实验部分中使用的任何测定法。特别地,本发明涵盖的galns的功能等效变体具有galns的至少一种功能,例如标准化或降低糖胺聚糖(gag)水平,特别是c6s和ks水平。在本发明的实施例部分中,详细描述了适合于确定功能性galns酶降低或标准化所述gag水平的能力的方法。
83.如本发明所附实施例所示,本发明的多核苷酸序列编码功能性galns酶。与wt相比,所述酶显示出增强的活性。结果表明,载体给药后galns活性得以恢复,这导致半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶活性大大超过了mpsiva动物中测得的水平。如本发明所附实施例所示,galns活性水平为肝脏wt水平的1500%至2600%。
84.在一个优选的实施方案中,如果多肽具有上述功能,特别是如果其能够以galns野生型多肽能力的至少10%、20%、30%、40%、50%、60%、70%、80%、90%或100%,优选具有galns野生型多肽至少50%或100%的能力降解糖胺聚糖硫酸角质素(ks)和硫酸软骨素(c6s),则该多肽被认为是galns酶的功能等效变体。
85.galns的功能等效变体是与天然galns基本上同源的多肽。表述“基本上同源”是指当所述蛋白质序列与galns野生型序列具有至少50%、至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%或至少99%。的同一性时的蛋白质序列。使用本领域技术人员众所周知的计算机算法和方法确定两种多肽之间的同一性程度。优选通过使用blastp算法[blast manual,altschul,s.,et al,ncbi nlm nih bethesda,md.20894,altschul,s.,et al,j.mol.biol.215:403
‑
410(1990)]确定两个氨基酸序列之间的同一性,尽管也可以使用其他类似的算法。
[0086]
galns的功能等效变体可以通过替换其编码多核苷酸内的核苷酸来获得,这考虑到宿主细胞中用于产生galns的密码子偏好。
[0087]
galns的功能等效变体可以通过进行保守的氨基酸变化并在上述功能测定之一或本领域已知的其他功能测定中测试所得变体来产生。保守氨基酸取代是指具有相似侧链的残基的互换性。例如,具有脂族侧链的一组氨基酸是甘氨酸,丙氨酸,缬氨酸,亮氨酸和异亮氨酸;具有脂族羟基侧链的氨基酸是丝氨酸和苏氨酸;具有酰胺基侧链的氨基酸是天冬酰胺和谷氨酰胺;具有芳族侧链的氨基酸基团是苯丙氨酸、酪氨酸和色氨酸;具有碱性侧链的一组氨基酸是赖氨酸、精氨酸和组氨酸;具有含硫侧链的氨基酸是半胱氨酸和蛋氨酸。优选的保守氨基酸取代基是:缬氨酸
‑
亮氨酸
‑
异亮氨酸、苯丙氨酸
‑
酪氨酸、赖氨酸
‑
精氨酸、丙氨酸
‑
缬氨酸和天冬酰胺
‑
谷氨酰胺。
[0088]
在本发明的特定实施方案中,本发明的多核苷酸中包含的编码galns蛋白或其功能等效变体的核苷酸序列与seq id no:1中设置的核苷酸序列具有75%至90%的同一性。在更特定实施方案中,所述核苷酸序列与seq id no:1中设定的核苷酸序列具有80%至85%的同一性。在更优选的实施方式中,所述序列选自seq id no:3、seq id no:5和seq id no:7。
[0089]
在本发明的另外实施方案中,由本发明的多核苷酸编码的galns蛋白选自人galns(hgalns)和小鼠galns(mgalns),优选人galns(hgalns)。
[0090]
本发明的多核苷酸可进一步包含表达控制序列,包括但不限于适当的转录调节序
列(即起始,终止,启动子和增强子),有效的rna加工信号(例如剪接和聚腺苷酸化(polya)信号)、稳定细胞质mrna的序列、增强翻译效率的序列(即kozak共有序列)、增强蛋白质稳定性的序列以及在需要时增强编码产物分泌的序列。许多表达控制序列是本领域已知的,并且可以根据本发明使用。
[0091]
因此,根据本发明,在特定的实施方案中,本发明的多核苷酸具有与编码galns的核苷酸序列可操作地连接的转录调节区。在本发明的特定实施方案中,所述转录调节区包含启动子。在本发明的另一个具体实施方案中,本发明的多核苷酸的转录调节区还包含与启动子可操作连接的增强子。
[0092]
可将本发明的多核苷酸掺入载体中。在一个特定的实施方案中,所述载体是表达载体。因此,另一方面,本发明涉及含有本发明的多核苷酸的表达载体,在本文中称为“本发明的载体”。在一个特定的实施方案中,所述载体是质粒。在另一个具体的实施方案中,所述载体是aav载体,所述aav载体含有包含根据本发明的多核苷酸的重组病毒基因组。
[0093]
在本发明的多核苷酸的上下文中公开的所有实施方案也适用于本发明的载体。
[0094]
在另外实施方案中,本发明的多核苷酸序列的侧翼是aav itr。在更特定实施方案中,所述aav itrs是aav2 itrs。
[0095]
在另外实施方案中,本发明的多核苷酸还包含转录后调控区。如本文所用,术语“转录后调控区”是指促进表达、稳定或定位在盒或所得基因产物中的序列的任何多核苷酸。转录后调节区可以是但不限于,土拨鼠肝炎病毒转录后区(wpre)。如本文所用,术语“土拨鼠乙型肝炎病毒后调节元件”或“wpre”是指dna序列,其在转录时产生能够增强基因表达的三级结构。
[0096]
在另外实施方案中,本发明的多核苷酸序列进一步包含聚腺苷酸化信号。
[0097]
如本文所用,术语“聚腺苷酸化信号”涉及介导聚腺嘌呤尾巴附着于mrna的3'末端的核酸序列。合适的聚腺苷酸化信号包括但不限于sv40早期聚腺苷酸化信号、sv40晚期聚腺苷酸化信号、hsv胸苷激酶聚腺苷酸化信号、鱼精蛋白基因聚腺苷酸化信号、腺病毒5elb聚腺苷酸化信号、牛生长激素聚腺苷酸化信号、人类变体生长激素聚腺苷酸化信号、兔β
‑
球蛋白聚a信号等。在一个特定的实施方案中,聚腺苷酸化信号是兔β
‑
球蛋白poly a信号或其功能变体和片段。
[0098]
正如刚才提到的,在本发明的特定实施方案中,将本发明的多核苷酸掺入载体中。在一个特定的实施方案中,所述载体是表达载体。在一个特定的实施方案中,所述表达载体包含与所述多核苷酸序列可操作连接的启动子序列。所述启动子可以是组成型启动子或组织特异性启动子。在一个特定的实施方案中,所述启动子选自cag启动子、haat启动子或cmv启动子。在本发明的一个优选的实施方案中,所述启动子是cag启动子。在另外特定实施方案中,所述启动子是haat启动子。
[0099]
本发明的多核苷酸包含编码galns或其功能等效变体的核苷酸序列。在一个实施方案中,所述核苷酸序列是编码人galns的核苷酸序列,其对应于登录号为nm_000512.4的ncbi数据库的序列,更具体地为seq id no:1。在一个优选的实施方案中,核苷酸序列是编码人galns的核苷酸序列的变体。更特别地,所述序列与seq id no:1中设定的核苷酸序列具有75
‑
90%的同一性。更特别地,所述序列与seq id no:1中所示的核苷酸序列具有80%至85%的同一性。优选地,所述序列是选自由seq id no:3、seq id no:5和seq id no:7组
no:12的4107
‑
4215核苷酸。
[0107]
在另一个优选的实施方案中,重组病毒基因组包含核苷酸序列seq id no:13。具体地,5'aav2 itr包含核苷酸1
‑
131,cag启动子包含核苷酸185
‑
1707,人galns cdna包含核苷酸1918
‑
3494,兔β
‑
球蛋白poly a信号包含核苷酸3520
‑
4048,而3'aav2 itr包含seq id no:13的核苷酸4107
‑
4215。
[0108]
在另一个优选的实施方案中,重组病毒基因组包含核苷酸序列seq id no:14。具体地,5'aav2 itr包含核苷酸1
‑
120,cmv增强子包含核苷酸194
‑
557,β
‑
肌动蛋白启动子包含核苷酸558
‑
839,鸡β
‑
肌动蛋白基因的第一个内含子包含核苷酸840
‑
1804,兔β
‑
珠蛋白基因的内含子2/外显子3包含核苷酸1805
‑
1906,人galns cdna包含核苷酸1934
‑
3592,兔β
‑
珠蛋白poly a信号包含核苷酸3619
‑
4147,并且3'aav2 itr包含seq id no:14的核苷酸4206
‑
4313。
[0109]
在另一个优选的实施方案中,重组病毒基因组包含核苷酸序列seq id no:15。具体地,5'aav2 itr包含核苷酸1
‑
120,cmv增强子包含核苷酸194
‑
557,β
‑
肌动蛋白启动子包含核苷酸558
‑
839,鸡β
‑
肌动蛋白基因的第一个内含子包含核苷酸840
‑
1804,兔β
‑
珠蛋白基因的内含子2/外显子3包含核苷酸1805
‑
1906,人galns cdna包含核苷酸1934
‑
3592,兔β
‑
珠蛋白poly a信号包含核苷酸3619
‑
4147,并且3'aav2 itr包含seq id no:15的核苷酸4206
‑
4313。
[0110]
修饰的aav序列也可用于本发明的上下文中。这样的修饰序列包括与已知的任何血清型的aav itr或vp具有至少约70%、至少约75%、至少约80%、至少约85%、至少约90%、至少约95%或更多的核苷酸和/或氨基酸序列(例如,具有约75
‑
99%核苷酸或氨基酸序列同一性的序列)同一性并保持所述组分功能的序列。用于确定aav itr或vp的功能的测定法是本领域已知的。所述修饰的序列可以代替野生型aav itr或vp序列使用。
[0111]
本发明的aav载体包含来自任何血清型的衣壳。通常,不同的aav血清型在氨基酸和核酸水平上具有明显同源性的基因组序列,提供相同的遗传功能,产生在物理和功能上基本相同的病毒体,并通过几乎相同的机制进行复制和组装。特别地,本发明的aav可以属于aav(aav1)、aav2、aav3(包括3a和3b型)、aav4、aav5、aav6、aav7、aav8、aav9、aav10、aav11、禽类aav、牛aav、犬类aav、马类aav、绵羊aav以及其他任何类型的aav的血清型1。不同aav血清型的基因组序列的例子可以在文献中或在诸如genbank的公共数据库中找到。请参见genbank登录号af028704.1(aav6)、nc006260(aav7)、nc006261(aav8)和ax753250.1(aav9)。在一个优选的实施方案中,本发明的腺相关病毒载体是选自aav2、aav5、aav7、aav8、aav9、aav10和aavrh10血清型的血清型。在一个更优选的实施方案中,所述aav是aav血清型9,aav9或aav血清型8,aav8。
[0112]
本发明的aav载体的基因组缺少rep和帽开放阅读框。此类aav载体只能复制并包装到已经用编码并表达rep和cap基因产物(即aav rep和cap蛋白)的载体转染的宿主细胞中的感染性病毒颗粒中,并且其中宿主细胞已被编码和表达腺病毒蛋白的载体转染。
[0113]
本发明的药物组合物
[0114]
可以通过常规方法将本发明的多核苷酸表达载体施用于人体或动物,这需要将其配制成药物组合物。因此,在第二方面,本发明涉及药物组合物(以下称为“本发明的药物组合物”),其包含治疗有效量的本发明的多核苷酸或本发明的载体。该药物组合物可以进一
步包含药学上可接受的载体。
[0115]
在本发明的多核苷酸或本发明的载体的上下文中公开的所有实施方案也适用于本发明的药物组合物。
[0116]
术语“治疗有效量”是指计算出产生所需效果的本发明的多核苷酸、载体或aav载体的量,并且除其他原因外,通常将由本发明的多核苷酸、载体或aav载体的自身特征以及所获得的治疗效果来确定。因此,可以通过本文所述或本领域已知的标准临床技术确定将有效治疗疾病的所述量。制剂中使用的精确剂量将取决于给药途径。初始剂量可以使用现有技术中公知的技术从体内数据(例如动物模型)估计。具有现有技术水平的正常经验的人员可以根据动物中的数据轻松优化对人的给药。
[0117]
在一个具体的实施方案中,制剂的剂量可以作为病毒颗粒或作为基因组拷贝(“gc”)/病毒基因组(“vg”)来测量或计算。
[0118]
本领域已知的任何方法均可用于确定每毫升本发明病毒组合物的基因组拷贝(gc)数。进行aav gc滴定的一种方法如下:首先用dnase处理纯化的aav载体样品,以消除生产过程中未包衣的aav基因组dna或污染质粒dna。然后使耐dnase的颗粒热处理以从衣壳中释放基因组。然后使用靶向病毒基因组特定区域的引物/探针组通过实时pcr对释放的基因组进行定量。
[0119]
本文可互换使用的术语“药学上可接受的载体”、“药学上可接受的稀释剂”、“药学上可接受的赋形剂”或“药学上可接受的载体”是指无毒的固体、半固体或液体填充剂、稀释剂、包囊材料,或任何常规类型的配方助剂。药学上可接受的载体在所采用的剂量和浓度下对接受者基本上是无毒的,并且与制剂的其他成分相容。药学上可接受的载体的数量和性质取决于所需的给药形式。药学上可接受的载体是已知的,并且可以通过本领域众所周知的方法制备。
[0120]
可以根据常规程序将药物组合物配制成适于静脉内、皮下、肌内、脑脊液内(csf)例如脑内或脑室内施用的药物组合物。在一个优选的实施方案中,药物组合物用于静脉内或脑脊液内(csf)施用。更优选地,药物组合物用于静脉内施用。
[0121]
可以将aav载体配制用于通过注射(例如通过推注或连续输注)进行肠胃外给药。注射剂可以单位剂量形式(例如在安瓿瓶中或在单剂量或多剂量容器中)与添加的防腐剂一起提供。病毒组合物可以采取诸如在油性或水性运载体中的悬浮液,溶液或乳剂的形式,并且可以包含配制剂,例如悬浮剂,稳定剂或分散剂。aav制剂的液体制剂可以通过常规方法与药学上可接受的添加剂一起制备,例如悬浮剂(例如山梨糖醇糖浆,纤维素衍生物或氢化食用脂肪),乳化剂(例如卵磷脂或阿拉伯胶),非水性媒介物(例如杏仁油,油性酯,乙醇或分馏植物油)和防腐剂(例如对羟基苯甲酸甲酯或对羟基苯甲酸丙酯或山梨酸)。制剂还可以包含缓冲盐。或者,组合物可以是粉末形式,以在使用前与合适的媒介物(例如无菌无热原水)一起配制。必要时,该组合物还可包含局部麻醉剂,例如利多卡因,以减轻注射部位的疼痛。当该组合物要通过渗透给药时,可以免除一个装有药物质量的水或盐溶液的渗透瓶。当通过注射施用组合物时,可以提供水瓶用于注射或无菌盐溶液,从而可以在施用之前将成分混合。优选地,药学上可接受的载体是盐溶液和去污剂,例如聚乙烯
‑
聚氧丙烯嵌段共聚物,
[0122]
可以配制本发明的组合物以递送给兽医用动物(例如牲畜(牛,猪,猪,其他))和其
他非人类哺乳动物受试者,以及人类受试者。本发明的药物组合物可以与生理上可接受的载体一起配制用于基因转移和基因治疗应用。
[0123]
还包括佐剂与本发明的多核苷酸,载体或aav载体组合或混合使用。所考虑的佐剂包括但不限于矿物盐佐剂或矿物盐凝胶佐剂,颗粒佐剂,微粒佐剂,粘膜佐剂。
[0124]
佐剂可以与本发明的多核苷酸,载体或aav载体的混合物形式给予受试者,或组合使用。
[0125]
本发明的药物组合物可以局部或全身给药。在一个实施方案中,药物组合物在要转导其细胞的组织或器官附近施用。在一个具体的实施方案中,本发明的药物组合物是全身给药的。
[0126]
如本文所用,术语“全身施用”和“全身施用”是指本发明的多核苷酸、载体、aav载体或组合物可以以非定位的方式施用于受试者。全身给药可以到达受试者体内的几个器官或组织,或者可以达到受试者的特定器官或组织。例如,静脉内给药可导致受试者中一种以上组织或器官的转导。本发明的药物组合物可以单剂量施用,或者在本发明的特定实施方案中,可以采用多剂量(例如两次、三次、四次或更多次施用)来达到治疗效果。在本发明的一个优选的实施方案中,本发明的药物组合物以单剂量施用,即其在生命中一次施用。
[0127]
因此,另一方面,本发明涉及用于医学的根据本发明的多核苷酸或载体或根据本发明的药物组合物。
[0128]
在另一方面,本发明涉及用于治疗iva型粘多糖贮积症或morquio a综合征的本发明的多核苷酸或载体或本发明的药物组合物。
[0129]
如本发明的实施例所示,通过尾静脉注射将含有不同版本的人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶表达盒的aav载体静脉内递送至患mpsiva的2个月大的小鼠。galns活性分析表明,与所有含半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的载体进行转导后,半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的活性大大超过了mpsiva动物中测得的水平。
[0130]
因此,在另一方面,本发明涉及用于增加半乳糖胺(n
‑
乙酰基)
‑
6硫酸酯酶活性的根据本发明的多核苷酸或载体或根据本发明的药物组合物。
[0131]
在另一方面,本发明提供了用于在有需要的受试者中治疗和/或预防粘多糖贮积型iva的方法,该方法包括向所述受试者施用根据本发明的多核苷酸或根据本发明的载体或根据本发明的药物组合物。
[0132]
如本文所用,术语“预防”和“防止”是指抑制受试者中疾病的发生或减少疾病的发生。预防可以是完全的(例如,受试者中完全没有病理细胞)或部分。预防还指对临床状况的敏感性降低。如本文所用,术语“治疗”是指给予本发明的多核苷酸、载体或aav载体或药物组合物以在疾病的临床症状出现后控制疾病的进展。疾病进展的控制被理解为是指获得有益或期望的临床结果,包括但不限于症状减轻、疾病持续时间减少、病理状态稳定(特别是避免进一步恶化)、疾病进展的延迟、病理状态的改善和缓解(部分和全部)。与不进行治疗的预期生存相比,疾病进展的控制还涉及生存期的延长。
[0133]
如本文所用,术语“受试者”是指个体或动物,例如人类,非人类灵长类动物(例如黑猩猩和其他猿猴物种),农场动物(例如鸟类,鱼类,牛,绵羊,猪,山羊和马),家养哺乳动物(例如狗和猫)或实验动物(例如啮齿动物,例如小鼠,大鼠和豚鼠)。该术语包括任何年龄或性别的对象。在一个优选的实施方案中,所述受试者是哺乳动物,优选人类。
[0134]
获得本发明的aav的方法
[0135]
本发明还涉及用于获得本发明的aav载体的方法。所述aav载体可通过将本发明的多核苷酸引入组成性表达rep和cap蛋白的细胞中而获得,或者rep和cap编码序列在质粒或载体中提供。
[0136]
因此,另一方面,本发明涉及一种用于获得aav载体的方法,该方法包括以下步骤:
[0137]
提供一种细胞,该细胞包含本发明的多核苷酸,aav帽蛋白,aav rep蛋白和(可选)aav依赖复制的病毒蛋白,
[0138]
将电池保持在足以组装aav的条件下
[0139]
纯化细胞产生的腺相关病毒载体。
[0140]
能够产生aav载体的任何细胞均可用于本发明。
[0141]
先前已经描述了用于该方法的本发明的多核苷酸。在本发明的多核苷酸的上下文中公开的任何实施方案都可用于获得本发明的aav的方法的上下文中。
[0142]
如本文所用,术语“帽蛋白”是指具有天然aav帽蛋白(例如vp1、vp2和vp3)的至少一种功能活性的多肽。帽蛋白的功能活性的例子包括诱导衣壳形成,促进单链dna积累,促进aav dna包装到衣壳中(即衣壳化),与细胞受体结合以及促进病毒体进入宿主细胞的能力。原则上,任何帽蛋白都可用于本发明。
[0143]
在优选的实施方案中,帽蛋白衍生自aav8或aav9。
[0144]
如本文所用,术语“衣壳”是指包装病毒基因组的结构。衣壳由蛋白质制成的几个寡聚结构亚基组成。例如,aav具有由三种衣壳蛋白(vp1,vp2和vp3)相互作用形成的二十面体衣壳。
[0145]
如本文所用,术语“rep蛋白”是指具有天然aav rep蛋白的至少一种功能活性的多肽。rep蛋白的“功能活性”是与蛋白的生理功能有关的任何活性,包括通过识别、结合和刻痕dna复制的aav起源促进dna复制以及dna解旋酶活性。其他功能包括调节aav(或其他异源)启动子的转录以及aav dna进入宿主染色体的位点特异性整合。在一个具体的实施方案中,aav rep基因衍生自血清型aav2。
[0146]
如本文所用,表述“aav依赖于复制的病毒蛋白”是指执行aav依赖于复制的功能的多肽(即“辅助功能”)。辅助功能包括但不限于激活aav基因转录,阶段特异性aav mrna剪接,aav dna复制,帽蛋白合成和aav衣壳装配所需的那些功能。基于病毒的辅助功能可以源自任何已知的辅助病毒,例如腺病毒,疱疹病毒(除单纯疱疹病毒1型以外)和牛痘病毒。辅助功能包括但不限于腺病毒e1,e2a,va和e4或疱疹病毒ul5,ul8,ul52和ul29以及疱疹病毒聚合酶。
[0147]
本发明的多核苷酸或基因aav rep,aav帽和提供辅助功能的基因可通过将所述基因掺入载体例如质粒中并将所述载体引入细胞中而引入细胞中。可以将基因掺入相同质粒或不同质粒中。在一个优选的实施方案中,将本发明的多核苷酸掺入一个质粒中,将aav rep和cap基因掺入另一质粒中,并将提供辅助功能的基因掺入另一质粒中。
[0148]
可以通过使用本领域公知的任何合适方法将含有本发明的多核苷酸和/或aav rep和cap基因或提供辅助功能的基因的质粒引入细胞。转染方法的实例包括但不限于与磷酸钙,deae
‑
葡聚糖,聚乙烯,电穿孔,显微注射,脂质体介导的融合,脂质转染,逆转录病毒感染和基因枪转染共沉淀。在一个特定的实施方案中,转染是通过与磷酸钙共沉淀进行的。
当细胞缺乏任何aav rep和cap基因以及提供腺病毒辅助功能的基因的表达时,可以将所述基因与本发明的多核苷酸同时引入细胞中。或者,可以在引入本发明的多核苷酸之前或之后将所述基因引入细胞中。
[0149]
在一个特定的实施方案中,用三种质粒同时转染细胞,i)包含本发明的多核苷酸的质粒,ii)包含aav rep和cap基因的质粒,和iii)包含提供辅助功能的基因的质粒。
[0150]
本发明方法的步骤(ii)涉及将细胞维持在足以组装aav的条件下。
[0151]
可以如本文实施例中所述进行培养细胞的方法和促进aav载体颗粒释放的示例性条件,例如细胞的裂解。生产细胞生长适当的时间,以促进aav的组装和病毒载体向培养基中的释放。通常,从病毒产生的角度来测量培养时间。例如,在aav的情况下,通常在如本文所述在合适的生产细胞中提供辅助病毒功能后开始病毒生产。
[0152]
本发明方法的步骤(iii)涉及纯化由细胞产生的aav载体。
[0153]
从所述细胞或所述培养基中纯化aav的任何方法均可用于获得本发明的aav。在一个特定的实施方案中,根据基于聚乙二醇沉淀步骤和两个连续的氯化铯(cscl)梯度的优化方法,纯化本发明的aav。
[0154]
已知各种天然存在和工程改造的aav,其编码核酸、aav帽和rep蛋白,以及分离或产生、繁殖和纯化此类aav的方法,特别是其衣壳,适合用于生产aav的技术是本领域已知的。
[0155]
本发明进一步提供了分离的细胞,其包含编码galns蛋白或其功能等同变体的本发明的多核苷酸序列。
[0156]
在本发明的多核苷酸,载体或aav载体和本发明的药物组合物的上下文中公开的所有实施方案均适用于本发明的治疗方法。
[0157]
一般程序
[0158]
1.重组aav载体
[0159]
本文所述的aav载体是通过三次转染获得的。制作载体所需的材料是:hek293细胞(表达腺病毒e1基因),提供腺病毒功能的辅助质粒,提供血清型2的aav rep基因和血清型8或9(aav8或aav9)的cap基因的质粒,最后是带有aav2 itr的骨架质粒和目的构建体。
[0160]
为了产生表达半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的aav载体,在普遍存在的杂合cag启动子或肝特异性haat启动子的控制下,将人或鼠的半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的优化或非优化编码序列克隆到aav主链质粒中。使用endofree plasmid megaprep kit(qiagen)进行质粒的大规模生产。
[0161]
通过使用三个具有修饰的质粒通过无辅助病毒转染hek293细胞来产生载体(matsushita等,1998;wright等,2005)。将细胞在装有10%fbs的dmem中的滚瓶(rb)(corning,corning,ny,us)中培养至70%汇合,然后共转染:1)带有表达盒的质粒,该表达盒的侧翼是血清型2aav的病毒itr(如上所述);2)携带aav rep2和cap8或cap9基因的质粒;3)具有腺病毒辅助功能的质粒。如前所述(ayuso et al。,2010),使用优化方案通过两个连续的氯化铯梯度纯化载体。用pbs+0.001%f68透析载体,过滤,通过qpcr滴定,保存在
‑
80℃直至使用。
[0162]
根据本领域公知的分子生物学技术构建本发明的载体。
[0163]
2.体外转染研究
[0164]
用4μgpaav
‑
cag
‑
omgalns、paav
‑
haat
‑
omgalns,paav
‑
cag
‑
hgalns,paav
‑
cag
‑
ohgalns
‑
v1,paav
‑
cag
‑
ohgalns
‑
v2或paav
‑
cag
‑
ohgalns
‑
v3转染hek293细胞,按照制造商的说明使用2000(invitrogen,thermo fisher scientific,ca,usa)。48小时后,收获细胞和培养基并加工用于蛋白质提取。
[0165]
通过在250μl mili
‑
q水中超声处理细胞获得蛋白质提取物,并使用bradford蛋白质测定法(bio
‑
rad,hercules,ca,美国)对蛋白质含量进行定量。在1微克细胞蛋白提取物和5微升培养基中测定半乳糖胺(n
‑
乙酰基)
‑
6硫酸酯酶的活性,并分别以4甲基伞形酮来源的荧光底物通过蛋白质总量和体积进行标准化(toronto rerearch chemicals inc,ontario,canada),如前所述(van diggelen等,1990)。
[0166]
3.动物
[0167]
获得了c57bl/6n
‑
a/a胚胎干细胞,其在国际小鼠表型研究协会(impc,www.mousephenotype.org)可获得的galns基因中带有标记有报告基因(lacz)的标签插入。巴塞罗那大学(uab)的动物生物技术和基因治疗中心(cbateg)的转基因动物科将克隆克隆显微注射到c57bl/6jolahsd胚泡中,然后将所得的雄性嵌合体与c57bl/6ntac雌性一起繁殖,以产生galns剔除后代(mpsiva或galns
‑
/
‑
小鼠)。通过扩增包含目标突变的序列的pcr分析,从尾巴修剪的样品的基因组dna上确定基因型。相应的有义和反义引物的序列为:有义引物:5’cca ggg aat gtc cca cct att t 3’(seq id no:20);反义引物:5'gtc agg ttg aca cga agc tg 3'(seq id no:21);反义引物ko:5
′
gga act tcg gtt ccg gcg 3
′
(seq id no:22)。有义和反义引物可对野生型小鼠进行基因分型。有义和反义引物ko允许对galns
‑
/
‑
小鼠进行基因分型。
[0168]
随意给小鼠喂食标准饮食(哈兰,tekland),并保持12小时的明暗循环(上午9:00点亮)。
[0169]
由于缺乏galns活性,这些动物早在一个月大时就表现出mpsiva疾病的几种病理特征,包括糖胺聚糖(gag)的积累和股骨和胫骨epiphyseal板不同区域溶酶体区室的扩大。此外,当动物变老时,许多这些病理学发现会恶化,这表明与衰老的动物相比,病理学恶化了。同样,随着动物年龄的增长,gag在肝、心脏和脾等周围器官中的积累也被观察到。但是,在galns
‑
/
‑
和wt同窝幼仔的寿命上没有观察到显着差异。
[0170]
4.向小鼠施用载体
[0171]
对于aav8
‑
haat
‑
omgalns载体的静脉内载体递送,通过3
‑
4周龄的galns
‑
/
‑
动物的尾静脉将总剂量为1x10
11 vg的小鼠总体积为200μl。向类似的动物群注射1x10
11 vg对照非编码(aav8
‑
haat
‑
null)载体。
[0172]
为了将aav8
‑
cag
‑
omgalns载体静脉内递送给小鼠,通过3
‑
4周龄的galns
‑
/
‑
动物的尾静脉向小鼠注射总剂量为1x10
12 vg,总体积为200μl。向类似的动物群注射1x10
12 vg对照非编码(aav8
‑
cag
‑
null)载体。
[0173]
为了将aav9
‑
cag
‑
omgalns载体静脉内递送给小鼠,通过3
‑
4周龄的galns
‑
/
‑
动物的尾静脉向小鼠注射总剂量为1x10
12 vg的总体积为200微升。向类似的动物群注射1x10
12 vg对照非编码(aav9
‑
cag
‑
null)载体。
[0174]
在载体施用后6个月大的7个月大时,处死小鼠并收获组织。
[0175]
对于静脉内载体递送,通过尾静脉注射2个月大的galns
‑
/
‑
动物,将200升的总体
积为200微升的aav9载体的5x10
10
载体基因组裸露了不同版本的人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶编码序列。wt和未处理的galns
‑
/
‑
动物用作对照。
[0176]
在施用载体后15天,在2.5个月大时,处死小鼠并收获组织。
[0177]
5.样品采集
[0178]
处死时,将动物深度麻醉,然后用50ml pbs经心脏灌注,以从组织中完全清除血液。收集整个大脑和多个躯体组织(包括肝脏,脾脏,肾脏,肺,心脏,脂肪组织,眼睛,泪腺和骨骼),并将其冷冻在液氮中并保存在
‑
80℃或浸入福尔马林中以用于随后的组织学分析。
[0179]
6.半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶活性和糖胺聚糖定量
[0180]
将肝和脂肪组织样品在mili
‑
q水中超声处理,并将股骨样品在均质缓冲液中均质化,该均质缓冲液由25mmol/l ph 7.2的tris
‑
hcl和1mmol/l苯甲基磺酰氟组成。如前所述(van diggelen等,1990),半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶活性是用4
‑
甲基伞形酮衍生的荧光底物测定的(toronto rerearch chemicals inc,ontario,canada)。将肝脏、脂肪组织和股骨galns活性水平相对于蛋白质总量进行标准化,并使用bradford蛋白质测定法(bio
‑
rad,hercules,ca,美国)进行定量。
[0181]
对于gag定量,将组织样品称重,然后用蛋白酶k消化,并通过离心和过滤澄清提取物。通过液相色谱
‑
质谱法(lc
‑
ms/ms)测定组织提取物和血清中的gag水平。将gag的水平相对于湿组织重量或消化样品的总体积标准化。
[0182]
7.组织学分析
[0183]
将组织在福尔马林中固定12
‑
24小时,包埋在石蜡中并切片。
[0184]
为了检测角膜上皮中的gag含量,对石蜡切片进行了mowry的胶体染色,显示出蓝色的gag。为了检测泪腺和胫骨骨phy生长板中的gag含量,对树脂切片进行了甲苯胺蓝染色,结果显示gag呈白色。
[0185]
使用nis elements advanced research 2.20软件对每只动物的每只眼睛的15
‑
20张图像中的gag+面积百分比(原始放大倍数,
×
40)进行量化,并对所有动物使用相同的信号阈值设置。然后,计算正区域的百分比,即以像素为单位的区域,该区域在图像中感兴趣区域中的整个组织区域中具有正信号。
[0186]
8.透射电子显微镜分析
[0187]
用过量的异氟烷(isoflo,labs.esteve,barcelona,es)处死小鼠,并通过下腔静脉灌注1ml的2.5%戊二醛和2%多聚甲醛。将一小部分(约1mm3)的齿状回和杏仁核切成薄片,并在相同的固定剂中于4℃孵育2小时。在冷的cacodylate缓冲液中洗涤后,将样品后固定在1%osmium tetroxide中,在醋酸铀酰水溶液中染色,然后通过分级乙醇系列脱水并包埋在环氧树脂中。用柠檬酸铅对树脂块的超薄切片进行染色,并在透射电子显微镜(h
‑
7000;日立,东京,日本)中进行检查。
[0188]
9.统计分析
[0189]
所有结果均表示为平均值
±
sem。使用单向方差分析进行统计比较。对照组和治疗组之间使用dunnett的后测进行了多个比较,所有组之间使用tukey的后测进行了比较。如果p<0.05,则认为具有统计学意义。
[0190]
实施例
[0191]
实施例1:paav
‑
cag
‑
hgalns的构建
[0192]
人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的cds(ncbi参考序列:nm_000512.4)用作起始原料,并为此目的进行了化学合成(geneart;life technologies)。接收到克隆在质粒pmk
‑
rq(kanr)内部的cds seq id no:1,所述质粒pmk
‑
rq(kanr)的侧翼分别为5'和3'的mlui和ecori限制性位点。
[0193]
从pmk
‑
rq质粒上切下mlui/ecori人半乳糖胺(n
‑
乙酰基)
‑
6硫酸酯酶cds片段,然后克隆到aav骨架质粒paav
‑
cag的mlui和ecori限制性位点之间。所得质粒命名为paav
‑
cag
‑
hgalns(登录号dsm32791)。参见图1a和seq id no:2。
[0194]
本文所用的aav主链质粒paav
‑
cag已预先产生,并包含aav2基因组的itr、cag启动子和兔β
‑
珠蛋白的polya信号,以及用于克隆目标cds的多克隆位点。cag启动子是由cmv早期/中间增强子和鸡β
‑
肌动蛋白启动子组成的杂种启动子。该启动子能够普遍驱动有效的表达。
[0195]
实施例2:构建paav
‑
cag
‑
ohgalns
‑
v1
[0196]
设计并获得了包括优化版本的半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶cdna序列(ohgalns)的表达盒。通过消除隐含的剪接位点和rna不稳定序列元素以提高rna稳定性,添加rna稳定序列元素,密码子优化和g/c含量适应,避免稳定的rna二级结构等变化,进行序列优化以最大程度地提高人体内半乳糖(n
‑
乙酰基)
‑6‑
硫酸酯酶蛋白的生产效率。人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的cds(ncbi参考序列:nm_000512.4)用作序列优化的起点。
[0197]
将优化的cds seq id no:3(geneart;life technologies)克隆到质粒pmk
‑
rq(kanr)中,该质粒侧翼分别位于5'和3'的mlui和ecori限制性位点。
[0198]
从pmk
‑
rq质粒上切下mlui/ecori优化的人半乳糖胺(n
‑
乙酰基)
‑
6硫酸酯酶cds片段,然后克隆到aav主链质粒paav
‑
cag的mlui和ecori限制性酶切位点之间。所得质粒命名为paav
‑
cag
‑
ohgalns
‑
v1(登录号dsm 32792)。参见图2a和seq id no:4。
[0199]
实施例3:构建paav
‑
cag
‑
ohgalns
‑
v2
[0200]
对人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的cds(ncbi参考序列:nm_000512.4)进行了序列优化(gensript,inc)。将优化的cds seq id no:5克隆到质粒puc57(ampr)中,该质粒侧翼分别位于5'和3'的mlui和ecori限制性位点。
[0201]
从puc57质粒切下mlui/ecori优化的人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶cds片段,随后克隆在aav主链质粒paav
‑
cag的mlui和ecori限制位点之间。所得质粒命名为paav
‑
cag
‑
ohgalns
‑
v2(登录号dsm 32793)。参见图3a和seq id no:6。
[0202]
实施例4:paav
‑
cag
‑
ohgalns
‑
v3的构建
[0203]
对人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的cds(ncbi参考序列:nm_000512.4)进行了序列优化(dna 2.0inc)。将优化的cds seq id no:7克隆到分别位于5'和3'的mlui和ecori限制性位点两侧的质粒pj201(kanr)内部。
[0204]
从pj201质粒上切下mlui/ecori优化的人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶cds片段,然后克隆到aav主链质粒paav
‑
cag的mlui和ecori限制性位点之间。所得质粒命名为paav
‑
cag
‑
ohgalns
‑
v3(登录号dsm 32794)。参见图4a和seq id no:8。
[0205]
实施例5:paav
‑
cag
‑
omgalns的构建
[0206]
对小鼠半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的cds(ncbi参考序列:nm_016722.4)进行了序列优化(geneart;life technologies)。将优化的cds seq id no:9克隆到质粒pma
‑
rq
‑
bb(ampr)中,该质粒侧翼分别位于5'和3'的mlui和ecori限制性位点。
[0207]
从pma
‑
rq
‑
bb质粒上切下mlui/ecori优化的鼠类半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶cds片段,然后克隆到aav主链质粒paav
‑
cag的mlui和ecori限制性酶切位点之间。所得质粒命名为paav
‑
cag
‑
omgalns。参见图5a和seq id no:10。
[0208]
实施例6:paav
‑
haat
‑
omgalns的构建
[0209]
对小鼠半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的cds(ncbi参考序列:nm_016722.4)进行了序列优化(geneart;life technologies)seq id no:9。
[0210]
将haat启动子(seq id no:19)克隆到质粒pgg2
‑
haat(ampr)中,该质粒分别侧接在5'和3'的bglii和mlui限制性位点。
[0211]
从paav
‑
cag
‑
omgalns质粒中切下cag启动子(seq id no:18),随后由haat启动子代替。所得质粒命名为paav
‑
haat
‑
omgalns。参见图6a和seq id no:11。
[0212]
haat启动子是一种杂种启动子,由人α1
‑
抗胰蛋白酶启动子和载脂蛋白e的三个拷贝的肝细胞控制区(hcr)增强子组成。该启动子能够驱动肝脏特异性表达。
[0213]
实施例7:生产aav9
‑
cag
‑
hgalns
[0214]
载体aav9
‑
cag
‑
hgalns(seq id no:12)是通过使用三个修饰的质粒通过无辅助病毒转染hek293细胞而产生的(matsushita等,1998;wright等,2005)。在装有10%fbs的dmem中的滚瓶(rb)(corning,corning,ny,us)中将细胞培养至70%汇合,然后共转染:1)带有表达盒的质粒,该表达盒侧接aav2 itr(paav
‑
cag
‑
hgalns;seq id no:2);2)携带aav2 rep和aav9 cap基因的质粒(prep2cap9);3)具有腺病毒辅助功能的质粒。如前所述(ayuso et al,2010),使用优化方案通过两个连续的氯化铯梯度纯化载体。用pbs+0.001%f68透析载体,过滤,通过qpcr滴定,保存在
‑
80℃直至使用。参见图1b。
[0215]
实施例8:生产aav9
‑
cag
‑
ohgalns
‑
v1
[0216]
使用三个修饰的质粒通过无辅助病毒转染hek293细胞产生了载体aav9
‑
cag
‑
ohgalns
‑
v1(seq id no:13)。(matsushita等,1998;wright等,2005)。将细胞在装有10%fbs的dmem中的滚瓶(rb)(corning,corning,ny,us)中培养至70%汇合,然后共转染:1)带有表达盒的质粒,该表达盒侧接aav2 itr(paav
‑
cag
‑
ohgalns
‑
v1;seq id no:4);2)携带aav2 rep和aav9 cap基因的质粒(prep2cap9);3)具有腺病毒辅助功能的质粒。如前所述(ayuso et al,2010),使用优化方案通过两个连续的氯化铯梯度纯化载体。用pbs+0.001%f68透析载体,过滤,通过qpcr滴定,保存在
‑
80℃直至使用。参见图2b。
[0217]
实施例9:aav9
‑
cag
‑
ohgalns
‑
v2的生产
[0218]
载体aav9
‑
cag
‑
ohgalns
‑
v2(seq id no:14)是通过使用三个具有修饰的质粒通过无辅助病毒转染hek293细胞而产生的。(matsushita等,1998;wright等,2005)。在装有10%fbs的dmem中的滚瓶(rb)(corning,corning,ny,us)中将细胞培养至70%汇合,然后共转染:1)带有表达盒的质粒,该表达盒侧接aav2 itr(paav
‑
cag
‑
ohgalns
‑
v2;seq id no:6);2)携带aav2 rep和aav9 cap基因的质粒(prep2cap9);3)具有腺病毒辅助功能的质粒。如前所述(ayuso et al,2010),使用优化方案通过两个连续的氯化铯梯度纯化载体。用pbs+0.001%f68透析载体,过滤,通过qpcr滴定,保存在
‑
80℃直至使用。参见图3b。
[0219]
实施例10:aav9
‑
cag
‑
ohgalns
‑
v3的生产
[0220]
载体aav9
‑
cag
‑
ohgalns
‑
v3(seq id no:15)通过使用三个修饰的质粒通过hek293
细胞的无辅助病毒转染而产生。(matsushita等,1998;wright等,2005)。在装有10%fbs的dmem中的滚瓶(rb)(corning,corning,ny,us)中将细胞培养至70%汇合,然后共转染:1)带有表达盒的质粒,该表达盒侧接aav2 itr(paav
‑
cag
‑
ohgalns
‑
v3;seq id no:7);2)携带aav2 rep和aav9 cap基因的质粒(prep2cap9);3)具有腺病毒辅助功能的质粒。如前所述(ayuso et al,2010),使用优化方案通过两个连续的氯化铯梯度纯化载体。用pbs+0.001%f68透析载体,过滤,通过qpcr滴定,保存在
‑
80℃直至使用。参见图4b。
[0221]
实施例11:aav9
‑
cag
‑
omgalns的产生
[0222]
载体aav9
‑
cag
‑
omgalns(seq id no:16)是通过使用三个具有修饰的质粒通过无辅助病毒转染hek293细胞而产生的。参见(matsushita等,1998;wright等,2005)。在装有10%fbs的dmem中的滚瓶(rb)(corning,corning,ny,us)中将细胞培养至70%汇合,然后共转染:1)带有表达盒的质粒,该表达盒侧接aav2 itr(paav
‑
cag
‑
omgalns;seq id no:10);2)携带aav2 rep和aav9 cap基因的质粒(prep2cap9);3)具有腺病毒辅助功能的质粒。如前所述(ayuso et al,2010),使用优化方案通过两个连续的氯化铯梯度纯化载体。用pbs+0.001%f68透析载体,过滤,通过qpcr滴定,保存在
‑
80℃直至使用。参见图5b和seq id no:16。
[0223]
实施例12:aav8
‑
cag
‑
omgalns的产生
[0224]
载体aav8
‑
cag
‑
omgalns(seq id no:16)是通过使用三个修饰的质粒通过无辅助病毒转染hek293细胞而产生的。参见(matsushita等,1998;wright等,2005)。在装有10%fbs的dmem中的滚瓶(rb)(corning,corning,ny,us)中将细胞培养至70%汇合,然后共转染:1)带有表达盒的质粒,该表达侧接aav2 itr(paav
‑
cag
‑
omgalns;seq id no:10);2)携带aav2 rep和aav8 cap基因的质粒(prep2cap8);3)具有腺病毒辅助功能的质粒。如前所述(ayuso et al,2010),使用优化方案通过两个连续的氯化铯梯度纯化载体。用pbs+0.001%f68透析载体,过滤,通过qpcr滴定,保存在
‑
80℃直至使用。参见图5b和seq id no:16。
[0225]
实施例13:aav8
‑
haat
‑
omgalns的产生
[0226]
载体aav8
‑
haat
‑
omgalns(seq id no:17)是通过使用三个修饰的质粒通过无辅助病毒转染hek293细胞而产生的。参见(matsushita等,1998;wright等,2005)。在装有10%fbs的dmem中的滚瓶(rb)(corning,corning,ny,us)中将细胞培养至70%汇合,然后共转染:1)带有表达盒的质粒,该表达盒侧接aav2 itr(paav
‑
haat
‑
omgalns;seq id no:11);2)携带aav2 rep和aav8 cap基因的质粒(prep2cap8);3)具有腺病毒辅助功能的质粒。如前所述(ayuso et al,2010),使用优化方案通过两个连续的氯化铯梯度纯化载体。用pbs+0.001%f68透析载体,过滤,通过qpcr滴定,保存在
‑
80℃直至使用。参见图6b和seq id no:17。
[0227]
实施例14:向mpsiva小鼠静脉内注射aav9
‑
cag
‑
hgalns、aav9
‑
cag
‑
ohgalns
‑
v1、aav9
‑
cag
‑
ohgalns
‑
v2或aav9
‑
cag
‑
ohgalns
‑
v3
[0228]
包含不同版本的人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶表达盒的aav9
‑
cag
‑
hgalns、aav9
‑
cag
‑
ohgalns
‑
v1、aav9
‑
cag
‑
ohgalns
‑
v2或aav9
‑
cag
‑
ohgalns
‑
v3的5x10
10
矢量基因组的总剂量通过尾静脉注射向2个月大受mp siva感染的小鼠静脉注射。
[0229]
载体递送后2周进行galns活性分析。与所有四个含半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的载体进行的转导导致半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的活性大大超过在mpsiva动物中测得的水平。半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的活性水平在肝脏中为野生型水平的1500%至2600%,在血清中为野生型的55%至99%。参见图7a和7b。在肝脏中,含有人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶版本2和版本3的表达盒所达到的活性水平高于含有野生型序列的载体介导的表达水平。参见图7a。在血清中,人半乳糖胺(n
‑
乙酰基)
‑6‑
硫酸酯酶的版本2和版本3均比野生型和版本1导致更高的酶活性增加。见图7b。
[0230]
实施例15:将aav9
‑
cag
‑
omgalns,aav8
‑
cag
‑
omgalns或aav8
‑
haat
‑
omgalns静脉内递送至mpsiva小鼠
[0231]
aav9
‑
cag
‑
omgalns的1x10
12
矢量基因组、aav8
‑
cag
‑
omgalns的1x10
12
矢量基因组或aav8
‑
haat
‑
omgalns载体的1x10
11
矢量基因组的总剂量通过3
‑
4周龄mpsiva动物的尾静脉注射,总体积为200μl。施用载体后四和六个月,处死动物并收集样品用于进一步分析。
[0232]
aav处理后六个月,galns在mpsiva处理的动物的肝脏、股骨、脂肪组织和血清中的酶促活性恢复正常,达到与健康动物中观察到的相似或更高的值。参见图8、9和10。galns活性的恢复导致该疾病在肝脏和血清中的底物蓄积特性完全正常化,如野生型对照和经治疗的galns
‑
/
‑
小鼠中相似浓度的硫酸角质素所表明的那样。参见图11。
[0233]
静脉内将不同载体静脉内给药主要在其他组织和器官中转导肝脏(ruzo等,2012)。因此,用不同载体处理的mpsiva雄性小鼠肝脏中的galns活性比健康动物中观察到的高约25倍。参见图8a、9a和10a。
[0234]
当在肝脏中过表达时,可溶性溶酶体蛋白会有效地分泌到血液中,从而使该器官成为循环酶的来源(ruzo等,2012)。在治疗的mpsiva小鼠的血清中,galns活性在注射后3个月左右达到峰值,此后长期稳定,其值比野生型同窝小鼠高20至50倍。参见图8d、9d和10d。通过量化血清和肝脏中gag含量评估该疗法的躯体功效时,观察到循环和肝ks水平完全正常化,见图11。
[0235]
aav传递后四个月,来自mpsiva处理的小鼠的胫骨epiphyseal生长板显示出胞内gag积聚的明显减少,这是由多个胞内gag库的存在所指示的。参见图12。
[0236]
用aav处理的动物还显示出泪腺中gag积累的完全正常化,这是由不存在细胞内gag贮藏所指示的,见图13b。同样,对用mowry胶体染色染色的角膜上皮切片中gag阳性区域的信号强度进行定量分析,揭示了用aav9
‑
cag
‑
omgalns或aav8
‑
haat
‑
omgalns处理的galns
‑
/
‑
小鼠的角膜上皮表面gag沉积的百分比降低了galns缺陷小鼠中记录的值。参见图13a。
[0237]
通过透射电子显微镜对7个月大的雄性小鼠的齿状回和杏仁核进行超微结构分析,发现来自未治疗的galns缺陷小鼠的细胞质中存在含有电致发光物质的大液泡。这些细胞被鉴定为齿状回中的血管周围巨噬细胞或杏仁核中的神经胶质细胞和内皮细胞。这些囊泡似乎是溶酶体,充满了储存物质,在用aav9
‑
cag
‑
omgalns处理的健康野生型或galns
‑
/
‑
动物的样品中完全不存在,从而确认基因转移后溶酶体区室正常大小的恢复。参见图14。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1