基于香豆素的交联剂的制作方法
基于香豆素的交联剂
背景技术:
1.免疫组织化学(ihc)是指使用对特定抗原具有特异性的抗体检测、定位和/或定量生物学样品中的抗原(例如蛋白质)的方法。ihc具有准确鉴定组织样品中特定蛋白质的位点的实质性优点。这也是一种检查组织本身的有效的方法。原位杂交(ish)是指检测、定位和定量核酸的方法。ihc和ish均可用于各种生物学样品,诸如组织(例如新鲜冷冻、福尔马林固定、石蜡包埋)和细胞学样品。无论靶标是核酸还是抗原,均可使用各种标记物(例如,发色、荧光、发光、放射标记)来检测靶标的识别。为了在临床环境中可靠地检测、定位和定量靶标,期望扩增识别事件,因为可靠地检测低丰度细胞标志物的能力对于诊断用途变得越来越重要。例如,响应于单个抗原检测事件,在标志物位点沉积数百个或数千个标记物分子,通过扩增增强了检测识别事件的能力。
2.使用小分子诸如半抗原检测组织抗原和核酸已成为ihc领域的主要方法。半抗原与抗半抗原抗体相结合,可用于检测特定的分子靶标。例如,可以用一种或多种半抗原分子标记特异性结合部分诸如一抗和核酸探针,并且一旦这些特异性结合部分与它们的分子靶标结合,即可使用抗半抗原抗体缀合物对其进行检测,该抗半抗原抗体缀合物包括作为基于发色团的检测系统的一部分的酶或可检测标记物诸如荧光标记。可检测的抗半抗原抗体缀合物与样品的结合表明样品中存在靶标。
3.某些半抗原难以检测,因此通常在半抗原负载中被高估,据信其导致对缀合物浓度的低估。
技术实现要素:
4.在本公开的一个方面,提供了一种由式(ia)或(ib)中的任一者所定义的化合物:
[0005][0006]
其中
[0007]
a和b独立地为反应性官能团、可检测标记物或酶反应部分;
[0008]
l1和l2为连接基;
[0009]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分;
[0010]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0011]
m和n独立地为1至4范围内的整数。
[0012]
在一些实施例中,a和b均为反应性官能团(例如羧酸基团)。在一些实施例中,a为反应性官能团,并且b为可检测标记物。在一些实施例中,可检测标记物为半抗原、发色团或
荧光团。在一些实施例中,b为半抗原。在一些实施例中,半抗原选自下组,该组由以下各项组成:噁唑、吡唑、噻唑、苯并呋咱、三萜烯、脲、除罗丹明硫脲外的硫脲、除二硝基苯基或三硝基苯基外的硝基芳基、类鱼藤酮、环木脂体、杂联芳基、偶氮芳基和苯二氮在一些实施例中,半抗原选自由苯并呋喃半抗原和噻唑磺酰胺半抗原组成的组。在一些实施例中,半抗原选自下组,该组由以下各项组成:5
‑
硝基
‑3‑
吡唑碳酰胺(np)、2
‑
乙酰氨基
‑4‑
甲基
‑5‑
噻唑磺酰胺(ts)、7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
羧酸(dcc)和2,1,3
‑
苯并噁二唑
‑5‑
碳酰胺(bf)。在一些实施例中,a为酶反应部分,该酶反应部分选自由酪酰胺部分、是酪酰胺部分的衍生物的部分和醌甲基化物前体部分组成的组。
[0013]
在一些实施例中,式(ia)或(ib)中任一项所示的化合物具有至少10,000m
‑
1cm
‑
1的消光系数。在其他实施例中,式(ia)或(ib)中任一项所示的化合物具有至少15,000m
‑
1cm
‑
1的消光系数。在其他实施例中,式(ia)或(ib)中任一项所示的化合物具有至少20,000m
‑
1cm
‑
1的消光系数。在进一步的实施例中,式(ia)或(ib)中任一项所示的化合物具有至少25,000m
‑
1cm
‑
1的消光系数。
[0014]
在一些实施例中,酶反应部分具有式(viia)结构:
[0015][0016]
其中每个r
11
基团独立地选自氢或具有在1个与4个之间的碳原子的低级烷基基团,并且其中r
x
为h或c1‑
c4烷基基团。
[0017]
在一些实施例中,酶反应部分具有式(viiia)所提供的结构:
[0018][0019]
其中
[0020]
r2为选自磷酸酯、酰胺、硝基、脲、硫酸酯、甲基、酯、β
‑
内酰胺或糖的基团;
[0021]
r
13
为卤化物;
[0022]
r
15
、r
16
、r
17
和r
18
独立地选自氢或具有在1个与4个之间的碳原子的脂族基团;并且
[0023]
r
14
为
‑
(ch2)
w
nh
‑
、
‑
o(ch2)
w
nh
‑
、
‑
n(h)c(o)(ch2)
w
nh
‑
、
‑
c(o)n(h)(ch2)
w
nh
‑
、
‑
(ch2)
w
o
‑
、
‑
o(ch2)
w
o
‑
、
‑
o(ch2ch2o)
w
‑
、
‑
n(h)c(o)(ch2)
w
o
‑
、
‑
c(o)n(h)(ch2)
w
o
‑
、
‑
c(o)n(h)(ch2ch2o)
w
‑
、
‑
(ch2)
w
s
‑
、
‑
o(ch2)
w
s
‑
、
‑
n(h)c(o)(ch2)
w
s
‑
、
‑
c(o)n(h)(ch2)
w
s
‑
、
‑
(ch2)
w
nh
‑
、
‑
c(o)n(h)(ch2ch2o)
w
ch2ch2nh、
‑
c(o)(ch2ch2o)
w
ch2ch2nh
‑
、
‑
c(o)n(h)(ch2)nhc(o)ch(ch3)(ch2)
w
nh
‑
或
‑
n(h)(ch2)
w
nh
‑
,其中w为1至12范围内的整数。
[0024]
在一些实施例中,b为能够参与点击化学反应的反应性基团(例如叠氮化物基团)。
在一些实施例中,能够参与点击化学反应的基团为dbco基团、叠氮化物基团、tco基团、烯烃基团或四嗪基团。
[0025]
在一些实施例中,w具有式(iva)或(ivb)结构:
[0026][0027]
其中q为键或者取代或未取代的直链或支化c1‑
c
16
烷基基团、
‑
[(ch2ch2)
j
‑
o]
k
‑
ch2‑
、
‑
[(ch2)
j
‑
o]
k
‑
ch2‑
,其中j为1至4范围内的整数并且k为1至16范围内的整数;
‑
n
‑
r
x
‑
;
‑
c(o)
‑
n
‑
r
x
‑
;或
‑
n
‑
r
x
‑
c(o)
‑
,r
x
为h或c1‑
c4烷基基团;并且y为取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分。在一些实施例中,其中取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分包括选自下组的一个或多个部分,该组由以下各项组成:取代或未取代的直链或支化c1‑
c6烷基基团;取代或未取代的直链或支化c1‑
c6烷氧基基团;取代或未取代的直链或支化c1‑
c6杂烷基基团;三氟甲基基团;羟基基团;硫酸酯基团;氰基基团;卤素;磷酸酯基团;糖基;羧酸基团;硝基基团;
‑
c(o)nr
x
r
y
;
‑
s
‑
r
x
;
‑
so2;
‑
so2cl;
‑
so3h;
‑
so4h;
‑
so2nr
x
r
y
;
‑
n(h)
‑
nr
x
r
y
;和
‑
nr
x
r
y
;并且其中r
x
和r
y
独立地为h或c1‑
c4烷基基团。
[0028]
在一些实施例中,w具有式(va)或(vb)结构:
[0029][0030]
其中所述式(va)部分可被0个、1个、2个、3个或4个r
t
基团取代;并且其中所述式(vb)化合物可被0个、1个、2个、3个、4个或5个r
t
基团取代;并且其中每个r
t
独立地选自取代或未取代的直链或支化c1‑
c
12
烷基基团;取代或未取代的直链或支化c1‑
c
12
烷氧基基团;取代或未取代的直链或支化c1‑
c
12
杂烷基基团;三氟甲基基团;羟基基团;硫酸酯基团;氰基基团;卤素;磷酸酯基团;糖;羧酸基团;硝基基团;
‑
c(o)nr
x
r
y
;
‑
s
‑
r
x
;
‑
so2;
‑
so2cl;
‑
so3h;
‑
so4h;
‑
so2nr
x
r
y
;
‑
n(h)
‑
nr
x
r
y
;
‑
nr
x
r
y
;并且其中r
x
和r
y
独立地为h或c1‑
c4烷基基团;
[0031]
r1为c1‑
c
10
取代或未取代的支化或非支化烷基基团、
‑
o
‑
、
‑
o
‑
ch2‑
、
‑
n(r
x
)
‑
或
‑
s
‑
;
[0032]
r5为c1‑
c
10
取代或未取代的支化或非支化烷基基团、
‑
c(o)
‑
o
‑
、
‑
c(o)
‑
n(h)
‑
;并且
[0033]
每个x独立地为键或者取代或未取代的直链或支化c1‑
c
16
烷基基团;
‑
[(ch2)
j
‑
o]
k
‑
ch2‑
,其中j为1至4范围内的整数,并且k为1至16范围内的整数;
‑
n
‑
r
x
‑
;
‑
c(o)
‑
n
‑
r
x
‑
;或
‑
n
‑
r
x
‑
c(o)
‑
,其中r
x
为h或c1‑
c4烷基基团。
[0034]
在一些实施例中,w具有式(vc)或(vd)结构:
[0035][0036]
其中
[0037]
r2、r3、r4、r6和r7独立地选自取代或未取代的直链或支化c1‑
c6烷基基团;取代或未取代的直链或支化c1‑
c6烷氧基基团;取代或未取代的直链或支化c1‑
c6杂烷基基团;三氟甲基基团;羟基基团;硫酸酯基团;氰基基团;卤素;磷酸酯基团;糖;羧酸基团;硝基基团;
‑
c(o)nr
x
r
y
;
‑
s
‑
r
x
;
‑
so2;
‑
so2cl;
‑
so3h;
‑
so4h;
‑
so2nr
x
r
y
;
‑
n(h)
‑
nr
x
r
y
;
‑
nr
x
r
y
;
[0038]
r5为c1‑
c
10
取代或未取代的支化或非支化烷基基团、
‑
c(o)
‑
o
‑
、
‑
c(o)
‑
n(h)
‑
;
[0039]
r1为c1‑
c
10
取代或未取代的支化或非支化烷基基团、
‑
o
‑
、
‑
o
‑
ch2‑
、
‑
n(r
x
)
‑
或
‑
s
‑
;并且
[0040]
每个x独立地为键或者取代或未取代的直链或支化c1‑
c
16
烷基基团;
‑
[(ch2)
j
‑
o]
k
‑
ch2‑
,其中j为1至4范围内的整数,并且k为1至16范围内的整数;
‑
n
‑
r
x
‑
;
‑
c(o)
‑
n
‑
r
x
‑
;或
‑
n
‑
r
x
‑
c(o)
‑
;并且
[0041]
其中每个r
x
和r
y
独立地为h或c1‑
c4烷基基团。
[0042]
在一些实施例中,每个l1和/或l2基团独立地具有式(via):
[0043][0044]
其中
[0045]
f为0或1至24范围内的整数;
[0046]
j为1至24范围内的整数;
[0047]
r8为键或者o、s、
‑
n(r
c
)(r
d
)或
‑
n
+
(r
c
)(r
d
)(r
e
);
[0048]
r
a
和r
b
独立地为h、c1‑
c4烷基基团、f、cl或
‑
n(r
c
)(r
d
);
[0049]
r
c
、r
d
和r
e
独立地选自h或c1‑
c4烷基基团;并且
[0050]
r9和r
10
独立地为键或基团,所述基团具有多至6个碳原子并且包括羰基、酰胺、酰亚胺、酯、醚、胺、硫酮或硫醇。
[0051]
在本公开的另一方面,提供了一种由式(ixa)或(ixb)中的任一者所定义的化合物:
[0052][0053][0054]
其中
[0055]
t为取代基,其选自特异性结合实体、氨基酸、肽、蛋白质、糖、核苷、核苷酸、寡核苷酸、药物、脂质或纳米颗粒;
[0056]
r
z
为可检测标记物;
[0057]
o为1至10范围内的整数;
[0058]
l1和l2为连接基;
[0059]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分;
[0060]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0061]
m和n独立地为1至4范围内的整数。
[0062]
在一些实施例中,t为抗体。在一些实施例中,抗体为一抗。在一些实施例中,抗体为二抗。在一些实施例中,t为核酸。在一些实施例中,r
z
为半抗原。在一些实施例中,r
z
为酶。在一些实施例中,酶选自由过氧化物酶和磷酸酶组成的组。
[0063]
在一些实施例中,w具有式(vc)或(vd)结构:
[0064][0065]
其中
[0066]
r2、r3、r4、r6和r7独立地选自取代或未取代的直链或支化c1‑
c6烷基基团;取代或未取代的直链或支化c1‑
c6烷氧基基团;取代或未取代的直链或支化c1‑
c6杂烷基基团;三氟甲基基团;羟基基团;硫酸酯基团;氰基基团;卤素;磷酸酯基团;糖;羧酸基团;硝基基团;
‑
c(o)nr
x
r
y
;
‑
s
‑
r
x
;
‑
so2;
‑
so2cl;
‑
so3h;
‑
so4h;
‑
so2nr
x
r
y
;
‑
n(h)
‑
nr
x
r
y
;
‑
nr
x
r
y
;
[0067]
r5为c1‑
c
10
取代或未取代的支化或非支化烷基基团、
‑
c(o)
‑
o
‑
、
‑
c(o)
‑
n(h)
‑
;
[0068]
r1为c1‑
c
10
取代或未取代的支化或非支化烷基基团、
‑
o
‑
、
‑
o
‑
ch2‑
、
‑
n(r
x
)
‑
或
‑
s
‑
;并且
[0069]
每个x独立地为键或者取代或未取代的直链或支化c1‑
c
16
烷基基团;
‑
[(ch2)
j
‑
o]
k
‑
ch2‑
,其中j为1至4范围内的整数,并且k为1至16范围内的整数;
‑
n
‑
r
x
‑
;
‑
c(o)
‑
n
‑
r
x
‑
;或
‑
n
‑
r
x
‑
c(o)
‑
;并且
[0070]
其中每个r
x
和r
y
独立地为h或c1‑
c4烷基基团。
[0071]
在一些实施例中,每个l1和/或l2基团独立地具有式(via):
[0072][0073]
其中
[0074]
f为0或1至24范围内的整数;
[0075]
j为1至24范围内的整数;
[0076]
r8为键或者o、s、
‑
n(r
c
)(r
d
)或
‑
n
+
(r
c
)(r
d
)(r
e
);
[0077]
r
a
和r
b
独立地为h、c1‑
c4烷基基团、f、cl或
‑
n(r
c
)(r
d
);
[0078]
r
c
、r
d
和r
e
独立地选自h或c1‑
c4烷基基团;并且
[0079]
r9和r
10
独立地为键或基团,所述基团具有多至6个碳原子并且包括羰基、酰胺、酰亚胺、酯、醚、胺、硫酮或硫醇。
[0080]
在本公开的另一方面提供了一种检测生物学样品内的一种或多种靶标的方法,该方法包括:(a)用一抗标记样品,该一抗对生物学样品中的靶标中的一种具有特异性;(b)使样品与式(ixc)或(ixd)中任一项所示的化合物接触:
[0081][0082]
其中
[0083]
ab为二抗;
[0084]
r
z
为可检测标记物;
[0085]
o为1至10范围内的整数;
[0086]
l1和l2为连接基;
[0087]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分;
[0088]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0089]
m和n独立地为1至4范围内的整数;以及
[0090]
(c)使样品与一种或多种试剂接触以检测可检测标记物r
z
。
[0091]
在一些实施例中,ab为抗一抗抗体。在一些实施例中,一抗缀合至半抗原,并且其中ab为抗半抗原抗体。
[0092]
在本公开的另一方面提供了一种检测生物学样品内的一种或多种靶标的方法,该方法包括:(a)通过使样品与缀合物接触,用酶标记样品,该缀合物包含酶和对生物学样品中的靶标中的一者具有特异性的一抗;(b)使样品与式(ia)或(ib)中任一项所示的化合物接触:
[0093][0094][0095]
其中
[0096]
a为酶反应部分;
[0097]
b为可检测标记物;
[0098]
l1和l2为连接基;
[0099]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分;
[0100]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0101]
m和n独立地为1至4范围内的整数;以及
[0102]
(c)使样品与一种或多种试剂接触以检测可检测标记物b。
[0103]
在一些实施例中,式(ia)或(ib)中任一项所示的化合物具有至少10,000m
‑
1cm
‑
1的消光系数。在其他实施例中,式(ia)或(ib)中任一项所示的化合物具有至少15,000m
‑
1cm
‑
1的消光系数。在其他实施例中,式(ia)或(ib)中任一项所示的化合物具有至少20,000m
‑
1cm
‑
1的消光系数。在进一步的实施例中,式(ia)或(ib)中任一项所示的化合物具有至少25,000m
‑
1cm
‑
1的消光系数。
[0104]
在一些实施例中,w具有式(vc)或(vd)结构:
[0105][0106]
其中
[0107]
r2、r3、r4、r6和r7独立地选自取代或未取代的直链或支化c1‑
c6烷基基团;取代或未取代的直链或支化c1‑
c6烷氧基基团;取代或未取代的直链或支化c1‑
c6杂烷基基团;三氟甲基基团;羟基基团;硫酸酯基团;氰基基团;卤素;磷酸酯基团;糖;羧酸基团;硝基基团;
‑
c(o)nr
x
r
y
;
‑
s
‑
r
x
;
‑
so2;
‑
so2cl;
‑
so3h;
‑
so4h;
‑
so2nr
x
r
y
;
‑
n(h)
‑
nr
x
r
y
;
‑
nr
x
r
y
;
[0108]
r5为c1‑
c
10
取代或未取代的支化或非支化烷基基团、
‑
c(o)
‑
o
‑
、
‑
c(o)
‑
n(h)
‑
;
[0109]
r1为c1‑
c
10
取代或未取代的支化或非支化烷基基团、
‑
o
‑
、
‑
o
‑
ch2‑
、
‑
n(r
x
)
‑
或
‑
s
‑
;并且
[0110]
每个x独立地为键或者取代或未取代的直链或支化c1‑
c
16
烷基基团;
‑
[(ch2)
j
‑
o]
k
‑
ch2‑
,其中j为1至4范围内的整数,并且k为1至16范围内的整数;
‑
n
‑
r
x
‑
;
‑
c(o)
‑
n
‑
r
x
‑
;或
‑
n
‑
r
x
‑
c(o)
‑
;并且
[0111]
其中每个r
x
和r
y
独立地为h或c1‑
c4烷基基团。
附图说明
[0112]
有关对本公开特征的一般理解,请参考附图。在附图中,整个附图使用相同的附图标记来识别相同的元素。
[0113]
图1示出用缀合至核酸探针的基于香豆素的化合物对样品染色,其中基于香豆素的化合物偶联至地高辛(“dig”),并且其中dig可通过应用本领域中已知的合适的检测试剂进行检测。
[0114]
图2示出用基于香豆素的缀合物对样品染色,其中基于香豆素的缀合物包含山羊抗兔抗体和dig半抗原。其中,使用对pd
‑
l1具有特异性的一抗标记两个扁桃体组织样品,然后引入基于香豆素的缀合物,以使用dig标记样品内的靶标。然后,通过引入偶联至过氧化物酶的抗dig抗体来检测dig,该过氧化物酶作用于引入的3,3
′‑
二氨基联苯胺(“dab”)。
[0115]
图3示出用基于香豆素的缀合物对样品染色,其中基于香豆素的缀合物包含山羊抗兔抗体和dig半抗原。其中,使用对雌激素受体(er)、孕激素受体(pr)、her2和ki67具有特异性的一抗标记两个扁桃体组织样品,然后引入基于香豆素的缀合物,以使用dig标记样品内的靶标。然后,通过引入偶联至过氧化物酶的抗dig抗体来检测dig,该过氧化物酶作用于引入的3,3
′‑
二氨基联苯胺(“dab”)。
[0116]
图4阐述了流程图,其示出根据一些实施例的多重检测策略的步骤。
[0117]
图5示出具有偶联至酪酰胺部分和半抗原的具有式(iiia)、(iiib)、(iiic)和(iiid)中的任一项的基于香豆素的部分的用途,并且比较了对那些直接偶联至dig的酪酰胺部分的染色性能。
[0118]
图6提供了一种将蛋白质共价固定化在ar2g生物传感器上以及随后的结合分析物的方案。在活化、固定化和淬灭后,测量固定化的配体与分析物之间缔合和解离的动力学。
[0119]
图7阐述了使用如上所示的bsa
‑
cl
‑
bf免疫原的小鼠抗半抗原抗体缔合和解离步骤的代表性交叉反应筛选过程。图中显示了ms抗bf mab(h1,h6)、ms抗ppt mab(c1,c6)和ms抗dabsyl mab(d1,d6)识别。未观察到与抗ppt或抗dabsyl mab之间的明显的相互作用。
[0120]
图8阐述了使用如上所示的bsa
‑
cl
‑
bf免疫原的小鼠抗半抗原抗体缔合和解离步骤的代表性交叉反应筛选过程。ms抗np mab(b1,b6;c1,c6)和ms抗ts mab(h1,h6;g1,g6)bsa
‑
clbf识别如上所示。
[0121]
图9阐述了使用如上所示的bsa
‑
cl
‑
bf免疫原的小鼠抗半抗原抗体缔合和解离步骤的代表性交叉反应筛选过程。ms抗nca mab(b1,b6;c1,c6)和ms抗hq mab(h1,h6;g1,g6)bsa
‑
clbf识别如上所示。
[0122]
图10阐述了使用如上所示的bsa
‑
cl
‑
bf免疫原的小鼠抗半抗原抗体缔合和解离步骤的代表性交叉反应筛选过程。ms抗dcc mab(b1,b6;d1,d6)和ms抗rot mab(f1,f6;g1,g6)bsa
‑
clbf识别如上所示。
[0123]
图11阐述了使用如上所示的bsa
‑
cl
‑
bf免疫原的小鼠抗半抗原抗体缔合和解离步骤的代表性交叉反应筛选过程。ms抗dig mab(b1,b6;c1,c6)和ms抗dnp mab(f1,f6;g1,g6)bsa
‑
clbf识别如上所示。
[0124]
图12阐述了使用如上所示的bsa
‑
cl
‑
bf免疫原的小鼠抗半抗原抗体缔合和解离步
骤的代表性交叉反应筛选过程。ms抗bd mab(c1,c6;d1,d6)和ms抗dnp mab(f1,f6;g1,g6)bsa
‑
clbf识别如上所示。
[0125]
图13阐述了支化发色团连接基gar
‑
lys(dcc)dpeg8ts(化合物a)和gar
‑
dpeg4
‑
lys(dcc)dpeg8ts(化合物b)。
[0126]
图14阐述了使用rb mab固定化(600
‑
1800s)、gar
‑
rb识别(2400
‑
4200s)和抗ts标记识别(6000
‑
7800s)获得所示的bli elisa测定曲线。图中显示了gar
‑
lys(dcc)dpeg8ts缀合物(d1,c1)、gar
‑
dpeg4
‑
lys(dcc)dpeg8ts缀合物(f1,e1)和未修饰的gar pab(g1,h1)识别。
[0127]
图15阐述了bli elisa测定曲线,显示了gar
‑
rb识别(2400
‑
4200s)以及随后的解离(4200
‑
6000s)。图中显示了gar
‑
lys(dcc)dpeg8ts缀合物(c1,c6;d1,d6)、gar
‑
dpeg4
‑
lys(dcc)dpeg8ts缀合物(f1,f6;e1,e6)和未修饰的gar pab(h1,h6;g1,g6)rb mab识别。
[0128]
图16阐述了bli elisa测定曲线,显示了ts
‑
半抗原标记的ms抗ts mab识别(6000
‑
7800s)以及随后的ab解离(7800
‑
8800s)。图中显示了gar
‑
lys(dcc)dpeg8ts缀合物(c1,c8;d1,d8)、gar
‑
dpeg4
‑
lys(dcc)dpeg8ts缀合物(e1,e8;f1,f8)和未修饰的gar pab(g1,g8;h1,h8)。
[0129]
图17阐述了使用rb mab固定化(600
‑
1800s)、gar
‑
rb识别(2400
‑
4200s)和抗bf标记识别(6000
‑
7800s)获得所示的bli elisa测定曲线。图中显示了gar
‑
dpeg8bf缀合物(g1,b1)和gar
‑
clbf缀合物(黄色,蓝绿色)。显示了未经rb mab固定化的阴性对照传感器(e1,a1)。
[0130]
图18阐述了bli elisa测定曲线,显示了gar
‑
rb识别(2400
‑
4200s)以及随后的解离(4200
‑
6000s)。图中显示了gar
‑
dpeg8bf缀合物(b1,b6;g1,g6)和gar
‑
clbf缀合物(a1,a8;e1,e8)。
[0131]
图19阐述了bli elisa测定曲线,显示了bf
‑
半抗原标记的ms抗bf mab识别(6000
‑
7800s)以及随后的ab解离(7800
‑
8800s)。图中显示了gar
‑
dpeg8bf缀合物(b1,b8;g1,g8)和gar
‑
clbf缀合物(a1,a8;e1,e8)。
[0132]
图20示出生物蛋白的标记试剂的实例,这些标记试剂可包括但不限于马来酰亚胺、nhs酯、酰肼和乙基氰胺。
[0133]
图21示出本公开的基于香豆素的缀合物的吸收光谱。
[0134]
图22示出本公开的基于香豆素的缀合物的吸收光谱。
[0135]
图23列出一个表格,其中提供了波长为280nm和346nm处的吸收光谱比。
[0136]
图24示出了根据本公开的图23的三种基于香豆素的缀合物的体积排阻色谱图。
具体实施方式
[0137]
还应该理解的是,除非指明是相反情况,否则在本文所要求保护的包括一个以上步骤或动作的任何方法中,所述方法的所述步骤或动作的顺序不必限于表述所述方法的所述步骤或动作的所述顺序。
[0138]
如本文所用,除非上下文另有明确指示,否则单数形式“一(a/an)”和“该/所述”包括复数个指代物。同样,除非上下文另有明确指示,否则词语“或”旨在包括“和”。术语“包括”定义为包容性,如“包括a或b”是指包括a、b或a和b。
[0139]
如本文在说明书和权利要求书中所用,“或”应理解为与上文定义的“和/或”具有相同的含义。例如,在分隔列表中的项目时,“或”或“和/或”应解释为具有包容性,即包含若干元素或元素列表中的至少一个元素,但也包含一个以上元素,以及可选地包含额外的未列出的项目。只有指明与之相反的术语,如“只有一个”或“恰好一个”,或者在权利要求中使用的“由...组成”,将指包含若干元素或元素列表中的恰好一个元素。一般来说,本文使用的术语“或者”只有在前面有“或”、“其中之一”、“只有一个”或“恰好一个”等排他性术语时,才应解释为表示排他性的替代选择(即“一个或另一个,但不是两个”)。在权利要求书中使用的“基本上由...组成”应具有在专利法领域使用的普通含义。
[0140]“包括”、“包含”、“具有”等术语可互换使用,且含义相同。同样,“包括”、“包含”、“具有”等可互换使用,且含义相同。具体而言,每个术语的定义都与普通美国专利法对“包括”的定义一致,因此每个术语都可理解为一个开放性术语,其含义为“至少以下”,并且也可理释为不排除额外的特征、限制、方面等。因此,例如“具有组件a、b和c的装置”是指所述装置至少包括组件a、b和c。同样,短语:“涉及步骤a、b和c的方法”是指所述方法至少包括步骤a、b和c。此外,尽管本文可以特定的顺序概述步骤和过程,但是本领域技术人员将认识到,所述顺序步骤和过程可能会有所不同。
[0141]
如本文在说明书和权利要求书中所用,就一个或多个元素的列表而言,短语“至少一个”应理解为选自元素列表中任何一个或多个元素的至少一个元素,但不一定包括元素列表中具体列出的每个元素中的至少一个,也不排除元素列表中的任何元素组合。除了在短语“至少一个”所涉及的元素列表中具体确定的元素之外,该定义还允许其他元素可选地存在,无论这些元素与具体确定的元素相关与否。因此,作为一个非限制性实例,“a和b中的至少一个”(或者等效地,“a或b中的至少一个”,或者等效地,“a和/或b中的至少一个”)在一个实施例中可以指至少一个可选地包括一个以上的a,但没有b(以及选择性地包括b以外的元素);在另一个实施例中,指至少一个选择性地包括一个以上的b,但没有a(以及选择性地包括a以外的元素);在又一个实施例中,指至少一个选择性地包括一个以上的a,以及至少一个选择性地包括一个以上的b(以及选择性地包括其他元素)等。
[0142]“类似物”或“衍生物”根据其在化学与生物学领域的一般含义使用,是指在结构上与另一种化合物(即所谓的“参比”化合物)相似但组成有所不同(例如,一个原子被不同元素的原子替代,或存在特定的官能团,或一种官能团被另一官能团替代,或与参比化合物的一个或多个手性中心的绝对立体化学结构不同)的化合物。因此,类似物是功能和外观与参比化合物相似或相当但结构或来源不同的化合物。
[0143]
除非另有说明,否则术语“烷基”本身或作为另一取代基的一部分是指直链(即,非支化)或支化链或其组合,其可以是完全饱和、单不饱和或多不饱和基团,并且可包括具有指定碳原子数(即,c1‑
c
10
意指1至10个碳)的二价和多价基团。“烷基”未环化。饱和烃基基团的实例包括但不限于甲基、乙基、正丙基、异丙基、正丁基、叔丁基、异丁基、仲丁基、(环己基)甲基以及例如正戊基、正己基、正庚基、正辛基的同系物和异构体等。不饱和烷基基团是具有一个或多个双键或三键的烷基基团。不饱和烷基基团的实例包括但不限于乙烯基、2
‑
丙烯基、巴豆基、2
‑
异戊烯基、2
‑
(丁二烯基)、2,4
‑
戊二烯基、3
‑
(1,4
‑
戊二烯基)、乙炔基、1
‑
丙炔基和3
‑
丙炔基、3
‑
丁炔基以及高级同系物和异构体。烷氧基是通过氧连接基(
‑
o
‑
)连接至分子其余部分的烷基。
[0144]
除非另有说明,否则术语“亚烷基”本身或作为另一取代基的一部分是指衍生自烷基的二价基团,例如但不限于
‑
ch2ch2ch2ch2‑
。通常,烷基(或亚烷基)基团将具有1个至24个碳原子,在本发明中优选那些具有10个或更少碳原子数的基团。“低级烷基”或“低级亚烷基”为短链烷基或亚烷基基团,其通常具有8个或更少的碳原子。
[0145]
除非另有说明,否则术语“杂烷基”本身或与另一术语结合使用时是指由至少一个碳原子和至少一个杂原子组成的稳定的直链或支化链,所述至少一个杂原子选自由o、n、p、si和s组成的组,并且其中氮和硫原子可任选地发生氧化,并且氮杂原子可任选地发生季铵化。杂原子o、n、p、s和si可位于杂烷基基团的任何内部位置,或位于烷基基团与分子其余部分相连的位置。杂烷基是未环化的。实例包括但不限于:
‑
ch2‑
ch2‑
o
‑
ch3、
‑
ch2‑
ch2‑
nh
‑
ch3、
‑
ch2‑
ch2‑
n(ch3)
‑
ch3、
‑
ch2‑
s
‑
ch2‑
ch3、
‑
ch2‑
ch2、
‑
s(o)
‑
ch3、
‑
ch2‑
ch2‑
s(o)2‑
ch3、
‑
ch=ch
‑
o
‑
ch3、
‑
si(ch3)3、
‑
ch2‑
ch=n
‑
och3、
‑
ch=ch
‑
n(ch3)
‑
ch3、
‑
o
‑
ch3、
‑
o
‑
ch2‑
ch3和
‑
cn。至多两个杂原子可以是连续的,例如
‑
ch2‑
nh
‑
och3。
[0146]
除非另有说明,否则术语“环烷基”和“杂环烷基”本身或与其他术语结合使用时分别表示“烷基”和“杂烷基”的环状形式。环烷基和杂环烷基是非芳族基团。
[0147]
上述术语(例如,“烷基”、“杂烷基”、“环烷基”等)中的每一个均包括所示自由基的取代和未取代形式。
[0148]
烷基和杂烷基自由基(包括那些通常称为亚烷基、烯基、杂亚烷基、杂烯基、炔基、环烷基、杂环烷基、环烯基和杂环烯基的基团)的取代基可为选自但不限于以下基团的各种基团中的一者或多者:
‑
or
′
、=o、=nr
′
、=n
‑
or
′
、
‑
nr
′
r
‑
sr
′
、
‑
卤素、
‑
sir
′
r
″
r
″′
、
‑
oc(o)r
′
、
‑
c(o)r
′
、
‑
co2r
′
、
‑
conr
′
r
″
、
‑
oc(o)nr
′
r
″
、
‑
nr
″
c(o)r
′
、
‑
nr
′‑
c(o)nr
″
r
″′
、
‑
nr
″
c(o)2r
′
、
‑
nr
‑
c(nr
′
r
″
r
″′
)=nr
″″
、
‑
nr
‑
c(nr
′
r
″
)=nr
″′
、
‑
s(o)r
′
、
‑
s(o)2r
′
、
‑
s(o)2nr
′
r
″
、
‑
nrso2r
′
、
‑
cn和
‑
no2,其数量在0至(2m
′
+1)的范围内,其中m
′
为此类自由基中的碳原子总数。r
′
、r
″
、r
″′
和r
″″
各自优选独立地是指氢、取代或未取代的杂烷基、取代或未取代的环烷基、取代或未取代的杂环烷基、取代或未取代的芳基(例如,被1
‑
3个卤素原子取代的芳基)、取代或未取代的烷基、烷氧基或硫代烷氧基基团或芳烷基基团。例如,当本发明的化合物包含一个以上的r基团时,每个r基团独立地选择为各个r
′
、r
″
、r
″′
和r
″″
基团(当这些基团中的一个以上的基团存在时)。当r
′
和r
″
连接至相同的氮原子时,它们可以与氮原子结合以形成4元环、5元环、6元环或7元环。例如,
‑
nr
′
r
″
包括但不限于1
‑
吡咯烷基和4
‑
吗啉基。根据有关取代基的上述讨论,本领域的技术人员将理解,术语“烷基”意指包括这样的基团,其包括与除氢基团以外的基团结合的碳原子,例如卤代烷基(例如,
‑
cf3和
‑
ch2cf3)和酰基(例如,
‑
c(o)ch3、
‑
c(o)cf3、
‑
c(o)ch2och3等)。
[0149]
如本文所用,术语“抗体”是指免疫球蛋白或免疫球蛋白样分子,包括(例如)但不限于:iga、igd、ige、igg和igm及其组合;在任何脊椎动物(例如,在哺乳动物诸如人类、山羊、兔和小鼠等中)的免疫应答过程中产生的类似分子;以及特异性结合至目标分子(或一组高度相似的目标分子)并且基本上排除与其他分子的结合的抗体片段。“抗体”进一步是指至少包含轻链或重链免疫球蛋白可变区的多肽配体,其特异性识别并结合抗原的表位。抗体可由重链和轻链组成,每条重链和轻链均具有可变区,称为可变重链(vh)区和可变轻链(vl)区。vh区和vl区共同负责结合由抗体识别的抗原。术语“抗体”还包括本领域中熟知的完整免疫球蛋白及其变体和部分。
[0150]
如本文所用,术语“生物学样品”、“组织样品”、“标本”或类似的术语是指从包括病毒在内的任何生物体中获得的包括生物分子(例如蛋白质、肽、核酸、脂质、碳水化合物或其组合)在内的任何样品。其他生物体的实例包括哺乳动物(例如人类;兽类动物,如猫、狗、马、牛和猪;以及实验室动物,如小鼠、大鼠和灵长类动物)、昆虫、环节动物、蛛形纲动物、有袋类动物、爬行类动物、两栖类动物、细菌和真菌。生物学样品包括组织样品(例如组织切片和组织的穿刺活检)、细胞样品(例如细胞学涂片,如子宫颈涂片或血液涂片或通过显微解剖获得),或细胞馏分、碎片或细胞器(例如通过裂解细胞并通过离心或其他方式分离其组分获得)。生物学样品的其他实例包括血液、血清、尿液、精液、粪便、脑脊液、间质液、粘液、眼泪、汗液、脓液、活检组织(例如,通过手术活检或穿刺活检获得)、乳头抽吸物、耵聍、乳汁、阴道分泌物、唾液、拭子(例如口腔拭子)、或任何含有生物分子且从第一生物学样品导出的材料。在某些实施例中,本文使用的术语“生物学样品”是指从受试者获得的肿瘤或其一部分制备的样品(例如经均质或液化处理的样品)。
[0151]
如本文所用,术语“缀合物”是指共价连接至较大构建体的两个或更多个分子或部分(包括大分子或超分子)。在一些实施例中,缀合物包括共价连接至一个或多个其他分子部分的一种或多种生物分子(诸如肽、蛋白质、酶、糖、多糖、脂质、糖蛋白和脂蛋白)。
[0152]
如本文所用,术语“香豆素”是指荧光衍生剂。如本文所用,香豆素包括其衍生物,诸如卤素取代的香豆素(例如氯代香豆素、氟代香豆素、溴代香豆素及其衍生物)、羟基香豆素及其衍生物(包括伞形酮及其衍生物)、氰基香豆素及其衍生物、甲基香豆素及其衍生物、乙氧基香豆素及其衍生物、苯并香豆素及其衍生物、苯基香豆素及其衍生物、乙酰香豆素及其衍生物以及它们的羧化衍生物和琥珀酰亚胺酯。上述衍生物并非限制性的,仅作为示例提供。
[0153]
如本文所用,术语“偶联”是指一个分子或原子与另一分子或原子的结合、键合(例如共价键合)或连接。
[0154]
除非另有说明,否则术语“卤代”或“卤素”本身或作为另一取代基的一部分是指氟、氯、溴或碘原子。另外,术语“卤代烷基”意指包括单卤代烷基和多卤代烷基。例如,术语“卤代(c1‑
c4)烷基”包括但不限于氟甲基、二氟甲基、三氟甲基、2,2,2
‑
三氟乙基、4
‑
氯丁基、3
‑
溴丙基等。
[0155]
如本文所用,“半抗原”是可与抗体特异性结合的小分子,但是除与载体分子结合外,通常基本上不能具有免疫原性。
[0156]
如本文所用,术语“杂原子”或“环杂原子”是指包括硼(b)、氧(o)、氮(n)、硫(s)、磷(p)和硅(si)。
[0157]
如本文所用,“低级取代基”或“低级取代基团”意指选自上文针对“取代基”所述的所有取代基中的基团,其中每个取代或未取代的烷基为取代或未取代的c1‑
c8烷基,每个取代或未取代的杂烷基为取代或未取代的2元至8元杂烷基,每个取代或未取代的环烷基为取代或未取代的c5‑
c7环烷基,并且每个取代或未取代的杂环烷基为取代或未取代的5元至7元杂环烷基。
[0158]
如本文所用,术语“一抗”是指与组织样品中的靶蛋白抗原特异性结合的抗体。一抗通常是免疫组织化学程序中使用的第一抗体。
[0159]
如本文所用,术语“反应性基团”或“反应性官能团”意指能够与不同部分的官能团
化学反应以形成共价键的官能团。
[0160]
如本文所用,术语“二抗”在本文中是指与一抗特异性结合,从而在一抗与随后的试剂(如有的话,例如标记物、酶等)之间形成桥的抗体。二抗通常是免疫组织化学程序中使用的第二抗体。
[0161]
如本文所用,术语“特异性结合实体”是指特异性结合对的成员。特异性结合对是特征在于彼此结合以实质性地排除与其他分子结合的分子对(例如,特异性结合对的结合常数可以比生物学样品中其他分子的结合对的两个成员中的任一者的结合常数大至少10^3m
‑
1、10^4m
‑
1或10^5m
‑
1)。特异性结合部分的特定实例包括特异性结合蛋白(例如,抗体、凝集素、链霉亲和素和蛋白a等抗生物素蛋白)。特异性结合部分也可以包括由这种特异性结合蛋白特异性结合的分子(或其部分)。
[0162]
如本文所用,术语“染色剂”、“染色”或类似的术语通常是指对生物学标本的任何处理,所述处理检测和/或区分生物学标本中特定分子(例如脂质、蛋白质或核酸)或特定结构(例如正常或恶性细胞、细胞质、细胞核、高尔基氏体或细胞骨架)的存在、位置和/或量(例如浓度)。例如,染色可以将生物学标本的特定分子或特定细胞结构与周围部分进行比对,并且染色的强度可以测定所述标本中特定分子的量。染色不仅可以和明视野显微镜一起使用,而且还可以和相衬显微镜、电子显微镜和荧光显微镜等其他观察工具一起使用,以用于辅助观察分子、细胞结构和生物体。一些由系统进行的染色可以让细胞的轮廓清晰可视。由所述系统进行的其他染色可依赖于染色的且不对其他细胞组分染色或对其他细胞组分相对极少染色的特定细胞组分(例如分子或结构)。由所述系统进行的各类染色方法的实例包括但不限于,组织化学方法、免疫组化方法和基于核酸分子间的杂交反应等分子间反应(包括非共价结合相互作用)的其他方法。特定的染色方法包括但不限于,初级染色方法(如h&e染色、子宫颈染色等)、酶联免疫组化方法,以及原位rna和dna杂交方法,例如荧光原位杂交(fish)。
[0163]
如本文所用,术语“靶标”是指确定或可以确定存在、位置和/或浓度的任何分子。靶分子的实例包括蛋白质、核酸序列和半抗原,例如与蛋白质共价结合的半抗原。通常,使用一个或多个特异性结合分子的缀合物和一个可检测标记物来检测靶分子。
[0164]
贯穿本说明书的对“一个实施例”、“一种实施例”等的引用,意指结合该实施例描述的特定特征、结构或特性包括在至少一个实施例中。因此,在本说明书中的不同位置出现的短语“在一个实施例中”或“在一种实施例中”不一定都是指同一个实施例。此外,具体特征、结构或特性可在一个或多个实施例中以任何合适的方式组合。
[0165]
本文提供的标题仅是为了方便,并不用于解释本发明所公开的实施例的范围或含义。
[0166]
基于香豆素的试剂
[0167]
如本文所进一步详述的,本公开提供了一种新颖的基于香豆素的试剂(例如连接基)以及包括本发明所公开的基于香豆素的试剂中的一种或多种的缀合物。在一些实施例中,所述基于香豆素的试剂中存在的香豆素部分使得能够检测通常难以检测的标记物,例如某些半抗原。在一些实施例中,难以检测的半抗原包括苯并呋喃半抗原和噻唑磺酰胺半抗原。在一些实施例中,难以检测的半抗原包括5
‑
硝基
‑3‑
吡唑碳酰胺(np)、2
‑
乙酰氨基
‑4‑
甲基
‑5‑
噻唑磺酰胺(ts)、7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
羧酸(dcc)和2,1,3
‑
苯并噁
二唑
‑5‑
碳酰胺(bf)。据信抗体变性和/或聚集通常导致在这些难以检测的标记物的分析范围内出现背景uv/vis吸收。因此,包含难以检测的半抗原标记物的缀合物通常在半抗原负载中被高估,导致对缀合物浓度的低估。据信使用本文所公开的基于香豆素的试剂可以缓解该问题。
[0168]
在一些实施例中,本公开的基于香豆素的试剂具有至少10,000m
‑
1cm
‑
1的消光系数。在其他实施例中,本公开的基于香豆素的试剂具有至少15,000m
‑
1cm
‑
1的消光系数。在其他实施例中,本公开的基于香豆素的试剂具有至少20,000m
‑
1cm
‑
1的消光系数。在进一步的实施例中,本公开的基于香豆素的试剂具有至少25,000m
‑
1cm
‑
1的消光系数。在一些实施例中,本公开的基于香豆素的试剂具有在约340nm至约500nm之间的吸收波长。
[0169]
在一些实施例中,本公开的基于香豆素的试剂具有式(ia)或(ib)结构:
[0170][0171]
其中
[0172]
a和b独立地为反应性官能团、可检测标记物或酶反应部分;
[0173]
l1和l2为连接基;
[0174]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分;
[0175]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0176]
m和n独立地为1至4范围内的整数。
[0177]
在一些实施例中,m和n独立地为1或2。在一些实施例中,m或n中的至少一个为1。在一些实施例中,m和n均为1。在一些实施例中,m或n中的一个为1并且m或n中的另一个为2。
[0178]
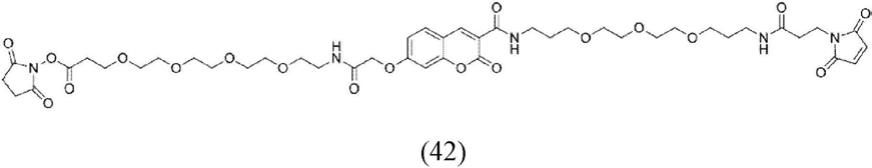
在一些实施例中,a和b均为反应性官能团。此类化合物的一个实例在本文中显示为化合物(42)。此类化合物可用作例如交联剂,例如使两种抗体或蛋白质彼此交联。
[0179]
基团a、b、l1、l2、w、m和n中的每一个的定义如本文所详述。
[0180]
在一些实施例中,本公开的基于香豆素的试剂具有式(iia)或(iib)结构:
[0181][0182][0183]
其中
[0184]
a1为反应性官能团;
[0185]
b1为可检测标记物;
[0186]
l1和l2为连接基;
[0187]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分;
[0188]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0189]
m和n独立地为1至4范围内的整数。
[0190]
在一些实施例中,可检测标记物为半抗原。在其他实施例中,可检测标记物为酶。在其他实施例中,可检测标记物为发色团。在进一步的实施例中,可检测标记物为荧光团。本文公开了这些类型的可检测标记物中的每一种的具体实例。
[0191]
在一些实施例中,式(iia)和(iib)化合物能够偶联至另一大分子、药物或生物分子。例如,反应性官能团可能与蛋白质或抗体上的胺基反应以形成蛋白质或抗体与基于香豆素的试剂的缀合物。本文设想并且公开了其他偶联方法。在一些实施例中,此类缀合物可用作组织标记或染色试剂。
[0192]
在一些实施例中,本公开的基于香豆素的试剂具有式(iic)或(iid)结构:
[0193][0194]
其中
[0195]
a1为反应性官能团;
[0196]
b2为半抗原;
[0197]
l1和l2为连接基;
[0198]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分;
[0199]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0200]
m和n独立地为1至4范围内的整数。
[0201]
在一些实施例中,半抗原为噁唑、吡唑、噻唑、苯并呋咱、三萜烯、脲、除罗丹明硫脲外的硫脲、除二硝基苯基或三硝基苯基外的硝基芳基、类鱼藤酮、环木脂体、杂联芳基、偶氮芳基、苯二氮在其他实施例中,半抗原为苯并呋咱或噻唑磺酰胺。在一些实施例中,半抗原为5
‑
硝基
‑3‑
吡唑碳酰胺、2
‑
乙酰氨基
‑4‑
甲基
‑5‑
噻唑磺酰胺、7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
羧酸和2,1,3
‑
苯并噁二唑
‑5‑
碳酰胺。其他合适的半抗原如本文所公开。在一些实施例中,a1包括马来酰亚胺部分或nhs
‑
酯基。在一些实施例中,l1或l2中的至少一者包括赖氨酸部分。在一些实施例中,l1或l2中的至少一者包括至少一个dpeg基团。
[0202]
具有式(iic)或(iid)的化合物的非限制性实例在本文中显示为化合物(16)、(24)、(34)、(54)和(66)。
[0203]
在一些实施例中,式(iic)和(iid)化合物能够偶联至另一大分子、药物或生物分子。例如,反应性官能团可能与蛋白质或抗体上的胺基反应以形成蛋白质或抗体与基于香豆素的试剂的缀合物。此类缀合物可用作组织标记或染色试剂。
[0204]
在一些实施例中,本公开的基于香豆素的试剂具有式(iiia)或(iiib)结构:
[0205][0206]
其中
[0207]
a2为酶反应部分;
[0208]
b1为可检测标记物;
[0209]
l1和l2为连接基;
[0210]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分;
[0211]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0212]
m和n独立地为1至4范围内的整数。
[0213]
酶反应部分中的每一种(包括酪酰胺部分、是酪酰胺部分的衍生物的部分以及醌甲基化物前体部分)、可检测标记物、l1、l2、w、z、m和n如本文所详述。
[0214]
在一些实施例中,a2为如本文所述的酪酰胺部分或包括酪酰胺衍生物的部分。在其他实施例中,a2为如本文所述的醌甲基化物前体部分。在一些实施例中,b1为半抗原。在一些实施例中,半抗原为噁唑、吡唑、噻唑、苯并呋咱、三萜烯、脲、除罗丹明硫脲外的硫脲、除二硝基苯基或三硝基苯基外的硝基芳基、类鱼藤酮、环木脂体、杂联芳基、偶氮芳基、苯二氮在其他实施例中,b1为发色团。在其他实施例中,b1为荧光团。在一些实施例中,l1或l2中的至少一者包括赖氨酸部分。在一些实施例中,l1或l2中的至少一者包括至少一个dpeg基团。
[0215]
在一些实施例中,式(iiia)和(iiib)化合物适用于检测生物学样品中已经用酶(例如磷酸酶或过氧化物酶)标记的靶标。可适于与本发明所公开的试剂一起使用的此类检测方法在美国专利公开号2017/0089911中有所描述,其公开内容通过引用整体并入本文。
[0216]
在一些实施例中,本公开的基于香豆素的试剂具有式(iiic)或(iiid)结构:
[0217][0218]
其中
[0219]
a2为酶反应部分;
[0220]
b2为半抗原;
[0221]
l1和l2为连接基;
[0222]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物
的部分;
[0223]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0224]
m和n独立地为1至4范围内的整数。
[0225]
如上所述,酶反应部分中的每一种(包括酪酰胺部分、是酪酰胺部分的衍生物的部分以及醌甲基化物前体部分)、可检测标记物、l1、l2、w、z、m和n如本文所详述。在一些实施例中,半抗原为噁唑、吡唑、噻唑、苯并呋咱、三萜烯、脲、除罗丹明硫脲外的硫脲、除二硝基苯基或三硝基苯基外的硝基芳基、类鱼藤酮、环木脂体、杂联芳基、偶氮芳基、苯二氮在其他实施例中,半抗原为苯并呋咱或噻唑磺酰胺。在一些实施例中,半抗原为5
‑
硝基
‑3‑
吡唑碳酰胺、2
‑
乙酰氨基
‑4‑
甲基
‑5‑
噻唑磺酰胺、7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
羧酸和2,1,3
‑
苯并噁二唑
‑5‑
碳酰胺。在一些实施例中,l1或l2中的至少一者包括赖氨酸部分。在一些实施例中,l1或l2中的至少一者包括至少一个dpeg基团。
[0226]
具有式(iiic)或(iiid)的化合物的非限制性实例在本文中表示为化合物(17)、(25)和(35)。
[0227]
在一些实施例中,式(iiic)和(iiid)化合物适用于检测生物学样品中已经用酶(例如本文所述的磷酸酶或过氧化物酶)标记的靶标。
[0228]
在一些实施例中,本公开的基于香豆素的试剂具有式(iiie)或(iiif)结构:
[0229][0230]
其中
[0231]
a2为酶反应部分;
[0232]
b3为能够参与点击化学反应的反应性基团;
[0233]
l1和l2为连接基;
[0234]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分;
[0235]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0236]
m和n独立地为1至4范围内的整数。
[0237]
在一些实施例中,b3为dbco基团。在其他实施例中,b3为叠氮化物基团。本文还公开了能够参与点击化学反应的其他合适的官能团。在一些实施例中,l1或l2中的至少一者包括赖氨酸部分。在一些实施例中,l1或l2中的至少一者包括至少一个dpeg基团。
[0238]
在一些实施例中,式(iiie)和(iiif)化合物适用于检测生物学样品中已经用酶(例如磷酸酶或过氧化物酶)标记的靶标,包括那些利用偶联至报告部分的点击缀合物的实施例,诸如pct公开号wo/2018/002016所述,其公开内容通过引用整体并入本文。
[0239]
取代或未取代的香豆素部分或是的取代或未取代的香豆素衍生物或类似物的部分
[0240]
在一些实施例中,w具有式(iva)或(ivb)结构:
[0241][0242]
其中q为键或者取代或未取代的直链或支化c1‑
c
16
烷基基团、
‑
[(ch2ch2)
j
‑
o]
k
‑
ch2‑
、
‑
[(ch2)
j
‑
o]
k
‑
ch2‑
,其中j为1至4范围内的整数,并且k为1至16范围内的整数;
‑
n
‑
r
x
‑
;
‑
c(o)
‑
n
‑
r
x
‑
;或
‑
n
‑
r
x
‑
c(o)
‑
、r
x
为h或c1‑
c4烷基基团;并且
[0243]
y为取代或未取代的香豆素部分或是取代或未取代的香豆素衍生物或类似物的部分。
[0244]
在一些实施例中,(i)取代或未取代的香豆素部分或者(ii)是取代或未取代的香豆素衍生物或类似物的部分包括选自下组的至少一个基团,该组由以下各项组成:取代或未取代的直链或支化c1‑
c6烷基基团;取代或未取代的直链或支化c1‑
c6烷氧基基团;取代或未取代的直链或支化c1‑
c6杂烷基基团;三氟甲基基团;羟基基团;硫酸酯基团;氰基基团;卤素;磷酸酯基团;糖;羧酸基团;硝基基团;
‑
c(o)nr
x
r
y
;
‑
s
‑
r
x
;
‑
so2;
‑
so2cl;
‑
so3h;
‑
so4h;
‑
so2nr
x
r
y
;
‑
n(h)
‑
nr
x
r
y
;
‑
nr
x
r
y
;并且其中r
x
和r
y
独立地为h或c1‑
c4烷基基团。
[0245]
在一些实施例中,w具有式(va)或(vb)结构:
[0246][0247]
其中所述式(va)部分可被0个、1个、2个、3个或4个r
t
基团取代;并且其中所述式(vb)化合物可被0个、1个、2个、3个、4个或5个r
t
基团取代;并且其中每个r
t
独立地选自取代或未取代的直链或支化c1‑
c
12
烷基基团;取代或未取代的直链或支化c1‑
c
12
烷氧基基团;取代或未取代的直链或支化c1‑
c
12
杂烷基基团;三氟甲基基团;羟基基团;硫酸酯基团;氰基基团;卤素;磷酸酯基团;糖;羧酸基团;硝基基团;
‑
c(o)nr
x
r
y
;
‑
s
‑
r
x
;
‑
so2;
‑
so2cl;
‑
so3h;
‑
so4h;
‑
so2nr
x
r
y
;
‑
n(h)
‑
nr
x
r
y
;
‑
nr
x
r
y
;并且其中r
x
和r
y
独立地为h或c1‑
c6烷基基团;
[0248]
其中式(va)部分被一个
‑
r1‑
x
‑
基团和一个
‑
r5‑
x
‑
基团取代;并且其中式(vb)部分被一个
‑
r3‑
x
‑
基团取代;
[0249]
r1为c1‑
c
10
取代或未取代的支化或非支化烷基基团、
‑
o
‑
、
‑
o
‑
ch2‑
、
‑
n(r
x
)
‑
或
‑
s
‑
。
[0250]
r5为c1‑
c
10
取代或未取代的支化或非支化烷基基团、
‑
c(o)
‑
o
‑
、
‑
c(o)
‑
n(h)
‑
;并且
[0251]
每个x独立地为键或者取代或未取代的直链或支化c1‑
c
16
烷基基团;
‑
[(ch2)
j
‑
o]
k
‑
ch2‑
,其中j为1至4范围内的整数,并且k为1至16范围内的整数;
‑
n
‑
r
x
‑
;
‑
c(o)
‑
n
‑
r
x
‑
;或
‑
n
‑
r
x
‑
c(o)
‑
,其中r
x
为h或c1‑
c4烷基基团。
[0252]
在一些实施例中,式(va)和(vb)化合物包括一个r
t
基团,其可以在香豆素部分的任一环上。在一些实施例中,式(va)和(vb)化合物包括两个r
t
基团。
[0253]
在一些实施例中,r1为c1‑
c6支化或非支化烷基基团。在一些实施例中,r5为c1‑
c6支化或非支化烷基基团。
[0254]
在一些实施例中,w具有式(vc)或(vd)结构:
[0255][0256]
其中
[0257]
r2、r3、r4、r6和r7独立地选自取代或未取代的直链或支化c1‑
c6烷基基团;取代或未取代的直链或支化c1‑
c6烷氧基基团;取代或未取代的直链或支化c1‑
c6杂烷基基团;三氟甲基基团;羟基基团;硫酸酯基团;氰基基团;卤素;磷酸酯基团;糖;羧酸基团;硝基基团;
‑
c(o)nr
x
r
y
;
‑
s
‑
r
x
;
‑
so2;
‑
so2cl;
‑
so3h;
‑
so4h;
‑
so2nr
x
r
y
;
‑
n(h)
‑
nr
x
r
y
;
‑
nr
x
r
y
;并且其中r
x
和r
y
独立地为h或c1‑
c4烷基基团;
[0258]
r3为c1‑
c
10
取代或未取代的支化或非支化烷基基团、
‑
c(o)
‑
o
‑
、
‑
c(o)
‑
n(h)
‑
;
[0259]
r1为c1‑
c
10
取代或未取代的支化或非支化烷基基团、
‑
o
‑
、
‑
o
‑
ch2‑
、
‑
n(r
x
)
‑
或
‑
s
‑
;并且
[0260]
每个x独立地为键或者取代或未取代的直链或支化c1‑
c
16
烷基基团;
‑
[(ch2)
j
‑
o]
k
‑
ch2‑
,其中j为1至4范围内的整数,并且k为1至16范围内的整数;
‑
n
‑
r
x
‑
;
‑
c(o)
‑
n
‑
r
x
‑
;或
‑
n
‑
r
x
‑
c(o)
‑
,其中r
x
为h或c1‑
c4烷基基团。
[0261]
在一些实施例中,r1为c1‑
c6支化或非支化烷基基团。在一些实施例中,r3为c1‑
c6支化或非支化烷基基团。
[0262]
连接基
[0263]
在一些实施例中,基团l1和l2各自独立地具有在约20g/mol至约3000g/mol范围内的分子量。在其他实施例中,基团l1和l2各自独立地具有在约40g/mol至约2000g/mol范围内的分子量。在其他实施例中,基团l1和l2各自独立地具有在约50g/mol至约1500g/mol范围内的分子量。在其他实施例中,基团l1和l2各自独立地具有在约50g/mol至约1250g/mol范围内
的分子量。在其他实施例中,基团l1和l2各自独立地具有在约75g/mol至约1000g/mol范围内的分子量。在其他实施例中,基团l1和l2各自独立地具有在约100g/mol至约800g/mol范围内的分子量。在其他实施例中,基团l1和l2各自独立地具有在约100g/mol至约600g/mol范围内的分子量。在其他实施例中,基团l1和l2各自独立地具有在约100g/mol至约400g/mol范围内的分子量。在其他实施例中,基团l1和l2各自独立地具有在约100g/mol至约200g/mol范围内的分子量。在其他实施例中,基团l1和l2各自独立地具有在约250g/mol至约500g/mol范围内的分子量。在其他实施例中,基团l1和l2各自独立地具有在约20g/mol至约150g/mol范围内的分子量。
[0264]
在一些实施例中,基团l1和l2各自独立地具有在约0.5nm至约150nm范围内的长度。在一些实施例中,基团l1和l2各自独立地具有在约0.5nm至约100nm范围内的长度。在一些实施例中,基团l1和l2各自独立地具有在约0.5nm至约50nm范围内的长度。在一些实施例中,基团l1和l2各自独立地具有在约0.5nm至约30nm范围内的长度。在其他实施例中,基团l1和l2各自独立地具有小于约20nm的长度。在其他实施例中,基团l1和l2各自独立地具有小于约15nm的长度。
[0265]
在一些实施例中,l1和l2中的每一个可独立地带电荷或不带电荷。在一些实施例中,基团l1和l2包括一个或多个带电基团。例如,在一些实施例中,基团l1和l2可包括季胺基团、吡啶鎓基团、环脲或硫酸酯基团。
[0266]
在其他实施例中,l1和l2可包括单个氨基酸残基(例如赖氨酸)、肽或聚合物,其可以带电荷或不带电荷。在一些实施例中,l1和l2可独立地包括具有2个至20个氨基酸的肽、具有2个至10个氨基酸的肽、具有2个至8个氨基酸的肽或具有1个至4个氨基酸的肽。以举例的方式,肽可以为赖氨酸
‑
[u]
q
‑
赖氨酸,其中u表示氨基酸,并且其中q为0或1至18范围内的整数。在q为1或更大的情况下,u可以表示同质或异质的肽序列,即包含相同或不同氨基酸的肽序列。在一些实施例中,u选自赖氨酸、丙氨酸、精氨酸、鸟嘌呤、谷氨酸或其任意组合。合适的带电聚合物描述于美国专利公开第2002/0052335号、第2004/0058446号、第2004/0197318号和第2004/0162235号中,这些公开内容通过引用整体并入本文。
[0267]
在一些实施例中,l1和l2基团独立地包括一个或多个增溶性基团。在一些实施例中,增溶性基团包括聚乙二醇(peg)基团(或可得自quanta biodesign的短链peg(dpeg))。在一些实施例中,l1和l2基团独立地包括约2个至24个之间的peg基团。在一些实施例中,l1和l2基团独立地包括约2个至18个之间的peg基团。在其他实施例中,l1和l2基团独立地包括约2个至12个之间的peg基团。在其他实施例中,l1和l2基团独立地包括约2个至6个之间的peg基团。在其他实施例中,l1和l2基团独立地包括4个peg基团。在其他实施例中,l1和l2基团独立地包括8个peg基团。在其他实施例中,l1和l2基团独立地包括12个peg基团。在其他实施例中,l1和l2基团独立地包括16个peg基团。在其他实施例中,l1和l2基团独立地包括24个peg基团。据信,此类环氧烷连接基的引入能够提高基于香豆素的试剂的亲水性。
[0268]
在一些实施例中,每个l1和l2独立地为支化或非支化、线性或环状取代或未取代的饱和或不饱和基团,其具有在2个与200个之间的碳原子,并且任选地具有一个或多个选自o、n或s的杂原子。在其他实施例中,每个l1和l2独立地为支化或非支化、线性或环状取代或未取代的饱和或不饱和基团,其具有在2个与120个之间的碳原子,并且任选地具有一个或多个选自o、n或s的杂原子。在其他实施例中,每个l1和l2独立地为支化或非支化、线性或环
状取代或未取代的饱和或不饱和基团,其具有在2个与80个之间的碳原子,并且任选地具有一个或多个选自o、n或s的杂原子。在一些实施例中,每个l1和l2独立地为支化或非支化、线性或环状取代或未取代的饱和或不饱和基团,其具有在4个与40个之间的碳原子,并且任选地具有一个或多个选自o、n或s的杂原子。在一些实施例中,每个l1和l2独立地为支化或非支化、线性或环状取代或未取代的饱和或不饱和基团,其具有在6个与20个之间的碳原子,并且任选地具有一个或多个选自o、n或s的杂原子。
[0269]
在一些实施例中,每个l1和/或l2基团独立地具有式(via):
[0270][0271]
其中
[0272]
f为0或1至24范围内的整数;
[0273]
j为1至24范围内的整数;
[0274]
r8为键或者o、s、
‑
n(r
c
)(r
d
)或
‑
n
+
(r
c
)(r
d
)(r
e
);
[0275]
r
a
和r
b
独立地为h、c1‑
c4烷基基团、f、cl或
‑
n(r
c
)(r
d
);
[0276]
r
c
、r
d
和r
e
独立地选自h或c1‑
c4烷基基团;
[0277]
r9和r
10
独立地为键或基团,所述基团具有多至6个碳原子并且包括羰基、酰胺、酰亚胺、酯、醚、胺、硫酮或硫醇。
[0278]
在一些实施例中,r
a
或r
b
中的至少一个为h。在一些实施例中,r
a
或r
b
中的至少一个为h,并且f为1或2。在一些实施例中,r
a
或r
b
中的至少一个为h,f为1,并且s为至少2。在一些实施例中,r
a
和r
b
为h,并且r8为键。在一些实施例中,式(via)连接基包含2个至40个之间碳原子。在一些实施例中,式(via)连接基包含4个至20个之间碳原子。在一些实施例中,基团l1和l2各自独立地具有在约100g/mol至约600g/mol范围内的分子量。在一些实施例中,基团l1和l2各自独立地具有在约100g/mol至约400g/mol范围内的分子量。在一些实施例中,基团l1和l2各自独立地具有在约100g/mol至约200g/mol范围内的分子量。
[0279]
在一些实施例中,每个l1和l2基团独立地具有式(vib):
[0280][0281]
其中f为1至12范围内的整数;
[0282]
r8为键或者o、s、
‑
n(r
c
)(r
d
)或
‑
n
+
(r
c
)(r
d
)(r
e
);
[0283]
r
c
、r
d
和r
e
独立地为ch3或h;
[0284]
r9和r
10
独立地为键或选自羰基、酰胺、酰亚胺、酯、醚、胺或硫醇的基团;并且
[0285]
j为1至24范围内的整数。
[0286]
在一些实施例中,f为1,并且s为至少2。在一些实施例中,r8为键;f为1;并且j为2至16。在其他实施例中,r8为键;f为1;并且j为2至12。在其他实施例中,r8为键;f为1;并且j为2至8。
[0287]
在一些实施例中,式(vib)连接基包含2个至40个之间碳原子。在一些实施例中,式(vib)连接基包含4个至20个之间碳原子。在一些实施例中,基团l1和l2各自独立地具有在约100g/mol至约600g/mol范围内的分子量。在一些实施例中,基团l1和l2各自独立地具有在约100g/mol至约400g/mol范围内的分子量。在一些实施例中,基团l1和l2各自独立地具有在约100g/mol至约200g/mol范围内的分子量。
[0288]
在一些实施例中,每个l1和l2基团独立地具有式(vic):
[0289][0290]
其中f为0或1至12范围内的整数;
[0291]
j为1至24范围内的整数;并且
[0292]
r9和r
10
独立地为键或选自羰基、酰胺、酰亚胺、酯、醚、胺或硫醇的基团。
[0293]
在一些实施例中,f为1;并且j为至少2。在一些实施例中,f为1,并且j为2。在一些实施例中,f为1,并且j为3。在一些实施例中,f为1,并且j为4。在一些实施例中,f为2,并且j为2至16范围内的整数。在一些实施例中,f为2,并且j为2至12范围内的整数。在一些实施例中,f为2,并且j为2至8范围内的整数。在一些实施例中,f为2,并且j为至少2。在一些实施例中,f为2,并且j为至少3。在一些实施例中,f为2,并且j为至少4。
[0294]
本领域技术人员将认识到,当式(ia)和/或(iib)的m和n大于1时,相应地可以结合多个l1或l2基团,并且每个l1或l2基团可以相同或不同。以举例的方式,在m为2的情况下,基团
‑
[l1]
‑
[l1]
‑
中的每个l1可以相同或不同。例如,基团
‑
[l1]
‑
[l1]
‑
中的一个l1可包括环氧烷基团,而基团
‑
[l1]
‑
[l1]
‑
中的另一个l1可包括未取代的c1‑
c
10
烷基基团。以另一个实例举例,基团
‑
[l1]
‑
[l1]
‑
中的一个l1可包括至少一个peg或dpeg基团,而基团
‑
[l1]
‑
[l1]
‑
中的另一个l1可包括赖氨酸残基。以另一个实例举例,基团
‑
[l1]
‑
[l1]
‑
中的一个l1可包括至少一个peg或dpeg基团,而基团
‑
[l1]
‑
[l1]
‑
中的另一个l1可包括赖氨酸残基,并且l2基团可包括至少一个peg或dpeg基团。
[0295]
反应性官能团
[0296]
一般而言,反应性官能团可以是促进两个分子偶联在一起以形成加合物的任意基团。在一些实施例中,反应性官能团是能够参与亲核取代(例如,胺和醇与酰基卤、活性酯的反应)、亲电取代(例如,烯胺反应)和加成至碳
‑
碳和碳
‑
杂原子多键(例如,迈克尔反应、狄尔斯
‑
阿尔德加成)的官能团。这些及其他有用的反应描述于例如以下文献中:march,advanced organic chemistry,3rd ed.,john wiley&sons,new york,1985;hermanson,bioconjugate techniques,academic press,san diego,1996;以及feeney等人,
modification of proteins;advances in chemistry series,vol.198,american chemical society,washington,d.c.,1982。
[0297]
在一些实施例中,反应性官能团为羧酸、羧酸的活化酯、碳化二亚胺、磺酰卤化物、酰基卤、甲硅烷基卤化物、酰基叠氮化物、酰基腈、丙烯酰胺、胺、醛、烷基卤(其中卤化物随后可被亲核基团取代,该亲和基团为例如胺、羧酸根阴离子、硫醇阴离子、碳负离子或烷氧基离子,从而使形成卤素原子位点的新基团的共价连接)、芳基卤化物、烷基磺酸盐、磺酸酯、酸酐、叠氮化物、氮丙啶、重氮烷、卤代乙酰胺、卤代三嗪、肼、羟基胺、异氰酸酯、异硫氰酸酯、马来酰亚胺、氨基磷酸酯、硫醇(在一些实施例中,可转化为二硫化物,与酰基卤反应或键合至金属)、羟基(可转化为酯、醚、醛等)、肼和炔烃(可发生例如环加成、酰化、迈克尔加成)。在一些实施例中,反应性官能团为羧基基团或其各种衍生物,包括但不限于n
‑
羟基琥珀酰亚胺酯、n
‑
羟基苯并三唑酯、酸性卤化物、酰基咪唑、硫代酯、对硝基苯酯、烷基、烯基、炔基和芳族酯。在一些实施例中,反应性官能团为能够参与狄尔斯
‑
阿尔德反应的亲二烯体基团,例如马来酰亚胺基团。在一些实施例中,反应性官能团为醛基或酮基,使得随后的衍生化能够通过形成羰基衍生物(诸如亚胺、腙、缩氨基脲或肟)或通过诸如格氏加成或烷基锂加成实现。
[0298]
在其他实施例中,反应性官能团选自羧酸、羧酸的活化酯、磺酰基卤化物、酰基卤、胺、烷基或芳基卤化物、酸酐、叠氮化物、卤代乙酰胺、卤代三嗪、肼、异氰酸酯、异硫氰酸酯、马来酰亚胺、氨基磷酸酯、硫醇、羟基和炔烃。在其他实施例中,反应性官能团选自羧酸、羧酸的活化酯、胺、叠氮化物、卤代乙酰胺、肼、异氰酸酯、马来酰亚胺和炔烃。
[0299]
在一些实施例中,反应性官能团可选择为使其不参与或干扰本文所述的缀合物的化学稳定性。替代性地,可通过存在的保护基团使其不参与交联反应来保护反应性官能团。
[0300]
在一些实施例中,反应性官能团是能够发生“点击化学”反应的部分。“点击化学”是一种化学原理,其由sharpless和meldal的研究组独立地定义,描述了定制以通过将小单元连接在一起而快速可靠地生成物质的化学过程。“点击化学”已应用于一组可靠并且自主的有机反应(kolb,h.c.;finn,m.g.;sharpless,k.b.angew.chem.int.ed.2001,40,2004
‑
2021)。例如,将铜催化的叠氮化物
‑
炔烃[3+2]环加成反应鉴定为水中高度可靠的分子连接(rostovtsev,v.v.等人,angew.chem.int.ed.2002,41,2596
‑
2599),其已经用于增强多种类型的生物分子相互作用的研究(wang,q.等人,j.am.chem.soc.2003,125,3192
‑
3193;speers,a.e.等人,j.am.chem.soc.2003,125,4686
‑
4687;link,a.j.;tirrell,d.a.j.am.chem.soc.2003,125,11164
‑
11165;deiters,a.等人,j.am.chem.soc.2003,125,11782
‑
11783)。此外,还已出现在有机合成(lee,l.v.等人,j.am.chem.soc.2003,125,9588
‑
9589)、药物发现(kolb,h.c.;sharpless,k.b.drug disc.today 2003,8,1128
‑
1137;lewis,w.g.等人,angew.chem.int.ed.2002,41,1053
‑
1057)以及表面功能化(meng,j.
‑
c.等人,angew.chem.int.ed.2004,43,1255
‑
1260;fazio,f.等人,j.am.chem.soc.2002,124,14397
‑
14402;collman,j.p.等人,langmuir 2004,asap,in press;lummerstorfer,t.;hoffmann,h.j.phys.chem.b 2004,in press)方面的应用。一般来讲,“点击化学”促进反应以模块化方式得到广泛应用,获得高化学收率,生成无害副产物,具有化学特异性,需要简单的反应条件,使用容易获得的起始材料和试剂,不使用溶剂或使用温和的溶剂(例如水),轻松分离产物,具有高热力学驱动力以有利于反应获得单一反应产物,和/或获得高的原子
经济性。尽管某些一般标准在本质上可能是主观的,但并非所有标准都需要得到满足。
[0301]
本领域技术人员将认识到,式(ia)、(ib)、(iiie)、(iiif)化合物中的任一者可终止于适当的反应性基团(例如dbco基团)处,该反应性基团可与另一种适当官能化的化合物(例如具有叠氮化物基团的化合物)形成点击加合物(包括pct公开wo/2018/002015中描述的那些化合物,其公开内容通过引用整体并入本文)。下表中列出了能够在点击化学反应中反应的成对反应性基团:
[0302][0303][0304]
可检测标记物
[0305]
一般而言,可检测标记物包括:发色、荧光、磷光和发光分子和材料;催化剂(诸如酶),其将一种物质转化为另一种物质以提供可检测的差异(诸如通过将一种无色物质转化为有色物质,反之亦然,或通过产生沉淀或提高样品浊度);半抗原,其可使用其他可检测的带有标记的抗体缀合物通过抗体
‑
半抗原结合相互作用进行检测;以及顺磁性和磁性分子或材料。当然,报告部分本身也可间接检测,例如,如果可检测标记物为半抗原,则可以利用对该可检测标记物具有特异性的另一种抗体检测该可检测标记物,如本领域的普通技术人员所知。
[0306]
在一些实施例中,合适的半抗原包括但不限于:吡唑(例如硝基吡唑);硝基苯基化合物;苯并呋咱;三萜烯;脲(例如苯基脲);硫脲(例如苯基硫脲);类鱼藤酮和类鱼藤酮衍生物;噁唑(例如噁唑磺酰胺);噻唑(例如噻唑磺酰胺);香豆素和香豆素衍生物;以及环木脂体。半抗原的其他非限制性实例包括:噻唑;硝基芳基化合物;苯并呋喃;三萜烯;以及环木脂体。半抗原的具体实例包括二硝基苯基、生物素、地高辛和荧光素及其任何衍生物或类似物。其他合适的半抗原描述于美国专利第8,846,320号、第8,618,265号、第7,695,929号、第8,481,270号以及第9,017,954号中,这些美国专利的公开内容通过引用整体并入本文。其
他合适的半抗原描述于美国专利公开第2013/0109019号和第2010/0184087号中,这些美国专利公开的公开内容通过引用整体并入本文。
[0307]
在一些实施例中,合适的荧光团属于多种常见的化学类别,包括香豆素、荧光素(或荧光素衍生物及类似物)、罗丹明、试卤灵、发光体和花菁。荧光分子的其他实例可参见:molecular probes handbook
‑
a guide to fluorescent probes and labeling technologies,molecular probes,eugene,or,therofisher scientific,第11版。在其他实施例中,荧光团选自黄嘌呤衍生物、花菁衍生物、方酸衍生物、萘衍生物、香豆素衍生物、噁二唑衍生物、蒽衍生物、芘衍生物、噁嗪衍生物、吖啶衍生物、芳基次甲基衍生物和四吡咯衍生物。在其他实施例中,荧光部分选自:cf染料(可得自biotium);draq和cytrak探针(可得自biostatus);bodipy(可得自invitrogen);alexa fluor(可得自invitrogen);dylight fluor(例如dylight 649)(可得自thermo scientific,pierce);atto和tracy(可得自sigma aldrich);fluoprobe(可得自interchim);abberior染料(可得自abberior);dy和megastokes染料(可得自dyomics);sulfo cy染料(可得自cyandye);hilyte fluor(可得自anaspec);seta、setau和square染料(可得自seta biomedicals);quasar和cal fluor染料(可得自biosearch technologies);surelight染料(可得自apc、rpepercp、phycobilisomes)(columbia biosciences);以及apc、apcxl、rpe、bpe(可得自phyco
‑
biotech、greensea、prozyme、flogen)。
[0308]
在一些实施例中,合适的酶包括但不限于辣根过氧化物酶、碱性磷酸酶、酸性磷酸酶、葡萄糖氧化酶、β
‑
半乳糖苷酶、β
‑
葡萄糖醛酸苷酶或β
‑
内酰胺酶。在其他实施例中,酶包括氧化还原酶或过氧化物酶(例如hrp、ap)。在这些实施例中,缀合至抗标记物抗体的酶催化显色底物转化为反应性部分,该反应性部分结合至靶标近侧或直接在靶标上的样品。
[0309]
发色化合物/底物的特定非限制性实例包括二氨基联苯胺(dab)、4
‑
硝基苯基磷酸酯(pnpp)、固红、溴氯吲哚磷酸酯(bcip)、硝基蓝四唑鎓(nbt)、bcip/nbt、固红、ap橙、ap蓝、四甲基联苯胺(tmb)、2,2
′‑
叠氮二
‑
[3
‑
乙基苯并噻唑啉磺酸酯](abts)、邻二苯甲啶、4
‑
氯萘酚(4
‑
cn)、硝基苯基
‑
β
‑
d
‑
吡喃半乳糖苷(onpg)、邻苯二胺(opd)、5
‑
溴
‑4‑
氯
‑3‑
吲哚基
‑
β
‑
吡喃半乳糖苷(x
‑
gal)、甲基伞形酮酰
‑
β
‑
d
‑
吡喃半乳糖苷(mu
‑
gal)、对硝基苯基
‑
α
‑
d
‑
吡喃半乳糖苷(pnp)、5
‑
溴
‑4‑
氯
‑3‑
吲哚基
‑
β
‑
d
‑
葡糖醛酸苷(x
‑
gluc)、3
‑
氨基
‑9‑
乙基咔唑(aec)、品红、碘代硝基四唑鎓(int)、四唑蓝、四唑紫、n,n
′‑
双羧基戊基
‑
5,5
′‑
二磺酰氨基
‑
二茂铁花青(cy5)、4
‑
(二甲基氨基)偶氮苯
‑4′‑
苯胺(dabsyl)、四甲基罗丹明(disco紫)和罗丹明110(罗丹明)。dab在过氧化物酶和过氧化氢存在下发生氧化,导致不溶于乙醇的棕色沉淀物沉积在酶活性位点。在一些实施例中,显色底物为信号传导缀合物,其包含潜在反应性部分和显色部分。
[0310]
在一些实施例中,信号传导缀合物的潜在反应性部分配置为发生催化活化,以形成可与样品或其他检测组分共价结合的反应性种类。催化活化由一种或多种酶(例如氧化还原酶和过氧化物酶,如辣根过氧化物酶)驱动,并且导致反应性种类的形成。这些反应性种类能够与生成它们的位点近侧(即,酶附近)的显色部分反应。信号传导缀合物的具体实例公开于美国专利公开第2013/0260379号中,其公开内容通过引用整体并入本文。
[0311]
其他合适的可检测标记物描述于pct公开wo/2018/002015中,其公开内容通过引用整体并入本文。例如,合适的标记物包括具有至少两个彼此直接或间接偶联的发色团的
多染料缀合物。
[0312]
可检测标记物的其他实例包括但不限于:dab;aec;cn;bcip/nbt;固红;固蓝;品红;nbt;alk金;瀑布蓝乙酰叠氮化物;dapoxyl磺酸/羧酸琥珀酰亚胺酯;dy
‑
405;alexa fluor 405琥珀酰亚胺酯;瀑布黄琥珀酰亚胺酯;吡啶基噁唑琥珀酰亚胺酯(pympo);海水蓝琥珀酰亚胺酯;dy
‑
415;7
‑
羟基香豆素
‑3‑
羧酸琥珀酰亚胺酯;dyq
‑
425;6
‑
fam亚磷酰胺;萤光黄;碘乙酰胺;alexa fluor 430琥珀酰亚胺酯;dabcyl琥珀酰亚胺酯;nbd氯化物/氟化物;qsy 35琥珀酰亚胺酯;dy
‑
485xl;cy2琥珀酰亚胺酯;dy
‑
490;俄勒冈绿488羧基琥珀酰亚胺酯;alexa fluor 488琥珀酰亚胺酯;bodipy 493/503c3琥珀酰亚胺酯;dy
‑
480xl;bodipy fl c3琥珀酰亚胺酯:bodipy fl c5琥珀酰亚胺酯;bodipy fl
‑
x琥珀酰亚胺酯;dyq
‑
505;俄勒冈绿514羧酸琥珀酰亚胺酯;dy
‑
510xl;dy
‑
481xl;6
‑
羧基
‑4′
,5
′‑
二氯
‑2′
,7
′‑
二甲氧基荧光素琥珀酰亚胺酯(joe);dy
‑
520xl;dy
‑
521xl;bodipy r6g c3琥珀酰亚胺酯;赤藓异硫氰酸松香酯;5
‑
羧基
‑2′
,4
′
,5
′
,7
′‑
四溴磺砜荧光素琥珀酰亚胺酯;alexa fluor 532琥珀酰亚胺酯;6
‑
羧基
‑2′
,4,4
′
,5
′
7,7
′‑
六氯荧光素琥珀酰亚胺酯(hex);bodipy530/550c3琥珀酰亚胺酯;dy
‑
530;bodipy tmr
‑
x琥珀酰亚胺酯;dy
‑
555;dyq
‑
1;dy
‑
556;cy3琥珀酰亚胺酯;dy
‑
547;dy
‑
549;dy
‑
550;alexa fluor 555琥珀酰亚胺酯;alexa fluor 546琥珀酰亚胺酯;dy
‑
548;bodipy 558/568c3琥珀酰亚胺酯;玫瑰红x琥珀酰亚胺酯;qsy 7琥珀酰亚胺酯;bodipy 564/570c3琥珀酰亚胺酯;bodipy 576/589c3琥珀酰亚胺酯;羧基
‑
x
‑
罗丹明(rox);琥珀酰亚胺酯;alexa fluor 568琥珀酰亚胺酯;dy
‑
590;bodipy 581/591c3琥珀酰亚胺酯;dy
‑
591;bodipy tr
‑
x琥珀酰亚胺酯;alexa fluor 594琥珀酰亚胺酯;dy
‑
594;羧基萘荧光素琥珀酰亚胺酯;dy
‑
605;dy
‑
610;alexa fluor 610琥珀酰亚胺酯;dy
‑
615;bodipy 630/650
‑
x琥珀酰亚胺酯;食用色素亮蓝;alexa fluor 633琥珀酰亚胺酯;alexa fluor 635琥珀酰亚胺酯;dy
‑
634;dy
‑
630;dy
‑
631;dy
‑
632;dy
‑
633;dyq
‑
2;dy
‑
636;bodipy 650/665
‑
x琥珀酰亚胺酯;dy
‑
635;cy5琥珀酰亚胺酯;alexa fluor 647琥珀酰亚胺酯;dy
‑
647;dy
‑
648;dy
‑
650;dy
‑
654;dy
‑
652;dy
‑
649;dy
‑
651;dyq
‑
660;dyq
‑
661;alexa fluor 660琥珀酰亚胺酯;cy5.5琥珀酰亚胺酯;dy
‑
677;dy
‑
675;dy
‑
676;dy
‑
678;alexa fluor 680琥珀酰亚胺酯;dy
‑
679;dy
‑
680;dy
‑
682;dy
‑
681;dyq
‑
3;dyq
‑
700;alexa fluor 700琥珀酰亚胺酯;dy
‑
703;dy
‑
701;dy
‑
704;dy
‑
700;dy
‑
730;dy
‑
731;dy
‑
732;dy
‑
734;dy
‑
750;cy7琥珀酰亚胺酯;dy
‑
749;dyq
‑
4;以及cy7.5琥珀酰亚胺酯。
[0313]
报告部分诸如偶联至二抗的那些可选自上述可检测标记物中的任一者。
[0314]
酶反应部分
[0315]
在一些实施例中,酶反应部分包括酪酰胺、酪酰胺衍生物以及醌甲基化物前体及其衍生物。
[0316]
在一些实施例中,酶反应部分为酪酰胺或其衍生物或类似物。合适的酪酰胺部分和酪酰胺衍生物包括描述于美国专利公开第2012/0171668号中的那些,其公开内容通过引用整体并入本文。在一些实施例中,酪酰胺部分或酪酰胺衍生物为酶(例如过氧化物酶、辣根过氧化物酶)的底物。
[0317]
在一些实施例中,酶反应部分具有式(viia)所提供的结构:
[0318][0319]
其中每个r
11
基团独立地选自氢或具有在1个与4个之间的碳原子的低级烷基基团,并且其中r
x
为h或c1‑
c4烷基基团。
[0320]
在其他实施例中,酶反应部分具有式(viib)所提供的结构:
[0321][0322]
在一些实施例中,酶反应部分为醌甲基化物前体或其衍生物。合适的醌甲基化物前体或衍生物包括描述于美国专利公开第2017/0089911号中的那些,其公开内容通过引用整体并入本文。在一些实施例中,醌甲基化物前体或其衍生物为酶(例如磷酸酶和碱性磷酸酶)的底物。
[0323]
在一些实施例中,酶反应部分具有式(viiia)所提供的结构:
[0324][0325]
其中
[0326]
r2为选自磷酸酯、酰胺、硝基、脲、硫酸酯、甲基、酯、β
‑
内酰胺或糖的基团;
[0327]
r
13
为卤化物;
[0328]
r
15
、r
16
、r
17
和r
18
独立地选自氢或具有在1个与4个之间的碳原子的脂族基团;并且
[0329]
r
14
为
‑
(ch2)
w
nh
‑
、
‑
o(ch2)
w
nh
‑
、
‑
n(h)c(o)(ch2)
w
nh
‑
、
‑
c(o)n(h)(ch2)
w
nh
‑
、
‑
(ch2)
w
o
‑
、
‑
o(ch2)
w
o
‑
、
‑
o(ch2ch2o)
w
‑
、
‑
n(h)c(o)(ch2)
w
o
‑
、
‑
c(o)n(h)(ch2)
w
o
‑
、
‑
c(o)n(h)(ch2ch2o)
w
‑
、
‑
(ch2)
w
s
‑
、
‑
o(ch2)
w
s
‑
、
‑
n(h)c(o)(ch2)
w
s
‑
、
‑
c(o)n(h)(ch2)
w
s
‑
、
‑
(ch2)
w
nh
‑
、
‑
c(o)n(h)(ch2ch2o)
w
ch2ch2nh、
‑
c(o)(ch2ch2o)
w
ch2ch2nh
‑
、
‑
c(o)n(h)(ch2)nhc(o)ch(ch3)(ch2)
w
nh
‑
或
‑
n(h)(ch2)
w
nh
‑
,其中w为1至12范围内的整数。
[0330]
在其他实施例中,酶反应部分具有式(viiib)所提供的结构:
[0331][0332]
在其他实施例中,酶反应部分具有式(viiic)所提供的结构:
[0333][0334]
其中r
13
‑
(ch2)
w
nh
‑
、
‑
o(ch2)
w
nh
‑
、
‑
n(h)c(o)(ch2)
w
nh
‑
、c(o)n(h)(ch2)
w
nh
‑
、
‑
(ch2)
w
o
‑
、
‑
o(ch2)
w
o
‑
、
‑
o(ch2ch2o)
w
‑
、
‑
n(h)c(o)(ch2)
w
o
‑
、
‑
c(o)n(h)(ch2)
w
o
‑
、
‑
c(o)n(h)(ch2ch2o)
w
‑
、
‑
(ch2)
w
s
‑
、
‑
o(ch2)
w
s
‑
、
‑
n(h)c(o)(ch2)
w
s
‑
、
‑
c(o)n(h)(ch2)
w
s
‑
、
‑
(ch2)
w
nh
‑
、
‑
c(o)n(h)(ch2ch2o)
w
ch2ch2nh、
‑
c(o)(ch2ch2o)
w
ch2ch2nh
‑
、
‑
c(o)n(h)(ch2)nhc(o)ch(ch3)(ch2)
w
nh
‑
或
‑
n(h)(ch2)
w
nh
‑
,其中w独立地为1至12范围内的整数。在一些实施例中,r7为c(o)n(h)(ch2)
w
nh并且w如上文所定义。在其他实施例中,r7为c(o)n(h)(ch2)
w
nh并且w在2至6的范围内。
[0335]
在其他实施例中,酶反应部分具有式(viiid)所提供的结构:
[0336][0337]
其中w在1至12的范围内。在一些实施例中,w在1至8的范围内。
[0338]
在其他实施例中,w在2至8的范围内。在其他实施例中,w在2至6的范围内。在进一步的实施例中,w为6。
[0339]
更多基于香豆素的试剂
[0340]
在一些实施例中,基于香豆素的试剂具有以下结构:
[0341][0342]
其中r
v
为酶反应部分或反应性官能团。
[0343]
在一些实施例中,基于香豆素的试剂具有以下结构:
[0344][0345]
其中r
v
为酶反应部分或反应性官能团。
[0346]
在一些实施例中,基于香豆素的试剂具有以下结构:
[0347][0348]
在一些实施例中,基于香豆素的试剂具有以下结构:
[0349][0350]
其中r
v
为酶反应部分或反应性官能团。
[0351]
在一些实施例中,基于香豆素的试剂具有以下结构:
[0352][0353]
其中r
v
为酶反应部分或反应性官能团。
[0354]
在一些实施例中,基于香豆素的试剂具有以下结构:
[0355][0356]
其中r
v
为酶反应部分或反应性官能团。
[0357]
包括基于香豆素的试剂的缀合物
[0358]
本公开还提供了基于香豆素的试剂与另一种取代基(例如大分子、药物或生物分子)的缀合物。在一些实施例中,式(ia)、(ib)、(iia)、(iib)、(iic)或(iid)所示的基于香豆素的试剂可与大分子、药物或生物分子反应。在一些实施例中,缀合物具有以下一般结构:t
‑
[基于香豆素的试剂]o,其中t为特异性结合实体、氨基酸、肽、蛋白质、糖、核苷、核苷酸、寡核苷酸、药物、脂质或纳米颗粒,并且o为1至10范围内的整数。
[0359]
可采用多种方法,使基于香豆素的试剂偶联至大分子、药物或生物分子。例如,为促进该结合,基于香豆素的试剂可连接至生物分子
‑
反应性基团,诸如活性酯基基团、氨基基团、巯基基团、碳水化合物基团、叠氮基团或羧基基团。可采用多种方法,使生物分子
‑
反应性基团与大分子或大分子片段反应。此类方法的实例为光交联和戊二醛交联。本领域的技术人员将清楚实现此类偶联的其他方法。参见例如以下方法:hermanson,g.t.,bioconjugate techniques,elsevier science,london,2008。
[0360]
本发明的活性酯基团应选择为使其不损害延伸的连接基团与蛋白质或大分子的键合。本领域的技术人员将认识到,在本发明中可以采用活性酯诸如n
‑
羟基琥珀酰亚胺或n
‑
羟基磺基琥珀酰亚胺。替代性地,延伸连接基团上的伯氨基基团可通过戊二醛与蛋白质上的伯氨基基团偶联。蛋白质上的氨基基团可偶联至延伸连接基团上的羧基基团。另外,延伸连接基团可以用硝基苯基叠氮化物进行修饰,使得在可见光照射下会发生与蛋白质的偶联。本领域的技术人员将清楚实现此类偶联的其他方法。
[0361]
在一些实施例中,本公开的缀合物具有式(ixa)或(ixb)结构:
[0362][0363]
其中t为取代基,其选自特异性结合实体、氨基酸、肽、蛋白质、糖、核苷、核苷酸、寡核苷酸、药物、脂质或纳米颗粒;
[0364]
r
z
为可检测标记物,诸如上文所定义;
[0365]
o为1至10范围内的整数;
[0366]
l1和l2为连接基;
[0367]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分;
[0368]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0369]
m和n独立地为1至4范围内的整数。
[0370]
在一些实施例中,特异性结合实体为抗体、抗体片段、药物/抗体复合物或核酸。在一些实施例中,抗体为一抗。在其他实施例中,抗体为二抗。
[0371]
在一些实施例中,r
z
为半抗原。在一些实施例中,r
z
为噁唑、吡唑、噻唑、苯并呋咱、三萜烯、脲、除罗丹明硫脲外的硫脲、除二硝基苯基或三硝基苯基外的硝基芳基、类鱼藤酮、环木脂体、杂联芳基、偶氮芳基、苯二氮在其他实施例中,r
z
为苯并呋咱或噻唑磺酰胺。
[0372]
在其他实施例中,r
z
为酶,例如过氧化物酶或磷酸酶。在其他实施例中,r
z
为荧光团。
[0373]
在一些实施例中,本公开的缀合物具有式(ixc)或(ixd)结构:
[0374][0375]
其中ab为抗体;
[0376]
r
z
为可检测标记物,诸如上文所定义;
[0377]
o为1至10范围内的整数;
[0378]
l1和l2为连接基;
[0379]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分;
[0380]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0381]
m和n独立地为1至4范围内的整数。
[0382]
在一些实施例中,本公开的缀合物具有式(ixe)或(ixf)结构:
[0383][0384][0385]
其中na为核酸;
[0386]
r
z
为可检测标记物,诸如上文所定义;
[0387]
o为1至10范围内的整数;
[0388]
l1和l2为连接基;
[0389]
w包括取代或未取代的香豆素部分或者是取代或未取代的香豆素衍生物或类似物的部分;
[0390]
z为键、
‑
ch
‑
基团、
‑
ch
‑
ch2‑
基团或
‑
ch2‑
ch
‑
基团;并且
[0391]
m和n独立地为1至4范围内的整数。
[0392]
在一些实施例中,r
z
为半抗原。在一些实施例中,r
z
为噁唑、吡唑、噻唑、苯并呋咱、三萜烯、脲、除罗丹明硫脲外的硫脲、除二硝基苯基或三硝基苯基外的硝基芳基、类鱼藤酮、
环木脂体、杂联芳基、偶氮芳基、苯二氮在其他实施例中,r
z
为苯并呋咱或噻唑磺酰胺。
[0393]
在一些实施例中,基于香豆素的试剂(例如具有式(iia)或(iib)的那些)可偶联至抗体的任意部分。抗体中的三个官能团为共价修饰位点:胺(
‑
nh2)、硫醇基团(
‑
sh)和碳水化合物残基(shrestha d等人,2012)。因此,本文所公开的具有至少一个反应性官能团的基于香豆素的试剂中的任一者可偶联至胺残基、硫醇残基和碳水化合物残基或其任意组合。在一些实施例中,基于香豆素的试剂偶联至抗体的fc部分。在其他实施例中,基于香豆素的试剂偶联至抗体的铰链区。在一些实施例中,基于香豆素的试剂偶联至抗体的fc区中的一个或多个以及抗体的铰链区中的一个或多个。实际上,本公开设想到任意组合。
[0394]
主要由于抗体中这些部分的丰度,通常首选氨基基团。但是,氨基基团的随机性可能导致抗体失活。(adamczyk m等人,1999,bioconjug chem;jeanson a等人,1988,j immunol methods;vira s等人,2010,anal biochem;pearson je等人,1998,j immunol methods)。在一些实施例中,一种或多种基于香豆素的试剂偶联至抗体的氨基基团。
[0395]
另一方面,在适当的反应条件下,巯基标记可为铰链区中抗体的两条重链之间的二硫键提供高特异性靶向。由于铰链区远离抗原结合位点,因此据信该修饰能够更好地保持抗体的结合亲和力。在一些实施例中,一种或多种基于香豆素的试剂偶联至抗体的硫醇基团。
[0396]
抗体的fc部分中存在的碳水化合物部分的缀合与硫醇基团相似,使得修饰发生在远离抗原结合位点的
‑
cho基团处。同样,据信碳水化合物的缀合对抗体的结合亲和力的负面影响较小。标记的程度取决于特定抗体的糖基化状态。但是,jeanson a等人(1988,j immunol methods)仍报道了抗体亲和力的损失。在一些实施例中,一种或多种基于香豆素的试剂偶联至抗体的碳水化合物基团。
[0397]
基于香豆素的缀合物的检测
[0398]
在一些实施例中,式(ixa)、(ixb)、(ixc)和(ixd)中任一项的缀合物包括有利于直接检测该缀合物的可检测标记物。例如,如果基于香豆素的缀合物的标记物包含荧光团或发色团,则可以根据本领域的普通技术人员已知的方法直接检测该荧光团或发色团。
[0399]
在其他实施例中,利用特异性试剂能够检测式(ixa)、(ixb)、(ixc)、(ixd)、(ixe)和(ixf)的缀合物中的任一项,并且由此检测组织样品中的靶标。在一些实施例中,利用对缀合物的特定可检测标记物具有特异性的检测试剂。在一些实施例中,检测试剂包含对缀合物的标记物(例如缀合物的半抗原部分)具有特异性的二抗。例如,二抗可以是本身缀合至报告部分的抗标记物抗体或抗半抗原抗体。
[0400]
在一些实施例中,二抗或抗半抗原抗体可缀合至“报告部分”,以实现对式(ixa)、(ixb)、(ixc)、(ixe)和(ixf)的缀合物的检测。上文所述的可检测标记物中的任一者均适用于此目的,即可以用作报告部分。在一些实施例中,二抗的报告部分包括:发色、荧光、磷光和发光分子和材料;催化剂(诸如酶),其将一种物质转化为另一种物质以提供可检测的差异(诸如通过将一种无色物质转化为有色物质,反之亦然,或通过产生沉淀或提高样品浊度)的;半抗原,其可使用其他可检测的带有标记的抗体缀合物通过抗体
‑
半抗原结合相互作用进行检测;以及顺磁性和磁性分子或材料。当然,可检测标记物本身也可间接检测,例如,如果可检测标记物为半抗原,则可以使用对该半抗原(例如抗半抗原抗体)具有特异性的另一种抗体检测该可检测标记物,如本领域的普通技术人员所知以及本文所述。
[0401]
使用式(ixa)、(ixb)、(ixc)和(ixd)中任一项的基于香豆素的缀合物检测靶标的方法以及检测试剂
[0402]
本公开还提供了使用本文所述的式(ixa)、(ixb)、(ixc)、(ixd)、(ixe)和(ixf)的缀合物中的任一者检测生物学样品内的一种或多种靶标的方法。在一些实施例中,式(ixa)、(ixb)、(ixc)、(ixd)、(ixe)和(ixf)中任一项的缀合物可用于简单测定中,以直接或间接检测生物学样品(例如pd
‑
l1、er、pr、her2 cd68、ki67、cd20等)内的特定靶标(例如生物标志物)。在一些实施例中,生物标志物为核酸(例如na、rna,mrna等)。例如,图1示出用缀合至核酸探针的基于香豆素的试剂(诸如使用式(ixe)和(ixf)的那些缀合物)染色(其中基于香豆素的试剂偶联至dig,其中dig可通过应用本领域中已知的合适的检测试剂进行检测)。
[0403]
在一些实施例中,式(ixa)、(ixb)、(ixc)和(ixd)中任一项的缀合物包含一抗(例如,对pd
‑
l1、er、pr、her2 cd68、ki67、cd20等具有特异性的抗体)。在这些实施例中,包含一抗的缀合物可用于直接用缀合物“标记”靶标。在其他实施例中,式(ixa)、(ixb)、(ixc)和(ixd)中任一项的缀合物包含二抗。在这些实施例中,并且如本文更详细地讨论的,可以用一抗(用于ihc)或核酸缀合物(例如用于ish的偶联至半抗原的核酸序列)标记靶标(例如蛋白质靶标或核酸靶标),然后可以用包含二抗(其随后可以得到检测)的式(ixa)、(ixb)、(ixc)和(ixd)中任一项的缀合物标记一抗或核酸缀合物。这些及其他实施例如本文进一步所述。
[0404]
以举例的方式,图2和3示出二抗
‑
基于香豆素的试剂缀合物,其用于标记沉积到组织上的一抗。在这些图中,二抗为抗抗体的抗体;并且缀合物偶联至dig。可以通过使用缀合至酶的抗dig抗体并且随后引入发色团(例如dab)来检测或观测dig。
[0405]
在一些实施例中,基于香豆素的缀合物可包括一抗,其中基于香豆素的一抗缀合物对感兴趣的靶标具有特异性,并且在将基于香豆素的一抗缀合物应用于组织样品的情况下,形成靶标
‑
基于香豆素的一抗缀合物复合物。在应用基于香豆素的一抗缀合物之后,随后可应用检测试剂(例如抗标记物抗体或抗半抗原抗体),使得可以检测靶标
‑
基于香豆素的一抗缀合物复合物。在一些实施例中,检测试剂包含对基于香豆素的一抗缀合物的特定半抗原可检测标记物具有特异性的抗半抗原抗体,其中抗半抗原抗体包含报告部分。然后可观测或以其他方式检测单个靶标。
[0406]
在其他实施例中,首先使组织样品与一抗或核酸探针接触,形成靶标
‑
一抗复合物或靶标
‑
核酸探针复合物。随后,将包含二抗的基于香豆素的缀合物引入组织样品,基于香豆素的缀合物的二抗部分对(i)一抗、(ii)缀合至一抗的标记物或(iii)缀合至核酸探针的标记物具有特异性。应用基于香豆素的二抗缀合物可形成二级复合物,从而对靶标进行“标记”。在应用基于香豆素的二抗缀合物并且形成二级复合物之后,可应用检测试剂(例如抗标记物抗体、抗半抗原抗体)以使得二级复合物可以得到检测。在一些实施例中,检测试剂包含对基于香豆素的二抗缀合物的特定标记物具有特异性的抗半抗原抗体,其中抗半抗原抗体包含报告部分。然后可通过偶联的报告部分观测或以其他方式检测靶标。
[0407]
在本公开的一些方面,提供了多重检测方法,这些方法包括自动化多重检测。图4提供了流程图,示出一种用于靶标的多重检测的方法,其中使组织样品与多种基于香豆素的缀合物同时接触(步骤100),其中每种基于香豆素的缀合物对特定靶标具有特异性,并且
其中每种基于香豆素的缀合物包含不同的可检测标记物。尽管图4示出基于香豆素的缀合物的应用,但是本领域的技术人员将理解,根据样品中的靶标不同(例如,核酸序列、由一抗基于香豆素的缀合物识别的蛋白质靶标或由二抗基于香豆素的缀合物识别的预沉积的一抗),基于香豆素的缀合物可包含基于香豆素的核酸缀合物、基于香豆素的一抗缀合物和基于香豆素的二抗缀合物。
[0408]
在一些实施例中,样品可与两种基于香豆素的缀合物接触,其中每种基于香豆素的缀合物对特定靶标具有特异性,并且其中每种基于香豆素的缀合物包含不同的可检测标记物。在其他实施例中,样品可与三种基于香豆素的缀合物接触,其中每种基于香豆素的缀合物对特定靶标具有特异性,并且其中每种基于香豆素的缀合物包含不同的可检测标记物。
[0409]
可将基于香豆素的缀合物(诸如式(ixa)、(ixb)缀合物中的任一者)作为“集合体”或“混合物”提供给组织样品,其包含特定测定所需的基于香豆素的缀合物中的每一种。据信基于香豆素的缀合物的聚集是可能的,因为据信基于香豆素的缀合物彼此不发生交叉反应,至少其任何交叉反应性未达到影响染色性能的程度。每种基于香豆素的缀合物将结合至其相应的靶标,并且形成可检测靶标
‑
基于香豆素的缀合物复合物。在一些实施例中,在施加基于香豆素的缀合物之后,实施阻断步骤。
[0410]
在同时施加基于香豆素的缀合物(步骤100)之后,将多种检测试剂同时施加于组织样品(步骤110),其中每种检测试剂有利于检测初始施加(作为步骤100)的基于香豆素的缀合物中的一者,并且其中每种检测试剂包含不同的可检测标记物。在其他实施例中,检测试剂是对基于香豆素的缀合物的可检测标记物具有特异性的二抗(例如,对基于香豆素的缀合物的标记物具有特异性的抗标记物抗体)。在其中采用抗半抗原抗体的实施例中,可以将抗半抗原作为“集合体”或“混合物”提供给组织样品,其包含检测靶标
‑
基于香豆素的抗体缀合物复合物所需的抗半抗原抗体中的每一种。在施加检测试剂之后,在一些实施例中,可以用复染剂对组织样品进行染色。可观测或以其他方式检测(例如,同时观测或检测)来自每个报告部分的信号。
[0411]
利用基于香豆素的缀合物进行多重测定的一个实例如下。将第一基于香豆素的抗体缀合物引入组织样品中,该第一基于香豆素的抗体缀合物包含第一可检测标记物并且对第一靶标具有特异性(例如,对pd
‑
l1、er、pr、her2、cd68、ki67、cd20等中的一者具有特异性)。在一些实施例中,该第一基于香豆素的抗体缀合物形成可检测的第一靶标
‑
基于香豆素的抗体缀合物复合物。同时,将第二基于香豆素的抗体缀合物引入样品中以形成靶标
‑
基于香豆素的抗体缀合物复合物,该第二基于香豆素的抗体缀合物包含可检测标记物并且对第二靶标(例如pd
‑
l1、er、pr、her2、cd68、ki67、cd20等中的另一者)具有特异性。与第一基于香豆素的缀合物和第二基于香豆素的缀合物同时进一步引入第三、第四和第n种额外的基于香豆素的缀合物,所述第三、第四和第n种额外的基于香豆素的缀合物对其他靶标具有特异性(形成“n”种靶标
‑
检测探针复合物)并且具有不同的可检测标记物。
[0412]
在沉积基于香豆素的抗体缀合物之后,可根据(当然)其配置直接或间接进行检测。在一些实施例中,引入抗标记物抗体以检测靶标
‑
基于香豆素的抗体缀合物复合物中的每一者。在一些实施例中,抗标记物抗体对基于香豆素的缀合物的不同报告部分具有特异性,并且其中抗标记物抗体各自缀合至不同的可检测标记物。在一些实施例中,可检测试剂
为各自缀合至荧光团的抗标记物抗体。在一些实施例中,同时引入第一、第二和第n抗标记物抗体,其中第一、第二和第n检测试剂中的每一种对不同的基于香豆素的缀合物具有特异性,其中抗标记物抗体中的每一种缀合至荧光团。在其他实施例中,依次引入第一、第二和第n抗标记物抗体,其中第一、第二和第n检测试剂中的每一种对不同的基于香豆素的缀合物具有特异性,并且其中抗标记物抗体中的每一种缀合至酶。
[0413]
作为根据本公开的多重测定的另一个实例,将对第一靶标(例如pd
‑
l1、er、pr、her2)具有特异性的第一基于香豆素的抗体缀合物引入组织样品中,该第一基于香豆素的抗体缀合物具有第一可检测标记物。在一些实施例中,该第一基于香豆素的抗体缀合物形成可检测的第一靶标
‑
基于香豆素的抗体缀合物复合物。将对第二靶标(例如pd
‑
l1、er、pr、her2)具有特异性的第二基于香豆素的抗体缀合物同时或依次引入样品中,以形成第二靶标
‑
基于香豆素的抗体缀合物复合物,该基于香豆素的抗体缀合物具有第二可检测标记物。可与第一基于香豆素的抗体缀合物和/或第二基于香豆素的抗体缀合物依次或同时进一步引入分别对其他靶标具有特异性的第三、第四和第n种额外的基于香豆素的抗体缀合物(形成“n”种靶标
‑
基于香豆素的抗体缀合物复合物),其中第三、第四和第n种基于香豆素的抗体缀合物各自具有不同的可检测标记物。在沉积基于香豆素的抗体缀合物后,可以对它们进行检测。在一些实施例中,引入额外的检测试剂以检测靶标,并且这些额外的检测试剂包括本文所述的那些(例如显色检测试剂)。在一些实施例中,依次引入第一检测试剂、第二检测试剂和第n检测试剂,其中该第一检测试剂、第二检测试剂和第n检测试剂中的每一种包含(i)对基于香豆素的抗体缀合物的可检测标记物中的每一种具有特异性的二抗,即抗标记物抗体,其中该二抗缀合至酶;以及(ii)显色底物;其中第一显色底物、第二显色底物和第n显色底物不同。
[0414]
在其他实施例中,多重检测方法包括以下步骤:(i)使生物学样品与第一基于香豆素的抗体缀合物接触,以形成第一靶标
‑
基于香豆素的抗体缀合物复合物;(ii)使生物学样品与第一标记缀合物接触,其中第一标记缀合物包含第一酶(其中第一标记缀合物为抗标记物抗体,其特异性结合至第一基于香豆素的抗体缀合物并且配置为用酶标记靶标);(iii)使生物学样品与第一信号传导缀合物接触,该第一信号传导缀合物包含第一潜在反应性部分和第一显色部分(参见例如美国专利申请第13/849,160号,其公开内容全文以引用方式并入本文,描述了信号传导缀合物及其组成成分);(iv)灭活第一酶,诸如通过使样品与第一酶灭活组合物接触以使生物学样品中包含的第一酶基本上失活或完全失活。
[0415]
在第一酶失活(可选)后,多重检测方法进一步包括以下步骤:(v)使生物学样品与第二基于香豆素的抗体缀合物接触以形成第二靶标
‑
基于香豆素的抗体缀合物;(vi)使生物学样品与第二标记缀合物接触,其中第二标记缀合物包含第二酶(其中第二标记缀合物为抗标记物抗体,其特异性结合至第二基于香豆素的抗体缀合物并且配置为用酶标记靶标);(vii)使生物学样品与第二信号传导缀合物接触,该第二信号传导缀合物包含第二潜在反应性部分和第二显色部分;(viii)灭活第二酶,诸如通过使样品与第一酶灭活组合物接触以使生物学样品中包含的第一酶基本上失活或完全失活。
[0416]
在第二酶失活后,可重复该方法,使得可以引入额外的基于香豆素的抗体缀合物以及额外的检测试剂,以实现对其他靶标的检测。在引入所有基于香豆素的抗体缀合物(及其他检测探针)和相应的检测试剂或试剂盒后,该方法进一步包括以下步骤:对样品和/或
来自第一显色部分、第二显色部分和第n显色部分的检测信号进行复染,其中第一显色部分、第二显色部分和第n显色部分中的每一者各不相同。替代性地,可同时或依次添加基于香豆素的抗体缀合物,但是在添加任何标记缀合物之前进行。作为另一个实例,最初可依次施加三种基于香豆素的抗体缀合物,其在引入任何检测试剂之前进行,然后依次添加检测试剂中的每一种。
[0417]
在其中需要依次检测多种靶标并且检测采用酶的多重检测的情况下,希望在连续检测步骤之间灭活任何试剂或内源性酶。因此,据信存在于任一检测步骤中的酶均不干扰随后的检测步骤中的酶。据信其继而改善了在多重测定中使用的不同可检测部分的观测和检测。本领域中已知的任何酶灭活组合物均可用于此目的。在一些实施例中,在每个检测步骤之后,施加酶灭活组合物以灭活试剂或内源性酶。示例性酶灭活组合物公开于美国专利公开第2018/0120202号中,其公开内容通过引用整体并入本文。
[0418]
在一些实施例中,变性步骤防止第一组检测试剂中所用的酶作用于第二底物。在一些实施例中,变性剂是第一检测试剂组中使酶变性的物质。在一些实施例中,变性剂为例如甲酰胺、烷基取代的酰胺、脲或基于脲的变性剂、硫脲、盐酸胍或其衍生物。烷基取代的酰胺的实例包括但不限于n
‑
丙基甲酰胺、n
‑
丁基甲酰胺、n
‑
异丁基甲酰胺和n,n
‑
二丙基甲酰胺。在一些实施例中,变性剂提供于缓冲液中。例如,甲酰胺可提供于杂交缓冲液中,该杂交缓冲液包含20mm硫酸葡聚糖(50
‑
57%甲酰胺,ultrapure甲酰胺储备液)、2
×
ssc(20
×
ssc储备液,包含0.3m柠檬酸盐和3m nacl)、2.5mm edta(0.5m edta储备液)、5mm tris(ph 7.4;1mm tris,ph 7.4储备液)、0.05%brij
‑
35(10%储备液,包含聚氧乙烯(23)十二烷基醚,ph 7.4)。在一些实施例中,将样品用变性剂处理一段时间,并且在足以使第一靶标探针检测酶(例如碱性磷酸酶)变性的条件下进行处理。在一些实施例中,将样品在约37℃用变性剂处理约15分钟至30分钟,优选约20分钟至24分钟。在一些实施例中,将样品用变性剂处理一段时间,并且在足以使靶酶变性并同时保留第二核酸探针与靶标的杂交的条件下进行处理。
[0419]
对于那些采用缀合至酶的抗标记物抗体的实施例,使用适合将信号传导缀合物或显色底物与生物学样品一起引入的条件,并且通常包括提供以下反应缓冲液或溶液,其包含过氧化物(例如,过氧化氢)并且盐浓度和ph适合于允许或促进酶发挥其所需的功能。一般而言,该方法的这一步骤在约35℃至约40℃范围内的温度下进行,但是本领域技术人员将能够选择适合于酶的合适温度范围并且向所选缀合物发出信号。例如,据信这些条件允许酶与过氧化物反应并且促进自由基形成于信号传导缀合物的潜在反应性部分上。潜在反应性部分以及整个信号传导缀合物将共价沉积至生物学样品上,特别是沉积至固定化的酶缀合物近侧的一个或多个酪氨酸残基、酶缀合物的酶部分的酪氨酸残基和/或酶缀合物的抗体部分的酪氨酸残基处。然后用光照射生物学样品,并且可通过吸收信号传导缀合物的显色部分所产生的光来检测靶标。
[0420]
与其他特异性结合实体结合的式(ixa)、(ixb)、(ixc)、(ixd)、(ixe)和(ixf)中任一项的缀合物的检测方法
[0421]
在本公开的一些方面,将式(ixa)、(ixb)、(ixc)和(ixd)中任一项的缀合物与其他特异性结合实体结合使用以实现对组织样品中的靶标的多重检测。本领域技术人员将认识到,上述方法和程序中的任一者均可相应地调整以用于采用式(ixa)、(ixb)、(ixc)和(ixd)
中任一项的缀合物及其他特异性结合实体。在一些实施例中,其他特异性结合实体包括用于原位杂交的核酸和用于ihc的未修饰的抗体。如本文所用,术语“未修饰的抗体”或“多种未修饰的抗体”是指不包含如本文所公开的基于香豆素的试剂的那些抗体,但是包括缀合至半抗原或另一标记物的那些抗体。本质上,“未修饰的抗体”是传统上用于ihc测定中的天然抗体,它们对特定靶标(例如抗cd3抗体)具有特异性,并且可以用抗物种的二抗或(如果包含标记)抗标记物抗体进行检测。以举例的方式,可以用山羊抗兔抗体检测兔抗cd3抗体。同样地,可以用抗半抗原抗体检测缀合至半抗原的兔抗cd3抗体。例如,可以将对er具有特异性的未修饰的抗体引入样品中,然后进行检测,而本公开的对pr具有特异性的基于香豆素的缀合物可同时或依次引入相同的样品中,然后进行检测。
[0422]
使用式(iiia)、(iiib)、(iiic)和(iiid)的基于香豆素的试剂检测样品中的靶标的方法
[0423]
本公开还提供了使用基于香豆素的试剂(例如式(iiia)、(iiib)、(iiic)和(iiid)的那些化合物)检测组织样品内的一种或多种靶标的方法。
[0424]
在一些实施例中,式(iiia)、(iiib)、(iiic)和(iiid)化合物具有酶反应部分(例如其中“a”为酪酰胺衍生物或醌甲基化物衍生物)并且具有可检测标记物(例如其中“b”为半抗原),使这些化合物与结合靶标的酶(例如,已沉积至生物学样品上的抗体
‑
酶缀合物或核酸
‑
酶缀合物)接触,以产生反应中间体。例如,抗体
‑
过氧化物酶缀合物可沉积至靶标上,并且过氧化物酶可在其引入样品时与式(iiia)、(iiib)、(iiic)和(iiid)中任一项的化合物的酶反应部分反应。以另一个实例举例,核酸
‑
磷酸酶缀合物可与样品内的靶标杂交,并且缀合的磷酸酶可在其引入样品时与式(iiia)、(iiib)、(iiic)和(iiid)中任一项的化合物的酶反应部分反应。
[0425]
在一些实施例中,反应性中间体与生物学样品上或内部的亲核试剂形成共价键,从而提供固定化的组织
‑
香豆素基化合物复合物。借助式(iiia)、(iiib)、(iiic)和(iiid)化合物的可检测标记物,可观测组织
‑
香豆素基化合物复合物。例如,如果可检测标记物为半抗原,可引入缀合至报告部分(例如发色团或荧光团)的抗半抗原抗体以检测组织
‑
香豆素基化合物复合物。使用具有酶反应部分的化合物进行检测和观测的方法描述于美国专利公开第2017/0089911号和第2012/0171668号中,其公开内容通过引用整体并入本文。
[0426]
图5示出具有偶联至酪酰胺部分和半抗原的具有式(iiia)、(iiib)、(iiic)和(iiid)中的任一项的基于香豆素的部分的用途,并且比较了对那些直接偶联至dig的酪酰胺部分的染色性能。
[0427]
使用式(iiie)和(iiif)的点击缀合物检测样品中的靶标的方法
[0428]
式(iiie)和(iiif)的试剂可用于通过使用某些点击缀合物检测样品内的靶标。在一些实施例中,使具有式(iiie)或(iiif)的试剂与结合靶标的酶(例如,结合靶标的酶可以是已经沉积在生物学样品上的抗体
‑
酶缀合物)接触以产生反应性中间体,该试剂包括酶反应部分并且进一步包括能够参与点击化学反应的官能团。在一些实施例中,反应性中间体与生物学样品上或内部的亲核试剂形成共价键,从而提供固定化的组织
‑
香豆素基化合物复合物。然后,固定化的组织
‑
点击缀合物复合物可与点击缀合物反应,该点击缀合物包含报告部分并且包含能够参与点击化学反应的官能团,条件是点击缀合物和固定化的组织
‑
点击缀合物复合物具有可彼此反应以形成共价键的反应性官能团。固定化的组织
‑
点击缀
合物复合物与点击缀合物的反应产物产生固定化组织
‑
点击加合物复合物。组织
‑
点击加合物复合物可借助链接的报告部分所发送的信号来检测。可用于与固定化的组织
‑
点击缀合物复合物反应的点击缀合物包括pct公开第wo/2018/002016号中描述的那些,其公开内容通过引用整体并入本文。检测方法的进一步细节也公开于pct公开第wo/2018/002016号中,并且这些公开内容各自同样通过引用整体并入本文。
[0429]
基于香豆素的试剂的合成
[0430]
合成各种类型的基于香豆素的试剂诸如式(ia)或(ib)的试剂中的任一种的方法如下文所述。
[0431]7‑
羟基
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
羧酸
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯的合成
[0432]
将7
‑
羟基
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
羧酸(sigma
‑
aldrich,500mg,2.27mmol)溶于10ml无水dmf中,并且向该溶液中加入dsc(641mg,2.50mmol)和dmap(416mg,3.40mmol)。将溶液在室温(r.t.)下搅拌1小时,然后用50ml dcm稀释。将该溶液用50ml水洗涤3次,并且用50ml盐水再次洗涤,然后在真空中浓缩,再利用硅胶层析法进行纯化(2%异丙醇/dcm至10%异丙醇/dcm),以得到632mg(产率86%)7
‑
羟基
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
羧酸
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯(化合物10)。
[0433][0434]
(1
‑
(7
‑
羟基
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
基)
‑1‑
氧代
‑
6,9,12
‑
三氧杂
‑2‑
氮杂十五烷
‑
15
‑
基)氨基甲酸叔丁酯的合成
[0435]
在本实例中,将连接基基团引入香豆素部分。
[0436]
将7
‑
羟基
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
羧酸
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯(500mg,1.65mmol)溶于10ml dcm中,并且向该溶液中加入(3
‑
(2
‑
(3
‑
氨基丙氧基)乙氧基)丙基)氨基甲酸叔丁酯(547mg,1.98mmol)和三乙胺(334mg,3.3mmol),然后将反应混合物在室温搅拌16h。反应完成后,将反应混合物在减压下浓缩,并且利用硅胶层析法进行纯化(2%甲醇/dcm至10%甲醇/dcm),以得到688mg(产率82%)(1
‑
(7
‑
羟基
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
基)
‑1‑
氧代
‑
6,9,12
‑
三氧杂
‑2‑
氮杂十五烷
‑
15
‑
基)氨基甲酸叔丁酯(化合物11),其为黄色油状物。
[0437][0438]2‑
((3
‑
((2,2
‑
二甲基
‑4‑
氧代
‑
3,9,12,15
‑
四氧杂
‑5‑
氮杂十八烷
‑
18
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸叔丁酯的合成
[0439]
将(1
‑
(7
‑
羟基
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
基)
‑1‑
氧代
‑
6,9,12
‑
三氧杂
‑2‑
氮杂十五烷
‑
15
‑
基)氨基甲酸叔丁酯(407mg,0.80mmol)溶于10ml无水dmf中,并且向该溶液中加入2
‑
溴乙酸叔丁酯(172mg,0.884mmol)和碳酸钾(330mg,2.41mmol),然后将反应混合物在油浴中于60℃搅拌。搅拌3h后,将反应混合物用70ml dcm稀释,然后将溶液用100ml水洗涤3次,并且用100ml盐水洗涤一次。将溶液在真空中浓缩,然后利用硅胶层析法进行纯化(2%甲醇/dcm至12%甲醇/dcm),以得到398mg(产率80%)2
‑
((3
‑
((2,2
‑
二甲基
‑4‑
氧代
‑
3,9,12,15
‑
四氧杂
‑5‑
氮杂十八烷
‑
18
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸叔丁酯(化合物12)。
[0440][0441]2‑
((3
‑
((3
‑
(2
‑
(2
‑
(3
‑
氨基丙氧基)乙氧基)乙氧基)丙基)
‑
氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸的合成
[0442]
将2
‑
((3
‑
((2,2
‑
二甲基
‑4‑
氧代
‑
3,9,12,15
‑
四氧杂
‑5‑
氮杂十八烷
‑
18
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸叔丁酯(398mg,0.64mmol)溶于20ml 35%tfa/dcm中,并且在r.t搅拌,直至通过hplc确定反应完成(约4h)。然后将反应混合物在真空中浓缩,与甲苯共沸3次,并且在高真空下过夜干燥,以得到372mg 2,2,2
‑
三氟乙酸化合物与2
‑
((3
‑
((3
‑
(2
‑
(2
‑
(3
‑
氨基丙氧基)乙氧基)乙氧基)丙基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸(化合物13)(1∶1),其直接使用而不经进一步纯化。
[0443][0444]2‑
((3
‑
((l
‑
(((3s.10s,12r,13s,14s,17r)
‑
12,14
‑
二羟基
‑
10,13
‑
二甲基
‑
17
‑
(5
‑
氧代
‑
2,5
‑
二氢呋喃
‑3‑
基)十六氢
‑
1h
‑
环戊二烯并[a]菲
‑3‑
基)氧基)
‑
2,10
‑
二氧代
‑
15,18,21
‑
三氧杂
‑
3,11
‑
二氮杂二十四烷
‑
24
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸的合成
[0445]
在本实例中,引入半抗原部分。
[0446]
向7
‑
(2
‑
(((3s,10s,12r,13s,14s,17r)
‑
12,14
‑
二羟基
‑
10,13
‑
二甲基
‑
17
‑
(5
‑
氧代
‑
2,5
‑
二氢呋喃
‑3‑
基)十六氢
‑
1h
‑
环戊二烯并[a]菲
‑3‑
基)氧基)乙酰氨基)庚酸
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯(90mg,0.137mmol)在3ml无水dmf中的溶液中加入2
‑
((3
‑
((3
‑
(2
‑
(2
‑
(3
‑
氨基丙氧基)乙氧基)乙氧基)丙基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸2,2,2
‑
三氟乙酸盐(1∶1)(120mg,0.205mmol)和huenigs碱(82μl,0.480mmol),并且将反应混合物在r.t搅拌过夜。将粗制反应产物通过0.2微米过滤器过滤,并且利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到116mg(产率83%)2
‑
((3
‑
((1
‑
(((3s,10s,12r,13s,14s,17r)
‑
12,14
‑
二羟基
‑
10,13
‑
二甲基
‑
17
‑
(5
‑
氧代
‑
2,5
‑
二氢呋喃
‑3‑
基)十六氢
‑
1h
‑
环戊二烯并[a]菲
‑3‑
基)氧基)
‑
2,10
‑
二氧代
‑
15,18,21
‑
三氧杂
‑
3,11
‑
二氮杂二十四烷
‑
24
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸(化合物14),其为灰白色粉末。
[0447][0448]1‑
((3
‑
((1
‑
(((3s,10s,12r,13s,14s,17r)
‑
12,14
‑
二羟基
‑
10,13
‑
二甲基
‑
17
‑
(5
‑
氧代
‑
2,5
‑
二氢呋喃
‑3‑
基)十六氢
‑
1h
‑
环戊二烯并[a]菲
‑3‑
基)氧基)
‑
2,10
‑
二氧代
‑
15,
18,21
‑
三氧杂
‑
3,11
‑
二氮杂二十四烷
‑
24
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸的合成
[0449]
在本实例中,将第二连接基引入香豆素部分。
[0450]
向2
‑
((3
‑
((1
‑
(((3s,10s,12r,13s,14s,17r)
‑
12,14
‑
二羟基
‑
10,13
‑
二甲基
‑
17
‑
(5
‑
氧代
‑
2,5
‑
二氢呋喃
‑3‑
基)十六氢
‑
1h
‑
环戊二烯并[a]菲
‑3‑
基)氧基)
‑
2,10
‑
二氧代
‑
15,18,21
‑
三氧杂
‑
3,11
‑
二氮杂二十四烷
‑
24
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸(130mg,0.129mmol)在10ml无水dmf中的溶液中加入n
‑
羟基琥珀酰亚胺(19mg,0.167mmol)和1.0m dcc的dcm溶液(167μl,0.167mmol),并且将反应混合物在r.t.搅拌,直至通过hplc确定活性酯的形成完成(约4小时)。将脲副产物通过过滤去除,并且向溶液中加入1
‑
氨基
‑
3,6,9,12
‑
四氧杂十五烷
‑
15
‑
酸(44mg,0.167mmol)和huenigs碱(66μl,0.167mmol),并且将反应混合物在r.t.搅拌过夜。将反应混合物浓缩,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到125mg(产率76%)1
‑
((3
‑
((1
‑
(((3s,10s,12r,13s,14s,17r)
‑
12,14
‑
二羟基
‑
10,13
‑
二甲基
‑
17
‑
(5
‑
氧代
‑
2,5
‑
二氢呋喃
‑3‑
基)十六氢
‑
1h
‑
环戊二烯并[a]菲
‑3‑
基)氧基)
‑
2,10
‑
二氧代
‑
15,18,21
‑
三氧杂
‑
3,11
‑
二氮杂二十四烷
‑
24
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(化合物15),其为灰白色粉末。
[0451][0452]1‑
((3
‑
((1
‑
(((3s,10s,12r,13s,14s,17r)
‑
12,14
‑
二羟基
‑
10,13
‑
二甲基
‑
17
‑
(5
‑
氧代
‑
2,5
‑
二氢呋喃
‑3‑
基)十六氢
‑
1h
‑
环戊二烯并[a]菲
‑3‑
基)氧基)
‑
2,10
‑
二氧代
‑
15,18,21
‑
三氧杂
‑
3,11
‑
二氮杂二十四烷
‑
24
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯的合成
[0453]
在本实例中,对起始材料进行衍生化,使得所得试剂能够偶联至大分子,诸如蛋白质或抗体。
[0454]
向1
‑
((3
‑
((1
‑
(((3s,10s,12r,13s,14s,17r)
‑
12,14
‑
二羟基
‑
10,13
‑
二甲基
‑
17
‑
(5
‑
氧代
‑
2,5
‑
二氢呋喃
‑3‑
基)十六氢
‑
1h
‑
环戊二烯并[a]菲
‑3‑
基)氧基)
‑
2,10
‑
二氧代
‑
15,18,21
‑
三氧杂
‑
3,11
‑
二氮杂二十四烷
‑
24
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(25mg,0.02mmol)在10ml无水dmf中的溶液中加入n
‑
羟基琥珀酰亚胺(2.3mg,0.03mmol)和1.0m dcc的dcm溶液(30μl,0.03mmol),并且将反应混合物在r.t.搅拌,直至通过hplc确定活性酯的形成完成(约4小时)。将脲副产物通过过滤去除,浓缩反应混合物,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到22mg(产率80%)1
‑
((3
‑
((1
‑
(((3s,10s,12r,13s,14s,17r)
‑
12,14
‑
二羟基
‑
10,13
‑
二甲基
‑
17
‑
(5
‑
氧代
‑
2,5
‑
二氢呋喃
‑3‑
基)十六氢
‑
1h
‑
环戊二烯并[a]菲
‑3‑
基)氧基)
‑
2,10
‑
二氧代
‑
15,18,21
‑
三氧杂
‑
3,11
‑
二氮杂二十四烷
‑
24
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯(化合物16),其为灰白色粉末。
[0455][0456]1‑
((3
‑
((1
‑
(((3s,10s,12r,13s,14s,17r)
‑
12,14
‑
二羟基
‑
10,13
‑
二甲基
‑
17
‑
(5
‑
氧代
‑
2,5
‑
二氢呋喃
‑3‑
基)十六氢
‑
1h
‑
环戊二烯并[a]菲
‑3‑
基)氧基)
‑
2,10
‑
二氧代
‑
15,18,21
‑
三氧杂
‑
3,11
‑
二氮杂二十四烷
‑
24
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑4‑
羟基苯乙基酯的合成
[0457]
在本实例中,引入酶反应部分,具体地引入酪酰胺部分。
[0458]
向1
‑
((3
‑
((1
‑
(((3s,10s,12r,13s,14s,17r)
‑
12,14
‑
二羟基
‑
10,13
‑
二甲基
‑
17
‑
(5
‑
氧代
‑
2,5
‑
二氢呋喃
‑3‑
基)十六氢
‑
1h
‑
环戊二烯并[a]菲
‑3‑
基)氧基)
‑
2,10
‑
二氧代
‑
15,18,21
‑
三氧杂
‑
3,11
‑
二氮杂二十四烷
‑
24
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯(20mg,0.015mmol)在2ml无水dmf的溶液中加入酪胺(4.1mg,0.030mmol)和三乙胺(4.2μl,0.030mmol),并且将反应混合物在r.t.搅拌过夜。将粗制反应产物通过0.2微米过滤器过滤,并且利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到17mg(产率81%)1
‑
((3
‑
((1
‑
(((3s,10s,12r,13s,14s,17r)
‑
12,14
‑
二羟基
‑
10,13
‑
二甲基
‑
17
‑
(5
‑
氧代
‑
2,5
‑
二氢呋喃
‑3‑
基)十六氢
‑
1h
‑
环戊二烯并[a]菲
‑3‑
基)氧基)
‑
2,10
‑
二氧代
‑
15,18,21
‑
三氧杂
‑
3,11
‑
二氮杂二十四烷
‑
24
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑4‑
羟基苯乙基酯(化合物17),其为灰白色粉末。
[0459][0460]2‑
((3
‑
((2,2
‑
二甲基
‑4‑
氧代
‑
3,9,12,15
‑
四氧杂
‑5‑
氮杂十八烷
‑
18
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸的合成
[0461]
向2
‑
((3
‑
((3
‑
(2
‑
(2
‑
(3
‑
氨基丙氧基)乙氧基)乙氧基)丙基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸的2,2,2
‑
三氟乙酸盐(1∶1)(8.03g,13.83mmol)在50ml二噁烷/水(1∶1)中的溶液中加入(boc)2o(3.02g,13.83mmol)和三乙胺(4.38ml,31.46),并且将反应混合物在r.t.搅拌过夜。将反应混合物用100ml dcm稀释,然后用50ml水洗涤2次,并且用盐水洗涤一次。将有机相通过mgso4塞过滤进行干燥,然后在浓缩后利用硅胶层析法进行纯化(4%甲醇/dcm至15%甲醇/dcm),以得到6.48g(产率83%)2
‑
((3
‑
((2,2
‑
二甲基
‑4‑
氧代
‑
3,9,12,15
‑
四氧杂
‑5‑
氮杂十八烷
‑
18
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸(化合物20)。
[0462][0463]1‑
((3
‑
((2,2
‑
二甲基
‑4‑
氧代
‑
3,9,12,15
‑
四氧杂
‑5‑
氮杂十八烷
‑
18
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸的合成
[0464]
向2
‑
((3
‑
((2,2
‑
二甲基
‑4‑
氧代
‑
3,9,12,15
‑
四氧杂
‑5‑
氮杂十八烷
‑
18
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸(6.48g,11.4mmol)在40ml无水dcm的溶液中加入1.0m dcc的dcm溶液(17.16ml,17.16mmol)和nhs(1.97g,17.16mmol),并且将反应混合物在r.t.搅拌,直至酯形成反应完成(5h)。将脲副产物通过过滤去除,并且向溶液中加入1
‑
氨基
‑
3,6,9,12
‑
四氧杂十五烷
‑
15
‑
酸(4.55g,17.16mmol)和huenigs碱(2.22g,17.16mmol),并且将反应混合物在r.t.搅拌过夜。将反应混合物浓缩,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到7.42g(产率80%)1
‑
((3
‑
((2,2
‑
二甲基
‑4‑
氧代
‑
3,9,12,15
‑
四氧杂
‑5‑
氮杂十八烷
‑
18
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(化合物21)。
[0465][0466]1‑
((3
‑
((3
‑
(2
‑
(2
‑
(3
‑
氨基丙氧基)乙氧基)乙氧基)
‑
丙基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(1∶1)的合成
[0467]
将1
‑
((3
‑
((2,2
‑
二甲基
‑4‑
氧代
‑
3,9,12,15
‑
四氧杂
‑5‑
氮杂十八烷
‑
18
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(7.42g,9.12mmol)溶于50ml 35%tfa/dcm中,并且在r.t.搅拌,直至通过hplc确定反应完成(约4h)。然后将反应混合物在真空中浓缩,与甲苯共沸3次,并且在高真空下过夜干燥,以得到7.92g 1
‑
((3
‑
((3
‑
(2
‑
(2
‑
(3
‑
氨基丙氧基)乙氧基)乙氧基)丙基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸的2,2,2
‑
三氟乙酸盐(化合物22)(1∶1),其为淡黄色油状物。
[0468][0469]1‑
((3
‑
((1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑1‑
氧代
‑
6,9,12
‑
三氧杂
‑2‑
氮杂十五烷
‑
15
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸的合成
[0470]
向苯并[c][1,2,5]噁二唑
‑5‑
羧酸(13mg,0.079mmol)在5ml无水dcm中的溶液中加入1.0m dcc的dcm溶液(100μl,0.10mmol)和n
‑
羟基琥珀酰亚胺(12mg,0.10mmol),并且将该
溶液在r.t.搅拌,直至通过hplc确定反应完成(约4h)。将脲副产物通过过滤去除,并且向溶液中加入1
‑
((3
‑
((3
‑
(2
‑
(2
‑
(3
‑
氨基丙氧基)乙氧基)乙氧基)丙基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸的2,2,2
‑
三氟乙酸盐(1∶1)(82.8mg,0.10mmol)和三乙胺(30mg,0.30mmol),并且将反应混合物在r.t.搅拌过夜。将反应混合物浓缩,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到42mg(产率62%)1
‑
((3
‑
((1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑1‑
氧代
‑
6,9,12
‑
三氧杂
‑2‑
氮杂十五烷
‑
15
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(化合物23)。
[0471][0472]1‑
((3
‑
((1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑1‑
氧代
‑
6,9,12
‑
三氧杂
‑2‑
氮杂十五烷
‑
15
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯的合成
[0473]
向1
‑
((3
‑
((1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑1‑
氧代
‑
6,9,12
‑
三氧杂
‑2‑
氮杂十五烷
‑
15
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(42mg,0.049mmol)在10ml的无水dcm溶液中加入1.0m dcc的dcm溶液(60μl,0.06mmol)和n
‑
羟基琥珀酰亚胺(12mg,0.06mmol),并且将溶液在r.t.搅拌,直至通过hplc确定反应完成(约4h)。将脲副产物通过过滤去除,浓缩反应混合物,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到38mg(产率81%)1
‑
((3
‑
((1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑1‑
氧代
‑
6,9,12
‑
三氧杂
‑2‑
氮杂十五烷
‑
15
‑
基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯(化合物24)。
[0474][0475]
n
‑
(1
‑
(7
‑
((21
‑
(4
‑
羟基苯基)
‑
2,18
‑
二氧代
‑
6,9,12,15
‑
四氧杂
‑
3,19
‑
二氮杂二十一烷基)氢基)
‑2‑
氢代
‑
2h
‑
色烯
‑3‑
基)
‑1‑
氢代
‑
6,9,12
‑
三氢杂
‑2‑
氮杂十五烷
‑
15
‑
基)苯并[c][1,2,5]噁二唑
‑5‑
甲酰胺的合成
[0476]
向苯并[c][1,2,5]噁二唑
‑5‑
羧酸(13mg,0.079mmol)在5ml无水dcm中的溶液中加入1.0m dcc的dcm溶液(100μl,0.10mmol)和n
‑
羟基琥珀酰亚胺(12mg,0.10mmol),并且将该溶液在r.t.搅拌,直至通过hplc确定反应完成(约4h)。将脲副产物通过过滤去除,并且向溶液中加入n
‑
(3
‑
(2
‑
(2
‑
(3
‑
氨基丙氧基)乙氧基)乙氧基)丙基)
‑7‑
((21
‑
(4
‑
羟基苯基)
‑
2,18
‑
二氧代
‑
6,9,12,15
‑
四氧杂
‑
3,19
‑
二氮杂二十一烷基)氧基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺2,2,2
‑
三氟乙酸叔丁酯(94.7mg,0.10mmol)和三乙胺(30mg,0.30mmol),并且将反应混合
物在r.t.搅拌过夜。将反应混合物浓缩,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到40mg(产率52%)n
‑
(1
‑
(7
‑
((21
‑
(4
‑
羟基苯基)
‑
2,18
‑
二氧代
‑
6,9,12,15
‑
四氧杂
‑
3,19
‑
二氮杂二十一烷基)氧基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
基)
‑1‑
氧代
‑
6,9,12
‑
三氧杂
‑2‑
氮杂十五烷
‑
15
‑
基)苯并[c][1,2,5]噁二唑
‑5‑
甲酰胺(化合物25)。
[0477][0478]3‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)丙酸叔丁酯的合成
[0479]
向2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰氯(1.01g,3.97mmol)在30ml无水dcm中的溶液中加入3
‑
氨基丙酸叔丁酯盐酸盐(1.44g,7.94mmol)和三乙胺(2.21ml,15.88mmol),并且将反应混合物在r.t.搅拌1小时。将反应混合物浓缩至约5ml,然后利用硅胶层析法进行纯化(1%甲醇/dcm至15%甲醇/dcm),以得到1.33g(产率92%)3
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)丙酸叔丁酯(化合物30)。
[0480][0481]3‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)丙酸的合成
[0482]
将3
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)丙酸叔丁酯(1.33g,3.65mmol)吸收于30ml的30%tfa/dcm中,并且将反应混合物在r.t.搅拌,直至通过hplc确定反应完成(约3h)。然后将反应混合物在真空中浓缩,与甲苯共沸3次,并且在高真空下干燥过夜,以得到3
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)丙酸(化合物31),其直接使用而不经进一步纯化。
[0483][0484]2‑
((3
‑
((l7
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸的合成
[0485]
向3
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)丙酸(325mg,1.06mmol)在20ml无水dcm中的溶液中加入1.0m dcc的dcm溶液(1.27ml,1.27mmol)和n
‑
羟基琥珀酰亚胺(146mg,1.27mmol),并且将溶液在r.t搅拌,直至通过hplc确定反应完成(约4h)。将脲副产物通过过滤去除,并且向溶液中加入2
‑
((3
‑
((3
‑
(2
‑
(2
‑
(3
‑
氨基丙氧基)乙氧基)乙氧基)丙基)氨基甲酰基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸2,2,2
‑
三氟乙酸盐(1:1)(850mg,1.46mmol)和三乙胺(442μl,3.17mmol),然后将反应混合物在室温搅拌过夜。将粗制反应产物通过0.2微米过滤器过滤,并且利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到627mg(产率79%)2
‑
((3
‑
((17
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸(化合物32)。
[0486][0487]1‑
((3
‑
((l7
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸的合成
[0488]
向2
‑
((3
‑
((l7
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸(142mg,0.188mmol)在10ml的无水dcm溶液中加入1.0m dcc的dcm溶液(0.226μl,0.226mmol)和n
‑
羟基琥珀酰亚胺(26mg,0.226mmol),并且将溶液在r.t.搅拌,直至通过hplc确定反应完成(约3.5h)。将脲副产物通过过滤去除,并且向溶液中加入1
‑
氨基
‑
3,6,9,12
‑
四氧杂十五烷
‑
15
‑
酸(60mg,0.226mmol)和三乙胺(79μl,0.564mmol),然后将反应混合物在r.t.搅拌过夜。将反应混合物浓缩,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到158mg(产率84%)1
‑
((3
‑
((17
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(化合物33)。
[0489][0490]1‑
((3
‑
((17
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯的合成
[0491]
向1
‑
((3
‑
((l7
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(250mg,0.216mmo1)在10ml的无水dcm溶液中加入1.0m dcc的dcm溶液(275μl,0.275mmol)和n
‑
羟基琥珀酰亚胺(32mg,0.275mmol),并且将溶液在r.t.搅拌,直至通过hplc确定反应完成(约3h)。将脲副产物通过过滤去除,浓缩反应混合物,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到193mg(产率83%)1
‑
((3
‑
((17
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯(化合物34)。
[0492][0493]
n
‑
(17
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)
‑7‑
((21
‑
(4
‑
羟基苯基)
‑
2,18
‑
二氧代
‑
6,9,12,15
‑
四氧杂
‑
3,19
‑
二氮杂二十一烷基)氧基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺的合成
[0494]
向2,5
‑
二氧代吡咯烷
‑1‑
基1
‑
((3
‑
((17
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基酯(50mg,0.045mmol)在5ml无水dcm中的溶液中加入酪胺(8mg,0.059mmol)和三乙胺(19μl,0.135mmol),并且将反应混合物在r.t.搅拌过夜。将粗制反应产物通过0.2微米过滤器过滤,并且利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到43mg(产率86%)n
‑
(17
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)
‑7‑
((21
‑
(4
‑
羟基苯基)
‑
2,18
‑
二氧代
‑
6,9,12,15
‑
四氧杂
‑
3,19
‑
二氮杂二十一烷基)氧基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺(化合物35)。
[0495][0496]2‑
((3
‑
((17
‑
(2,5
‑
二氧代
‑
2,5
‑
二氢
‑
1h
‑
吡咯
‑1‑
基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸的合成
[0497]
向3
‑
(2,5
‑
二氧代
‑
2,5
‑
二氢
‑
1h
‑
吡咯
‑1‑
基)丙酸(500mg,2.96mmol)在20ml无水dcm中的溶液中加入1.0m dcc的dcm溶液(3.55ml,3.55mmol)和n
‑
羟基琥珀酰亚胺(408mg,3.55mmol),并且将溶液在r.t搅拌,直至通过hplc确定反应完成(约1h)。将脲副产物通过过滤去除,并且向溶液中加入2
‑
((3
‑
((3
‑
(2
‑
(2
‑
(3
‑
氨基丙氧基)乙氧基)乙氧基)丙基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸2,2,2
‑
三氟乙酸盐(1∶1)(1.20g,2.00mmol)和三乙胺(700μl,5.00mmol),然后将反应混合物在室温搅拌过夜。将粗制反应产物通过0.2微米过滤器过滤,并且利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到889mg(产率72%)2
‑
((3
‑
((17
‑
(2,5
‑
二氧代
‑
2,5
‑
二氢
‑
1h
‑
吡咯
‑1‑
基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸(化合物40)。
[0498][0499]1‑
((3
‑
((17
‑
(2,5
‑
二氧代
‑
2,5
‑
二氢
‑
1h
‑
吡咯
‑1‑
基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸的合成
[0500]
向2
‑
((3
‑
((17
‑
(2,5
‑
二氧代
‑
2,5
‑
二氢
‑
1h
‑
吡咯
‑1‑
基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸(573mg,0.928mmol)在20ml无水dcm中的溶液中加入1.0m dcc的dcm溶液(1.20ml,01.20mmol)和n
‑
羟基琥珀酰亚胺(139mg,01.26mmol),并且将溶液在r.t.搅拌,直至通过hplc确定反应完成(约3h)。将脲副产物通过过滤去除,并且向溶液中加入1
‑
氨基
‑
3,6,9,12
‑
四氧杂十五烷
‑
15
‑
酸(369mg,1.80mmol)和三乙胺(388μl,0.564mmol),然后将反应混合物在r.t.搅拌过夜。将反应混合物浓缩,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到586mg(产率73%)1
‑
((3
‑
((17
‑
(2,5
‑
二氧代
‑
2,5
‑
二氢
‑
1h
‑
吡咯
‑1‑
基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(化合物41)。
[0501][0502]
向2
‑
((3
‑
((17
‑
(2,5
‑
二氧代
‑
2,5
‑
二氢
‑
1h
‑
吡咯
‑1‑
基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)乙酸(573mg,0.928mmol)在20ml无水dcm中的溶液中加入1.0m dcc的dcm溶液(1.20ml,01.20mmol)和n
‑
羟基琥珀酰亚胺(139mg,01.26mmol),并且将溶液在r.t.搅拌,直至通过hplc确定反应完成(约3h)。将脲副产物通过过滤去除,并且向溶液中加入1
‑
氨基
‑
3,6,9,12
‑
四氧杂十五烷
‑
15
‑
酸(369mg,1.80mmol)和三乙胺(388μl,0.564mmol),然后将反应混合物在r.t.搅拌过夜。将反应混合物浓缩,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到586mg(产率73%)1
‑
((3
‑
((17
‑
(2,5
‑
二氧代
‑
2,5
‑
二氢
‑
1h
‑
吡咯
‑1‑
基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(化合物41)。
[0503]1‑
((3
‑
((17
‑
(2,5
‑
二氧代
‑
2,5
‑
二氢
‑
1h
‑
吡咯
‑1‑
基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯的合成
[0504]
向1
‑
((3
‑
((17
‑
(2,5
‑
二氧代
‑
2,5
‑
二氢
‑
1h
‑
吡咯
‑1‑
基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(367mg,0.424mmol)在5ml无水dmf中的溶液中加入dsc(双(2,5
‑
二氧代吡咯烷
‑1‑
基)碳酸酯)(120mg,0.467)和dmap(78mg,0.636mmol),然后将溶液在r.t.搅拌,直至通过hplc确定反应完成(约30min)。将粗制反应产物通过0.2微米过滤器过滤,并且利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到351mg(产率86%)1
‑
((3
‑
((17
‑
(2,5
‑
二氧代
‑
2,5
‑
二氢
‑
1h
‑
吡咯
‑1‑
基)
‑
15
‑
氧代
‑
4,7,10
‑
三氧杂
‑
14
‑
氮杂十七烷基)氨基甲酰基)
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氧基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯(化合物42)。
[0505][0506]
n
‑
(1
‑
(7
‑
氨基
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
基)
‑2‑
氧代
‑
7,10,13
‑
三氧杂
‑3‑
氮杂十六烷
‑
16
‑
基)苯并[c][1,2,5]噁二唑
‑5‑
甲酰胺的合成
[0507]
向2
‑
(7
‑
氨基
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
基)乙酸(152mg,0.652mmol)在5ml无水dmf中的溶液中加入dsc(176mg,0.685)和dmap(120mg,0.978mmol),并且将溶液在r.t.搅拌,直至通过hplc确定反应完成(约30min)。然后加入n
‑
(3
‑
(2
‑
(2
‑
(3
‑
氨基丙氧基)乙氧基)乙氧基)丙基)苯并[c][1,2,5]噁二唑
‑5‑
甲酰胺
‑
2,2,2
‑
三氟乙酸叔丁酯(360mg,0.749mmol)和三乙胺(273μl,1.956mmol),并且将反应混合物在r.t.搅拌过夜。将反应混合物浓缩,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到269mg(产率71%)n
‑
(1
‑
(7
‑
氨基
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
基)
‑2‑
氧代
‑
7,10,13
‑
三氧杂
‑3‑
氮杂十六烷
‑
16
‑
基)苯并[c][1,2,5]噁二唑
‑5‑
甲酰胺(化合物50)。
[0508][0509]2‑
((3
‑
(1
‑
(苯并[c][1,25]噁二唑
‑5‑
基)
‑
1,17
‑
二氧代
‑
6,9,12
‑
三氧杂
‑
2,16
‑
二氮杂十八烷
‑
18
‑
基)
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氨基)乙酸叔丁酯的合成
[0510]
向n
‑
(1
‑
(7
‑
氨基
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
基)
‑2‑
氧代
‑
7,10,13
‑
三氧杂
‑3‑
氮杂十六烷
‑
16
‑
基)苯并[c][1,2,5]噁二唑
‑5‑
甲酰胺(200mg,0.344mmol)在10ml无水dmf中的溶液中加入2
‑
溴乙酸叔丁酯(67mg,0.344mmol)和三乙胺(144μl,1.03mmol),并且将反应混合物在60℃搅拌过夜。将反映混合物用50ml dcm稀释,然后用50ml饱和碳酸氢钠洗涤2次,并且用50ml盐水洗涤2次。将有机相浓缩至约5ml,然后利用硅胶层析法进行纯化(2%甲醇/dcm至16%甲醇/dcm),以得到218mg(产率91%)2
‑
((3
‑
(1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑
1,17
‑
二氧代
‑
6,9,12
‑
三氧杂
‑
2,16
‑
二氮杂十八烷
‑
18
‑
基)
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氨基)乙酸叔丁酯(51)。
[0511][0512]2‑
((3
‑
(1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑
1,17
‑
二氧代
‑
6,9,12
‑
三氧杂
‑
2,16
‑
二氮杂十八烷
‑
18
‑
基)
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氨基)乙酸的合成
[0513]
将2
‑
((3
‑
(1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑
1,17
‑
二氧代
‑
6,9,12
‑
三氧杂
‑
2,16
‑
二氮杂十八烷
‑
18
‑
基)
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氨基)乙酸叔丁酯(218mg,0.313mmol)吸收于20ml的30%tfa/dcm中,并且将反应混合物在r.t.搅拌,直至通过hplc确
定反应完成(约4.5h)。然后将反应混合物在真空中浓缩,与甲苯共沸3次,并且在高真空下过夜干燥,以得到220mg(定量产率)2
‑
((3
‑
(1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑
1,17
‑
二氧代
‑
6,9,12
‑
三氧杂
‑
2,16
‑
二氮杂十八烷
‑
18
‑
基)
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氨基)乙酸,其直接使用而不经进一步纯化(52)。
[0514][0515]1‑
((3
‑
(1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑
1,17
‑
二氧代
‑
6,9,12
‑
三氧杂
‑
2,16
‑
二氮杂十八烷
‑
18
‑
基)
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氨基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸的合成
[0516]
向2
‑
((3
‑
(1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑
1,17
‑
二氧代
‑
6,9,12
‑
三氧杂
‑
2,16
‑
二氮杂十八烷
‑
18
‑
基)
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氨基)乙酸(220mg,0.345mmol)在10ml无水dmf中的溶液中加入1.0m dcc的dcm溶液(413μl,0.413mmol)和n
‑
羟基琥珀酰亚胺(47mg,0.413mmol),并且将溶液在r.t.搅拌,直至通过hplc确定反应完成(约4h)。将脲副产物通过过滤去除,并且向溶液中加入1
‑
氨基
‑
3,6,9,12
‑
四氧杂十五烷
‑
15
‑
酸(182mg,0.686mmol)和三乙胺(200μl,1.44mmol),然后将反应混合物在r.t.搅拌过夜。将反应混合物浓缩,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到517mg(产率85%)1
‑
((3
‑
(1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑
1,17
‑
二氧代
‑
6,9,12
‑
三氧杂
‑
2,16
‑
二氮杂十八烷
‑
18
‑
基)
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氨基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(化合物53)。
[0517][0518]1‑
((3
‑
(1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑
1,17
‑
二氧代
‑
6,9,12
‑
三氧杂
‑
2,16
‑
二氮杂十八烷
‑
18
‑
基)
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氨基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑
2,5
‑
2氧代吡咯烷
‑1‑
基酯的合成
[0519]
向1
‑
((3
‑
(1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑
1,17
‑
二氧代
‑
6,9,12
‑
三氧杂
‑
2,16
‑
二氮杂十八烷
‑
18
‑
基)
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氨基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
酸(120mg,0.135mmol)在10ml无水dcm中的溶液中加入1.0m dcc的dcm溶液(156μl,0.156mmol)和n
‑
羟基琥珀酰亚胺(18mg,0.156mmol),并且将溶液在r.t.搅拌,直至通过hplc确定反应完成(约5h)。将脲副产物通过过滤去除,浓缩反应混合物,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到109mg(产率82%)1
‑
((3
‑
(1
‑
(苯并[c][1,2,5]噁二唑
‑5‑
基)
‑
1,17
‑
二氧代
‑
6,9,12
‑
三氧杂
‑
2,16
‑
二氮杂十八烷
‑
18
‑
基)
‑4‑
甲基
‑2‑
氧代
‑
2h
‑
色烯
‑7‑
基)氨基)
‑2‑
氧代
‑
6,9,12,15
‑
四氧杂
‑3‑
氮杂十八烷
‑
18
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯(化合物54)。
[0520][0521]2‑
((叔丁氧基羰基)氨基)
‑6‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)己酸的合成
[0522]
向7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
羧酸(1.57g,6.02mmol)在25ml无水dcm中的溶液中加入1.0m dcc的dcm溶液(7.22ml,7.22mmol)和n
‑
羟基琥珀酰亚胺(830mg,7.22mmol),并且将溶液在r.t搅拌,直至通过hplc确定反应完成(约4h)。将脲副产物通过过滤去除,并且向溶液中加入6
‑
氨基
‑2‑
((叔丁氧基羰基)氨基)己酸(1.77g,0.686mmol)和三乙胺(2.52ml,18.06mmol),然后将反应混合物在r.t.搅拌过夜。将反映混合物用50ml dcm稀释,然后用50ml饱和碳酸氢钠洗涤2次,并且用50ml盐水洗涤2次。将有机相浓缩至约5ml,然后利用硅胶层析法进行纯化(3%甲醇/dcm至16%甲醇/dcm),以得到2.62g(产率89%)2
‑
((叔丁氧基羰基)氨基)
‑6‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)己酸(化合物60)。
[0523][0524]2‑
氨基
‑6‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)己酸的合成
[0525]
将2
‑
((叔丁氧基羰基)氨基)
‑6‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)己酸(2.62g,5.36mmol)溶于50ml的35%tfa/dcm中,并且在r.t.搅拌,直至通过hplc确定反应完成(约3h)。然后将反应混合物在真空中浓缩,与甲苯共沸3次,并且在高真空下过夜干燥,以得到2
‑
氨基
‑6‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)己酸的2,2,2
‑
三氟乙酸盐(化合物61)(1∶1),其直接使用而不经进一步纯化。
[0526][0527]1‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
3,6,9,12,15,18,21,24
‑
八氧杂二十七烷
‑
27
‑
酸的合成
[0528]
向2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰氯(246mg,0.967mmol)在15ml无水dcm中的溶液中加入1
‑
氨基
‑
3,6,9,12,15,18,21,24
‑
八氧杂二十七烷
‑
27
‑
酸(507mg,0.967mmol)和三乙胺(350μl,2.50mmol),并且将反应混合物在r.t.搅拌过夜。将反映混合物用20ml dcm稀释,然后用30ml饱和碳酸氢钠洗涤2次,并且用30ml盐水洗涤2次。将有机相浓缩至约5ml,然
后利用硅胶层析法进行纯化(4%甲醇/dcm至15%甲醇/dcm),以得到530mg(产率83%)1
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
3,6,9,12,15,18,21,24
‑
八氧杂二十七烷
‑
27
‑
酸(化合物62)。
[0529][0530]
2,5
‑
二氧代吡咯烷
‑1‑
基1
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
3,6,9,12,15,18,21,24
‑
八氧杂二十七烷
‑
27
‑
基酯的合成
[0531]
向1
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
3,6,9,12,15,18,21,24
‑
八氧杂二十七烷
‑
27
‑
酸(530mg,0.803mmol)在20ml无水dcm中的溶液中加入1.0m dcc的dcm溶液(964μl,0.964mmol)和n
‑
羟基琥珀酰亚胺(111mg,0.964mmol),并且将溶液在r.t.搅拌,直至通过hplc确定反应完成(约3h)。将脲副产物通过过滤去除,浓缩反应混合物,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到510mg(产率84%)1
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
3,6,9,12,15,18,21,24
‑
八氧杂二十七烷
‑
27
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯(化合物63)。
[0532][0533]1‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
29
‑
(4
‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)丁基)
‑
27
‑
氧代
‑
3,6,9,12,15,18,21,24
‑
八氧杂
‑
28
‑
氮杂三十烷
‑
30
‑
酸的合成
[0534]
向1
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
3,6,9,12,15,18,21,24
‑
八氧杂二十七烷
‑
27
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯(608mg,0.803mmol)在25ml无水dcm中的溶液中加入2
‑
氨基
‑6‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)己酸的2,2,2
‑
三氟乙酸盐(1∶1)(485,0.9636mmol)和三乙胺(336μl,2.409mmol),并且将溶液在r.t.搅拌,直至通过hplc确定反应完成(约6h)。将反映混合物用30ml dcm稀释,然后用40ml饱和碳酸氢钠洗涤2次,并且用40ml盐水洗涤2次。将有机相浓缩,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到637mg(产率77%)1
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
29
‑
(4
‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)丁基)
‑
27
‑
氧代
‑
3,6,9,12,15,18,21,24
‑
八氧杂
‑
28
‑
氮杂三十烷
‑
30
‑
酸(化合物64)。
[0535][0536]1‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
29
‑
(4
‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)丁基)
‑
27,30
‑
二氧代
‑
3,6,9,12,15,18,21,24,34,37,40,43
‑
十二氧杂
‑
28,31
‑
二氮杂四十六烷
‑
46
‑
酸的合成
[0537]
向1
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
29
‑
(4
‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)丁基)
‑
27
‑
氧代
‑
3,6,9,12,15,18,21,24
‑
八氧杂
‑
28
‑
氮杂三十烷
‑
30
‑
酸(310mg,0.301mmol)在20ml无水dcm中的溶液中加入1.0mdcc的dcm溶液(450μl,0.450mmol)和n
‑
羟基琥珀酰亚胺(52mg,0.450mmol),并且将溶液在r.t.搅拌,直至通过hplc确定反应完成(约3.5h)。将脲副产物通过过滤去除,并且向反应混合物中加入1
‑
氨基
‑
3,6,9,12
‑
四氧杂十五烷
‑
15
‑
酸(96mg,0.361mmol)和三乙胺(126μl,0.903mmol),然后将反应混合物在r.t.搅拌过夜。将反映混合物用30ml dcm稀释,然后用50ml饱和碳酸氢钠洗涤2次,并且用50ml盐水洗涤2次。将有机相浓缩,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到327mg(产率97%)1
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
29
‑
(4
‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)丁基)
‑
27,30
‑
二氧代
‑
3,6,9,12,15,18,21,24,34,37,40,43
‑
十二氧杂
‑
28,31
‑
二氮杂四十六烷
‑
46
‑
酸(化合物65)。
[0538][0539]1‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
29
‑
(4
‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)丁基)
‑
27,30
‑
二氧代
‑
3,6,9,12,15,18,21,24,34,37,40,43
‑
十二氧杂
‑
28,31
‑
二氮杂四十六烷
‑
46
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯的合成
[0540]
向1
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
29
‑
(4
‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)丁基)
‑
27,30
‑
二氧代
‑
3,6,9,12,15,18,21,24,34,37,40,43
‑
十二氧杂
‑
28,31
‑
二氮杂四十六烷
‑
46
‑
酸(178mg,0.139mmol)在15ml无水dcm中的溶液中加入1.0m dcc的dcm溶液(167μl,0.167mmol)和n
‑
羟基琥珀酰亚胺(19mg,0.167mmol),并且将溶液在r.t搅拌,直至通过hplc确定反应完成(约4.5h)。将脲副产物通过过滤去除,浓缩反应混合物,并且吸收于微量甲醇中,然后利用制备型hplc进行纯化。将纯馏分合并并且冻干,以得到168mg(产率88%)1
‑
(2
‑
乙酰氨基
‑5‑
甲基噻唑
‑4‑
磺酰胺基)
‑
29
‑
(4
‑
(7
‑
(二乙基氨基)
‑2‑
氧代
‑
2h
‑
色烯
‑3‑
甲酰胺基)丁基)
‑
27,30
‑
二氧代
‑
3,6,9,12,15,18,21,24,34,37,40,43
‑
十二氧杂
‑
28,31
‑
二氮杂四十六烷
‑
46
‑
基
‑
2,5
‑
二氧代吡咯烷
‑1‑
基酯(化合物66)。
[0541][0542]
自动化
[0543]
多重测定和方法可自动化完成,也可以与标本处理设备结合使用。该标本处理设备可以是自动化设备,诸如由ventana medical systems,inc.销售的benchmark xt仪器和symphony仪器。ventana medical systems,inc.是多项美国专利的受让人,这些专利公开了执行自动分析的系统和方法,包括美国专利第5,650,327号、第5,654,200号、第6,296,
809号、第6,352,861号、第6,827,901号和第6,943,029号,以及美国已公布的专利申请第2003/0211630号和第2004/0052685号,其中每项专利公开的内容均通过引用整体合并于本文。替代地,还可以人工处理标本。
[0544]
该标本处理设备可以将固定剂涂在标本上。固定剂可以包括交联剂(例如醛类,如甲醛、聚甲醛和戊二醛,以及非醛类交联剂)、氧化剂(如金属离子和络合物,例如四氧化二锇和铬酸)、蛋白质变性剂(如乙酸、甲醇和乙醇)、机理不明的固定剂(如氯化汞、丙酮和苦味酸)、组合试剂(如carnoy固定剂、methacam、bouin液、b5固定剂、rossman液和gendre液)、微波以及其他固定剂(如排除体积固定和蒸汽固定)。
[0545]
如果标本为嵌入石蜡中的样品,可通过标本处理设备使用相应的去石蜡流体对样品进行去石蜡。在废物清除器去除去石蜡流体后,可连续地将任意数量的物质施加至标本上。这些物质可以用于预处理(例如蛋白质交联、暴露核酸等)、变性、杂交、洗涤(如严格洗涤)、检测(如将显示或标记物分子与探针连接)、扩增(如扩增蛋白质、基因等)、复染、盖玻片等。
[0546]
所述标本处理设备可以将各种不同的化学物质应用到所述标本。这些化学物质包括但不限于染色剂、探针、试剂、漂洗剂和/或调节剂。这些化学物质可以是流体(如气体、液体或气体/液体混合物)或类似物质。所述流体可以是溶剂(如极性溶剂、非极性溶剂等)、溶液(如水溶液或其他类型的溶液)或类似物质。试剂可以包括但不限于染色剂、润湿剂、抗体(如单克隆抗体、多克隆抗体等)、抗原回收液(如水基或非水基抗原修复液、抗原回收缓冲液等)或类似物质。探针可以是分离的核酸或分离的合成寡核苷酸,附接到可检测标记物或报道分子上。标记物可以包括放射性同位素、酶底物、辅助因子、配体、化学发光或荧光剂、半抗原和酶。
[0547]
标本处理完毕后,用户可以将标本载片运送到成像设备上。本文所用的成像设备为明视野成像器幻灯扫描仪。一种明视野成像器是由ventana medical systems,inc.销售的iscan coreo
tm
明视野扫描仪。在自动化实施例中,成像设备是题为“imaging system and techniques”的国际专利申请第pct/us2010/002772号(专利公开号:wo/2011/049608)或于2011年9月9日提交的题为“imaging systems,cassettes,and methods of using the same”的美国专利公开第2014/0178169号中公开的数字病理装置。
[0548]
复染
[0549]
在样品已经用试剂染色以检测一种或多种靶标后对样品进行复染,使得可以在显微镜下更容易地观察它们的结构。例如,在盖玻片之前可任选地使用复染剂,以使免疫组织化学染色更明显。复染剂的颜色不同于初染剂。许多复染剂是众所周知的,诸如苏木素、曙红、甲基绿、亚甲蓝、姬姆色素、阿尔新蓝和核固红。可使用dapi(4
′
,6
‑
二脒基
‑2‑
苯基吲哚)为荧光染色剂。
[0550]
在一些实例中,可将一种以上的染色剂混合在一起以得到复染剂。这样提供了灵活性和选择染色剂的能力。例如,可针对具有特定属性但不具有其他所需属性的混合物选择第一染色剂。可以将第二染色剂添加至混合物中,其显示缺少的所需属性。例如,可将甲苯胺蓝、dapi和滂胺天蓝混合在一起以形成复染剂。
[0551]
成像
[0552]
本发明所公开的实施例的某些方面或全部可实现自动化,并且由计算机分析和/
或图像分析系统带来便利。在一些应用中,测量精确的颜色或荧光比率。在一些实施例中,利用光学显微镜进行图像分析。某些公开的实施例涉及采集数字图像。这可以通过将数码相机耦接至显微镜来完成。使用图像分析软件对获得的染色样品的数字图像进行分析。可以通过多种不同的方法来测量颜色或荧光。例如,颜色可以用红色、蓝色和绿色值以及色相、饱和度和强度值来衡量;和/或通过使用光谱成像相机测量特定的波长或波长范围。还可对样品进行定性和半定量评估。定性评估包括评估染色强度、鉴定阳性染色细胞和参与染色的细胞内结构以及评估总体样品或载玻片质量。对检测样品进行单独评估,并且该分析可包括与已知平均值的比较,以确定样品是否代表异常状态。
[0553]
样品和靶标
[0554]
样品包括生物成分,并且通常怀疑其包含一种或多种感兴趣的靶分子。靶分子可以在细胞表面,并且细胞可以在悬液或组织切片中。靶分子也可以在细胞内,并且在细胞裂解或通过探针穿透细胞后进行检测。本领域的普通技术人员将认识到,检测样品中靶分子的方法将根据样品类型和所用探针而变化。采集和制备样品的方法是本领域已知的。
[0555]
可使用本领域的普通技术人员已知的任何方法来制备用于该方法的实施例中并且具有本文所公开的组合物的样品,诸如组织或其他生物学样品。样品可得自接受常规筛查的受试者,或得自疑似患有病症的受试者,诸如遗传异常、感染或瘤形成。本发明所公开的方法的所述实施例还可应用于无遗传异常、疾病、病症等的样品,这些样品称为“正常”样品。此类正常样品在诸多用途之外可用作与其他样品进行比较的对照。可出于多种不同的目的对样品进行分析。例如,样品可用于科学研究中,或用于诊断可疑的疾病,或用作治疗成功、生存期等的预后指标。
[0556]
样品可能包含可由探针或报告分子特异性结合的多种靶标。靶标可以是核酸序列或蛋白质。在一些实例中,靶标为来自病原体(诸如病毒、细菌)或细胞内寄生物(诸如来自病毒基因组)的蛋白质或核酸分子。例如,靶蛋白可以由与疾病相关(例如,关联、存在因果关系等)的靶核酸序列产生。
[0557]
本领域技术人员将认识到,可以开发对以下靶标具有特异性的基于香豆素的缀合物:
[0558]
在具体的非限制性实例中,靶蛋白由与肿瘤(例如,癌症)相关联的靶核酸序列(例如,基因组靶核酸序列)产生。在肿瘤细胞中,尤其是在癌细胞(诸如b细胞和t细胞白血病、淋巴瘤、乳腺癌、结肠癌、神经系统癌等)中,已经鉴定出许多染色体异常(包括易位及其他重排、扩增或缺失)。因此,在一些实例中,靶分子的至少一部分由样品中的至少细胞亚群中扩增或缺失的核酸序列(例如,基因组靶核酸序列)产生。
[0559]
在其他实例中,由核酸序列(例如,基因组靶核酸序列)产生的靶蛋白为肿瘤细胞中缺失(丢失)的肿瘤抑制基因。例如,在某些膀胱癌中,位于染色体9p21上的p16区(包括d9s1749、d9s1747、p16(ink4a)、p14(arf)、d9s1748、p15(ink4b)和d9s1752)缺失。涉及染色体1的短臂的远端区域(包括例如shgc57243、tp73、egfl3、abl2、angptl1和shgc
‑
1322)和19号染色体(包括man2b1、znf443、znf44、crx、gltscr2和gltscr1)的着丝粒区域(例如19p13
‑
19q13)的染色体缺失是某些类型的中枢神经系统实体瘤的特征性分子特征。
[0560]
与致瘤性转化和/或生长相关的许多其他细胞遗传学异常是本领域的普通技术人员所知的。由核酸序列(例如,基因组靶核酸序列)产生的与致瘤性转化相关并且可用于本
发明所公开的方法中的靶蛋白还包括egfr基因(7p12;例如,genbank
tm
登录号nc
‑
000007,核苷酸55054219
‑
55242525)、c
‑
myc基因(8q24.21;例如,genbank
tm
登录号nc
‑
000008,核苷酸128817498
‑
128822856)、d5s271(5p15.2)、脂蛋白脂酶(lpl)基因(8p22;例如,genbank
tm
登录号nc
‑
000008,核苷酸19841058
‑
19869049)、rb1(13q14;例如,genbank
tm
登录号nc
‑
000013,核苷酸47775912
‑
47954023)、p53(17p13.1;例如,genbank
tm
登录号nc
‑
000017,补体,核苷酸7512464
‑
7531642)、n
‑
myc(2p24;例如,genbank
tm
登录号nc
‑
000002,补体,核苷酸151835231
‑
151854620)、chop(12q13;例如,genbank
tm
登录号nc
‑
000012,补体,核苷酸56196638
‑
56200567)、fus(16p11.2;例如,genbank
tm
登录号nc
‑
000016,核苷酸31098954
‑
31110601)、fkhr(13p14;例如,genbank
tm
登录号nc
‑
000013,补体,核苷酸40027817
‑
40138734),以及例如:alk(2p23;例如,genbank
tm
登录号nc
‑
000002,补体,核苷酸29269144
‑
29997936)、ig重链、ccnd1(11q13;例如,genbank
tm
登录号nc
‑
000011,核苷酸69165054.69178423)、bcl2(18q21.3;例如,genbank
tm
登录号nc
‑
000018,补体,核苷酸58941559
‑
59137593)、bcl6(3q27;例如,genbank
tm
登录号nc
‑
000003,补体,核苷酸188921859
‑
188946169)、malfl、ap1(1p32
‑
p31;例如,genbank
tm
登录号nc
‑
000001,补体,核苷酸59019051
‑
59022373)、top2a(17q21
‑
q22;例如,genbank
tm
登录号nc
‑
000017,补体,核苷酸35798321
‑
35827695)、tmprss(21q22.3;例如,genbank
tm
登录号nc
‑
000021,补体,核苷酸41758351
‑
41801948)、erg(21q22.3;例如,genbank
tm
登录号nc
‑
000021,补体,核苷酸38675671
‑
38955488);etv1(7p21.3;例如,genbank
tm
登录号nc
‑
000007,补体,核苷酸13897379
‑
13995289)、ews(22q12.2;例如,genbank
tm
登录号nc
‑
000022,核苷酸27994271
‑
28026505);fli1(11q24.1
‑
q24.3;例如,genbank
tm
登录号nc
‑
000011,核苷酸128069199
‑
128187521)、pax3(2q35
‑
q37;例如,genbank
tm
登录号nc
‑
000002,补体,核苷酸222772851
‑
222871944)、pax7(1p36.2
‑
p36.12;例如,genbank
tm
登录号nc
‑
000001,核苷酸18830087
‑
18935219)、pten(10q23.3;例如,genbank
tm
登录号nc
‑
000010,核苷酸89613175
‑
89716382)、akt2(19q13.1
‑
q13.2;例如,genbank
tm
登录号nc
‑
000019,补体,核苷酸45431556
‑
45483036)、mycl1(1p34.2;例如,genbank
tm
登录号nc
‑
000001,补体,核苷酸40133685
‑
40140274)、rel(2p13
‑
p12;例如,genbank
tm
登录号nc
‑
000002,核苷酸60962256
‑
61003682)以及csf1r(5q33
‑
q35;例如,genbank
tm
登录号nc
‑
000005,补体,核苷酸149413051
‑
149473128)。
[0561]
实例
[0562]
生物缀合物合成和纯化
[0563]
bsa
‑
半抗原缀合物
[0564]
将bsa蛋白固体(馏分v,60mg)溶于3ml pbs(100mm磷酸盐、150mm nacl,ph=7.5)中,并且在室温旋转1h。将所得溶液通过0.2μpall ghp注射器式过滤器过滤,并且利用uv
‑
vis分析其浓度,得到浓度为18.1mg/ml的溶液。将bsa储备液(1ml)用20当量的无水dmf中适当标记试剂的nhs酯进行处理。dmf体积保持为约15%(v/v)或更低。将所得混合物在室温旋转过夜。将所得混合物通过0.2μpall ghp注射器式过滤器过滤,并且利用体积排阻色谱进行纯化。将所得缀合物馏分合并,并且利用uv
‑
vis分析其浓度和标记物/蛋白质比率。将样品储存于2
‑
6℃待用。
[0565]
gar
‑
半抗原缀合物
[0566]
将山羊抗兔pab(1mg/ml的pbs溶液)用30当量的无水dmf中适当标记试剂的nhs酯进行处理。dmf体积保持为约15%(v/v)或更低。将所得混合物在室温旋转过夜。将所得混合物通过0.2μpall ghp注射器式过滤器过滤,并且利用体积排阻色谱进行纯化。将所得缀合物馏分合并,并且利用uv
‑
vis分析其浓度和标记物/蛋白质比率。将样品储存于2
‑
6℃待用。
[0567]
生物膜干涉(bli)分析
[0568]
将单独的蛋白质缀合物(抗体缀合物或bsa免疫原)用本文所公开的新型基于香豆素的试剂以及酪酰胺
‑
dpeg8
‑
半抗原和nhs
‑
dpeg8
‑
半抗原标记试剂(见图20)(并且如pct专利申请第pct/us201i/042849号所公开,其公开内容通过引用整体并入本文)标记。使用生物膜干涉(bli)在配备胺反应性第2代(ar2g)生物传感器的pall
‑
fortebio octet red仪器上表征蛋白质标记对蛋白质相互作用的影响(图6)。ar2g生物传感器提供了具有高密度羧酸并且非特异性相互作用倾向低的表面。通过标准edc催化的酰胺键形成,在蛋白质上的反应性胺与羧基封端的生物传感器表面之间形成共价键,从而实现蛋白质固定化。通过与edc(1
‑
乙基
‑3‑
[3
‑
二甲基
‑
氨基丙基]碳二亚胺盐酸盐)和s
‑
nhs(n
‑
羟基磺基琥珀酰亚胺)反应,活化羧酸,以生成高反应性nhs酯。这些酯与蛋白质的伯胺迅速反应,以形成高度稳定的酰胺键。共价固定化将蛋白质固定在生物传感器表面,从而可以分析结合事件和动力学特征。
[0569]
代表性bli测定
[0570]
使用pall
‑
fortebio ar2g生物传感器尖端进行octet red bli分析测定。测定条件符合pall
‑
fortebio dip和read
tm
胺反应性第二代技术说明26中建议的条件,但经过细微修改。按照技术说明26中的建议进行ar2g生物传感器活化和淬灭。在每次测定中,根据需要修改各种试剂的浓度,以最大程度提高信噪比,同时最大程度减少背景结合事件。所有bli测定步骤均在37℃进行。各种代表性测定如下文所述。
[0571]
基于香豆素的试剂抗体交叉反应性研究
[0572]
该测定用于评估与本文所述的基于香豆素的试剂的任何潜在的交叉反应性。将bsa
‑
clbf免疫原在100mm naoac(ph=5)中以1.25μg/ml的浓度固定化在ar2g生物传感器上。使用pall
‑
fortebio动力学添加剂,在pbs(100mm磷酸盐、150mm nacl,ph=7.5)中以浓度为725ng/ml的抗半抗原mab评估抗半抗原交叉反应性。时间步长如下表所示。
[0573]
步骤步骤名称时间(s)振摇速度1传感器平衡30010002edc/s
‑
nhs传感器活化30010003bsa免疫原固定化120010004乙醇胺传感器淬灭30010005传感器基线30010006抗半抗原mab结合240010007抗半抗原mab解离24001000
[0574]
基于香豆素的试剂对抗原和抗标记物识别[rb固定化
‑
标记的gar识别
‑
抗标记物识别]的影响
[0575]
该测定用于更好地了解基于香豆素的试剂结构如何影响带标记的抗体检测其抗原的能力。另外,使用第二抗标记物抗体以更好地了解连接基结构如何影响标记物检测。将
兔pab在100mm naoac(ph=5)中以25μg/ml的浓度固定化在ar2g生物传感器上。使用pall
‑
fortebio动力学添加剂,在pbs(100mm磷酸盐、150mm nacl,ph=7.5)中以3μg/ml对rb mab进行gar识别。使用pall
‑
fortebio动力学添加剂,在pbs(100mm磷酸盐、150mm nacl,ph=7.5)中浓度为3μg/ml的条件下进行抗标记物识别。时间步长如下表所示。
[0576][0577][0578]
结果与讨论
[0579]
基于香豆素的试剂抗体交叉反应性研究
[0580]
使用本公开的基于香豆素的试剂能够检测难以检测的半抗原标记物。半抗原标记物通常用于多重染色测定,其要求了解是否观察到与抗半抗原抗体文库的任何相互作用。进行生物膜干涉研究,其中将bsa
‑
clbf免疫原固定化在尖端。然后对抗半抗原抗体文库筛选任何潜在的交叉反应。图7阐述了ms抗bf mab(h1,h6)与经修饰的尖端的预期相互作用的实例。ms抗bf mab结合至传感器尖端,导致尖端的层生长发生净增加,从而在4800s内得到正关联信号。在4800s后,在最后一帧中显示了净解离。ms抗ppt mab(c1,c6)和ms抗dabsyl mab(d1,d6)抗体与香豆素连接基修饰的生物传感器尖端之间无明显的相互作用。
[0581]
在单独的bli实验中,针对类似的bsa
‑
clbf修饰的生物传感器尖端,对其余ms抗半抗原文库进行筛选。在图8中,在基于香豆素的试剂修饰的生物传感器尖端与ms抗np mab(b1,b6;c1,c6)和ms抗ts mab(h1,h6;g1,g6)抗体之间未观察到显著的相互作用。ms抗nca mab(b1,b6;c1,c6)和ms抗hq mab(h1,h6;g1,g6)抗体与基于香豆素的试剂修饰的生物传感器尖端也未表现出任何显著的相互作用(见图8)。在图10中,在基于香豆素的试剂修饰的生物传感器尖端与ms抗dcc mab(b1,b6;d1,d6)和ms抗rot mab(f1,f6;g1,g6)抗体之间未观察到显著的相互作用。图11的bli结果表明,未观察到与ms抗dig mab(红色,淡蓝色)的相互作用;但是,ms抗dnp mab(b1,b6;c1,c6)抗体与基于香豆素的试剂表现出正相互作用。观察到ms抗dnp mab bli结合响应(80pm)为ms抗bf mab bli结合响应(520pm,图7)的约15%。此外,ms抗dnp mab抗体非特异性结合未能从生物传感器尖端上轻松解离,表明将观察到组织背景染色。在图11所示的单独的bli实验中确认了ms抗dnp mab(f1,f6;g1,g6)香豆素连接基识别。同样,抗dnp mas抗体未能从生物传感器尖端上轻松解离。图12中的bli结果也表
明,在ms抗bd mab(c1,c6;d1,d6)与生物传感器尖端之间未观察到相互作用。
[0582]
连接基对抗原和抗标记物识别[rb固定化标记的gar识别
‑
抗标记物识别]的影响
[0583]
gar
‑
lvs(dcc)dpeg8ts与gar
‑
dpeg4
‑
1vs(dcc)dpeg8ts缀合物:
[0584]
gar
‑
lys(dcc)dpeg8ts和gar
‑
dpeg4
‑
lys(dcc)dpeg8ts缀合物利用赖氨酸核心作为支化配体。利用易于检测的dcc香豆素半抗原作为潜在的发色团并且直接结合至赖氨酸伯胺。使用第二
‑
dpegts半抗原基团作为难以定量的标记物,该标记物结合至赖氨酸核心仲胺(见图13
‑
化合物a)。该基团直接缀合至蛋白质,其中nhs基团直接处于赖氨酸支链上。生成第二桥接赖氨酸连接基核心,其中添加dpeg4柄部以使其与赖氨酸桥分离(见图13
‑
化合物b)。预期额外的dpeg4间隔子基团减小空间相互作用,并且为标记基团提供更高的灵活性,从而更容易增加蛋白负荷能力和分析检测性能(1
°
抗原和抗标记物识别)。
[0585]
用30当量的两种连接基构建物缀合gar pab(1mg,1mg/ml)。提供连接基/gar比率=3.3的gar
‑
lys(dcc)dpeg8ts缀合物(gar+化合物a;913mg,产率89%)。提供连接基/gar比率=5.4的gar
‑
dpeg4
‑
lys(dcc)dpeg8ts缀合物(gar+化合物b;913mg,产率84%)。赖氨酸桥与nhs酯之间额外的dpeg4间隔子之间的作用符合预期,提供了更高的抗体标记负载量。两种缀合物获得了等同的产率。
[0586]
bli测定设计用于模拟组织染色测定。将兔mab结合至生物传感器尖端,然后用上述缀合物进行识别。另外,使用未修饰的gar标准品比较标记物对兔识别的影响。用ts ms抗ts mab对ts半抗原标记物进行三级识别(见图14)。gar抗体缀合物与未修饰的gar抗体相似,可识别兔抗体负载的生物传感器尖端。用gar
‑
dpeg4
‑
lys(dcc)dpeg8ts缀合物观察到的elisa层略厚于gar
‑
lys(dcc)dpeg8ts缀合物(见图15)。在修饰gar缀合物解离速率方面未观察到差异。gar
‑
dpeg4
‑
1ys(dcc)dpeg8ts中赖氨酸桥与nhs酯之间额外的dpeg4间隔子也提供了更多的ms抗ts mab(见图16)。
[0587]
gar
‑
clbf缀合物
[0588]
将gar pa(2mg,1mg/ml)用30当量的bfdpeg8nhs和bfclnhs试剂进行标记。gar
‑
clbf缀合物uv/vis分析结果表明,bf/gar比率=5.85(1.6mg,产率80%)。cl香豆素可检测部分提供了具有在预期范围内的标记物/ab比率和产率的缀合物。gar
‑
dpeg8bf缀合物uv/vis分析将bf/gar比率高估为38.1(860mg,产率43%),与预期一致。gar
‑
dpeg8bf缀合物数据不准确,必须用作相对近似值。
[0589]
bli测定同样设计用于模拟组织染色测定。将兔mab结合至生物传感器尖端,然后用上述缀合物进行识别。用ms抗bf mab对bf半抗原标记物进行三级识别(见图17)。gar抗体缀合物类似地识别出兔抗体负载的生物传感器尖端(见图18)。使用gar
‑
clbf缀合物观察到的elisa层略厚于gar
‑
dpeg8bf缀合物。在修饰gar缀合物解离速率方面未观察到显著差异。据信
‑
dpeg4
‑
香豆素
‑
dpeg4
‑
bf连接基比
‑
dpeg
‑
bf标记物更具刚性。当通过抗bf mas抗体进行识别时,gar
‑
clbf缀合物在生物传感器尖端提供了较厚的elisa层(见图19)。ms抗bf mab从gar
‑
clbf缀合物中解离的速率略快于从gar
‑
dpeg8bf缀合物中的解离。
[0590]
ms抗bf mab从gar
‑
clbf缀合物中的解离速度加快,可能是由ms抗bf mab亲和力相互作用高于亲合力相互作用所引起的松散结合(更快速断开)的结果。如前文所述,预期cl香豆素连接基为刚性的。
‑
dpeg
‑
bf标记物增加的灵活性很可能使未结合的bf标记物弯曲并且结合至ms抗bf mab的其他互补结构域,该互补结构域具有亲和力相互作用,导致更强的
亲合力结合。亲合力结合(2
‑
1)导致的解离始终少于亲和力相互作用(1
‑
1),后者可能与香豆素连接基发生竞争。在交叉反应性研究中观察到类似的解离现象(见上图7)。
[0591]
本说明书中提及的和/或在申请数据表中列出的所有美国专利、美国专利申请出版物、美国专利申请、外国专利、外国专利申请和非专利出版物通过引用整体并入本文。如果需要采用各种专利、申请和出版物的概念来提供其它实施例,则可以修改实施例的各方面。
[0592]
尽管已经参考许多例示性实施例描述了本公开,但是应当理解,本领域技术人员可以设计出许多其他修改和实施例,它们将落入本公开原理的精神和范围内。更具体地,在不违背本公开的精神的情况下,在上述公开、附图和所附权利要求的范围内,所述主题组合排列的组成部分和/或布置可以进行合理的变化和修改。除了在所述组成部分和/或布置中的变化和修改外,对于本领域技术人员来说,替代用途也将是显而易见的。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1