DNA/Fe3O4网状结构结合磁性三相萃取法的核酸检测方法与流程
dna/fe3o4网状结构结合磁性三相萃取法的核酸检测方法
技术领域
[0001]
本发明涉及一种核酸检测方法,更具体地,涉及一种dna/fe3o4网状结构结合磁性三相萃取法的核酸检测方法。
背景技术:
[0002]
生物液中成分复杂,因此在检测某些核酸(microrna或dna)容易受到基质效应的影响,导致现有检测方法的不准确度不够高。目前绝大多数核酸检测方法依赖于杂交,如目标microrna或dna分子与互补标记的寡核苷酸探针杂交。然而,单独的核酸杂交不能满足灵敏度和准确性的要求。近年来,dna与纳米材料相结合的纳米技术的发展为用于早期诊断的生物传感器提供了一种新的信号放大策略。dna纳米技术不仅可以利用dna的刚性链在可编程的纳米尺度上构建高度有序的结构,也可以利用可控和预先设计的dna与纳米材料相结合的方法,产生稳定的放大信号。然而,由于检测只依赖于dna的杂交,因此检出限过高,通常在pm到nm范围内,因此限制了其实际应用。
技术实现要素:
[0003]
发明目的:本发明的目的是提供一种检出限低、检测效率高、适于实际应用的dna/fe3o4网状结构结合磁性三相萃取法的核酸检测方法。
[0004]
技术方案:本发明所述的利用类过氧化物酶超支化dna/fe3o4网状结构结合磁性三相单滴微萃取技术定量检测核酸的方法,包括以下步骤:
[0005]
(1)制备fe3o4纳米片;
[0006]
(2)在fe3o4纳米片上修饰碱基单链dna得到fe3o4/ssdna;
[0007]
(3)将含有目标核酸的待测样品进行超支化cha处理,得到超支化dna结构样品,将超支化dna结构样品与fe3o4/ssdna混合进行反应,得到dna/fe3o4网状结构;
[0008]
(4)将dna/fe3o4网状结构所在体系作为水相,和有机相混合,将带有萃取液滴的磁性棒浸入有机相,萃取dna/fe3o4网状结构后取出后,利用紫外-可见光谱仪对发生催化显色反应的液滴进行监测,分析紫外-可见光谱数据即得待测样品中目标核酸的含量。
[0009]
其中,步骤2中利用磁铁将fe3o4/ssdna的上清液分离丢弃,可以将为修饰到ssdna的fe3o4进行分离,避免影响后续实验,fe3o4纳米片和单链dna的体积比为1:1至10:1;单链dna是含有10~100个碱基的脱氧核糖核酸序列,步骤4中有机相为烷烃,萃取液滴为tmb-h2o2溶液。
[0010]
反应原理:超支化dna网状结构是通过一系列链置换反应触发形成。首先目标链打开hp1粘性末端,然后经过链置换过程,生成一个新的目标/hp1杂交链。新暴露hp1的环部碱基序列打开hp2,并导致hp2和hp1杂交。类似地,展开的hp2再打开hp3,由此启动级联自组装过程,直到目标/hp1杂交链被取代,导致cha产物分支化dna结构的形成。释放的目标链进入下一个循环,从而实现循环放大。同时,经cha打开的hp2和hp3的新暴露片段是hcr的触发点,随后,hp2和hp3暴露的碱基序列与末端修饰尾链的hp4和hp5杂交,形成具有树突状结构
[0034]
ssdna:
[0035]5’-
nh
2-(ch2)
6-cccccccccccccccaaaaaaaaaaaaa-3’[0036]
实施例1
[0037]
(1)将1.8g fecl3·
6h2o和0.9g feso4·
7h2o用50ml纯水溶解在烧杯中,再转移至三颈圆底烧瓶中,磁力搅拌,并用n2吹扫混合物,待反应温度上升至80℃时,缓慢滴加10ml 25%的nh4oh,溶液迅速变黑。反应混合物在80℃水浴中搅拌30min,连续用n2吹扫,然后用磁铁分离fe3o4纳米片和上清液,并去除上清液,用煮沸的超纯水进行5次洗涤。将纳米材料重新溶于15ml超纯水后添加1.25g柠檬酸,并在90℃下搅拌2h,用12kda透析膜在超纯水中透析24h,其中每8h换一次水,冷却至室温。然后,fe3o4纳米片在1000rpm离心洗涤10min,将fe3o4纳米片溶液在4000rpm离心6min,去除上清液,将最终的fe3o4产品在60℃真空烘箱中干燥48h,研磨,收集,储存于密封瓶中;
[0038]
(2)室温下,称量0.5mg fe3o4纳米片溶于3ml去离子水,振荡均匀。取100μl fe3o4纳米片溶液加入500μl单链dna,其中单链dna为1.5μm ssdna。将混合物在饱和磷酸盐缓冲液中反应2h,通过edc-nhs偶联反应使ssdna修饰在fe3o4纳米片表面,然后用磁铁将上清液分离出来丢弃。最后,用饱和磷酸盐缓冲液冲洗得到的fe3o4/ssdna,使用前在室温下保存。
[0039]
(3)将含有mirna-122的动物血清样品与10nm hp1、100nm hp2、hp3和1μm hp4、hp5(各40μl)混合,在37℃孵育2h。将所有的发夹链分别在95℃下加热5min,缓慢冷却1h至25℃,得到超支化dna结构样品。向100μl fe3o4/ssdna纳米片中加入240μl超支化dna结构样品,并在25℃下进一步反应1h。然后将产品转移到新的1.5ml透明色谱瓶中。其中,te缓冲液:将50ml 10mm tris-hcl,0.0931g edta和0.6353g mgcl2混合,定容至250ml。
[0040]
(4)在0.1m naac/hac缓冲液中,加入5.0μl 0.1m tmb和5μl 10.0m h2o2,得到tmb-h2o2溶液,作为萃取液滴,取6.0μl tmb-h2o2溶液滴在磁棒的底部,将步骤3中得到的超支化dna结构样品和fe3o4/ssdna纳米片的反应产物作为水相,在240μl水相加入200μl烷烃,出现分层,将滴有萃取液滴的磁性棒快速轻轻地浸入有机相,保持5秒钟,然后取出萃取液滴用紫外-可见光谱仪和透射电镜对反应进行监测,在650nm处记录吸光度的变化。
[0041]
本实施例中用到的序列包括:
[0042][0043]
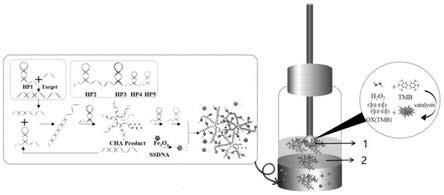
如图1所示,超支化dna网状结构是通过一系列链置换反应触发形成。首先目标链打开hp1粘性末端,然后经过链置换过程,生成一个新的目标/hp1杂交链。新暴露hp1的环部碱基序列打开hp2,并导致hp2和hp1杂交。类似地,展开的hp2再打开hp3,由此启动级联自组装过程,直到目标/hp1杂交链被取代,导致cha产物分支化dna结构的形成。释放的目标链进入下一个循环,从而实现循环放大。同时,经cha打开的hp2和hp3的新暴露片段是hcr的触发点,随后,hp2和hp3暴露的碱基序列与末端修饰尾链的hp4和hp5杂交,形成具有树突状结构的超支化dna网状结构。再利用磁性fe3o4纳米片表面修饰的ssdna可以与hp4和hp5的尾链杂交,使fe3o4纳米片与超支化的dna网状结构相结合,得扩增后的dna/fe3o4网状结构。在mtp-sdme过程中,磁棒1上的萃取剂浸没在有机相2时,dna/fe3o4网状结构快速通过有机相2,从样品相底部被萃取到液滴中,而未反应的fe3o4纳米片被有机相阻隔,在抽去磁棒后沉回样品溶液。最后,dna/fe3o4网状结构催化萃取剂中tmb发生氧化反应,产生uv-vis信号的变化。
[0044]
图2(a)、(b)分别是在目标分析物mirna-122浓度分别为1nm和10nm的条件下dna/fe3o4网状结构的tem图。从图2中可以看出在hcr过程中,fe3o4纳米片已经成功地连接到超支化dna链上,形成了dna/fe3o4网状结构。
[0045]
用紫外-可见纳米光度计评价了用三相sdme制备的dna/fe3o4网状结构的灵敏度。从图3(a)、(b)中可以看出mirna-122的浓度与吸光度值之间呈线性正相关。基于mtp-sdme结合类过氧化物酶超支化dna/fe3o4网状结构对mirna-122的检出限为0.147am,线性范围为0.5am至1pm,标准校准曲线显示在0.5am至1pm范围内,峰面积与mirna-122的浓度对数相关,r2=0.993。表1为不同mirna-122含量的动物血清样本的检测结果,从中可以看出向样品中掺入不同含量mirna-122时的相对回收率都接近100%,说明了该方法能够准确定量检测样品中mirna-122的含量。
[0046]
表1不同mirna-122含量的样本的检测结果
[0047] 掺入mirna-122的量相对回收率样品10-样品20.6fm102.4样品36fm103.9样品460fm103.3样品5600fm104.4
[0048]
相对回收率=(总浓度-空白浓度)/掺入浓度
[0049]
实施例2
[0050]
本实施例与实施例1区别是:步骤3中为含有dna的动物血清样品,用到的序列包括:
[0051][0052]
表2为不同dna含量的动物血清样本的检测结果表格,从中可以看出向样品中掺入不同含量dna时的相对回收率都接近100%,表明了该方法能够准确地定量样品中的dna。
[0053]
表2不同dna含量的样本的检测结果
[0054] 掺入dna的量相对回收率样品60-样品70.6fm100.7样品86fm104.9样品960fm101.2样品10600fm103.8
[0055]
相对回收率=(总浓度-空白浓度)/掺入浓度
[0056]
从图4(a)、(b)中可以看出dna的浓度与吸光度之间呈线性正相关。基于mtp-sdme结合类过氧化物酶超支化dna/fe3o4网状结构对dna的检出限为0.34am,线性范围为1am至
1pm,标准校准曲线显示在1am至1pm范围内,r2=0.996。
[0057]
对比例
[0058]
(1)将1.8g fecl3·
6h2o和0.9g feso4·
7h2o用50ml纯水溶解在烧杯中,再转移至三颈圆底烧瓶中,磁力搅拌,并用n2吹扫混合物,待反应温度上升至80℃时,缓慢滴加10ml 25%的nh4oh,溶液迅速变黑。反应混合物在80℃水浴中搅拌30min,连续用n2吹扫,然后用磁铁分离fe3o4纳米片和上清液,并去除上清液,用煮沸的超纯水进行5次洗涤。将纳米材料重新溶于15ml超纯水后添加1.25g柠檬酸,并在90℃下搅拌2h,用12kda透析膜在超纯水中透析24h,其中每8h换一次水,冷却至室温。然后,fe3o4纳米片在1000rpm离心洗涤10min,将fe3o4纳米片溶液在4000rpm离心6min,去除上清液,将最终的fe3o4产品在60℃真空烘箱中干燥48h,研磨,收集,储存于密封瓶中;
[0059]
(2)将含有mirna-122的动物血清样品与fe3o4纳米片混合;
[0060]
(3)在0.1m naac/hac缓冲液中,加入5.0μl 0.1m tmb和5μl 10.0m h2o2,得到tmb-h2o2溶液,作为萃取液滴,取6.0μl tmb-h2o2溶液滴在磁棒的底部,将步骤2中fe3o4纳米片和动物血清样品混合物的反应产物作为水相,在240μl水相加入200μl烷烃,出现分层,将滴有萃取液滴的磁性棒快速轻轻地浸入有机相,保持5秒钟,然后取出萃取液滴用紫外-可见光谱仪和透射电镜对反应进行监测,在650nm处记录吸光度的变化。
[0061]
图5(a)是合成的fe3o4纳米片的tem图,从中可以看出原始的fe3o4纳米片的直径大约为10nm,图5(b)是形成的超支化dna/fe3o4网状结构的tem图,表明成功制备了类过氧化物酶超支化dna/fe3o4网状结构。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1