一种AGTR1基因rs5186位点多态性检测用引物组及其应用的制作方法
本发明属于基因检测技术领域,具体涉及一种agtr1基因rs5186位点多态性检测用引物组及其应用。
背景技术:
高血压是我国最常见的慢性疾病之一,主要受遗传因素和环境因素的共同影响。研究表明,血管紧张素ii受体拮抗剂(angiotensiniireceptorantagonists)是一类作用于肾素-血管紧张素系统(rennin-angiotensinsystem,ras)的药物,主要应用于治疗高血压、糖尿病肾病和充血性心力衰竭。i型血管紧张素ii受体(angiotensiniireceptortype1,agtr1)是血管紧张素ii(angiotensin,angii)的受体,血管紧张素ⅱ主要通过其i型受体的介导从而发挥其作用。agtr1基因位于人染色体3q21-25,仅含1个外显子,无内含子区域。研究表明,agtr1基因是高血压发病的最重要的候选易感基因。
目前用于检测基因多态性的方法主要包括dna测序技术、高分辨率溶解曲线法、基因芯片技术和taqman-qpcr法。dna测序法的操作复杂,成本较高且检测时间长。基因芯片技术的检测成本高,特异性差,假阳性率高且耗时较长;高分辨率溶解曲线法对仪器和操作人员要求较高,不适合临床推广。taqman-qpcr法虽然检测灵敏度高,但检测特异性不高。
因此如何在agtr1基因检测保持高灵敏度的同时,提高其检测特异性,降低假阳性率,操作简便,适于临床推广应用,仍是本领域亟待解决的技术问题。
技术实现要素:
针对现有技术中存在的检测agtr1基因时检测灵敏度低、假阳性率高、检测周期长、操作复杂、成本高等问题,本发明提供一种agtr1基因rs5186位点多态性检测用引物组,及利用该引物组简便地检测agtr1基因的方法。其具有灵敏度高、特异性强、操作简便、检测周期短、低成本等特点,可快速精准的对agtr1基因的多态性进行检测,从而指导高血压个体化用药。
本发明技术方案为,一种agtr1基因rs5186位点多态性检测用引物组,含有野生型上游引物seqidno.1,突变型上游引物seqidno.6,及下游引物seqidno.11。
野生型上游引物seqidno.1:5’-agcacttcactaccaaatgagca-3’;
突变型上游引物seqidno.6:5’-agcacttcactaccaaatgagcc-3’;
下游引物seqidno.11:5’-agccgtcatctgtctaatgca-3’。
本发明还提供一种agtr1基因rs5186位点多态性检测用试剂盒,含有本发明agtr1基因rs5186位点多态性检测用引物组,所述引物组含有野生型上游引物seqidno.1,突变型上游引物seqidno.6,及下游引物seqidno.11。
本发明试剂盒还包括agtr1基因rs5186位点野生型质粒阳性对照,agtr1基因rs5186位点突变型质粒阳性对照,及无核酸酶ddh2o阴性对照。
本发明还提供一种agtr1基因rs5186位点多态性检测方法,包含步骤:
(1)提取样本dna;
(2)利用本发明引物组:野生型上游引物seqidno.1,突变型上游引物seqidno.6,及下游引物seqidno.11,进行实时荧光pcr扩增;
(3)对生成的实时荧光定量pcr扩增曲线进行数据采集和分析,计算△ct值,确定样本dna的基因型。
所述步骤(1)中,样本来源有唾液样本、口腔拭子或非肝素抗凝全血等,样本dna采用试剂盒提取,如qiagendneasyblood&tissuekit试剂盒,样本中提取dna的含量不超过50ng/μl。
所述步骤(2)中,实时荧光pcr扩增的条件为:pcr预混反应液有:2×pcr反应液,10xsybrgreeni,无核酸酶ddh2o;扩增程序为:第一阶段:95℃10min;第二阶段:95℃10s,58℃45s,40个循环;信号收集:第二阶段58℃时收集荧光信号。
相对于现有技术,本发明的优点在于:
本发明该检测用引物与相关试剂的价格比常规使用探针法的价格低,检测成本较低,操作简便。在节省了检测成本的同时,还大大缩短了检测周期,提高了检测的效率。通过直接探测pcr过程中荧光信号值获得检测的结果,全程闭管,且不需要pcr后处理或电泳检测,克服了常规pcr技术的易污染、出现假阳性的问题,能有效降低污染风险,保证检测的准确性。如本发明实施例所示,本发明该检测用引物具有很好的特异性,还能实现高效分型,又能降低假阳性。
附图说明
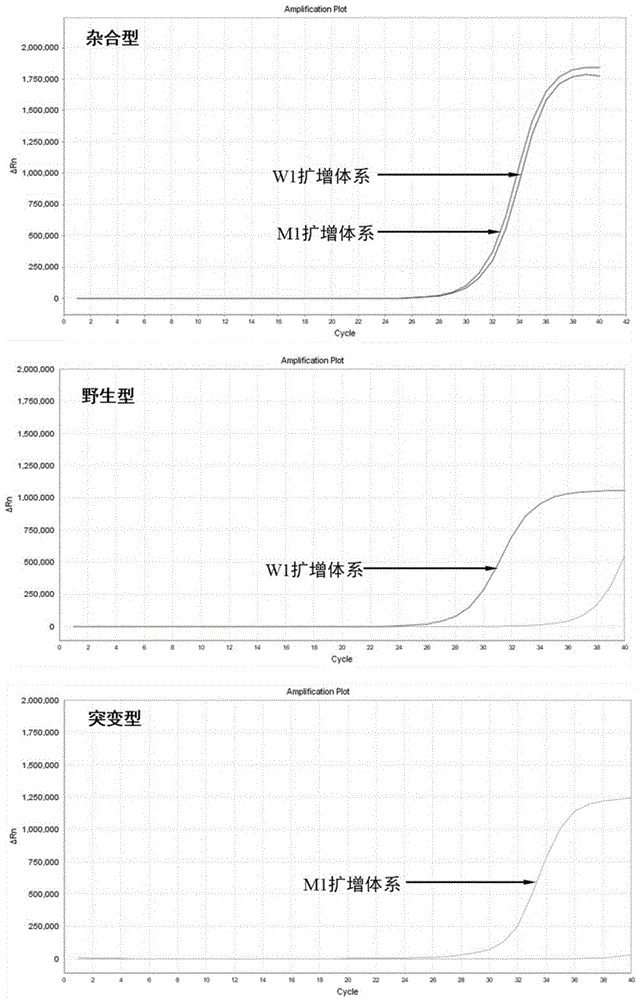
图1为采用引物wf1(w1)/mf1(m1)对agtr1(rs5186)野生型样本(aa)、突变性样本(cc)及杂合型样本(ac)的分型结果。
图2为采用引物wf2(w2)/mf2(m2)对agtr1(rs5186)野生型样本(aa)、突变性样本(cc)及杂合型样本(ac)的分型结果。
图3为采用引物wf3(w3)/mf3(m3)对agtr1(rs5186)野生型样本(aa)、突变性样本(cc)及杂合型样本(ac)的分型结果。
图4为采用引物wf4(w4)/mf4(m2)对agtr1(rs5186)野生型样本(aa)、突变性样本(cc)及杂合型样本(ac)的分型结果。
图5为采用引物wf5(w5)/mf5(m5)对agtr1(rs5186)野生型样本(aa)、突变性样本(cc)及杂合型样本(ac)的分型结果。
图6为采用引物wf1(w1)对agtr1(rs5186)野生型样本(aa)的一代测序结果。
图7为采用引物wf1(w1)对agtr1(rs5186)突变型样本(cc)的一代测序结果。
图8为采用引物wf1(w1)对agtr1(rs5186)杂合型样本(ac)的一代测序结果。
具体实施方式
为了便于理解本发明,通过以下实施例对本发明进行说明,但不构成对本发明的限制。
一、引物的设计与合成
针对人基因组中的agtr1基因位点(序列参见ncbi数据库公开的人类全基因组序列),使用primerpremier5.0软件,设计特异性的arms引物,详见表1。
表1引物
注:核苷酸序列中加粗部分为错配碱基,3’第一位为agtr1基因rs5186(a1166c)多态性位点。
二、对照品选择
阳性对照品一为agtr1基因位点野生型质粒。
阳性对照品二为agtr1基因位点突变型质粒。
阴性对照品为无核酸酶ddh2o。
三、pcr体系组成
第一组pcr反应的体系包括2xpcr反应液10μl,2.5μm正向引物seqidno.1或seqidno.62.4μl,2.5μm反向引物seqidno.112.4μl,人基因组dna2μl,10xsybrgreeni1μl,无核酸酶ddh2o2.2μl。结果见图1。
第二组pcr反应的体系包括2xpcr反应液10μl,2.5μm正向引物seqidno.2或seqidno.72.4μl,2.5μm反向引物seqidno.112.4μl,人基因组dna2μl,10xsybrgreeni1μl,无核酸酶ddh2o2.2μl。分型结果见图2。
第三组pcr反应的体系包括2xpcr反应液10μl,2.5μm正向引物seqidno.3或seqidno.82.4μl,2.5μm反向引物seqidno.112.4μl,人基因组dna2μl,10xsybrgreeni1μl,无核酸酶ddh2o2.2μl。结果见图3。
第四组pcr反应的体系包括2xpcr反应液10μl,2.5μm正向引物seqidno.4或seqidno.92.4μl,2.5μm反向引物seqidno.112.4μl,人基因组dna2μl,10xsybrgreeni1μl,无核酸酶ddh2o2.2μl。结果见图4。
第五组pcr反应的体系包括2xpcr反应液10μl,2.5μm正向引物seqidno.5或seqidno.102.4μl,2.5μm反向引物seqidno.112.4μl,人基因组dna2μl,10xsybrgreeni1μl,无核酸酶ddh2o2.2μl。结果见图5。
其中,所述2×pcr反应液(2×goldstarmastermix)购自北京康为世纪生物科技有限公司;所述sybrgreeni购自天根生化科技(北京)有限公司。
人基因组dna的含量不超过50ng/μl,从待测样本(如唾液样本、口腔拭子或非肝素抗凝全血等)中提取基因组dna,推荐使用qiagendneasyblood&tissuekit,按照试剂盒说明书操作步骤进行dna提取。
三、pcr反应的条件
配置pcr各反应体系后充分混匀并离心,然后将离心管置于pcr仪中,设置实时荧光pcr反应程序:95℃10min;95℃10s,58℃45s,40个循环,收集荧光信号。
四、数据采集和分析
采用实时荧光定量pcr软件对荧光扩增曲线进行数据采集与分析:确认未选择校正荧光参照,对扩增曲线进行分析。根据分析后图像调节baseline的start值、end值以选择为扩增曲线升起的拐点处,点击analyze进行分析,然后到plate窗口下记录每个反应的ct值。计算所述野生型反应体系和突变型反应体系的△ct值来确定所述样品dna的基因型。
五、结果判定
阴性对照ct值应大于等于36或显示无扩增,再确定所述样本dna的基因型;否则应重新进行检测;当每一个基因位点至少有一个反应ct值为
-2<δct=野生型ct值-突变型ct值<2,判定为杂合突变型样本;
δct=野生型ct值-突变型ct值<-6,判定为野生型样本;
δct=野生型ct值-突变型ct值>4,判定为突变型样本。
同时,利用一代测序法对提取的dna进行基因分型检测,并将本方法的基因分型结果与一代测序的基因分型结果进行对比。
如图1至图5所示,采用正向引物seqidno.1、seqidno.6,及反向引物seqidno.11组成的引物组,进行实时荧光pcr扩增时,野生型样本与突变性样本的荧光扩增曲线分型效果优于其他引物组;野生型与突变型杂合样本的荧光扩增曲线的重叠效果优于其他引物组;即在agtr1基因rs5186位点的核酸片段的多对不同位置错配的arms引物对,发现其分型效果均比不设计错配的引物对(wf1和mf1)要差,说明由正向引物seqidno.1、seqidno.6,及反向引物seqidno.11组成的引物组特异性好,实现高效分型,降低假阳性。
并且,如图6至8所示,利用本发明所述方法测定agtr1(rs5186)基因的一代测序的结果与图1的检测图谱对比分析,结果完全一致。由此可知,采用本发明由正向引物seqidno.1、seqidno.6,反向引物seqidno.11组成的引物组进行agtr1基因rs5186位点多态性检测的效果最好,基因分型判读准确,所能检测的人基因组dna浓度小于等于5ng/μl,该引物组特异性高,灵敏度高,且检测周期短,80分钟左右,即可完成atgr1基因多态性的3种基因分型,成本低。
采用正向引物seqidno.1或seqidno.6,反向引物seqidno.11组成的引物组,进行实时荧光pcr扩增时,野生型样本、突变性样本及杂合性样本的△ct值见表2。
表2
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干改进和润饰,也应视为在本发明的专利保护范围之内。
序列表
<110>上海鼎晶生物医药科技股份有限公司
<120>一种agtr1基因rs5186位点多态性检测用引物组及其应用
<141>2020-10-21
<160>11
<170>siposequencelisting1.0
<210>1
<211>23
<212>dna
<213>artificialsequence
<400>1
agcacttcactaccaaatgagca23
<210>2
<211>23
<212>dna
<213>artificialsequence
<400>2
agcacttcactaccaaatgtgca23
<210>3
<211>23
<212>dna
<213>artificialsequence
<400>3
agcacttcactaccaaatgtaca23
<210>4
<211>23
<212>dna
<213>artificialsequence
<400>4
agcacttcactaccaaatgatca23
<210>5
<211>23
<212>dna
<213>artificialsequence
<400>5
agcacttcactaccaaatgagta23
<210>6
<211>23
<212>dna
<213>artificialsequence
<400>6
agcacttcactaccaaatgagcc23
<210>7
<211>23
<212>dna
<213>artificialsequence
<400>7
agcacttcactaccaaatgtgcc23
<210>8
<211>23
<212>dna
<213>artificialsequence
<400>8
agcacttcactaccaaatgtacc23
<210>9
<211>23
<212>dna
<213>artificialsequence
<400>9
agcacttcactaccaaatgatcc23
<210>10
<211>23
<212>dna
<213>artificialsequence
<400>10
agcacttcactaccaaatgagtc23
<210>11
<211>21
<212>dna
<213>artificialsequence
<400>11
agccgtcatctgtctaatgca21
- 还没有人留言评论。精彩留言会获得点赞!