一种miR-139及其抑制物与应用
一种mir-139及其抑制物与应用
技术领域
1.本发明属于疾病基因治疗领域,具体涉及一种mir-139及其抑制物与应用。
背景技术:
2.痛风性关节炎是临床常见的代谢性疾病,由于嘌呤最终代谢产物尿酸排泄或生成异常,尿酸盐大量沉积于关节囊腔、滑膜囊、软骨、骨质等组织中,引起关节炎性反应,以关节红、肿、热、痛、活动障碍为主要临床表现。临床上治疗药物不良反应大,停药后易复发,远期疗效有限。
3.微小rna(micro rna,简称mirna)是一类短序列、非编码、具有调控功能的单链小分子rna,长约18~25nt。mirna具有多种生物学功能,目前认为它参与多种病理生理网络,包括癌症和炎症在内的人类疾病的发病机制,参与人体大约30%的基因调节。然而目前,尚无mir-139的抑制物能够用于预防和/或治疗痛风性关节炎的相关报道。
技术实现要素:
4.针对现有技术中存在的缺点与不足,本发明的目的在于提供一种mir-139,所述的mir-139作为一种新的mirna,其抑制物对于痛风性关节炎具有一定的预防和/或治疗作用,进而为痛风性关节炎的药物治疗提供新的靶点。
5.本发明的另一目的在于提供上述mir-139的抑制物,所述的mir-139的抑制物能够降低痛风性关节炎的关节肿胀程度以及炎症指标。
6.本发明的再一目的在于提供上述mir-139及其抑制物的应用。
7.本发明的目的通过如下技术方案实现:
8.一种mir-139,其核苷酸序列为:
[0009]5’-
uccccucccggcuugucccacca-3’(seq id no.1)。
[0010]
mir-139在作为开发预防和/或治疗痛风性关节炎药物中的应用。
[0011]
所述的药物为以mir-139作为药物治疗靶点的药物。mir-139作为一种新的mirna,其抑制物对痛风性关节炎具有一定的预防和/或治疗作用,进而为痛风性关节炎的药物治疗提供新的靶点。
[0012]
一种mir-139的抑制物,所述的mir-139的抑制物是针对上述mir-139的核苷酸序列设计并合成的小片段单链rna,所述的小片段单链rna的序列与上述mir-139的核苷酸序列反向互补;
[0013]
所述的mir-139的抑制物的核苷酸序列为:
[0014]5’-
uggugggacaagccgggagggga-3’(seq id no.2)。
[0015]
所述的mir-139的抑制物为能够减少mir-139的表达量,和/或抑制其活性的物质或基因工具。
[0016]
所述的mir-139的抑制物在制备预防和/或治疗痛风性关节炎药物中的应用。
[0017]
所述的mir-139的抑制物在制备白介素-1β调节剂中的应用。
[0018]
mir-139的抑制物通过减少mir-139的表达量进而下调白介素-1β蛋白的表达水平。
[0019]
一种预防和/或治疗痛风性关节炎的药物组合物,包含上述mir-139的抑制物。
[0020]
所述的药物组合物的制剂形式包括但不限于冻干粉针、口服片剂、胶囊和注射剂中的至少一种。
[0021]
所述的药物组合物的给药方法优选包括直接裸rna注射法、脂质体包裹rna直接注射法、细菌携带质粒表达rna法、病毒包装表达rna法和纳米材料组装法中的至少一种。
[0022]
所述的直接裸rna注射法的使用方法优选为:用depc水将干粉状的mir-139抑制物配制成20μm的注射剂,经灭菌后直接注射进膝关节,每次20μl,每天1次,持续使用至症状缓解。
[0023]
一种白介素-1β调节剂,包含上述mir-139的抑制物。
[0024]
所述的mir-139的抑制物通过抑制mir-139的表达进而下调白介素-1β蛋白的表达水平。
[0025]
本发明相对于现有技术具有如下有益效果:
[0026]
(1)本发明提供了mir-139的抑制物在急性痛风性关节炎小鼠模型中的应用,还提供了一种可能的mirna注射剂。本发明首次发现,敲降mir-139可以明显降低炎症指标,对治疗痛风性关节炎具有极大临床意义。
[0027]
(2)痛风性关节炎模型的复制普遍采用注射msu作为诱导因素,刺激滑膜、关节腔等产生急性应激反应,导致炎症细胞浸润周围组织,产生水肿。本发明采用小鼠作为痛风性关节炎的模型动物,采用msu膝关节注射,动物症状较为明显,实验结果稳定。因此,使用该模型能更好地模拟人类痛风机制。经研究表明:1)mir-139的抑制物可以减轻关节肿胀;2)mir-139的抑制物可以降低白介素-1β的表达水平。
[0028]
(3)本发明人意外发现mir-139的抑制物具有保护关节的功能,并创造性地发现mir-139能够作为mir-139的抑制物治疗/预防痛风性关节炎的药物治疗靶点,经研究表明,mir-139的抑制物可以通过降低白介素-1β蛋白的表达水平,减少痛风性关节炎的炎症反应,从而减轻关节肿胀,在痛风性关节炎的预防和治疗方面具有巨大的应用潜力。
附图说明
[0029]
图1为造模后各组小鼠膝关节直径测量结果图。
[0030]
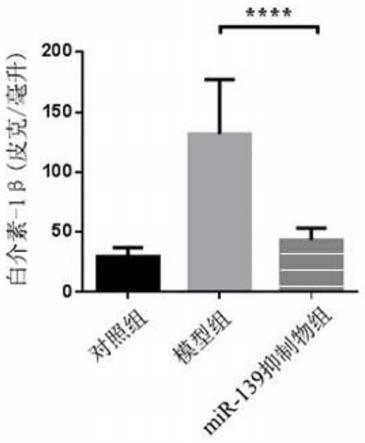
图2为mir-139抑制物显著降低白介素-1β的表达情况结果图;其中,
**
p<0.01,
***
p<0.001,
****
p<0.0001,与对照组相比较。
[0031]
图3为各组小鼠he染色结果图。
[0032]
图4为各组小鼠免疫组化检测白介素-1β结果图。
具体实施方式
[0033]
下面结合实施例及附图对本发明作进一步详细的描述,但本发明的实施方式不限于此。
[0034]
实施例1
[0035]
1、实验材料
[0036]
1.1实验动物
[0037]
健康的spf级c57bl/6小鼠,8~10周龄,体重22~25g,由广州中医药大学实验动物中心提供。动物许可证号:scxk(粤)2018-0034。
[0038]
1.2试剂
[0039]
单尿酸钠结晶(msu)购自美国invivogen公司;mir-139的抑制物,来源于sd大鼠(由广州中医药大学实验动物中心提供)的大脑黑质,取材测序后得到的mirna序列,将其前体序列、成熟体序列与mirbase、starbase、mirecords、mirtarbase等mirna数据库进行比对,未找到与他们序列完全一致的mirna。mir-139的抑制物粉末是委托苏州吉玛基因有限公司根据mir-139的抑制物的核苷酸序列利用小核酸合成仪进行化学合成并经减压离心干燥处理得到的干粉状制品;其中,本实施例中合成的mir-139的抑制物的量为2od,纯度达90%以上,1od的mir-139的抑制物相当于33μg的rnaoligo;酶联免疫吸附法(elisa)检测试剂盒,购自欣博盛生物科技有限公司;苏木素伊红(he)染色试剂盒和免疫组化试剂盒,购自博奥森生物有限公司;dmem培养基,购自美国gibco公司;白介素-1β一抗,购自美国abcam公司。
[0040]
1.3仪器
[0041]
co2孵箱,德国heraeus公司产品;多功能酶标仪,购自铂金埃尔默企业管理有限公司;奥林巴斯图像分析系统,购自日本olympus公司;游标卡尺,购自得力集团有限公司。
[0042]
2、方法
[0043]
20μm mir-139的抑制物注射液是以depc水为溶剂,以mir-139的抑制物粉末为溶质,经灭菌后制备而成;mir-139的抑制物注射液的质量符合企业要求标准。
[0044]
10mg/ml msu混悬液:通过将0.5mg单尿酸钠结晶粉末溶于0.05ml生理盐水中得到。
[0045]
2.1急性痛风性关节炎小鼠模型制备
[0046]
将12只c57bl/6小鼠随机分为3组,每组4只,测量小鼠膝关节直径;模型组和对照组均注射20μl 0.9%(m/v)生理盐水,mir-139抑制物组注射20μl 20μm mir-139的抑制物注射液;1小时后,对照组注射30μl 0.9%(m/v)的生理盐水,模型组注射30μl 10mg/ml的单尿酸钠结晶(msu)混悬液造模,mir-139抑制物组注射30μl 10mg/ml的单尿酸钠结晶(msu)混悬液造模,1小时后,使用游标卡尺测量小鼠膝关节直径。
[0047]
2.2酶联免疫吸附法(elisa)测定白介素-1β含量
[0048]
造模24小时后取材,把c57bl/6小鼠股骨和胫骨剪断,保留完整的膝关节,置于24孔板中,每孔放置300μl含1%(v/v)青霉素和1%(v/v)链霉素的dmem高糖培养基中,放入37℃孵箱培养,1小时后,收集培养基上清液,离心,取上清,用于elisa检测。
[0049]
2.3he染色观察关节腔内组织情况
[0050]
把小鼠膝关节放入4%(v/v)的福尔马林溶液中固定7天,制作石蜡切片,进行he染色,显微镜观察小鼠膝关节组织的病理改变情况。
[0051]
2.4免疫组化检测白介素-1β的表达情况
[0052]
石蜡切片常规脱蜡至水,按照免疫组化试剂盒说明书记载检测切片中白介素-1β的表达情况。
[0053]
3、结果
[0054]
3.1膝关节测量结果
[0055]
结果如图1所示。与对照组相比,各组在造模后,膝关节肿胀度高于对照组,差异具有统计学意义(p《0.05),提示造模成功。与模型组相比,mir-139的抑制物+msu组(即mir-139抑制物组)肿胀程度明显降低,差异具有统计学意义(p《0.05)。
[0056]
3.2elisa结果
[0057]
结果如图2所示。与对照组相比,注射msu的模型组白介素-1β明显升高,说明造模成功。使用了mir-139的抑制物后,白介素-1β显著降低,说明mir-139的抑制物在痛风性关节炎的治疗中具有一定效果。
[0058]
3.3he染色结果
[0059]
结果如图3所示。对照组组织关节面完整光滑透明,关节腔大小适中,仅有极少量的炎性细胞浸润,骨膜厚度适中;模型组关节面粗糙缺损,有大量的炎性细胞浸润,关节腔与对照组相比变大,可能存在关节积液与水肿,且关节腔内有散在结缔纤维组织,另有骨膜增厚情况;与模型组相比,mir-139的抑制物组关节腔大小适中,关节面平滑完整,其骨膜厚度与对照组几乎相等,仅有少许炎性细胞浸润组织。说明mir-139的抑制物可以预防msu对滑膜组织的炎症作用。
[0060]
3.4免疫组化结果
[0061]
结果如图4所示。对照组的关节软骨细胞中有少量白介素-1β蛋白表达;而模型组的关节软骨细胞中有大量的白介素-1β蛋白表达,与模型组相比,mir-139抑制物组关节软骨细胞白介素-1β蛋白表达明显降低,说明mir-139的抑制物可以缓解炎症反应,有利于痛风性关节炎的治疗。
[0062]
实施例2
[0063]
1、将委托苏州吉玛基因有限公司根据mir-139的抑制物的核苷酸序列化学合成的mir-139的抑制物粉末,采用药用针剂的制备方法制成注射液。具体为:将mir-139的抑制物500mg溶于1,2丙二醇20ml和吐温-80 2ml的混合液中,再加注射用水至250ml。混合均匀后灌入瓶中,密封,消毒制成2mg/ml一支的注射液。本品用于静脉注射(iv.),成人每天1支,即2mg/天;小儿常用量:按体重0.05mg/kg/天。
[0064]
2、将委托苏州吉玛基因有限公司根据mir-139的抑制物的核苷酸序列化学合成的mir-139的抑制物粉末采用药用胶囊的制备方法制成胶囊。具体为:将mir-139的抑制物25000mg,加碳酸钙4500mg,加淀粉500mg,混合均匀制成颗粒,灌装成每粒内容物为30mg的胶囊,每粒胶囊含mir-139的抑制物25mg。
[0065]
服用方法:口服,成人常用量,每日2次,每次1-2粒;小儿常用量,按体重一次0.5mg/kg,每六小时一次。4周为一疗程,两个疗程后,药量酌减。
[0066]
3、将委托苏州吉玛基因有限公司根据mir-139的抑制物的核苷酸序列化学合成的mir-139的抑制物粉末采用药用片剂的制备方法制成片剂。具体为:将mir-139的抑制物40000mg,加碳酸钙9000mg,加淀粉1000mg,混合均匀,过90目筛,压片。制成片重为50mg的片剂,每片含mir-139的抑制物40mg。
[0067]
服用方法:口服,成人常用量,每日2次,每次1-2片;小儿常用量,按体重一次0.5mg/kg,每六小时一次。4周为一疗程,两个疗程后,药量酌减。
[0068]
经研究发现,mir-139的抑制物注射液、胶囊、片剂均适用于预防和治疗痛风性关
节炎。
[0069]
上述实施例为本发明较佳的实施方式,但本发明的实施方式并不受上述实施例的限制,其他的任何未背离本发明的精神实质与原理下所作的改变、修饰、替代、组合、简化,均应为等效的置换方式,都包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1