一种基于CRISPR技术检测目标突变的方法与流程
一种基于crispr技术检测目标突变的方法
技术领域
1.本发明涉及核酸检测领域,涉及利用crispr技术检测目标突变,尤其涉及检测靶核酸是否存在目标突变和检测靶核酸在目标区域是否存在突变的方法、系统和试剂盒。
背景技术:
2.特异性检测核酸分子(nucleic acid detection)方法具有重要的应用价值,例如病原体的检测,遗传病检测等。在病原体检测方面,由于每种病原体微生物都有其独一无二的特征核酸分子序列,因此可以开发出针对特定物种的核酸分子检测,也称为核酸诊断(nads,nucleic acid diagnostics),在食品安全、环境微生物污染检测,人体病原菌感染等领域具有重要义。另一个方面是对人或其他物种的单核苷酸多态性(snps,single nucleotide polymorphisms)的检测。在基因组水平上去理解遗传变异和生物学功能之间的关系为现代分子生物学提供了新视角,而其中snps对生物学的功能、进化和疾病等密切相关,因此snps的检测与分析技术的发展尤为重要。
3.目前建立的特异性核酸分子检测通常需要分为两步,第一步是目的核酸的扩增,第二步是目的核酸检测。现有检测技术包括限制性核酸内切酶方法、southern、northern、斑点杂交、荧光pcr检测技术、lamp环介导等温扩增技术、重组酶聚合酶扩增技术(rpa)等方法。2012年之后,crispr基因编辑技术兴起,张锋团队基于rpa技术开发了一种以cas13为核心的靶向rna的新核酸诊断技术(sherlock技术),doudna团队开发了一种以cas12酶为核心的诊断技术(detectr技术),中国科学院上海植物生理生态研究所王金博士等也开发了一种基于cas12的新型核酸检测技术(holmes技术)。基于crispr技术开发的核酸检测技术正在日益发挥重要作用。
4.本发明将crispr的核酸检测技术应用到检测靶核酸在目标区域是否存在突变和检测靶核酸是否存在目标突变中,具体的,提供给了高效的检测方法。
技术实现要素:
5.本发明提供了一种基于crispr技术检测靶核酸是否存在目标突变位点和检测靶核酸在目标区域是否存在突变的方法、系统和试剂盒。
6.检测目标突变的方法
7.一方面,本发明提供了一种基于crispr技术检测靶核酸是否存在目标突变位点的方法,所述方法包括将靶核酸与v型crispr/cas效应蛋白、grna(指导rna)和单链核酸检测器接触,所述grna包括与所述crispr/cas效应蛋白结合的区域和与含有目标突变的突变型靶核酸杂交的导向序列,所述导向序列包括与所述目标突变位点配对的碱基;检测由crispr/cas效应蛋白切割单链核酸检测器产生的可检测信号。
8.一种实施方式中,所述目标突变是野生型靶核酸与突变型靶核酸在grna导向序列所靶向区域内不一致的位点;由于grna的导向序列与突变型靶核酸杂交、包括与所述目标突变位点配对的碱基,此时,所述目标突变位点也是指grna导向序列与其所靶向的野生型
靶核酸序列不一致的位点。
9.所述目标突变可以是单碱基突变、两个碱基突变、三个碱基突变或四个碱基突变;可以是连续的单碱基突变,也可以是不连续的单碱基突变。
10.在一个实施方式中,所述目标突变是单碱基突变,与所述目标突变位点配对的碱基设置于grna导向序列的5’端第10位、第11位、第12位和第13位中的的任一个;
11.在其他的实施方式中,所述目标突变可以是两个碱基突变,与所述目标突变位点配对的碱基设置于grna导向序列的5’端第10位和第11位、第10位和第12位、第10位和第13位、第11位和第12位、第11位和第13位、第12位和第13位中的任意一种。
12.在其他的实施方式中,所述目标突变可以是三个碱基突变,与所述目标突变位点配对的碱基设置于grna导向序列的5’端第10位和第11位和第12位、第11位和第12位和第13位、第10位和第11位和第13位、第10位和第12位和第13位中的任意一种。
13.在其他的实施方式中,所述目标突变可以是四个碱基突变,与所述目标突变位点配对的碱基设置于grna导向序列的5’端第10位、第11位、第12位和第13位。
14.进一步的,所述grna导向序列在非与所述目标突变位点配对的碱基处设置有突变的碱基,所述突变的碱基为与所述靶核酸相应位置不能杂交的碱基,所述突变的碱基的位置位于所述grna导向序列的非5’端第10位-13位。
15.优选的,突变的碱基的位置位于所述grna导向序列的5’端第1位、第2位、第3位、第4位、第5位、第6位、第7位、第8位、第9位、第14位、第15位或第16位,更优选,5’端第1位、第2位、第6位、第7位、第8位或第9位。
16.在一种实施方式中,上述grna导向序列在非与所述目标突变位点配对的碱基处设置有突变的碱基可以提高检测的效率,所述效率包括准确度、灵敏度。
17.上述方法中检测突变型靶核酸的可检测信号强度与检测野生型靶核酸时的信号明显不同;具体而言,检测突变型靶核酸的可检测信号明显强于检测野生型靶核酸时的信号,此时,可以根据可检测信号的强弱确定靶核酸中是否存在目标突变位点。
18.在一种实施方式中,野生型靶核酸的可检测信号与突变型靶核酸的可检测信号可以是不同的可检测信号,野生型靶核酸的可检测信号与突变型靶核酸的可检测信号也可以是相同的可检测信号。
19.优选的,所述方法中还包括检测野生型靶核酸进行对照的步骤,所述方法中还包括提供标准野生型靶核酸的步骤。
20.优选的,所述方法中还包括检测突变型靶核酸进行对照的步骤,所述方法中还包括提供标准突变型靶核酸的步骤。
21.在其他的实施方式中,本发明还提供了上述v型crispr/cas效应蛋白、grna(指导rna)和单链核酸检测器在制备用于检测靶核酸是否存在目标突变位点的试剂、组合物或试剂盒中的用途。
22.在一种实施方式中,所述grna中与所述crispr/cas效应蛋白结合的区域设置在与含有目标突变的突变型靶核酸杂交的导向序列的5'端。
23.在优选的实施方式中,上述目标突变位点为snp。
24.检测目标区域是否存在突变的方法
25.一方面,本发明提供了一种基于crispr技术检测靶核酸在目标区域是否存在突变
的方法,所述方法包括将样品与v型crispr/cas效应蛋白、grna(指导rna)和单链核酸检测器接触,所述grna包括与所述crispr/cas效应蛋白结合的区域和与野生型型靶核酸杂交的导向序列;检测由crispr/cas效应蛋白切割单链核酸检测器产生的可检测信号。
26.所述目标区域是指grna导向序列5’端第10位-第13位所靶向的靶核酸的位置。
27.上述方法中,野生型靶核酸和突变型靶核酸可以产生明显不同的可检测信号;具体而言,检测突变型靶核酸的可检测信号明显弱于检测野生型靶核酸时的信号,此时,可以根据可检测信号的强弱确定靶核酸中是否存在目标突变位点。如果可检测信号明显变弱,则说明grna导向序列5’端第10位-第13位所靶向的靶核酸的位置存在突变,所述突变位于grna导向序列5’端第10位、第11位、第12位和第13位所靶向的靶核酸的位置中的一个或多个。
28.进一步的,所述grna导向序列在非目标区域设置有突变的碱基,所述突变的碱基为与所述靶核酸相应位置不能杂交的碱基,所述突变的碱基的位置位于所述grna导向序列的非5’端第10位-13位。优选的,突变的碱基的位置位于所述grna导向序列的5’端第1位、第2位、第3位、第4位、第5位、第6位、第7位、第8位、第9位、第14位、第15位或第16位,更优选,5’端第1位、第2位、第6位、第7位、第8位或第9位。
29.在一种实施方式中,上述grna导向序列在非目标区域设置突变的碱基可以提高检测的效率,所述效率包括准确度、灵敏度。
30.在其他的实施方式中,本发明还提供了上述v型crispr/cas效应蛋白、grna(指导rna)和单链核酸检测器在制备用于检测靶核酸在目标区域是否存在突变的试剂、组合物或试剂盒中的用途;优选的,所述目标区域为grna导向序列5’端第10位-第13位所靶向的靶核酸的位置。
31.在一种实施方式中,所述grna中与所述crispr/cas效应蛋白结合的区域设置在与含有目标突变的突变型靶核酸杂交的导向序列的5'端。
32.试剂、试剂盒、组合物
33.一方面,本发明提供了一种基于crispr技术检测靶核酸是否存在目标突变位点的试剂、试剂盒或组合物,所述试剂、试剂盒或组合物包括上述v型crispr/cas效应蛋白、grna(指导rna)和单链核酸检测器,所述grna包括与所述crispr/cas效应蛋白结合的区域和与含有目标突变的突变型靶核酸杂交的导向序列,所述导向序列包括与所述目标突变位点配对的碱基,优选的,所述导向序列在非与所述目标突变位点配对的碱基处设置有突变的碱基。
34.一方面,本发明提供了一种基于crispr技术检测靶核酸在目标区域是否存在突变的试剂、试剂盒或组合物,所述试剂、试剂盒或组合物包括上述v型crispr/cas效应蛋白、grna(指导rna)和单链核酸检测器,所述grna包括与所述crispr/cas效应蛋白结合的区域和与野生型靶核酸杂交的导向序列,所述目标区域是指grna导向序列5’端第10位-第13位所靶向的靶核酸的位置,优选的,所述grna导向序列在非目标区域设置有突变的碱基,所述突变的碱基为与所述靶核酸相应位置不能杂交的碱基,所述突变的碱基的位置位于所述grna导向序列的非5’端第10位-13位。
35.单链核酸检测器
36.在一些实施方式中,所述单链核酸检测器不与所述grna杂交。
37.在一种实施方式中,所述的单链核酸检测器两端包括不同的报告基团或标记分子,当其处于初始状态(即未被切割状态时)不呈现报告信号,当该单链核酸检测器被切割后,呈现出可检测的信号,即切割后与切割前表现出可检测的区别。
38.在一些实施方式中,所述单链核酸检测器的5’端和3’端分别设置不同的报告基团,当所述单链核酸检测器被切割后,可以表现出可检测的报告信号;例如,单链核酸检测器的两端分别设置荧光基团和淬灭基团;或者单链核酸检测器的两端分别设置第一分子(如fam或fitc)和连接至3’端的第二分子(如生物素)。
39.当单链核酸检测器两端分别设置的是荧光基团和淬灭基团时,当所述单链核酸检测器被切割后,可以表现出可检测的荧光信号。所述荧光基团选自fam、fitc、vic、joe、tet、cy3、cy5、rox、texas red或lc red460中的一种或任意几种。所述淬灭基团选自bhq1、bhq2、bhq3、dabcy1或tamra中的一种或任意几种。
40.当单链核酸检测器两端分别设置的是第一分子(如fam或fitc)和第二分子(如生物素)时,所述的含有单链核酸检测器的反应体系与流动条配合用以检测特征序列(优选,胶体金检测方式)。所述的流动条被设计为具有两条捕获线,在样品接触端(胶体金)设有结合第一分子的抗体(即第一分子抗体),在第一线(control line)处含有结合第一分子抗体的抗体,在第二线(test line)处含有与第二分子结合的第二分子的抗体(即第二分子抗体,如亲和素)。当反应沿着条带流动时,第一分子抗体与第一分子结合携带切割或未切割的寡核苷酸至捕获线,切割的报告子将在第一个捕获线处结合第一分子抗体的抗体,而未切割的报告子将在第二捕获线处结合第二分子抗体。报告基团在各条线的结合将导致强读出/信号(例如颜色)。随着更多的报告子被切割,更多的信号将在第一捕获线处累积,并且在第二线处将出现更少的信号。
41.在一种实施方式中,所述单链核酸检测器包含一个或多个:1)碱基修饰的核苷酸,2)糖基修饰的核苷酸,3)改变的化学键,4)已修饰的骨架。
42.在一种实施方式中,所述核苷酸为核糖核苷酸、脱氧核糖核苷酸、核酸类似物中的一种或几种;所述核糖核苷酸的碱基选自腺嘌呤a、尿嘧啶u、胞嘧啶c、鸟嘌呤g、胸腺嘧啶t、次黄嘌呤i中的一种或任意几种;所述脱氧核糖核苷酸的碱基选自a、t、c、g、u、i中的一种或任意几种。
43.在一种实施方式中,所述碱基修饰是对一个核苷酸中的腺嘌呤、胞嘧啶、鸟嘌呤、尿嘧啶、或胸腺嘧啶成分进行化学修饰所产生的。对此工艺熟悉的人很容易便可以了解其它类似的碱基修饰,因而这些其他方法也应该属于本发明的范围。
44.在一种实施方式中,所述碱基修饰的核苷酸还包括无碱基间隔物(包含锁核酸的单链核酸检测器还记载在了中国申请cn2020108880363中);所述无碱基间隔物选自dspacer,spacer c3,spacer c6,spacer c12,spacer9,spacer12,spacer18,inverted abasic site(dspacer abasic furan)和rabasic site(rspacer abasic furan)中的一种或任意几种
45.在一种实施方式中,所述糖基修饰的核苷酸包括、2
’‑
氟基修饰、2’氧甲基修饰、锁核酸(包含锁核酸的单链核酸检测器还记载在了中国申请cn2020105609327中)、桥核酸、吗啉核酸、乙二醇核酸、己糖醇核酸、苏糖核酸、阿拉伯糖核酸、2’甲氧基乙酰基修饰、2
’‑
氨基修饰、4
’‑
硫rna、肽核酸(pna)、环己烯基核酸(cena)及其组合;所述糖基修饰的核苷酸的碱
基选自a、u、c、g、t、i中碱基的一种或任意几种。
46.在一种实施方式中,所述改变的化学键包括修饰的核酸骨架和非天然核苷间连接,具有修饰主链的核酸包括那些在主链中保留磷原子的核酸和那些在主链中不具有磷原子的核酸。
47.在一种实施方式中,所述单链核酸检测器可以是线性的或环状的。
48.在一种实施方式中,所述的检测方法,可用于待检测特征序列的定量检测。所述的定量检测指标可以根据报告基团的信号强弱进行定量,如根据荧光基团的发光强度,或根据显色条带的宽度等。
49.crispr/cas效应蛋白
50.进一步的,所述v型crispr/cas效应蛋白选自下组:
51.(1)seq id no.1所示的蛋白;
52.(2)将seq id no.1所示氨基酸序或其活性片段经过一个或多个(如2个、3个、4个,5个,6个,7个,8个,9个或10个)氨基酸残基的取代、缺失或添加而形成的,且具有基本相同功能的衍生蛋白;
53.(3)与seq id no.1所示的序列有80%,85%,90%,91%,92%,93%,94%,95%,96%,97%,98%,99%同一性的蛋白。
54.在一个实施方式中,所述cas蛋白突变体包括氨基酸取代、缺失或替换,且所述突变体至少保留其trans切割活性。优选地,所述突变体具有cis和trans切割活性。
55.靶核酸
56.本发明中,所述靶核酸包括核糖核苷酸或脱氧核糖核苷酸,包括单链核酸、双链核酸,例如单链dna、双链dna、单链rna、双链rna、dna-rna杂交体、或核酸修饰物。
57.在一个实施方式中,所述靶核酸来源于病毒、细菌、微生物、土壤、水源、人体、动物、植物等样品。
58.在一个实施方式中,所述靶核酸为pcr、nasba、rpa、sda、lamp、had、near、mda、rca、lcr、ram等方法富集或扩增的产物。
59.在一个实施方式中,所述方法还包括从样品中获得靶核酸的步骤。
60.在一个实施方式中,所述靶核酸为病毒核酸、细菌核酸、与疾病相关的特异核酸,如特定的突变位点或snp位点或与对照有差异的核酸;优选地,所述病毒为植物病毒或动物病毒,例如,乳头瘤病毒,肝dna病毒,疱疹病毒,腺病毒,痘病毒,细小病毒,冠状病毒;优选地,所述病毒为冠状病毒,优选地,sars、sars-cov2(covid-19)、hcov-229e、hcov-oc43、hcov-nl63、hcov-hku1、mers-cov。
61.在一些实施方式中,所述靶核酸来源于细胞,例如,来源于细胞裂解液。
62.可检测信号
63.在一些实施方式中,本发明的方法还包括测量crispr/cas效应蛋白(cas蛋白)产生的可检测信号的步骤。v型crispr/cas效应蛋白与grna和靶核酸接触后,被激发trans活性,能更高效的切割本发明中的单链核酸检测器,体现出可检测信号。
64.本发明中,所述可检测信号可以是当切割单链核酸检测器时产生的任何信号。例如,基于金纳米颗粒的检测,荧光偏振,荧光信号,胶体相变/分散,电化学检测,基于半导体的传感。
65.所述可检测信号可通过任何合适的方式读出,包括但不限于:可检测的荧光信号的测量,凝胶电泳检测(通过检测凝胶上的条带的变化),基于视觉或传感器的颜色的存在或不存在的检测、或者颜色存在的差异(例如,基于金纳米颗粒)以及电信号的差异。
66.在一些实施方式中,所述可检测信号的测量可以是定量的,在其他的实施方式中,所述可检测信号的测量可以是定性的。
67.比例
68.在一个实施方式中,所述cas蛋白与grna的用量摩尔比为(0.8-1.2):1。
69.在一个实施方式中,所述cas蛋白的用量终浓度为20-200nm,优选,30-100nm,更优选,40-80nm,更优选,50nm。
70.在一个实施方式中,所述grna的用量终浓度为20-200nm,优选,30-100nm,更优选,40-80nm,更优选,50nm。
71.在一个实施方式中,所述靶核酸的用量终浓度为5-100nm,优选,10-50nm。
72.在一个实施方式中,所述单链核酸检测器的用量终浓度为100-1000nm,优选,150-800nm,优选,200-800nm,优选,200-500nm,优选,200-300nm。
73.应用
74.另一方面,本发明还提供了上述cas12i在制备检测靶核酸是否存在目标突变的组合物、试剂或试剂盒中的应用。
75.另一方面,本发明还提供了上述cas12i在制备检测靶核酸在目标区域是否存在突变的组合物、试剂或试剂盒中的应用。
76.另一方面,本发明还提供了上述cas12i在检测靶核酸是否存在目标突变和检测靶核酸在目标区域是否存在突变的中的应用。
77.另一方面,本发明还提供了上述组合物、试剂或试剂盒在检测靶核酸是否存在目标突变和检测靶核酸在目标区域是否存在突变的中的应用。
78.另一方面,本发明还提供了上述在非目标区域设置突变碱基在提高检测靶核酸在目标区域是否存在突变的效率中的应用。
79.一般定义:
80.除非另有定义,否则本文所用的技术和科学术语具有与所属领域的普通技术人员之一通常理解的相同的含义。
81.术语“杂交”或“互补的”或“基本上互补的”是指核酸(例如rna、dna)包含使其能够非共价结合的核苷酸序列,即以序列特异性,反平行的方式(即核酸特异性结合互补核酸)与另一核酸形成碱基对和/或g/u碱基对,“退火”或“杂交”。杂交需要两个核酸含有互补序列,尽管碱基之间可能存在错配。两个核酸之间杂交的合适条件取决于核酸的长度和互补程度,这是本领域公知的变量。典型地,可杂交核酸的长度为8个核苷酸或更多(例如,10个核苷酸或更多,12个核苷酸或更多,15个核苷酸或更多,20个核苷酸或更多,22个核苷酸或更多,25个核苷酸或更多,或30个核苷酸或更多)。
82.应当理解,多核苷酸的序列不需要与其靶核酸的序列100%互补以特异性杂交。多核苷酸可包含60%或更高,65%或更高,70%或更高,75%或更高,80%或更高,85%或更高,90%或更高,95%或更高,98%或更高,99%或更高,99.5%或更高,或与其杂交的靶核酸序列中的靶区域的序列互补性为100%。
83.术语“氨基酸”是指含有氨基的羧酸。生物体内的各种蛋白质是由20种基本氨基酸构成的。
84.术语“多核苷酸”、“核苷酸序列”、“核酸序列”、“核酸分子”和“核酸”可以互换使用,包括dna、rna或者其杂交体,可以是双链或单链的。
85.术语“同源性”或“同一性”用于指两个多肽之间或两个核酸之间序列的匹配情况。当两个进行比较的序列中的某个位置都被相同的碱基或氨基酸单体亚单元占据时(例如,两个dna分子的每一个中的某个位置都被腺嘌呤占据,或两个多肽的每一个中的某个位置都被赖氨酸占据),那么各分子在该位置上是同一的。两个序列之间。通常,在将两个序列比对以产生最大同一性时进行比较。这样的比对可通过使用,例如,氨基酸序列的同一性可以通过常规方法,参考例如smith and waterman,1981,adv.appl.math.2:482pearson lipman,1988,proc.natl.acad.sci.usa 85:2444,thompsonetal.,1994,nucleic acids res 22:467380等的教导,通过计算机化运行运算法则(wisconsin genetics软件包中的gap,bestfit,fasta,和tfasta,genetics computer group)来确定。也可使用可从美国国立生物技术信息中心(ncbi www.ncbi.nlm.nih.gov/)获得的blast运算法则,使用默认参数确定。
86.如本文所用,“生物素(biotin)”也称维生素h,是一种分子量为244da的小分子维生素。“亲和素(avidin)”,又称抗生物素,是一种碱性糖蛋白,具有4个同生物素亲和例极高的结合位点,常用亲和素有链霉亲合素。生物素与亲和素的极强亲和力可用于在检测体系中放大或增强检测信号。如生物素很易与蛋白质(如抗体等)以共价键结合,而结合了酶的亲和素分子与结合有特异性抗体的生物素分子产生反应,既起到了多级放大作用,又由于酶在遇到相应底物时的催化作用而呈色,达到检测未知抗原(或抗体)分子的目的。
87.无碱基间隔物
88.如本文所用,“无碱基间隔物(spacer)”是指表示不包含具体编码信息的核苷。无碱基间隔物可与寡核苷酸结合,包括3’和5’末端,或核苷酸链内部。常见的spacer包括:dspacer(abasic furan),spacer c3,spacer c6,spacer c12,spacer9,spacer12,spacer18,,inverted abasic site(dspacer abasic furan)和rabasic site(rspacer abasic furan)。
89.上述无碱基间隔物是本领域公知的无碱基间隔物,例如,美国专利us8153772b2中公开了dspacer,spacer 9,spacer 18,spacer c3;中国专利申请cn101454451a公开了dspacer。
90.本文优选的无碱基间隔物“dspacer”又称为无碱基位点,四氢呋喃(tetrahydrofuran,thf)或无嘌呤/无嘧啶位点(apurinic/apyrimidinic(ap)site),或,无碱基连接子,其中亚甲基位于2'-脱氧核糖的1位。dspacer不仅在结构上与天然位点非常相似,而且相当稳定。结构如下所
91.regularly interspaced short palindromic repeats),其来自微生物的免疫系统。
101.cas蛋白
102.本文所述“cas蛋白”是指crispr-associated蛋白,优选来自v型或vi型crispr/cas蛋白(crispr/cas效应蛋白),其一旦与待检测特征序列(靶序列)结合(即形成cas蛋白-grna-靶序列的三元复合物),就可以诱发其trans活性,即随机切割非靶向单链核苷酸(即本文所述单链核酸检测器)。当cas蛋白与特征序列结合后,其切割或不切割特征序列,均可以诱发其trans活性;优选地,其通过切割特征序列诱发其trans活性;更优选地,其通过切割单链特征序列诱发其trans活性。所述cas蛋白通过识别与特征序列临近的pam(protospacer adjacent motif)识别特征序列。
103.本发明所述的cas蛋白为至少具有trans切割活性的蛋白,优选地,所述的cas蛋白为具有cis和trans切割活性的蛋白。所述的cis活性是指cas蛋白可在grna的作用下识别pam位点并特异性切割靶序列的活性。
104.本发明所述的cas蛋白包括v型crispr/cas效应蛋白,包括cas12、cas14等蛋白家族。优选地,例如cas12蛋白,例如cas12a、cas1 2b、cas12i;优选地,所述cas蛋白为cas12i。
105.在实施方式中,本文所称的cas蛋白,如cas12,也涵盖cas的功能变体或其同源物或直系同源物。如本文所用的蛋白的“功能变体”是指至少部分保留该蛋白的活性的这样的蛋白的变体。功能变体可以包括突变体(其可以是插入、缺失或替换突变体),包括多晶型物等。功能变体中还包括这样的蛋白与另一种通常不相关的核酸、蛋白质、多肽或肽的融合产物。功能变体可以是天然存在的或可以是人造的。有利的实施方式可以涉及工程化或非天然存在的v型dna靶向效应蛋白。
106.在一个实施方式中,编码cas蛋白,如cas12,的一种或多种核酸分子或其直系同源物或同源物可以被密码子优化用于在真核细胞中表达。真核生物可如本文所述。一种或多种核酸分子可以是工程化的或非天然存在的。
107.在一个实施方式中,cas12蛋白或其直系同源物或同源物可以包含一个或多个突变(并且因此编码其的核酸分子可以具有一个或多个突变。突变可以是人工引入的突变并且可以包括但不限于催化结构域中的一个或多个突变。
108.在一个实施方式中,cas蛋白可以来自:纤毛菌属、李斯特菌属、棒状杆菌属、萨特氏菌属、军团菌属、密螺旋体属、产线菌属、真细菌属、链球菌属、乳酸菌属、支原体属、拟杆菌属、flaviivola、黄杆菌属、固氮螺菌属、sphaerochaeta、葡糖醋杆菌属、奈瑟氏菌属、罗氏菌属、parvibaculum、葡萄球菌属、nitratifractor、支原体属、弯曲杆菌属和毛螺菌属。
109.在一个实施方式中,cas蛋白选自如下序列组成的蛋白:
110.(1)seq id no.1所示的蛋白;
111.(2)将seq id no.1所示氨基酸序或其活性片段列经过一个或多个(如2个、3个、4个,5个,6个,7个,8个,9个或10个)氨基酸残基的取代、缺失或添加而形成的,且具有基本相同功能的衍生蛋白。
112.在一个实施方式中,所述cas蛋白还包括与上述序列具有50%,优选55%,优选60%,优选65%,优选70%,优选75%,优选80%,优选85%,优选90%,优选99%,序列同一性(同源性)的,且具有trans活性的蛋白。
113.所述的cas蛋白可以通过重组表达载体技术获得,即将编码该蛋白的核酸分子构
建到合适的载体上,再转化到宿主细胞中,使得所述的编码核酸分子在细胞中表达,从而获得相应的蛋白。所述的蛋白可以被细胞分泌出来,或者破解细胞通过常规的提取技术获得该蛋白。所述的编码核酸分子可以整合至宿主细胞的基因组中进行表达,也可以不整合到宿主细胞中进行表达。所述的载体还进一步包括有利于序列整合,或进行自我复制的调节元件。所述的载体可以是例如质粒、病毒、粘粒、噬菌体等类型,它们是本领域技术人员所熟知的,优选地,本发明中的表达载体是质粒。所述的载体进一步包括一种或多种调控元件,选自启动子、增强子、翻译起始的核糖体结合位点、终止子、多聚腺苷酸序列、筛选标记基因。
114.宿主细胞可以是原核细胞,如大肠杆菌,链霉菌属、农杆菌:或是低等真核细胞,如酵母细胞;或是高等真核细胞,如植物细胞。本领域一般技术人员都清楚如何选择适当的载体和宿主细胞。
115.grna
116.如本文所用,所述的“grna”又称为guide rna或导向rna,并且具有本领域技术人员通常理解的含义。一般而言,导向rna可以包含同向(direct)重复序列和导向序列(guide sequence),或者基本上由或由同向重复序列和导向序列(在内源性crispr系统背景下也称为间隔序列(spacer))组成。所述grna中,同向重复序列设置在导向序列的5'端。grna在不同的crispr系统中,依据其所依赖的cas蛋白的不同,可以包括crrna和tracrrna,也可以只含有crrna。crrna和tracrrna可以经过人工改造融合形成single guide rna(sgrna)。在某些情况下,导向序列是与靶序列(本发明中所述特征序列)具有足够互补性从而与所述靶序列杂交并引导crispr/cas复合物与所述靶序列的特异性结合的任何多核苷酸序列,通常具有12-25nt的序列长度,在优选的实施方式中,所述导向序列具有13-20nt的序列长度,例如,14nt、15nt、16nt、17nt、18nt、19nt或20nt。所述的同向重复序列可折叠形成特定结构(如茎环结构)供cas蛋白识别,以形成复合物。所述的导向序列不需要与特征序列(靶序列)100%互补。所述的导向序列不与单链核酸检测器互补。
117.在某些实施方案中,当最佳比对时,导向序列与其相应靶序列之间的互补程度(匹配度)为至少50%、至少60%、至少70%、至少80%、至少90%、至少95%、或至少99%。确定最佳比对在本领域的普通技术人员的能力范围内。例如,存在公开和可商购的比对算法和程序,诸如但不限于clustalw、matlab中的史密斯-沃特曼算法(smith-waterman)、bowtie、geneious、biopython以及seqman。
118.本发明所述的grna可以是天然的,也可以是经过人工改造或设计合成的。
119.序列信息
120.seq id no.1详情类型1cas12iprotein
附图说明
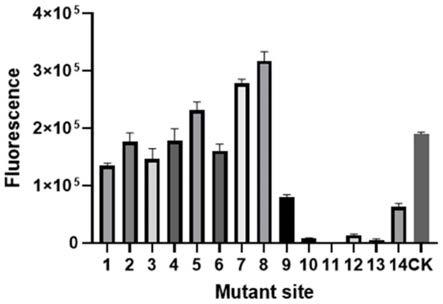
121.图1.待测靶核酸与grna导向序列只有一个碱基的差异,并且差异的碱基在第10、11、12、13任一位置时,检测信号会有明显差异(明显降低)。
122.图2.目标突变位于第10位,非与所述目标突变位点配对的碱基处设置的突变碱基位于第2位时的检测结果。
123.图3.目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基位于第1位时的检测结果。
124.图4.目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基位于第2位时的检测结果。
125.图5.目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基位于第6位时的检测结果。
126.图6.目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基位于第6位时的检测结果。
127.图7.目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基位于第7位时的检测结果。
128.图8.目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基位于第8位时的检测结果。
129.图9.目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基位于第9位时的检测结果。
130.实施方式
131.下面结合实施例对本发明做进一步的说明,以下所述,仅是对本发明的较佳实施例而已,并非对本发明做其他形式的限制,任何熟悉本专业的技术人员可能利用上述揭示的技术内容加以变更为同等变化的等效实施例。凡是未脱离本发明方案内容,依据本发明的技术实质对以下实施例所做的任何简单修改或等同变化,均落在本发明的保护范围内。
132.本发明技术方案基于如下原理,获得待测样品的核酸,比如,可以通过扩增的方法得到靶核酸,利用可以与靶核酸配对的grna引导cas蛋白识别并结合在靶核酸上;随后,cas蛋白激发单链核酸检测器的切割活性,从而切割体系里的单链核酸检测器;单链核酸检测器的两端分别设置荧光基团和淬灭基团,如果单链核酸检测器被切割,则会激发荧光;如果单链核酸检测器无法被切割,则不会激发荧光;在其他的实施方式中,单链核酸检测器的两端还可以设置成能够被胶体金检测的标记。
133.实施例1、测试目标单碱基突变设置在grna导向序列上不同位置对检测效率的影响
134.合成一条vp1-14序列为:
135.agagaaugugugcauagucacac augcagaguucacu
136.与cas蛋白结合的区域 导向序列(14bp)
137.为使待测靶核酸与grna导向序列靶向有且只有一个碱基的突变,合成不同的ssdna(单链dna)作为靶核酸,检测目标单碱基突变在grna导向序列上不同位置对检测效率的影响,靶核酸的序列为如表1所示:
138.表.1靶核酸的序列
[0139][0140][0141]
注:下划线标注的是导向序列靶向的位置,黄色表示突变的位置,突变位置是在grna导向序列从5’端向3’端计数
[0142]
结果如图1所示,待测靶核酸与grna导向序列靶向的碱基的突变位置设置在第10、11、12、13任一位置时,检测信号会有明显差异(明显降低),也就是,在检测突变靶核酸是,将目标单碱基突变的位置设置在grna导向序列的5’端第10、11、12、13位的任一位置,可以明显区分野生型靶核酸和突变型靶核酸;待测靶核酸与grna导向序列靶向的碱基的突变设置在第1、2、3、4、5、6、7、8、9、14任一位置时,检测信号差异不明显,也就是在检测突变靶核酸时,非与所述目标突变位点配对的碱基处设置有突变的碱基设置在grna导向序列的5’端第1、2、3、4、5、6、7、8、9、14任一位置,不会明显影响检测的结果;也就是说检测目标区域内是否存在突变时,非目标区域设置的突变的碱基,设置在grna导向序列的5’端第1、2、3、4、5、6、7、8、9、14任一位置,不会明显影响检测的结果。
[0143]
实施例2、测试在grna导向序列5’端1号、2号或6号位置设置非与所述目标突变位点配对的碱基处设置的突变碱基对检测突变效率的影响
[0144]
如实施例1所示,在grna导向序列的5’端第1、2、3、4、5、6、7、8、9、14任一位置存在突变时,对于野生型和突变型的检测效率没有明显影响。本实施例中验证上述没有影响的位置与上述有影响的位置(grna导向序列的5’端第10-13位)的组合对于检测效率的影响。
[0145]
本实施例中合成4条grna序列(如表2所示),并对每一条grna设置完全匹配的靶核酸,存在目标突变的靶核酸,存在目标突变和非与所述目标突变位点配对的碱基处设置的突变碱基(靶核酸与grna的导向序列有两个碱基的差异),所述4组靶核酸的序列如表3所示:
[0146]
表2. 4条grna序列的序列
[0147][0148]
表3.对应4个基因分别设置的靶核酸序列
[0149][0150][0151]
注:加粗标注的是导向序列靶向的位置,黄色表示突变的位置,突变位置是在grna导向序列从5’端向3’端计数。
[0152]
如图2所示,仅存在非与所述目标突变位点配对的碱基处设置的突变碱基于第2位时,检测结果与阳性对照(grna与靶核酸无差异)基本一致;当目标突变位于第10位,非与所述目标突变位点配对的碱基处设置的突变碱基位于第2位时,检测结果与阳性对照有极明显的差别;
[0153]
如图3所示,仅存在非与所述目标突变位点配对的碱基处设置的突变碱基于第1位时,检测结果与阳性对照(grna与靶核酸无差异)基本一致;当目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基位于第1位时,检测结果与阳性对照有极明显的差别;
[0154]
如图4所示,仅存在非与所述目标突变位点配对的碱基处设置的突变碱基于第2位时,检测结果与阳性对照(grna与靶核酸无差异)基本一致;当目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基位于第2位时,检测结果与阳性对照有极明显的差别;
[0155]
如图5所示,仅存在非与所述目标突变位点配对的碱基处设置的突变碱基于第6位时,检测结果与阳性对照(grna与靶核酸无差异)基本一致;当目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基位于第6位时,检测结果与阳性对照有极明显的差别;
[0156]
以上实验结果说明,设置非与所述目标突变位点配对的碱基处(5’端第1、2、6位)设置的突变碱基不会影响检测的结果;在目标突变的基础上设置非与所述目标突变位点配对的碱基处设置的突变碱基可以增强检测的效率。
[0157]
实施例3、测试在grna导向序列上第6号-第9号位置设置非与所述目标突变位点配对的碱基处设置的突变碱基对检测突变体效率的影响
[0158]
合成1条grna序列(如表4所示),并对grna设置:
①
存在目标突变的靶核酸,目标突变位于11号位置,
②
存在目标突变和非与所述目标突变位点配对的碱基处设置的突变碱基的靶核酸,非与所述目标突变位点配对的碱基处设置的突变碱基突变位于6、7、8、9位,存在目标突变和非与所述目标突变位点配对的碱基处设置的突变碱基的靶核酸的序列依次如表5所示:
[0159]
表4.grna的序列
[0160][0161]
表5.存在目标突变和非与所述目标突变位点配对的碱基处设置的突变碱基的靶核酸的序列
[0162][0163]
注:灰底色字为grna靶向的区域,大写字母为突变位置,大写t为目标突变,突变位置是在grna导向序列从5’端向3’端计数。
[0164]
如图6所示,当目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基设置于第6位时,可以明显看出,当仅存在非与所述目标突变位点配对的碱基处设置的突变碱基于第6位时,检测结果与阳性对照(grna与靶核酸无差异)基本一致;当目标突变和非与所述目标突变位点配对的碱基处设置的突变碱基同时存在时,检测结果与阳性对照有极明显的差别;
[0165]
如图7所示,当目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基设置于第7位时,可以明显看出,当仅存在非与所述目标突变位点配对的碱基处设
置的突变碱基于第7位时,检测结果与阳性对照(grna与靶核酸无差异)基本一致;当目标突变和非与所述目标突变位点配对的碱基处设置的突变碱基同时存在时,检测结果与阳性对照有极明显的差别;
[0166]
如图8所示,当目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基设置于第8位时,可以明显看出,当仅存在非与所述目标突变位点配对的碱基处设置的突变碱基于第8位时,检测结果与阳性对照(grna与靶核酸无差异)基本一致;当目标突变和非与所述目标突变位点配对的碱基处设置的突变碱基同时存在时,检测结果与阳性对照有极明显的差别;
[0167]
如图9所示,当目标突变位于第11位,非与所述目标突变位点配对的碱基处设置的突变碱基设置于第9位时,可以明显看出,当仅存在非与所述目标突变位点配对的碱基处设置的突变碱基于第9位时,检测结果与阳性对照(grna与靶核酸无差异)基本一致;当目标突变和非与所述目标突变位点配对的碱基处设置的突变碱基同时存在时,检测结果与阳性对照有极明显的差别;
[0168]
以上实验说明,设置非与所述目标突变位点配对的碱基处设置的突变碱基不会影响检测的结果;说明在目标突变的基础上设置非与所述目标突变位点配对的碱基处设置的突变碱基可以增强检测的效率。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1