ABCC11抑制剂
abcc11抑制剂
技术领域
1.本发明涉及12次跨膜型多药耐药性相关蛋白质抑制剂、及abcc11抑制剂。本发明进一步涉及含有上述抑制剂的组合物。更具体而言,本发明涉及用于腋臭的预防及治疗的药剂、以及含有该药剂的医药组合物或化妆用组合物。
背景技术:
2.尽管人类与其他动物类似,也会散发体味,但在人类的文化中,并不期望被感知到强烈的体味或特定的体味。其中,腋臭(axillary osmidrosis,以下本说明书中有时记载为“ao”)是以令人不快的体味和腋下的过度发汗为特征的慢性皮肤疾病(非专利文献1)。特别是,在体味强烈的人的比例较少的日本、中国等亚洲各国,有更厌烦ao的倾向,并认定其为疾病(非专利文献2)。
3.有报告称人atp结合盒转运蛋白c11(atp-binding cassette subfamily c member 11,abcc11)是ao的风险因子(非专利文献1~4)。abcc11的生理学的基质尚未完全阐明,但综合考虑abcc11缺失个体几乎没有患ao的风险、在分泌各种气味前体物质的腋窝大汗腺中存在发挥功能的abcc11,能够期待abcc11的抑制对于克服ao是有用的。
4.另一方面,为了治疗或减轻以高尿酸血症为原发疾病的急性关节炎、痛风的症状,已知各种尿酸排泄促进剂及尿酸产生抑制剂,其中,作为针对高尿酸血症管理而开发的黄嘌呤氧化酶的非嘌呤选择性抑制剂,非布司他(febuxostat)作为高尿酸血症治疗剂,由teijin pharma株式会社销售(商品名“菲布力”,专利文献1)。
5.现有技术文献
6.专利文献:
7.专利文献1:日本特许第2725886号
8.非专利文献:
9.非专利文献1:inoue y等、journal of plastic,reconstructive&aesthetic surgery:jpras 2010,63:1369-1374
10.非专利文献2:ishikawa t等、frontiers in genetics 2013,3:306
11.非专利文献3:toyoda y等、faseb journal:official publication of the federation of american societies for experimental biology 2009,23:2001-2013
12.非专利文献4:martin a等、j invest dermatol 2010,130:529-540
技术实现要素:
13.发明要解决的技术问题
14.ao的现存的应对方法主要为涂布除臭剂,该除臭剂含有:用于对腋臭的成因成分进行中和/消臭的碱及香料、以及以皮肤常驻菌的杀菌/除菌为目的的药剂。另外,作为ao的成因疗法,也会进行外科治疗,但成本高且有手术的风险,因此有时会对积极地进行治疗产生犹豫。
15.另一方面,目前并不存在以ao的治疗本身为目的的批准药剂,也不存在临床上使用的abcc11抑制剂。事实上几乎没有关于abcc11抑制剂的可利用的信息。
16.因此,需要开发对于ao等不适的状态的治疗方法。
17.用于解决课题的技术手段
18.本发明人等意外地发现,如上所述,包括作为以往用于高尿酸血症相的药剂的非布司他的多个化合物具有作为abcc11抑制剂的功能。进而,本发明人等发现,这些化合物还能够作为与abcc11具有类似的结构及功能的12次跨膜型多药耐药性相关蛋白质的抑制剂发挥功能,并基于这些见解完成了本发明。
19.即,本发明提供以下的发明。
20.[1]一种12次跨膜型多药耐药性相关蛋白质抑制剂,其有效成分为高尿酸血症治疗用化合物或其盐。
[0021]
[2]一种abcc11抑制剂,其有效成分为高尿酸血症治疗用化合物或其盐。
[0022]
[3]根据上述[1]或[2]所述的抑制剂,其中,化合物用通式i表示,
[0023][0024]
[式中,
[0025]
r1为卤素原子、硝基(-no2)、氰基(-cn)、甲酰基(-cho)或三氟甲基(-cf3),
[0026]
r2为氢原子或具有碳原子数1~10个的直链或支链的烷基的烷氧基,
[0027]
x为羧基(-co2h)、氨甲酰基(-conh2)或具有碳原子数1~5个的直链或支链的烷氧基的烷氧羰基,并且,
[0028]
y为氢原子或碳原子数1~4个的直链或支链的烷基。]
[0029]
[4]根据上述[3]所述的抑制剂,其中,x为羧基,y为甲基。
[0030]
[5]根据上述[3]或[4]所述的抑制剂,r2为具有碳原子数1~4个的直链或支链的烷基的烷氧基。
[0031]
[6]根据上述[3]~[5]中任一项所述的抑制剂,其中,r1为氰基。
[0032]
[7]根据上述[1]或[2]所述的抑制剂,其中,化合物用通式ii表示,
[0033][0034]
[式中,
[0035]
r3为氢原子、卤素原子、氰基(-cn)、羟基(-oh)、硝基(-no2)或氨基(-nh2),
[0036]
r4为羟基(-oh)、氨基(-nh2)、具有碳原子数1~6个的直链或支链的烷基的烷氧基
或者被碳原子数1~6个的直链或支链的烷基取代而成的单烷基氨基或二烷基氨基,
[0037]
r5为氰基(-cn)、碳原子数1~6个的直链或支链的烷基或碳原子数3~5个的环烷基,
[0038]
z为碳原子或氮原子,并且,
[0039]
w为硫原子或氧原子。]
[0040]
[8]根据上述[7]所述的抑制剂,其中,r3为f、cl或br。
[0041]
[9]根据上述[7]或[8]所述的抑制剂,其中,r4为羟基或具有碳原子数1~4个的直链或支链的烷基的烷氧基。
[0042]
[10]根据上述[7]~[9]中任一项所述的抑制剂,其中,r5为氰基或环丙基。
[0043]
[11]根据上述[7]~[10]中任一项所述的抑制剂,其中,z为氮原子,w为硫原子。
[0044]
[12]一种12次跨膜型多药耐药性相关蛋白质抑制剂,其有效成分为选自由非布司他(febuxostat)、雷西那德(lesinurad)或它们的盐组成的组中的化合物。
[0045]
[13]根据上述[1]~[12]中任一项所述的抑制剂,其在体外使表达12次跨膜型多药耐药性相关蛋白质的质膜小泡的12次跨膜型多药耐药性相关蛋白质介导的低分子物质的转运降低至80%以下。
[0046]
[14]一种医药组合物或化妆用组合物,其含有上述[1]~[13]中任一项所述的抑制剂。
[0047]
[15]根据上述[14]所述的医药组合物或化妆用组合物,其用于腋臭的预防或治疗。
[0048]
[16]根据上述[15]所述的医药组合物或化妆用组合物,其为外用药。
[0049]
[17]根据上述[16]记载的医药组合物或化妆用组合物,其为软膏、乳膏、乳液、露、喷雾、粉末或凝胶的方式。
[0050]
本说明书包括2019年8月21日申请的、作为本技术的优先权的基础的美国临时申请第62/890,053号的公开内容。
[0051]
发明效果
[0052]
通过本发明,可以以与以往使用的药剂及治疗法不同的机制,进行ao的预防及治疗。本发明的抑制剂具有安全性及稳定性,在对人的应用中是非常适宜的。另外,通过本发明,可以提供对于抗癌药物耐药性的全新治疗药物。
附图说明
[0053]
图1示出质膜小泡中的abcc11的表达。na
+
/k
+-atpase:内参(loading control)。
[0054]
图2示出在atp的存在下或不存在下的[1,2,6,7-3
h(n)]-硫酸脱氢表雄酮(dhea-s)的转运活性(n=3)。**:p<0.01、ns:无显著性差异(参量tukey-kramer多重比较检验、相对于其他组)。
[0055]
图3示出基于abcc11的dhea-s转运随时间增加(n=3)。++:p<0.01(双侧t检验)。
[0056]
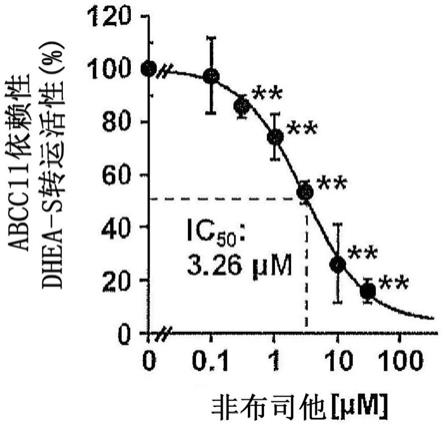
图4示出基于非布司他的、abcc11介导的dhea-s转运的浓度依赖性抑制(n=4)。**:p<0.01(dunnett检验、相对于0μm的值)。
[0057]
图5示出非布司他对于abcc2功能的效果。在3.26μm的非布司他(fb)的存在下或不存在下,对雌二醇17β-d-葡糖苷酸[estradiol-6,7-3
h(n)](e217βg)转运活性进行5分钟测
定。数据以平均
±
标准偏差的形式示出(n=3)。统计分析使用bartlett检验及参量tukey-kramer多重比较检验进行。图中的a、b及c表示示出的组间存在显著性差异(p<0.05)。
[0058]
图6示出别嘌醇(alloprinol、al)、苯溴香豆酮(benzbromarone、bz)、非布司他(fb)、雷西那德(lesinurad、ls)、羟嘌呤醇(oxypurinol、ox)、及丙磺舒(probenecid、pr)对于abcc11介导的dhea-s转运的效果(n=4)。对照表示无药剂添加。
[0059]
图7示出非布司他对于abcc2及abcc4的功能的效果。在3.26μm的非布司他(fb)的存在下或不存在下,测定表达abcc2或abcc4的质膜小泡中的atp依赖的e217βg转运活性。数据以平均
±
标准偏差的形式示出(n=3)。
[0060]
图8示出非布司他对于abcc2及abcc4的功能的效果。在3.26μm的非布司他(fb)的存在下或不存在下,测定表达abcc2或abcc4的质膜小泡中的atp依赖的dhea-s转运活性。数据以平均
±
标准偏差的形式示出(n=3)。
具体实施方式
[0061]
《12次跨膜型多药耐药性相关蛋白质抑制剂》
[0062]
本发明提供一种有效成分为高尿酸血症治疗用化合物或其盐的12次跨膜型多药耐药性相关蛋白质抑制剂。
[0063]
本说明书中使用的用语“12次跨膜型多药耐药性相关蛋白质”是局部存在于细胞膜上,负责低分子物质的膜透过的atp结合盒(atp-binding cassette、abc)转运体的一种(toyoda y等、xenobiotica 2008 jul,38(7-8):833-62)。具体而言,本说明书中的“12次跨膜型多药耐药性相关蛋白质”选自由abcc4、abcc5、abcc11及abcc12组成的组。
[0064]
abc转运体中,报告有10种包括假基因在内的属于多药耐药性相关蛋白质(multidrug resistance-associated protein,mrp)类的abc转运体。其中,与相对于其他多药耐药性相关蛋白质的情况相比,abcc4、abcc5、abcc11及abcc12具有彼此类似的氨基酸序列。已知这4种转运体蛋白质会形成12次跨膜型的多药耐药性相关蛋白质组,并且与相对于其他多药耐药性相关蛋白质相的情况相比,atp依赖地转运的物质的种类、所谓的底物特异性也彼此类似(toyoda y等、xenobiotica 2008 jul,38(7-8):833-62)。
[0065]
本发明人等的发现中,本发明的抑制剂会抑制abcc4、abcc5、abcc11及abcc12介导的转运,另一方面,还表现出可能不会抑制属于与abcc11不同的组(17次跨膜型多药耐药性相关蛋白质组)的abcc1、abcc2、abcc3、abcc6、及abcc10介导的转运。
[0066]
因此,当初确认到具有abcc11抑制作用的高尿酸血症治疗用化合物或其盐抑制12次跨膜型多药耐药性相关蛋白质介导的物质的转运,可以作为abcc4抑制剂、abcc5抑制剂、abcc11抑制剂和/或abcc12抑制剂发挥功能。
[0067]
特别是确认了abcc4、abcc5、及abcc11可以将抗癌剂排出细胞外,因此本发明的抑制剂也可作为用于克服癌症的多药耐药性的助剂发挥功能。
[0068]
abcc4基因的碱基序列信息能够作为由ncbi等提供的数据库中的geneid:10257而获取,氨基酸序列信息例如能够作为参照序列:np_005836.2等而获取。
[0069]
abcc5基因的碱基序列信息能够作为由ncbi等提供的数据库中的geneid:10057而获取,氨基酸序列信息例如能够作为参照序列:np_005679等而获取。
[0070]
abcc11基因的碱基序列信息能够作为由ncbi等提供的数据库中的geneid:85320、
登记(accession)no.nm_033151等而获取,氨基酸序列信息例如能够作为参照序列:np_149163.2等而获取。
[0071]
abcc12基因的碱基序列信息能够作为由ncbi等提供的数据库中的geneid:94160而获取,氨基酸序列信息例如能够作为登记(accession)no.np_150229.2等而获取。
[0072]
本说明书中,“12次跨膜型多药耐药性相关蛋白质抑制”是指:在体外或体内使12次跨膜型多药耐药性相关蛋白质的功能降低或消失,例如可以指使12次跨膜型多药耐药性相关蛋白质介导的低分子物质的转运或分泌降低或消失。降低为统计学上被视为显著的降低即可,并无特别限定,例如相对于在预想具有12次跨膜型多药耐药性相关蛋白质抑制效果的化合物不存在的情况下的转运量或分泌量,可以将转运量或分泌量降低至80%以下、70%以下、60%以下、50%以下或40%以下。
[0073]
作为12次跨膜型多药耐药性相关蛋白质介导并分泌的“低分子物质”,并无特别限定,可举出例如硫酸脱氢表雄酮(dhea-s)、雌酮-3-硫酸等雄激素类固醇、camp及cgmp等环状核苷酸、白三烯c4及s-(2,4-二硝基苯基)-谷胱甘肽等谷胱甘肽共轭体、雌二醇17-β-d-葡糖苷酸及胆汁酸盐等葡糖醛酸共轭体、5-氟尿嘧啶(5-fu)及氨甲蝶呤(mtx)等抗癌剂、9-(2-膦酰基-甲氧基乙基)腺嘌呤(pmea)等抗病毒药物。
[0074]
本说明书中,“高尿酸血症治疗用化合物”是指显示血清尿酸值下降作用或可以期待血清尿酸值下降作用的物质,是特征在于具有尿酸生成酶抑制活性及尿酸转运体抑制活性的物质。
[0075]
《abcc11抑制剂》
[0076]
另外,本发明提供一种abcc11抑制剂,其有效成分为高尿酸血症治疗用化合物或其盐。
[0077]
本发明人等团队等报告了腋臭(axillary osmidrosis、ao)的风险是由abcc11基因中的非同义单核苷酸多态性c.538g》a(p.gly180arg)决定的(inoue y等、journal of plastic,reconstructive&aesthetic surgery:jpras 2010,63:1369-1374;toyoda y等、faseb journal:official publication of the federation of american societies for experimental biology 2009,23:2001-2013;martin a等、j invest dermatol 2010,130:529-540)。通过生物化学分析,该氨基酸取代(变异类型:arg180)会促进de novo合成abcc11蛋白质的蛋白酶体分解,由此丧失abcc11的细胞内功能。发挥功能的abcc11(野生型:gly180)存在于分泌各种气味的前体的腋窝大汗腺(toyoda y等、int j mol sci 2017,18:417),因此abcc11功能的抑制有助于ao的预防和治疗。
[0078]
如上所述,abcc11局部存在于细胞膜上,是负责低分子物质的膜透过的atp结合盒(atp-binding cassette、abc)转运体的一种(toyoda y等、xenobiotica 2008 jul,38(7-8):833-62)。
[0079]
需要说明的是,本说明书中,“abcc11抑制”是指在体外或体内使上述的野生型(功能性)abcc11的功能降低或消失,例如可以指使abcc11介导的低分子物质的转运或分泌降低或消失。降低为统计学上被视为显著的降低即可,并无特别限定,例如相对于预想具有abcc11抑制效果的化合物在不存在下的转运量或分泌量,可以将转运量或分泌量降低至80%以下、70%以下、60%以下、50%以下或40%以下。此处,作为abcc11介导分泌的“低分子物质”,并无特别限定,可举出例如硫酸脱氢表雄酮(dhea-s)、雌酮-3-硫酸等雄激素类固
醇、camp及cgmp等环状核苷酸、白三烯c4及s-(2,4-二硝基苯基)-谷胱甘肽等谷胱甘肽共轭体、雌二醇17-β-d-葡糖苷酸及胆汁酸盐等葡糖醛酸共轭体、5-氟尿嘧啶(5-fu)及氨甲蝶呤(mtx)等抗癌剂、9-(2-膦酰基-甲氧基乙基)腺嘌呤(pmea)等抗病毒药物。
[0080]
因此,本发明的abcc11抑制剂特别地基于使功能性abcc11介导的腋臭诱发物质的分泌降低或消失,由此可以适宜地用于腋臭的预防或治疗。然而,本发明的abcc11抑制剂通过使abcc11介导的其他功能、例如其他低分子物质的转运降低或消失,可以具有其他有利的效果。例如,报告了abcc11高表达细胞系在肺癌等中获得对5-fu等抗癌剂的抗性(uemura,t等、cancer sci.101(11):2404-2410,2010),因此,能够预想abcc11抑制剂也可用于使抗癌剂的效果增强。
[0081]
与人类不同,小鼠、大鼠等啮齿类不具有abcc11基因,因此通过体内实验来研究abcc11抑制的生理学影响几乎是不现实的。本发明人等使用表达abcc11的质膜小泡,开发了适于abcc11抑制剂的探索的体外转运试验(toyoda y等、journal of dermatology 2020,doi:10.1111/1346-8138.15512)。
[0082]
简而言之,通过腺病毒介导的一过性abcc11表达293a细胞来制备质膜小泡,进行作为abcc11基质的[1,2,6,7-3
h(n)]-硫酸脱氢表雄酮(dhea-s)的免疫印迹及体外转运试验。如图1所示,制备的小胞表达abcc11,借助abcc11可以atp依赖地向小胞内转运dhea-s(图2)。还确认该dhea-s转运会随时间增大(图3)。
[0083]
然后,在各种化合物的存在下,研究该abcc11介导的dhea-s转运活性,意外地确认到作为高尿酸血症治疗用化合物而已知的化合物能够浓度依赖地抑制转运,特别是确认到非布司他及雷西那德(lesinurad)具有较高效果,能够确认它们为新型的abcc11抑制剂。若考虑与abcc11蛋白质的相互作用,特别是非布司他及雷西那德的类似化合物也可以具有同样的活性。
[0084]
另外,本发明人等还发现:已知有高尿酸血症的治疗效果的别嘌醇(alloprinol)、苯溴香豆酮(benzbromarone)、羟嘌呤醇(oxypurinol)、及丙磺舒(probenecid)均可抑制abcc11介导的dhea-s转运活性。
[0085]
进而,本发明人等发现:抑制abcc11介导的物质的转运的化合物并不会抑制属于17次跨膜型多药耐药性相关蛋白质组的abcc2介导的物质的转运,与此相对,抑制abcc11介导的物质的转运的化合物会抑制与abcc11同属于12次跨膜型多药耐药性相关蛋白质组介导的abcc4的低分子物质的转运。若考虑由12次跨膜型多药耐药性相关蛋白质组的结构及功能的类似性、及与17次跨膜型多药耐药性相关蛋白质组的不同而产生的基质的不同,则与本发明的抑制剂的机制共通。
[0086]
一个实施方式中,本发明提供一种12次跨膜型多药耐药性相关蛋白质抑制剂或abcc11抑制剂,其有效成分为通式i所示的化合物或其盐。
[0087]
[0088]
[式中,
[0089]
r1为卤素原子、硝基(-no2)、氰基(-cn)、甲酰基(-cho)或三氟甲基(-cf3),
[0090]
r2为氢原子或具有碳原子数1~10个的直链或支链的烷基的烷氧基,
[0091]
x为羧基(-co2h)、氨甲酰基(-conh2)或具有碳原子数1~5个的直链或支链的烷氧基的烷氧羰基,并且,
[0092]
y为氢原子或碳原子数1~4个的直链或支链的烷基。]
[0093]
并无特别限定,上述式i中,优选x为羧基、y为甲基的化合物。
[0094]
作为一例,式i中,优选r2为具有碳原子数1~4个的直链或支链的烷基的烷氧基的化合物。
[0095]
另外,作为一例,式i中,优选r1为氰基的化合物。
[0096]
式i所示的化合物中,作为特别优选的化合物,可举出下述的结构所示的非布司他或其盐。
[0097][0098]
另一实施方式中,本发明提供一种12次跨膜型多药耐药性相关蛋白质抑制剂或abcc11抑制剂,其有效成分为通式ii所示的化合物或其盐。
[0099][0100]
[式中,
[0101]
r3为氢原子、卤素原子、氰基(-cn)、羟基(-oh)、硝基(-no2)或氨基(-nh2),
[0102]
r4为羟基(-oh)、氨基(-nh2)、具有碳原子数1~6个的直链或支链的烷基的烷氧基或被碳原子数1~6个的直链或支链的烷基取代而成的单烷基氨基或二烷基氨基,
[0103]
r5为氰基(-cn)、碳原子数1~6个的直链或支链的烷基或碳原子数3~5个的环烷基,
[0104]
z为碳原子或氮原子,并且,
[0105]
w为硫原子或氧原子。]
[0106]
并无特别限定,上述式ii中,优选r3为卤素原子、特别是为f、cl或br的化合物。
[0107]
另外,并无特别限定,上述式ii中,r4优选羟基或具有碳原子数1~4个的直链或支链的烷基的烷氧基的化合物。
[0108]
另外,并无特别限定,上述式ii中,优选r5为氰基或环丙基的化合物。
[0109]
另外,并无特别限定,上述式ii中,优选z为氮原子、w为硫原子的化合物。
[0110]
式ii所示的化合物中,作为特别优选的化合物,可举出下述的结构所示的雷西那德或其盐。
[0111][0112]
因此,本发明此外还提供一种12次跨膜型多药耐药性相关蛋白质抑制剂或abcc11抑制剂,其有效成分为选自由非布司他、雷西那德或它们的盐组成的组的化合物。
[0113]
作为包含上述通式i及通式ii的化合物的、高尿酸血症治疗用化合物的盐,为制药上允许的盐即可,并无特别限定,可举出例如钠盐、钾盐、镁盐、钙盐、铝盐、锌盐、铵盐、盐酸盐、硫酸盐、乙酸盐、苯甲酸盐、三氟乙酸盐等。
[0114]
本发明的抑制剂并无特别限定,与抑制剂不存在下的分泌量相比,能够将表达野生型abcc11蛋白质的个体中的大汗腺分泌物质的分泌量降低至例如80%以下、70%以下、60%以下、50%以下或40%以下。
[0115]
上述的效果可以通过本发明人等确立的上述的体外转运试验容易地确认。即,本发明的抑制剂在体外可以使表达野生型abcc11蛋白质的质膜小泡的abcc11介导的低分子物质的转运降低至80%以下、70%以下、60%以下、50%以下或40%以下。
[0116]
另外,本发明的抑制剂在体外可以使表达12次跨膜型多药耐药性相关蛋白质的质膜小泡的12次跨膜型多药耐药性相关蛋白质介导的低分子物质的转运降低至80%以下、70%以下、60%以下、50%以下或40%以下。
[0117]
作为确认体外转运试验的效果可以使用的低分子物质,由abcc4、abcc5、abcc11和/或abcc12介导并能够转运的天然或合成的化合物均可,并无特别限定,例如可适宜地使用下述的实施例中使用的[1,2,6,7-3
h(n)]-硫酸脱氢表雄酮(dhea-s)或雌二醇17β-d-葡糖苷酸[estradiol-6,7-3
h(n)](e217βg)。
[0118]
本发明的抑制剂例如可以作为克服癌症的多药耐药性的助剂使用。此外,本发明的抑制剂还可特别适宜地用于腋臭的预防或治疗。
[0119]
《医药组合物/化妆用组合物》
[0120]
本发明此外还提供含有上述的本发明的abcc11抑制剂或12次跨膜型多药耐药性相关蛋白质抑制剂的医药组合物或化妆用组合物。此处,医药组合物包括含有abcc11抑制剂作为有效成分的医药品及准药品。本发明的医药组合物例如可以为腋臭的预防或治疗用组合物。另外,本发明的化妆用组合物可以为含有abcc11抑制剂的止汗剂或除臭制品。另外,本发明的医药组合物可以为含有12次跨膜型多药耐药性相关蛋白质抑制剂作为有效成分的、用于癌症的治疗或预防的医药组合物。
[0121]
本发明的组合物可以通过任意的适宜的给药路经进行给药。例如,本发明的组合物可以通过片剂、粉末剂、液剂等方式进行口服给药。另外,本发明的组合物也可进行包括通过注射或注入对静脉内、肌肉内、腹腔内、肿瘤内等进行给药的、全身的或局部的非口服
给药。人的腋窝大汗腺对毛囊开放,因此以腋臭的预防或治疗为目的时,或者以止汗或除臭为目的时,给药路经为对腋窝等皮肤进行局部地给药是有效的,因此,组合物优选制成外用组合物。
[0122]
以外用组合物方式使用时的医药组合物及化妆用组合物的方式为本领域中通常使用的方式即可,并无特别限定,可采用软膏、乳膏、乳液、露、喷雾、粉末、凝胶等方式。涂布或喷雾组合物时,不仅是腋窝,应用于发汗等可能导致产生体味的部位,例如脖子、后背,手脚、脚底、头部、阴部等均可。
[0123]
本发明的组合物中,除上述的abcc11抑制剂外,可以添加腋臭的预防或治疗等目的中有效的其他成分,例如杀菌剂、抗菌剂、碱物质、香料等。另外,本发明的组合物中并无限定,根据给药方式,可以适当添加赋形剂、缓冲剂、表面活性剂、抗氧化剂、保存剂、紫外线吸收剂、粉末等。另外,用于癌症的治疗或预防时,本发明的组合物中,可以单独或例如与抗癌剂组合而包含12次跨膜型多药耐药性相关蛋白质抑制剂。
[0124]
作为本发明的医药组合物中的有效成分的抑制剂,以已经获得临床使用许可的药物非布司他及雷西那德为代表,是容许用于人并且安全稳定的药剂。
[0125]
进行口服给药时,在连续12天,以1天1次40mg的用量对健康的受检者进行给药时,非布司他的最大血浆游离浓度显示为0.126μm(khosravan r等、clin pharmacokinet 2006,45:821-841),为了发挥腋窝中腋臭的预防或治疗效果,口服给药的非布司他需要更高的用量。
[0126]
本发明的组合物并无特别限定,相对于组合物的总重量,可以以0.001~10重量%、优选为0.01~3重量%、更优选为0.1~1重量%的范围含有上述的本发明的abcc11抑制剂。
[0127]
将本发明的组合物以外用组合物形式应用时,根据剂形不同,并无特别限定,例如1天1~数次、将例如10mg~10g、优选为50mg~5g的组合物通过通常的涂布或喷雾等应用于腋窝等,可以期待理想的效果。
[0128]
《方法》
[0129]
此外,本发明还提供一种腋臭的治疗方法及预防方法,其包括将上述的本发明的abcc11抑制剂或含有该抑制剂的本发明的组合物对对象进行给药的过程。另外,本发明提供一种止汗或除臭方法,其包括将上述的本发明的abcc11抑制剂或本发明的组合物对对象进行给药的过程。本发明中,并无特别限定,对象为人,特别是表达野生型(功能性)abcc11的人。
[0130]
另外,本发明提供一种疾病的治疗方法及预防方法,其包括将上述的本发明的12次跨膜型多药耐药性相关蛋白质抑制剂或含有该抑制剂的本发明的组合物对对象进行给药的过程。疾病并无限定,例如可以为具有抗癌药物耐药性的癌症。
[0131]
实施例
[0132]
以下举出实施例对本发明进行进一步详细的说明,但本发明并不受这些实施例的任和限定。以下的实施例中无特别记载的化学物质均为市售,使用分析级的化学物质。
[0133]
需要说明的是,统计分析均采用excel 2019和statcel4 add-in软件(oms出版社、埼玉、日本)一同进行。分析多组时,使用bartlett检验比较组间方差的相似性。方差一致性的检验合格时,全部配对比较均采用参量tukey-kramer多重比较检验,或对对照组的比较
使用dunnett检验。分析一对定量数据的情况下,使用f检验比较数据组的方差后,进行无对应的student的t检验。统计学的显著性用小于0.05或小于0.01的p值定义。
[0134]
[实施例1 表达abcc11的质膜小泡的制备]
[0135]
在添加有10%胎牛血清(biowest、nuaille、france)、1%青霉素-链霉素(nacalai tesque)、2mm l-谷氨酰胺(nacalai tesque、京都、日本)、及1
×
非必须氨基酸(life technologies、东京、日本)的达尔伯克改良伊格尔培养基(nacalai tesque)中,于37℃,空气中5%(v/v)co2的加湿气氛下,维持源自人胎肾293(hek293)的293a细胞(r70507、invitrogen)。
[0136]
使293a细胞感染按toyoda y等、international journal of molecular sciences 2017,18:417记载的方式制作的abcc11表达或egfp表达(对照)腺病毒后,以toyoda y等、international journal of molecular sciences 2017,18:417记载的方式制备质膜小泡。
[0137]
在液氮中将得到的质膜小泡急速冻结,使用前保存于-80℃。质膜小泡的蛋白质浓度按照制造者的流程(protocol),使用以牛血清白蛋白为标准的bca蛋白质检测试剂盒(pierce、rockford、il、美国)定量。
[0138]
对于质膜小泡中的abcc11蛋白质的表达,通过toyoda y等、international journal of molecular sciences 2017,18:417;toyoda y等、faseb journal:official publication of the federation of american societies for experimental biology 2009,23:2001-2013记载的免疫印迹法,稍作修饰进行了研究。
[0139]
简而言之,将制备的试样在聚丙烯酰胺凝胶上进行电泳分离,以15v进行70分钟电泳,并移至hybond(注册商标)ecl
tm
硝酸纤维素膜(ge healthcare、buckinghamshire、英国)。
[0140]
为了封闭,在包含0.05%tween 20及5%脱脂奶(tbst脱脂奶)的tris缓冲生理盐水中,将膜在4℃下孵育一夜。
[0141]
用大鼠单克隆抗abcc11抗体(m8i-74;abcam、cambridge、ma、usa;200倍稀释)及兔多克隆抗na
+
/k
+-atpaseα抗体(sc-28800、santa cruz biotechnology、santa cruz、ca、美国、1000倍稀释)进行探针后,分别与山羊抗大鼠免疫球蛋白g(igg)-辣根过氧化物酶(hrp)偶联抗体(na935v、ge healthcare、2000倍稀释)及驴抗兔igg-hrp偶联抗体(na934v、ge healthcare、3000倍稀释)一起孵育。全部抗体均在tbst脱脂奶中使用。
[0142]
对于hrp依赖性发光,用ecl
tm prime western blotting detection reagent(ge healthcare)使其着色,使用multi-imaging analyzer fusion solo4
tm
系统(vilber lourmat、eberhardzell、德国)检验。
[0143]
其结果,如图1所示,源自感染abcc11表达腺病毒的293a细胞的质膜小泡中,确认到abcc11的表达。另一方面,源自感染egfp表达(对照)腺病毒的细胞的质膜小泡(mock)中,未确认abcc11的表达。需要说明的是,全部小胞中均确认到na
+
/k
+-atpase同程度的地表达。
[0144]
[实施例2 小胞转运试验]
[0145]
对toyoda y等、international journal of molecular sciences 2017,18:417记载的迅速过滤技术进行轻微修正并进行对作为abcc11基质的[1,2,6,7-3
h(n)]-硫酸脱氢表雄酮(dhea-s)(perkinelmer、waltham、ma、美国)的abcc11表达质膜小泡及向对照质膜
小泡的转运进行研究的体外实验。
[0146]
简而言之,将质膜小泡与反应混合物(10mm tris/hcl、250mm蔗糖、10mm mgcl2、10mm磷酸肌酸、1mg/ml磷酸肌酸激酶、及50mm atp或作为atp代替的amp、ph7.4)中的[1,2,6,7-3
h(n)]-dhea-s 100nm一同在37℃下孵育5分钟,测定源自捕获的dhea-s的放射活性。
[0147]
为了使源自用于捕获质膜小泡的滤膜(mf-millipore membrane、hawp02500;0.45μm孔径及25mm径、millipore、日本、东京)上非特异吸附的放射性标识dhea-s的本底信号减少,在使用前,将滤膜与包含0.2%(v/v)dmso的冰冷终止缓冲液(250mm蔗糖、0.1m nacl、2mm edta、及10mm tris-hcl、ph7.4)中的胆固醇2μm(和光纯药工业、东京、日本)一同孵育。
[0148]
其结果,如图2所示,表达abcc11的质膜小泡中,示出dhea-s被atp依赖地转运。
[0149]
[实施例3 dhea-s转运的经时观察]
[0150]
与实施例2同样地,对表达abcc11的质膜小泡及对照质膜小泡中的atp依赖性的dhea-s的转运进行经时观察(2.5分钟、5分钟、10分钟及20分钟的孵育)。对于atp依赖的dhea-s转运,通过用atp不存在下的情况的dhea-s转运活性减去atp存在下的活性来计算。
[0151]
其结果,图3如所示,观察到表达abcc11的质膜小泡中,dhea-s的转运量随时间增大。
[0152]
[实施例4 非布司他通过abcc11抑制效果]
[0153]
本发明人等在预备筛选阶段确认了非布司他的abcc11抑制效果(未示出数据),因此对非布司他(0.1~30μm)对于abcc11的浓度依赖的抑制效果进行了研究。对于abcc11依赖的dhea-s转运活性,通过用对于对照质膜小泡的atp依赖的dhea-s转运活性减去对于表达abcc11的质膜小泡的活性来计算。dhea-s转运活性在指定的浓度的非布司他的存在下测定5分钟。
[0154]
本实施例中,以捕获的间隙[ml/mg蛋白质/分=dhea-s的捕获水平(每分钟崩坏(dpm)/mg蛋白质/分钟)/孵育混合液中的dhea-s水平(dpm/ml)]的形式计算各组的转运活性,以在非布司他不存在下(0μm)的转运活性为100,以相对百分比的形式表示。
[0155]
基于计算的值,通过上述的excel 2019(microsoft、redmond、wa、usa),使用最小二乘法,按照以下式,求出拟合曲线(chen zs等、mol pharmacol 2005;67:545-557)。
[0156]
预测值[%]=100-((e_max
×cn
)/(ec
50n
+cn)
[0157]
(式中,emax为最大效果、ec
50
为最大有效浓度的一半、c为被验化合物的浓度、n为sigmoid拟合因子。)
[0158]
最后,基于该结果,计算ic
50
。
[0159]
其结果,如图4所示,非布司他浓度依赖地抑制abcc11依赖的dhea-s转运活性,计算ic
50
值为3.26μm。
[0160]
[实施例5 对于abcc2依赖的转运的效果]
[0161]
为了确认非布司他的抑制效果对于abcc11是否具有特异性,研究非布司他对于作为与abcc11不同的atp结合盒转运体的abcc2(已知mrp2)的功能有无效果。
[0162]
出于该目的,使用功能在以前的研究(toyoda y等、scientific reports 2016,6:24586)中得到确认的人abcc2表达质膜小泡及对照质膜小泡(genomembrane公司、横浜、日本),使用雌二醇17β-d-葡糖苷酸[estradiol-6,7-3
h(n)](e217βg)(perkinelmer)(反应混合物中100nm)作为abcc2基质,在实施例4中计算的ic
50
值为3.26μm的非布司他(fb)的存在
下或不存在下,在37℃下孵育5分钟。其他测定条件依据实施例2进行。
[0163]
其结果,如图5所示,观察到abcc2表达质膜小泡中atp依赖性的e217βg转运,但未确认到非布司他引起的abcc2的抑制。
[0164]
[实施例6 各种化合物引起的abcc11抑制活性]
[0165]
与实施例4同样地,对别嘌醇(alloprinol、al)、苯溴香豆酮(benzbromarone、bz)、非布司他(fb)、雷西那德(lesinurad、ls)、羟嘌呤醇(oxypurinol、ox)、及丙磺舒(probenecid、pr)对于abcc11依赖的dhea-s转运活性有无抑制效果进行研究。
[0166]
简而言之,将质膜小泡与包含最终浓度3μm的各化合物的反应混合物(10mmtris/hcl、250mm蔗糖、10mm mgcl2、10mm磷酸肌酸、1mg/ml磷酸肌酸激酶、及50mm atp或作为atp的代替amp、ph7.4)中的[1,2,6,7-3
h(n)]-dhea-s的100nm一同在37℃下孵育5分钟,测定捕获到的源自dhea-s的放射活性。以捕获的间隙[ml/mg蛋白质/分=dhea-s的捕获水平(每分钟崩坏(dpm)/mg蛋白质/分钟)/孵育混合液中的dhea-s水平(dpm/ml)]的形式计算各组的转运活性,以在试验化合物不存在下(0μm)的转运活性为100的相对百分比形式表示。
[0167]
其结果,如图6所示,发现已知具有高尿酸血症的治疗效果的别嘌醇、苯溴香豆酮、雷西那德、羟嘌呤醇、及丙磺舒与非布司他同样,均抑制abcc11介导的dhea-s转运活性,与未添加化合物的情况(对照)相比,使转运活性降低至80%左右。特别地发现:雷西那德具有与非布司他同程度的抑制活性,与3μm的浓度下的对照相比,使转运活性降低至约30%。
[0168]
[实施例7 对于abcc4依赖的转运的效果]
[0169]
实施例5中,确认表达abcc2的质膜小泡中的atp依赖性的e217βg转运未被非布司他抑制
[0170]
此处,对非布司他对于报告中与abcc11结构及功能接近的abcc4(已知mrp4)的功能有无效果进行研究。abcc4对于作为abcc11的基质的dhea-s、及作为abcc2的基质的e217βg均可atp依赖地进行转运。
[0171]
使用人abcc2表达质膜小泡、人abcc4表达质膜小泡及对照质膜小泡(均从genomembrane公司获得),使用雌二醇17β-d-葡糖苷酸[estradiol-6,7-3
h(n)](e217βg)(perkinelmer)及[1,2,6,7-3
h(n)]-硫酸脱氢表雄酮(dhea-s)(perkinelmer)(反应混合物中100nm)作为基质,在3.26μm的非布司他的存在下(fb)或不存在下(non),于37℃下孵育5分钟。其他测定条件依据实施例2进行。
[0172]
其结果,如图7及8所示,表达abcc4的质膜小泡中,观察到atp依赖性的e217βg转运及dhea-s转运,但在非布司他存在下,转运活性均被抑制。对此,表达abcc2的质膜小泡中,如实施例5所示,未确认到abcc2介导的e217βg转运的基于非布司他的抑制(图7)。另外,表达abcc2的质膜小泡中,未观察到atp依赖的dhea-s转运活性(图8)。
[0173]
对于本说明书中引用的全部出版物、专利及专利申请,均通过直接引用并入本说明书。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1