脂肪酸酯化方法与流程
1.本发明涉及一种游离脂肪酸的酶促酯化方法。特别地,本发明涉及使用闪蒸操作从酶反应混合物中除去水的这样的方法。
背景技术:
2.来自化石燃料的co2会引发的环境问题,这迫使世界寻求可持续的解决方案。
3.源自化石碳源的传统柴油燃料是目前co2排放的主要贡献者,开发能够驱动现有柴油发动机的可持续和可再生燃料将是一种降低与柴油相关的co2排放的可能方式。这种燃料是例如脂肪酸甲酯,也被称为生物柴油,可通过对源自由甘油酯和游离脂肪酸(ffa)组成的脂肪和油的脂肪酸进行酯化而获得。
4.用于生产生物柴油的生物质原料主要由甘油酯组成,但廉价、低质量的原料通常也含有大量的游离脂肪酸(ffa)。然而,ffa也是生物柴油的潜在来源,因为它们可通过酯化(酯交换)转化为生物柴油。
5.传统上,生物柴油的生产是通过化学催化进行的。通过甘油酯的酯交换进行碱催化生产生物柴油是最常用的方法,但也有缺点。重要的是,在ffa浓度较高的情况下,化学碱催化无法处理低质量和多变质量的原料。为了开发这样的原料,需要广泛的预处理。目前,典型的预处理是硫酸催化ffa的酯化。
6.对广泛的预加工的需求是一个问题,因为这大大降低了方法的盈利能力。为了在低质量原料的可用性方面获得更环保、更盈利和更稳健的方法,酶促催化提供了一种解决方案。
7.酶促催化对原料质量不太敏感。它需要更接近环境的操作条件,并且由于高选择性和低添加需求,会产生更小、更清洁和更容易处理的废物流。此外,酶是可再生的催化剂,并且利用酶的方法往往比化学方法更环保。
8.相对于化学方法,酶促生物柴油方法仅需要较少的预加工,并且能够将ffa和甘油酯都转化为生物柴油。
9.然而,酶促方法确实有一些局限性。游离脂肪酸与短链醇的酶促酯化反应生成生物柴油和水是可逆的。因此,过量的水将使该反应朝着不利于生物柴油生产的方向进行。同时,水的除去有利于生物柴油的形成,从而具有降低酶稳定性的负面作用。
10.尽管目前的酶促方法具有高转化率,但由于不可避免的平衡,产物仍含有2-3wt%ffa(不考虑原料)。一种解决方案是使用碱洗来消除残留的ffa,但是因为会产生皂,所以需要额外加工,这会伴随大量废水作为副产物产生。
11.因此,仍然需要开发用于生物柴油生产的酶促方法,特别是提高酶促方法的效率。
12.另一个目的可以是避免碱洗,以减少废物产生和皂回收的成本。
技术实现要素:
13.本发明的第一方面涉及一种游离脂肪酸的酶促酯化方法,该方法包括以下步骤:
14.a.提供包含游离脂肪酸的组合物i),
15.b.向步骤a中提供的组合物中添加:
16.ii)酯酶,
17.iii)甘油,和
18.iv)短链醇
19.并且混合
20.c.培养步骤b的混合物,使得该酯酶催化游离脂肪酸的酯化,
21.d.对从步骤c得到的经培养的混合物进行闪蒸干燥,
22.e.将步骤d中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合
23.f.培养步骤e中获得的混合物,由此,步骤b中提供的酯酶(ii)催化游离脂肪酸的酯化。
24.本发明的第二方面涉及酯酶在本发明的方法中的用途。
25.本发明的第三方面涉及一种用于闪蒸干燥包含游离脂肪酸的混合物的方法,所述混合物包含游离脂肪酸、酯酶、甘油、短链醇和水;并且所述方法包括提供所述混合物和随后闪蒸干燥所述混合物的步骤,其中该闪蒸干燥在不使该酯酶变性的条件下进行。
附图说明
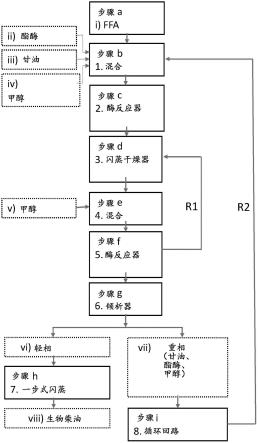
26.图1示出了根据本发明的方法的一个实施例的流程图。
27.步骤a、步骤b、步骤c、步骤d、步骤e、步骤f、步骤g、步骤h、和步骤i是如权利要求1所描述的本发明的方法中的步骤。组成如下:i)包含脂肪酸的组合物;ii)酯酶,iii)甘油,iv)短链醇,在一个实施例中为甲醇;v)短链醇,在一个实施例中为甲醇;vi)轻相;vii)重相(包含甘油、酯酶和短链醇,在一个实施例中为甲醇),viii)生物柴油。
28.图2示出了通过脂肪酸或脂肪酸原料与醇的酶催化酯交换来制造脂肪酸烷基酯的方法的示意图。
29.图3示出了典型的酶促生物柴油酯交换方法的示意图,该方法包括在酶步骤之后进行碱洗以除去ffa。
30.图4示出了本发明的ffa酯化方法的示意图。(排出对应于吹扫)。
31.图5示出了来自实例1的结果。随着时间推移,ffa的量减少。
32.图6示出了来自实例3的结果:酯酶和甘油重复使用。黑色柱:初始速率,灰色柱:平衡时的ffa
33.图7示出了来自实例4逐步干燥的结果。圆圈:1%脂肪酶calb l,5%甘油,4%甲醇,300g fame,初始水≈5500ppm。三角形:0.455%脂肪酶calb l,5%甘油,6%甲醇,30g fame,初始水≈2000ppm。
34.图8示出了来自实例5的结果。在不同温度培养后的ffa转化率。
35.这些图仅用于说明目的,不应被解释为限制本发明。calb(南极假丝酵母(candida antarctica)脂肪酶b)是可用于本发明的酯酶的实例。
具体实施方式
36.定义
37.生物柴油-术语生物柴油用于指短链醇的脂肪酸烷基酯(faae),例如脂肪酸甲酯(fame)和/或脂肪酸乙酯(faee),因为它们被用作化石燃料的添加剂或替代品。
38.短链醇-术语短链醇(sca)用于指具有1个至5个碳原子的醇。
39.脂肪酸原料-术语“脂肪酸原料”在本文中定义为包含任何脂肪酸来源的底物,包括甲酯、乙酯、甘油三酯、甘油二酯、甘油单酯或其任何组合。原则上,任何包含脂肪酸的植物或动物来源的油和脂肪可在本发明的方法中用作生产脂肪酸烷基酯的底物。
40.根据本发明使用的脂肪酸原料可以包含以下中的一种或多种或由以下中的一种或多种组成:海藻油;低芥酸菜籽油;椰子油;蓖麻油;椰子油;椰子核油;玉米油;酒糟玉米油;棉花籽油;亚麻油;鱼油;葡萄籽油;大麻油;麻疯果油;荷荷芭油;芥菜油;低芥酸菜籽油;棕榈油;棕榈硬脂;棕榈油精;棕榈仁油;花生油;菜籽油;米糠油;红花油;大豆油;向日葵油;妥尔油;来自盐生植物的油;和/或动物脂肪,包括来自猪、牛和羊的油脂,猪油,鸡脂肪;鱼油;棕榈油游离脂肪酸馏出物;豆油游离脂肪酸馏出物;皂原料脂肪酸材料;黄色油脂;和棕色油脂或其任何组合。
41.术语脂肪酸原料在本文中可与术语生物柴油原料互换使用。
42.方法概述
43.在根据本发明的方法的第一步,即步骤a中,提供了一种包含游离脂肪酸的组合物。该组合物表示为i)。
44.在第二步,即步骤b中,将甘油ii)、酯酶iii)和短链醇(例如甲醇和/或乙醇)iii)添加到组合物i)中并混合。
45.步骤a和步骤b的顺序不重要;即组分i)至iv)能以任何顺序提供并以任何顺序混合。例如,i)可以是生物柴油原料(本文其他地方定义),并且组分ii)-iv)可以添加到其中提供生物柴油原料的罐中,并且将所有组分混合。
46.本发明的方法可被视为生物柴油原料向生物柴油的两步式酶促转化中的第二步,其中第一步是通过脂肪酶(例如疏棉状嗜热丝孢菌(thermomyces lanuginosus)脂肪酶)进行酶促酯交换,并且第二步是通过酯酶(例如calb)将游离脂肪酸酯化为生物柴油。在这种情况下,组合物i)可以是来自酶促酯交换的混合物的轻相。
47.替代性地,组合物i)可以是来自酯交换反应的完全反应混合物,然后将其干燥以推动酯化方法。
48.然后将混合物在酶反应器中培养。酶反应器可以是适于酶培养的任何容器,并且对用于培养的参数进行选择以促进酶反应。本领域技术人员知道这些参数,并且能够选择例如温度、混合、以及容器来支持该酶反应。
49.将培养后的酶反应混合物,即包含酶反应产物和步骤b中提供并混合在一起的残留组分的混合物进行闪蒸干燥。
50.本发明基于以下令人惊讶的认识:即使在温和条件下,酶反应混合物也会在闪蒸干燥器中干燥。步骤d的闪蒸干燥在这些温和条件下进行。
51.经闪蒸干燥的酶反应混合物将含有从步骤b的初始添加中残留的酯酶,并且该酶将保留至少部分活性。由于混合物也已经除去了水,并且该混合物可以在酶反应器中进行第二次培养(步骤f),以进一步降低游离脂肪酸含量。为了使该反应进行,可以通过步骤e补充短链醇含量,步骤e是在闪蒸干燥器步骤d之后和第二次酶培养步骤f之前,向经干燥的酶
反应混合物中添加短链醇v)。
52.在步骤g中分离第二次酶培养后的酶反应混合物,这通常通过倾析来进行,并产生轻相(vi)和重相(vii)。
53.轻相含有fame,即生物柴油。它可以通过一步式闪蒸干燥步骤(即在通常用于干燥生物柴油的温度和条件下的常规闪蒸干燥)来干燥。
54.步骤h中获得的组合物是组合物viii),fame产物(即生物柴油)。
55.重相包含甘油、酯酶和短链醇。由于步骤d中使用的温和闪蒸干燥条件,酯酶仍将保留活性。此外,甘油和短链醇也是将游离脂肪酸反应为生物柴油所需的组分。
56.因此,在该方法中,重相可以全部或部分循环使用。在该方法中重相可以送回到步骤b中,该步骤中将甘油、酯酶和短链醇添加到组合物i)中并混合。步骤b的组分可以全部或部分地来源于重相。在一些实施例中,可以通过添加新鲜甘油、短链醇和/或酯酶来补充循环使用的重相。
57.下面将详细描述该方法和另外的实施例。
58.关于本发明的一个实施例的概述,也参见图1。
59.因此,本发明一方面涉及一种游离脂肪酸的酶促酯化方法,该方法包括以下步骤:
60.a.提供包含游离脂肪酸的组合物i),
61.b.向步骤a中提供的组合物中添加:
62.ii)酯酶,
63.iii)甘油,和
64.iv)短链醇
65.并且混合
66.c.培养步骤b的混合物,使得该酯酶催化游离脂肪酸的酯化,
67.d.对从步骤c得到的经培养的混合物进行闪蒸干燥,
68.e.将步骤d中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合
69.f.培养步骤e中获得的混合物,由此,步骤b中提供的酯酶ii)催化游离脂肪酸的酯化。
70.1.1步骤a-提供包含游离脂肪酸的组合物i)
71.在步骤a中提供的包含游离脂肪酸的组合物(称为i),也参见图1中的流程图)是使用本方法生产fame的起始材料。
72.因此,在一些实施例中,组合物i)包含在0.25至10wt%,如1至8wt%、1至7wt%、1至5wt%或1至4wt%,或例如1至6wt%,如2至6wt%、或2至4wt%范围内的量的脂肪酸。
73.一些实施例涉及根据本发明的方法,其中在步骤a中提供的组合物i)是生物柴油原料。
74.一些生物柴油原料具有高水平的游离脂肪酸。例如,来自棕榈或大豆的脂肪酸馏出物、酸性油、动物脂肪或可含有10%-90%ffa的类似原料。这些原料通常用硫酸或树脂作为催化剂进行酯化,以制备用于与例如甲醇钠进行碱催化的酯交换反应。
75.因此,另外的实施例涉及其中组合物i)包含大于10wt%的量的游离脂肪酸;例如在10-90wt%范围内,如10至85wt%、10至80wt%、10至75wt%、10至70wt%、10至65wt%、10至60wt%、10至55wt%、10至50wt%、10至45wt%、10至40wt%、10至35wt%、10至30wt%、10
至25wt%、10至20wt%、10至15wt%范围内的游离脂肪酸;或例如10至85wt%、15至80wt%、20至75wt%、20至65wt%或20至55wt%的游离脂肪酸。
76.生物柴油原料可以是例如植物油、动物脂肪或微生物油或其组合。因此,生物柴油原料可选自由以下组成的组:蓖麻油、棉花籽油、玉米油、棕榈油、花生油、菜籽油、米糠油、大豆油、鱼油、油脂、猪油、羊油、酵母油、微生物油、脂肪酸馏出物及其组合。
77.一些实施例涉及根据本发明的方法,其中步骤a中提供的包含脂肪酸的组合物(i)为反应混合物,其中生物柴油原料已与脂肪酶反应以产生脂肪酸烷基酯,特别是直到反应基本达到平衡为止。
78.术语“平衡”在这里可以定义为反应混合物中游离脂肪酸没有进一步净减少的点,或者例如ffa的减少小到无法使反应在酯交换容器中继续进行。
79.因此,i)中的组合物可以特别是来自酯交换反应的反应产物,该反应已经被允许进行到游离脂肪酸没有进一步净减少或基本没有进一步净减少的点。
80.在一些实施例中,组合物i)是生物柴油原料,已对其进行处理使其与脂肪酶培养并酯交换,如在例如wo 2017060471中所描述。在酶促酯交换之后,将重相倾析,然后进行根据本发明的逐步酯化方法。参见讨论和图2。
81.因此,一个实施例涉及根据本发明的方法,其中在步骤a中提供的包含游离脂肪酸的组合物i)通过包括以下步骤的方法生产:
82.a.1-提供生物柴油原料
83.a.2-通过脂肪酶将甘油酯和游离脂肪酸酶促酯交换为脂肪酸甲酯
84.a.3-分离轻相与重相
85.由此组合物i)包含步骤a.3中获得的轻相或由其组成。
86.用于获得组合物i)的步骤a.2的脂肪酶可以选自由以下组成的组:南极假丝酵母脂肪酶a(如wo 88/02775中所披露),疏棉状嗜热丝孢菌脂肪酶、疏棉状嗜热丝孢菌(以前称为疏棉状腐质霉)脂肪酶变体(wo 00/60063中列出),特异腐质霉角质酶变体(wo 01/92502的实例2披露),来自疏棉状腐质霉(ep 258 068)、皱落假丝酵母(candida rugosa)、洋葱假单胞菌(pseudomonas cepacia)、白地霉(geotricum candidum)、米黑根毛霉(rhizomucor miehei)、隐球酵母属(crytococcus)物种s-2、近平滑假丝酵母(candida parapsilosis)的脂肪酶,eversa transform(诺维信公司(novozymes a/s))和callera trans(诺维信公司)。
87.在特定实施例中,步骤a.2的脂肪酶选自由以下组成的组:疏棉状嗜热丝孢菌脂肪酶和疏棉状嗜热丝孢菌(以前称为疏棉状腐质霉)脂肪酶变体(wo 00/60063中列出)。
88.在特定实施例中,步骤a.2的脂肪酶选自由以下组成的组:eversa transform和callera trans。
89.图2示出了酯交换、随后是逐步酯化和闪蒸的系统。
90.在酯交换之后,富含水的组分可以被混合并闪蒸,以在反应之前降低水浓度。
91.因此,一个实施例涉及根据本发明的方法,其中在步骤a中提供的包含游离脂肪酸的组合物i)通过包括以下步骤的方法生产:
92.a.1-提供生物柴油原料
93.a.2-通过脂肪酶将甘油酯和游离脂肪酸酶促酯交换为脂肪酸甲酯
94.a.3-分离轻相与重相
95.a.4-干燥(例如闪蒸干燥)轻相
96.由此组合物i)包含步骤a.4中获得的重相或由其组成。
97.如所讨论的,根据本发明的方法的一个优点是可以使用低质量和/或不同质量的生物柴油原料。因此,在一个实施例中,包含游离脂肪酸的组合物i)或步骤a.1中提供的生物柴油原料可以是低质量的生物柴油原料,如一种或多种用过的烹饪油、油和脂精炼废料、地沟油、酸化油、棕色油脂、淤渣油如淤渣棕榈油、脂肪酸馏出物等,或其组合。
98.1.2步骤b-混合
99.步骤a中提供的组合物与酯酶ii)甘油iii)和短链醇iv)混合。组分ii)-iv)是在步骤c中进行酯化反应所需要的。
100.混合可以通过任何合适的方式进行,该方式的选择在本领域技术人员的范围内。
101.1.2.1 ii)酯酶
102.步骤b中提供的酯酶ii)是一种或多种酯酶,例如根据酶命名法分类为ec 3.1.1羧酸酯水解酶(国际生物化学和分子生物学联合会命名委员会的建议,1992年或以后)的一种或多种酶。
103.一些实施例涉及根据本发明的方法,其中酯酶ii)选自由以下组成的组:
104.(a)多肽,其包含以下的序列或由以下的序列组成:南极假丝酵母(candida antarctica)脂肪酶b(如wo 88/02775中所披露和wo 2008065060的seq id no:1中所示)、酵母样丝孢菌属(hyphozyma)物种脂肪酶(wo 98/018912)、近平滑假丝酵母脂肪酶或其组合。
105.(b)多肽,其是(a)中阐述的氨基酸序列的子序列;
106.(c)多肽,其与(a)和(b)中定义的多肽中的任一个具有至少60%序列同一性,例如至少65%、至少70%、至少75%、至少80%,至少85%,至少90%,至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%和至少99%。
107.特别地,酯酶ii)可以是与成熟多肽具有至少60%序列同一性的酯酶,例如与来自南极假丝酵母(calb)(如wo 88/02775中所披露)的脂肪酶b多肽具有至少65%、至少70%、至少75%、至少80%、至少85%、至少90%、至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%、至少99%、或甚至100%序列同一性的酯酶。
108.在本发明的方法的优选实施例中,本发明的酯酶ii)是来自南极假丝酵母(calb)(如wo 88/02775中所披露)的脂肪酶b。
109.出于本发明的目的,同一性的程度可以根据needleman,s.b.和wunsch,cd.,(1970),journal of molecular biology[分子生物学杂志],48,443-45中所描述的方法来适当地确定,多肽序列比较的设置如下:gap创建罚分为3.0,gap延伸罚分为0.1。可通过已知的计算机程序,如gcg程序包中提供的gap(威斯康星包程序手册(program manual for the wisconsin package),第8版,1994年8月,美国威斯康星州麦迪逊575科学大道(science drive)遗传学计算机组(genetics computer group),53711)进行测定。两个给定的序列可以根据needleman(见上文)中描述的方法使用相同参数进行比对。这可以通过gap程序(见上文)来进行。
[0110]
适用于本发明的方法的步骤b的商业酯酶制剂包括可从诺维信公司获得的
lipozyme calb l和ns88007。
[0111]
calb在低水浓度下也保留活性。
[0112]
因此,一个实施例涉及根据本发明的方法,其中酯酶是在低水活度下具有活性的酯酶;或者换句话说,在低水浓度下显示出与calb相似的活性,如通过对比研究所确定的,如在calb活性的60%至100%范围内,例如70%至100%、75%至100%、80%至100%、85%至100%、90%至100%、95%至100%。
[0113]
因此,一个实施例涉及根据本发明的方法,其中如通过比较研究所确定的,酯酶在500ppm水下显示的酯化速率是在500ppm水下calb活性的60%至100%范围内,例如70%至100%、75%至100%、80%至100%、85%至100%、90%至100%、95%至100%。
[0114]
calb的活性可以确定为酯化速率,参见材料与方法以及实例3。
[0115]
与calb的序列同一性可以被认为是在低水浓度下相似活性的指示。
[0116]
特定实施例涉及根据本发明的方法,其中酯酶ii)是calb。
[0117]
在一个实施例中,本发明涉及酯酶ii)的用途,该酯酶是例如在低水浓度下显示出与calb相似的活性(如通过对比研究所确定的,如在calb稳定性的60%至100%范围内,例如70%至100%、75%至100%、80%至100%、85%至100%、90%至100%、95%至100%)的酯酶。
[0118]
在另一实施例中,本发明涉及calb在根据本发明的方法中的用途。
[0119]
本发明在第二方面涉及酯酶ii)在根据本发明的方法中的用途。
[0120]
该第二方面的一个实施例涉及calb在根据本发明的方法中的用途。
[0121]
在本发明的第一方面的上下文中提出的考虑和实施例也适用于本发明的第二方面(参照)。
[0122]
所添加的酯酶的量可以在基于组合物i)的重量的0.05至8wt%范围内,例如在基于组合物i)的0.05至7wt%、0.05至6wt%、0.05至5wt%、0.05至5wt%、0.05至4wt%、0.05至3wt%、0.05至2wt%、0.05至1.5wt%的范围内。
[0123]
酯酶配制品
[0124]
本文所用的术语“酯酶”是指催化ffa酯化为脂肪酸甲酯的酶。
[0125]
酯酶ii)能以任何合适的配制品(例如冻干粉末、固定化的或在水溶液/液体溶液中)提供。在一个实施例中,酯酶以干燥配制品(例如喷雾干燥的或颗粒化的)提供。如果酯酶以干燥配制品提供,则将酯酶溶解/悬浮在水溶液/液体溶液中,使得培养(步骤c)发生在液体中。
[0126]
在另一实施例中,酯酶以液体配制品提供。也就是说,酯酶不是固定在载体上,而是存在于水性配制品中。这代表了成本节约,因为液体配制品酶更容易生产,因此更便宜。
[0127]
固定化酶(例如novozym 435)与固体颗粒结合,便于从反应混合物中回收并能够在方法中重复使用。然而,固定化酶的回收和重复使用需要额外的方法步骤,例如过滤。此外,小颗粒可能会对仪器造成污染或损坏,从而降低方法的盈利能力。
[0128]
此外,由于进行固定化,固定化酶本身的成本更高。
[0129]
本发明提供了一种令人惊讶的重复使用液体配制品酶的方法,从而降低了成本/提高了使用液体配制品酶的方法效率。
[0130]
虽然在液体配制品中使用酯酶具有优点,但是如果需要,可以使用固定化酯酶。
[0131]
一个特定实施例涉及根据本发明的方法,其中酯酶iii)包含液体配制品中的calb或由其组成。
[0132]
提供呈液体的酯酶具有将水引入系统的缺点(这将使平衡偏离生物柴油生产方向)。然而,本发明人令人惊讶地发现,甘油引起平衡向ffa转化增加的方向显著偏移,从而减轻了水引入的影响(参见实例2)。
[0133]
此外,通过分离其中酶所在的甘油重相,可对酶进行回收,参见1.10分离。
[0134]
1.2.2 iii)-甘油
[0135]
在步骤b中添加甘油iii)并混合。
[0136]
在酯化反应中产生甘油。添加甘油可以在有利于生产生物柴油的方向上推动酯化反应,这是在本发明的方法中添加甘油的原因。
[0137]
选择要在步骤b中添加的甘油(如干燥程度等)在本领域技术人员的范围内。
[0138]
不希望受理论的束缚,据信甘油重相随后充当酶载体,并降低水活度,并且calb在甘油和fame之间的相界线或界面起作用。
[0139]
此外,正如将要介绍的,通过分离其中酶所在的甘油重相,发现酶是可回收的。这可以通过倾析来完成。
[0140]
特定实施例涉及根据本发明的方法,其中在步骤b中,甘油iii)的添加量在基于组合物i)的3至12wt%,如3至11wt%、例如3至10wt%、如3至9wt%、例如3至8wt%、如3至7wt%、例如3至6wt%;或例如4至9wt%,如4至8wt%,例如4至6wt%的范围内,如约5wt%。
[0141]
1.2.3 iv)短链醇
[0142]
本文使用的术语短链醇意指甲醇、乙醇、丙醇或丁醇中的一种或多种。
[0143]
可用作生物柴油的主要短链脂肪酸酯是脂肪酸甲酯(fame)和脂肪酸乙酯(faee)。
[0144]
因此,在特定实施例中,本发明涉及根据本发明的方法,其中步骤b的一种或多种短链醇iv)是甲醇和/或乙醇,优选甲醇。
[0145]
在一些实施例中涉及根据本发明的方法,其中在步骤b中,短链醇iv)(例如甲醇和/或乙醇,特别是甲醇)的添加量在基于组合物i)的2至12wt%,如3至11wt%、例如3至10wt%、如3至9wt%、例如3至8wt%、如3至7wt%、例如3至6wt%;或例如4至9wt%,如4至8wt%,例如4至7wt%的范围内。
[0146]
1.3 步骤c-培养
[0147]
本发明的方法包括步骤c:培养步骤b的混合物,使得该酯酶催化游离脂肪酸的酯化。
[0148]
选择适合于步骤c的培养的条件对于本领域技术人员而言是清楚的。参数可取决于例如所选择的一种或多种酶及其温度敏感性、生物柴油原料在起始点的质量和最终产物的所需质量。
[0149]
一些实施例涉及根据本发明的方法,其中所述培养在30℃至60℃,例如30℃至55℃,如45℃至55℃、50℃至55℃的温度范围内;或例如在30℃至65℃、或30℃至50℃、或40℃-50℃的温度范围内。
[0150]
一些实施例涉及根据本发明的方法,其中所述培养持续足以确保游离脂肪酸减少至少20%,如至少30%、至少40%、至少50%、至少60%或至少75%的时间段。
[0151]
一些实施例涉及根据本发明的方法,其中所述培养持续在2至24小时范围内,例如
2至24小时、5至24小时、6至24小时、10至24小时范围内的时间段。
[0152]
1.4 步骤d-闪蒸干燥
[0153]
本发明的方法包括步骤d:对从步骤c得到的经培养的混合物进行闪蒸干燥。
[0154]
如前所提及的,酯化反应产生水,并且一定水平的水的存在阻碍反应在生产生物柴油的方向上进一步进行。除去水将使平衡偏移并有利于生物柴油的进一步生产。
[0155]
因此,希望从反应产物混合物(由步骤c得到的经培养的混合物)中除去水。
[0156]
令人惊讶的是,已经发现含有来自脂肪酶处理生物柴油原料的反应产物、甘油、水和液体配制的脂肪酶的总反应混合物可以在闪蒸系统中干燥,以提供足够低的含水量以达到ffa的高酯化程度。
[0157]
基于生物柴油反应的重相和轻相的沸点差异,闪蒸干燥是用于干燥生物柴油的常规技术。
[0158]
选择闪蒸干燥的条件,使得酯酶ii)可以重复使用。
[0159]
换句话说,选择闪蒸干燥的条件,使得酯酶ii)保留至少部分活性。可以选择闪蒸干燥的条件,使得酯酶ii)不完全变性和/或不完全失活。
[0160]
在本发明的一些实施例中,步骤d的所述闪蒸干燥在如下温度范围内进行:40℃至75℃,例如45℃至75℃、50℃至75℃、55℃至75℃;或例如40℃至65℃、40℃至60℃、40℃至55℃或40℃至50℃;
[0161]
在本发明的特定实施例中,步骤d的所述闪蒸干燥在45℃至70℃、45℃至65℃、50℃至60℃的温度范围内进行。
[0162]
很难确定闪蒸干燥室内的温度,因此可以在入口点测量温度。
[0163]
因此,本发明的一些实施例涉及其中步骤d的闪蒸干燥在如上所提及的温度范围内进行,其中在入口点测量温度。
[0164]
一些实施例涉及根据本发明的方法,其中步骤d的所述闪蒸干燥在如下压力范围内进行:小于250毫巴,如小于200毫巴、或小于150毫巴;或例如80毫巴至250毫巴,如100毫巴至220毫巴,例如100毫巴至200毫巴,如120毫巴至180毫巴,如约150毫巴。
[0165]
闪蒸干燥的条件取决于所选择的温度、压力和时间。因此,一些实施例涉及根据本发明的方法,其中步骤d的所述闪蒸干燥在80至250毫巴的压力范围和40℃至75℃的温度范围内进行;例如在80至220毫巴的压力范围和45℃至70℃的温度范围内进行;如在80至200毫巴的压力范围和45℃至70℃的温度范围内进行;例如在100至200毫巴的压力范围和45℃至65℃的温度范围内进行;如在100至200毫巴的压力范围和50℃至60℃的温度范围内进行。
[0166]
在一些实施例中,闪蒸干燥在100至200毫巴的压力范围和50℃至60℃的温度范围内进行;例如在140至160毫巴的压力范围和50℃至60℃的温度范围内进行;如在约150毫巴的压力和约55℃的温度下进行。
[0167]
在一些实施例中,步骤a中的酯酶ii)是南极假丝酵母脂肪酶b(calb),并且闪蒸干燥在100至200毫巴的压力范围和50℃至60℃的温度范围内进行;例如在140至160毫巴的压力范围和50℃至60℃的温度范围内进行;如在约150毫巴的压力和约55℃的温度下进行。
[0168]
一些实施例涉及根据本发明的方法,其中步骤d的所述闪蒸干燥在如下时间范围内进行:1至100分钟(min),如1至60分钟,例如1至25分钟,如1至20分钟;或例如5至50分钟,
如5至20分钟;或例如10至20分钟。
[0169]
在一些实施例中,闪蒸干燥在100至200毫巴的压力范围、50℃至60℃的温度范围和1至60分钟的时间范围内进行;或例如在140至160毫巴的压力范围、50℃至60℃的温度范围和1至25分钟的时间范围内进行;或例如在约150毫巴的压力、约55℃的温度和约15分钟的时间范围内进行。
[0170]
特别地,在一些实施例中,步骤a中的酯酶ii)是南极假丝酵母脂肪酶b(calb),并且闪蒸干燥在100至200毫巴的压力范围、50℃至60℃的温度范围和1至60分钟的时间范围内进行;或例如在140至160毫巴的压力范围、50℃至60℃的温度范围和1至25分钟的时间范围内进行;或例如在约150毫巴的压力、约55℃的温度和约15分钟的时间范围内进行。
[0171]
步骤d的闪蒸干燥导致水的量减少,这对如上所提及的反应是有利的。
[0172]
因此,一些实施例涉及根据本发明的方法,其中在步骤d中获得的经闪蒸干燥的混合物的含水量在如下范围内:0-700ppm,如50-600ppm、50至500ppm、50至400ppm、50至300ppm;或例如55至500ppm,如60至600ppm、70至600ppm、100至600ppm、200至600ppm。
[0173]
在一些实施例中,闪蒸干燥在100至200毫巴的压力范围、50℃至60℃的温度范围、1至60分钟的时间范围内进行,并且在步骤d中获得的经闪蒸干燥的混合物的含水量在50至600ppm范围内;或例如在140至160毫巴的压力范围、50℃至60℃的温度范围、1至25分钟的时间范围内进行,并且在步骤d中获得的经闪蒸干燥的混合物的含水量在50至500ppm范围内;或例如在约150毫巴的压力、约55℃的温度、约15分钟的时间范围内进行,并且在步骤d中获得的经闪蒸干燥的混合物的含水量在50至400ppm范围内。
[0174]
在特定实施例中,步骤a中的酯酶ii)是南极假丝酵母脂肪酶b(calb),并且闪蒸干燥在100至200毫巴的压力范围、50℃至60℃的温度范围、1至60分钟的时间范围内进行,并且在步骤d中获得的经闪蒸干燥的混合物的含水量在50至600ppm范围内;或例如在140至160毫巴的压力范围、50℃至60℃的温度范围、1至25分钟的时间范围内进行,并且在步骤d中获得的经闪蒸干燥的混合物的含水量在50至500ppm范围内;或例如在约150毫巴的压力、约55℃的温度、约15分钟的时间范围内进行,并且在步骤d中获得的经闪蒸干燥的混合物的含水量在50至400ppm范围内。
[0175]
根据本发明的方法涉及闪蒸干燥方法,其中该闪蒸干燥在不使酯酶变性的条件下进行。换句话说,酯酶ii)在步骤d的闪蒸干燥后保留至少部分活性,例如酯酶ii)保留其活性的至少40%。
[0176]
因此,本发明涉及根据本发明的方法,其中步骤d是:
[0177]
d.对从步骤c得到的经培养的混合物进行闪蒸干燥,
[0178]
其中该闪蒸干燥在使得经闪蒸干燥的酯酶ii)保留其活性的至少40%的条件下进行;
[0179]
因此,一些实施例涉及根据本发明的方法,其中经闪蒸干燥的酯酶ii)保留其活性的至少40%,例如至少50%,如至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%。
[0180]
根据权利要求1所述的方法,其中步骤d的闪蒸干燥在如下条件下进行,这些条件使得经闪蒸干燥的酯酶ii)保留其活性的至少40%,例如至少50%,如至少55%、至少60%、至少65%、至少70%、至少75%、至少80%、至少85%、至少90%。
[0181]
保留的活性量可以通过测定闪蒸干燥前酶的酯化速率并将其与闪蒸干燥后酶的酯化速率进行比较来确定。酯化速率可以通过在材料与方法和实例3中描述的方法确定。
[0182]
闪蒸干燥领域的技术人员将认识到,干燥效率可以例如以以下两种方式提高:1)让第二闪蒸干燥器在第一闪蒸干燥器之后立即运行,2)从干燥器建立一个回路,重新循环一部分闪蒸出口气流,并将其混合到入口气流中,使出口气流重新循环例如60%。
[0183]
因此,一些实施例涉及根据本发明的方法,其中步骤d的闪蒸干燥后立即进行第二闪蒸干燥。
[0184]
本发明的另外的特定实施例涉及一种游离脂肪酸的酶促酯化方法,该方法包括以下步骤:
[0185]
a.提供包含游离脂肪酸的组合物i),
[0186]
b.向步骤a中提供的组合物中添加:
[0187]
ii)酯酶,
[0188]
iii)甘油,和
[0189]
iv)短链醇
[0190]
并且混合
[0191]
c.培养步骤b的混合物,使得该酯酶催化游离脂肪酸的酯化,
[0192]
d.对从步骤c得到的经培养的混合物进行闪蒸干燥,任选地立即进行一个或多个另外的闪蒸干燥步骤,
[0193]
e.将步骤d中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合
[0194]
f.培养步骤e中获得的混合物,由此,步骤b中提供的酯酶ii)催化游离脂肪酸的酯化。
[0195]
另外的特定实施例涉及根据本发明的发明,步骤d:对从步骤c得到的经培养的混合物进行闪蒸干燥,任选地立即进行一个或多个另外的闪蒸干燥,例如至少一个另外的闪蒸干燥,例如一个另外的闪蒸干燥,例如2、3、4个另外的闪蒸干燥。步骤d中的另外的闪蒸干燥按照上文标题1.4所描述进行。
[0196]
本发明的优点之一在于可以对反应混合物进行闪蒸干燥步骤,而不需要分离。
[0197]
因此,特定实施例涉及根据本发明的方法,其中来自步骤c的混合物在步骤d的闪蒸干燥步骤之前没有被分离。这里的分离意指轻相与重相的分离。
[0198]
1.5 步骤e和f-与另外的短链醇混合
[0199]
根据本发明的闪蒸干燥既提供了允许酯化反应进一步继续的条件(即降低含水量),又保留了酶的活性并因此能够被重复使用。
[0200]
酯酶的这种重复使用导致盈利能力显著提高。此外,在根据本发明的方法中,酯酶的重复使用采用简单的设置,避免了与例如固定化酶的回收和重复使用相关的问题(例如污染)。
[0201]
因此,本发明的方法包括:步骤e,将步骤d中获得的经闪蒸干燥的混合物与另外的短链醇(例如甲醇和/或乙醇,特别是甲醇)任选地混合,和步骤f,培养步骤e中获得的混合物,由此,步骤b中提供的酯酶ii)催化游离脂肪酸的酯化。
[0202]
在不添加另外的短链醇并混合的情况下,步骤f涉及培养步骤d中获得的混合物。
[0203]
因此,特定实施例涉及根据本发明的方法,其中在步骤f或f.n中获得的组合物的
游离脂肪酸含量小于5wt%,例如小于3wt%、小于0.5wt%或小于0.25wt%;例如在0.02wt%至5wt%,例如0.02wt%至3wt%,如0.02wt%至2wt%、0.02wt%至1wt%的范围内。
[0204]
短链醇的添加量与步骤b中所描述的量相同。
[0205]
对经闪蒸干燥的混合物中存在的酯酶的这种重复使用是本发明使酶的循环使用成为可能的一个水平。
[0206]
1.6 r1闪蒸干燥回路
[0207]
尽管如步骤d所描述已经进行了中间闪蒸干燥,反应混合物中存在的酯酶仍保留了活性,因此可以重复使用几次。
[0208]
因此,一个实施例涉及根据本发明的方法,其中酯酶在1次至10次,例如1次至8次如1次至6次、或例如1次至5次范围内重复使用。
[0209]
酯酶的重复使用也可以按照如下方式进行描述:可以根据需要重复如步骤d中所描述的闪蒸干燥步骤,从而有效地在方法中插入快速干燥回路(参见图1,r1)。这意味着,可以按照步骤d中所描述的对步骤f中获得的酶反应混合物进行另外的闪蒸干燥步骤d.1,然后任选地进行按照步骤e中所描述的添加另外的短链醇v)的步骤e.1,以及按照步骤f中所描述的进行步骤f.1。
[0210]
因此,在一个实施例中,根据本发明的方法进一步包括以下步骤
[0211]
d.1-对从步骤f得到的经培养的混合物进行闪蒸干燥,
[0212]
e.1-将步骤d.1中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合,以及
[0213]
f.1-培养步骤e.1中获得的混合物,由此,步骤b中提供的酯酶ii)催化游离脂肪酸的酯化。
[0214]
在另一实施例中,根据本发明的方法进一步包括以下步骤
[0215]
d.1-对从步骤f得到的经培养的混合物进行闪蒸干燥,其中该闪蒸干燥在使得经闪蒸干燥的酯酶ii)保留至少40%其活性的条件下进行
[0216]
e.1-将步骤d.1中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合,以及
[0217]
f.1-培养步骤e.1中获得的混合物,由此,步骤b中提供的酯酶ii)催化游离脂肪酸的酯化。
[0218]
可以理解,该闪蒸干燥回路包括步骤d.n、e.n和f.n,其中n表示酶被重复使用的次数,并且可以根据需要进行多次。对步骤f.(n-1)得到的经培养的混合物进行d.n的闪蒸干燥步骤。步骤d.n、e.n和f.n分别按照步骤d、e和f所描述的方式进行(参见相应标题说明)。
[0219]
在特定实施例中,根据本发明的方法涉及其中n在1至10,如1至9,例如1至8、1至7、1至6或例如1至5的范围内。
[0220]
在特定实施例中,根据本发明的发明进一步包括步骤d.1、e.1、f.1;然后是步骤d.2、e.2和f.2;d.3、e.3、f.3、d.4、e.4、f.4和d.5、e.5和f.5。
[0221]
在特定实施例中,根据本发明的发明进一步包括步骤d.1、e.1、f.1;然后是步骤d.2、e.2和f.2;d.3、e.3、f.3和d.4、e.4、f.4。
[0222]
在特定实施例中,根据本发明的发明进一步包括步骤d.1、e.1、f.1;然后是步骤
d.2、e.2和f.2;和d.3,e.3,f.3。
[0223]
图7(闪蒸步骤反应)的反应结果表明,仅需要2个酯化步骤。因此,在特定实施例中,根据本发明的发明进一步包括步骤d.1、e.1、f.1;然后是步骤d.2、e.2和f.2。
[0224]
特定实施例涉及根据本发明的发明,其包括以下步骤:
[0225]
a.提供包含游离脂肪酸的组合物i),
[0226]
b.向步骤a中提供的组合物中添加:
[0227]
ii)酯酶,
[0228]
iii)甘油,和
[0229]
iv)短链醇
[0230]
并且混合
[0231]
c.培养步骤b的混合物,使得该酯酶催化游离脂肪酸的酯化,
[0232]
d.对从步骤c得到的经培养的混合物进行闪蒸干燥,
[0233]
e.将步骤d中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合
[0234]
f.培养步骤e中获得的混合物,由此,步骤b中提供的酯酶ii)催化游离脂肪酸的酯化,
[0235]
d.1-对从步骤f得到的经培养的混合物进行闪蒸干燥,其中该闪蒸干燥在不使该酯酶变性的条件下进行
[0236]
e.1-将步骤d.1中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合,以及
[0237]
f.1-培养步骤e.1中获得的混合物,由此,步骤b中提供的酯酶ii)催化游离脂肪酸的酯化;
[0238]
d.2-对从步骤f.1得到的经培养的混合物进行闪蒸干燥,其中该闪蒸干燥在不使该酯酶变性的条件下进行
[0239]
e.2-将步骤d.2中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合,以及
[0240]
f.2-培养步骤e.2中获得的混合物,由此,步骤b中提供的酯酶ii)催化游离脂肪酸的酯化,
[0241]
g.将步骤f.2中获得的混合物分离成
[0242]
vi)轻相,其包含脂肪酸甲酯,和
[0243]
vii)重相,其包含酯酶、甘油和短链醇。
[0244]
h.对通过步骤g的分离获得的轻相(vii)进行干燥。
[0245]
i,其中来自步骤g的重相(vii)被循环使用并添加回该方法的步骤b中,从而补充ii)酯酶、iii)甘油和iv)短链醇中的一种或多种。
[0246]
另外的特定实施例涉及根据本发明的发明,其包括以下步骤:
[0247]
a.提供包含游离脂肪酸的组合物i),
[0248]
其中所述组合物i)通过包括以下步骤的方法制备:
[0249]
a.1-提供生物柴油原料
[0250]
a.2-通过脂肪酶将甘油酯和游离脂肪酸酶促酯交换为脂肪酸甲酯
[0251]
a.3-分离轻相与重相,
[0252]
由此组合物i)包含步骤a.3中获得的轻相或由其组成
[0253]
b.向步骤a中提供的组合物中添加:
[0254]
ii)酯酶,
[0255]
iii)甘油,和
[0256]
iv)短链醇
[0257]
并且混合
[0258]
c.培养步骤b的混合物,使得该酯酶催化游离脂肪酸的酯化,
[0259]
d.对从步骤c得到的经培养的混合物进行闪蒸干燥,
[0260]
e.将步骤d中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合
[0261]
f.培养步骤e中获得的混合物,由此,步骤b中提供的酯酶(ii)催化游离脂肪酸的酯化,
[0262]
d.1-对从步骤f得到的经培养的混合物进行闪蒸干燥,其中该闪蒸干燥在不使该酯酶变性的条件下进行
[0263]
e.1-将步骤d.1中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合,以及
[0264]
f.1-培养步骤e.1中获得的混合物,由此,步骤b中提供的酯酶(ii)催化游离脂肪酸的酯化;
[0265]
d.2-对从步骤f.1得到的经培养的混合物进行闪蒸干燥,其中该闪蒸干燥在不使该酯酶变性的条件下进行
[0266]
e.2-将步骤d.2中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合,以及
[0267]
f.2-培养步骤e.2中获得的混合物,由此,步骤b中提供的酯酶(ii)催化游离脂肪酸的酯化,
[0268]
g.将步骤f.2中获得的混合物分离成
[0269]
vi)轻相,其包含脂肪酸甲酯,和
[0270]
vii)重相,其包含酯酶、甘油和短链醇。
[0271]
h.对通过步骤g的分离获得的轻相(vii)进行干燥。
[0272]
i,其中来自步骤g的重相(vii)被循环使用并添加回该方法的步骤b中,从而补充ii)酯酶、iii)甘油和iv)短链醇中的一种或多种。
[0273]
1.7 步骤g-分离
[0274]
根据本发明的方法可进一步包括分离步骤。因此,本发明的一个实施例涉及根据本发明的方法,该方法进一步包括步骤g,将步骤f中获得的混合物分离成vi)轻相,其包含脂肪酸甲酯和vii)重相,其包含酯酶、甘油和短链醇。
[0275]
在包含步骤f.n(如f1、f.2、f.3、f.4、f.5,参见上文)的实施例中,分离步骤g涉及分离在最终步骤f.n中获得的混合物。
[0276]
该分离步骤能以任何合适的方式进行,例如重力沉降、离心和/或倾析。分离方法的选择在本领域技术人员的范围内。
[0277]
在一个优选实施例中,分离步骤g为倾析。
[0278]
1.8-vii)重(甘油和酯酶)相
[0279]
g的分离步骤得到vii)重相,其包含酯酶、甘油和短链醇。该相中存在的酯酶仍将保留活性,因此可以进一步重复使用。
[0280]
组分甘油和短链醇也用于步骤b中的酯化反应。因此,重相vii)是组分ii)酯酶、iii)甘油和iv)短链醇的来源,并且重相的循环使用可提高方法效率和盈利能力。
[0281]
因此,本发明的一个实施例涉及根据本发明的方法,该方法进一步包括步骤i,其中,来自步骤g的重相vii)被循环使用并添加回该方法的步骤b中,从而补充步骤b中提供的ii)酯酶、iii)甘油和iv)短链醇中的一种或多种(参见图1,由r2表示)。
[0282]
这是本发明的方法可以提供的循环使用的第二水平。
[0283]
1.9-vi)轻(fame或生物柴油)相
[0284]
g的分离步骤得到vi)轻相,其包含生物柴油(fame)。
[0285]
本发明的一些实施例涉及根据本发明的方法,其中,在步骤g中获得的轻相vi)的游离脂肪酸含量小于5wt%、小于3wt%、小于0.5wt%,如小于3wt%、小于0.5wt%或小于0.25wt%;例如在0.02wt%至5wt%,例如0.02wt%至3wt%,如0.02wt%至2wt%、0.02wt%至1wt%的范围内。
[0286]
1.10 一步式闪蒸干燥
[0287]
在一些情况下,可能需要进一步干燥和/或处理在步骤g中获得的轻相vi)。
[0288]
因此,本发明的方法的一个实施例进一步包括步骤h:对通过步骤g的分离获得的轻相vii)进行干燥,例如闪蒸干燥。
[0289]
该进一步的闪蒸干燥步骤在本文中也称为一步式闪蒸干燥,以区别于步骤d和步骤d.n的闪蒸干燥。该一步式闪蒸干燥可在任何适合于达到所需干燥水平并确保短链醇完全蒸发的温度/压力/时间下进行。此时,由于不存在酯酶,无需调整闪蒸干燥的参数,以确保酶活性得到保留。
[0290]
替代性地,可通过任何其他合适的干燥方法实现进一步干燥,该干燥方法的选择在本领域技术人员的范围内。
[0291]
本发明的一些实施例涉及根据本发明的方法,其中,在步骤g中获得的轻相vi)在一步式闪蒸干燥后的游离脂肪酸含量小于5wt%、小于3wt%、小于0.5wt%,如小于3wt%、小于0.5wt%或小于0.25wt%;例如在0.02wt%至5wt%,例如0.02wt%至3wt%,如0.02wt%至2wt%、0.02wt%至1wt%的范围内。
[0292]
1.11 任选的碱洗
[0293]
根据本发明的方法将产生低游离脂肪酸水平的生物柴油。避免碱洗具有优点。当使用碱洗时,可能导致部分fame在分离皂时被截留,从而降低产率。将循环使用的皂酸化,以产生ffa。这种酸化是使用硫酸进行的,这增加了总成本。根据本方法的ffa酯化可以避免这种成本。本方法提高了生产率,并减少了或没有皂循环流,从而减少了废物的产生。
[0294]
因此,一个实施例涉及根据本发明的方法,其中该方法不包括碱洗步骤。
[0295]
然而,在某些情况下,可能需要进一步降低在步骤g中获得的轻相vi)的游离脂肪酸含量。
[0296]
因此,根据本发明的方法的一个实施例进一步包括步骤j,碱洗。
[0297]
碱洗是本领域熟知的方法,并且参数的选择在本领域技术人员的范围内。
[0298]
碱洗步骤也可用于除去硫酸化合物和其他杂质,如甘油酯,并且无论ffa浓度如何
都可能是有用的。
[0299]
1.12 任选的甘油减少
[0300]
重相中甘油的存在可能会使酯交换反应的平衡向形成甘油酯而非fame的方向偏移。我们对此进行了检查,并且发现在不进行干燥的单步反应期间,甘油酯水平略有增加,从b100生物柴油中0.05wt%总甘油增加到平衡时的0.25wt%(反应中甘油负载为5%(fame的w/w))。根据生物柴油规范(欧洲标准),这是精确甘油限值,但主要来源于甘油单酯(从0.24wt%增加到0.61wt%)和甘油(从无限低值(接近零)增加到0.09wt%)的形成。两者均使用qta法进行测量。特别地,在后续的下游处理中,甘油很容易减少,从而使fame在生物柴油规范内。
[0301]
1.13 分批或连续方法
[0302]
此外,本发明涉及生产脂肪酸烷基酯的分批方法和/或连续分阶段方法,其中连续或逐步添加醇,并且其中酶循环使用或仅使用一次。如果酶处于水相中,可以通过倾析器、沉降器或离心将该水相与脂肪相分离。在连续方法中,油相和水相可以逆流(counter-currently)处理。
[0303]
1.14 calb的用途
[0304]
本发明在第二方面涉及calb在根据本发明的方法中的用途。关于本发明前述方面的参数的讨论也适用于本发明的第二方面(参照)。
[0305]
1.15 闪蒸干燥法
[0306]
本发明基于一个令人惊讶的发现,即在使酯酶变性的条件下,可以在闪蒸干燥器中对包含fame、游离脂肪酸、酯酶、甘油、短链醇和水的反应混合物进行干燥(除去其中的水)。这使得酯酶的重复使用成为可能。
[0307]
因此,本发明的第三方面涉及一种用于闪蒸干燥包含游离脂肪酸的混合物的方法,所述混合物包含fame、游离脂肪酸、酯酶、甘油、短链醇和水;并且所述方法包括提供所述混合物和随后闪蒸干燥所述混合物的步骤,其中该闪蒸干燥在不使该酯酶变性的条件下进行。
[0308]
关于本发明前述方面的参数的讨论也适用于本发明的第三方面(参照)。
[0309]
优点
[0310]
本发明提供至少以下优点:
[0311]-反应混合物的重复使用带来的方法经济益处,包括酶的重复使用、甘油的循环使用和/或短链醇的循环使用
[0312]-闪蒸干燥方法使酶反应进一步产生fame,从而增加fame的产率
[0313]-这种改善的经济性反过来导致现在可以考虑以前无法使用的ffa原料。
[0314]
另一个益处是基于常规工程单元操作的简单方法布局,其可以与较低成本的液体脂肪酶配制品一起使用。
[0315]
实例
[0316]
材料与方法
[0317]
酯化反应混合物的规模不同,并且30、300或450g粗fame(b100生物柴油(酸度相当于约0.2wt%ffa),来自添加了油酸的棕榈油,基本上消除了来自ffa以外来源的酸度的显著存在)进行反应。在用于显示甘油、甲醇和酶的显著性的全因子设计结果中,使用了来自
棕榈油的粗棕榈油甲酯(fame)。
[0318]
在150ml方形烧瓶(杜兰公司(duran))中进行30g规模的实验。
[0319]
在离心管(聚碳酸酯,500ml,69x160,贝克曼库尔特生命科学公司(beckman coulter life sciences))中进行300g规模的实验,
[0320]
这两种实验都是在振荡培养箱(new brunswick scientific
tm
innova
tm
44培养摇床)中、在250rpm和40℃下进行的。
[0321]
通常使用5%的甘油负载(粗fame的w/w)。甲醇和酶的负载各不相同,并且本文中负载将以%(粗fame的w/w)表示。
[0322]
将含有粗fame、甘油和甲醇的反应混合物预热至40℃。在t=0时添加酶,并通过1-2ml样品监测反应进程,取出并加热至100℃持续10分钟,然后离心2分钟以分离相。
[0323]
按照正常程序测量酶的热失活,尽管在规定温度下培养15分钟,并进行适当预热和快速冷却,同时在t=0样品之前向10wt%ffa中添加油酸。
[0324]
使用计算为油酸的aocs方法分析样品在fame相中的酸度(aocs,2017a)。根据aocs规范(aocs,2017b),使用欧陆集团(eurofins)质量性状分析(qta)校准服务支持的中红外系统(medium infrared system,布鲁克(bruker)tensor ii)测量甲醇和甘油酯。使用卡尔
·
费歇尔滴定法(具有774烘箱样品处理器的831kf库仑计)测量含水量,并通过组分质量平衡进行计算。
[0325]
闪蒸塔vlle计算是利用pro/ii中的unifac热力学模型(fredenslund等人,1975)进行计算的。
[0326]
材料
[0327]
甘油和甲醇的分析级纯度》99.5%。甘油水浓度≈1000ppm,甲醇水浓度≈200ppm。油酸的工业级纯度》90%,其余主要为其他脂肪酸。使用的酶是calb(ns88007,丹麦巴格斯韦德的诺维信公司(novozymes),含有43.7wt%水)。
[0328]
实例1
[0329]
使用旋转蒸发仪进行模拟闪蒸的实验。这是通过液体酶系统进行的,使用30g粗fame和0.8%(粗fame的w/w)脂肪酶calb l、6%(粗fame的w/w)甲醇和5%(粗fame的w/w)甘油。
[0330]
将30g fame转移到反应瓶中,并与甲醇混合。在添加酶之前,将fame/甲醇混合物预热至40℃。
[0331]
反应在连接到旋转蒸发仪(步琪公司(b
ü
chi)旋转蒸发仪,型号r-124)的2000ml干燥瓶(步琪公司)中进行。混合是通过旋转蒸发仪装置的旋转进行的,转速设定为100rpm。
[0332]
让反应进行20、24和76小时,同时在全真空下(5分钟后为1-4毫巴)闪蒸30分钟。每次闪蒸后,再添加6%(粗fame的w/w)甲醇。将2ml反应混合物样品转移到2ml带安全锁的艾本德(eppendorf)试管中,并在99℃下在加热块(艾本德舒适型恒温混匀器(eppendorf thermommixer comfort),5355 32447,德国艾本德公司)中培养10min,以使酶失活。样品在6000rpm下离心2min(微型离心机(mini centrifuge),c1413v-230,美国vwr国际公司(vwr international)),并在5℃下储存。然后假设样品是稳定的。
[0333]
压力以设定的间隔降低,类似于闪蒸塔。在闪蒸程序期间,温度保持在40℃。结果示于图5中。
[0334]
可见,游离脂肪酸水平降低。
[0335]
实例2:预测平衡ffa(以wt%计)的估计线性模型参数及其统计意义
[0336]
在三个中心点的全析因实验中研究了甘油对平衡的贡献。以30g规模在粗fame上进行反应。fame中的初始ffa浓度为2.9wt%,反应后测量的最小ffa为1.3wt%。总水浓度范围从0.3%(fame的w/w)酶处的1700ppm到0.8%酶处的3600ppm。甘油和甲醇对总水浓度的影响可以忽略不计。
[0337]
表1:参数和结果。
[0338]
甘油wt%甲醇wt%酶wt%ffa eq 1天wt%0,520,32,6330,560,32,11560,31,433520,31,6242,7540,551,9662,7540,551,8762,7540,552,013560,81,7750,560,82,498520,82,3080,520,83,697
[0339]
表2:预测平衡ffa(以wt%计)的估计线性模型参数及其统计意义。负载范围以%(fame的w/w)表示。
[0340]
因子估计p值截距2.686《0.0001甘油(0.5-5[%])-0.2110.0016甘油(2-6[%])-0.1530.0148酶(0.3-0.8[%])1.2390.0140
[0341]
2正如预期的那样,甲醇用量的增加导致ffa向fame的转化提高。对于酶用量,发现平衡时的ffa含量降低,这是由于酶用量越高,添加的水量越大。
[0342]
表2示出了从使用粗fame在30g规模实验中进行研究获得的线性模型。它显示了甘油对平衡时fame相产生的ffa浓度的显著影响。还测试了10%的甘油负载。
[0343]
目前认为甘油通过降低酶在其活性部位的表观水浓度来影响平衡。活性部位及其开口将指向疏水相,并且可能不会遇到亲水甘油相中存在的水。此外,发现甘油对酶的活性很重要,这归因于酶作用的相界面的形成。参见表2,其中甘油和-0.211因子的显著影响表明,较高甘油的ffa较低,范围为0.5%-5%。
[0344]
实例3:酯酶和甘油重复使用
[0345]
检查了酶的可重复使用性。在300g规模的实验中研究了反应速率和达到的平衡ffa浓度,初始约3.2wt%ffa,初始添加1%(fame的w/w)酶、5%甘油。使用通过离心分离的相同甘油相以及随后的fame相倾析,在连续批次的fame上测量反应速率。每批fame添加6%甲醇。结果示于图6
[0346]
尽管观察到活性损失的损失(参见图6),但大部分活性都恢复了。在酯化期间形成水,并且水会在甘油相中积聚,因此第三批的水浓度必然会升高。通过平衡ffa浓度之间的差异间接观察到水的积聚。初始ffa浓度和可达到的平衡之间的相对距离的减小将最终影响速率,并且这解释了所观察到的速率减小的一部分。此外,反应混合物在两批之间在40℃下保持6天,在这两批之间进行额外的批次运行,包括倾析,并且因此有额外的酶损失。总活性损失约为15%,即每批约为7.5%,但基本上可以从上述原因得到解释。因此,结果表明,当在稳定状态下进行工业操作时,酶在使用中具有很高的稳定性,并且具有重复使用和酶回收的潜力,其中每批的酶添加需求较低。
[0347]
实例4:逐步闪蒸/反应方法
[0348]
在高初始水浓度下进行模拟第一步和第二步反应的反应。圆圈:1%脂肪酶calb l,5%甘油,4%甲醇,300g fame,初始水≈5500ppm。三角形:0.455%脂肪酶calb l,5%甘油,6%甲醇,30g fame,初始水≈2000ppm。
[0349]
水的浓度通过平衡控制可获得的ffa浓度降低。利用水和fame之间的沸点差异,可以通过闪蒸除去水。因此,一个逐步反应-闪蒸-反应系统将使平衡向从ffa形成fame的方向偏移。
[0350]
图8的结果显示了不同初始ffa和水浓度下的反应,以及相应的可获得的ffa转化。该图可用于估算所需的反应步骤数。在3.6wt%ffa下开始反应,在0.9wt%ffa下达到平衡,干燥后再次与新的甲醇反应,然后应达到低于0.5wt%ffa的ffa浓度。事实上,这些反应是在相对于通过工业生物柴油闪蒸可获得的水浓度相比较高的水浓度下进行的。通常,在工业规模上,水在反应前由闪蒸控制。此外,如上所述,由于干燥器甘油与酶的循环使用,添加的酶更少,导致酶在稳定状态下积聚,并且添加的水更少,新酶更少。
[0351]
实例5:热培养研究
[0352]
为了研究酶稳定性的最高温度,进行了热培养实验。这反映了在模拟闪蒸干燥方法的加热条件下测试的酶的保留活性。
[0353]
用6%甲醇、5%甘油和4.55%脂肪酶calb l在指定温度下进行30g规模的反应,其中进行15分钟培养。在速率测量之前,添加10wt%的ffa。在40℃下测量速率。
[0354]
如图8所示,在55℃下培养15分钟时,在含有5%甘油和6%甲醇的混合物中,发现calb具有热稳定性,并且没有测量到活性损失。这15min培养相当于闪蒸塔中的典型停留时间。
[0355]
实例6:闪蒸塔模拟
[0356]
利用unifac热力学模式(fredenslund等人,1975)模拟相平衡产生闪蒸塔模拟。模拟了简单的一步式闪蒸塔:在塔中在55℃入口进料温度和0.15巴下操作,入口进料由32.64%m-棕榈酸盐、5.87wt%m-硬脂酸盐、41.00wt%m-油酸盐、7.65wt%m-亚油酸盐、4.49wt%甘油、5.39wt%甲醇、2.70wt%ffa(油酸)和2500ppm水组成,模仿湿的粗生物柴油作为模型fame,直接来自于主eversa transform酯交换反应容器,其中添加5%甘油和6%甲醇(粗fame的w/w)。这在所得液体闪蒸塔出口中产生了963ppm的水浓度,但也将甲醇浓度降低至2.28wt%。通过闪蒸塔和热交换器周围的循环回路,可以更有效地除去水,当循环使用60%的液体出口时,所得水浓度达到500ppm。这意味着水浓度可能会显著降低至低于获得规范ffa浓度(《0.25wt%)所需的浓度,尤其是考虑到上图6的结果时,其中在初始
1.1wt%ffa和约2000ppm水(根据质量平衡计算)的反应后测量0.35wt%ffa。
[0357]
方法流程图
[0358]
图2中示出了根据本发明的方法的实例。在eversa transform之后,富含水的组分应混合并闪蒸,以降低反应前的水浓度。在第一反应器之后,ffa被转化为fame,产生更高的水浓度。然后,第二闪蒸步骤除去大量的水和甲醇,从而使平衡向第二反应器中的进一步ffa转化的方向偏移。最后,使用倾析步骤以循环使用大部分酶,同时通过吹扫除去级分,以减少不需要的副产物的积聚。来自闪蒸和吹扫的酶/甘油相的富含甲醇的蒸汽可循环使用至eversa transform反应步骤。
[0359]
实施例
[0360]
本发明至少涉及以下实施例:
[0361]
1.一种游离脂肪酸的酶促酯化方法,该方法包括以下步骤:
[0362]
a.提供包含游离脂肪酸的组合物i),
[0363]
b.向步骤a中提供的组合物中添加:
[0364]
ii)酯酶,
[0365]
iii)甘油,和
[0366]
iv)短链醇
[0367]
并且混合
[0368]
c.培养步骤b的混合物,使得该酯酶催化游离脂肪酸的酯化,
[0369]
d.对从步骤c得到的经培养的混合物进行闪蒸干燥,
[0370]
e.将步骤d中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合
[0371]
f.培养步骤e中获得的混合物,由此,步骤b中提供的酯酶ii)催化游离脂肪酸的酯化。
[0372]
2.根据实施例1所述的方法,其中
[0373]
步骤d的闪蒸干燥在使得经闪蒸干燥的酯酶ii)保留其活性的至少40%的条件下进行。
[0374]
3.根据前述实施例中任一项所述的方法,其中该闪蒸干燥在40℃-75℃的温度范围内进行。
[0375]
4.根据前述实施例中任一项所述的方法,其中步骤d的闪蒸干燥在低于250毫巴的压力下进行。
[0376]
5.根据前述实施例中任一项所述的方法,其中该闪蒸干燥步骤d在1至100分钟的时间范围内进行。
[0377]
6.根据前述实施例中任一项所述的方法,其中在步骤d中获得的经闪蒸干燥的混合物的含水量在0-700ppm的范围内。
[0378]
7.根据前述实施例中任一项所述的方法,其中来自步骤c的混合物在步骤d的闪蒸干燥步骤之前没有被分离。
[0379]
8.根据前述实施例中任一项所述的方法,酯酶ii)在1次至10次,例如1次至8次、如1次至6次、或例如1次至5次范围内重复使用。
[0380]
9.根据前述实施例中任一项所述的方法,该方法进一步包括以下步骤
[0381]
d.1-对从步骤f得到的经培养的混合物进行闪蒸干燥,
[0382]
e.1-将步骤d.1中获得的经闪蒸干燥的混合物与另外的短链醇v)任选地混合,以及
[0383]
f.1-培养步骤e.1中获得的混合物,由此,步骤b中提供的酯酶(ii)催化游离脂肪酸的酯化。
[0384]
10.根据前述实施例中任一项所述的方法,其中在步骤f中获得的组合物的游离脂肪酸含量小于5wt%,例如小于3wt%、小于0.5wt%或小于0.25wt%;例如在0.02wt%至5wt%,例如0.02wt%至3wt%,如0.02wt%至2wt%、0.02wt%至1wt%的范围内。
[0385]
11.根据前述实施例中任一项所述的方法,该方法进一步包括以下步骤
[0386]
g.将步骤f中获得的混合物分离成
[0387]
vi)轻相,其包含脂肪酸甲酯,和
[0388]
vii)重相,其包含酯酶、甘油和短链醇。
[0389]
12.根据实施例11所述的方法,其中步骤g的轻相vi)的游离脂肪酸含量小于5wt%,例如小于3wt%、小于0.5wt%或小于0.25wt%;例如在0.02wt%至5wt%,例如0.02wt%至3wt%,如0.02wt%至2wt%、0.02wt%至1wt%的范围内。
[0390]
13.根据实施例11或12所述的方法,该方法进一步包括步骤
[0391]
h.对通过步骤g的分离获得的轻相(vii)进行干燥。
[0392]
14.根据前述实施例11至13中任一项所述的方法,该方法进一步包括步骤i,其中来自步骤g的重相(vii)被循环使用并添加回该方法的步骤b中,从而补充步骤b中添加的ii)酯酶、iii)甘油和iv)短链醇中的一种或多种。
[0393]
15.根据前述实施例中任一项所述的方法,该方法进一步包括步骤j,碱洗。
[0394]
16.根据前述实施例中任一项所述的方法,其中该方法不包括碱洗步骤。
[0395]
17.根据前述实施例中任一项所述的方法,其中步骤a中提供的组合物i)包含0.25至10wt%范围内的量的游离脂肪酸。
[0396]
18.根据前述实施例中任一项所述的方法,其中步骤a中提供的组合物i)包含10至90wt%范围内的量的游离脂肪酸。
[0397]
19.根据前述实施例中任一项所述的方法,其中步骤a中提供的组合物i)为生物柴油原料。
[0398]
20.根据前述实施例中任一项所述的方法,其中在步骤a中提供的包含游离脂肪酸的组合物i)通过包括以下步骤的方法生产:
[0399]
a.1-提供生物柴油原料
[0400]
a.2-通过脂肪酶将游离脂肪酸酶促酯交换为脂肪酸甲酯
[0401]
a.3-分离轻相与重相
[0402]
由此组合物i)包含步骤a.3中获得的轻相或由其组成
[0403]
21.根据前述实施例中任一项所述的方法,其中该酯酶是在低水活度下具有活性的酯酶。
[0404]
22.根据本发明的方法,其中酯酶ii)选自由以下组成的组:
[0405]
(a)多肽,其包含以下的序列或由以下的序列组成:南极假丝酵母脂肪酶b(如wo 88/02775中所披露和wo 2008065060的seq id no:1中所示)、酵母样丝孢菌属物种脂肪酶(wo 98/018912)、近平滑假丝酵母脂肪酶或其组合。
[0406]
(b)多肽,其是a)中阐述的氨基酸序列的子序列;
[0407]
(c)多肽,其与(a)和(b)中定义的多肽中的任一个具有至少60%序列同一性,例如至少65%、至少70%、至少75%、至少80%,至少85%,至少90%,至少91%、至少92%、至少93%、至少94%、至少95%、至少96%、至少97%、至少98%和至少99%。
[0408]
23.根据前述实施例中任一项所述的方法,其中在步骤b中,甘油的添加量在基于组合物i)的3至12wt%的范围内。
[0409]
24.根据前述实施例中任一项所述的方法,其中在步骤b中,短链醇的添加量在基于组合物i)的2至12wt%,如3至11wt%、例如3至10wt%、如3至9wt%、例如3至8wt%、如3至7wt%、例如3至6wt%;或例如4至9wt%,如4至8wt%,例如4至7wt%的范围内。
[0410]
25.酯酶ii)在根据前述实施例中任一项所述的方法中的用途。
[0411]
26.一种用于闪蒸干燥包含游离脂肪酸的混合物的方法,所述混合物包含fame、游离脂肪酸、酯酶、甘油、短链醇和水;并且所述方法包括提供所述混合物和随后闪蒸干燥所述混合物的步骤,其中该闪蒸干燥在不使该酯酶变性的条件下进行。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1