作为农药的异噁唑啉衍生物的制作方法
作为农药的异噁唑啉衍生物
1.相关申请的交叉引用
2.本技术要求于2019年12月18日提交的美国临时申请62/950,018的优先权,该临时申请的内容通过引用整体并入本文。
技术领域
3.本发明涉及药物化学、药理学以及兽医学和人类医学。
背景技术:
4.芳基异噁唑啉用于农业、林业、草皮、家庭、木材产品、苗圃作物保护和兽医学领域。兽医学领域包括伴侣动物和家畜,包括鱼。例如,在wo 2005/085216、wo2007/079162、us 2007/066617、us20130131017、wo 2009/002809、wo 2009/112275、 wo 2010/003923、wo 2010/070068、wo 2012/120399和wo 2013/079407中公开了此类抑制剂。
5.在许多应用中,希望对害虫形成长效作用。对于伴侣动物,例如猫、狗以及小鼠、豚鼠、雪貂和兔;以及驯养的动物,例如牛、绵羊、猪和鱼,特别是鲑鱼和海鲈,长效保护是特别重要的。
技术实现要素:
6.本发明涉及对伴侣动物和家畜,特别是温血动物,尤其是狗、猫和牛,具有延长的半衰期的具有式(i)的化合物及其在控制外寄生物中的用途。在许多情况下,具有式(i) 的化合物在单次口服给药或注射后提供数月的长效作用。
7.本发明还提供了有效治疗和/或控制伴侣动物和家畜的体外寄生虫的具有式(i)的化合物。
8.在一个实施例中,本发明提供具有式(i)的化合物:
[0009][0010]
其中
[0011]
a1选自由cf3、chf2、ch2f和cf2cf3组成的组;
[0012]
a2为o或s;
[0013]
r1选自由氢和卤素组成的组;
[0014]
r2选自由氢、卤素、二氟甲基和三氟甲基组成的组;
[0015]
r3选自由氢、卤素和三氟甲基组成的组;
[0016]
r4选自由氢、卤素、二氟甲基和三氟甲基组成的组;
[0017]
r5选自由氢和卤素组成的组;
[0018]
条件是:
[0019]
仅当r2为三氟甲基、二氟甲基或溴时,r1可以为氢;
[0020]
仅当r4为三氟甲基或溴时,r5可以为氢;
[0021]
仅当r2或r4中的一个为三氟甲基、二氟甲基或溴时,r3可以为氢;
[0022]
当r2和r4为三氟甲基时,r1、r3和r5不能够都为氢;以及
[0023]
r1、r2、r3、r4和r5中至多三个为氢;
[0024]
q选自由以下组成的组
[0025][0026]
其中
[0027]
p为0、1或2;
[0028]
q为0、1、2或3;
[0029]
r为0或1;
[0030]
s为0、1或2;
[0031]
t为0或1;
[0032]
r6在每次出现时独立地选自由以下组成的组:卤素;氰基;硝基;羟基;-nh2;
ꢀ‑
nh(c
1-c4烷基);-n(c
1-c4烷基)2;c
2-c
5-烷氧羰基;c
1-c
6-烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,氧代,c
3-c6环烷基,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基和-so2c
1-c4烷基;c
1-c
6-烷氧基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
卤素,氰基,硝基,羟基,氧代,c
3-c6环烷基,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基和-so2c
1-c4烷基;-nr8c(o)(c
1-c4烷基),其任选地在c
1-c4烷基上被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,c
3-c6环烷基,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基)和-n(c
1-c4烷基)2,其中r8独立地选自由氢和c
1-c4烷基组成的组;-c(o)nr8(c
1-c4烷基),其任选地在c
1-c4烷基上被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,c
3-c6环烷基,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基)和-n(c
1-c4烷基)2,其中r8独立地选自由氢和c
1-c4烷基组成的组;-sc
1-c6烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,氧代,c
3-c6环烷基,c
1-c4烷氧基,-nh2, c
1-c7氨基羰基,-nh(c
1-c4烷基)和-n(c
1-c4烷基)2;和-s(o)c
1-c6烷基,其任选地被1 至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,氧代,c
3-c6环烷基,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基)和-n(c
1-c4烷基)2;
[0033]
r7在每次出现时独立地选自由氧代、c
1-c4烷基和c
3-c6环烷基组成的组;
[0034]
a3为o或s;
[0035]
a4为ch或n;
[0036]
a5为ch或n;
[0037]
a6为ch或n;
[0038]
a7为ch o、s、键或n;
[0039]
a8为ch o、s、键或n;
[0040]
a9为ch或n;
[0041]a10
为ch或n;
[0042]a11
为ch或n;
[0043]a12
为ch或n;
[0044]a13
为ch或n;
[0045]a14
为ch或n;
[0046]a15
为ch或n;
[0047]a16
为nr、o或s,其中r选自由氢、c
1-c4烷基和c
3-c6环烷基组成的组;
[0048]
w1选自由-o-、-s-、-nr
9-、-nc(o)r
10-、-ch
2-和-c(o)-组成的组;
[0049]
w2选自由-o-、-s-、-nr
9-、-nc(o)r
10-、-ch
2-和-c(o)-组成的组;
[0050]
条件是:
[0051]
当w1为-o-、-s-、-nr
9-或-nc(o)r
10-时,则w2为-ch
2-或-c(o)-;以及
[0052]
当w2为-o-、-s-、-nr
9-或-nc(o)r
10-时,则w1为-ch
2-或-c(o)-;
[0053]
w3选自由零、-o-、-s-、-s(o)-、-s(o)
2-、-nr
9-、-ch-、-n-、-ch
2-和-c(o)-组成的组;
[0054]
w4选自由零、-o-、-s-、-s(o)-、-s(o)
2-、-nr
9-、-ch-、-n-、-ch
2-和-c(o)-组成的组;
[0055]
w5选自由零、-o-、-s-、-s(o)-、-s(o)
2-、-nr
9-、-ch-、-n-、-ch
2-和-c(o)-组成的组;
[0056]
w6选自由零、-o-、-s-、-s(o)-、-s(o)
2-、-nr
9-、-ch-、-n-、-ch
2-和-c(o)-组成的
组;
[0057]
其中w1、w2、w3和w4之间的键可以是单键或双键;
[0058]
条件是:
[0059]
(i)w1、w2、w3和w4中不多于两个为零;
[0060]
(ii)w1、w2、w3和w4中不多于两个为-o-、-s-、-s(o)-、-s(o)
2-、-nr
9-或-c(o)-;
[0061]
(iii)如果w1、w2、w3和w4中的两个是-o-和/或-s-,则在它们之间存在至少一个碳原子;以及
[0062]
(iv)当w1、w2、w3或w4为-ch-和/或-nr
9-时,则在由w1、w2、w3和w4形成的环内形成双键;
[0063]
r9在每次出现时独立地选自由以下组成的组:氢,和c
1-c
6-烷基,其任选地被1至 5个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,氧代,c
3-c6环烷基,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基和-so2c
1-c4烷基;
[0064]r10
在每次出现时独立地选自由氧代、c
1-c4烷基和c
3-c6环烷基组成的组;
[0065]
x为具有1或2个选自由o、s和n组成的组的杂原子的5至10元杂芳基,
[0066]
其中所述5至10元杂芳基的碳任选地被1、2或3个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,氧代,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基,-c(o)nh-c
1-c6烷基和-c(o)nh-c
1-c6卤代烷基,c
3-c6环烷基,c
1-c4卤代烷基,c
1-c4烷氧基,-nh2,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,
ꢀ‑
c(o)nh-c
3-c6环烷基,-c(o)nh-c
1-c6烷基和-c(o)nh-c
1-c6卤代烷基,
[0067]
其中在化合价允许下,所述杂芳基中的任意n任选地被选自由以下组成的组的取代基取代:氢,c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,氧代,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基,-c(o)nh-c
1-c6烷基和-c(o)nh-c
1-c6卤代烷基,和c
3-c6环烷基,
[0068]
或
[0069]
x选自由以下组成的组:
[0070][0071]
其中
[0072]r11
选自由以下组成的组:氢,c
1-c4烷基,c
1-c4卤代烷基,c
3-c6环烷基,c
4-c7烷基环烷基,c
2-c7烷基羰基,c
2-c5烷氧羰基,c
2-c6烯基和c
2-c6炔基;
[0073]
w选自由以下组成的组:
[0074]
(i)氢;
[0075]
(ii)c
1-c6烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素;氰基;羟基;氧代;c
1-c4烷氧基;c
3-c6环烷基,其任选地被1至3个独立地选自由卤素和氰基组成的组的取代基取代;乙炔基;-nh2;c
1-c7氨基羰基;-nh(c
1-c4烷基);-n(c
1-c4烷基)2;-sc
1-c4烷基;-s(o)c
1-c4烷基;-so2c
1-c4烷基;-c(o)nh-c
3-c6环烷基,其任选地被1至3个独立地选自由以下组成的组的取代基取代:卤素,羟基,氰基,和c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,c
1-c4烷氧基,c
3-c6环烷基和-nh2;-c(o)nh-c
1-c6烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素、氰基、羟基、c
1-c4烷氧基、c
3-c6环烷基和-nh2;任选地被1至3个卤素取代的-c(o)nh-c
1-c6氰烷基;
ꢀ‑
c(o)nh-c
1-c6卤代烷基;-c(o)-4至7元杂环烷基,其通过氮连接并且任选地具有1或 2个选自由o、s和n组成的组的其它杂原子,其中所述4至7元杂环烷基的碳任选地被1至4个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,氧代,
ꢀ‑
nh2,c
1-c7氨基羰基,c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,氧代,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,
ꢀ‑
nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,
ꢀ‑
c(o)nh-c
3-c6环烷基和-c(o)nh-c
1-c6烷基,和c
3-c6环烷基,其中在化合价允许下,所述4至7元杂环烷基中的任意其它n被选自由以下组成的组的取代基取代:氢,-nh2, c
1-c7氨基羰基,-so2c
1-c4烷基,-so2c
1-c4卤代烷基,和c
1-c4烷基,其任选地被1至 5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,c
1-c4烷氧基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,
ꢀ‑
c(o)nh-c
3-c6环烷基,-c(o)nh-c
1-c6烷基和-c(o)nh-c
1-c6卤代烷基;具有1或2个选自由o、s和n组成的组的杂原子的5至10元杂芳基,其中所述5至10元杂芳基的碳任选地被1、2或3个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,氧代,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基,
ꢀ‑
c(o)nh-c
1-c6烷基和-c(o)nh-c
1-c6卤代烷基,c
3-c6环烷基,c
1-c4卤代烷基,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2和-c(o)nh-c
3-c6环烷基,其中在化合价允许下,所述杂芳基中的任意n任选地被选自由以下组成的组的取代基取代:氢,c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,氧代,c
3-c6环烷基,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和-c(o)nh-c
1-c6烷基,和c
3-c6环烷基,其中所述杂芳基中的任意s任选地被1或2个氧原子取代;苯基,其任选地被1至3个选自由卤素、c
1-c4烷基、氰基和羟基组成的组的取代基取代;c
3-c6环烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,氧代,c
1-c4烷氧基,任选地被1至3个选自由卤素和氰基组成的组的基团取代的c
1-c4烷基,c
1-c4卤代烷基,-nh2, c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,
ꢀ‑
so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基,-c(o)nh-c
1-c6烷基,-c(o)nh-c
1-c6卤代烷基,c
2-c6烯基和c
2-c6炔基;和具有1或2个选自由o、s、b和n组成的组的杂原子的4至7元杂环烷基,其中所述杂环烷基任选地是苯并稠合的,其中所述4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基的碳任选地被1至4个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,氧代,和c
1-c4烷基,其任选地被1至5个独立地
选自由以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,氧代,c
1-c4烷氧基,c
3-c6环烷基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基,-c(o)nh-c
1-c6烷基和-c(o)nh-c
1-c6卤代烷基,其中在化合价允许下,所述4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基中的任意b被羟基取代,其中在化合价允许下,所述4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基中的任意n被选自由以下组成的组的取代基取代:氢,-nh2,c
1-c7氨基羰基,-so2c
1-c4烷基,-so2c
1-c4卤代烷基,-c(o)-nh2,c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,c
1-c4烷氧基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,
ꢀ‑
s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和-c(o)nh-c
1-c6卤代烷基, c
3-c6环烷基,5至6元杂芳基,和苯基,其任选地被1至3个独立地选自由卤素、c
1-c4烷基、氰基和羟基组成的组的取代基取代,其中所述4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基中的任意s任选地被1或2个氧原子取代;
[0076]
(iii)c
3-c6环烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,氧代,c
1-c4烷氧基,任选地被1至3个选自由卤素和氰基组成的组的基团取代的c
1-c4烷基,c
1-c4卤代烷基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),
ꢀ‑
n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基,-c(o)nh-c
1-c6烷基,-c(o)nh-c
1-c6卤代烷基,任选地被1至3个卤素取代的c
2-c6烯基和c
2-c6炔基;
[0077]
(iv)具有1、2或3个选自由o、s和n组成的组的杂原子的6元芳基或5至10 元杂芳基,其中所述6元芳基和5至10元杂芳基的碳任选地被1、2或3个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,c
1-c4烷基,其任选地被1 至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,氧代,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和-c(o)nh-c
1-c6烷基,c
3-c6环烷基, c
1-c4卤代烷基,c
1-c4烷氧基,-nh2,-nh(c
1-c4烷基),-n(c
1-c4烷基)2和-c(o)nh-c
3-c6环烷基,其中在化合价允许下,所述杂芳基中的任意n任选地被选自由以下组成的组的取代基取代:氢,和c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,氧代,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,
ꢀ‑
nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,
ꢀ‑
c(o)nh-c
3-c6环烷基和-c(o)nh-c
1-c6烷基;
[0078]
(v)具有1或2个选自由o、s和n组成的组的杂原子的4至7元杂环烷基,其中所述杂环烷基任选地是苯并稠合的,其中所述4至7元杂环烷基或任选苯并稠合的4至 7元杂环烷基的碳任选地被1至4个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,氧代,c
1-c4烷氧基,c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,氧代,c
1-c4烷氧基,c
3-c6环烷基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基,-c(o)nh-c
1-c6烷基和-c(o)nh-c
1-c6卤代烷基,其中在化合价允许下,所述4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基中的任意n被选自由以下组成的组的取代基取代:氢,-nh2,c
1-c7氨基羰基,
ꢀ‑
so2c
1-c4烷基,-so2c
1-c4卤代烷基,-c(o)-nh2,c
1-c4烷基,其任选地被1至5个独立地选自以下由组成的组的取代基取代:卤素,氰基,羟基,乙炔基,氧代,c
1-c4烷氧基,c
3-c6环烷基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,
ꢀ‑
so2c
1-c4烷基,-so2nh(c
1-c4烷基),-so2n(c
1-c4烷基)2,-c(o)nh-c
3-c6环烷基和
ꢀ‑
c(o)nh-c
1-c6卤代烷基,c
3-c6环烷基,5至6元杂芳基,和苯基,其任选地被1至3 个独立地选自由卤素、c
1-c4烷基、氰基和羟基组成的组的取代基取代,其中所述4至7 元杂环烷基或任选苯并稠合的4至7元杂环烷基中的任意s任选地被1或2个氧原子取代;以及
[0079]
(vi)-nr
12r13
[0080]
其中
[0081]r12
选自由以下组成的组:氢,c
1-c6烷基,c
2-c6烯基,c
2-c6炔基,c
3-c6环烷基, c
4-c7烷基环烷基,c
1-c7烷基羰基,c
1-c7氨基羰基和c
2-c5烷氧羰基;
[0082]r13
选自由以下组成的组:氢,c
1-c6烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,氧代,c
3-c6环烷基,c
1-c4烷氧基,
ꢀ‑
nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基和-so2c
1-c4烷基,c
3-c6环烷基,-c(o)-c
1-c6烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,氧代,c
3-c6环烷基,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基和-so2c
1-c4烷基,具有1或2个选自由o、s和n组成的组的杂原子的4至7元杂环烷基,其中所述杂环烷基任选地是苯并稠合的,其中所述4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基的碳任选地被1至4个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,氧代,c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,氧代,c
1-c4烷氧基,-nh2, c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,
ꢀ‑
so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基,-c(o)nh-c
1-c6烷基和-c(o)nh-c
1-c6卤代烷基,和c
3-c6环烷基,其中在化合价允许下,所述4至7元杂环烷基或任选苯并稠合的 4至7元杂环烷基中的任意n被选自由以下组成的组的取代基取代:氢,c
1-c4烷基,其任选地被1至5个独立地选自以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和-c(o)nh-c
1-c6烷基, c
3-c6环烷基,5至6元杂芳基,和苯基,其任选被1至3个独立地选自卤素、c
1-c4烷基、氰基和羟基组成的组的取代基取代,其中所述4至7元杂环烷基或任选苯并稠合的 4至7元杂环烷基中的任意s任选地被1或2个氧原子取代;以及具有1或2个选自由 o、s和n组成的组的杂原子的5至10元杂芳基,其中所述5至10元杂芳基的碳任选地被1、2或3个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基, c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,氧代,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和
ꢀ‑
c(o)nh-c
1-c6烷基,c
3-c6环烷基,c
1-c4卤代烷基,c
1-c4烷氧基,-nh2,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-c(o)nh-c
3-c6环烷基和-c(o)nh-c
1-c6烷基,其中在化合价允许下,所述杂芳基中的任意n任选地被选自由以下组成的组的取代基取代:氢,c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,氧代,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和
ꢀ‑
c(o)nh-c
1-c6烷基,和c
3-c6环烷基;
[0083]
或
烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和
ꢀ‑
c(o)nh-c
1-c6烷基,和c
3-c6环烷基,和具有1或2个选自由o、s和n组成的组的杂原子的4至7元杂环烷基,其中所述杂环烷基任选地是苯并稠合的,其中所述4至7 元杂环烷基或任选苯并稠合的4至7元杂环烷基的碳任选地被1至4个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,氧代,c
1-c4烷基,其任选地被1 至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,氧代, c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,
ꢀ‑
s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和-c(o)nh-c
1-c6烷基,和c
3-c6环烷基,其中在化合价允许下,所述4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基中的任意n被选自由以下组成的组的取代基取代:氢,c
1-c4烷基,其任选地被1 至5个独立地选自以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和c(o)nh-c
1-c6烷基,c
3-c6环烷基,和 5至6元杂芳基,其中所述4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基中的任意s任选地被1或2个氧原子取代;
[0086]
或其盐。
[0087]
在一个实施例中,本发明还提供组合物,包含:具有式(i)的化合物,或其盐,以及至少一种可接受的赋形剂,组合物任选地还包含至少一种另外的活性化合物。
[0088]
在一个实施例中,本发明还提供了一种用于处理害虫的方法,其包括:向有需要的受试者施用有效量的具有式(i)的化合物,或其盐,该方法任选地还包含有效量的至少一种另外的活性化合物。
[0089]
在一个实施例中,本发明还提供了一种用于控制害虫的方法,其包括:向有需要的受试者施用有效量的具有式(i)的化合物,或其盐,该方法任选地还包含有效量的至少一种另外的活性化合物。
[0090]
在一个实施例中,本发明还提供了一种用于处理或控制害虫的方法,其包括:使受试者的环境与有效量的具有式(i)的化合物或其盐接触,该方法任选地还包含有效量的至少一种另外的活性化合物。
[0091]
因此,本发明提供本发明化合物作为药物的用途,包括用于制备药物。在一个实施例中,本发明提供用于治疗寄生虫的包含具有式(i)的化合物或其盐的药物的制备。在一个实施例中,本发明提供用于控制害虫的包含具有式(i)的化合物或其盐的药物的制备。
[0092]
本发明还提供制备本发明化合物及其中间体的方法。
具体实施方式
[0093]
术语“c
1-c2烷基”是指具有1至2个碳原子的烷基链,并且包括甲基和乙基。
[0094]
术语“c
1-c4烷基”是指具有1至4个碳原子的直链或支链的烷基链,并且包括甲基、乙基、丙基、异丙基、丁基等。
[0095]
同样,术语“c
1-c6烷基”是指具有1至6个碳原子的直链或支链的烷基链,并且包括甲基、乙基、丙基、异丙基、丁基、戊基、己基等。
[0096]
术语“c
1-c4卤代烷基”和“c
1-c4卤素烷基”是指具有1至4个碳原子和1至5个卤素的直链或支链的烷基链,并且包括氟甲基、二氟甲基、三氟甲基、2,2,2-三氟乙基、 1,2,2-三氟乙基、3,3,3-三氟丙基等。
[0097]
术语“c
1-c6卤代烷基”和“c
1-c6卤素烷基”是指具有1至6个碳原子和1至5个卤素的直链或支链的烷基链,并且包括氟甲基、二氟甲基、三氟甲基、2,2,2-三氟乙基、 1,2,2-三氟乙基、3,3,3-三氟丙基、4,4,4-三氟丁基等。
[0098]
术语“c
2-c6烯基”是指具有2至4个碳原子和一个碳-碳双键的直链或支链的烯基链,并且包括乙烯、丙烯、异丙烯、丁烯、异丁烯、仲丁烯等。
[0099]
术语“c
2-c6炔基”是指具有2至4个碳原子和一个碳-碳三键的直链或支链的炔基链,并且包括乙炔、炔丙基等。
[0100]
术语“c
1-c2烷氧基”是指通过氧原子连接的c
1-c2烷基,并且包括甲氧基和乙氧基。
[0101]
术语“c
1-c4烷氧基”是指通过氧原子连接的c
1-c4烷基,并且包括甲氧基、乙氧基、丙氧基、异丙氧基、丁氧基等。
[0102]
术语“c
1-c6烷氧基”是指通过氧原子连接的c
1-c6烷基,并且包括甲氧基、乙氧基、丙氧基、异丙氧基、丁氧基等。
[0103]
术语“c
3-c6环烷基”是指3至6个碳原子的烷基环,并且包括环丙基、环丁基、环戊基和环己基。应当理解,环烷基环可以是稠合的、桥接的或螺环稠合的。
[0104]
术语“c
4-c7烷基环烷基”是指被c
3-c6环烷基取代的c
1-c4烷基,使得碳的总数为四至七个,并且包括环丙基甲基、环丁基甲基、环戊基甲基、环己基甲基、环丙基乙基等。
[0105]
术语“卤代”、“卤素”和“卤代”是指氯、氟、溴或碘原子。
[0106]
术语“具有1或2个选自由o、s、n组成的组的杂原子的4至7元杂环烷基,其中杂环烷基任选地是苯并稠合的”和“具有1或2个选自由o、s、b、n组成的组的杂原子的4至7元杂环烷基,其中杂环烷基任选地是苯并稠合的”是指具有一个或两个选自由氮、氧和硫组成的组的杂原子或具有一个或两个选自由氮、氧、硼和硫组成的组的杂原子的4至7元饱和或部分(但不是完全)不饱和的环,且该环任选地包括羰基以形成内酰胺或内酯。应当理解,当包括硫时,硫可以是-s-、-so-或-so
2-。杂环可以是单环或双环,并且任何双环可以是稠合的、桥接的或螺环稠合的。所定义的4至7元不包括任何任选的苯并稠环。此外,如本领域技术人员完全理解的,饱和或部分(但不是完全)不饱和的4至7元杂环烷基环适用于杂环烷基环,但不适用于任何苯并稠环,苯并稠环在本质上将是完全不饱和的。还应当理解,该基团可以作为取代基在化合价允许下通过任何环杂原子、杂环烷基的碳原子或任何苯并稠合环的碳原子连接。还应当理解,当任选苯并稠合的4至7元杂环烷基任选地在碳上被取代时,取代基可以在杂环和/或苯并稠合的环的碳原子上。例如但不限于,该术语包括氮杂环丁烷基、吡咯烷基、哌啶基、哌嗪基、吗啉基、硫代吗啉基、氧杂环丁烷基、硫代氧杂环丁烷基、二氧戊环基、四氢吡喃基、四氢硫吡喃基、四氢呋喃基、六氢嘧啶基、四氢嘧啶基、2,6-二氮杂螺[3.3]庚烷基、异噁唑烷、二氢咪唑基、吲哚基、异吲哚基等。
[0107]
术语“5或6元杂芳基”是指具有一至五个碳原子和一个或多个,通常一至四个选自由氮、氧和硫组成的组的杂原子的六元单环完全不饱和环。例如但不限于,该术语包括吡咯基、呋喃基、噻吩基、咪唑基、噁唑基、异噁唑基、噻唑基、三唑基、吡嗪基、吡唑基、哒嗪基、吡啶基、嘧啶基等。应当理解,6元杂芳基可作为取代基通过环碳或环氮原子连接,在这种连接模式可用处。
[0108]
当r
11
和w与其所连接的氮合在一起时,术语“任选地含有1至2个选自由n、s 和o组成的组的杂原子的4至7元环”是指具有包括r
11
和w所连接的氮在内的四至七元的完全饱和
或部分不饱和(但不是完全)环,并且包括氮杂环丁烷基、吡咯烷基、哌啶基、哌嗪基、吗啉基、硫代吗啉基、氧杂环丁烷基、二氧戊环基、四氢吡喃基、四氢硫吡喃基、四氢呋喃基、六氢嘧啶基、四氢嘧啶基、二氢咪唑基等。
[0109]
术语“具有1或2个选自由o、s和n组成的组的杂原子的5至10元杂芳基”是指具有一至九个碳原子和一或两个选自由氮、氧和硫组成的组的杂原子的五至十元单环或多环完全不饱和环或环系。例如但不限于,该术语包括呋喃基、噻吩基、吡咯基、咪唑基、异噻唑基、异噁唑基、噁二唑基、噁唑基、噻唑基、吡嗪基、吡唑基、哒嗪基、吡啶基、嘧啶基、氮杂基、二氮杂基、苯并呋喃基、苯并噻吩基、吲哚基、异吲哚基、苯并咪唑基、苯并异噻唑基、苯并异噁唑基、苯并噁唑基、苯并吡嗪基、苯并吡唑基、喹唑啉基、噻吩并吡啶基、喹啉基、异喹啉基苯并噻唑基等。应当理解,具有1或2个选自由o、s和n组成的组的杂原子的5至10元杂芳基可作为取代基通过环碳或环氮原子连接,在这种连接模式可用处。
[0110]
术语“氧代”是指与其所连接的碳双键键合以形成酰胺、酮或醛的羰基的氧原子。例如,吡啶酮基团被认为是氧代取代的6元杂芳基。
[0111]
术语“羧基”是指以下基团:
[0112][0113]
术语“n,n-二-c
1-c
4-烷基氨基羰基”是指以下基团:
[0114][0115]
其中氮上的氢被两个独立选择的c
1-c4烷基取代。
[0116]
同样地,术语“n-c
1-c
4-烷基氨基羰基”是指下述基团:
[0117][0118]
其中氮上的一个氢被c
1-c4烷基取代。
[0119]
术语“c
2-c5烷氧羰基”是指以下基团:
[0120][0121]
其中r为c
1-c4烷基。
[0122]
术语“c
2-c7烷基羰基”是指以下基团:
[0123][0124]
其中r为c
1-c6烷基。
[0125]
同样地,术语“c
2-c7卤代烷基羰基”是指上述基团,其中r为c
1-c6卤代烷基。
[0126]
术语“c
1-c7氨基羰基”是指具有以下基团:
[0127][0128]
其中r为氢或c
1-c4烷基。
[0129]
本文所用的关于基团、取代基、部分等的术语“无”表示该基团、取代基或部分不存在。其中基团、取代基或部分通常键合至两个或更多个其它基团、取代基或部分,其它基团、取代基或部分代替为零的基团、取代基或部分键合。例如,具有结构a-b-c的化合物;其中b为零,则a直接键合至c,并且该化合物为a-c。作为另一实例,具有结构a-b-c的化合物反应;其中c为零,则该化合物为a-b。
[0130]
术语“盐”是指兽医学或药学上可接受的有机酸和碱或无机酸和碱的盐。这样的盐是本领域公知的,并且包括在《药物科学杂志(journal ofpharmaceutical science)》,66, 2-19(1977)中描述的那些。一个实例是盐酸盐。
[0131]
术语“被取代的”,包括当在“任选地被取代的”中使用时,是指基团的一个或多个氢基团被非氢基团(取代基)替代。应当理解,每个取代位置处的取代基可以相同或不同。本发明设想的基团和取代基的组合是稳定的或化学上可行的那些。对于本文所述的化合物,其基团和取代基可根据原子和取代基的允许化合价来选择,使得选择和取代产生稳定的化合物,例如其不会自发地发生转化,例如通过重排、环化、消除等。
[0132]
术语“稳定的”是指当经受允许其产生的条件时基本上没有改变的化合物。在非限制性实例中,稳定化合物或化学上可行的化合物是当在不存在水分或其它化学反应性条件的情况下在40℃或更低的温度下保持约一周时基本上没有改变的化合物。
[0133]
应当理解,当本文定义的术语提及碳原子数时,所提及的数指所提及的基团且不包括可存在于其上的任何任选取代基中的任何碳或可作为稠环、包括苯并稠环的一部分存在的任何碳。
[0134]
本领域技术人员将理解本发明的某些化合物作为异构体存在。本发明化合物的所有立体异构体,包括任何比例的几何异构体、对映异构体和非对映异构体,都包括在本发明的范围内。
[0135]
如本文所用,化学命名法中的术语“(rs)”是指在指定立构中心处的外消旋混合物。
[0136]
如本文所用,化学命名中的术语“(r或s)”或“(s或r)”是指所示立构中心处的两种可能构型之一。
[0137]
本领域技术人员还将理解本发明的某些化合物作为互变异构体存在。本发明化合物的所有互变异构形式均涵盖在本发明的范围内。
[0138]
本发明的化合物还包括所有同位素变体,其中具有主要原子质量的至少一个原子被具有相同原子数但原子质量不同于主要原子质量的原子替代。使用同位素变体(例如氘,2h)可提供更大的代谢稳定性。另外,本发明化合物的某些同位素变体可掺入放射性同位素(例如氚,3h或
14
c),其可用于药物和/或底物组织分布研究。使用正电子发射同位素如
11
c、
18
f、
15
o和
13
n的取代可用于正电子发射拓扑学(pet)研究。
[0139]
术语“发明的化合物”和“发明的一种化合物”和“本发明的化合物”等包括具有式(i)的实施例和本文所述的式(i)涵盖的其它更具体的实施例以及本文所述的示例性化合
物和这些实施例各自的盐。
[0140]
具有多种实施例的具有式(i)的化合物如下:
[0141]
式(i):
[0142]
[0143][0144]
应当理解,对于a4、a5、a6、a7、a9、a
10
、a
11
、a
12
、a
14
和/或a
15
,r6取代基当存在时替换ch的氢。
[0145]
还应当理解,对于具有式(ig)的化合物,x基团当存在时通过替换-ch
2-或-ch
‑ꢀ
基团的氢或-nr-基团的r而连接在w3、w4、w5或w6处。
[0146]
本发明化合物的其它实施例提供如下:
[0147]
(1)一个实施例涉及一种具有式(i)的化合物或其盐。
[0148]
(a)一个实施例涉及具有式(ia)的化合物或其盐。
[0149]
(b)一个实施例涉及具有式(ib)的化合物或其盐。
[0150]
(c)一个实施例涉及具有式(ic)的化合物或其盐。
[0151]
(d)一个实施例涉及具有式(id)的化合物或其盐。
[0152]
(e)一个实施例涉及具有式(ie)的化合物或其盐。
[0153]
(f)一个实施例涉及具有式(if)的化合物或其盐。
[0154]
(g)一个实施例涉及具有式(ig)的化合物或其盐。
[0155]
(h)一个实施例涉及实施例(1)、(a)、(b)、(c)、(d)、(e)、(f)和(g),其中 r1为氢,r2为三氟甲基,r3为氢,r4为三氟甲基,并且r5为卤素;或其盐。
[0156]
(i)一个实施例涉及实施例(1)、(a)、(b)、(c)、(d)、(e)、(f)和(g),其中r1为氢,r2为三氟甲基,r3为氢,r4为卤素,并且r5为卤素;或其盐。
[0157]
(j)一个实施例涉及实施例(1)、(a)、(b)、(c)、(d)、(e)、(f)和(g),其中r1为氢,r2为三氟甲基,r3为氢,r4为氯,并且r5为卤素;或其盐。
[0158]
(k)一个实施例涉及实施例(1)、(a)、(b)、(c)、(d)、(e)、(f)和(g),其中 r1为氢,r2为三氟甲基,r3为氢,r4为卤素,并且r5为氯;或其盐。
[0159]
(l)一个实施例涉及实施例(1)、(a)、(b)、(c)、(d)、(e)、(f)和(g),其中r1为氢,r2为三氟甲基,r3为氢,r4为卤素,并且r5为氟;或其盐。
[0160]
(m)一个实施例涉及实施例(1)、(a)、(b)、(c)、(d)、(e)、(f)和(g),其中 r1为氢,r2为三氟甲基,r3为氢,r4为氯,并且r5为氟;或其盐。
[0161]
(n)一个实施例涉及实施例(1)、(a)、(b)、(c)、(d)、(e)、(f)、(g)、(h)、(i)、 (j)、(k)、(l)和(m),其中a2为o;或其盐。
[0162]
(o)一个实施例涉及实施例(1)、(a)、(b)、(c)、(d)、(e)、(f)、(g)、(h)、(i)、 (j)、(k)、(l)、(m)和(n),其中a1为cf3;或其盐。
[0163]
(p)一个实施例涉及实施例(1)、(a)、(b)、(c)、(d)、(e)、(f)、(g)、(h)、(i)、 (j)、(k)、((l)、(m)和(n),其中a1为chf2;或其盐。
[0164]
(q)一个实施例涉及实施例(1)、(a)、(h)、(i)、(j)、(k)、(l)、(m)、(n)、(o) 和(p),其中a3为s;或其盐。
[0165]
(r)一个实施例涉及实施例(q),其中p为1,并且r5为c
1-c6烷基;或其盐。
[0166]
(s)一个实施例涉及实施例(r),其中r6为甲基;或其盐。
[0167]
(t)一个实施例涉及实施例(1)、(b)、(h)、(i)、(j)、(k)、(l)、(m)、(n)、(o) 和(p),其中a4、a5和a6为ch;或其盐。
[0168]
(u)一个实施例涉及实施例(t),其中p为1,并且r6为c
1-c6烷基;或其盐。
[0169]
(v)一个实施例涉及实施例(u),其中r6为甲基;或其盐。
[0170]
(w)一个实施例涉及实施例(1)、(c)、(h)、(i)、(j)、(k)、(l)、(m)、(n)、(o) 和(p),其中a7、a8、a9、a
10
、a
11
和a
12
为ch;或其盐。
[0171]
(x)一个实施例涉及实施例(1)、(d)、(h)、(i)、(j)、(k)、(l)、(m)、(n)、(o) 和(p),其中a
13
、a
14
和a
15
为ch;或其盐。
[0172]
(y)一个实施例涉及实施例(x),其中w1为-ch
2-,并且w2为o;或其盐。
[0173]
(z)一个实施例涉及实施例(1)、(a)、(b)、(c)、(g)、(h)、(i)、(j)、(k)、(l)、 (m)、(n)、(o)、(p)、(q)、(r)、(s)、(t)、(u)、(v)、(w)和(x),其中x为
[0174][0175]
其中r
11
是氢;或其盐。
[0176]
(aa)一个实施例涉及实施例(z),其中w为c
1-c6烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0177]
卤素,
[0178]
氰基,
[0179]
羟基,
[0180]
氧代,
[0181]c1-c4烷氧基,
[0182]c3-c6环烷基,其任选地被1至3个独立地选自由卤素和氰基组成的组的取代基取代;
[0183]
乙炔基,
[0184]-nh2,
[0185]c1-c7氨基羰基,
[0186]-nh(c
1-c4烷基),
[0187]-n(c
1-c4烷基)2,
[0188]-sc
1-c4烷基,
[0189]-s(o)c
1-c4烷基,
[0190]-so2c
1-c4烷基,
[0191]-c(o)nh-c
3-c6环烷基,其任选地被1至3个独立地选自由以下组成的组的取代基取代:
[0192]
卤素,
[0193]
羟基,
[0194]
氰基,和
[0195]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0196]
卤素,
[0197]
氰基,
[0198]
羟基,
[0199]c1-c4烷氧基,
[0200]c3-c6环烷基,和
[0201]-nh2,
[0202]-c(o)nh-c
1-c6烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0203]
卤素,
[0204]
氰基,
[0205]
羟基,
[0206]c1-c4烷氧基,
[0207]c3-c6环烷基,和
[0208]-nh2;
[0209]
任选地被1至3个卤素取代的-c(o)nh-c
1-c6氰烷基,
[0210]-c(o)nh-c
1-c6卤代烷基,
[0211]-c(o)-4至7元杂环烷基,其通过氮连接并且任选地具有1或2个选自由o、s、n 组成的组的其它杂原子,其中4至7元杂环烷基的碳任选地被1至4个独立地选自由以下组成的组的取代基取代:
[0212]
卤素,
[0213]
氰基,
[0214]
硝基,
[0215]
羟基,
[0216]
氧代,
[0217]-nh2,
[0218]c1-c7氨基羰基,
[0219]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0220]
卤素,
[0221]
氰基,
[0222]
羟基,
[0223]
乙炔基,
[0224]
氧代,
[0225]c1-c4烷氧基,
[0226]-nh2,
[0227]c1-c7氨基羰基,
[0228]-nh(c
1-c4烷基),
[0229]-n(c
1-c4烷基)2,
[0230]-sc
1-c4烷基,
[0231]-s(o)c
1-c4烷基,
[0232]-so2c
1-c4烷基,
[0233]-c(o)nh-c
3-c6环烷基,和
[0234]-c(o)nh-c
1-c6烷基,和
[0235]c3-c6环烷基;
[0236]
并且在化合价允许下,4至7元杂环烷基中的任何其它n被选自由以下组成的组的
取代基取代:
[0237]
氢,
[0238]-nh2,
[0239]c1-c7氨基羰基,
[0240]-so2c
1-c4烷基,
[0241]-so2c
1-c4卤代烷基,
[0242]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0243]
卤素,
[0244]
氰基,
[0245]
羟基,
[0246]
乙炔基,
[0247]c1-c4烷氧基,
[0248]-nh(c
1-c4烷基),
[0249]-n(c
1-c4烷基)2,
[0250]-sc
1-c4烷基,
[0251]-s(o)c
1-c4烷基,
[0252]-so2c
1-c4烷基,
[0253]-c(o)nh-c
3-c6环烷基,
[0254]-c(o)nh-c
1-c6烷基,
[0255]-c(o)nh-c
1-c6卤代烷基;
[0256]
具有1或2个选自由o、s和n组成的组的杂原子的5至10元杂芳基,并且其中5 至10元杂芳基的碳任选地被1、2或3个独立地选自由以下组成的组的取代基取代:
[0257]
卤素,
[0258]
氰基,
[0259]
硝基,
[0260]
羟基,
[0261]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0262]
卤素,
[0263]
氰基,
[0264]
羟基,
[0265]
氧代,
[0266]c1-c4烷氧基,
[0267]-nh2,
[0268]c1-c7氨基羰基,
[0269]-nh(c
1-c4烷基),
[0270]-n(c
1-c4烷基)2,
[0271]-sc
1-c4烷基,
[0272]-s(o)c
1-c4烷基,
[0273]-so2c
1-c4烷基,
[0274]-c(o)nh-c
3-c6环烷基,
[0275]-c(o)nh-c
1-c6烷基,和
[0276]-c(o)nh-c
1-c6卤代烷基;
[0277]c3-c6环烷基,
[0278]c1-c4卤代烷基,
[0279]c1-c4烷氧基,
[0280]-nh2,
[0281]c1-c7氨基羰基,
[0282]-nh(c
1-c4烷基),
[0283]-n(c
1-c4烷基)2,和
[0284]-c(o)nh-c
3-c6环烷基;
[0285]
并且在化合价允许下,杂芳基中的任意n任选地被选自由以下组成的组的取代基取代:
[0286]
氢,
[0287]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0288]
卤素,
[0289]
氰基,
[0290]
羟基,
[0291]
乙炔基,
[0292]
氧代,
[0293]c3-c6环烷基,
[0294]c1-c4烷氧基,
[0295]-nh2,
[0296]c1-c7氨基羰基,
[0297]-nh(c
1-c4烷基),
[0298]-n(c
1-c4烷基)2,
[0299]-sc
1-c4烷基,
[0300]-s(o)c
1-c4烷基,
[0301]-so2c
1-c4烷基,
[0302]-c(o)nh-c
3-c6环烷基,和
[0303]-c(o)nh-c
1-c6烷基;和
[0304]c3-c6环烷基;
[0305]
并且杂芳基中的任意s被1或2个氧原子取代;
[0306]
苯基,其任选地被1至3个选自由以下组成的组的取代基取代:
[0307]
卤素,
[0308]c1-c4烷基,
[0309]
氰基,或
[0310]
羟基;
[0311]c3-c6环烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0312]
卤素,
[0313]
氰基,
[0314]
羟基,
[0315]
氧代,
[0316]c1-c4烷氧基,
[0317]
任选地被1至3个选自由卤素和氰基组成的组的基团取代的c
1-c4烷基,
[0318]c1-c4卤代烷基,
[0319]-nh2,
[0320]c1-c7氨基羰基,
[0321]-nh(c
1-c4烷基),
[0322]-n(c
1-c4烷基)2,
[0323]-sc
1-c4烷基,
[0324]-s(o)c
1-c4烷基,
[0325]-so2c
1-c4烷基,
[0326]-c(o)nh-c
3-c6环烷基,
[0327]-c(o)nh-c
1-c6烷基,
[0328]-c(o)nh-c
1-c6卤代烷基,
[0329]c2-c6烯基,和
[0330]c2-c6炔基;和
[0331]
具有1或2个选自由o、s、b和n组成的组的杂原子的4至7元杂环烷基,其中杂环烷基任选地是苯并稠合的,并且其中4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基的碳任选地被1至4个独立地选自由以下组成的组的取代基取代:
[0332]
卤素,
[0333]
氰基,
[0334]
硝基,
[0335]
羟基,
[0336]
氧代,
[0337]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0338]
卤素,
[0339]
氰基,羟基,
[0340]
乙炔基,
[0341]
氧代,
[0342]c1-c4烷氧基,
[0343]c3-c6环烷基,
[0344]-nh2,
[0345]c1-c7氨基羰基,
[0346]-nh(c
1-c4烷基),
[0347]-n(c
1-c4烷基)2,
[0348]-sc
1-c4烷基,
[0349]-s(o)c
1-c4烷基,
[0350]-so2c
1-c4烷基,
[0351]-c(o)nh-c
3-c6环烷基,
[0352]-c(o)nh-c
1-c6烷基,和
[0353]
和-c(o)nh-c
1-c6卤代烷基;
[0354]
并且在化合价允许下,4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基中的任意b被羟基取代,
[0355]
并且在化合价允许下,4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基中的任意n被选自由以下组成的组的取代基取代:
[0356]
氢,
[0357]-nh2,
[0358]c1-c7氨基羰基,
[0359]-so2c
1-c4烷基,
[0360]-so2c
1-c4卤代烷基,
[0361]-c(o)-nh2,
[0362]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0363]
卤素,
[0364]
氰基,
[0365]
羟基,
[0366]
乙炔基,
[0367]c1-c4烷氧基,
[0368]-nh(c
1-c4烷基),
[0369]-n(c
1-c4烷基)2,
[0370]-sc
1-c4烷基,
[0371]-s(o)c
1-c4烷基,
[0372]-so2c
1-c4烷基,
[0373]-c(o)nh-c
3-c6环烷基,和
[0374]-c(o)nh-c
1-c6卤代烷基;
[0375]c3-c6环烷基;
[0376]
5至6元杂芳基;和
[0377]
苯基,其任选地被1至3个独立地选自由以下组成的组的取代基取代:
[0378]
卤素,
[0379]c1-c4烷基,
[0380]
氰基,和
[0381]
羟基;并且
[0382]
4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基中的任意s被1或2个氧原子取代;
[0383]
或其盐。
[0384]
(ab)一个实施例涉及实施例(aa),其中w为c
1-c6烷基,c
1-c6烷基被选自由以下组
成的组的取代基取代:
[0385]-c(o)nh-c
1-c6烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0386]
卤素,
[0387]
氰基,
[0388]
羟基,
[0389]c1-c4烷氧基,
[0390]c3-c6环烷基,和
[0391]-nh2;
[0392]
任选地被1至3个卤素取代的-c(o)nh-c
1-c6氰烷基,
[0393]-c(o)nh-c
1-c6卤代烷基,和
[0394]-c(o)-4至7元杂环烷基,其通过氮连接并且任选地具有1或2个选自由o、s、n 组成的组的其它杂原子,其中4至7元杂环烷基的碳任选地被1至4个独立地选自由以下组成的组的取代基取代:
[0395]
卤素,
[0396]
氰基,
[0397]
硝基,
[0398]
羟基,
[0399]
氧代,
[0400]-nh2,
[0401]c1-c7氨基羰基,
[0402]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0403]
卤素,
[0404]
氰基,
[0405]
羟基,
[0406]
乙炔基,
[0407]
氧代,
[0408]c1-c4烷氧基,
[0409]-nh2,
[0410]c1-c7氨基羰基,
[0411]-nh(c
1-c4烷基),
[0412]-n(c
1-c4烷基)2,
[0413]-sc
1-c4烷基,
[0414]-s(o)c
1-c4烷基,
[0415]-so2c
1-c4烷基,
[0416]-c(o)nh-c
3-c6环烷基,和
[0417]-c(o)nh-c
1-c6烷基,和
[0418]c3-c6环烷基;
[0419]
并且在化合价允许下,4至7元杂环烷基中的任何其它n被选自由以下组成的组的
取代基取代:
[0420]
氢,
[0421]-nh2,
[0422]c1-c7氨基羰基,
[0423]-so2c
1-c4烷基,
[0424]-so2c
1-c4卤代烷基,
[0425]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0426]
卤素,
[0427]
氰基,
[0428]
羟基,
[0429]
乙炔基,
[0430]c1-c4烷氧基,
[0431]-nh(c
1-c4烷基),
[0432]-n(c
1-c4烷基)2,
[0433]-sc
1-c4烷基,
[0434]-s(o)c
1-c4烷基,
[0435]-so2c
1-c4烷基,
[0436]-c(o)nh-c
3-c6环烷基,
[0437]-c(o)nh-c
1-c6烷基,
[0438]-c(o)nh-c
1-c6卤代烷基;
[0439]
或其盐。
[0440]
(ac)一个实施例涉及实施例(ab),其中w为
[0441][0442]
或其盐。
[0443]
(ad)一个实施例涉及实施例(z),其中w为被-c(o)nh-c
3-c6环烷基取代的c
1-c6烷基,-c(o)nh-c
3-c6环烷基任选地被1至3个独立地选自由以下组成的组的取代基取代:卤素,羟基,氰基和c
1-c4烷基,c
1-c4烷基任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,c
1-c4烷氧基和-nh2;或其盐。
[0444]
(ae)一个实施例涉及实施例(z),其中w为被-c(o)nh-c
1-c6烷基取代的c
1-c6烷基,-c(o)nh-c
1-c6烷基任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0445]
卤素,
[0446]
氰基,
[0447]
羟基,
[0448]c1-c4烷氧基,
[0449]c3-c6环烷基,和
[0450]-nh2;
[0451]
或其盐。
[0452]
(ae1)一个实施例涉及实施例(ae),其中w为
[0453][0454]
或其盐。
[0455]
(ae2)一个实施例涉及实施例(ae),其中w为
[0456][0457]
或其盐。
[0458]
(af)一个实施例涉及实施例(z),其中w为c
1-c6烷基,c
1-c6烷基被具有1或2 个选自由o、s、b和n组成的组的杂原子的5至10元杂芳基取代,并且其中5至10 元杂芳基的碳任选地被1、2或3个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基,c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,氧代,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和-c(o)nh-c
1-c6烷基;c
3-c6环烷基,c
1-c4卤代烷基,c
1-c4烷氧基,-nh2,
[0459]-nh(c
1-c4烷基),-n(c
1-c4烷基)2和-c(o)nh-c
3-c6环烷基;并且杂芳基中的任意b 被羟基取代,并且在化合价允许下,杂芳基中的任意n任选地被选自由以下组成的组的取代基取代:氢,c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,乙炔基,氧代,c
3-c6环烷基,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,
[0460]-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和-c(o)nh-c
1-c6烷基,并且杂芳基中的任意s被1或2个氧原子取代;或其盐。
[0461]
(af1)一个实施例涉及实施例(z),其中w是被吡啶取代的c
1-c6烷基,吡啶任选地被1、2或3个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基, c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,氧代,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和
ꢀ‑
c(o)nh-c
1-c6烷基;c
3-c6环烷基,c
1-c4卤代烷基,c
1-c4烷氧基,-nh2,-nh(c
1-c4烷基),-n(c
1-c4烷基)2和-c(o)nh-c
3-c6环烷基;或其盐。
[0462]
(af2)一个实施例涉及实施例(z),其中w为被噻唑取代的c
1-c6烷基,噻唑任选地被1、2或3个独立地选自由以下组成的组的取代基取代:卤素,氰基,硝基,羟基, c
1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:卤素,氰基,羟基,氧代,c
1-c4烷氧基,-nh2,c
1-c7氨基羰基,-nh(c
1-c4烷基),-n(c
1-c4烷基)2,-sc
1-c4烷基,-s(o)c
1-c4烷
基,-so2c
1-c4烷基,-c(o)nh-c
3-c6环烷基和
ꢀ‑
c(o)nh-c
1-c6烷基;c
3-c6环烷基,c
1-c4卤代烷基,c
1-c4烷氧基,-nh2,-nh(c
1-c4烷基),-n(c
1-c4烷基)2和-c(o)nh-c
3-c6环烷基;或其盐。
[0463]
(ag)一个实施例涉及实施例(z),其中w为具有1或2个选自由o、s、n组成的组的杂原子的4至7元杂环烷基,其中杂环烷基任选地是苯并稠合的,并且其中4至7 元杂环烷基或任选苯并稠合的4至7元杂环烷基的碳任选地被1至4个独立地选自由以下组成的组的取代基取代:
[0464]
卤素,
[0465]
氰基,
[0466]
硝基,
[0467]
羟基,
[0468]
氧代,
[0469]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0470]
卤素,
[0471]
氰基,羟基,
[0472]
乙炔基,
[0473]
氧代,
[0474]c1-c4烷氧基,
[0475]c3-c6环烷基,
[0476]-nh2,
[0477]c1-c7氨基羰基,
[0478]-nh(c
1-c4烷基),
[0479]-n(c
1-c4烷基)2,
[0480]-sc
1-c4烷基,
[0481]-s(o)c
1-c4烷基,
[0482]-so2c
1-c4烷基,
[0483]-c(o)nh-c
3-c6环烷基,
[0484]-c(o)nh-c
1-c6烷基,
[0485]
和
[0486]-c(o)nh-c
1-c6卤代烷基;和
[0487]
并且在化合价允许下,4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基中的任意n被选自由以下组成的组的取代基取代:
[0488]
氢,
[0489]-nh2,
[0490]c1-c7氨基羰基,
[0491]-so2c
1-c4烷基,
[0492]-so2c
1-c4卤代烷基,
[0493]-c(o)-nh2,
[0494]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0495]
卤素,
[0496]
氰基,
[0497]
羟基,
[0498]
乙炔基,
[0499]c1-c4烷氧基,
[0500]c3-c6环烷基,
[0501]-nh(c
1-c4烷基),
[0502]-n(c
1-c4烷基)2,
[0503]-sc
1-c4烷基,
[0504]-s(o)c
1-c4烷基,
[0505]-so2c
1-c4烷基,
[0506]-c(o)nh-c
3-c6环烷基,和
[0507]-c(o)nh-c
1-c6卤代烷基;
[0508]c3-c6环烷基;
[0509]
5至6元杂芳基;和
[0510]
苯基,其任选地被1至3个独立地选自由以下组成的组的取代基取代:
[0511]
卤素,
[0512]c1-c4烷基,
[0513]
氰基,和
[0514]
羟基;并且
[0515]
4至7元杂环烷基或任选苯并稠合的4至7元杂环烷基中的任意s被1或2个氧原子取代;
[0516]
或其盐。
[0517]
(ag1)一个实施例涉及实施例(ag),其中w为具有1或2个选自由o、s组成的组的杂原子的4至7元杂环烷基,n选自由以下组成的组:吡咯基,氮杂环丁烷基,2
‑ꢀ
氧代氮杂环丁烷基,异噁唑烷基,2,6-二氮杂螺[3.3]庚烷基和1,6-二氮杂螺[3.3]庚烷基其中4至7元杂环烷基的碳任选地被1至4个独立地选自由以下组成的组的取代基取代:
[0518]
卤素,
[0519]
氰基,
[0520]
硝基,
[0521]
羟基,
[0522]
氧代,
[0523]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0524]
卤素,
[0525]
氰基,羟基,
[0526]
乙炔基,
[0527]
氧代,
[0528]c1-c4烷氧基,
[0529]c3-c6环烷基,
[0530]-nh2,
[0531]c1-c7氨基羰基,
[0532]-nh(c
1-c4烷基),
[0533]-n(c
1-c4烷基)2,
[0534]-sc
1-c4烷基,
[0535]-s(o)c
1-c4烷基,
[0536]-so2c
1-c4烷基,
[0537]-c(o)nh-c
3-c6环烷基,
[0538]-c(o)nh-c
1-c6烷基,
[0539]
和
[0540]-c(o)nh-c
1-c6卤代烷基;
[0541]
并且在化合价允许下,4至7元杂环烷基中的任意n被选自由以下组成的组的取代基取代:
[0542]
氢,
[0543]-so2c
1-c4烷基,
[0544]-so2c
1-c4卤代烷基,
[0545]-c(o)-nh2,
[0546]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0547]
卤素,
[0548]
氰基,
[0549]
羟基,
[0550]
乙炔基,
[0551]c1-c4烷氧基,
[0552]c3-c6环烷基,
[0553]-nh(c
1-c4烷基),
[0554]-n(c
1-c4烷基)2,
[0555]-sc
1-c4烷基,
[0556]-s(o)c
1-c4烷基,
[0557]-so2c
1-c4烷基,
[0558]-c(o)nh-c
3-c6环烷基,和
[0559]-c(o)nh-c
1-c6卤代烷基;和
[0560]c3-c6环烷基;
[0561]
或其盐。
[0562]
(ah)一个实施例涉及实施例(ag)和(ag1),其中4至7元杂环烷基的碳任选地被 1至2个独立地选自由氧代和c
1-c4烷基组成的组的取代基取代
[0563]
并且在化合价允许下,4至7元杂环烷基中的任意n被氢和任选地被1至3个卤素取代的c
1-c4烷基、氰基、乙炔基或c
3-c6环烷基取代;或其盐。
[0564]
(ai)一个实施例涉及实施例(ag)、(ag1)和(ah),其中4至7元杂环烷基的碳被 1个氧代取代,并且在化合价允许下,4至7元杂环烷基中的任意n被1个氰基取代的 c
1-c4烷基取代;或其盐。
[0565]
(aj)一个实施例涉及实施例(ag)、(ag1)和(ah),其中4至7元杂环烷基的碳被1个氧代取代,并且在化合价允许下,4至7元杂环烷基中的任意n被1至3个卤素取代的c
1-c4烷基取代;或其盐。
[0566]
(ak)一个实施例涉及实施例(ag)、(ag1)和(ah),其中4至7元杂环烷基的碳被 1个氧代取代,并且在化合价允许下,4至7元杂环烷基中的任意n被1个c
3-c6环烷基取代的c
1-c4烷基取代;或其盐。
[0567]
(al)一个实施例涉及实施例(ag)、(ag1)和(ah),其中在化合价允许下,4至7 元杂环烷基中的任意n被1个氰基取代的c
1-c4烷基取代;或其盐。
[0568]
(am)一个实施例涉及实施例(ag)、(ag1)和(ah),其中在化合价允许下,4至7 元杂环烷基中的任意n被1至3个卤素取代的c
1-c4烷基取代;或其盐。
[0569]
(an)一个实施例涉及实施例(ag)、(ag1)和(ah),其中在化合价允许下,4至7 元杂环烷基中的任意n被1个c
3-c6环烷基取代的c
1-c4烷基取代;或其盐。
[0570]
(an1)一个实施例涉及实施例(z),其中w为c
3-c6环烷基,c
3-c6环烷基任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0571]
卤素,
[0572]
氰基,
[0573]
羟基,
[0574]
氧代,
[0575]c1-c4烷氧基,
[0576]
任选地被1至3个选自由卤素和氰基组成的组的基团取代的c
1-c4烷基,
[0577]c1-c4卤代烷基,
[0578]-nh2,
[0579]c1-c7氨基羰基,
[0580]-nh(c
1-c4烷基),
[0581]-n(c
1-c4烷基)2,
[0582]-sc
1-c4烷基,
[0583]-s(o)c
1-c4烷基,
[0584]-so2c
1-c4烷基,
[0585]-c(o)nh-c
3-c6环烷基,
[0586]-c(o)nh-c
1-c6烷基,
[0587]-c(o)nh-c
1-c6卤代烷基,
[0588]
任选地被1至3个卤素取代的c
2-c6烯基;和
[0589]c2-c6炔基;
[0590]
或其盐。
[0591]
(ao)涉及实施方案(1)、(d)、(e)、(f)、(h)、(i)、(j)、(k)、(l)、(m)、(n)、 (o)、(p)、(t)、(x)和(y),其中y为c
1-c6烷基,c
1-c6烷基任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0592]
卤素,
[0593]
氰基,
[0594]
羟基,
[0595]
氧代,
[0596]c3-c6环烷基,
[0597]c1-c4烷氧基,
[0598]
乙炔基,
[0599]-nh2,
[0600]c1-c7氨基羰基,
[0601]-nh(c
1-c4烷基),
[0602]-n(c
1-c4烷基)2,
[0603]-sc
1-c4烷基,
[0604]-s(o)c
1-c4烷基,
[0605]-so2c
1-c4烷基,
[0606]-c(o)nh-c
3-c6环烷基,其任选地被1至3个独立地选自由以下组成的组的取代基取代:
[0607]
卤素,
[0608]
羟基,
[0609]
氰基,和
[0610]c1-c4烷基,其任选地被1至5个独立地选自由以下组成的组的取代基取代:
[0611]
卤素,
[0612]
氰基,
[0613]
羟基,
[0614]c1-c4烷氧基,和
[0615]-nh2,
[0616]-c(o)nh-c
1-c6烷基,
[0617]
任选地被1至3个卤素取代的-c(o)nh-c
1-c6氰烷基,
[0618]-c(o)nh-c
1-c6卤代烷基;
[0619]
或其盐。
[0620]
(ap)一个实施例涉及实施例(aq),其中y为被1个-so2c
1-c4烷基取代的c
1-c6烷基;或其盐。
[0621]
(aq)一个实施例涉及实施例(aq),其中y为被1个-so2ch3取代的c
1-c6烷基;或其盐。
[0622]
(xa)另一实施例涉及各示例性化合物或其盐。
[0623]
(xb)另一实施例涉及各例示、描绘或命名的化合物的各立体异构体;或其盐。
[0624]
(xc)另一实施例涉及各示例性化合物的盐。
[0625]
本发明的化合物通过多种程序制备,其中许多程序已在本领域中描述。例如,参见 wo 2005/085216、wo 2007/079162、us 2007/066617、us20130131017、wo 2009/002809、 wo 2009/112275、wo 2010/003923、wo 2010/070068、wo 2012/120399和wo2013/079407。
[0626]
本公开涉及具有延长的半衰期的具有式(i)的化合物。具有式(i)的化合物在间位具有三氟甲基或在对位和/或邻位具有卤素。因此,具有式(i)的化合物包括以下特征:位于
一个或两个间位的三氟甲基;位于邻位的卤素;位于每个邻位和对位的卤素;或位于每个邻位的卤素和位于对位的三氟甲基。应当理解,具有式(i)的化合物可以具有其它取代基,但包括上述基团。不受任何特定理论的束缚,申请人相信在口服给药或注射后,在邻位和对位抑制代谢增强了持续时间。
[0627]
以下实例旨在说明而非限制,并代表本发明的具体实施例。
[0628]
[0629]
[0630]
[0631]
[0632][0633]
以及上述化合物的每种立体异构体。
[0634]
在另一方面,公开了具有式(ii)的化合物,或其盐,
[0635][0636]
其中,
[0637]
a1为-cf3或-chf2;
[0638]
cy1选自:
[0639][0640]
cy2选自:
[0641]
并且
[0642]
t1选自:
[0643]
[0644]
[0645][0646]
在一个实施例中,公开了具有式(iia)的化合物,或其盐,
[0647][0648]
其中a1、cy1、cy2和t1如上所定义。
[0649]
在另一实施例中,公开了具有式(iib)的化合物,或其盐,
[0650][0651]
其中a1、cy1、cy2和t1如上所定义。
[0652]
在某些实施例中,式(ii)、(iia)或(iib)中的a1为-cf3。
[0653]
在某些实施例中,式(ii)、(iia)或(iib)中的cy1为
[0654][0655]
在某些实施例中,式(ii)、(iia)或(iib)中的cy2为
[0656][0657]
在某些实施例中,式(ii)、(iia)或(iib)中的t1为
[0658][0659]
在某些实施例中,公开了具有式(ii)、(iia)和(iib)的化合物,或其盐,其中 a1为-cf3;
[0660]
cy1选自:
[0661][0662]
cy2为
[0663]
并且
[0664]
t1为
[0665]
[0666][0667]
在某些实施例中,公开了具有式(ii)、(iia)和(iib)的化合物,或其盐,其中
[0668]
a1为-cf3;
[0669]
cy1为
[0670][0671]
cy2选自:
[0672]
并且
[0673]
t1为
[0674]
[0675]
[0676][0677]
在某些实施例中,公开了具有式(ii)、(iia)和(iib)的化合物,或其盐,其中
[0678]
a1为-cf3;
[0679]
cy1为
[0680][0681]
cy2选自:
[0682]
并且
[0683]
t1为
[0684][0685]
在另一方面,公开了具有式(iii)的化合物,或其盐,
[0686][0687]
其中,
[0688]
a1为-cf3或-chf2;
[0689]
cy3选自:
[0690][0691]
cy4为:
[0692]
并且
[0693]
t2选自:
[0694][0695]
在一个实施例中,公开了具有式(iiia)的化合物,或其盐,
[0696][0697]
其中a1、cy3、cy4和t2如上所定义。
[0698]
在另一实施例中,公开了具有式(iiib)的化合物,或其盐,
[0699][0700]
其中a1、cy3、cy4和t2如上所定义。
[0701]
在某些实施例中,式(iii)、(iiia)或(iiib)中的a1为-cf3。
[0702]
在某些实施例中,式(iii)、(iiia)或(iiib)中的cy3为
[0703][0704]
在某些实施例中,式(iii)、(iiia)或(iiib)中的t2为
[0705][0706]
在某些实施例中,公开了具有式(iii)、(iiia)或(iiib)的化合物,或其盐,其中
[0707]
a1为-cf3;
[0708]
cy3为
[0709][0710]
cy4选自:
[0711]
并且
[0712]
t3为
[0713][0714]
以下实例旨在说明而非限制,并代表本发明的具体实施例。
[0715]
使用agilent 1200无限系列液相色谱(lc)系统进行分析,该系统由1260hip脱气器(g4225a)、1260二元泵(g1312b)、1290自动进样器(g4226a)、1290热稳定柱室(g1316c)和与agilent 6150单四极质谱(ms)检测器联接的1260二极管阵列检测器(g4212b)组成。默认将注射体积设定为1μl。在40hz下进行uv(dad)采集,扫描范围为190至400nm(5nm步长)。在ms检测器之前使用1:1分流。使用电喷雾电离源(esi)以正离子模式和负离子模式操作ms。喷雾器压力设定为345kpa,干燥气体温度和流量分别设定为350℃和12.0l/分钟。所使用的毛细管电压在正模式下为 4000v,在负模式下为3500v。在两种极性模式下,ms采集范围设定为100至800m/z,步长为0.2m/z。碎裂电压设定为70(esi+)或120(esi-),增益设定为0.40(esi+) 或1.00(esi-),离子计数阈值设定为4000(esi+)或1000(esi-)。总ms扫描周期时间为0.15秒/周期。使用agilent化学工作站软件进行数据采集。
[0716]
方法a:在50mm长、2.1mm内径和3μm粒度的phenomenex gemini-nx c18柱上进行分析。使用的流动相为:a=含0.1%甲酸的水/b=含0.1%甲酸的ch3cn。
[0717]
方法b:在50mm长、2.1mm内径和3.5μm粒度的waters xbridge c18柱上进行分析。使用的流动相为:a=含10mm碳酸氢铵的水,用氢氧化铵调节至ph 9/b=ch3cn。
[0718]
方法i:在50mm长、2.1mm内径和2.5μm粒度的waters xbridge beh c18上进行分析。使用的流动相为:a=含10mm乙酸铵的水/b=ch3cn。
[0719]
使用与waters sq detector 2单四极质谱(ms)检测器联接的waters acquity uplc 液相色谱(lc)系统进行分析。以200至400nm的扫描范围(1.2nm分辨率)进行uv (dad)采集。使用电喷雾电离源(esi)以正离子模式和负离子模式操作ms。毛细管电压3.50(kv),锥孔电压35(v),以及去溶剂化温度550℃。去溶剂化气流1000(l/ 小时),锥形气流50(l/小
时)。ms采集范围设定为100至1500m/z。ms扫描周期时间为0.5秒。用waters masslynx软件进行数据采集。
[0720]
方法c:在50mm长、2.1mm内径和1.7μm粒度的acquity uplc beh c18柱上进行分析。使用的流动相为:a=含0.1%甲酸的水/b=含0.1%甲酸的ch3cn。
[0721]
方法d:在50mm长、2.1mm内径和1.7μm粒度的acquity uplc beh c18柱上进行分析。使用的流动相为:a=含0.1%甲酸的水/b=ch3cn。
[0722]
方法e:在50mm长、2.1mm内径和1.7μm粒度的acquity uplc beh c18柱上进行分析。使用的流动相为:a=含10mm乙酸铵的水/b=ch3cn。
[0723]
方法h:在50mm长、2.1mm内径和1.6μm粒度的luna omega-ps c18柱上进行分析。使用的流动相为:a=含10mm乙酸铵的水/b=ch3cn。
[0724]
使用超高效液相色谱(uhplc)系统(make-thermo scientific),联接离子阱质量分析仪进行分析。以200至400nm的扫描范围(1nm分辨率)进行uv采集。使用电喷雾电离源(esi)以正离子模式和负离子模式操作ms,鞘气流速(arb):40,辅助气体流速(arb):20,吹扫气体流速(arb):1,喷雾电压(kv):5,毛细管温度(℃):350,毛细管电压(v):30,镜筒透镜(v):正模式30和负模式-30。ms采集范围设定为100至 2000m/z。ms扫描循环时间为3次微扫描。用xcalibur软件进行数据采集。
[0725]
方法f:在5cm长、2.1mm内径和2.7μm粒度的ascentis express c18上进行分析。使用的流动相为:a=含0.1%甲酸的水/b=100%ch3cn。
[0726]
方法g:在5cm长、2.1mm内径和2.7μm粒度的ascentis express c18上进行分析。使用的流动相为:a=含10mm乙酸铵的水/b=100%ch3cn。
[0727]
如本文所用:aq.是指含水的,br是指宽的,ch3cn是指乙腈,d是指二重峰,dd 是指双二重峰,dcm是指二氯甲烷,dce是指二氯乙烷,dipea是指n-二异丙基乙胺, dmf是指n,n-二甲基甲酰胺,dmso是指二甲亚砜,ee是指对映体过量,es是指电喷雾电离,etoac是指乙酸乙酯,h是指小时,hatu是指1-[双(二甲基氨基)亚甲基]-1h-1,2,3-三唑[4,5-b]吡啶3-氧化物,六氟磷酸盐,hplc是指高效液相色谱,iproh 是指异丙醇,j是指偶联常数,lcms是指液相色谱-质谱,m/z是指质荷比,m是指摩尔浓度,m是指多重峰,meoh是指甲醇,min是指分钟,nahco3是指碳酸氢钠,na2co3是指碳酸钠,net3是指三乙胺,nmr是指核磁共振,q是指四重峰,quint是指五重峰, rt是指室温,r
t
是指保留时间,s是指单峰,sat.是指饱和,t是指温度,t是指三重峰, td是指二重峰的三重峰,thf是指四氢呋喃,wt是指重量,并且δ是指化学位移。
[0728]
实例1.1和1.2
[0729]
2-甲基磺酰基-1-[6-[(5s或r)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]螺[1h-异苯并呋喃-3,3'-氮杂环丁烷]-1'-基]乙酮
[0730]
和
[0731]
2-甲基磺酰基-1-[6-[(5r或s)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]螺[1h-异苯并呋喃-3,3'-氮杂环丁烷]-1'-基]乙酮
[0732][0733]
在含有6-溴螺[1h-异苯并呋喃-3,3'-氮杂环丁烷]-1'-羧酸叔丁酯(8.86g,24.7mmol) 和n,n,n',n'-四甲基乙二胺(2.8ml,18mmol)于甲苯(50ml)中的溶液的压力容器中添加乙酸钯(ii)(286mg,1.21mmol)和丁基二-1-金刚烷基膦(1.42g,3.76mmol)。将容器密封,用n2气体冲洗三次,然后用co气体和氢气冲洗三次至310kpa的压力。将反应物加热至90℃,并搅拌过夜。使反应物冷却至室温,然后用n2气冲洗三次。将反应混合物通过过滤(用etoac冲洗)。将滤液真空浓缩,并且粗产物通过硅胶柱色谱(含0至20%etoac的环己烷)纯化,得到6-甲酰基螺[1h-异苯并呋喃-3,3'-氮杂环丁烷]-1'-羧酸叔丁酯。lc-ms(方法a)r
t
=1.10分钟,m/z=234.2[m-tbu+h]
+
。
[0734]
向含有6-甲酰基螺[1h-异苯并呋喃-3,3'-氮杂环丁烷]-1'-羧酸叔丁酯(6.57g,21.6 mmol)于meoh(110ml)中的搅拌溶液的烧瓶中缓慢添加nh2oh溶液(50%水溶液, 3ml,49.0mmol)。将反应物在室温下搅拌2小时。将反应物真空浓缩,并将所得固体置于真空烘箱中干燥过夜,得到6-(羟基亚氨基甲基)螺[1h-异苯并呋喃-3,3'-氮杂环丁烷]-1'-羧酸叔丁酯。lc-ms(方法a)r
t
=1.00分钟和1.02分钟,m/z=303.0[m-h]-(e/z 异构体的混合物)。
[0735]
在含有6-(羟基亚氨基甲基)螺[1h-异苯并呋喃-3,3'-氮杂环丁烷]-1'-羧酸叔丁酯(3.05 g,9.52mmol)于dmf(10ml)中的搅拌溶液的烧瓶中添加n-氯琥珀酰亚胺(1.54g, 11.3mmol)。将反应物搅拌30分钟。将反应冷却至0℃,并加入1-氯-2-氟-5-(三氟甲基)-3-[1-(三氟甲基)乙烯基]苯(2.96g,8.61mmol),然后缓慢加入net3(1.9ml,13 mmol)。使反应物升温至室温,并搅拌过夜。将反应物在etoac和盐水(各50ml)之间分配,并分离各层。用etoac(2
×
25ml)萃取含水层,并将合并的有机层真空浓缩。通过硅胶柱色谱(含0至15%etoac的环己烷)纯化粗产物,得到标题化合物6-[(外消旋)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]螺[1h-异苯并呋喃
ꢀ‑
3,3'-氮杂环丁烷]-1'-羧酸叔丁酯。lc-ms(方法a)r
t
=1.57分钟,m/z=539.0 [m-tbu+h]
+
。
[0736]
在0℃下向含有6-[(外消旋)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]螺[1h-异苯并呋喃-3,3'-氮杂环丁烷]-1'-羧酸叔丁酯(4g,6.38mmol)于dcm (60ml)中的搅拌溶液的烧瓶中缓慢添加tfa(5ml)。使反应物升温至室温,并在室温下搅拌过夜。将反应混合物真空浓缩,并将残余物在饱和nahco3水溶液和含10% meoh的dcm(各50ml)之间分配。分离各层,并用含10%meoh的dcm(2
×
50ml) 萃取含水层。将合并的有机层真空浓缩,得到6-[(外消旋)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]螺[1h-异苯并呋喃-3,3'-氮杂环丁烷]。lc-ms(方法a) r
t
=1.35分钟,m/z=495.0[m+h]
+
。
[0737]
向含有6-[(外消旋)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基] 螺[1h-异苯并呋喃-3,3'-氮杂环丁烷](3.94g,7.57mmol)和2-甲磺酰基乙酸(1.49g, 10.3mmol)于etoac(25ml)中的搅拌溶液的烧瓶中缓慢添加net3(1.5ml,11mmol)。将反应物冷却至0℃,并且经10分钟逐滴添加2,4,6-三丙基-1,3,5,2,4,6-三氧三磷酸-2,
4,6
‑ꢀ
三氧化物(50wt%于etoac中)(9.1ml,15mmol)。使反应物升温至室温,并搅拌过夜。将反应混合物用etoac(50ml)稀释,用nahco3水溶液(50ml)、盐水(100ml) 洗涤,并真空浓缩。将粗产物通过硅胶柱色谱(含20至70%etoac的环己烷)纯化,得到标题化合物。lc-ms(方法a)r
t
=1.36分钟,m/z=615.0[m+h]
+
。1h nmr(cdcl3, 400mhz)δ8.03(dd,j=2,6hz,1h),7.81(dd,1.6,6hz,1h),7.59-7.71(m,3h),5.17(s, 2h),4.64-4.70(m,2h),4.1-4.47(m,3h),3.87(m,3h)3.20(s,3h)。
[0738]
通过sfc分离两种对映异构体。在oj-h上进行分离,柱尺寸为250 mm
×
30mm(5μm),流速为175ml/分钟,并且co2基流动相为含有0.2%n,n-二甲基乙胺作为添加剂的12%iproh,得到实例1.1:2-甲基磺酰基-1-[6-[(5s或r)-5-[3-氯-2
‑ꢀ
氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]螺[1h-异苯并呋喃-3,3'-氮杂环丁烷]-1'-基]乙酮,和实例1.2:2-甲基磺酰基-1-[6-[(5r或s)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]螺[1h-异苯并呋喃-3,3'-氮杂环丁烷]-1'-基]乙酮。
[0739]
实例2.1和2.2
[0740]
n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5s或r)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]萘-1-甲酰胺
[0741]
和
[0742]
n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5r或s)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]萘-1-甲酰胺
[0743][0744]
将圆底压力烧瓶中的4-溴-1-萘甲醛(3.04g,12.31mmol)于1,4-二噁烷(30ml) 和meoh(30ml)中的溶液用net3(36.6mmol,5.10ml)和[1,1'-双(二苯基膦基)二茂铁]二氯化钯(ii)(0.95g,1.23mmol)处理,然后在90℃下在co气氛(380kpa)下搅拌过夜。将反应混合物直接稀释到硅胶上并进行硅胶柱色谱(含0至15%etoac的环己烷),得到4-甲酰基萘-1-羧酸甲酯。lc-ms(方法a)r
t
=1.06分钟,m/z=215.0[m+h]
+
。
[0745]
将烧瓶中的4-甲酰基萘-1-羧酸甲酯(2.52g,11.2mmol)于thf(50ml)中的溶液用naoh水溶液(2m,52.0g,100mmol)处理,并在室温下搅拌4小时。将反应混合物用浓hcl酸化至ph~1,并用dcm(3
×
40ml)萃取。将合并的有机层通过并真空浓缩,得到4-甲酰基萘-1-羧酸。lc-ms(方法a)r
t
=0.36分钟,m/z=199.0[m-h]-。
[0746]
将4-甲酰基萘-1-所述(2.54g,10.8mmol,85%)于dcm(55ml)中的悬浮液置于n2气氛下,并用dmf(0.02ml)处理。然后将所得混合物用草酰氯(13.8mmol, 1.20ml)缓慢处理,并在室温下进一步搅拌30分钟。将反应混合物真空浓缩,并直接用于下一步骤。将4-甲酰基萘-1-碳酰氯(2.36g,10.8mmol)和2-氨基-n-(2,2,2-三氟乙基)乙酰胺
·
hcl(2.14g,10.9mmol)的混合物置于n
2-气氛下,并用dcm(55ml) 和dipea(29mmol,5.0ml)处理。将反应混合物用hcl溶液(2m,40ml)稀释,并分离两层。用dcm(2
×
30ml)萃取水性层,并将合并的有
机层通过并在真空中浓缩,然后经受硅胶柱色谱(含60至80%etoac的环己烷),以获得4-甲酰基-n-[2
‑ꢀ
氧代-2-(2,2,2-三氟乙基氨基)乙基]萘-1-甲酰胺。lc-ms(方法a)r
t
=0.86分钟,m/z= 339.0[m+h]
+
。
[0747]
将4-甲酰基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]萘-1-甲酰胺(3.05g,8.55mmol) 于etoh(45ml)中的悬浮液置于n2气氛下,用nh2oh溶液(50%水溶液,3ml,49.0 mmol)处理,并在室温下搅拌4小时。将反应混合物真空浓缩,得到4-(羟基亚氨基甲基)-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]萘-1-甲酰胺。lc-ms(方法a)r
t
=0.77分钟,m/z=354.0[m+h]
+
。
[0748]
向配有冷凝器的烧瓶中加入[3-氯-2-氟-5-(三氟甲基)苯基]硼酸(6.1g,24.41mmol) 和xphos pd(巴豆基)cl(pd-170)(537mg,0.76mmol)。将烧瓶用n2气体冲洗,然后加入thf(50ml),随后加入磷酸三钾(10.9g,49.8mmol)于水(100ml)中的脱气溶液。加入2-溴-3,3,3-三氟-丙-1-烯(4.0ml,37mmol),将反应物加热至70℃并搅拌1 小时。使反应物冷却至室温,分离各层。用et2o(2
×
50ml)萃取水性层,将合并的有机层通过过滤,并在真空中除去溶剂。通过硅胶柱色谱(等度异己烷)纯化粗产物,得到1-氯-2-氟-5-(三氟甲基)-3-[1-(三氟甲基)乙烯基]苯。lc-ms(方法a)r
t
=1.45 分钟(无电离)。
[0749]
将4-(羟基亚氨基甲基)-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]萘-1-甲酰胺(1.54g, 3.71mmol)和n-氯代琥珀酰亚胺(0.63g,4.59mmol)的混合物置于n2气氛下,并用 dmf(7.5ml)处理。将所得溶液温热至40℃,并搅拌10分钟。lc-ms(方法a)r
t
=0.88 分钟,m/z=350.0[m-h]-。将反应混合物在冰上冷却,并用1-氯-2-氟-5-(三氟甲基)-3-[1-(三氟甲基)乙烯基]苯(1.29g,3.76mmol)和net3(5.7mmol,0.80ml)处理。然后除去冰浴,将反应混合物搅拌4小时。将反应混合物用饱和nahco3水溶液(60ml) 稀释,并用叔丁基甲基醚(3
×
30ml)萃取。合并的有机层经无水mgso4干燥,过滤并真空浓缩。通过硅胶柱色谱(含40至75%etoac的环己烷)纯化残余物,得到标题化合物。lc-ms(方法a)r
t
=1.39分钟,m/z=644.0[m+h]
+
。1h-nmr(dmso-d6,400mhz) δ8.95(t,j=6hz,1h),8.79(d,j=8hz,1h)8.71(t,j=6.4hz,1h),8.39(d,j=7.6hz, 2h),7.94-8.01(m,2h),7.64-7.74(m,3h),4.70(m,2h),4.4-3.95(m,4h)。
[0750]
通过sfc分离两种对映异构体。在oj-h上进行分离,柱尺寸为250 mm
×
30mm(5μm),流速为120ml/分钟,并且基于co2的流动相为含有0.2%n,n-二甲基乙胺作为添加剂的10%meoh,得到实例2.1:n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5s或r)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]萘-1-甲酰胺,以及实例2.2:n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5r或s)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]萘-1-甲酰胺。
[0751]
实例3.1和3.2
[0752]
2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5s或r)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺
[0753]
和
[0754]
2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5r或s)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺
[0755][0756]
将4-溴-2-甲基-苯甲酸甲酯(10.0g,42.3mmol)、n,n,n',n'-四甲基乙二胺(3.96ml, 26.3mmol)、乙酸钯(ii)(0.5g,2.12mmol)、丁基二-1-金刚烷基膦(2g,5.29mmol) 和甲苯(65ml)的混合物装入压力容器中。将反应物用co气体(~414kpa)加压,并加热至85℃过夜。将反应物冷却至室温。反应混合物通过过滤,用甲苯洗涤,减压除去溶剂。将得到的残余物通过硅胶柱色谱(含0至10%etoac的环己烷)纯化,得到4-甲酰基-2-甲基-苯甲酸甲酯。lc-ms(方法a)r
t
=0.95分钟(无电离)。
[0757]
将含4-甲酰基-2-甲基-苯甲酸甲酯(2.05g,11.2mmol)的meoh(65ml)和含 naoh的水(2m,65ml)的混合物在室温下搅拌5小时。将反应混合物用浓hcl酸化直至ph~1。将反应物用etoac稀释,分离有机层,并将含水层用etoac用洗涤。然后合并有机层,用无水mgso4干燥,过滤,并真空浓缩,得到4-甲酰基-2-甲基-苯甲酸。 lc-ms(方法b)r
t
=0.71分钟,m/z=163.0[m-h]-。
[0758]
在室温下,在n2气氛下将dmf(25μl)添加至4-甲酰基-2-甲基-苯甲酸(1.8g, 10.4mmol)和草酰氯(995μl,11.5mmol)于dcm(35ml)中的悬浮液中。将反应物在室温下搅拌3小时。将反应混合物浓缩,得到粗酰氯。在0℃下将2-氨基-n-n-(2,2,2
‑ꢀ
三氟乙基)乙酰胺
·
hcl(2.25g,11.5mmol)和net3(3.2ml,23mmol)于dcm(35ml) 中的溶液添加至粗酰氯,然后将反应物升温至室温并搅拌30分钟。将反应物用dcm/ 水稀释,收集有机层,并减压除去溶剂。通过硅胶柱色谱(含0至10%meoh的dcm) 纯化粗产物,得到4-甲酰基-2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]苯甲酰胺。 lc-ms(方法a)r
t
=0.69分钟,m/z=303.0[m+h]
+
。
[0759]
将nh2oh溶液(32.6m的水溶液,385μl,6.28mmol)添加到含4-甲酰基-2-甲基
ꢀ‑
n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]苯甲酰胺(1.00g,3.14mmol)的meoh(15ml) 中,并将反应物在室温下搅拌6小时。减压除去溶剂,得到4-[(e和z)-羟基亚氨基甲基]-2
‑ꢀ
甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]苯甲酰胺。lc-ms(方法b)r
t
=0.68分钟和0.70分钟,m/z=318.0[m+h]
+
。
[0760]
向4-[(e和z)-羟基亚氨基甲基]-2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]苯甲酰胺(1.08g,3.16mmol,)于dmf(3.34ml)中的溶液中加入n-氯代琥珀酰亚胺(548 mg,4.10mmol),并将反应物加热至40℃持续15分钟。将反应物冷却至0℃,加入1
‑ꢀ
氯-2-氟-5-(三氟甲基)-3-[1-(三氟甲基)乙烯基]苯(1.03g,3.15mmol),然后添加net3(484 μl,3.47mmol)。将反应物在室温下搅拌。将反应物用etoac和盐水稀释。分离有机层并用更多的盐水洗涤,用无水mgso4干燥,过滤,并减压浓缩。将粗产物通过硅胶柱色谱(含0至60%etoac的环己烷)纯化,得到标题化合物。lc-ms(方法a)r
t
=1.38 分钟,m/z=608.0[m+h]
+
。1h nmr(cdcl3,400mhz)δ8.04(dd,j=2,6hz,1h),7.81 (dd,j=2,6hz,1h),7.47-7.56(m,3h),6.90(br s,1h),6.71(br s,1h),4.18-4.23(m,3 h),3.84-4.00(m,3h),2.48(s,3h)。
[0761]
在as-h上通过sfc分离两种对映异构体,柱尺寸为250mm
×
30mm(5 μ
m),流速为152ml/分钟,并且基于co2的流动相为含有0.2%n,n-二甲基乙胺作为添加剂的10%meoh,得到实例3.1:2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5s 或r)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺,以及实例 3.2:2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5r或s)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺。
[0762]
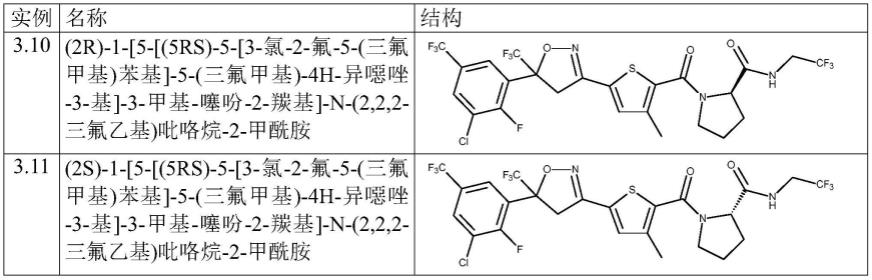
通过实例3.1和3.2的方法类似地制备以下化合物:
[0763]
[0764]
[0765]
[0766]
[0767]
[0768]
[0769]
[0770]
[0771]
[0772]
[0773][0774]
实例3.9
[0775]
3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-5-[(5rs)-5-(三氟甲基)-5-(2,4,6-三氟苯基)-4h-异噁唑-3-基]噻吩-2-甲酰胺
[0776][0777]
将2,4,6-三氟溴苯(1.00g,4.76mmol)溶解于干燥et2o(5ml)中,并冷却至-78℃。
经30分钟逐滴添加n-buli于thf中溶液(3.25ml,5.2mmol,1.6m),且将所得溶液在-78℃下搅拌1小时。然后立刻加入三氟乙酸乙酯(675mg,4.76mmol)于et2o(5 ml)中的溶液,并将反应物在-78℃搅拌20分钟,并在-40℃再搅拌40分钟。然后滴加已经制备的2,2,2-三氟-1-(2,4,6-三氟苯基)乙-1-酮(866mg,3.8mmol)和lihmds (6.6ml,6.6mmol)于干燥et2o(5ml)中的冷却(-78℃)溶液,并将所得反应混合物搅拌4h,其中使其升温至室温。将反应混合物通过加入饱和nh4cl水溶液进行淬灭,并用etoac萃取。将合并的有机层用盐水洗涤,经无水na2so4干燥,过滤,并真空浓缩。获得呈淡黄色液体状的1-(5-溴-4-甲基-2-噻吩基)-4,4,4-三氟-3-羟基-3-(2,4,6-三氟苯基)丁-1-酮,且不经进一步纯化即用于下一步骤中。lc-ms(方法e)r
t
=2.88分钟,m/z =447.2/449.1[m+h]
+
。
[0778]
将1-(5-溴-4-甲基-2-噻吩基)-4,4,4-三氟-3-羟基-3-(2,4,6-三氟苯基)丁-1-酮(800mg, 1.79mmol)和吡啶(0.578ml,7.16mmol)于dcm(10ml)中的混合物在冰浴中冷却至0℃。然后,在0℃滴加socl2(0.43ml,3.58mmol)。移除冰浴,并将反应混合物在室温下搅拌4小时。此后,缓慢加入饱和nh4cl水溶液。分离含水层,并用dcm (3
×
)萃取。将合并的有机层用盐水洗涤,经无水na2so4干燥,过滤,并真空浓缩。获得呈淡黄色液体状的所需产物,且不经进一步纯化即用于下一步骤中。lc-ms(方法c) r
t
=2.52和2.56分钟(e/z异构体的混合物),m/z=429.1/431.1[m+h]
+
。
[0779]
在室温下向以上1-(5-溴-4-甲基噻吩-2-基)-4,4,4-三氟-3-(2,4,6-三氟苯基)丁-2-烯-1
‑ꢀ
酮(450mg,1.05mmol)于dce(10ml)中的溶液中添加nh2oh溶液(50%水溶液, 52mg,1.57mmol)和dbu(0.319mg,2.10mmol)。将混合物在室温下搅拌3小时。此后,加入水,分离含水层,并用dcm(3
×
)萃取。将合并的有机层用盐水洗涤,经无水na2so4干燥,过滤,并真空浓缩。获得呈淡黄色固体的3-(5-溴-4-甲基噻吩-2
‑ꢀ
基)-5-(2,4,6-三氟苯基)-5-(三氟甲基)-异噁唑,且不经进一步纯化即用于下一步骤中。 lc-ms(方法c)r
t
=2.53分钟,m/z=444.1/449.1[m+h]
+
。
[0780]
在n2气氛下在0℃将3-(5-溴-4-甲基噻吩-2-基)-5-(2,4,6-三氟苯基)-5-(三氟甲基)-异噁唑(220mg,485μmol)溶解于thf(5ml)中。滴加iprmgcl于thf中的溶液(0.77 ml,1.49mmol,2m),并将该混合物在0℃在冰浴中搅拌30分钟。然后,在0℃下将 co2气体鼓泡通过溶液1小时。将反应物通过添加hcl水溶液(1m)进行淬灭。分离含水层,并用etoac(3
×
)萃取。将合并的有机层用盐水洗涤,经无水na2so4干燥,过滤,并真空浓缩。获得呈黄色液体状的所需产物,且不经进一步纯化立即用于下一步骤中。lc-ms(方法c)r
t
=2.53分钟,m/z=410.1[m+h]
+
。
[0781]
将以上3-甲基-5-(5-(三氟甲基)-5-(2,4,6-三氟苯基)-4,5-二氢异噁唑-3-基)噻吩-2-羧酸(200mg,0.49mmol)、pybop(307mg,0.59mmol)和net3(144mg,1.47mmol)) 在dmf(10ml)中混合,并在冰浴中冷却至0℃。然后在0℃加入2-氨基-n-(2,2,2-三氟乙基)乙酰胺(92mg,0.59mmol)。移除冰浴,并将反应混合物在室温下搅拌4小时。此后,加入冷水。分离含水层,并用etoac(3
×
)萃取。将合并的有机层用盐水洗涤,经无水na2so4干燥,过滤,并真空浓缩。将粗产物通过硅胶柱色谱(含5至14%etoac 的石油醚)纯化,得到实例3.9:呈无色固体的3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基) 乙基]-5-[(5rs)-5-(三氟甲基)-5-(2,4,6-三氟苯基)-4h-异噁唑-3-基]噻吩-2-甲酰胺。lc-ms (方法d)r
t
=2.07分钟,m/z=546.1[m-h]-。1h-nmr(dmso-d6,400mhz)δ8.61(br s, 1h),8.38(br s,1h),7.53(s,1h),
7.41(t,j=9.6hz,2h),4.42(q,j=18hz,2h), 3.98-3.87(m,4h),2.43(s,3h)。
[0782]
实例3.56
[0783]
3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-5-[(5rs)-5-[2,4-二氟-5-(三氟甲基) 苯基]-5-(三氟甲基)-4h-异噁唑-3-基]噻吩-2-甲酰胺
[0784][0785]
向5-溴-4-甲基-噻吩-2-甲醛(4.74g,22.7mmol)于meoh(113ml)的溶液中逐滴加入nh2oh溶液(50%水溶液,2.7ml,44mmol)。将反应物在室温下搅拌4.5小时。此后,将反应物真空浓缩,并将得到的固体在真空烘箱中干燥,得到呈奶油色固体的5
‑ꢀ
溴-4-甲基-噻吩-2-甲醛肟。lc-ms(方法a)r
t
=0.99和1.02分钟,m/z=217.6/219.6[m+h]
+ (e/z异构体的混合物)。
[0786]
将2-[2,4-二氟-5-(三氟甲基)苯基]-4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷(2.75g,5.80 mmol)、甲磺酸(2-二环己基膦-2',4',6'-三-异丙基-1,1'-联苯)(2'-甲基氨基-1,1'-联苯-2-基) 钯(ii)(256mg,292μmol)和2-溴-3,3,3-三氟丙烯(2.53g,14.5mmol)的混合物置于n2气氛下,并用磷酸钾(0.5m水溶液,11.0mmol,22ml)和thf(11ml)处理。将所得反应混合物在70℃搅拌30分钟。使反应混合物冷却至室温,且用水(30ml)稀释,并用dcm(3
×
25ml)萃取。将合并的有机层用无水na2so4干燥,过滤,并减压浓缩。通过硅胶柱色谱(100%异己烷)纯化粗产物,得到呈无色油状物的1,5-二氟-2-(三氟甲基)-4-[1-(三氟甲基)乙烯基]苯。lc-ms(方法a)r
t
=1.37分钟(未观察到显著的质量离子)。
[0787]
将上述5-溴-4-甲基-噻吩-2-甲醛肟(950mg,4.10mmol)和n-氯代琥珀酰亚胺(0.73 g,5.36mmol)的混合物置于n2气氛下,用dmf(3.0ml)处理,并在40℃下搅拌5 分钟,在此期间形成亮黄色沉淀。将反应混合物在冰浴中冷却至0℃,并用上述1,5-二氟-2-(三氟甲基)-4-[1-(三氟甲基)乙烯基]苯(1.34g,4.12mmol)处理。然后缓慢加入 net3(0.47g,4.6mmol),将得到的混合物在0℃搅拌10分钟,然后在室温再搅拌30 分钟。将反应混合物用饱和nahco3水溶液(40ml)稀释,并用dcm(3
×
25ml)萃取。将合并的有机层减压浓缩。残余物通过硅胶柱色谱(含0至10%叔丁基甲基醚的环己烷)纯化,得到呈淡黄色半固体状的3-(5-溴-4-甲基-2-噻吩基)-5-[2,4-二氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑。lc-ms(方法a)r
t
=1.64分钟,m/z=493.8/495.8 [m+h]
+
。
[0788]
将3-(5-溴-4-甲基-2-噻吩基)-5-[2,4-二氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑(851mg,1.29mmol)于thf(6.5ml)中的溶液置于n2气氛下,在冰浴中冷却至 0℃,并用iprmgcl于thf中的溶液(1.3ml,2.6mmol,2.0m)处理。将所得混合物在0℃下搅拌30分钟。然后将co2气体鼓泡通过反应混合物15分钟。此后,将反应混合物用2m hcl溶液酸化至ph~2,然后用dcm(3
×
15ml)萃取。合并的有机层经无水na2so4干燥,过滤,并真空浓缩。将残余物溶解于meoh中,过滤,并通过制备型 hplc(phenomenex gemini-nx 10微米50*150mm c-18)(ch3cn、水-两者均含有0.1%甲酸,30至100%ch3cn,历时11分钟,120ml/分钟)
纯化(2次注射)。从主峰获得呈乳白色固体的5-[5-[2,4-二氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-3-甲基
ꢀ‑
噻吩-2-甲酸。lc-ms(方法a)r
t
=1.02分钟,m/z=458.0[m-h]-。
[0789]
将5-[5-[2,4-二氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-3-甲基-噻吩-2
‑ꢀ
甲酸(154mg,318μmol)、2-氨基-n-(2,2,2-三氟乙基)乙酰胺
·
hcl(96.0mg,473μmol) 和pybop(254mg,488μmol)的混合物置于n2气氛下,并用thf(1.6ml)和net
3 (94.4mg,933μmol,0.13ml)处理,然后在室温下搅拌30分钟。将反应混合物用饱和nahco3水溶液(20ml)稀释,并用dcm(3
×
10ml)萃取。合并的有机层经无水 na2so4干燥,过滤,并真空浓缩。将残余物溶解于meoh(加~1ml dmf)中,过滤,并通过制备型hplc(phenomenex gemini-nx 10微米50*150mm c-18)(ch3cn,含有 10mm碳酸氢铵的水,用氢氧化铵调节至ph 9,30至100%ch3cn,历时10分钟,120 ml/分钟)纯化(1次注射)。实例3.56:从主峰获得呈无色固体的3-甲基-n-[2-氧代-2-(2,2,2
‑ꢀ
三氟乙基氨基)乙基]-5-[外消旋-(5r)-5-[2,4-二氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]噻吩-2-甲酰胺。lc-ms(方法a)r
t
=1.33分钟,m/z=598.0[m+h]
+
。1h-nmr (dmso-d6,400mhz)δ8.62(t,j=6hz,1h),8.38(t,j=5.6hz,1h),7.92-7.97(m,2h), 7.49(s,1h),4.30-4.55(m,2h),3.89-3.97(m,4h),2.43(s,3h)。
[0790]
实例4.1和4.2
[0791]
3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-5-[(5s或r)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]噻吩-2-甲酰胺
[0792]
和
[0793]
3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-5-[(5r或s)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]噻吩-2-甲酰胺
[0794][0795]
在n
2-气氛下将5-溴-4-甲基-噻吩-2-甲醛肟(3.36g,14.5mmol)和n-氯代琥珀酰亚胺(2.74g,20.1mmol)的混合物合并在dmf(11ml)中。将所得溶液温热至40℃并搅拌5分钟,在这段时间内观察到亮黄色沉淀物。将混合物在冰浴中冷却至0℃,并用1-氯-2-氟-5-(三氟甲基)-3-[1-(三氟甲基)乙烯基]苯(4.35g,11.2mmol)处理,然后缓慢加入net3(2.40ml,17.0mmol)。当net3的添加完成时,移除冰浴,并将反应混合物在室温下搅拌15分钟。将反应混合物在室温下再搅拌30分钟,然后用naoh溶液(1m, 60ml)稀释,并用叔丁基甲基醚(3
×
40ml)萃取。将合并的有机层经无水mgso4干燥,过滤,并真空浓缩。所得残余物通过硅胶柱色谱(含0至10%dcm的环己烷)纯化,得到呈无色固体状的3-(5-溴-4-甲基-2-噻吩基)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑。lc-ms(方法b):r
t
=1.65分钟,m/z=509.8[m+h]
+
。
[0796]
将3-(5-溴-4-甲基-2-噻吩基)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑(2.84g,5.28mmol)于thf(26ml)中的溶液置于n2气氛下,在冰浴中冷却至0
℃,并用iprmgcl于thf中的溶液(2.0m,5.50ml,11mmol)处理,然后搅拌30分钟。然后,将二氧化碳(232mg,5.28mmol)鼓泡通过反应混合物15分钟。然后将反应混合物用hcl溶液(2m,40ml)处理,并用dcm(3
×
30ml)萃取。将合并的有机层用饱和nahco3水溶液(20ml)洗涤,并且用dcm(2
×
20ml)反萃取含水层。将合并的有机层用无水mgso4干燥,过滤,并真空浓缩,得到呈浅黄色固体的3-甲基-5-[外消旋-(5r)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]噻吩-2-羧酸。 lc-ms(方法b)r
t
=1.06分钟,m/z=473.8[m-h]-。
[0797]
将5-[5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-3-甲基-噻吩-2
‑ꢀ
羧酸(2.48g,4.17mmol)、2-氨基-n-(2,2,2-三氟乙基)乙酰胺
·
hcl和pybop(3.26g, 6.27mmol)的混合物置于n
2-气氛下,并用thf(20ml)和net3(1.31g,12.9mmol) 处理。将所得混合物在室温下搅拌30分钟。然后将反应混合物用nahco3水溶液(40ml) 稀释,并用dcm(3
×
40ml)萃取。合并的有机层经无水mgso4干燥,过滤并真空浓缩。将粗产物通过硅胶柱色谱(含0至50%etoac的环己烷)纯化,得到所需产物。 lc-ms(方法b)r
t
=1.40分钟,m/z=614.0[m+h]
+
。1h-nmr(dmso-d6,400mhz)δ 8.62(t,j=6hz,1h),8.35(m,2h),7.87-7.87(m,1h),7.50(s,1h),4.38-4.59(m,2h), 3.89-3.97(m,4h),2.43(s,3h)。
[0798]
通过sfc分离两种对映异构体。在oj-h上进行分离,柱尺寸为250 mm
×
30mm(5μm),流速为160ml/分钟,并且基于co2的流动相为含有0.2%n,n-二甲基乙胺作为添加剂的6%meoh,得到实例4.1:3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-5-[(5s或r)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]噻吩
ꢀ‑
2-甲酰胺,以及实例4.2:3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-5-[(5r或 s)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]噻吩-2-甲酰胺。
[0799]
通过实例4.1和4.2的方法类似地制备以下化合物:
[0800]
氯-2-氟-5-(三氟甲基)苯基]-2,2-二氟-乙酮(5.84g,21.1mmol)于thf (5ml)中的溶液逐滴添加至反应混合物中,并维持1小时。使反应混合物在16小时内升温至室温。将反应物在-10℃下用饱和nh4cl水溶液(20ml)淬灭,并用etoac(2
×
80 ml)萃取。将合并的有机层用盐水(70ml)洗涤,经无水na2so4干燥并减压浓缩,得到粗品1-(4-溴-3-甲基-苯基)-3-[3-氯-2-氟-5-(三氟甲基)苯基]-4,4-二氟-3-羟基-丁-1
‑ꢀ
酮,将其通过硅胶柱色谱(含5%etoac的石油醚)纯化。
[0807]
在0℃下向1-(4-溴-3-甲基-苯基)-3-[3-氯-2-氟-5-(三氟甲基)苯基]-4,4-二氟-3-羟基
‑ꢀ
丁-1-酮(1.0g,2.04mmol)于干燥dcm(10ml)中的搅拌溶液中添加吡啶(0.64g, 8.16mmol),随后逐滴添加socl2(0.3ml,4mmol)。将反应混合物在0℃搅拌1小时。将反应物用水(25ml)淬灭,并用etoac(2
×
20ml)萃取。将合并的有机层用盐水(35 ml)洗涤,经无水na2so4干燥并减压浓缩,得到(z)-1-(4-溴-3-甲基-苯基)-3-[3-氯-2-氟
ꢀ‑
5-(三氟甲基)苯基]-4,4-二氟-丁-2-烯-1-酮,其不经进一步纯化即用于下一步骤。lc-ms (方法b)r
t
=3.06和3.13分钟,m/z=469.0[m-h]-。
[0808]
在0℃向(z)-1-(4-溴-3-甲基-苯基)-3-[3-氯-2-氟-5-(三氟甲基)苯基]-4,4-二氟-丁-2-烯
ꢀ‑
1-酮(1.0g,2.12mmol)于干燥dce(10ml)中的搅拌溶液中加入nh2oh溶液(50%水溶液,0.58g,8.48mmol),然后滴加dbu(0.645g,4.20mmol)。使反应混合物在1 小时内升温至室温。将反应物用水(30ml)淬灭,并用etoac(2
×
20ml)萃取。将合并的有机层用盐水(30ml)洗涤,经无水na2so4干燥并减压浓缩。通过硅胶柱色谱(含 2%etoac的石油醚)纯化粗混合物,得到3-(4-溴-3-甲基-苯基)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(二氟甲基)-4h-异噁唑。lc-ms(方法b)r
t
=2.66分钟,m/z=487.9[m+h]
+
。
[0809]
将3-(4-溴-3-甲基-苯基)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(二氟甲基)-4h-异噁唑 (0.80g,1.64mmol)和naoac(0.27g,3.28mmol)于无水meoh(10ml)中的搅拌溶液用n2气体脱气5分钟,并加入pd(dppf)cl2(0.24g,0.32mmol)。将反应混合物转移到高压釜中,并在100℃下在co气体氛围下在500psi压力下搅拌20小时。将反应混合物通过塞过滤,并用meoh(10ml)洗涤。减压蒸发滤液。将粗产物通过硅胶柱色谱(含50至90%etoac的石油醚)纯化,得到4-[5-[3-氯-2-氟-5-(三氟甲基) 苯基]-5-(二氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸甲酯。lc-ms(方法b)r
t
=2.56分钟,m/z=466.4[m+h]
+
。
[0810]
向4-[5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(二氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸甲酯(0.8g,1.71mmol)于thf:水(1:1,10ml)中的溶液中加入lioh
·
h2o(0.288 g,6.87mmol),并将得到的混合物在70℃搅拌6小时。将反应混合物减压浓缩,将残余物用2.5ml水稀释,并用hcl溶液(1m)酸化直至ph~6。将含水层用etoac(2
×
50 ml)萃取,并将合并的有机层用盐水(100ml)洗涤,用无水na2so4干燥,并减压浓缩,得到4-[5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(二氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸。lc-ms(方法b)r
t
=2.30分钟,m/z=452.3[m+h]
+
。
[0811]
向4-[5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(二氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸 (0.2g,0.44mmol)于干燥dmf(3ml)中的溶液中添加dipea(0.193ml,1.10mmol) 和hatu(0.2g,0.53mmol),并将所得混合物在室温下搅拌10分钟。添加2-氨基
ꢀ‑
n-(2,2,2-三氟乙基)乙酰胺(0.083g,0.53mmol)于干燥dmf(1ml)中的溶液,且将所得反应混合物在室温下搅拌16小时。将反应混合物用冷水(10ml)淬灭,并用etoac (2
×
15ml)萃取。将合并的
有机层用无水na2so4干燥,过滤,并减压浓缩。通过硅胶柱色谱(含30至70%etoac的石油醚)纯化粗混合物,得到实例5.1:(rs)-4-[5-[3-氯
ꢀ‑
2-氟-5-(三氟甲基)苯基]-5-(二氟甲基)-4h-异噁唑-3-基]-2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]苯甲酰胺。lc-ms(方法b)r
t
=2.19分钟,m/z=590.2[m+h]
+
。1h-nmr (dmso-d6,400mhz)δ8.65-8.58(m,2h),8.27(dd,j=6,2hz,1h),7.84(dd,j=6,2hz, 1h),7.64-7.59(m,2h),7.49(d,j=8hz,1h),6.54(t,j=54hz,1h),4.18(q,j=18hz, 2h),4.0-3.89(m,4h),2.40(s,3h)。
[0812]
实例6.1和6.2
[0813]
4-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-6-[(5r或s)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]哒嗪-3-甲酰胺
[0814]
和
[0815]
4-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-6-[(5s或r)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]哒嗪-3-甲酰胺
[0816][0817]
在100ml钢瓶中,将3,6-二溴-4-甲基哒嗪(4.00g,15.9mmol)和et3n(6.69ml, 47.6mmol)于meoh(40ml)中的混合物用n2气体脱气10分钟,然后加入pd(dppf)cl
2 (1.16g,1.59mmol)。然后将反应混合物在65℃在co气体压力(~60psi)下加热16 小时。使反应混合物通过(用etoac(2
×
30ml)洗涤。将合并的滤液减压浓缩。将粗产物通过硅胶柱色谱(含20%etoac的石油醚)纯化,得到呈黄色固定的6-溴-5
‑ꢀ
甲基哒嗪-3-羧酸甲酯。
[0818]
在0℃下向6-溴-5-甲基哒嗪-3-羧酸甲酯(3.30g,14.3mmol)于meoh(28ml) 和dcm(7ml)中的溶液中分批添加nabh4(1.08g,28.6mmol),并将所得反应混合物在室温下搅拌3小时。将反应混合物减压浓缩,并将残余物溶解于etoac(50ml) 中。有机层用hcl水溶液(0.1m,30ml)、盐水(30ml)洗涤,经无水na2so4干燥,过滤,并减压浓缩。将粗产物通过硅胶柱色谱(含0至100%etoac石油醚)纯化,得到呈黄色固体的(6-溴-5-甲基哒嗪-3-基)甲醇。lc-ms(方法c)r
t
=0.99分钟,m/z= 203.1[m+h]
+
。
[0819]
在0℃向(6-溴-5-甲基哒嗪-3-基)甲醇(1.70g,8.37mmol)于氯仿(30ml)中的搅拌溶液中分批加入mno2(7.30g,83.7mmol)。然后使反应混合物升温至室温,并搅拌2小时。通过用etoac(2
×
20ml)洗过的垫过滤反应混合物。将合并的滤液减压浓缩,得到6-溴-5-甲基哒嗪-3-甲醛,其不经纯化立即用于下一步骤。lc-ms(方法e)r
t
=1.08分钟,m/z=202.9[m+h]
+
。
[0820]
向6-溴-5-甲基哒嗪-3-甲醛(1.30g,6.47mmol)于meoh(6ml)中的搅拌溶液中添加nh2oh溶液(50%水溶液,6ml),并将所得混合物在室温下搅拌16小时。此后,减压浓缩反应混合物。加入饱和nahco3水溶液(2
×
20ml),并将混合物用etoac (3
×
25ml)萃取。将合并的有机层用盐水洗涤,用无水na2so4干燥,并减压浓缩。将粗化合物通过硅胶柱色谱(含10%etoac的石油醚)纯化,得到呈褐色半固体的6-溴-5
‑ꢀ
甲基哒嗪-3-甲醛肟。lc-ms(方法d)r
t
=1.12分钟,m/z=216.1[m+h]
+
。
[0821]
在0℃在冰浴中向6-溴-5-甲基哒嗪-3-甲醛肟(315mg,1.46mmol)于dmf(4ml) 中的搅拌溶液中加入ncs(253mg,1.90mmol),然后将混合物在40℃搅拌30分钟。然后将反应物在冰浴中冷却至0℃,并滴加net3(0.22ml,1.60mmol)和1-氯-2-氟-5-(三氟甲基)-3-(3,3,3-三氟丙-1-烯-2-基)苯(512mg,1.75mmol)。使混合物缓慢升温至室温并搅拌3小时。将反应混合物通过加入水(15ml)淬灭,然后用etoac(3
×
20ml)萃取。将合并的有机层用盐水洗涤,用无水na2so4干燥,然后减压浓缩。将粗产物通过硅胶柱色谱(含5%etoac的石油醚)进行纯化,得到呈褐色半固体的3-(6-溴-5-甲基
‑ꢀ
哒嗪-3-基)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑。lc-ms(方法d) r
t
=2.66分钟,m/z=506.1[m+h]
+
。
[0822]
在100ml钢瓶中,将3-(6-溴-5-甲基-哒嗪-3-基)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑(200mg,395mmol)于meoh(10ml)中的混合物和et3n (0.16ml,1.18mmol)用n2气体脱气10分钟,然后加入pd(dppf)cl2(29.0mg,39.4mmol)。然后将反应混合物在70℃下在co气体压力(~120psi)下在压力容器中加热16小时。将反应混合物通过过滤,用etoac(2
×
20ml)洗涤。将合并的滤液减压浓缩。将粗制化合物通过硅胶柱色谱(含20%etoac的石油醚)纯化,得到呈淡黄色固体的 6-[5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-4-甲基-哒嗪-3-羧酸甲酯。lc-ms(方法d)r
t
=2.52分钟,m/z=486.6[m+h]
+
。
[0823]
向6-[5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-4-甲基-哒嗪-3
‑ꢀ
羧酸甲酯(67.0mg,138mmol)于thf(1ml)和水(1ml)中的搅拌溶液中加入lioh
·
h2o (17.3mg,414mmol),并将得到的反应混合物在室温搅拌1小时。加入水(5ml),并将反应混合物用etoac(3
×
10ml)萃取。将合并的有机层用盐水洗涤,经无水na2so4干燥并减压浓缩,得到6-[5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3
‑ꢀ
基]-4-甲基-哒嗪-3-羧酸,其未经进一步纯化即用于下一步骤。lc-ms(方法g)r
t
=2.00 分钟,m/z=472.2[m+h]
+
。
[0824]
向6-[5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-4-甲基-哒嗪-3
‑ꢀ
羧酸(67mg,142mmol)于dmf(2ml)中的搅拌溶液中添加hatu(64.8mg,170mmol),并将所得反应混合物在室温下搅拌10分钟。然后加入2-氨基-n-(2,2,2-三氟乙基)乙酰胺
·
hcl(33.0mg,170mmol),随后加入dipea(0.70ml,426mmol),并将得到的混合物在室温搅拌2小时。将反应混合物通过加入冰水(10ml)淬灭,并用etoac(3
×
15 ml)萃取。将合并的有机层用盐水洗涤,用无水na2so4干燥,并减压浓缩。将粗产物通过硅胶柱色谱(含0至10%etoac的石油醚)纯化,得到标题化合物。lc-ms(方法 d)r
t
=2.41分钟,m/z=610.5[m+h]
+
。1h-nmr(dmso-d6,400mhz)δ9.36(s,1h), 8.36-8.34(m,1h),7.92-7.89(m,1h),7.69-7.62(m,2h),7.58(d,j=8.0hz,1h),4.51(d, j=18hz,1h),4.36(d,j=18hz,1h),3.50-3.40(m,1h),3.20-3.09(m,1h),2.60-2.50 (m,2h),2.35-2.22(m,2h),2.25(s,3h)。
[0825]
通过sfc分离两种对映异构体。在as-h上进行分离,柱尺寸为250 mm
×
30mm(5μm),流速为95.0g/分钟,并且基于co2的流动相为含有0.2%n,n-二甲基乙胺作为添加剂的15%meoh,得到实例6.1:4-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-6-[(5r或s)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]哒嗪
ꢀ‑
3-甲酰胺,以及实例6.2:4-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-6-[(5s或r)-5-[3
‑ꢀ
氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]哒嗪-3-甲酰胺。
[0826]
实例7.1和7.2
[0827]
3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-5-[(5r或s)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]吡嗪-2-甲酰胺
[0828]
和
[0829]
3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-5-[(5s或r)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]吡嗪-2-甲酰胺
[0830][0831]
向3-甲基吡嗪-2-羧酸甲酯(15g,98.6mmol)于氯仿(300ml)中的搅拌溶液中加入间氯过苯甲酸(34g,197mmol),并将混合物在80℃搅拌4小时。将混合物冷却至室温,用dcm(200ml)稀释,并用nahco3水溶液(2
×
150ml)洗涤。将有机层用盐水(150ml)洗涤,经无水na2so4干燥,并减压浓缩。将粗产物通过硅胶柱色谱 (含0至100%etoac的石油醚)纯化,得到3-甲基-4-氧代-吡嗪-2-羧酸甲酯。lc-ms (方法d)r
t
=0.81分钟,m/z=169.4[m+h]
+
。
[0832]
在0℃向3-甲基-4-氧代-吡嗪-2-羧酸甲酯(11g,65.4mmol)于dmf(110ml)中的搅拌溶液中逐滴加入磷酰氯(22ml,235mmol),然后将混合物加热至120℃持续15 分钟。然后将反应混合物冷却至室温并倒入冰水中,并用etoac(300ml)萃取。将有机层用盐水(4
×
100ml)洗涤,用无水na2so4干燥,过滤,并减压浓缩。将粗产物通过硅胶柱色谱(含0至100%etoac的石油醚)纯化,得到5-氯-3-甲基-吡嗪-2-羧酸甲酯和6-氯-3-甲基-吡嗪-2-羧酸甲酯的混合物。lc-ms(方法d)r
t
=1.43分钟,m/z=186.9 [m+h]
+
。
[0833]
在室温下,向异构体(8.12g,43.5mmol)的混合物于1,4-二噁烷(80ml)中的搅拌溶液中添加5m naoh(13.1g),并将混合物搅拌2小时,然后减压浓缩。将所得残余物用水(15ml)稀释,用2n hcl水溶液酸化至ph~2至3,并用etoac(2
×
100ml) 萃取。将合并的有机层用盐水洗涤,用无水na2so4干燥并减压浓缩,得到5-氯-3-甲基
‑ꢀ
吡嗪-2-羧酸和6-氯-3-甲基-吡嗪-2-羧酸的混合物,其不经进一步纯化立即用于下一步骤。
[0834]
在室温向羧酸异构体(7.0g,40.6mmol)和2-氨基-n-(2,2,2-三氟乙基)乙酰胺
·
hcl (8.40g,44.0mmol)的混合物于dmf(70ml)中的搅拌溶液中加入hatu(18.2g, 48.0mmol),然后加入dipea(21.0ml,120mmol)。1小时后,通过加入水(5ml) 淬灭反应混合物,然后用etoac(100ml)萃取。将有机层用盐水(3
×
75ml)洗涤,经无水na2so4干燥,并减压浓缩。粗产物通过硅胶柱色谱(含0至100%etoac的石油醚)纯化,得到异构体的混合物:5-氯-3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基] 吡嗪-2-甲酰胺和6-氯-3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]吡嗪-2-甲酰胺。 lc-ms(方法d)r
t
=1.40/1.44分钟,m/z=311.1[m+h]
+
。
[0835]
向高压釜容器中的5-氯-3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]吡嗪-2-甲酰胺(8.00g,26.0mmol)于meoh(160ml)中的搅拌溶液中加入net3(11.0ml,78.0 mmol),并将混合物用n2气体脱气15分钟,然后加入1,1'-双(二苯基膦基)二茂铁] 二氯化钯(ii)(1.88g,2.57mmol)。然后将反应混合物在80℃在150psi的co气体下加热16小时。使
混合物冷却至室温并过滤。将固体用乙醚洗涤,得到6-甲基-5-[[2-氧代
ꢀ‑
2-(2,2,2-三氟乙基氨基)乙基]氨基甲酰基]吡嗪-2-羧酸甲酯。lc-ms(方法d)r
t
=1.99 分钟,m/z=333.1[m-h]-。
[0836]
在n2气氛下在0℃向的6-甲基-5-[[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]氨基甲酰基] 吡嗪-2-羧酸甲酯(1.30g,3.90mmol)于thf(65ml)中的搅拌溶液中分批加入硼氢化钠(0.44g,12.0mmol),并将所得混合物在室温搅拌3小时。通过加入冰淬灭反应物,并用etoac(2
×
50ml)萃取。将合并的有机层用盐水(20ml)洗涤,经无水na2so4干燥,并减压浓缩。将粗产物通过硅胶柱色谱(含0至100%etoac的石油醚)纯化,得到5-(羟基甲基)-3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]吡嗪-2-甲酰胺。lc-ms (方法d)r
t
=1.41分钟,m/z=307.1[m+h]
+
。
[0837]
向5-(羟基甲基)-3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]吡嗪-2-甲酰胺(370 mg,1.20mmol)于dcm(20ml)中的搅拌溶液中加入戴斯-马丁高碘烷(750mg,1.80 mmol),并将混合物在室温搅拌6小时。将反应混合物用dcm(30ml)稀释,并用饱和nahco3水溶液(2
×
40ml)洗涤。将有机层减压浓缩,得到5-甲酰基-3-甲基-n-[2
‑ꢀ
氧代-2-(2,2,2-三氟乙基氨基)乙基]吡嗪-2-甲酰胺,将其不经进一步纯化立即用于下一步骤。
[0838]
在室温下向5-甲酰基-3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]吡嗪-2-甲酰胺 (500mg,1.63mmol)于etoh(10ml)和水(5ml)中的搅拌溶液中加入羟基氯化铵 (0.17g,2.40mmol)和乙酸钠(200mg,2.44mmol),并将所得混合物搅拌3小时。将混合物减压浓缩,并将残余物用水(10ml)稀释,并用etoac(2
×
25ml)萃取。将合并的有机层用nahco3水溶液(30ml)洗涤,经无水na2so4干燥,过滤并减压浓缩,得到5-(羟基亚氨基甲基)-3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]吡嗪-2-甲酰胺。 lc-ms(方法d)r
t
=1.18分钟,m/z=318.2[m-h]-。
[0839]
在室温下向5-(羟基亚氨基甲基)-3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]吡嗪-2-甲酰胺(0.28g,0.88mmol)于dmf(3ml)中的搅拌溶液中加入n-氯代琥珀酰亚胺(152mg,1.14mmol),然后将混合物在40℃加热10分钟。然后将混合物冷却至0℃,加入1-氯-2-氟-5-(三氟甲基)-3-[1-(三氟甲基)乙烯基]苯(0.29g,0.99mmol),然后加入 net3(0.13ml,0.92mmol):将反应物在室温下搅拌16小时。然后,将反应混合物通过加入水(5ml)淬灭,并用etoac(25ml)萃取。将有机层用盐水(3
×
10ml)洗涤,经无水na2so4干燥,并减压浓缩。将粗产物通过硅胶柱色谱(含0至100%etoac 的石油醚)纯化,得到标题化合物。lc-ms(方法d)r
t
=2.51分钟,m/z=610.4[m+h]
+
。 1h-nmr(dmso-d6,400mhz)δ9.10-9.03(m,2h),8.65(t,j=6.0hz,1h),8.40-8.35(m, 1h),7.96-7.92(m,1h),4.49(s,2h),4.00-3.87(m,4h),2.82(s,3h)。
[0840]
通过sfc分离两种对映异构体。在dcpak p4vp上进行分离,柱尺寸为250mm
×
21 mm(5μm),流速为60.0g/分钟,并且基于co2的流动相为10%meoh,得到实例7.1: 3-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-5-[(5r或s)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]吡嗪-2-甲酰胺,以及实例7.2:3-甲基-n-[2-氧代
ꢀ‑
2-(2,2,2-三氟乙基氨基)乙基]-5-[(5s或r)-5-[3-氯-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]吡嗪-2-甲酰胺。
[0841]
实例8.1和8.2
[0842]
2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5r或s)-5-[3-溴-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺
[0843]
和
[0844]
2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5s或r)-5-[3-溴-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺
[0845][0846]
向2-[3-溴-2-氟-5-(三氟甲基)苯基]-4,4,5,5-四甲基-1,3,2-二氧杂环戊硼烷(1.3g,3.5 mmol)于thf(15ml)和水(7.5ml)中的搅拌溶液中加入碳酸二钾(1.02g,7.38mmol),并将混合物用n2气体脱气10分钟。加入2-溴-3,3,3-三氟-丙-1-烯(0.76g,4.3mmol) 和双(三苯基膦)二氯化钯(ii)(0.25g,0.36mmol),并将反应混合物在80℃下加热 3小时。然后,将混合物冷却至室温,并用乙醚(2
×
10ml)萃取。将合并的有机层用盐水(10ml)洗涤,经无水na2so4干燥并减压浓缩,得到呈棕色液体的1-溴-2-氟-5-(三氟甲基)-3-[1-(三氟甲基)乙烯基]苯,其不经进一步纯化立即用于下一步骤。
[0847]
在室温下,向4-(羟基亚氨基甲基)-2-甲基-苯甲酸甲酯(500mg,2.59mmol)于dmf (5ml)中的搅拌溶液中加入n-氯代琥珀酰亚胺(0.45g,3.4mmol),并将混合物在40℃下加热10分钟。然后,将混合物冷却至0℃,加入1-溴-2-氟-5-(三氟甲基)-3-[1-(三氟甲基)乙烯基]苯(1.05g,3.12mmol),然后加入net3(0.40ml,2.85mmol),并将反应物在室温下搅拌3小时。将反应混合物通过加入水(10ml)淬灭,并用etoac(30ml) 萃取。将有机层用盐水(3
×
15ml)洗涤,用无水na2so4干燥,并减压浓缩。将粗产物通过硅胶柱色谱(含0至20%etoac的石油醚)纯化,得到呈米色半固体状的4-[5-[3
‑ꢀ
溴-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸甲酯。lc-ms (方法c)r
t
=2.78分钟,m/z=528.1[m+h]
+
。
[0848]
在室温下向4-[5-[3-溴-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸甲酯(500mg,0.9mmol)于thf(5ml)和水(5ml)中的搅拌溶液中加入氢氧化锂一水合物(0.12g,2.9mmol),并将混合物在60℃下加热16小时。然后,使混合物冷却至室温,并减压蒸发溶剂。将残余物溶解于水(5ml)中,用hcl溶液(1 m)酸化至ph~2至3,并用etoac(2
×
25ml)萃取。将合并的有机层用盐水(10ml) 洗涤,经无水na2so4干燥并减压浓缩,得到呈米色固体的4-[5-[3-溴-2-氟-5-(三氟甲基) 苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸。lc-ms(方法f)r
t
=2.74分钟, m/z=514.3[m+h]
+
。
[0849]
在室温下向4-[5-[3-溴-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸(0.31g,0.60mmol)和2-氨基-n-(2,2,2-三氟乙基)乙酰胺
·
hcl(0.14g,0.73 mmol)于dmf(5ml)中的搅拌溶液中加入hatu(0.28g,0.74mmol),然后加入 dipea(0.32ml,1.8mmol),并将混合物搅拌2小时。将反应混合物通过添加水(5ml) 淬灭,并且用etoac(3
×
15ml)萃取。将合并的有机层用盐水洗涤,用无水na2so4干燥,并减压浓缩。将
粗产物通过硅胶柱色谱(含0至50%etoac的石油醚)纯化,得到标题化合物。lc-ms(方法f)r
t
=2.66分钟,m/z=652.0[m+h]
+
。1h-nmr(dmso-d6, 400mhz)δ8.65-8.58(m,2h),8.45-8.41(m,1h),7.96-7.91(m,1h),7.69-7.63(m,2h), 7.49(d,j=7.6hz,1h),4.56(d,j=18hz,1h),4.39(d,j=18hz,1h),4.00-3.89(m,4 h),2.40(s,3h).
[0850]
通过sfc分离两种对映异构体。在chiralcel-oj-h上进行分离,柱尺寸为250mm
×
30 mm(5μm),流速为95.0g/分钟,并且基于co2的流动相为含有0.2%n,n-异丙胺作为添加剂的10%iproh,得到实例8.1:2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5r或s)-5-[3-溴-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺,以及实例8.2:2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5s或r)-5-[3-溴-2
‑ꢀ
氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺。
[0851]
通过实例8.1和8.2的方法类似地制备以下化合物:
[0852][0853][0854]
实例9.1和9.2
[0855]
2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5r或s)-5-[3-(二氟甲基)-2-氟
ꢀ‑
5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺
[0856]
和
[0857]
2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5s或r)-5-[3-(二氟甲基)-2-氟
ꢀ‑
5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺
[0858][0859]
在密封管中,在n2气氛下将1-溴-3-(二氟甲基)-2-氟-5-(三氟甲基)苯(500mg,1.71 mmol)、三氟-钾-[1-(三氟甲基)乙烯基]硼(515mg,2.55mmol)、乙酸钯(ii)(0.020g,0.089mmol)、三苯基膦(0.053g,0.20mmol)和碳酸铯(1.65g,5.08mmol)溶解于 thf(4ml)和水(2ml)中。封闭密封管,并在80℃下搅拌6小时。将反应混合物冷却至室温,并加入et2o和水。分离有机层,并减压蒸发溶剂。粗产物(1-(二氟甲基)-2
‑ꢀ
氟-5-(三氟甲基)-3-[1-(三氟甲基)乙烯基]苯)未经进一步纯化即用于下一步骤。
[0860]
在n2气氛下,将甲基4-[(e)-羟基亚氨基甲基]-2-甲基-苯甲酸酯(200mg,1.03mmol) 和1-氯吡咯烷-2,5-二酮(0.413g,3.09mmol)在干燥dmf(5ml)中混合。将反应混合物在40℃搅拌1小时。然后,将反应混合物在冰浴中冷却至0℃,并加入粗品1-(二氟甲基)-2-氟-5-(三氟甲基)-3-[1-(三氟甲基)乙烯基]苯(350mg,1.14mmol)和net3(0.15 ml)。将所得反应混合物在室温下搅拌12小时。反应完成后,加入冰,并且混合物用 et2o萃取。分离有机层,并真空浓缩。将粗产物通过硅胶柱色谱(含1%etoac的石油醚)纯化,得到4-[5-[3-(二氟甲基)-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3
‑ꢀ
基]-2-甲基-苯甲酸甲酯。lc-ms(方法d)r
t
=2.53分钟,m/z=500.2[m+h]
+
。
[0861]
向4-[5-[3-(二氟甲基)-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸甲酯(100mg,0.20mmol)于thf(2ml)和水(2ml)中的溶液中加入氢氧化锂一水合物(0.025g,0.60mmol)。将所得混合物在60℃下搅拌6小时。反应完成后,减压蒸发溶剂,并使用hcl水溶液(1m)将含水层酸化至ph~3。滤出沉淀,并真空干燥,得到4-[5-[3-(二氟甲基)-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸。lc-ms(方法d)r
t
=2.29分钟,m/z=484.2[m-h]-。
[0862]
在0℃下向4-[5-[3-(二氟甲基)-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3
‑ꢀ
基]-2-甲基-苯甲酸(0.085g,0.18mmol)和hatu(100mg,263μmol)于干燥dmf (1ml)中的溶液中逐滴加入2-氨基-n-(2,2,2-三氟乙基)乙酰胺(0.050g,0.32mmol) 于干燥dmf(1ml)中的溶液。然后,加入dipea(0.1ml,0.6mmol),并将得到的反应混合物在室温搅拌4小时。通过添加冰水淬灭反应混合物,并且用etoac(3
×
)萃取。将合并的有机层用盐水洗涤,用无水na2so4干燥,过滤,并减压浓缩。将粗产物通过硅胶柱色谱(含0至100%etoac的石油醚)纯化,得到标题化合物。lc-ms(方法d)r
t
=2.23分钟,m/z=624.3[m+h]
+
。1h-nmr(dmso-d6,400mhz)δ8.66-8.57(m, 2h),8.26-8.23(m,1h),8.17-8.11(m,1h),7.69-7.64(m,2h),7.49(d,j=7.6hz,1h), 7.36(t,j=53hz,1h),4.59(d,j=18hz,1h),4.37(d,j=18hz,1h),4.00-3.88(m,4h), 2.40(s,3h)。
[0863]
通过sfc分离两种对映异构体。在chiralcel oj-h上进行分离,柱尺寸为250mm
×
21 mm(5μm),流速为90.0g/分钟,并且基于co2的流动相为8%meoh,得到实例9.1: 2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5r或s)-5-[3-(二氟甲基)-2-氟-5-(三氟
甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺,以及实例9.2:2-甲基-n-[2-氧代
ꢀ‑
2-(2,2,2-三氟乙基氨基)乙基]-4-[(5s或r)-5-[3-(二氟甲基)-2-氟-5-(三氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺。
[0864]
通过实例9.1和9.2的方法类似地制备以下化合物:
[0865][0866][0867]
实例10.1和10.2
[0868]
2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5r或s)-5-[3,5-双(二氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺
[0869]
和
[0870]
2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5s或r)-5-[3,5-双(二氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺
[0871]
[0872]
在0℃下向5-溴苯-1,3-二甲醛(2.00g,9.4mmol)于dcm(40ml)中的搅拌溶液中逐滴添加dast(6.2g,38mmol),并将所得混合物在室温下搅拌3小时。在0℃下通过添加水淬灭混合物,分离含水层,并用dcm(3
×
)萃取。将合并的有机层用无水 na2so4干燥,过滤,并真空浓缩。将粗产物通过硅胶柱色谱(100%石油醚)纯化,得到1-溴-3,5-双(二氟甲基)苯。
[0873]
将1-溴-3,5-双(二氟甲基)苯(1.2g,4.7mmol)和三氟钾基-[1-(三氟甲基)乙烯基] 硼(1.44g,7.09mmol)于thf(6ml)和水(3ml)中的混合物在n2气氛下脱气10 分钟。然后加入乙酸钯(168mg,1.02mmol)、三苯基膦(156mg,595μmol)和cs2co
3 (3.72g,11.4mmol),并将反应混合物在80℃搅拌24小时。将混合物通过添加水淬灭。分离含水层,用乙醚萃取,并减压蒸发溶剂。将粗产物通过硅胶柱色谱(100%石油醚) 纯化,得到1,3-双(二氟甲基)-5-[1-(三氟甲基)乙烯基]苯。
[0874]
向4-[(e)-羟基亚氨基甲基]苯甲酸甲酯(465mg,2.60mmol)于dmf(2.0ml)中的搅拌溶液中加入ncs(0.36g,2.7mmol),并将混合物在40℃加热10分钟。然后将反应混合物冷却至0℃,并加入1,3-双(二氟甲基)-5-[1-(三氟甲基)乙烯基]苯(0.75g,2.8 mmol)和net3(0.3ml)于dmf(1ml)中的溶液。将所得混合物在室温下搅拌3小时。通过加入水淬灭反应物,分离含水层,并用etoac(3
×
)萃取。将合并的有机层用盐水洗涤,用无水na2so4干燥,过滤,并减压浓缩。将粗产物通过硅胶柱色谱(含0 至100%etoac的石油醚)纯化,得到4-[5-[3,5-双(二氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸甲酯。lc-ms(方法d)r
t
=2.37分钟,m/z=464.18[m+h]
+
。
[0875]
将4-[5-[3,5-双(二氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸乙酯 (0.3g,0.6mmol)和lioh(81.0mg,3.4mmol)于1,4-二噁烷(5.0ml)和水(5.0ml) 中的混合物在90℃加热过夜。然后,将反应混合物减压浓缩,并通过加入hcl溶液(1m) 酸化。用5%meoh-dcm溶液(3
×
)萃取含水层。将合并的有机层用无水na2so4干燥,过滤,并真空浓缩。粗产物不经进一步纯化即用于下一步骤。lc-ms(方法d)r
t
=2.47 分钟,m/z=450.29[m+h]
+
。
[0876]
将4-[5-[3,5-双(二氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]-2-甲基-苯甲酸(246 mg,548μmol)、1-氨基-3-(三氟甲基氨基)丙-2-酮
·
hcl(164mg,1.05mmol)、hatu(317 mg,834μmol)和dipea(351μl,2.0mmol)于dmf(4.0ml)中的混合物在室温下搅拌2小时。反应完成后,将混合物用水淬灭,并且用etoac萃取含水层。将合并的有机层用盐水洗涤,经无水na2so4干燥,过滤,并真空浓缩。将粗产物通过硅胶柱色谱 (含0至10%etoac的石油醚)纯化,得到标题化合物。lc-ms(方法d)r
t
=2.08分钟,m/z=588.28[m+h]
+
。1h-nmr(dmso-d6,400mhz)δ8.64-8.57(m,2h),7.98(s,2 h),7.93(s,1h),7.66-7.60(m,2h),7.49(d,j=8.4hz,1h),7.23(t,j=55hz,2h),4.50 (d,j=18hz,1h),4.29(d,j=18hz,1h),3.99-3.88(m,4h),2.40(s,3h)。
[0877]
通过sfc分离两种对映异构体。在chiralcel oj-h上进行分离,柱尺寸为250mm
×
21 mm(5μm),流速为60.0g/分钟,并且基于co2的流动相为10%meoh,得到实例10.1:2-甲基-n-[2-氧代-2-(2,2,2-三氟乙基氨基)乙基]-4-[(5r或s)-5-[3,5-双(二氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3-基]苯甲酰胺,以及实例10.2:2-甲基-n-[2-氧代-2-(2,2,2
‑ꢀ
三氟乙基氨基)乙基]-4-[(5s或r)-5-[3,5-双(二氟甲基)苯基]-5-(三氟甲基)-4h-异噁唑-3
‑ꢀ
基]苯甲酰胺。
[0878]
表中化合物的实验细节:
[0879]
[0880]
[0881]
[0882]
[0883]
[0884]
[0885]
[0886]
[0887][0888]
本发明的化合物是用于害虫防治的有价值的活性成分。术语“害虫”包括动物体表和动物体内以及卫生领域中的外寄生物和内寄生物。特别地,害虫是蚤、蜱、螨、蝇、蠕虫和虱。甚至更特别地,害虫是蚤和蜱。
[0889]
在本发明的上下文中,动物应理解为包括脊椎动物。在本文中,术语脊椎动物应理解为包括例如鱼类、两栖动物、爬行动物、鸟类和人在内的哺乳动物。本发明的一组优选脊椎动物包含温血动物,包括农场动物,如牛、马、猪、绵羊和山羊,家禽,如鸡、火鸡、珍珠鸡和鹅,毛皮动物,如水貂、狐狸、毛丝鼠、兔等,以及伴侣动物,如雪貂、豚鼠、大鼠、仓鼠、猫和狗,以及人。本发明的另一组优选脊椎动物包含鱼,包括鲑鱼。
[0890]
在本发明的上下文中,外寄生虫被理解为特别是昆虫类、螨类(螨和蜱)和甲壳类 (海虱)。这些包括以下目次的昆虫:鳞翅目(lepidoptera)、鞘翅目(coleoptera)、同翅目(homoptera)、半翅目(hemiptera)、异翅目(heteroptera)、双翅目(diptera)、网翅目(dictyoptera)、缨翅目(thysanoptera)、直翅目(orthoptera)、虱目(anoplura)、蚤目(siphonaptera)、食毛目(mallophaga)、缨尾目(thysanura)、等翅目(isoptera)、子翅目(psocoptera)和膜翅目(hymenoptera)。然而,可特别提及的外寄生虫是那些困扰人类或动物并携带病原体的外寄生虫,例如蝇,如家蝇(musca domestica)、澳大利亚灌木蝇(musca vetustissima)、秋家蝇(musca autumnalis)、夏厕蝇(fanniacanicularis)、肉食麻蝇(sarcophaga carnaria)、铜绿蝇(lucilia cuprina)、丝光绿蝇(luciliasericata)、牛皮蝇(hypoderma bovis)、纹皮蝇(hypoderma lineatum)、绿尾金蝇 (chrysomyia chloropyga)、人肤蝇(dermatobia hominis)、美洲旋丽蝇(cochliomyiahominivorax)、肠胃蝇(gasterophilus intestinalis)、羊狂蝇(oestrus ovis),叮咬蝇如西方角蝇(haematobia irritans irritans)、东方角蝇(haematobia irritans exigua)、厩螫蝇 (stomoxys calcitrans),马蝇(tabanids)及亚科虻科(tabanidae),如麻虻属种(haematopotaspp.)(例如雨麻虻(haematopota pluvialis))和虻属种(tabanus spp.)(例如绿头马蝇(tabanus nigrovittatus)),以及斑虻亚科(chrysopsinae),如斑虻属种(chrysops spp.) (例如盲斑虻(chrysops caecutiens));虱蝇(hippoboscids),如羊虱蝇(melophagus ovinus) (绵羊蜱);舌蝇,如舌蝇属种(glossinia spp.);其它叮咬昆虫,如蠓虫,如蠓科 (ceratopogonidae)(咬蠓)、蚋科(simuliidae)(墨蚊)、毛蛉科(psychodidae)(白蛉);以及吸血昆虫,例如蚊子,如按蚊属种(anopheles spp.)、伊蚊属种(aedes spp.)和库蚊属种(culex spp.)、蚤,如猫栉首蚤(ctenocephalidesfelis)和犬栉首蚤(ctenocephalidescanis)(猫和狗蚤)、印鼠客蚤(xenopsylla cheopis)、人蚤(pulex irritans)、鸡角叶蚤 (ceratophyllus gallinae)、穿皮蜱(dermatophiluspenetrans),吸
血虱(anoplura),如长颚虱属种(linognathusspp.)、血虱属种(haematopinusspp.)、管虱属种(solenopotesspp.)、人虱(pediculushumanis);以及咀毛虱(mallophaga),如羊毛虱(bovicola(damalinia)ovis)、牛毛虱(bovicola(damalinia)bovis),和其它羽虱属种(bovicolaspp.)。外寄生虫还包括蜱螨目(acarina)的成员,如螨(例如牛痒螨(chorioptesbovis),姬螯螨属种(cheyletiellaspp.),鸡皮刺螨(dermanyssusgallinae),禽刺螨属种(ortnithonyssusspp.),犬蠕形螨(demodexcanis),疥螨(sarcoptesscabiei),绵羊痒螨(psoroptesovis)和疮螨属种(psorergatesspp.),和蜱。代表性的蜱为例如牛蜱(boophilus)、花蜱(amblyomma)、暗眼蜱(anocentor)、革蜱(dermacentor)、血蜱(haemaphysalis)、璃眼蜱(hyalomma)、硬蜱(ixodes)、扇革蜱(rhipicentor)、巨足蜱(margaropus)、扇头蜱(rhipicephalus)、锐缘蜱(argas)、残喙蜱(otobius)和钝缘蜱(ornithodoros)等,其优选侵染脊椎动物,例如温血动物,包括农场动物,如牛、马、猪、绵羊和山羊,家禽,如鸡、火鸡、珍珠鸡和鹅,毛皮动物,如水貂、狐狸、毛丝鼠、兔等,以及伴侣动物,如雪貂、豚鼠、大鼠、仓鼠、猫和狗,以及人和鱼。
[0891]
根据本发明的本发明化合物还对显示正常敏感性的动物害虫的所有或个别发育阶段,以及显示对广泛使用的杀寄生虫剂的抗性的那些具有活性。对于具有抗性的昆虫和蜱螨目成员尤其如此。本发明的活性物质的杀虫、杀卵和/或杀螨效果可直接表现,即立即或在经过一段时间后杀死害虫,例如当发生蜕皮时或通过破坏它们的卵来杀死害虫,或间接表现,例如降低产卵数和/或孵化率,效力良好,相当于至少50至60%的杀虫率(死亡率)。
[0892]
本发明的化合物还可以用于对抗卫生害虫,特别是双翅目(diptera)的蝇科(muscidae)、食蝇科(sarcophagidae)、按蚊亚科(anophilidae)和蚊科(culicidae);直翅目(orthoptera)、网翅目(dictyoptera)(例如蜚蠊科(blattidae)(蟑螂),如德国小蠊(blatellagermanica)、东方蜚蠊(blattaorientalis)、美洲大蠊(periplanetaamericana))和膜翅目(hymenoptera)(例如蚁科(formicidae)(蚂蚁)和胡蜂科(vespidae)(黄蜂))。
[0893]
具有式(i)的化合物还有效对抗鱼类的外寄生虫,尤其是桡足亚纲(copepoda)(例如管口水蚤目(siphonostomatoida)(海虱)),同时被鱼良好耐受。
[0894]
具有式(i)的化合物还可用于对抗绦虫纲(cestoda)的蠕虫,包括真绦虫亚纲(eucestoda)和单节亚纲(cestodaria)的蠕虫。
[0895]
本发明的化合物还对植物的寄生螨和昆虫具有可持续的功效。对于蜱螨目(acarina)的蛛螨,它们有效对抗叶螨科(tetranychidae)(叶螨属种(tetranychusspp.)和全爪螨属种(panonychusspp.))的卵、若虫和成虫。
[0896]
它们对同翅目(homoptera)的吮吸昆虫具有高活性,尤其是对蚜科(aphididae)、飞虱科(delphacidae)、蝉科(cicadellidae)、木虱科(psyllidae),蝗虫科(loccidae)、蚊科(diaspididae)和蝗虫科(eriophydidae)(例如柑橘类水果上的锈螨);半翅目(hemiptera)、异翅亚目(heteroptera)和缨尾目(thysanoptera)的害虫,以及鳞翅目(lepidoptera)、鞘翅目(coleoptera)、双翅目(diptera)和直翅目(orthoptera)的食植物昆虫具有高活性。
[0897]
它们同样适合作为对抗土壤中害虫的土壤杀虫剂。
[0898]
因此,具有式(i)的化合物有效对抗作物如谷物、棉花、稻、玉米、大豆、马铃薯、蔬菜、水果、烟草、蛇麻草、柑橘、鳄梨和其它作物上的吮吸昆虫和进食昆虫的所有发育阶段。
[0899]
具有式i的化合物还有效对抗根结线虫属(meloidogyne)、胞囊线虫属(heterodera)、短体线虫属(pratylenchus)、茎线虫属(ditylenchus)、穿孔线虫属(radopholus)、根螨属(rizoglyphus)等物种的植物线虫。
[0900]
本发明的化合物对蠕虫有效。蠕虫在商业上很重要,因为它们引起哺乳动物和家禽的严重疾病,例如引起绵羊、猪、山羊、牛、马、驴、骆驼、狗、猫、兔、豚鼠、仓鼠、鸡、火鸡、珍珠鸡和其它养殖的鸟类以及外来鸟类的严重疾病。典型的线虫是:血矛线虫属(haemonchus)、毛圆线虫属(trichostrongylus)、胃线虫属(ostertagia)、细颈线虫属(nematodirus)、古柏线虫属(cooperia)、蛔虫属(ascaris)、仰口线虫属(bunostonum)、结节线虫属(oesophagostonum)、夏柏特线虫属(charbertia)、鞭虫属(trichuris)、圆线虫属(strongylus)、毛线属(trichonema)、网尾属(dictyocaulus)、毛细线虫属(capillaria)、异刺属(heterakis)、弓蛔虫属(toxocara)、鸡蛔虫属(ascaridia)、尖尾线虫属(oxyuris)、钩口线虫属(ancylostoma)、钩虫属(uncinaria)、弓蛔线虫属(toxascaris)和副蛔虫属(parascaris)。吸虫包括,特别是片形科(fasciolideae),尤其是肝片吸虫(fasciola hepatica)。
[0901]
根据本发明的具有化学式(i)的化合物的杀有害生物活性对应于所提及的有害生物的约50至60%的死亡率,更优选地对应于超过90%,最优选地达95至100%的死亡率。具有式(i)的化合物优选以未修饰的形式内部和外部使用,或者优选与制剂领域中常规使用的佐剂一起使用,因此可以以已知的方式加工以得到例如液体制剂(例如点涂、浇泼、喷雾、乳液、悬浮液、溶液、可乳化浓缩物、溶液浓缩物)、半固体制剂(例如乳膏、软膏、糊剂、凝胶、脂质体制剂)和固体制剂(例如食品添加剂片剂,包括例如胶囊,粉末,包括可溶性粉末、颗粒,或将活性成分包埋在聚合物物质中,如植入物和微粒)。与组合物一样,施用方法根据预期目的和主要环境来选择。
[0902]
本发明的化合物可以单独给药或以组合物的形式给药。实际上,本发明的化合物通常以组合物的形式给药,即与至少一种可接受的赋形剂混合。任何可接受的赋形剂的比例和性质由所选的本发明化合物的性质、所选的给药途径和兽医学和药物领域中的标准实践来确定。
[0903]
在一个实施例中,本发明提供了组合物,其包含:本发明的化合物和至少一种可接受的赋形剂。
[0904]
在实现这样的治疗和/或控制中,本发明的化合物可以以使得化合物能够生物利用的任何形式和途径施用。本发明的化合物可以通过多种途径施用,包括口服,特别是通过片剂和胶囊。本发明的化合物可以肠胃外途径施用,更特别地通过吸入、皮下、肌内、静脉内、动脉内、透皮、鼻内、直肠、阴道、眼、局部、舌下和颊、腹膜内、脂肪内、鞘内和经由局部递送,例如通过导管或支架。
[0905]
本领域技术人员可根据所选化合物的具体特性、待治疗的病症或病况、病症或病况的阶段和其它相关情况容易地选择适当的给药形式和途径。本发明的药物组合物可以例如以片剂(包括咀嚼片)、胶囊剂、扁囊剂、纸剂、锭剂、糯米纸囊剂、酏剂、丸剂、软膏剂、透皮贴剂、气雾剂、吸入剂、栓剂、灌肠剂、溶液剂、注射剂和混悬剂的形式施用于受试者。
[0906]
术语“可接受的赋形剂”是指通常用于制备兽医学和药物组合物的那些赋形剂,并且在所用量下应为纯品且无毒。它们通常是固体、半固体或液体材料,其在聚集体中可用作活性成分的媒介物或介质。可接受的赋形剂的一些实例见于《雷明登氏药学 (remington's pharmaceutical sciences)》和《药用辅料手册(the handbook ofpharmaceutical excipients)》中,并且包括稀释剂、媒介物、载体、软膏基质、粘合剂、崩解剂、润滑剂、助流剂、甜味剂、调味剂、凝胶基质、持续释放基质、稳定剂、防腐剂、溶剂、悬浮剂、缓冲剂、乳化剂、染料、推进剂、包衣剂等。
[0907]
在一个实施例中,组合物适合于口服给药,例如片剂或胶囊或液体制剂,例如适合于口服给药的溶液或悬浮液。在一个实施例中,组合物适合于口服给药,例如适合于口服给药的咀嚼制剂。在另一个实施例中,组合物是液体或半固体制剂,例如适合于肠胃外施用的溶液或悬浮液或糊剂。
[0908]
在一个实施例中,组合物适合于注射给药,例如适合于注射给药的溶液或悬浮液。
[0909]
用于受试者以治疗和/或控制线虫/蠕虫的特定组合物包含溶液;注射剂;乳液,包括经典乳液、微乳液和自乳化组合物,其为无水有机组合物,优选油性组合物,其在添加至受试者身体后与体液一起形成乳液;悬浮液(灌药);浇淋制剂;食品添加剂;散剂;片剂,包括泡腾片剂;大丸剂(boli);胶囊,包括微囊;以及可咀嚼的零食。特别地,组合物形式是片剂、胶囊、食品添加剂或可咀嚼的零食。
[0910]
本发明的组合物以兽医学和药物领域中熟知的方式制备,并且包括至少一种本发明的化合物作为活性成分。本发明化合物的量可以根据其具体形式而变化,并且可以方便地为单位剂型重量的1%至约50%。本发明的药物组合物优选配制成单位剂型,每个剂量通常含有约0.5mg至约100mg的本发明化合物。可采用一种或多种单位剂型来影响治疗剂量。
[0911]
在一个实施例中,本发明还提供了一种用于处理害虫的方法,其包括:向有需要的受试者施用有效量的具有式(i)的化合物,或其盐,该方法任选地还包含有效量的至少一种另外的活性化合物。
[0912]
在一个实施例中,本发明还提供了一种用于控制害虫的方法,其包括:向有需要的受试者施用有效量的具有式(i)的化合物,或其盐,该方法任选地还包含有效量的至少一种另外的活性化合物。
[0913]
在一个实施例中,本发明还提供了一种用于处理或控制害虫的方法,其包括:使受试者的环境与有效量的具有式(i)的化合物或其盐接触,该方法任选地还包含有效量的至少一种另外的活性化合物。
[0914]
因此,本发明提供本发明化合物作为药物的用途,包括用于制备药物。在一个实施例中,本发明提供用于治疗害虫的包含具有式(i)的化合物或其盐的药物的制备。在一个实施例中,本发明提供用于控制害虫的包含本发明化合物或其盐的药物的制备。
[0915]
术语“治疗(treating\treat\treated\treatment)”包括但不限于抑制、减缓、停止、减少、改善、逆转现有症状的进展或严重程度,或预防病症、病况或疾病。例如,将通过施用本发明的化合物来治疗成年心丝虫感染。治疗可以在通过疗法应用或施用。
[0916]
术语“控制(control\controlling\controlled)”是指包括但不限于降低、减少或改善症状、障碍、病症或疾病的风险,以及保护动物免于经受症状、障碍、病症或疾病。控制可以指治疗性、预防性或防止性给药。例如,幼虫或不成熟的害虫可以是无症状的,但将通
过作用于幼虫或不成熟的害虫来进行控制,防止感染发展为由成熟害虫引起的症状性或衰弱性感染。
[0917]
因此,本发明化合物在治疗和/或防治体内寄生线虫和吸虫的害虫,特别是蠕虫的用途,指本发明化合物在其整个生命周期中作用于各种形式的害虫的用途,与受试者是否表现出症状(包括发病率或死亡率)无关,并且与攻击阶段无关。
[0918]
如本文所用,“向受试者施用”包括但不限于皮肤、皮下、肌内、粘膜、粘膜下、透皮、口服或鼻内施用。施用可包括注射或局部施用,例如,浇泼或点涂施用。浇淋法或点涂法对于畜群动物,如牛、马、绵羊或猪,是特别有利的,这些动物进行口服或注射治疗都是困难的或耗时的。由于其简单性,该方法当然也可用于所有其它动物,包括个别家畜或宠物,并且极大地受到动物饲养者的青睐,因为其通常可在没有兽医专家在场的情况下进行。
[0919]
术语“受试者”和“患者”是指包括人类和非人类哺乳动物和鱼,本文所述的脊椎动物,例如狗、猫、小鼠、大鼠、豚鼠、兔、雪貂、牛、马、绵羊、山羊和猪。具体的受试者是哺乳动物宠物或伴侣动物,例如狗和猫以及小鼠、豚鼠、雪貂和兔。
[0920]
术语“有效量”是指给予受试者所需益处的量,并且包括用于治疗和控制的施用。该量将在个体受试者之间不同,并且将取决于多种因素,包括受试者的总体身体状况和待治疗病症的潜在原因的严重程度、伴随治疗,以及用于将所需反应维持在有益水平的本发明化合物的量。
[0921]
有效量可以容易地由作为本领域技术人员的主治诊断医师通过使用已知技术和通过观察在类似情况下获得的结果来确定。在确定有效量、剂量时,主治诊断医师考虑许多因素,包括但不限于:患者的品种;尺寸,年龄,一般健康状况;涉及的具体病症、障碍、感染或疾病;病症、障碍或疾病的程度或涉及或严重程度、个体患者的反应;给予的具体化合物;给药的方式;给药的制剂的生物利用度特性;选择的给药方案;伴随用药的使用;以及其它相关情况。本发明的有效量,即治疗剂量,预期在0.5mg至100 mg的范围内。具体的量可以由本领域技术人员确定。虽然这些剂量是基于具有约1kg 至约20kg的质量的受试者,但诊断医师将能够确定质量落在该重量范围之外的受试者的适当剂量。本发明的有效量,即治疗剂量,预期为0.1mg至10mg/kg受试者。给药方案预期为每月、每季度、半年或每年给药。
[0922]
本发明化合物可与一种或多种其它活性化合物或疗法组合用于治疗一种或多种障碍、疾病或病症,包括治疗其适用的害虫。本发明的化合物可与一种或多种用于治疗害虫和其它病症的化合物或疗法同时、依序或分开施用。
[0923]
因此,应当理解,本发明的组合物和方法任选地包括包含有效量的至少一种另外的活性化合物。可用于本发明的另外的活性化合物包括用于治疗蚤、蜱、蝇和蚊的那些化合物,并且包括大环内酯,如米尔贝肟(milbemycin oxime)、吡虫啉(imidacloprid)、多杀菌素(spinosad)、吡丙醚(pyriproxyfen),异丙菊酯(premethrin)、s-烯虫酯 (s-methoprene),吡喹酮(praziquantel)和莫西菌素(moxidectin)。其它示例性加成活性化合物包括但不限于阿福拉纳(afoxolaner)、氟雷拉纳(fluralaner)、洛替拉纳 (lotilaner)、沙罗拉纳(sarolaner)、阿苯达唑(albendazole)、坎苯达唑(cambendazole)、芬苯达唑(fenbendazole)、氟苯达唑(flubendazole)、甲苯达唑(mebendazole)、奥芬达唑(oxfendazole)、对苯达唑(parabendazole)、噻苯咪唑(tiabendazole)、三氯苯达唑 (triclabendazole)、双甲脒(amitraz)、去甲螈(demiditraz)、氯舒隆(clorsulon)、氰氯碘
柳胺(closantel)、羟氯硝胺(oxyclonazide)、碘醚柳胺(rafoxanide)、苯醚氰菊酯 (cyphenothrin)、氟氯苯菊酯(flumethrin)、氯氰菊酯(permethrin)、灭蝇胺(cyromazine)、得曲恩特(derquantel)、地芬尼泰(diamphenetide)、地昔尼尔(dicyclanil)、呋虫胺 (dinotefuran)、吡虫啉(imidacloprid)、烯啶虫胺(nitenpyram)、噻虫嗪(thiamethoxam)、阿巴克丁(thiamethoxam)、多拉克丁(doramectin)、埃玛菌素(emamectin)、埃普利诺克丁(eprinomectin)、伊维菌素(ivermectin)、莫昔克丁(moxidectin)、司拉克丁 (selamectin)、米尔倍肟(milbemycin oxime)、艾默德斯(emodepside)、依西太尔 (epsiprantel)、氟虫腈(fipronil)、氟佐隆(fluazuron)、氟己芬(fluhexafon)、茚虫威 (indoxacarb)、左旋咪唑(levamisol)、虱螨脲(lufenuron)、氰氟虫腙(metaflumizone)、烯虫酯(methoprene)、莫奈太尔(monepantel)、莫仑太尔(morantel)、氯硝柳胺 (niclosamide)、硝硫氰酯(nitroscanate)、硝碘酚腈(nitroxynil)、诺伐隆(novaluron)、奥克太尔(oxantel)、吡喹酮(praziquantel)、噻嘧啶(pyrantel)、吡咯(pyriprole)、蚊蝇醚(pyriproxyfen)、西沙罗尼(sisapronil)、多杀菌素(spinosad)、乙基多杀菌素 (spinetoram)和三氟苯嘧啶(triflumezopyrim),或前述任一项的盐。
[0924]
本发明化合物的活性可通过多种方法测定,包括体外和体内方法。
[0925]
实例a
[0926]
针对蚤(猫栉首蚤(ctenocephalidesfelis))的摄食活性的体外评价
[0927]
对于蚤摄取测试,使用dmso对化合物储备液进行连续稀释,以达到ec
50
和ec
90
测定的所需范围。将各化合物稀释液的等分试样加入到最终dmso浓度为0.5%的有机牛血中,并置于人工喂养容器中。氟虫腈(fipronil)包括其中作为阳性对照。将来自实验室菌落的10只新出现的未进食的成年蚤,0至7天龄猫栉首蚤吸入各小瓶或笼0中。将用于蚤摄取测定的笼子保持在温度受控的人工饲养装置中,以允许连续获取含有所需浓度的化合物的有机牛血。在研究期间每天提供掺入化合物的牛血的新鲜等分试样。在侵染后2小时至48小时之间的不同时间点评价蚤的死亡率百分比。表现出正常运动和/ 或跳跃能力的蚤被认为是有活力的,而在轻敲小瓶后表现无运动的蚤被评定为死亡。
[0928]
在该试验中,例如,来自制备实例的以下化合物显示ec50《1ppm:实例2.1或2.2; 3.1或3.2;3.3或3.4;3.8;3.19或3.20;3.21或3.22;3.23;3.27,3.28,3.29或3.30; 3.34或3.35;3.36或3.37;3.38或3.39;3.40或3.41;3.43或3.44;3.45或3.46;3.49; 3.50;3.51;3.52;3.53;3.55;3.62;3.65;3.66;3.71;3.73;3.74;3.76;3.77;3.78 或3.79;3.80:3.83;3.84;3.85;3.86;3.87;3.90;3.91;3.93;5.1;8.1或8.2;8.3或 8.4;8.5或8.6;9.1或9.2;以及9.3或9.4;以及10.1或10.2。
[0929]
在该试验中,例如,来自制备实例的以下化合物显示ec50《3ppm:实例1.1或1.2; 3.5或3.6;3.15;3.16或3.17;3.25;3.26;3.47;3.61;3.72;以及3.75;3.81;3.75; 3.92;以及4.3或4.4。
[0930]
对于上述数据,当测试单一异构体时,在不知道异构体的绝对构型的情况下,数据表明测试制品是一种异构体或另一种异构体,例如测试来自实例2的单一异构体并给出 ec
50 of《1ppm,因此上述数据表明对于“2.1或2.2”获得结果。
[0931]
实例b
[0932]
对成年蜱(血红扇头蜱(rhipicephalus sanguineus))的接触活性的体外评价
[0933]
对于蜱试验,预先钻取小瓶盖,在每个瓶盖的中心具有单个孔以允许空气交换。将滤纸(whatman等级5402.1cm)置于每个小瓶的盖子中。将来自各化合物储备液的等分试样添加到丙酮/曲拉通(triton)溶液中,以得到用于研究的所需最高剂量。从最高剂量进行系列稀释,以达到ec
50
和ec
90
测定的所需滴定范围。每个测试小瓶中的最终 dmso浓度为0.5%。将各化合物制剂的459μl等分试样转移至含有whatman等级540 2.1cm滤纸的小瓶中。将小瓶立即放置在未加热的辊单元上,以使得小瓶壁均匀涂覆。小瓶被涂覆后,将每种化合物41μl制剂加入到包埋在各小瓶盖中的滤纸中。使每个盖干燥。将小瓶松散地加盖,并使其在化学通风橱中干燥至少4小时。将10只成年蜱加入到每个小瓶中并保持在24℃,80%湿度下12小时光/暗循环。在侵染后2小时至48 小时之间的不同时间点评估成年蜱的死亡率百分比。在加热的滚筒装置上刺激蜱,并评价。未表现出运动或非常缓慢和不协调运动的蜱被记录为死亡。
[0934]
实例c
[0935]
对比格犬给药后的pk测定
[0936]
对比格犬评价单一口服或静脉内剂量的所需化合物的行为。动物(n=6)通过经口管饲法(3或10mg/kg)或静脉内剂量(1或2mg/kg)接受化合物。在给药前和给药后 0.25、0.5、1、2、4、8、24、48、72、96、168、336、504、672、1008、1344、1680、 2016、2352、2688、2856和3024小时收集血样。将每份全血样品的一部分加工成血浆。使用lc-ms/ms测定血浆和全血中的供试品浓度。
[0937]
供试品的结果总结在下表中:
[0938][0939]
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1