检测人外周血白细胞中基因C4BPAmRNA的特异性引物对、试剂和试剂盒及其应用的制作方法
本申请是申请日为2019年04月01日、申请号为201910255608.1、发明名称为《人外周血细胞补体抑制剂c4bpamrna检测预测氯吡格雷抵抗及其试剂盒的制备》的分案申请,申请人为南京市第一医院。
本发明属于生物检测领域,涉及一种检测人外周血白细胞中基因c4bpamrna的特异性引物对、试剂和试剂盒及其应用。
背景技术:
作为一种经典的抗血小板药物,氯吡格雷常用于脑卒中、急性冠脉综合征(acs)和经皮冠脉介入(pci)术植入药物涂层支架后(预防支架内血栓形成),与阿司匹林合用所组成的“双抗血小板治疗”方案是acs或pci术后(植入支架)抗血小板治疗方案的“金标准”,被世界各国广泛认可与采纳。氯吡格雷抵抗(或耐受)是指病人在服用推荐剂量的氯吡格雷后达不到预期的抗血小板作用,导致临床疗效较差或无效的现象。据估计,约10%~45%的服药病人可能有氯吡格雷抵抗。
判断氯吡格雷临床疗效的“金标准”是冠脉造影,而替代指标是服药前、后adp诱导的血小板聚集的抑制率大小,根据抑制率大小来反映氯吡格雷抵抗的有或无。但是,血小板聚集率检测的重复性欠佳,难以精准指导临床合理使用氯吡格雷。
氯吡格雷抵抗的形成原因较多,但详细机制并不十分清楚。临床上也缺乏有效的预测氯吡格雷抵抗的生物标志物。目前,检测病人cyp2c19基因型被推荐作为指导病人合理用药的依据之一。国外学者fontanap(2013)等报道,cyp2c19基因分型预测氯吡格雷抵抗的灵敏度只有37.6%,与我们的数据30.4%较接近,显示其临床诊断价值或预测意义十分有限。dna基因分型只能进行定性分析,mrna的相对表达水平可以定量分析,对预测不同个体的基因转录水平有更大帮助。
技术实现要素:
本发明的主要目的是针对现有相关技术的上述不足,提供一种全新的预测氯吡格雷抵抗的生物标志物的应用。
本发明的另一个目的是提供一种预测氯吡格雷抵抗的全新试剂盒。
本发明的目的可通过以下技术方案实现:
一种人外周血白细胞中补体抑制剂基因c4bpa的mrna作为检测靶点在制备预测氯吡格雷抵抗的试剂盒中的应用。
检测人外周血白细胞中补体抑制剂基因c4bpa的mrna的试剂在制备预测氯吡格雷抵抗的试剂盒中的应用。一种预测氯吡格雷抵抗的试剂盒,包含检测人外周血白细胞中补体抑制剂基因c4bpamrna的试剂。
其中,所述的检测人外周血白细胞中补体抑制剂基因c4bpamrna的试剂优选检测人外周血白细胞中补体抑制剂基因c4bpamrna的特异性引物序列;进一步优选如seqidno.1和seqidno.2所示的检测人外周血白细胞中补体抑制剂基因c4bpamrna的特异性引物序列。
一种预测氯吡格雷抵抗的试剂盒,包含检测人外周血白细胞中补体抑制剂基因c4bpamrna的试剂。
其中,所述的检测人外周血白细胞中补体抑制剂基因c4bpamrna的试剂优选检测人外周血白细胞中补体抑制剂基因c4bpamrna的特异性引物序列;进一步优选如seqidno.1和seqidno.2所示的检测人外周血白细胞中补体抑制剂基因c4bpamrna的特异性引物序列。
有益效果:
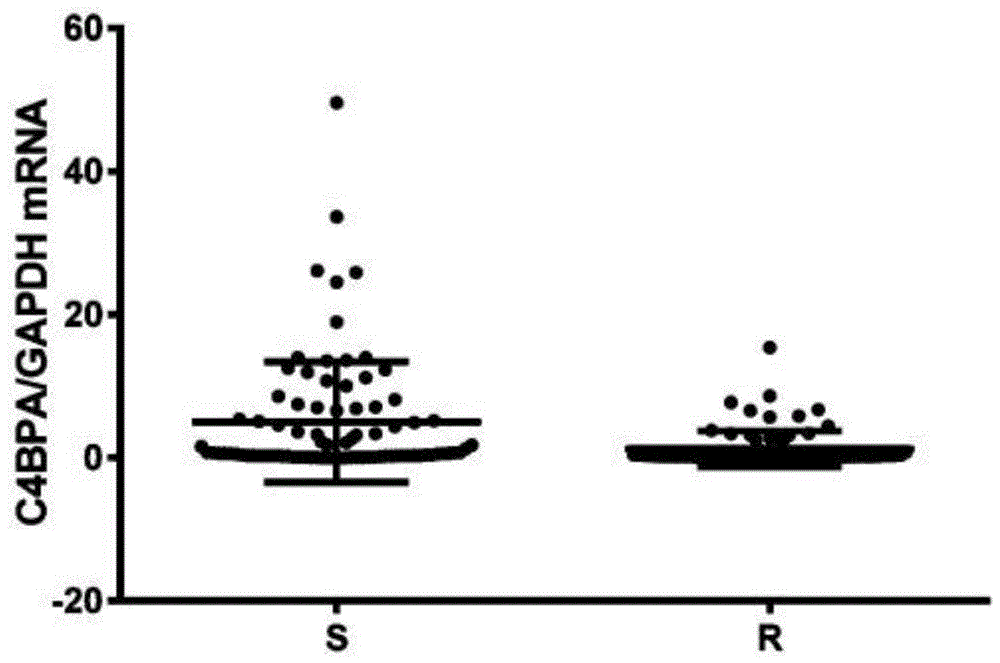
本发明发现人外周血白细胞中补体抑制剂基因c4bpa的mrna相对表达量在对氯吡格雷反应的敏感者和抵抗(或不敏感)者间存在显著差异,即对氯吡格雷反应敏感者的外周血白细胞中c4bpa的mrna表达水平显著高于对氯吡格雷反应抵抗者的表达水平(见图1)。基于上述发现,本发明提供了一种全新的预测氯吡格雷抵抗的标志物,即人外周血白细胞中补体抑制剂基因c4bpa的mrna,该标志物作为检测靶点以辅助预测或判断病人服药后的临床疗效或预后。本发明还提供一种检测氯吡格雷抵抗的试剂盒,包括检测该标志物的引物序列;使用该试剂盒预测氯吡格雷抵抗,其诊断敏感性(真阳性率)和特异性(真阴性率)均显著高于cyp2c19基因型作为生物标志物用于预测氯吡格雷抵抗的诊断敏感性和特异性。
附图说明
图1.人外周血白细胞c4bpa的mrna相对表达量及其在氯吡格雷敏感者(s)和抵抗者(r)两组间的差异(mean±sd:5.002±8.416vs.1.219±2.519;svs.r;p<0.0001)。
图2.人外周血白细胞c4bpamrna诊断氯吡格雷抵抗的roc曲线。
具体实施方式
实施例1.人外周血白细胞中c4bpa的mrna表达水平在制备检测氯吡格雷抵抗的试剂盒中的应用。
一、检测氯吡格雷抵抗的试剂盒,包括以下成分:
trizol试剂;
氯仿;
异丙醇;
depc水
gdnaeraser
5×gdnaeraserbuffer
5×
rtprimermix
rnase-freedh2o
roxreferencedyeii(50×)
针对c4bpamrna检测的特异性引物序列seqidno.1和seqidno.2。
mrna定量分析时所需内参照gapdh的引物对(seqidno.3和seqidno.4)。
二、试剂盒的使用方法
提取病人外周血白细胞的总rna,用qrt-pcr技术检测其中c4bpa的mrna表达水平。具体操作步骤,如下所示。
1)外周血白细胞总rna提取:
(1)白细胞,加入1mltrizol;
(2)充分混匀,室温下静置5min;
(3)加200μl氯仿,上下剧烈摇晃或涡旋震动15s,室温下静置10min;
(4)离心12000×g,4℃,15min;
(5)吸取含有总rna的上清,转移至新的1.5mlep管中,加入等体积异丙醇后颠倒混匀,室温下静置10min;
(6)离心12000×g,4℃,10min,弃上清;
(7)加入1ml75%乙醇(由depc水配制)涡旋震荡混匀;
(8)离心7500×g,4℃,5min,弃上清;
(9)室温放置,挥干rna沉淀,约10min;
(10)待rna无明显液滴时,加10μlrnase-freedh2o(或depc水),冰上静置10min;
(11)混匀,置冰上备用。
2)rna的定量与纯度测定:
取上述rna2μl,加入tecan检测板,通过tecan酶标仪测定其浓度并根据在260nm和280nm处的光密度值(即od260与od280)比值,判断rna的纯度。比值小于1.6表明样品中含有蛋白质,大于1.9表明样品纯度很高,介于二者之间表明含有不同程度的dna。
3)rna逆转录为cdna(在冰上操作):
(1)基因组dna的去除反应:
反应条件为42℃,2min,4℃保存。
(2)逆转录反应(生成其cdna):
反应条件为37℃,15min,85℃,5s,4℃保存。
4)荧光定量pcr实验步骤(在冰上操作):
实时荧光定量pcr(应用abi7500real-timepcrsystem的操作方法)检测c4bpa的cdna水平,采用sybrpremixextaqtm(大连takarabiotechco.,ltd.)荧光定量pcr试剂。
引物设计见表1,反应体系20μl,包含:
pcr反应条件:预变性:95℃,30s;pcr反应:95℃,5s,60℃,34s,共40个循环。
溶解曲线:95℃,15s,60℃,1min,95℃,15s。
荧光定量pcr的结果以每个反应管内的荧光信号达到设定的阈值时所经历的循环数(ct值表示)。δct=ct(c4bpa)–ct(gapdh),结果采用2-δδct计算c4bpa的mrna相对表达量。
表1.qrt-pcr引物及其序列
*c4bpa是编码c4bpα肽链的基因。
三、有效性
选取165名冠心病病人,经皮冠脉介入(pci)植入药物涂层支架后,口服氯吡格雷75mg/天和阿司匹林100mg/天长达至少6个月,预约来医院门诊进行冠脉造影复查。造影前抽取病人早晨空腹静脉血1管(约1ml),枸橼酸抗凝(蓝盖管)用于adp诱导的全血血小板聚集率测定,用剩余的全血提取血细胞总rna。
根据测得的全血血小板聚集率将病人分为两组(参考文献,以5欧姆为分界点),其中:
阴性组:对氯吡格雷反应敏感者(s),血小板聚集率为0–5欧姆,共85名;
阳性组:对氯吡格雷反应抵抗者(r),血小板聚集率>5欧姆,共80名。
根据上述实验方法提取病人外周血白细胞rna,用qrt-pcr检测其中c4bpa的mrna含量。本发明以85名对氯吡格雷反应敏感者(s)外周血白细胞中c4bpa的mrna表达水平作为(氯吡格雷抵抗)阴性组,以80名氯吡格雷反应抵抗者(r)外周血白细胞中c4bpa的mrna表达水平作为(氯吡格雷抵抗)阳性组,分别检测并比较两组之间c4bpa的mrna表达水平的差异(见图1);建立c4bpa的mrna表达水平诊断氯吡格雷抵抗的roc曲线(见图2)。结果显示,roc曲线下面积(auc)为0.725(95%ci:0.647–0.802,p<0.0001)。诊断敏感性(真阳性率)为74.1%,特异性(真阴性率)为68.8%,约登(youden)指数j为0.429,诊断氯吡格雷抵抗的最佳临界(cutoff)值为0.265。
- 还没有人留言评论。精彩留言会获得点赞!