一种含硼有机化合物及含有其的有机光电元件与应用的制作方法
1.本发明属于有机光电技术领域,尤其涉及一种含硼有机化合物及含有其的有机光电元件,特别是有机电致发光二极管。
背景技术:
2.有机光电元件中,尤其是有机电致发光器件(oled)、有机场效应晶体管(ofet)、有机太阳能电池(opv)引起了众多科学家和产业界的研究。其中,oled作为新一代的平板显示技术逐渐进入人们的视野,其广泛的应用前景和近年来技术上的突飞猛进使得oled成为平板信息显示领域和科学研究产品开发最热门的研究之一。oled技术在显示和照明领域的发展一直受蓝光oled的效率和寿命的制约,高效率蓝光oled可明显提高显示逼真性,降低显示和照明器件的功耗。尤其是蓝光oled器件发光效率低的主要原因有两点,一、核心蓝光客体材料发光效率低;二、蓝光主体材料和客体材料之间能量传输效率低,主要是三线态激子利用率不高。
技术实现要素:
3.为了解决现有oled技术中存在的oled元件电流效率低,操作电压高等问题,本发明的目的在于提供一种新型有机化合物及含有该化合物的有机光电元件,从新材料设计角度给出具有高效发光效率的有机化合物;从有机光电元件角度,明显改善有机光电器件中电荷传输平衡性好和三线态激子能量利用率高的元件结构,可以使得使用本发明提供的有机化合物和含有该化合物的有机光电元件,特别是oled具有更高电流效率,低的操作电压,明显改善oled的综合性能。
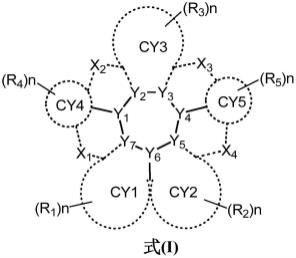
4.本发明提供了一种新型的含硼有机化合物,所述的含硼有机化合物的结构由式(i)表示:
[0005][0006]
其中,y1至y7构成独立选自碳原子、氮原子、硼原子中的一个,且至少有一个为硼原子,相邻的y1至y7不形成b—n、n—n、或b—b键;环cy1至环cy5独立构成五元环、或六元环、或七元环,且cy1或cy2至少有一个为五元环;x1至x4独立地为不存在、或独立选自单键、o、s、nr6、cr6r7、sir6r7、o=p-r6、b-r6中的一种;r1至r7独立选自氢、氘、cn、卤素、c1~c60烷基、c1~c60烷氧基、含c1~c60烷硅基、含c1~c60烷氧硅基、取代或未取代c6~c60的芳
基、取代或未取代c1~c60的杂芳基、取代或未取代的烯基、取代或未取代的芳基醚基、取代或未取代的杂芳基醚基、取代或未取代的芳基胺基、取代或未取代的杂芳基胺基、取代或未取代的芳基硅基、取代或未取代的杂芳基硅基、取代或未取代的芳基氧硅基、取代或未取代的芳基酰基、取代或未取代的杂芳基酰基、取代或未取代的氧膦基中的任意一种;杂芳基是指含有b、n、o、s、p(=o)、si、p中至少一个杂原子;当r1至r6为两个或以上时,可以相同或不同,相邻的基团可以成环;n根据价键原理独立选自0,1,2,3,4,5,或6;所有基团可以被部分氘代或全氘代,可以被部分氟代或全氟代。
[0007]
本发明要保护的含硼有机化合物的结构由式i-1至式i-6表示,但不代表限于此:
[0008]
在式i-1至式i-6中,x1至x4独立地为不存在、或独立选自单键、o、s、nr6、cr6r7、sir6r7、o=p-r6、b-r6中的一种;y1至y4构成独立选自碳原子、氮原子、硼原子中的一个,且至少有一个为硼原子,相邻的y1至y4不形成b—n、n—n、或b—b键;z独立选自o、s、nr2、cr2r1、sir2r2、o=p-r2、b-r2中的一种;z1、z2、z4、z5、z6独立选自n或cr1;z3选自n或b,y1—z3不形成b—n、n—n、或b—b键;环cy3至cy5独立构成五元环或六元环,r1至r7独立选自氢、氘、cn、卤素、c1~c60烷基、c1~c60烷氧基、含c1~c60烷硅基、含c1~c60烷氧硅基、取代或未取代c6~c60的芳基、取代或未取代c1~c60的杂芳基、取代或未取代的烯基、取代或未取代的芳基醚基、取代或未取代的杂芳基醚基、取代或未取代的芳基胺基、取代或未取代的杂芳基胺基、取代或未取代的芳基硅基、取代或未取代的杂芳基硅基、取代或未取代的芳基氧硅基、取代或未取代的芳基酰基、取代或未取代的杂芳基酰基、取代或未取代的氧膦基中的任意一种;杂芳基是指含有b、n、o、s、p(=o)、si、p中至少一个杂原子;当r1至r7为两个或以上时,可以相同或不同,相邻的基团可以成环;n根据价键原理独立选自0,1,2,3,4,5,或6;所有基团可以被部分氘代或全氘代,可以被部分氟代或全氟代。
[0009]
优选地,本发明的含硼有机化合物的结构由式i-1a至式i-6f表示,但不代表限于此:
[0010][0011]
其中,z7至z10选自n或cr3;x1至x4、y1至y4、z、z1至z6、环cy4至cy5、r1至r7与上述的定义相同。
[0012]
优选地,本发明要求保护的含硼有机化合物代表地独立选自式1至式76所表示的代表结构中的一种或多种,但不代表限于此:
[0013]
[0014][0015]
其中,x1至x4,z,z1至z10,环cy4、cy5,r1至r7与上述的定义相同。
[0016]
特别优选地,本发明所述的含硼有机化合物选自以下结构的一种或多种,但不代表限于此:
[0017]
[0018]
[0019]
[0020]
[0021]
[0022]
[0023]
[0024]
[0025]
[0026]
[0027]
[0028]
[0029]
[0030]
[0031]
[0032]
[0033]
[0034]
[0035][0036]
其中,r1至r7独立选自氢、氘、cn、卤素、c1~c60烷基、c1~c60烷氧基、含c1~c60烷硅基、含c1~c60烷氧硅基、取代或未取代c6~c60的芳基、取代或未取代c1~c60的杂芳基、取代或未取代的烯基、取代或未取代的芳基醚基、取代或未取代的杂芳基醚基、取代或未取代的芳基胺基、取代或未取代的杂芳基胺基、取代或未取代的芳基硅基、取代或未取代的杂芳基硅基、取代或未取代的芳基氧硅基、取代或未取代的芳基酰基、取代或未取代的杂芳基酰基、取代或未取代的氧膦基中的任意一种;杂芳基是指含有b、n、o、s、p(=o)、si、p中至少一个杂原子;当r1至r7为两个或以上时,可以相同或不同,相邻的基团可以成环;n根据价键原理独立选自0,1,2,3,4,5,或6;所有基团可以被部分氘代或全氘代,可以被部分氟代或全氟代。
[0037]
优选地,以上系列结构式中的r1至r7独立选自以下结构的一种或多种的组合,但不代表限于此:
[0038]
[0039][0040]
优选地,本发明所述的含硼有机化合物选自以下代表结构的一种,但不代表本发明限于此:
[0041]
[0042]
[0043]
[0044][0045]
本发明还提供一种制剂,用本发明所述的含硼有机化合物可以和至少一种溶剂或有机化合物组成。所用的有机溶剂或有机化合物没有特别限制,可以是如甲苯、二甲苯、均三甲苯、四氢化萘、十氢萘、双环己烷、正丁基苯、仲丁基苯、叔丁基苯等不饱和烃溶剂、四氯化碳、氯仿、二氯甲烷、二氯乙烷、氯丁烷、溴丁烷、氯戊烷、溴戊烷、氯己烷、溴己烷、氯环己烷、溴环己烷等卤化饱和烃溶剂,氯苯、二氯苯、三氯苯等卤化不饱和烃溶剂,四氢呋喃、四氢吡喃等醚溶剂,苯甲酸烷基酯等酯类溶剂或有机化合物。
[0046]
本发明要求保护一种有机光电元件,包括衬底、位于所述衬底上的阳极层,位于所述阳极层上的功能层,位于所述功能层上的阴极层。
[0047]
本发明的有机光电元件,所述功能层包括空穴注入层、空穴传输层、电子阻挡层、发光层或活性层、空穴阻挡层、电子传输层以及电子注入层或者他们的组合中的一种;所述功能层由本发明所述的含硼有机化合物与一种或多种有机化合物混合构成。功能层还含有其他有机化合物、金属或金属化合物作为掺杂剂。
[0048]
本发明所述的有机光电元件是有机光伏器件、有机发光器件(oled)、有机太阳电池(osc)、电子纸(e-paper)、有机感光体(opc)、有机薄膜晶体管(otft)及有机内存器件(organic memory element)、照明和显示装置中任意一种。
[0049]
在本发明中,有机光电元件是可以利用喷溅涂覆法、电子束蒸发、真空蒸镀等方法在基板上蒸镀金属或具有导电性的氧化物以及它们的合金形成阳极;在制备得到的阳极表面按顺序蒸镀空穴注入层、空穴传输层、发光层或活性层、空穴阻挡层和电子传输层,再蒸镀阴极的方法制备。除以上方法以外在基板上按阴极、有机物层、阳极顺序蒸镀制作有机光电元件。所述有机物层是也可以包括空穴注入层、空穴传输层、发光层或活性层、空穴阻挡层及电子传输层等多层结构。
[0050]
根据本发明中的有机电致发光元件可以分为顶发射、低发射或双面发射。
[0051]
本发明还要求保护含有这种有机电致发光元件的显示器装置,特别是以amoled或pmoled为基础的显示装置,包括手机、相机、平板、电脑、电视、投影、微显示、电子书等显示屏,用于构筑显示装置的像素单元。
[0052]
本发明还要求保护含有有机电致发光元件的照明装置或背板光源,包括oled灯具,汽车尾灯、led、lcd元件背光源等。
[0053]
本发明提供了一种新型的含硼有机化合物并应用于有机光电元件中,特别是有机电致发光二极管,与已有方案不同的是,本发明的化合物硼和氮中间至少间隔了一个或两个碳原子,形成了类似七元环的方案。采用本发明的有机化合物和相应的主体材料作为oled元件的发光层,主体和客体间的能量传输十分高效,获得的oled器件在效率、电压和使用寿命上与已知的含硼有机化合物相当,有些具有更好的效果。说明本发明的设计方案具有商业应用前景。
附图说明
[0054]
图1为本发明有机发光元件的结构示意图。
具体实施方式
[0055]
为了使本技术领域的人员更好地理解本技术方案,下面将结合本技术实施例中的附图,对本技术实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本技术一部分实施例,而不是全部的实施例。基于本技术中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本技术保护的范围。
[0056]
化合物的合成:
[0057]
根据本领域的技术基础(参考文献:j.am.chem.soc.2018,140,1195),本发明涉及的化合物可以通过以下反应路径进行合成.
[0058]
[0059]
以含卤素的取代芳烃或杂芳烃为原料,与二取代芳基或杂芳基胺在钯催化下获得关键中间体,结合已有的参考文献的方法,将此关键中间体与三卤化硼进行反应,得到本发明结构式(i)所述的中间体1-22。
[0060][0061]
通用合成步骤(1):在氮气氛下,于圆底烧瓶中将含卤素的取代芳烃或杂芳烃(10毫摩尔)和1.1~3.3当量的rr’nh完全溶解于二甲苯(80ml)中后,向其中添加叔丁醇钠(5~15克),双(三-叔丁基膦)钯(0.1~0.3g),将混合物加热回流6-18小时。降至室温后,过滤除去盐,将溶剂真空浓缩后,用石油醚:二氯甲烷(20:1~2:1)作为淋洗剂在硅胶柱上进行纯化分离,得到目标中间体,用lcms,1h nmr确定结构。
[0062]
通用步骤(2)在氮气保护下,通用步骤(1)得到的中间体—二芳胺基芳烃或杂芳烃(10毫摩尔)溶解在邻二氯苯(30毫升)中,滴加到三碘化硼(30毫摩尔)、三苯基硼(20毫摩尔)、邻二氯苯(80毫升)的溶液中,升温至回流反应48小时,反应结束冷却至室温,混合物滴加到冰水(200毫升),用二氯甲烷进行萃取。以上所有二氯甲烷溶液合并后,用饱和食盐水(80毫升)清洗3次,再用10%碳酸氢钠溶液(80毫升)洗涤两次,用无水硫酸镁干燥,减压蒸馏除去二氯甲烷和邻二氯苯溶剂,粗产品用冷石油醚洗涤,用石油醚/二氯甲烷过硅胶柱本发明所述的含硼有机化合物,通过nmr,lcms检测确定结构。化合物最后通过高真空升华提纯,用于制备有机光电元件。
[0063]
通用步骤(3)在氮气保护下,通用步骤(1)得到的中间体—二芳胺基卤代芳烃或杂芳烃(10毫摩尔)溶解在无水四氢呋喃(50毫升)中,在-78度下滴加正丁基锂溶液(12毫摩尔),反应液继续反应1小时后,滴加到三碘化硼(20毫摩尔)、乙醚(50毫升)的溶液中(-78度),缓慢升温至室温反应2小时。继续在反应液中补加邻二氯苯(80毫升)减压蒸馏除去乙醚、四氢呋喃,加入三苯基硼(20毫摩尔),升温至回流(190度左右)反应48小时,反应结束冷却至室温,混合物滴加到冰水(200毫升),用二氯甲烷进行萃取。以上所有二氯甲烷溶液合并后,用饱和食盐水(80毫升)清洗3次,再用10%碳酸氢钠溶液(80毫升)洗涤两次,用无水硫酸镁干燥,减压蒸馏除去二氯甲烷和邻二氯苯溶剂,用石油醚/二氯甲烷过硅胶柱本发明所述的有机化合物,通过h nmr,lcms检测确定结构。化合物最后通过高真空升华提纯,用于制备有机光电元件。
[0064]
实施例1:化合物1的合成
[0065]
中间体1,以通用步骤(1)的方法合成,产率74%;ms(esi):理论值,508.25;实测,508.2;1h nmr(500mhz,cdcl3δ)ppm:1.51(s,9h),6.97-7.02(m,4h),7.08-7.09(m,4h),7.15-7.18(m,2h),7.22-7.26(m,9h),7.30(dd,1h),7.48(d,1h),7.76(d,1h)。
[0066]
化合物1用通用步骤(2)的方法合成,产率41%;ms(esi):理论值,516.24;实测,517.2(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.56(s,9h),6.87-7.00(m,3h),7.01-7.09(m,4h),7.15(s,1h),7.19-7.28(m,6h),7.35-7.41(m,3h),7.48(d,1h),7.71(d,1h)。
[0067]
实施例2:化合物2的合成
[0068]
中间体2,用通用步骤(1)的方法合成,产率84%;ms(esi):理论值,524.23;实测,524.2;1h nmr(500mhz,cdcl3δ)ppm:1.46(s,9h),6.97-7.02(m,4h),7.06-7.10(m,4h),7.16(d,1h),7.21-7.28(m,12h),7.68(s,1h),7.73(d,1h)。
[0069]
化合物2用通用步骤(2)的方法合成,产率为43%;ms(esi):理论值,532.21;实测,533.2(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.49(s,9h),6.86-7.08(m,7h),7.11(dd,1h),7.19-7.27(m,5h),7.36(dd,1h),7.39-7.48(m,3h),7.68-7.75(m,3h)。
[0070]
实施例3:化合物3的合成
[0071]
中间体3,用通用步骤(1)的方法合成,产率88%;ms(esi):理论值,732.5;实测,732.5;1h nmr(500mhz,cdcl3δ)ppm:1.30(s,18h),1.32(s,18h),1.52(s,9h),7.03-7.16(m,2h),7.10-7.19(m,8h),7.20-7.29(m,7h),7.43(d,1h),7.76(s,1h)。
[0072]
化合物3用通用步骤(2)的方法合成,产率为48%;ms(esi):理论值,740.49;实测,741.5(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.33(s,18h),1.36(s,18h),1.57(s,9h),6.85(d,1h),6.87(d,1h),7.06(d,2h),7.16-7.21(m,3h),7.32-7.39(m,5h),7.40(d,2h),7.46(s,1h),7.56(s,1h)。
[0073]
实施例4:化合物4的合成
[0074]
中间体4,用通用步骤(1)的方法合成,产率82%;ms(esi):理论值,748.48;实测,748.5;1h nmr(500mhz,cdcl3δ)ppm:1.31(s,18h),1.33(s,18h),1.46(s,9h),7.08-7.13(m,6h),7.15-7.27(m,11h),7.63(s,1h),7.75(d,1h)。
[0075]
化合物4用通用步骤(2)的方法合成,产率为45%;ms(esi):理论值,756.46;实测,757.5(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.34(s,18h),1.36(s,18h),1.49(s,9h),6.81(d,1h),6.97(d,1h),7.02(d,2h),7.13-7.19(m,3h),7.31-7.39(m,5h),7.42(d,1h),7.46(s,1h),7.56(s,1h),7.76(d,1h)。
[0076]
实施例5:化合物5的合成
[0077]
中间体5,用通用步骤(1)的方法合成,产率87%;ms(esi):理论值,564.22;实测,564.2;1h nmr(500mhz,cdcl3δ)ppm:1.49(s,9h),6.56(s,1h),7.00-7.09(m,7h),7.21-7.33(m,11h),7.50(d,1h),7.86(s,1h),7.92-7.99(m,2h)。
[0078]
化合物5,用通用步骤(3)的方法合成,产率52%;ms(esi):理论值,572.21;实测,573.2(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.51(s,9h),6.99-7.09(m,9h),7.15-7.26(m,5h),7.30(dd,1h),7.39(dd,1h),7.46(d,1h),7.76(d,1h),7.81(d,1h),7.96(d,1h)。
[0079]
实施例6:化合物6的合成
[0080]
中间体6,用通用步骤(1)的方法合成,产率86%;ms(esi):理论值,788.47;实测,
788.5;1h nmr(500mhz,cdcl3δ)ppm:1.29(s,18h),1.31(s,9h),1.41(s,9h),1.48(s,9h),6.46(s,1h),7.04-7.11(m,4h),7.17-7.29(m,8h),7.30(d,1h),7.39(d,1h),7.51(d,1h),7.74(s,1h),7.81(d,1h),7.94(s,1h)。
[0081]
化合物6用通用步骤(3)的方法合成,产率58%;ms(esi):理论值,796.46;实测,797.5(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.30(s,9h),1.31(s,9h),1.33(s,9h),1.43(s,9h),1.51(s,9h),7.01-7.06(m,6h),7.23-7.33(m,6h),7.40-7.42(m,2h),7.80(d,1h),7.84(s,1h)。
[0082]
实施例7:化合物8的合成
[0083]
中间体8,用通用步骤(1)的方法合成,产率84%;ms(esi):理论值,788.47;实测,788.5;1h nmr(500mhz,cdcl3δ)ppm:1.28(s,9h),1.30(s,18h),1.40(s,9h),1.49(s,9h),6.33(s,1h),7.15(d,2h),7.17-7.20(m,4h),7.23-7.68(m,6h),7.35-7.41(m,2h),7.51(d,1h),7.69(s,1h),7.72(d,1h),7.84(s,1h)。
[0084]
化合物8用通用步骤(3)的方法合成,产率63%;ms(esi):理论值,796.46;实测,797.5(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.28(s,9h),1.34(s,9h),1.35(s,9h),1.44(s,9h),1.48(s,9h),6.99-7.05(m,6h),7.25-7.29(m,5h),7.31(s,1h),7.45-7.47(m,2h),7.78(d,1h),7.81(s,1h)。
[0085]
实施例8:化合物10的合成
[0086]
中间体10,用通用步骤(1)的方法合成,产率91%;ms(esi):理论值,532.29;实测,532.3;1h nmr(500mhz,cdcl3δ)ppm:1.48(s,9h),1.88(s,6h),6.95-7.03(m,2h),7.07-7.09(m,5h),7.21-7.32(m,6h),7.51-7.52(m,2h),7.58-7.61(m,2h),7.86(d,1h),7.93-7.96(m,2h),8.18(s,1h)。
[0087]
化合物10用通用步骤(2)的方法合成,产率41%;ms(esi):理论值,540.27;实测,541.3(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.47(s,9h),1.91(s,6h),6.91-7.18(m,6h),7.24(dd,2h),7.33-7.42(m,4h),7.52(dd,1h),7.68(d,1h),7.82(d,1h),7.87(d,1h),7.96(d,1h),8.12(s,1h)。
[0088]
实施例9:化合物11的合成
[0089]
中间体11,用通用步骤(1)的方法合成,产率89%;ms(esi):理论值,530.27;实测,530.3;1h nmr(500mhz,cdcl3δ)ppm:1.47(s,9h),1.85(s,6h),7.06(d,1h),7.23-7.42(m,5h),7.57-7.62(m,2h),7.76(d,1h),7.81(d,1h),7.88(d,1h),7.98-8.02(m,3h),8.05(d,1h),8.14(s,1h),8.33(d,1h),8.38(d,1h),8.50(s,1h)。
[0090]
化合物11用通用步骤(2)的方法合成,产率43%;ms(esi):理论值,538.26;实测,539.3(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.45(s,9h),1.81(s,6h),7.13(d,1h),7.33(d,1h),7.35-7.42(m,3h),7.57(dd,1h),7.62(d,1h),7.70(d,1h),7.83(d,1h),7.98(d,1h),7.99-8.02(m,2h),8.11(d,1h),8.16(s,1h),8.36(dd,1h),8.48(d,1h)。
[0091]
实施例10:化合物12的合成
[0092]
中间体12,用通用步骤(1)的方法合成,产率86%:ms(esi):理论值,700.48;实测,700.5;1h nmr(500mhz,cdcl3δ)ppm:1.29(s,18h),1.31(s,9h),1.45(s,9h),1.78(s,6h),7.08-7.18(m,5h),7.24-7.32(m,5h),7.38(d,2h),7.50-7.52(m,2h),7.80-7.82(m,2h),7.88(d,1h),8.14(s,1h)。
[0093]
化合物12用通用步骤(3)的方法合成,产率68%;1h nmr(500mhz,cdcl3δ)ppm:1.29(s,18h),1.35(s,9h),6.84(d,1h),6.88-6.94(m,3h),7.09-7.16(m,4h),7.21(d,1h),7.31-7.36(m,4h),7.50(d,1h),7.58(dd,1h),7.65-7.77(m,4h),7.90(d,1h);ms(esi):理论值638.38;实测,638.4。
[0094]
实施例11:化合物13的合成
[0095]
中间体13,用通用步骤(1)的方法合成,产率85%:ms(esi):理论值698.46;实测,698.4;1h nmr(500mhz,cdcl3δ)ppm:1.31(s,9h),1.45(s,18h),1.47(s,9h),1.85(s,6h),7.10(d,1h),7.24(d,1h),7.55-7.62(m,3h),7.73-7.79(m,2h),7.86(d,1h),7.90-7.94(m,2h),8.00-8.04(m,2h),8.16(s,1h),8.35-8.40(m,3h)。
[0096]
化合物13用通用步骤(2)的方法合成,产率44%;ms(esi):理论值706.45;实测,707.5(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.38(s,9h),1.41(s,9h),1.43(s,9h),1.49(s,9h),1.87(s,6h),7.14(d,1h),7.45(d,1h),7.66(d,1h),7.68(s,1h),7.73(d,1h),7.77(s,1h),7.87(d,1h),7.92(d,1h),8.04(d,1h),8.14(d,1h),8.19(s,1h),8.41-8.45(m,2h)。
[0097]
实施例12:化合物14的合成
[0098]
中间体14,用通用步骤(1)的方法合成,产率90%;ms(esi):理论值,756.45;实测,756.5;1h nmr(500mhz,cdcl3δ)ppm:1.30(s,9h),1.31(s,9h),1.43(s,9h),1.46(s,9h),1.82(s,6h),6.39(s,1h),7.08(d,1h),7.20(d,2h),7.26(d,2h),7.30(d,1h),7.36(d,2h),7.42-7.45(m,3h),7.78(d,2h),7.82(d,1h),7.99(d,1h),8.03(s,1h)。
[0099]
化合物14用通用步骤(3)的方法合成,产率54%;ms(esi):理论值,764.43;实测,765.4(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.36(s,9h),1.38(s,9h),1.45(s,9h),1.49(s,9h),1.85(s,6h),6.88(d,1h),7.09(d,2h),7.16(d,1h),7.23(d,2h),7.31(d,1h),7.33(d,1h),7.40(s,1h),7.44-7.47(m,2h),7.58(d,1h),7.77-7.85(m,2h),7.98(s,1h)。
[0100]
实施例13:化合物15的合成
[0101]
中间体15,用通用步骤(1)的方法合成,产率87%;ms(esi):理论值,726.38;实测,726.4;1h nmr(500mhz,cdcl3δ)ppm:1.31(s,18h),1.32(s,9h),1.43(s,9h),6.99(d,1h),7.03(s,1h),7.05(d,1h),7.08(d,2h),7.10-7.17(m,3h),7.20-7.28(m,8h),7.35-7.39(m,2h),7.81(d,1h)。
[0102]
化合物15用通用步骤(3)的方法合成,产率57%;ms(esi):理论值,700.40;实测,701.4(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.35(s,9h),1.36(s,9h),1.43(s,9h),1.47(s,9h),6.79(d,1h),6.95(d,1h),7.03-7.06(m,3h),7.09-7.19(m,4h),7.08(d,2h),7.30-7.37(m,4h),7.40(dd,1h),7.45(s,1h),7.55(d,2h),7.99(d,1h)。
[0103]
实施例14:化合物18的合成
[0104]
中间体18,用通用步骤(1)的方法合成,产率82%;ms(esi):理论值,678.37;实测,678.4;1h nmr(500mhz,cdcl3δ)ppm:1.30(s,18h),1.41(s,9h),1.68(s,6h),7.05-7.09(m,3h),7.20-7.29(m,7h),7.33(dd,1h),7.43(dd,1h),7.56(dd,1h),7.64-7.69(m,2h),7.83(d,1h),7.88(s,1h),8.03(s,1h)。
[0105]
化合物18用通用步骤(3)的方法合成,产率52%;ms(esi):理论值,652.4;实测,653.4(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.34(s,9h),1.41(s,9h),1.47(s,9h),1.68(s,6h),6.95-7.09(m,2h),7.10-7.23(m,3h),7.33-7.39(m,4h),7.45(d,1h),7.51(dd,1h),
7.54(s,1h),7.63(d,1h),7.81(d,1h),7.95(d,1h),8.04(s,1h)。
[0106]
实施例15:化合物22的合成
[0107]
中间体22,用通用步骤(1)的方法合成,产率90%:ms(esi):理论值,732.45;实测,732.4;1h nmr(500mhz,cdcl3δ)ppm:1.25(s,18h),1.31(s,9h),1.46(s,9h),1.92(s,6h),7.09(d,2h),7.15(d,2h),7.17-7.29(m,9h),7.33(s,1h),7.40(d,2h),7.73(d,1h),7.87(d,1h)。
[0108]
化合物22用通用步骤(2)的方法合成,产率41%;ms(esi):理论值,740.43;实测,741.4(m+h
+
);1h nmr(500mhz,cdcl3δ)ppm:1.28(s,9h),1.29(s,9h),1.33(s,9h),1.36(s,9h),1.86(s,6h),6.98(d,1h),7.03(d,1h),7.15-7.33(m,5h),7.36-7.48(m,5h),7.53(s,1h),7.56(s,1h),7.78(d,1h)。
[0109][0110]
为了使本发明的目的、技术方案及优点更加清楚明白,结合具体发光器件实施例,对本发明进行进一步详细说明。应当理解,此处所描述的具体实施例仅仅用以解释本发明,并不用于限定本发明。
[0111]
在本发明的一种优选实施方式中,本发明的oled器件中含有空穴传输层,空穴传输材料可以优选自已知或未知的材料,如以下结构的一种或多种,但并不代表本发明限于此:
[0112][0113]
在本发明的一种优选实施方式中,本发明的oled器件中含有的空穴传输层,其包含一种或多种p型掺杂剂。本发明优选的p型掺杂剂为以下结构,但并不代表本发明限于以
下结构:
[0114][0115]
本发明中式(1)或(2)表示的化合物被用作空穴传输层、空穴注入层或激子阻挡层中的空穴传输材料,式(1)或(2)表示的化合物可以单独使用,也可以将式(1)或(2)表示的化合物与上述一种或多种p型掺杂剂共同形成。
[0116]
本发明的一种优选实施方式中,所述的电子传输层可以选自化合物et-1至et-13的至少一种,但并不代表本发明限于以下结构:
[0117][0118]
电子传输层可以有机材料与一种或多种n型掺杂剂(如liq)共同形成。
[0119]
本发明还提供一种包括所述组合物和溶剂的制剂,所用的溶剂没有特别限制,可以使用本领域技术人员熟知的例如甲苯、二甲苯、均三甲苯、四氢化萘、十氢萘、双环己烷、正丁基苯、仲丁基苯、叔丁基苯等不饱和烃溶剂、四氯化碳、氯仿、二氯甲烷、二氯乙烷、氯丁烷、溴丁烷、氯戊烷、溴戊烷、氯己烷、溴己烷、氯环己烷、溴环己烷等卤化饱和烃溶剂,氯苯、二氯苯、三氯苯等卤化不饱和烃溶剂,四氢呋喃、四氢吡喃等醚溶剂,苯甲酸烷基酯等酯类溶剂。所述的制剂直接用于制备光电器件。
[0120]
如图1所示,有机光电器件包含基板101、阳极102、空穴注入层103、空穴传输层104、电子阻挡层105、发光层或活性层106、空穴阻挡层107、电子传输层108、电子注入层109、阴极110组合而成的元件。
[0121]
oled器件的制造:
[0122]
具体实施底发射oled器件的结构为在含有ito的玻璃上,hil为ht-1:p-3(97:3v/v%),厚度为10纳米;htl为ht-1,厚度为90纳米;ebl为ht-10,厚度为10纳米,eml为主体(bh):所述有机化合物(97:3v/v%),厚度为25纳米,etl为et-2:liq(50:50v/v%),厚度为35纳米,然后蒸镀阴极al为40纳米。
[0123]
为了更好地说明本发明实际的增益效果,将常用的客体化合物bd-1或bd-2掺杂在主体材料bh-1中作对比制备了相应的对比oled器件。
[0124][0125]
依据上述器件实施例,oled器件的电流效率、电压等特性显示在下表1中。
[0126]
表1
[0127]
[0128][0129]
以上器件结果表明,对比器件1以客体材料bd-1和bh-1构成器件的发光层,优选的器件中将本发明的含硼有机化合物替换bd-1,器件的效率提升,驱动电压持平或有所下降。客体材料bd-2与本发明的含硼有机化合物结构相近,同样作为客体材料与bh-1形成发光层后,对比器件例2与器件例1至15相比,器件的综合性能相当,电流效率有明显的提升,比如器件例15的电流效率为对比器件2的166%。特别是器件例16至21,器件的效率达到了20.3cd/a以上,外量子效率20%以上。器件例21的电流效率是对比器件2的350%以上。本发明提供了一种全新的含硼有机化合物,实现了高电流效率、低驱动电压的oled器件,发光器件综合性能有突破性的提升。
[0130]
以上对本发明的实施方式进行了详细的说明,本领域技术人员在考虑说明书及实践这里公开的发明后,将容易想到本技术的其它实施方案。本技术旨在涵盖本技术的任何变型、用途或者适应性变化,这些变型、用途或者适应性变化遵循本技术的一般性原理并包括本公开未公开的本技术领域中的公知常识或惯用技术手段。说明书和实施例仅被视为示例性的,本技术的真正范围和精神由下面的权利要求指出。
[0131]
应当理解的是,本技术并不局限于上面已经描述并示出的精确结构,并且可以在不脱离其范围进行各种修改和改变。本技术的范围仅由所附的权利要求来限制。以上所述仅为本技术的较佳实施例,并不用以限制本技术,凡在本技术的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本技术的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1