一种检测SARS-CoV-2变异毒株核酸的方法及其应用
本发明属于生物技术领域,具体涉及一种检测sars-cov-2变异毒株核酸的方法及其应用。
背景技术:
新型冠状病毒(sars-cov-2)是一种可引起人新型冠状病毒肺炎(covid-19)的新发呼吸道病原体,与重症急性呼吸道综合症冠状病毒(sars-cov)和中东呼吸综合征冠状病毒(mers-cov)同属于β-冠状病毒,具有较高的传染性和一定的致死率。
棘突蛋白(s)是sars-cov-2表面最主要的糖蛋白,由s1和s2两个亚单位组成。s1末端的受体结合域(rbd)通过与细胞表面受体血管紧张素转化酶2(ace2)结合,从而感染细胞启动病毒复制。阻断rbd与受体结合可抑制病毒复制,因此s蛋白和rbd蛋白是大部分疫苗的靶抗原。而且,已发现的大部分有效单克隆抗体也主要识别rbd区域。由于冠状病毒属于rna病毒,因此具有较高的变异性。已经有越来越多的变异毒株被发现,包括首次发现于英国的b.1.1.7(501y.v1),发现于南非的b.1.351(501y.v2),发现于巴西的p.1(501y.v3),发现于印度的b.1.617(452r.v3)等。这些变异毒株较初期分离的野生型毒株感染性更强,而且发生于rbd区的突变会影响疫苗的保护效果,造成病毒免疫逃逸。研究证明,尽管rbd区发现了多个位点的突变,包括k417n/t、e484k和n501y,但相比其他位点突变,位于e484位点变异会严重影响疫苗及抗体的保护效果,导致疫苗中和保护下降10倍以上,而且多个获批的单克隆抗体药物也对该位点的变异毒株失去中和活性(antibodyresistanceofsars-cov-2variantsb.1.351andb.1.1.7.nature.(2021).)。因此快速鉴别e484位点变异对于疫苗接种、疫情防控及流行病学调查具有重要意义。研究证明存在免疫逃逸的变异毒株,包括b.1.351、p.1和b.1.617,均含有e484位点变异,而且这些毒株的逃逸反应均与e484位点直接相关(sars-cov-2spikee484kmutationreducesantibodyneutralisation.lancetmicrobe(2021))。
目前对于变异毒株的鉴定主要以测序技术为主,然而由于测序技术难以实现高通量快速测定,而且对于技术和设备要求较高,因此限制了其大规模推广应用。荧光pcr技术是应用最为广泛的核酸检测技术,而且目前sars-cov-2的核酸检测也主要是基于taqman荧光pcr技术。目前国内的县级检测机构均已具备开展荧光pcr的条件,若能用荧光pcr实现变异毒株的快速鉴别将是最优选择。然而taqman荧光pcr技术无法实现对于单碱基的鉴别,有研究人员尝试对变异毒株进行序列分析,发现变异毒株除具备最为关注的e484位点突变外,约80%的b.1.351在orf1a基因上还存在3675-3677碱基缺失,因此基于该碱基缺失设计了taqman荧光pcr检测方法(pcrassaytoenhanceglobalsurveillanceforsars-cov-2variantsofconcern.medrxiv.(2021).)。由于b.1.1.7变异毒株同样具有该碱基缺失,而且约0.03%的野生毒株也存在该缺失,因此该检测方法的应用并不能有效区分e484位点突变毒株。而且b.1.1.7变异毒株并不会影响疫苗的免疫保护效果,因此该方法存在较大的应用限制。
现有技术中认为,鸟嘌呤可通过电子转移的方式淬灭和其相邻的荧光染料的荧光(fluorescence-quenchingphenomenonbyphotoinducedelectrontransferbetweenafluorescentdyeandanucleotidebase.analsci.(2001).17,155-160,10.2116/analsci.17.155.),因此taqman探针要求荧光基团不要标记在核苷酸g上。
技术实现要素:
本发明的目的是提供一种检测sars-cov-2变异毒株核酸的方法及其应用。
本发明提供了一种用于检测核酸分子中的核苷酸突变的探针,为探针甲或探针乙;
对于所述探针甲来说,所述核苷酸突变为涉及核苷酸g的突变,即突变前为核苷酸g或突变后为核苷酸g;所述探针为正向杂交探针,是基于所述核苷酸突变设计的,其中具有对应于所述核苷酸突变的核苷酸g,将其命名为目标g;所述探针标记有荧光染料,且所述荧光染料标记在目标g的相邻核苷酸上;
对于所述探针乙来说,所述核苷酸突变为涉及核苷酸c的突变,即突变前为核苷酸c或突变后为核苷酸c;所述探针为反向杂交探针,是基于所述核苷酸突变设计的,其中具有对应于所述核苷酸突变的核苷酸g,将其命名为目标g;所述探针标记有荧光染料,且所述荧光染料标记在目标g的相邻核苷酸上。
所述探针用于核酸检测,例如杂交、荧光pcr等。
所述荧光染料包括但不限于fam、hex、vic、tamra、cy5等。
所述相邻核苷酸可为目标g的5’端的相邻核苷酸,也可为目标g的3’端的相邻核苷酸。
目标g可位于所述探针的3’末端,也位于所述探针的5’末端,也可位于探针的内部。
所述核酸分子可为dna分子或rna分子。
本发明还提供了一种用于检测核酸分子中的核苷酸突变的引物探针组,包括以上所述探针和特异引物对;所述特异引物对的靶序列包括所述探针对应的序列。
采用以上所述引物探针组,利用pcr体系即可实现对于模板核酸的扩增及单碱基的鉴别。
所述引物探针组中的探针为探针甲时,所述核苷酸突变为涉及核苷酸g的突变,即突变前为核苷酸g或突变后为核苷酸g。
所述引物探针组中的探针为探针乙时,所述核苷酸突变为涉及核苷酸c的突变,即突变前为核苷酸c或突变后为核苷酸c。
所述核酸分子可为dna分子或rna分子。
本发明还保护一种用于鉴定核酸分子中的核苷酸突变的荧光pcr方法(方法甲),包括如下步骤:以供试dna为模板,采用以上所述引物探针组进行pcr扩增;根据扩增曲线鉴定核酸分子中的核苷酸突变。所述核酸分子可为dna分子。
所述引物探针组中的探针为探针甲时,所述核苷酸突变为涉及核苷酸g的突变,即突变前为核苷酸g或突变后为核苷酸g。
所述引物探针组中的探针为探针乙时,所述核苷酸突变为涉及核苷酸c的突变,即突变前为核苷酸c或突变后为核苷酸c。
本发明还保护一种用于鉴定核酸分子中的核苷酸突变的荧光pcr方法(方法乙),包括如下步骤:以供试rna为模板,采用以上所述引物探针组在含有反转录酶的体系中进行pcr扩增;根据扩增曲线鉴定核酸分子中的核苷酸突变。所述核酸分子可为rna分子。
所述引物探针组中的探针为探针甲时,所述核苷酸突变为涉及核苷酸g的突变,即突变前为核苷酸g或突变后为核苷酸g。
所述引物探针组中的探针为探针乙时,所述核苷酸突变为涉及核苷酸c的突变,即突变前为核苷酸c或突变后为核苷酸c。
以上任一所述方法中,所述pcr扩增的反应体系中,上游引物的浓度可为0.5-10mm(例如可为0.8μm),下游引物的浓度可为0.5-10mm(例如可为0.8μm)。
以上任一所述方法中,所述pcr扩增的反应体系中,探针的浓度可为0.01-0.4μm(例如可为0.2μm)。
由于本发明中采用的探针无需借助核酸外切酶处理发射荧光,因此与仅可选择拥有核酸外切酶活性的pcr酶的taqmanpcr技术不同。以上任一所述方法中,所述pcr扩增采用的dna聚合酶,包括但不限于taq聚合酶、pfu聚合酶、kod聚合酶、tth聚合酶、deepvent聚合酶、bst聚合酶。任何可以实现核酸扩增的dna聚合酶均可采用。
本发明还保护以上所述探针或以上所述引物探针组在制备试剂盒中的应用;所述试剂盒用于鉴定核酸分子中的核苷酸突变。所述核酸分子可为dna分子或rna分子。
所述探针为探针甲时,所述核苷酸突变为涉及核苷酸g的突变,即突变前为核苷酸g或突变后为核苷酸g。
所述探针为探针乙时,所述核苷酸突变为涉及核苷酸c的突变,即突变前为核苷酸c或突变后为核苷酸c。
所述引物探针组中的探针为探针甲时,所述核苷酸突变为涉及核苷酸g的突变,即突变前为核苷酸g或突变后为核苷酸g。
所述引物探针组中的探针为探针乙时,所述核苷酸突变为涉及核苷酸c的突变,即突变前为核苷酸c或突变后为核苷酸c。
示例性的,以上任一所述核酸分子可为病毒特异性核酸分子。
示例性的,所述病毒可为新型冠状病毒。
示例性的,以上任一所述核酸分子中的核苷酸突变可为e484位点突变。
e484位点突变的含义:新型冠状病毒野生型毒株e484位点对应的核苷酸为核苷酸g,e484变异毒株的e484位点变异成k或q,对应的核苷酸变异成核苷酸a或核苷酸c。
示例性的,所述探针可为探针sars2dp-1或探针sars2dp-2。
探针sars2dp-1如下(序列表的序列3):
3'末端核苷酸是目标g,tamra标记在于目标g上游相邻的t上。
探针sars2dp-2如下(序列表的序列4):
3'末端起的第2个核苷酸是目标g,tamra标记在于目标g下游相邻的t上。
示例性的,所述特异引物对如下:
sars2f(上游引物,序列表的序列5):5’-gctgcgttatagcttggaattc-3';
sars2b(下游引物,序列表的序列6):5’-gggttggaaaccatatgattgt-3'。
本发明还保护一种用于检测新型冠状病毒e484位点变异的试剂盒,包括特异性探针;所述特异性探针是基于新型冠状病毒e484位点变异设计的,其中具有对应于新型冠状病毒e484位点变异的核苷酸g,将其命名为目标g;所述特异性探针标记有荧光染料,且所述荧光染料标记在目标g的相邻核苷酸上。
所述荧光染料包括但不限于fam、hex、vic、tamra、cy5等。
所述相邻核苷酸可为目标g的5’端的相邻核苷酸,也可为目标g的3’端的相邻核苷酸。
目标g可位于所述特异性探针的3’末端,也位于所述特异性探针的5’末端,也可位于所述特异性探针的内部。
所述试剂盒还包括特异引物对;所述特异引物对的靶序列包括所述特异性探针对应的序列。
所述试剂盒还包括通用探针;所述通用探针是基于新型冠状病毒的保守区设计的,其中具有核苷酸g并且在该核苷酸g的相邻核苷酸上标记有荧光染料。
所述荧光染料包括但不限于fam、hex、vic、tamra、cy5等。
所述相邻核苷酸可为所述核苷酸g的5’端的相邻核苷酸,也可为所述核苷酸g的3’端的相邻核苷酸。
所述核苷酸g可位于所述通用探针的3’末端,也位于所述通用探针的5’末端,也可位于所述通用探针的内部。
所述特异引物对的靶序列包括所述通用探针对应的序列。
所述特异性探针上的荧光染料与所述通用探针上的荧光染料不相同。
示例性的,所述特异性探针可为探针sars2dp-1或探针sars2dp-2。
探针sars2dp-1如下(序列表的序列3):
3'末端核苷酸是目标g,tamra标记在于目标g上游相邻的t上。
探针sars2dp-2如下(序列表的序列4):
3'末端起的第2个核苷酸是目标g,tamra标记在于目标g下游相邻的t上。
示例性的,所述特异引物对如下:
sars2f(上游引物,序列表的序列5):5’-gctgcgttatagcttggaattc-3';
sars2b(下游引物,序列表的序列6):5’-gggttggaaaccatatgattgt-3'。
示例性的,所述通用探针为探针sars2dp-u。
探针sars2dp-u如下(序列表的序列7):
3'末端核苷酸是目标g,fam标记在于目标g上游相邻的t上。
本发明还保护(a)或(b)或(c)或(d)在制备用于检测新型冠状病毒e484位点变异的试剂盒中的应用;
(a)所述特异性探针;
(b)所述特异性探针和所述通用探针;
(c)所述特异性探针和所述特异引物对;
(d)所述特异性探针和所述通用探针和所述特异引物对。
本发明还保护(a)或(b)或(c)或(d)在制备用于检测新型冠状病毒e484变异株的试剂盒中的应用;
(a)所述特异性探针;
(b)所述特异性探针和所述通用探针;
(c)所述特异性探针和所述特异引物对;
(d)所述特异性探针和所述通用探针和所述特异引物对。
本发明的发明人发现,当核苷酸g与核苷酸c互补结合后,鸟嘌呤的淬灭能力显著降低,进一步的发明人利用这一发现设计了一种可鉴定单碱基差异的自淬灭探针(鸟嘌呤淬灭荧光染料的荧光,鸟嘌呤与胞嘧啶互补结合后荧光染料发射荧光),可以实现对单碱基突变的快速鉴定,从而突破了荧光pcr技术难以实现单碱基鉴别的技术瓶颈。
进一步,本发明可以实现对新冠病毒变异毒株的单碱基快速鉴定。因此,对于新型冠状病毒肺炎的变异株快速鉴别及疫情防控具有重大价值。
附图说明
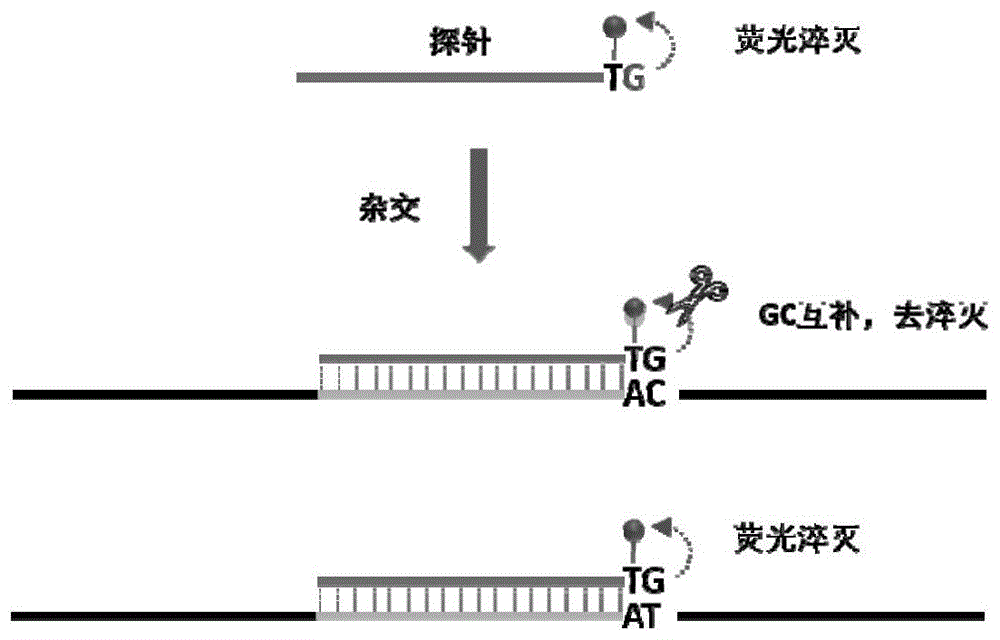
图1为特异性探针的工作原理示意图。
图2为特异性探针和通用探针的工作原理示意图。
图3为实施例2的结果图。
图4为实施例3的结果图。
具体实施方式
下面结合具体实施方式对本发明进行进一步的详细描述,给出的实施例仅为了阐明本发明,而不是为了限制本发明的范围。以下提供的实施例可作为本技术领域普通技术人员进行进一步改进的指南,并不以任何方式构成对本发明的限制。
下述实施例中的实验方法,如无特殊说明,均为常规方法,按照本领域内的文献所描述的技术或条件或者按照产品说明书进行。下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。pgem-t载体为商业化载体(货号:a3600,promega,usa)。引物/探针的工作浓度,即pcr反应体系中,引物/探针的浓度。如无特殊说明,以下实施例中的定量试验,均设置三次重复实验,结果取平均值。
实施例1、关于解除鸟嘌呤淬灭荧光的新发现以及技术方案的初步形成
前期研究发现鸟嘌呤可以淬灭标记荧光基团(fluorescence-quenchingphenomenonbyphotoinducedelectrontransferbetweenafluorescentdyeandanucleotidebase.analsci17,155-160(2001)),基于该理论,设计taqman探针时荧光基团不可以标记在核苷酸g或其临近核苷酸上。发明人发现,当寡核苷酸与互补序列形成双链后,寡核苷酸上的鸟嘌呤淬灭荧光的能力会显著下降。
利用上述重要发现,发明人得到了如下技术方案(该技术方案适用于涉及核苷酸g或c的突变,即突变前为核苷酸g或c或突变后为核苷酸g或c;所述探针是基于所述核苷酸突变设计的,其中具有对应于所述核苷酸突变的核苷酸g,将其命名为目标g):将荧光染料标记在探针中目标g的相邻核苷酸上,探针上的荧光染料由于鸟嘌呤的淬灭功能不会发射荧光;当探针与互补序列结合后,互补序列上的核苷酸c与探针上的目标g结合后,即可消除鸟嘌呤的淬灭能力,使得探针上的荧光染料发出荧光;如果互补序列缺失核苷酸c,不能与探针上的目标g结合,则探针不会发出荧光。通过上述技术方案,可以实现对核酸单碱基的鉴别,配合荧光pcr技术,即可实现类似于taqman荧光pcr技术的快速核酸检测,同时具备了taqman技术不具备的单碱基突变鉴别功能。
实施例2、sars-cov-2自淬灭探针的设计和鉴定
一、探针的设计
利用实施例1的方案,设计可识别变异毒株e484位点的自淬灭探针。野生型毒株e484位点对应的核苷酸为g(鸟嘌呤核糖核苷酸),将其定义为目标g;b.1.351和p.1等变异毒株的e484位点变异成k,对应的核苷酸为a(腺嘌呤核糖核苷酸);b.1.617变异毒株的e484位点变异成q,对应的核苷酸为c(胞嘧啶核糖核苷酸)。可以将目标g设计在探针的3’末端,也可以将目标g设计在探针的5’末端,也可以将目标g设计在探针内部,不影响最终的检测效果。探针根据野生型毒株e484位点设计,将荧光基团(例如fam或tamra)标记在目标g的相邻核苷酸上。确保探针无明显的发夹环等二级结构。
本实施例仅提供一种探针序列及标记方式,但不限于该设计方案。根据wuhan-hu-1毒株(genbank:mn908947.3)、b.1.351变异毒株(gisaidepi_isl_1250476)、p.1变异毒株(gisaidepi_isl_1073034)和b.1.617(gisaidepi_isl_1360382)的rbd基因序列设计探针,荧光染料分别标记在目标g的5’端的相邻核苷酸上或者标记在目标g的3’端的相邻核苷酸上。探针sars2dp-1和探针sars2dp-2均为针对e484位点的特异性探针。
探针sars2dp-1如下(序列表的序列3):
下划线标注的是目标g,tamra标记在于目标g上游相邻的t上(该t用方框标注)。
探针sars2dp-2如下(序列表的序列4):
下划线标注的是目标g,tamra标记在于目标g下游相邻的t上(该t用方框标注)。
配套于上述探针的pcr扩增引物如下:
sars2f(上游引物,序列表的序列5):5’-gctgcgttatagcttggaattc-3';
sars2b(下游引物,序列表的序列6):5’-gggttggaaaccatatgattgt-3'。
二、荧光pcr鉴别野生毒株和变异毒株
模板溶液分别为质粒p0溶液或质粒pv溶液。质粒po为将wuhan-hu-1毒株的rbd基因(如序列表的序列1所示)克隆至pgem-t载体得到的重组质粒。质粒pv为将b.1.351变异毒株的rbd基因(如序列表的序列2所示)克隆至pgem-t载体得到的重组质粒。模板溶液中,dna含量为106拷贝/毫升或104拷贝/毫升。
进行pcr扩增。pcr扩增分别采用三种扩增体系。扩增体系均采用sars2f(上游引物)和sars2b(下游引物)。扩增体系采用探针sars2dp-1或探针sars2dp-2。
taq扩增体系的组成(25微升):反应缓冲液、dntp、taq聚合酶、上游引物、下游引物、探针、模板溶液和水。上游引物的工作浓度为0.8μm,下游引物的工作浓度为0.8μm,探针的工作浓度为0.2μm。反应体系中,模板溶液的加入量为5微升。反应缓冲液、dntp、taq聚合酶均由商品化试剂taqpcrmix(北京全式金公司,货号:as111-01)提供。
pfu扩增体系的组成(25微升):反应缓冲液、dntp、pfu聚合酶、上游引物、下游引物、探针、模板溶液和水。上游引物的工作浓度为0.8μm,下游引物的工作浓度为0.8μm,探针的工作浓度为0.2μm。反应体系中,模板溶液的加入量为5微升。反应缓冲液、dntp、pfu聚合酶均由商品化试剂pfupcrmix(北京全式金公司,货号:as211-01)提供。
kod扩增体系的组成(25微升):反应缓冲液、dntp、kod聚合酶、上游引物、下游引物、探针、模板溶液和水。上游引物的工作浓度为0.8μm,下游引物的工作浓度为0.8μm,探针的工作浓度为0.2μm。反应体系中,模板溶液的加入量为5微升。反应缓冲液、dntp、kod聚合酶均由商品化试剂kodmix(北京全式金公司,货号:as301-01)提供。
三种扩增体系采用的pcr扩增程序均如下:95℃3min;95℃15s、58℃30s(收集荧光),40个循环。
wuhan-hu-1毒株的rbd基因为靶标时,不管采用探针sars2dp-1还是探针sars2dp-2,不管采用哪种扩增体系,不管模板溶液的dna含量为106拷贝/毫升还是104拷贝/毫升,均显示s型扩增曲线。
b.1.351变异毒株的rbd基因为靶标时,不管采用探针sars2dp-1还是探针sars2dp-2,不管采用哪种扩增体系,不管模板溶液的dna含量为106拷贝/毫升还是104拷贝/毫升,均无扩增曲线。
结果见图3。图3中,野生毒株对应的是质粒po,e484变异毒株对应的是质粒pv。
三、结果判断和原理分析
当模板中含有新冠病毒的rbd基因时,特异的引物会启动pcr扩增。在探针与扩增序列中的探针互补序列结合后,会使鸟嘌呤的淬灭能力降低从而发射荧光。wuhan-hu-1毒株的rbd基因可与探针完全互补结合从而发射荧光,形成s型扩增曲线。包含e484位点突变的变异毒株的rbd基因无法与探针完全互补结合,导致无法影响鸟嘌呤的淬灭能力,从而无法发射荧光,进而无法形成s型扩增曲线。通过观察是否形成扩增s型曲线,即可判断扩增序列是否含有e484位点突变。原理示意图见图1。
实施例3、sars-cov-2双探针检测与突变株鉴别体系的建立和验证
通过实施例2可实现对于新冠病毒rbd基因中是否含e484位点突变进行快速鉴别,但仅用该方法无法区分e484位点突变毒株与阴性结果。本实施例通过增加一条通用探针,标记与特异性探针不同的荧光基团,建立一种双探针淬灭荧光pcr技术,既可实现对于新冠病毒的核酸检测,同时还可鉴别变异毒株。
一、探针的设计
本实施例所设计探针与实施例2探针设计策略一致,同为鸟嘌呤淬灭探针。探针选择在两条引物扩增序列的内部,与实施例2探针的靶标序列不重叠,且为新冠病毒保守区,探针序列与wuhan-hu-1毒株和含e484位点变异毒株均完全互补,且标记荧光染料与实施例1探针不同。探针sars2dp-u为新型冠状病毒通用探针。
探针sars2dp-u如下(序列表的序列7):
下划线标注的是目标g,fam标记在于目标g上游相邻的t上(该t用方框标注)。
二、荧光pcr鉴别野生毒株和变异毒株
模板溶液同实施例2。
采用taq扩增体系进行pcr扩增。
taq扩增体系的组成(25微升):反应缓冲液、dntp、taq聚合酶、sars2f(上游引物)、sars2b(下游引物)、探针sars2dp-1、探针sars2dp-u、模板溶液和水。sars2f(上游引物)的工作浓度为0.8μm,sars2b(下游引物)的工作浓度为0.8μm,探针sars2dp-1的工作浓度为0.2μm,探针sars2dp-u的工作浓度为0.04μm。反应体系中,模板溶液的加入量为5微升。反应缓冲液、dntp、taq聚合酶均由商品化试剂taqpcrmix(北京全式金公司,货号:as111-01)提供。
pcr扩增程序同实施例2。
wuhan-hu-1毒株的rbd基因为靶标时,不管模板溶液的dna含量为106拷贝/毫升还是104拷贝/毫升,不管是通用探针的fam荧光信号还是特异性探针的tamra荧光信号,均显示s型扩增曲线。
b.1.351变异毒株的rbd基因为靶标时,不管模板溶液的dna含量为106拷贝/毫升还是104拷贝/毫升,通用探针的fam荧光信号均显示s型扩增曲线。
b.1.351变异毒株的rbd基因为靶标时,不管模板溶液的dna含量为106拷贝/毫升还是104拷贝/毫升,特异性探针的tamra荧光信号均无扩增曲线。
结果见图4。图4中,野生毒株对应的是质粒po,e484变异毒株对应的是质粒pv。
三、结果判断和原理分析
当模板中含有无e484突变的新冠病毒rbd基因时,特异性探针和通用探针都会发射不同波长的荧光,出现两条s型扩增曲线;当模板中含有e484突变的新冠病毒rbd基因时,则通用探针会发射荧光,特异性探针不会发射荧光,出现1条s型扩增曲线;当模板中不含有新冠病毒rbd基因,则两条探针都不会发射荧光,则不会出现s型扩增曲线。从而实现了新冠病毒核酸检测及同时鉴别变异毒株两个功能。原理示意图见图2。
实施例4、sars-cov-2双探针检测与突变株鉴别体系最低检出限和特异性评价一、最低检测限的评价
1、制备标准品溶液
取质粒,采用t7ribomaxtmexpresslargescalernaproductionsystem试剂盒(promega,货号:p1320)进行体外转录;然后,在转录产物中加入dnase(promega,货号:p1320),以去除残留的质粒;然后,用rneasycleanupkit试剂盒(qiagen,货号:74204)进行纯化获得高纯度体外转录rna。
将高纯度体外转录rna用nano-drop2000核酸定量仪(thermofisherscientific)进行定量,计算获得rna拷贝数浓度(拷贝数/毫升),然后用rnase-freeddh2o稀释,得到不同拷贝数浓度的标准品溶液。
质粒分别为质粒p0或质粒pv。质粒p0进行上述步骤,得到rna0,相应的得到rna0标准品溶液。质粒pv进行上述步骤,得到rnav,相应的得到rnav标准品溶液。
2、荧光pcr
模板溶液为rna0标准品溶液或rnav标准品溶液。
采用taq扩增体系进行pcr扩增。
taq扩增体系的组成(25微升):反应缓冲液、dntp、taq聚合酶、反转录酶、sars2f(上游引物)、sars2b(下游引物)、探针sars2dp-1、探针sars2dp-u、模板溶液和水。sars2f(上游引物)的工作浓度为0.8μm,sars2b(下游引物)的工作浓度为0.8μm,探针sars2dp-1的工作浓度为0.2μm,探针sars2dp-u的工作浓度为0.04μm。反应体系中,模板溶液的加入量为5微升,反转录酶的加入量为5u。反应缓冲液、dntp、taq聚合酶均由商品化试剂taqpcrmix(北京全式金公司,货号:as111-01)提供。反转录酶:takara,货号:639522。
用水代替标准品溶液作为阴性对照;
pcr扩增程序如下:50℃15min;95℃3min;95℃10s、58℃30s(收集荧光),40个循环。
ct值结果见表1。
3、对比试验
模板溶液为rna0标准品溶液或rnav标准品溶液。
采用taq扩增体系进行pcr扩增。
taq扩增体系的组成(25微升):反应缓冲液、dntp、taq聚合酶、反转录酶、sars2f(上游引物)、sars2b(下游引物)、taqman探针、模板溶液和水。sars2f(上游引物)的工作浓度为0.8μm,sars2b(下游引物)的工作浓度为0.8μm,taqman探针的工作浓度为0.2μm。反应体系中,模板溶液的加入量为5微升,反转录酶的加入量为5u。反应缓冲液、dntp、taq聚合酶均由商品化试剂taqpcrmix(北京全式金公司,货号:as111-01)提供。反转录酶:takara,货号:639522。
taqman探针(sars2taqmanp):5’-fam-accattacaaggtgtgctaccggcctg-bhq-3’。
ct值结果见表1。
通用探针和特异探针对wuhan-hu-1毒株的rbd基因的最低检出限均为2拷贝/反应。通用探针对b.1.351变异毒株的rbd基因的最低检出限为2拷贝/反应。taqman探针对wuhan-hu-1毒株的rbd基因以及b.1.351变异毒株的rbd基因的最低检出限均为2拷贝/反应。
表1
二、特异性的评价
分别用不同呼吸道病原,包括甲型流感病毒h1n1和h3n2(记载于:interactionamonginfluenzavirusesa/h1n1,a/h3n2,andbinjapan.internationaljournalofenvironmentalresearchandpublichealth16(2019)),乙型流感病毒yamagata和victoria型(记载于:anewlydevelopedreal-timepcrassayfordiscriminatinginfluenzabvirusyamagataandvictorialineages.journalofmedicalvirology(2020)),合胞病毒a/b型(记载于:noveldualmultiplexreal-timert-pcrassaysfortherapiddetectionofsars-cov-2,influenzaa/b,andrespiratorysyncytialvirususingthebdmaxopensystem.emergingmicrobes&infections10,161-166(2021)),副流感病毒1/2/3型(记载于:phylogeneticandpathogenicityanalysisofanovellineageofcaprineparainfluenzavirustype3.microbialpathogenesis154,104854(2021)),腺病毒型(记载于:humanadenovirusspeciesinchildrenwithacuterespiratoryillnesses.journalofclinicalvirology:theofficialpublicationofthepanamericansocietyforclinicalvirology134,104716(2021)),鼻病毒(viralloadsanddiseaseseverityinchildrenwithrhinovirus-associatedillnesses.viruses13(2021)),冠状病毒nl63和hku1(记载于:apatientwithhumancoronavirusnl63falselydiagnosedwithcovid-19;lessonlearnedfortheimportanceofdefinitivediagnosis.jinfectchemother27,1126-1128(2021)),评价本发明检测方法的特异性。
提取病原的总rna,作为模板溶液。按照步骤一的2的方法进行检测。
不管是通用探针还是特异性探针,均无扩增曲线。
结果证明,本发明的检测方法与以上病原均无交叉反应。
以上对本发明进行了详述。对于本领域技术人员来说,在不脱离本发明的宗旨和范围,以及无需进行不必要的实验情况下,可在等同参数、浓度和条件下,在较宽范围内实施本发明。虽然本发明给出了特殊的实施例,应该理解为,可以对本发明作进一步的改进。总之,按本发明的原理,本申请欲包括任何变更、用途或对本发明的改进,包括脱离了本申请中已公开范围,而用本领域已知的常规技术进行的改变。按以下附带的权利要求的范围,可以进行一些基本特征的应用。
序列表
<110>中国科学院微生物研究所
<120>一种检测sars-cov-2变异毒株核酸的方法及其应用
<130>gncyx211746
<160>7
<170>siposequencelisting1.0
<210>1
<211>618
<212>dna
<213>人工序列(artificialsequence)
<400>1
tctattgttagatttcctaatattacaaacttgtgcccttttggtgaagtttttaacgcc60
accagatttgcatctgtttatgcttggaacaggaagagaatcagcaactgtgttgctgat120
tattctgtcctatataattccgcatcattttccacttttaagtgttatggagtgtctcct180
actaaattaaatgatctctgctttactaatgtctatgcagattcatttgtaattagaggt240
gatgaagtcagacaaatcgctccagggcaaactggaaagattgctgattataattataaa300
ttaccagatgattttacaggctgcgttatagcttggaattctaacaatcttgattctaag360
gttggtggtaattataattacctgtatagattgtttaggaagtctaatctcaaacctttt420
gagagagatatttcaactgaaatctatcaggccggtagcacaccttgtaatggtgttgaa480
ggttttaattgttactttcctttacaatcatatggtttccaacccactaatggtgttggt540
taccaaccatacagagtagtagtactttcttttgaacttctacatgcaccagcaactgtt600
tgtggacctaaaaagtct618
<210>2
<211>618
<212>dna
<213>人工序列(artificialsequence)
<400>2
tctattgttagatttcctaatattacaaacttgtgcccttttggtgaagtttttaacgcc60
accagatttgcatctgtttatgcttggaacaggaagagaatcagcaactgtgttgctgat120
tattctgtcctatataattccgcatcattttccacttttaagtgttatggagtgtctcct180
actaaattaaatgatctctgctttactaatgtctatgcagattcatttgtaattagaggt240
gatgaagtcagacaaatcgctccagggcaaactggaaatattgctgattataattataaa300
ttaccagatgattttacaggctgcgttatagcttggaattctaacaatcttgattctaag360
gttggtggtaattataattacctgtatagattgtttaggaagtctaatctcaaacctttt420
gagagagatatttcaactgaaatctatcaggccggtagcacaccttgtaatggtgttaaa480
ggttttaattgttactttcctttacaatcatatggtttccaacccacttatggtgttggt540
taccaaccatacagagtagtagtactttcttttgaacttctacatgcaccagcaactgtt600
tgtggacctaaaaagtct618
<210>3
<211>25
<212>dna
<213>人工序列(artificialsequence)
<400>3
ggtagcacaccttgtaatggtgttg25
<210>4
<211>26
<212>dna
<213>人工序列(artificialsequence)
<400>4
ggtagcacaccttgtaatggtgttgt26
<210>5
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>5
gctgcgttatagcttggaattc22
<210>6
<211>22
<212>dna
<213>人工序列(artificialsequence)
<400>6
gggttggaaaccatatgattgt22
<210>7
<211>28
<212>dna
<213>人工序列(artificialsequence)
<400>7
attaccaccaaccttagaatcaagattg28
- 还没有人留言评论。精彩留言会获得点赞!