六氟苯并四苯和四氟四苯并四苯盘状液晶半导体的合成
1.本发明涉及两类六氟苯并四苯和四氟四苯并四苯盘状液晶半导体的合成。
背景技术:
2.盘状液晶是一类独特的具有显著电导和光导性能的有机半导体材料,它的分子结构含有大π键共轭稠环芳烃和柔性烷基链,由于其一维分子间柱状堆积,使其能够自组装成柱状液晶相,这为电荷载流子迁移提供独特的一维通道,因此,盘状液晶半导体在分子电子学、光电子学、复印机、太阳能电池和电致发光装置等有应用前途,富电子的盘状液晶分子的研究已经非常广泛,而贫电子含氟盘状液晶化合物因合成困难而少有报道,而氟原子在芳核上的引入对盘状液晶分子的柱状相稳定性以及载流子种类和迁移速率有重要影响。
技术实现要素:
3.基于此, 本发明专利设计合成一类多氟苯并四苯(benzo[f]tetraphene)以及四苯并四苯(tetrabenzo[a,c,j,l]tetracene)盘状液晶化合物,通过2,2
’‑
二溴-4,4’,5,5
’‑
四烷氧基-1,1'-联苯与丁基锂反应, 再与全氟萘反应,得到六氟苯并四苯衍生物;之后再与联苯二锂试剂反应,得到四氟四苯并四苯衍生物,经研究表明:该两类化合物可以在较宽的温度范围(包括室温)形成稳定的六方柱状液晶相,本发明专利提供这两类含氟芳烃的合成方法。
[0004]
一类六氟四烷氧基苯并四苯或者(2,3,6,7-四烷氧基苯并[f]四苯)盘状液晶化合物,其特征在于具有通式(i)所示的结构:其中,r为
ꢀ‑cnh2n+1
,n表示碳原子数为6-16的整数。
[0005]
一种四氟八烷氧基四苯并四苯其特征在于具有通式(ii)所示的结构:其中r为
ꢀ‑cnh2n+1
,n表示碳原子数为6-16的整数。
[0006]
一种权利要求1所述的通式(i),9,10,11,12,13,14-六氟-2,3,6,7-四烷氧基苯并[f]四苯其特征结构制备方法为:步骤一:9,10,11,12,13,14-六氟-2,3,6,7-四烷氧基苯并[f]四苯化合物的制备;
第一步是在50 ml反应管中加入a,用thf将其溶解,再加入n-buli,然后在氩气保护
ꢀ‑
78 ℃下反应3 h,升至室温搅拌4 h,第二步是在-78 ℃下加入全氟萘试剂反应,升至室温再反应12 h,第三步是用二氯甲烷和饱和食盐水进行萃取,有机相用无水mgso4干燥,过滤,旋干,用硅胶柱层析提纯[洗脱剂:v
二氯甲烷
:v
石油醚
=1:3],最后用乙酸乙酯和乙醇进行重结晶,得到黄色固体(i),其中r 为-c
nh2n+1
,n表示碳原子数为6-16的整数。
[0007]
步骤二:一种四氟八烷氧基四苯并四烯盘状液晶化合物的制备:第一步是在50 ml反应管中加入 a, 用thf将其溶解之后,加入n-buli,然后在氩气的保护和
ꢀ‑
78 ℃下反应3 h,升至室温搅拌4 h,第二步是在-78 ℃下加入9,10,11,12,13,14-六氟-2,3,6,7-四烷氧基苯并[f]四苯试剂与之反应,升至室温再反应12 h,第三步是用二氯甲烷和饱和食盐水进行萃取,有机相用无水mgso4干燥,过滤,旋干,用硅胶柱层析提纯[洗脱剂:v
三氯甲烷
:v
石油醚
=1:3]。最后用石油醚和甲苯进行重结晶,得到橙黄色固体(ii),其中r为-c
nh2n+1
,n表示碳原子数为6-16的整数。
附图说明
[0008]
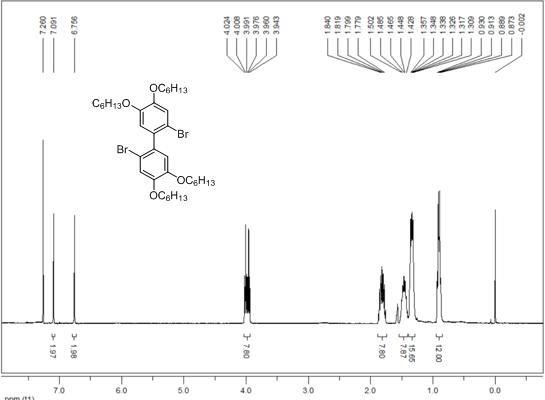
图1实施例1中所获r为c6h
13
的中间体a的核磁氢谱。
[0009]
图2实施例1中所获r为c6h
13
的通式(i)的核磁氢谱。
[0010]
图3实施例2中所获r为c6h
13
时通式(ii)的核磁氢谱。
[0011]
图4实施例1中所获r为c6h
13
的通式(i)的核磁氟谱。
[0012]
图5实施例1中所获r为c6h
13
的通式(ii)的核磁氟谱。
[0013]
图6实施例1中所获r为c6h
13
时通式(i)的dsc曲线图。
[0014]
图7实施例2中所获r为c6h
13
时通式(ii)的dsc曲线图。
[0015]
图8实施例1中所获r为c6h
13
时通式(i)的偏光织构图。
[0016]
图9实施例2中所获r为c6h
13
时通式(ii)的偏光织构图。
具体实施方式
[0017]
下面给出的实例是对本发明的具体描述,必须强调的是下面给出的实施例子只是对本发明的进一步阐述,而不是对本发明的保护范围的一种限制。本领域熟练技术人员根据上述发明内容在实际实施过程中,涉及到的改进或者调整若不是本质意义上的改变,仍然属于本发明的保护范围。
[0018]
以下各个实施案例中所用到的合成方法均为现有技术:
rebecca e. yardley, joseph a. paquette, hi taing, heather m. gaebler, s. holger eichhorn, ian p. hamilton, and kenneth e. maly.stabilization of columnar liquid crystal phases via arene-perfluoroarene interactions[j].organicletters,2019,21(24):10102-10105。
[0019]
实施例1。
[0020]
本实施例提供的化合物是通式(i)合物的制备,其中r为c6h
13,
其制备反应如下:第一步是在50 ml反应管中加入a (400 mg, 0.56 mmol)用thf(10 ml)将其溶解完全,之后再加入n-buli(143.69 mg , 2.24 mmol),在氩气保护
ꢀ‑
78 ℃下反应3 h,升至室温在搅拌4 h,第二步是将反应管转移至-78 ℃下加入全氟萘试剂(610.88 mg, 2.24 mmol)反应,升至室温再反应12 h,第三步是用二氯甲烷和饱和食盐水进行萃取,第四步是用无水mgso4干燥有机相,过滤,旋干,用硅胶柱层析提纯[洗脱剂:v
二氯甲烷
:v
石油醚
=1:3],最后用乙酸乙酯和乙醇进行重结晶,得到黄色固体(i)。(320 mg,72%)。
[0021]
核磁氢谱1h nmr(cdcl3, tms, 400 mhz),δ 8.30 (s, 1h, arh), 8.25 (s, 1h, arh), 7.63 (d, j = 7.9 hz, 1h, arh), 7.59 (s, 1h, arh), 4.26
ꢀ–ꢀ
4.19 (m, 4h, och2), 4.14 (d, j = 6.3 hz, 4h, ch2), 2.00
ꢀ–ꢀ
1.89 (m, 8h, ch2), 1.59 (d, j = 15.2, hz, 8h, ch2), 1.40 (d, j = 13.9 hz, 16h, ch2), 0.95 (t, j = 6.5 hz, 12h, ch3)。
[0022]
实施例2。
[0023]
本实施例提供的化合物是通式(ii)合物的制备,其中r为c6h
13,
其制备反应如下:第一步是在50 ml反应管中加入d(331.27 mg,0.42 mmol)用thf(10 ml)将其溶解完全之后加入n-buli(107.6 mg,1.68 mmol),在氩气保护和
ꢀ‑
78 ℃下反应3 h,之后升至室温搅拌4 h;第二步是在-78 ℃加入9,10,11,12,13,14-六氟-2,3,6,7-四己氧基苯并[f]四苯试剂(150 mg,0.21 mmol)反应,升至室温再反应12 h,第三步用二氯甲烷和饱和食盐水进行萃取,有机相用无水mgso4干燥,过滤,旋干,用硅胶柱层析提纯[洗脱剂:v
三氯甲烷
:v
石油醚
=1:3],最后用石油醚和甲苯进行重结晶,得到橙黄色固体(ii) (110 mg,40 %)。
[0024]
核磁氢谱1h nmr(cdcl3, tms, 400 mhz),δ: 8.58 (s, 4h, arh), 7.67 (s, 4h, arh), 4.28(s, 4h,och2), 4.18 (s, 4h, och2), 2.00-1.90 (m, 16h, ch2), 1.65-1.56 (m, 18h, ch2), 1.46-1.32 (m, 34h, ch2),0.93-0.97 (m, 24h, ch3)。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1