一种席夫碱-金属有机配合物及其制备方法与应用
一种席夫碱
‑
金属有机配合物及其制备方法与应用
技术领域
1.本发明属于co2环加成技术领域,涉及一种席夫碱
‑
金属有机配合物及其制备方法与应用。
背景技术:
2.近年来,化石燃料的大量消耗直接导致大气中co2的积累。自19世纪初以来,大气中的co2浓度急剧持续上升。co2是主要的温室气体,co2的富集对全球变暖负有责任,并导致高温、干旱、酷寒等极端天气更加频繁地出现以及海平面升高、土地沙漠化严重等现象。另一方面,碳氢化合物的过度消耗也导致能源日渐匮乏,使全球陷入了能源危机。因此,co2过度排放模式以及非持续性能源消耗已经引起了世界各国政府和科学界的广泛关注。
3.co2作为自然界碳循环的基本组分,能够参与“co2‑
有机碳
‑
碳酸盐”的循环,是地球上分布广、储量丰富的碳资源。从绿色化学和可持续发展的角度考虑,co2作为优良的碳一合成子,在化学、化工生产中被用于制备高附加值化学品,co2的资源化利用具有广阔的应用前景,其研究也具有非常重要的学术价值。co2可用作化学合成的原料,其中一类被直接或作为合成中间体广泛使用的化学品是由co2和环氧化合物合成的环状有机碳酸酯。环状有机碳酸酯的应用广泛,可作为生产聚碳酸酯和聚氨酯的单体以及锂电子电池的电解质溶液,还可用作化妆品添加剂和其他化学品生产的中间体。因此,用co2为原料生产环状有机碳酸酯具有十分重要的意义及广阔的应用前景。
4.由于co2具有热力学稳定性和动力学惰性,表现出反应活性低的特点,因此,需要将co2活化,才能实现其转化反应,而关键在于发展高效的催化剂。然而,现有的co2环加成合成环碳酸酯的催化剂,大都存在催化转化率低、催化剂负载量大、反应时间过长、需要高温高压的苛刻条件等问题,应用受到限制。
技术实现要素:
5.本发明的目的是提供一种席夫碱
‑
金属有机配合物及其制备方法与应用。本发明利用5
‑
醛基香兰素与二胺类化合物合成席夫碱有机配体,并负载金属离子以对催化活性产生协同作用,从而达到高效催化的目的,制备出的席夫碱
‑
金属有机配合物可作为催化剂,用于催化co2环加成合成环碳酸酯。
6.本发明的目的可以通过以下技术方案来实现:
7.一种席夫碱有机配体,该配体的化学结构式为:
[0008][0009]
其中,为
[0010]
一种席夫碱有机配体的制备方法,该方法为:将5
‑
醛基香兰素、二胺类化合物(1当量)与溶剂混合,并进行搅拌反应,后经分离(冷却至室温后,将溶剂蒸发至干燥)得到所述的席夫碱有机配体。
[0011]
进一步地,所述的二胺类化合物为丙二胺、顺式
‑
1,2
‑
环己二胺、反式
‑
1,2
‑
环己二胺或1,4
‑
环己二胺(顺反混合物),所述的溶剂包括二氯甲烷、乙醇或n,n
‑
二甲基甲酰胺(dmf)中的一种或更多种。
[0012]
进一步地,搅拌反应过程中,反应温度为35
‑
105℃,反应时间为3
‑
4h。
[0013]
席夫碱有机配体的制备过程如下:
[0014][0015]
根据选择的不同,席夫碱有机配体分别记为l1、l2、l3、l4。
[0016]
一种席夫碱
‑
金属有机配合物,该配合物的化学结构式为:
[0017][0018]
其中,为
[0019]
m为ru
3+
、ni
3+
、al
3+
、co
2+
或zn
2+
。
[0020]
一种席夫碱
‑
金属有机配合物的制备方法,该方法为:将席夫碱有机配体、金属盐(1当量)与溶剂混合,并进行搅拌反应,后经分离(冷却至室温后,将溶剂蒸发至干燥)得到所述的席夫碱
‑
金属有机配合物。
[0021]
进一步地,所述的席夫碱有机配体的化学结构式为:
[0022][0023]
所述的金属盐为三氯化钌、乙酸镍、氯化铝、乙酸钴或硫酸锌,所述的溶剂包括二氯甲烷、乙醇或n,n
‑
二甲基甲酰胺中的一种或更多种。
[0024]
进一步地,搅拌反应过程中,反应温度为35
‑
105℃,反应时间为3
‑
4h。
[0025]
席夫碱
‑
金属有机配合物的制备过程如下:
[0026][0027]
一种席夫碱
‑
金属有机配合物的应用,所述的配合物作为催化剂,用于催化co2环加成反应合成环碳酸酯。
[0028]
进一步地,环加成反应过程为:将催化剂(例如rul1、rul2、nil3、all3、rul3、rul4)、环氧化合物与溶剂混合,在co2气氛中进行搅拌反应,即得到环碳酸酯;搅拌反应过程中,温度为40
‑
140℃,压力为0.1
‑
2.5mpa,反应时间为4
‑
12h。优选地,催化剂与环氧化合物的摩尔比为1:(10
‑
400)。
[0029]
co2与环氧化合物环加成反应合成环碳酸酯的过程如下:
[0030][0031]
其中,r可选为ch3、ch3cl、ch2ch3、ch2oph、ph、ch2oc4h9等。
[0032]
研究发现,席夫碱
‑
金属有机配合物不仅易于合成,而且将其用于催化co2环加成反应,具有高活性、低催化剂负载量和较温和的反应条件。同时,由于金属中心的存在,促进了环氧化合物的开环,能协同活化和稳定co2环加成过程中的环氧化合物和相应的中间体。由于它们的协同作用,可以显著加快反应速率,提高环碳酸酯的收率。
[0033]
此外,5
‑
醛基香兰素是香兰素工业中的一个主要副产物。香兰素(3
‑
甲氧基
‑4‑
羟基苯甲醛)是目前应用量最大的香料之一,被广泛应用到奶制品、烘焙、冰激凌、香水等领域中,被称为香料皇后,年需求量达到1.7万吨。而同时,香兰素生产过程中会产生大量的5
‑
醛基香兰素副产物。5
‑
醛基香兰素中有两个醛基,为席夫碱型金属有机配合物的合成创造了条件。
[0034]
因此,本发明以香兰素副产物5
‑
醛基香兰素为主要原料,合成香兰素副产物衍生的多齿螯合型席夫碱
‑
金属有机配合物,可作为催化剂用于催化转化co2合成环碳酸酯,不仅实现了工业副产物的综合利用,还能促进co2转化为环碳酸酯这一可用能源,对环境保护、废弃物资源化利用等领域都具有重要的理论研究意义和现实价值。
[0035]
具体而言,本发明中的席夫碱
‑
金属有机配合物具有良好的热稳定性,其金属中心能够活化环氧化合物,作为催化剂,能协同活化和稳定co2环加成过程中的相应中间体,从而显示出优异的催化转化效果。本发明中的配合物可以在较温和的条件下催化co2与环氧化合物的环加成反应,解决了co2活化困难、反应效率低、反应时间长、产品收率低等诸多问题。
[0036]
与现有技术相比,本发明具有以下特点:
[0037]
1)本发明创造性地利用香兰素副产物5
‑
醛基香兰素与二胺类化合物反应制备出席夫碱有机配体,并进一步负载金属离子,得到席夫碱
‑
金属有机配合物,其制备方法简单,条件温和,后处理方便,且负载的金属离子对其催化活性有协同作用。
[0038]
2)本发明中的席夫碱
‑
金属有机配合物可作为催化剂,将催化活化co2与环氧化合物相耦合,从而实现低压温和条件下co2的环加成反应,并显示出良好的催化效果,且不需要助催化剂辅助开环。
[0039]
3)本发明中的席夫碱
‑
金属有机配合物适用范围广,同时可以通过高效液相色谱仪和气相色谱仪对主产物和副产物进行监控,结果表明:该配合物可以在较温和的条件下实现co2与环氧化合物的催化转化,呈现优异的转化率,选择性可高达99%以上,且具有良好的底物包容性、普适性,具有潜在的工业化利用价值。
附图说明
[0040]
图1为实施例1中制备得到的配体l1的核磁图谱;
[0041]
图2为实施例1中制备得到的配体l2的核磁图谱;
[0042]
图3为实施例1中制备得到的配体l3的核磁图谱;
[0043]
图4为实施例1中制备得到的配体l4的核磁图谱;
[0044]
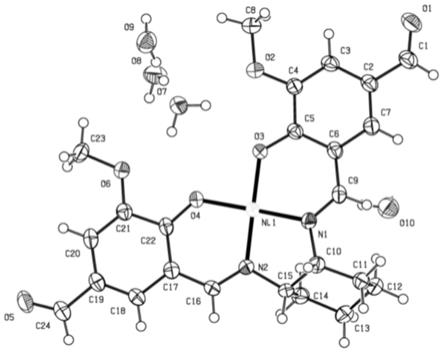
图5为实施例1中制备得到的席夫碱
‑
金属有机配合物nil3的单晶结构图。
具体实施方式
[0045]
下面结合附图和具体实施例对本发明进行详细说明。本实施例以本发明技术方案为前提进行实施,给出了详细的实施方式和具体的操作过程,但本发明的保护范围不限于下述的实施例。
[0046]
本发明提供了一种席夫碱有机配体,该配体的化学结构式为:
[0047][0048]
其中,为
[0049]
本发明进一步提供了上述席夫碱有机配体的制备方法,该方法为:将5
‑
醛基香兰素、二胺类化合物与溶剂混合,并进行搅拌反应,后经分离得到所述的席夫碱有机配体。
[0050]
其中,二胺类化合物为丙二胺、顺式
‑
1,2
‑
环己二胺、反式
‑
1,2
‑
环己二胺或1,4
‑
环己二胺,溶剂包括二氯甲烷、乙醇或n,n
‑
二甲基甲酰胺中的一种或更多种。搅拌反应过程中,反应温度为35
‑
105℃,反应时间为3
‑
4h。
[0051]
本发明同时提供了一种席夫碱
‑
金属有机配合物,该配合物的化学结构式为:
[0052][0053]
其中,为
[0054]
m为ru
3+
、ni
3+
、al
3+
、co
2+
或zn
2+
。
[0055]
本发明进一步提供了上述席夫碱
‑
金属有机配合物的制备方法,该方法为:将席夫碱有机配体、金属盐与溶剂混合,并进行搅拌反应,后经分离得到所述的席夫碱
‑
金属有机配合物。
[0056]
其中,金属盐为三氯化钌、乙酸镍、氯化铝、乙酸钴或硫酸锌,溶剂包括二氯甲烷、乙醇或n,n
‑
二甲基甲酰胺中的一种或更多种。搅拌反应过程中,反应温度为35
‑
105℃,反应时间为3
‑
4h。
[0057]
本发明还提供了上述席夫碱
‑
金属有机配合物的应用,将配合物作为催化剂,用于催化co2环加成反应合成环碳酸酯。环加成反应过程为:将催化剂、环氧化合物与溶剂混合,在co2气氛中进行搅拌反应,即得到环碳酸酯;搅拌反应过程中,温度为40
‑
140℃,压力为0.1
‑
2.5mpa,反应时间为4
‑
12h。
[0058]
其中,环氧化合物可选用1,2
‑
环氧丙烷、环氧氯丙烷、环氧丁烷、丁氧基甲基环氧乙烷、1,2
‑
环氧
‑3‑
苯氧基丙烷或苯基环氧乙烷等。
[0059]
实施例1:
[0060]
席夫碱有机配体通过以下方法制备得到:在圆底烧瓶中加入5
‑
醛基香兰素,再加入1当量丙二胺(或反式
‑
1,2
‑
环己二胺、或顺式
‑
1,2
‑
环己二胺、或1,4
‑
环己二胺)和溶剂乙醇(30ml),在配备有搅拌的水浴锅中进行加热(75℃)回流4h,反应结束冷却至室温后,将溶剂蒸发至干燥,得到席夫碱有机配体l。
[0061]
制备过程如下:
[0062][0063]
根据的不同,制得的席夫碱有机配体l分别记为l1、l2、l3、l4。
[0064]
其中,l1
‑
l4的核磁图谱分别见图1、图2、图3、图4。
[0065]
利用上述席夫碱有机配体制备席夫碱
‑
金属有机配合物,制备过程为:在圆底烧瓶中加入配体(l1、l2、l3或l4),再加入1当量的金属盐和溶剂二氯甲烷,在配备有搅拌的40℃水浴锅中加热回流3
‑
4h,反应结束冷却至室温后,将溶剂蒸发至干燥,得到席夫碱
‑
金属有
机配合物ml。根据m及l的不同,制得的席夫碱
‑
金属有机配合物ml分别记为rul1、rul2、rul3、nil3、all3、rul4等。
[0066]
其中,nil3的单晶结构见图5。
[0067]
采用本实施例制得的一系列席夫碱
‑
金属有机配合物作为催化剂,高效催化co2环加成合成环碳酸酯,分别如实施例2
‑
19所示。
[0068]
实施例2:
[0069]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丙烷10mmol,催化剂rul11.0mol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到2.0mpa后,将反应釜放入加热套中加热到120℃,同时以大约350r/min的速度搅拌反应8h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为78%,选择性为95%。
[0070]
实施例3:
[0071]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丙烷10mmol,催化剂rul10.5mol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到2.5mpa后,将反应釜放入加热套中加热到140℃,同时以大约350r/min的速度搅拌反应6h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为65%,选择性为93%。
[0072]
实施例4:
[0073]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧氯丙烷10mmol,催化剂rul1 1.0mol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到2.0mpa后,将反应釜放入加热套中加热到120℃,同时以大约350r/min的速度搅拌反应8h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为70%,选择性为95%。
[0074]
实施例5:
[0075]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丙烷10mmol,催化剂rul2 2.0mol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到1.5mpa后,将反应釜放入加热套中加热到140℃,同时以大约350r/min的速度搅拌反应6h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为92%,选择性为97%。
[0076]
实施例6:
[0077]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丙烷10mmol,催化剂nil3 1.0mol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到2.0mpa后,将反应釜放入加热套中加热到120℃,同时以大约350r/min的速度搅拌反应8h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为84%,选择性为97%。
[0078]
实施例7:
[0079]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丁烷10mmol,催化剂rul4 2.0mol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到1.5mpa后,将反应釜放入加热套中加热到140℃,同时以大约350r/min的速度搅拌反应6h,反应结束之后,反应
器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为59%,选择性为92%。
[0080]
实施例8:
[0081]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丙烷10mmol,催化剂rul3 1.0mol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到2.5mpa后,将反应釜放入加热套中加热到100℃,同时以大约350r/min的速度搅拌反应8h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为97%,选择性为>99%。
[0082]
实施例9:
[0083]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丙烷10mmol,催化剂rul3 5.0mmol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到0.5mpa后,将反应釜放入加热套中加热到140℃,同时以大约350r/min的速度搅拌反应4h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为76%,选择性为96%。
[0084]
实施例10:
[0085]
在配备有搅拌的50ml不锈钢高压釜中,加入1,2
‑
环氧
‑3‑
苯氧基丙烷10mmol,催化剂rul3 1.0mol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到2.5mpa后,将反应釜放入加热套中加热到100℃,同时以大约350r/min的速度搅拌反应8h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为64%,选择性为92%。
[0086]
实施例11:
[0087]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丙烷10mmol,催化剂nil3 2.0mol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到1.0mpa后,将反应釜放入加热套中加热到120℃,同时以大约350r/min的速度搅拌反应8h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为42%,选择性为77%。
[0088]
实施例12:
[0089]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丙烷10mmol,催化剂nil3 10.0mmol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到1.5mpa后,将反应釜放入加热套中加热到60℃,同时以大约350r/min的速度搅拌反应10h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为48%,选择性为69%。
[0090]
实施例13:
[0091]
在配备有搅拌的50ml不锈钢高压釜中,加入苯基环氧乙烷10mmol,催化剂nil3 2.0mmol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到1.0mpa后,将反应釜放入加热套中加热到120℃,同时以大约350r/min的速度搅拌反应8h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为34%,选择性为57%。
[0092]
实施例14:
[0093]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丙烷10mmol,催化剂all3 2.0mmol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到2.5mpa后,将反应釜放入加热套中加热到100℃,同时以大约350r/min的速度搅拌反应8h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为68%,选择性为87%。
[0094]
实施例15:
[0095]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丙烷10mmol,催化剂all3 10.0mmol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到2.0mpa后,将反应釜放入加热套中加热到120℃,同时以大约350r/min的速度搅拌反应10h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为62%,选择性为87%。
[0096]
实施例16:
[0097]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧氯丙烷10mmol,催化剂all3 2.0mmol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到2.5mpa后,将反应釜放入加热套中加热到100℃,同时以大约350r/min的速度搅拌反应8h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为59%,选择性为74%。
[0098]
实施例17:
[0099]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丙烷10mmol,催化剂rul4 0.5mmol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到1.0mpa后,将反应釜放入加热套中加热到120℃,同时以大约350r/min的速度搅拌反应10h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为82%,选择性为91%。
[0100]
实施例18:
[0101]
在配备有搅拌的50ml不锈钢高压釜中,加入环氧丙烷10mmol,催化剂rul4 0.25mmol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到2.0mpa后,将反应釜放入加热套中加热到80℃,同时以大约350r/min的速度搅拌反应12h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为43%,选择性为80%。
[0102]
实施例19:
[0103]
在配备有搅拌的50ml不锈钢高压釜中,加入丁氧基甲基环氧乙烷10mmol,催化剂rul4 0.5mmol%和溶剂dmf 10ml,通入co2吹扫三次,再用co2将反应釜加压到1.0mpa后,将反应釜放入加热套中加热到120℃,同时以大约350r/min的速度搅拌反应10h,反应结束之后,反应器被冷却到环境温度,未反应的co2被缓慢释放。收集产物并经气相分析鉴定,测定转化率为43%,选择性为67%。
[0104]
实施例2
‑
19的数据汇总如表1所示。
[0105]
表1
[0106][0107]
上述的对实施例的描述是为便于该技术领域的普通技术人员能理解和使用发明。熟悉本领域技术的人员显然可以容易地对这些实施例做出各种修改,并把在此说明的一般原理应用到其他实施例中而不必经过创造性的劳动。因此,本发明不限于上述实施例,本领域技术人员根据本发明的揭示,不脱离本发明范畴所做出的改进和修改都应该在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1