抗菌肽YHX-3及其组合物和应用
抗菌肽yhx
‑
3及其组合物和应用
技术领域
1.本发明属于生物技术领域,具体涉及一种抗菌肽yhx
‑
3及其组合物和应用。
背景技术:
2.自第一种抗生素——青霉素被发现以来,抗生素一直作为一类抗感染药物在人类与病原体的斗争中发挥着重要的作用,拯救了无数人的生命。但近年来抗生素滥用的情况愈演愈烈,导致病原微生物产生耐药性,甚至出现了“超级细菌”,严重威胁着人类的卫生健康事业。2017年,世界卫生组织发表了首份抗生素耐药“重点病原体”清单,列出了当前对人类健康构成最大威胁的12种细菌种族目录,其中包括鲍曼不动杆菌和绿脓杆菌等对包括碳青霉烯类和第三代头孢菌素类药物产生耐药性的细菌,因此解决病原菌的耐药性问题已经刻不容缓。而解决这一问题的方法,除了严格管控抗生素的使用之外,开发新型抗菌药物是一个重要途径。
3.抗菌肽(antimicrobial peptides,amps),又称宿主防御肽,是由特定基因编码并在外界环境诱导下产生的一类生物活性多肽,是生物体先天免疫系统的重要组成部分,在动物、植物、细菌等生物体中均有发现。抗菌肽具有一些共同的性质:其大部分为短肽(氨基酸残基<50),带正电荷,具有两亲性结构(含有疏水性和亲水性结构域),这些特性使得抗菌肽具有独特的抑菌机制。然而,目前大部分抗菌肽还存在生产成本高、生物活性较低以及易引发溶血等问题,因此,如何通过理性设计,开发出生产难度低、抑菌活性显著且无明显溶血活性的抗菌肽是抗菌肽研究开发领域的热点。
技术实现要素:
4.本发明的目的在于解决现有技术中存在的上述问题,提出了一种抗菌肽yhx
‑
3及其组合物和应用,该新型抗菌肽的溶血活性低,且对革兰氏阳性菌(单核细胞增生李斯特氏菌、金黄色葡萄球菌、变异链球菌)、革兰氏阴性菌(大肠杆菌、沙门氏菌)均具有显著的抗菌活性,应用前景广泛。
5.本发明的技术方案是:
6.一种抗菌肽yhx
‑
3,所述抗菌肽yhx
‑
3的氨基酸序列如seq id no.1所示,具体为leu
‑
lys
‑
leu
‑
leu
‑
ser
‑
lys
‑
leu
‑
leu
‑
lys
‑
lys
‑
leu
‑
leu
‑
lys
‑
nh2。
7.进一步的,所述抗菌肽yhx
‑
3包含13个氨基酸残基,其分子量为1538.08da,净电荷数为+5。
8.所述的抗菌肽yhx
‑
3在制备生物抗菌剂中的应用。
9.进一步,所述生物抗菌剂以抗菌肽yhx
‑
3为主要成分,所述生物抗菌剂用于抑制革兰氏阳性菌和革兰氏阴性菌,包括单核细胞增生李斯特氏菌、变异链球菌、沙门氏菌、大肠杆菌和金黄色葡萄球菌。
10.进一步的,所述抗菌肽yhx
‑
3对单核细胞增生李斯特氏菌的最小抑菌浓度为4μg/ml;对变异链球菌的最小抑菌浓度为16μg/ml;对沙门氏菌的最小抑菌浓度为8μg/ml;对大
肠杆菌的最小抑菌浓度为32μg/ml;对金黄色葡萄球菌的最小抑菌浓度为128μg/ml。
11.所述的抗菌肽yhx
‑
3在制备防腐剂或者动物饲料中的应用,所述动物饲料包括所述抗菌肽yhx
‑
3或其任意比例的混合物;所述防腐剂包括所述抗菌肽yhx
‑
3或其任意比例的混合物。
12.进一步的,所述防腐剂为用于食品或化妆品的防腐剂。
13.一种组合物,所述组合物为含有所述抗菌肽yhx
‑
3或其任意比例的混合物。
14.进一步的,所述组合物为洗手液、香皂、沐浴液、洗发剂、牙膏、洗衣液或洗衣粉等。
15.本发明的有益效果:
16.本发明所提供的抗菌肽yhx
‑
3具有广谱的抗菌活性,对包括单核细胞增生李斯特氏菌、金黄色葡萄球菌、变异链球菌、大肠杆菌以及沙门氏菌在内的革兰氏阳性菌和革兰氏阴性菌均具有显著的抗菌活性。
17.本发明的抗菌肽,溶血活性较低,序列长度短,分子量小,化学合成难度小,能够更加特异性地杀死生物体内的病原菌的同时很好的节约规模化生产成本。
附图说明
18.图1为本发明提供的抗菌肽yhx
‑
3的螺旋轮结构示意图;
19.图2为本发明提供的抗菌肽yhx
‑
3的二级结构预测示意图;
20.图3为本发明提供的抗菌肽yhx
‑
3在333μg/ml浓度条件下对单核细胞增生李斯特氏菌的抑菌效果示意图;
21.图4为本发明提供的抗菌肽yhx
‑
3在333μg/ml浓度条件下对大肠杆菌的抑菌效果示意图;
22.图5为本发明提供的抗菌肽yhx
‑
3在333μg/ml浓度条件下对变异链球菌的抑菌效果示意图;
23.图6为本发明提供的抗菌肽yhx
‑
3在333μg/ml浓度条件下对沙门氏菌的抑菌效果示意图。
具体实施方式
24.下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
25.为了进一步理解本发明,将结合附图和实施例对本发明作进一步的说明。
26.实施例1抗菌肽的设计
27.在抗菌肽从头设计及对构效关系理解的基础上,对从apd3数据库中筛选得到的针对革兰氏阳性菌和革兰氏阴性菌有抑菌作用的843条抗菌肽序列进行序列参数分析,包括序列长度、带电荷数、疏水氨基酸比例和氨基酸组成等参数的分析,选择出其中的优势参数,确定了新抗菌肽yhx
‑
3的各项序列参数,具体如下表1所示:
28.表1从头设计抗菌肽的序列参数
29.序列长度带电荷数疏水氨基酸个数氨基酸组成
13+57lys、ser、leu
30.氨基酸序列长度确定为13,以在降低合成成本的同时提高其安全性。选取带正电氨基酸lys和极性不带电荷氨基酸ser组成抗菌肽的极性面,选取疏水性氨基酸leu形成疏水面,来保证抗菌肽的两亲性结构;疏水氨基酸个数确定为7个,以保证抗菌肽抗菌活性发挥所必须的疏水性;带电荷数确定为+5,保证抗菌肽对细菌细胞膜的亲和力。
31.采用生物信息学预测及分析工具进行抗菌肽一级结构的辅助设计,对不同氨基酸排列顺序的肽序列分子量、平均疏水值、平均疏水力矩、不稳定性指数、脂肪族指数、半衰期、螺旋轮图、成为amps的可能性以及二级结构进行预测,选出最优的抗菌肽序列。
32.所用生物信息学工具如下:
33.物化性质分析网站:expasy protparam(https://web.expasy.org/protparam/);
34.螺旋轮图及疏水性分析网站:heliquest(https://heliquest.ipmc.cnrs.fr/);
35.amps可能性预测网站:camp
r3
(http://www.camp.bicnirrh.res.in/);
36.二级结构预测网站:
37.pep
‑
fold(https://bioserv.rpbs.univ
‑
paris
‑
diderot.fr/services/pep
‑
fold3/);
38.zhang lab(https://zhanglab.ccmb.med.umich.edu/)
39.通过上述工具得到的最优抗菌肽序列及物化性质如表2所示,通过gravy(总平均疏水值)和疏水力矩可以看出肽序列具有适当的疏水性和较高的疏水力矩,因而具有很好的两亲性,在对细菌细胞膜具有较好亲和力的同时有利于深入细胞膜的磷脂双分子层,进而破坏细胞膜的完整性。脂肪族指数(aliphatic index)和不稳定性指数(instability index)均被认为与肽的稳定性相关,其中不稳定性指数低于40则表明了序列较好的稳定性,脂肪族指数代表了肽序列中脂肪族氨基酸所占的相对体积,与热稳定性相关,通过预测结果可知抗菌肽yhx
‑
3具有较好的预测稳定性。
40.表2抗菌肽yhx
‑
3的序列及物化性质
41.序列gravy脂肪族指数不稳定指数等电点疏水力矩lkllskllkkllk0.485210
‑
29.9510.60.803
42.图1为抗菌肽yhx
‑
3的螺旋轮结构图,其中一侧由5个lys和1个ser组成抗菌肽的亲水面,在螺旋轴另一侧由7个leu组成抗菌肽的疏水面。使用camp
r3
基于三种不同算法(svm、random forest、ann)对抗菌肽的成肽可能性进行预测,肽序列yhx
‑
3的amp probability均在0.97以上。基于pep
‑
fold和zhang lab对肽序列yhx
‑
3的二级结构预测结果如图2所示,表明抗菌肽yhx
‑
3的二级结构主要为α
‑
螺旋,在c
‑
末端呈现一小段无规则卷曲结构。
43.实施例2抑菌活性检测
44.抗菌肽由强耀生物科技(上海)有限公司合成,抗菌肽c末端进行了酰胺化修饰,纯度在95%以上。
45.将金黄色葡萄球菌、大肠杆菌和沙门氏菌分别划线接种于lb固体培养基,将单核细胞增生李斯特氏菌和变异链球菌划线接种于bhi固体培养基,置于37℃恒温培养箱培养18h,挑取各个菌株的单菌落置于各自对应的液体培养基中,37℃恒温振荡培养12h。测量菌液的od
600
值,并将其稀释至1
×
106cfu/ml。
46.(1)抑菌圈实验
47.配置lb和bhi半固体培养基(琼脂质量分数0.6%),每皿20ml加入7μl菌液振荡混匀后倒入摆放好牛津杯的培养皿中,待培养基冷却凝固后拔除牛津杯完成打孔,每孔中加入160μl抗菌肽溶液(配置使用1mg抗菌肽溶于3ml超纯水)。置于37℃恒温培养箱培养24h后测量抑菌圈直径,测试结果如图3
‑
6所示。
48.(2)最小抑菌浓度(mic)的测定
49.向96孔板中加入培养至对数生长期的各菌株菌液(单核细胞增生李斯特氏菌、变异链球菌、金黄色葡萄球菌、沙门氏菌、大肠杆菌)50μl,同时在各孔中加入各浓度梯度抗菌肽溶液(512μg/ml、256μg/ml、128μg/ml、64μg/ml、32μg/ml、16μg/ml、8μg/ml、4μg/ml)50μl,并分别做阳性对照和阴性对照组。在37℃恒温培养箱培养8h后测量各孔的od
600
值,取菌株生长被完全抑制的最低浓度作为抗菌肽的最小抑菌浓度(mic),测试结果如表3所示。
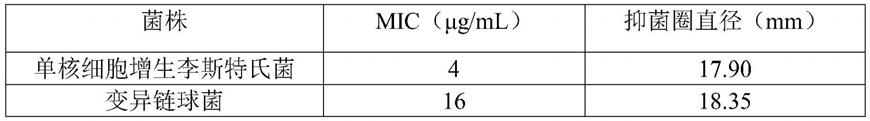
50.表3抗菌肽yhx
‑
3的抑菌活性分析结果
[0051][0052][0053]
实施例3溶血活性检测
[0054]
取健康兔血液1ml加于肝素抗凝管中,在1000xg转速下离心10min后取沉淀,用pbs缓冲液冲洗3次,将红细胞用10ml pbs重悬。用pbs缓冲液将抗菌肽yhx
‑
3的浓度调整至4
‑
512μg/ml,以每孔50μl的剂量加入96孔板中,并加入等体积(50μl)的红细胞悬液混匀。以pbs缓冲液作为阴性对照,以0.1%tritonx
‑
100作为阳性对照,在37℃恒温培养1h后取出,1000xg离心10min,取出上清液用酶标仪在570nm处测od值,测试结果如表4所示。
[0055]
溶血率计算公式为:溶血率=(a
t
‑
a
o
)/(a
c
‑
a
o
)
×
100%;
[0056]
式中,a
t
为实验组的吸光值,a
c
为阳性对照组的吸光值,a
o
为阴性对照组的吸光值。
[0057]
表4抗菌肽yhx
‑
3的溶血活性(测定3次取平均值)
[0058]
抗菌肽浓度(μg/ml)3264128256512溶血率(%)0000.8002.432
[0059]
由表4可知,在最小抑菌浓度(mic)条件下,抗菌肽yhx
‑
3不表现溶血活性,即使在512μg/ml浓度条件下,溶血率也未达到10%,说明抗菌肽yhx
‑
3具有极好的安全性,在生物抗菌剂、畜牧业所用动物饲料、食品及化妆品防腐剂等方面的应用前景较大,可进一步深入研究和开发利用。
[0060]
上述说明仅为本发明的优选实施例,并非是对本发明的限制,尽管参照前述实施例对本发明进行了详细的说明,对于本领域技术人员来说,其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分技术特征进行等同替换。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改型等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1