抗人IL-33中和性自身抗体及其制备方法和应用
抗人il
‑
33中和性自身抗体及其制备方法和应用
技术领域
1.本技术涉及生物医学领域,特别涉及抗人il
‑
33中和性自身抗体及其制备方法和应用。
背景技术:
2.过敏性哮喘是支气管哮喘的主要临床表型,是一种常见的慢性气道炎症性疾病,轻则影响患者工作生活,重者可导致残疾甚至死亡[1]。近三十年来,过敏性哮喘的发病率在世界范围内呈逐年上升趋势。目前,全球约有3亿过敏性哮喘患者,预计到2025年这一数字将会超过4亿。因此如何有效的控制过敏性哮喘病,特别是重症哮喘的发生和发展已经成为公共卫生、临床医学以及经济上全球性的重大挑战。
[0003]
白细胞介素
‑
33(il
‑
33)是多功能的免疫活化因子,可以由多种因素诱导产生,包括过敏原、炎性分子和病原体感染等环境因素,与多种疾病,包括感染、自身免疫,特别是过敏性疾病密切相关,如过敏性鼻炎,皮炎,结膜炎,食物过敏和过敏性休克[2
‑
5]。与其他细胞因子不同,il
‑
33蛋白产生后可以被细胞分泌出来,也可以储藏到细胞核,在细胞发生炎症和坏死时释放。研究发现分泌释放的il
‑
33可通过细胞膜上的受体st2直接激活病理性先天和适应免疫细胞来引起或加重自身免疫和过敏性疾病;在过敏性哮喘,il
‑
33直接激活哮喘病理性ilc2,巨噬、嗜酸、肥大和th2细胞等并诱生多种重要的细胞因子,包括il
‑
4、il
‑
5、il
‑
13、tnfα来触发过敏性和部分非过敏性哮喘反应[2
‑
5]。因此,il
‑
33可能是哮喘的重要诊断,预后和治疗新靶点。
[0004]
为了治疗重症哮喘,许多针对上述细胞因子的人源化单克隆抗体药物已经研发完成或正在开发中,显示一定的治疗作用,还不理想;同时国内外目前还没有靶向il
‑
33的抗体药物在临床上的应用,其在哮喘以及其它疾病的治疗中的重要性仍是未知的。
技术实现要素:
[0005]
有鉴于此,本技术提供了一种抗人il
‑
33中和性自身抗体,该抗人il
‑
33中和性自身抗体可以结合并特异性的阻断il
‑
33介导的生物功能,在制备诊断、预防、治疗或预后评估il
‑
33相关疾病的产品中具有广泛的应用前景。
[0006]
第一方面,本技术提供了一种抗人il
‑
33中和性自身抗体,所述抗人il
‑
33中和性自身抗体的重链可变区包括如seq id no:1所示的氨基酸序列,轻链可变区包括如seq id no:2所示的氨基酸序列。
[0007]
可选的,所述抗人il
‑
33中和性自身抗体还包括重链恒定区,所述重链恒定区为higg1、higg2、higg3或higg4。
[0008]
可选的,所述抗人il
‑
33中和性自身抗体的重链包括如seq id no:3所示的氨基酸序列。
[0009]
可选的,所述抗人il
‑
33中和性自身抗体的轻链包括如seq id no:4所示的氨基酸序列。
[0010]
本技术第一方面提供了一种抗人il
‑
33中和性自身抗体,该抗人il
‑
33中和性自身抗体可以在患者中诱导产生,为中和抗体,在il
‑
33介导的相关疾病的诊断、预防、治疗或预后评估的产品中具有广泛的应用前景。
[0011]
第二方面,本技术提供了第一方面所述的抗人il
‑
33中和性自身抗体的制备方法,包括通过基因工程或体外诱导获得。
[0012]
本技术第二方面提供了抗人il
‑
33中和性自身抗体的制备方法简单、操作方便,且制备得到活性强的抗人il
‑
33中和性自身抗体。
[0013]
第三方面,本技术提供了一种核酸分子,所述核酸分子编码第一方面所述的抗人il
‑
33中和性自身抗体。
[0014]
第四方面,本技术提供了含有第三方面所述的核酸分子的表达盒、重组载体或重组细胞。
[0015]
第五方面,本技术提供了一种药物组合物,包括第一方面所述的抗人il
‑
33中和性自身抗体。
[0016]
第六方面,本技术提供了第一方面所述的抗人il
‑
33中和性自身抗体,第二方面所述的制备方法制得的抗人il
‑
33中和性自身抗体,第三方面所述的核酸分子,第四方面所述的表达盒、重组载体或重组细胞,或第五方面所述的药物组合物在诊断或预后评估il
‑
33介导的疾病的试剂中的应用。
[0017]
第七方面,本技术提供了第一方面所述的抗人il
‑
33中和性自身抗体,第二方面所述的制备方法制得的抗人il
‑
33中和性自身抗体,第三方面所述的核酸分子,第四方面所述的表达盒、重组载体或重组细胞,或第五方面所述的药物组合物在制备预防或治疗il
‑
33介导的疾病的药品中的应用。
附图说明
[0018]
为了更清楚地说明本技术实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本技术的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
[0019]
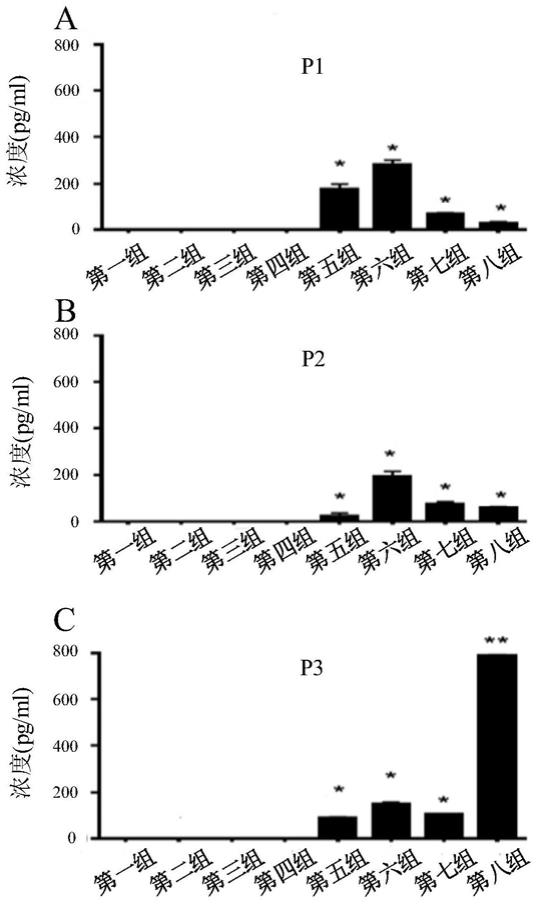
图1为体外诱导产生抗人il
‑
33中和性自身抗体的检测结果图,其中图1中a为加入人il
‑
33多肽抗原1的检测结果,图1中b为加入人il
‑
33多肽抗原2的检测结果,图1中c为加入人il
‑
33多肽抗原3的检测结果。
[0020]
图2为过敏性哮喘患者的抗细胞因子自身抗体滴度检测结果图,其中图2中a为轻型过敏性哮喘患者的抗il
‑
4抗体的检测结果,图2中b为轻型过敏性哮喘患者的抗il
‑
5抗体的检测结果,图2中c为轻型过敏性哮喘患者的抗il
‑
13抗体的检测结果,图2中d为轻型过敏性哮喘患者的抗il
‑
33抗体的检测结果,图2中e为重型过敏性哮喘患者的抗il
‑
33抗体的检测结果,图2中f为轻型和重型过敏性哮喘患者的抗人il
‑
33自身抗体的阳性率。
[0021]
图3为轻、重型过敏性哮喘患者的抗人il
‑
33中和性自身抗体类型检测结果图,其中图3中a为igg型抗体,图3中b为igm型抗体,图3中c为iga型抗体。
[0022]
图4为抗人il
‑
33中和性自身抗体在il
‑
33蛋白的识别位点的检测结果图,其中图4中a为对p1识别的检测结果,图4中b为对p2识别的检测结果,图4中c为p3识别的检测结果。
[0023]
图5为抗人il
‑
33中和性自身抗体对il
‑
33活性的中和能力检测结果图,其中图5中a为il
‑
5的检测结果,图5中b为il
‑
33的检测结果。
[0024]
图6为轻型哮喘患者的血清中细胞因子浓度和其il
‑
33自身抗体相关性的检测结果图,其中图6中a为il
‑
4的检测结果,图6中b为il
‑
9的检测结果,图6中c为il
‑
13的检测结果,图6中d为il
‑
25的检测结果,图6中e为il
‑
33的检测结果。
[0025]
图7为轻型哮喘患者的血清中ige浓度和其il
‑
33自身抗体相关性的检测结果。
[0026]
图8为抗人il
‑
33中和性自身抗体抑制il
‑
33
‑
引起的小鼠肺炎实验检测结果,其中图8中a为小鼠肺部灌洗液中的淋巴细胞计数,图8中b为血清中il
‑
5的检测结果,图8中c为血清中il
‑
13的检测结果,图8中d为血清中tslp的检测结果。
具体实施方式
[0027]
下面将结合本技术实施例中的附图,对本技术实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本技术一部分实施例,而不是全部的实施例。基于本技术中的实施例,本领域普通技术人员在没有作出创造性劳动前提下所获得的所有其他实施例,都属于本技术保护的范围。实施例中采用的分子生物学和免疫学技术,如pcr反应、限制性酶解反应等分子克隆技术、elisa、细胞分离和培养、流式细胞分选术等,均为本领域常用方法,对此不作赘述;实施例中所用的材料、试剂等,如无特殊说明,均可由商业途径获得。
[0028]
本技术提供了一种抗人il
‑
33中和性自身抗体,抗人il
‑
33中和性自身抗体的重链可变区包括如seq id no:1所示的氨基酸序列,轻链可变区包括如seq id no:2所示的氨基酸序列。
[0029]
可以理解的,抗人il
‑
33中和性自身抗体包括重链(h链)和轻链(l链),重链包括重链可变区(vh),轻链包括轻链可变区(vl),可变区存在可以与抗原特异性结合的部位,即抗原结合位点,用以决定抗体识别的特异性。
[0030]
本技术提供的抗人il
‑
33中和性自身抗体是由发明人从患者血液中b细胞发现获得,是天然人抗体,抗人il
‑
33中和性自身抗体序列中不含有异源组分,在使用过程中不会引起人体的排异免疫反应,更加安全有效;本技术提供的抗人il
‑
33中和性自身抗体为中和抗体,在制备诊断、预防或治疗il
‑
33相关疾病的产品中的应用具有广泛的应用前景。
[0031]
在本技术实施方式中,抗人il
‑
33中和性自身抗体的重链可变区的编码基因包括如seq id no:5所示的核苷酸序列。可以理解的,抗人il
‑
33中和性自身抗体的重链可变区的编码基因应该考虑简并碱基,即如seq id no:1所示的氨基酸序列的编码基因包括如seq id no:5所示的核苷酸序列,保护范围还应该保护与seq id no:5具有碱基简并性质的核苷酸序列,这些核苷酸序列对应的氨基酸序列仍然为seq id no:1。
[0032]
在本技术实施方式中,抗人il
‑
33中和性自身抗体的轻链可变区的编码基因包括如seq id no:6所示的核苷酸序列。可以理解的,抗人il
‑
33中和性自身抗体的轻链可变区的编码基因应该考虑简并碱基,即如seq id no:2所示的氨基酸序列的编码基因包括如seq id no:6所示的核苷酸序列,保护范围还应该保护与seq id no:6具有碱基简并性质的核苷酸序列,这些核苷酸序列对应的氨基酸序列仍然为seq id no:2。
[0033]
在本技术实施方式中,抗人il
‑
33中和性自身抗体还包括重链恒定区。进一步的,
重链恒定区为higg1、higg2、higg3或higg4。抗人il
‑
33中和性自身抗体为igg型,稳定性好,半衰期长,有利于其应用。进一步的,重链恒定区为higg1。
[0034]
在本技术实施方式中,抗人il
‑
33中和性自身抗体的重链包括如seq id no:3所示的氨基酸序列。进一步的,抗人il
‑
33中和性自身抗体的重链的编码基因包括如seq id no:7所示的核苷酸序列。可以理解的,抗人il
‑
33中和性自身抗体的重链的编码基因应该考虑简并碱基,即如seq id no:3所示的氨基酸序列的编码基因包括如seq id no:7所示的核苷酸序列,保护范围还应该保护与seq id no:7具有碱基简并性质的核苷酸序列,这些核苷酸序列对应的氨基酸序列仍然为seq id no:3。
[0035]
在本技术实施方式中,抗人il
‑
33中和性自身抗体还包括轻链恒定区。在本技术实施方式中,抗人il
‑
33中和性自身抗体的轻链为κ链或λ链。
[0036]
在本技术实施方式中,抗人il
‑
33中和性自身抗体的轻链包括如seq id no:4所示的氨基酸序列。进一步的,抗人il
‑
33中和性自身抗体的轻链的编码基因包括如seq id no:8所示的核苷酸序列。可以理解的,抗人il
‑
33中和性自身抗体的轻链的编码基因应该考虑简并碱基,即如seq id no:4所示的氨基酸序列的编码基因包括如seq id no:8所示的核苷酸序列,保护范围还应该保护与seq id no:8具有碱基简并性质的核苷酸序列,这些核苷酸序列对应的氨基酸序列仍然为seq id no:4。
[0037]
在本技术实施方式中,抗人il
‑
33中和性自身抗体为天然的人抗体。本技术发明人通过基因工程方法产生的,或通过体外诱生人b细胞产生的抗人il
‑
33中和性自身抗体,该抗人il
‑
33中和性自身抗体为天然的人抗体,不含异源片段,不会引起人体的免疫反应,更加安全有效。
[0038]
本技术提供了上述抗人il
‑
33中和性自身抗体的制备方法,包括通过基因工程或体外诱导获得。
[0039]
在本技术实施方式中,基因工程方法产生抗人il
‑
33中和性自身抗体,包括:通过鉴定获得产生抗人il
‑
33中和性自身抗体的b细胞,利用单个细胞pcr方法产生抗人il
‑
33中和性自身抗体的重链、轻链可变区的编码基因,将抗人il
‑
33中和性自身抗体的重链可变区的编码基因插入至编码人的抗体重链恒定区序列的表达质粒载体中,将抗人il
‑
33中和性自身抗体的轻链可变区的编码基因插入至编码人的抗体轻链恒定区序列的表达质粒载体中;将上述编码重链的质粒载体以及编码轻链的质粒载体同时转染哺乳动物宿主细胞,通过蛋白表达和纯化得到完整的抗人il
‑
33中和性自身抗体。具体的,重链恒定区为higg1、higg2、higg3或higg4,哺乳动物宿主细胞可以但不限于为hek293,编码人的抗体重链恒定区序列的表达质粒载体可以但不限于根据参考文献6的方法构成,也可以是商品化的表达质粒如abvec
‑
higg1(ntcc)、pfuse
‑
chig(invivogen)等,编码人的抗体轻链恒定区序列的表达质粒载体可以但不限于根据参考文献6的方法构成,也可以是商品化的表达质粒如abvec
‑
higkappa(ntcc)、pfuse2
‑
clig
‑
hk(invivogen)等。
[0040]
在本技术实施方式中,通过体外诱导获得抗人il
‑
33中和性自身抗体的方法,包括:il
‑
33抗原表位片段为免疫原,对分离的人外周血单核细胞进行体外免疫,诱导产生抗人il
‑
33中和性自身抗体。进一步的,诱导产生抗人il
‑
33中和性自身抗体的特定il
‑
33抗原表位肽段的氨基酸序列为ettkrpslktgrkh、dlkkdekkdkvlls和nnkehsvelhkcek中的至少一种。
[0041]
本技术提供了一种核酸分子,核酸分子编码上述的抗体。在本技术实施方式中,核酸分子中包括编码重链可变区的核苷酸序列。在一实施例中,核酸分子包括如seq id no:5所示的核苷酸序列,或与seq id no:5具有碱基简并性质的核苷酸序列。进一步的,核酸分子包括如seq id no:7所示的核苷酸序列,或与seq id no:7具有碱基简并性质的核苷酸序列。在本技术实施方式中,核酸分子中包括编码轻链可变区的核苷酸序列。在一实施例中,核酸分子包括如seq id no:6所示的核苷酸序列,或与seq id no:6具有碱基简并性质的核苷酸序列。进一步的,核酸分子包括如seq id no:8所示的核苷酸序列,或与seq id no:8具有碱基简并性质的核苷酸序列。
[0042]
本技术提供了含有上述核酸分子的表达盒、重组载体或重组细胞。通过将编码抗人il
‑
33中和性自身抗体的核酸分子保存在表达盒、重组载体或重组细胞中,来产生和制备抗人il
‑
33中和性自身抗体。
[0043]
在本技术实施方式中,表达盒包括上述核酸分子。进一步的,表达盒还包括启动子和终止子中的至少一种,启动子在核酸分子的上游,终止子在核酸分子的下游。
[0044]
在本技术实施方式中,重组细胞可以但不限于为重组真核细胞。
[0045]
本技术提供了一种药物组合物,包括上述的抗人il
‑
33中和性自身抗体。通过提供含有抗人il
‑
33中和性自身抗体的药物组合物,有利于其在预防或治疗il
‑
33相关疾病中的应用。
[0046]
在本技术实施方式中,药物组合物还包括药物载体,药物载体用于负载抗人il
‑
33中和性自身抗体。可选的,载体包括溶剂、聚合物和脂质体中的至少一种。具体的,溶剂包括但不限包括水、生理盐水,以及其他非水性溶剂;聚合物可以但不限于包括聚赖氨酸、聚乙烯亚胺及其改性物、壳聚糖、聚乳酸、明胶;脂质体可以但不限于包括胆固醇、豆卵磷脂、蛋黄卵磷脂。在一实施例中,药物载体还包括稀释剂和赋形剂中的至少一种。进一步的,稀释剂包括淀粉类、糖类、纤维素类和无机盐中的至少一种;赋形剂包括片剂中的黏合剂、填充剂、润滑剂,半固体制剂软膏剂、霜剂中的基质部分,液体制剂中的防腐剂、抗氧剂、矫味剂、芳香剂、助溶剂、乳化剂、着色剂中的至少一种。
[0047]
在本技术实施方式中,药物组合物中抗人il
‑
33中和性自身抗体的质量分数为10%
‑
95%。进一步的,药物组合物中抗人il
‑
33中和性自身抗体的质量分数为20%
‑
80%、25%
‑
75%或30%
‑
60%等。
[0048]
在本技术实施方式中,药物组合物还可以包括第二活性成分。第二活性成分根据药物组合物的用途进行选择,在此不作限定。具体的可以但不限于,当药物组合物用于过敏性哮喘时,第二活性成分具有治疗过敏性哮喘的作用;当药物组合物用于过敏性皮炎时,第二活性成分具有治疗过敏性皮炎的作用等。
[0049]
在本技术实施方式中,药物组合物的形式包括片剂、胶囊、粉剂、颗粒剂、丸剂、糖浆剂、溶液剂、混悬剂和气雾剂中的至少一种。
[0050]
本技术提供了上述抗人il
‑
33中和性自身抗体、核酸分子、表达盒、重组载体、重组细胞、或药物组合物在制备诊断或预后评估il
‑
33介导的疾病的试剂中的应用。在一实施例中,可以采用上述抗人il
‑
33中和性自身抗体、核酸分子、表达盒、重组载体或重组细胞来制备试剂,该试剂可以用于诊断il
‑
33介导的疾病,或者对il
‑
33介导的疾病进行预后评估。
[0051]
本技术提供了上述抗人il
‑
33中和性自身抗体、核酸分子、表达盒、重组载体、重组
细胞、或药物组合物在制备预防或治疗il
‑
33介导的疾病的药品中的应用。在一实施例中,可以采用上述抗人il
‑
33中和性自身抗体、核酸分子、表达盒、重组载体、重组细胞、或药物组合物来制备药品,该药品可以用于预防il
‑
33介导的疾病的产生,或者对il
‑
33介导的疾病进行治疗。
[0052]
在本技术实施方式中,il
‑
33介导的疾病可以但不限于感染性疾病、自身免疫病等,其中感染性疾病包括感染性休克、流感病毒引起的肺炎等,自身免疫病包括系统性红斑狼疮、结肠炎、硬皮病、类风湿关节炎等。
[0053]
实施例1基因工程方法制备抗人il
‑
33中和性自身抗体
[0054]
通过抗原表位预测软件(dnastar protean软件、sopma以及the bepi pred2.0)设计并合成了三个主要的il
‑
33抗原表位肽,结果如表1所示。通过酶联免疫吸附实验(elisa)发现,抗il
‑
33抗体阳性患者血清样本都能够识别这三个il
‑
33抗原表位肽,证明这三个il
‑
33抗原表位肽具有很高抗原性和免疫原性,可诱生il
‑
33抗体产生。因此,这三个il
‑
33抗原表位肽能够作为抗原检测患者血液中的抗人il
‑
33中和性自身抗体的水平,也可以用于活化及扩增il
‑
33特异性b细胞产生抗人il
‑
33中和性自身抗体,还能在荧光标记后可以用于通过流氏细胞分选术从血液中获得il
‑
33特异性的b细胞供克隆抗人il
‑
33中和性自身抗体基因。
[0055]
表1 il
‑
33抗原表位肽信息
[0056]
序号名称氨基酸序列长度氨基酸序列p1hil
‑
33 peptide start at 63aa14ettkrpslktgrkhp2hil
‑
33 peptide start at 149aa14dlkkdekkdkvllsp3hil
‑
33 peptide start at 197aa14nnkehsvelhkcek
[0057]
根据参考文献6报道的抗体轻链可变区、重链可变区序列设计pcr引物。收集产生il
‑
33自身抗体的哮喘患者外周血单核细胞(pbmc)。由于患者il
‑
33自身抗体可以识别表1中的il
‑
33抗原表位肽,因此,荧光标记表1中的il
‑
33抗原表位肽,并通过流式单细胞分选术找到并获得患者的il
‑
33
‑
特异性cd19
+
igg
+
cd27
+
记忆b细胞,用成熟的单个b细胞rt
‑
pcr方法(详见参考文献6),采用qiagen onestep rt
‑
pcr kit扩增获得抗人il
‑
33中和性自身抗体igg重链和轻链可变区cdna序列。获得igg轻链可变区和重链可变区片段通过1.5%琼脂糖凝胶电泳来检测,轻链可变区和重链可变区片段大约为400bp。所产生的dna片段通过切胶、dna测序以及分析(igblast和http://www.imgt.org/img t_vquest/vquest)来确认是抗体可变区。
[0058]
将以上获得的主要igg可变区cdna片段,经找出天然配对的抗体轻/重链可变区基因,巢式pcr反应来扩增全部igg可变区并引入限制性酶切位点。将抗体轻/重链可变区基因通过引入的限制性酶切位点分别插入到含有igg1轻/重链保守区的表达载体。这类表达载体通常含有真核细胞基因表达启动子和增强子,表达基因插入位点及igg1轻/重链保守区dna序列和终止密码。其中产生的抗人il
‑
33中和性自身抗体的重链可变区包括如seq id no:1所示的氨基酸序列,轻链可变区包括如seq id no:2所示的氨基酸序列。然后将构建好的表达载体质粒共转染入真核细胞hek
‑
293细胞中表达并产生完全人源单克隆igg1型的抗人il
‑
33中和性自身抗体。
[0059]
实施例2体外诱导抗人il
‑
33中和性自身抗体
[0060]
人外周血单个核细胞(pbmc)经体外抗原免疫可诱导产生特异性抗体,是一种产生人特异性抗体的方法[7],我们利用并改进这个体外免疫方法来产生抗人il
‑
33中和性自身抗体。简要来说,从抗人il
‑
33中和性自身抗体阴性的健康供体中分离出pbmc,用leu
‑
leu甲酯氢溴酸(llme)去除免疫抑制细胞。然后分别用三种il
‑
33抗原表位肽(表1)与tlr9配体cpg
‑
odn(1μm)、细胞因子il
‑
2(50ng/ml)、il
‑
4(50ng/ml)混合,在体外免疫细胞7天后,收集上清,获得抗人il
‑
33中和性自身抗体。
[0061]
效果实施例
[0062]
为了评估本技术保护的抗人il
‑
33中和性自身抗体的效果,进行如下效果实施例。
[0063]
从抗人il
‑
33中和性自身抗体阴性的健康供体中分离出pbmc,用leu
‑
leu甲酯氢溴酸(llme)去除免疫抑制细胞。然后用不同剂量的三种il
‑
33抗原肽(表1)与tlr9配体cpg
‑
odn(1μm)、细胞因子il
‑
2(50ng/ml)、il
‑
4(50ng/ml)单独或共同作用,在体外免疫细胞7天后,收集上清,通过elisa检测抗人il
‑
33中和性自身抗体浓度,结果如图1所示,其中,第一组为外周血单核细胞,第二组为外周血单核细胞加入tlr9配体cpg
‑
odn,第三组为外周血单核细胞加入细胞因子il
‑
2,第四组为外周血单核细胞加入细胞因子il
‑
4,第五组为外周血单核细胞加入tlr9配体cpg
‑
odn、细胞因子il
‑
2、il
‑
4和0.1μg/ml的抗原表位肽,第六组为外周血单核细胞加入tlr9配体cpg
‑
odn、细胞因子il
‑
2、il
‑
4和1μg/ml的抗原表位肽,第七组为外周血单核细胞加入tlr9配体cpg
‑
odn、细胞因子il
‑
2、il
‑
4和5μg/ml的抗原表位肽,第八组为外周血单核细胞加入tlr9配体cpg
‑
odn、细胞因子il
‑
2、il
‑
4和10μg/ml的抗原表位肽,其中图1中a为加入人il
‑
33多肽抗原1(p1)的检测结果,图1中b为加入人il
‑
33多肽抗原2(p2)的检测结果,图1中c为加入人il
‑
33多肽抗原3(p3)的检测结果,数据代表3个独立实验,*p<0.05,**p<0.01与pbmc或细胞因子单独实验组作为对照。il
‑
2、il
‑
4和tlr9信号可以增强b细胞增殖、向浆细胞分化以及抗体从igm向igg转换。从图1可以看出,cpg或单独的细胞因子对il
‑
33自身抗体产生没有作用,单独的抗原对抗体诱导也无显著影响(数据未显示)。然而,il
‑
33抗原表位肽抗原与细胞因子和cpg一起可以诱导抗il
‑
33抗体的产生。il
‑
33的三种抗原表位肽不但可被哮喘患者抗人il
‑
33中和性自身抗体识别,也可以诱生抗人il
‑
33中和性自身抗体。抗原量效研究结果表明,不同il
‑
33抗原表位肽免疫诱生抗人il
‑
33中和性自身抗体的最佳抗原剂量不同。这一结果表明,当存在cpg和细胞因子il
‑
2、il
‑
4时,il
‑
33多肽抗原可以在体外诱导人b细胞产生igg型抗人il
‑
33中和性自身抗体。这个方法不仅可以直接用来产生抗il
‑
33抗体,也可以用于获得il
‑
33抗体产生b细胞,然后按实施例1方法来克隆抗体可变区,通过基因工程方法产生单克隆抗人il
‑
33中和性自身抗体。
[0064]
用荧光素酶免疫沉淀系统(lips,详细方法见参考文献8)检测了36例轻型过敏性哮喘患者和96例健康对照者血清中抗4种关键th2细胞因子的自身抗体滴度,抗体滴度以相对发光单位(rlu)/微升血清表示,同时测定182例重症过敏性哮喘患者和96例健康对照者血清中il
‑
33自身抗体滴度,并比较轻、重型过敏性哮喘患者抗il33抗体阳性样本的百分比,其中过敏性哮喘患者按诊断标准划分为轻型过敏性哮喘患者和重型过敏性哮喘患者[9
‑
10]。检测结果如图2所示,其中健康对照者血清样本滴度的95%作为正常值上限(图2中的虚线),图2中a
‑
d是轻型过敏性哮喘患者自身抗体检测结果,图2中a为抗il
‑
4抗体的检测结果,图2中b为抗il
‑
5抗体的检测结果,图2中c为抗il
‑
13抗体的检测结果,图2中d为抗il
‑
33抗体的检测结果,图2中e为重型过敏性哮喘患者抗il
‑
33自身抗体的检测结果,图2中f为
轻型和重型过敏性哮喘患者抗il
‑
33自身抗体的阳性率,数据为平均值
±
标准偏差(sd),代表三个独立的实验,*p<0.05,**p<0.01,***p<0.001。在4种血清细胞因子自身抗体检测结果中,轻型哮喘患者血清中只有抗人il
‑
33自身抗体滴度与健康对照组有显著差异(图2中d),其他炎症和调节细胞因子自身抗体的血清滴度没有显著差异。这说明过敏性哮喘患者选择性的产生il
‑
33自身抗体。此外还比较了轻型过敏性哮喘患者和182例重型过敏性哮喘患者间的差异,发现极少数(6%)的重型哮喘患者产生il
‑
33自身抗体,明显低于轻型哮喘患者(28%)(图2中f)。由此可以看出,主要是轻型过敏性哮喘患者产生抗人il
‑
33中和性自身抗体。因此,抗人il
‑
33中和性自身抗体可以作为过敏性哮喘的生物标志来区分轻重型哮喘患者以及评估哮喘患者的病情发展预后情况。
[0065]
用il
‑
33重组蛋白(0.2μg/ml)包被elisa板,与图2中发现的轻、重型哮喘患者抗il
‑
33抗体阳性血清各10例孵育,然后加入荧光酶标记的抗人igg、igm或iga抗体和底物后测定抗体滴度(od),用elisa方法测定轻、重型过敏性哮喘患者抗人il
‑
33中和性自身抗体类型,结果如图3所示,其中图3中a为igg型抗体,图3中b为igm型抗体,图3中c为iga型抗体,数据为平均值
±
sd,代表三个独立的实验,*p<0.05,**p<0.01,***p<0.001。抗体类型分析表明轻、重型哮喘患者产生的il
‑
33自身抗体类型水平不同,重型哮喘患者血清中的igm型il
‑
33自身抗体水平显著高于轻型哮喘患者,说明这些抗体是新近产生的,很可能是发展成重型哮喘后产生的(图3中b)。因此,图2和图3说明il
‑
33自身抗体及抗体类型可以作为过敏性哮喘的生物标志来区分轻重型哮喘,以及哮喘患者的病情发展预后。
[0066]
合成表1中所示的三个il
‑
33主要的抗原表位肽片段,p1、p2和p3肽抗原分别包被elisa板过夜,并用elisa法对10例抗人il
‑
33中和性自身抗体阳性的轻型哮喘患者血清和3例正常对照组的血清进行了il
‑
33肽抗原特异性检测,确定抗人il
‑
33中和性自身抗体在il
‑
33蛋白的识别位点,结果如图4所示,其中图4中a为对p1识别的检测结果,图4中b为对p2识别的检测结果,图4中c为p3识别的检测结果,每个条柱表示单个血清样本获得的结果,数据为平均值
±
sd,代表三个独立的实验,*p<0.05,**p<0.01,***p<0.001。从图4中可以看出,所有lips检测il
‑
33抗体阳性的哮喘样本经elisa检测也均为阳性,阴性正常对照组中il
‑
33抗体elisa检测也均为阴性;所有的抗il
‑
33抗体阳性血清样本都能够识别il
‑
33的三种主要肽抗原,但不同样本识别的抗原表位的水平和图谱不同。以上数据表明哮喘患者血清抗人il
‑
33中和性自身抗体是多克隆的,至少识别表1中所示的三个il
‑
33结构表位。
[0067]
为了评估哮喘患者抗人il
‑
33中和性自身抗体是否有中和作用,基于il
‑
33可以诱导活化t细胞产生il
‑
5,以及通过其受体st2在巨噬细胞中诱生il
‑
33的能力,建立抗体介导的il
‑
33体外中和实验方法。用体外培养的健康人外周血单核细胞(pbmc)检测患者血清抗人il
‑
33中和性自身抗体是否能阻断il
‑
33诱导的il
‑
5和il
‑
33产生。在抗
‑
cd3抗体活化的人外周血单核细胞(pbmc)中加或不加il
‑
33重组蛋白刺激,或抗人il
‑
33中和性自身抗体和il
‑
33抗体阳性血清培养24小时,提取细胞rna,用qpcr方法检测抗人il
‑
33中和性抗体和il
‑
33抗体阳性血清(n=10)对il
‑
33活性的中和能力,即采用qpcr检测il
‑
33诱导的il
‑
5和il
‑
33mrna表达水平,结果如图5所示,数据为平均值
±
sd,代表三个独立的实验。*p<0.05,**p<0.01,***p<0.001,其中第一组为外周血单核细胞,第二组为外周血单核细胞加入il
‑
33重组蛋白,第三组为外周血单核细胞加入il
‑
33重组蛋白和抗人il
‑
33中和性抗体,第四组为外周血单核细胞加入il
‑
33重组蛋白和抗人il
‑
33中和性自身抗体阳性血清,第五
组为外周血单核细胞加入il
‑
33重组蛋白和抗人il
‑
33中和性自身抗体阴性血清,其中图5中a为il
‑
5的检测结果,图5中b为il
‑
33的检测结果。结果表明抗人il
‑
33中和性自身抗体和抗人il
‑
33中和性自身抗体阳性的哮喘血清样品明显抑制il
‑
33诱导的il
‑
5和il
‑
33的mrna表达,但哮喘患者抗人il
‑
33中和性自身抗体阴性的血清没有抑制作用。这10份来自轻型哮喘患者血清样本的汇总结果表明,哮喘患者产生的抗人il
‑
33中和性自身抗体均具有il
‑
33活性中和作用。因此,抗人il
‑
33中和性自身抗体是中和性抗体。
[0068]
采用milliplex map细胞因子测试盒(8
‑
plex)检测35例轻型哮喘患者的血清细胞因子浓度(其中9例il
‑
33自身抗体阳性,26例阴性)中关键细胞因子,结果如图6所示,数据为平均值
±
sd,*p<0.05,**p<0.01,图6中a为il
‑
4的检测结果,图6中b为il
‑
9的检测结果,图6中c为il
‑
13的检测结果,图6中d为il
‑
25的检测结果,图6中e为il
‑
33的检测结果。与抗人il
‑
33中和性自身抗体阴性哮喘患者相比,抗人il
‑
33中和性自身抗体阳性患者血清中哮喘病理相关的细胞因子il
‑
4、il
‑
13、il
‑
25和il
‑
33的浓度显著降低,但il
‑
9的浓度变化不显著。ige在过敏性哮喘发病中起重要的促进作用,采用elisa法检测这35例哮喘患者血清ige水平,结果如图7所示,数据为平均值
±
sd,*p<0.05,**p<0.01。抗人il
‑
33中和性自身抗体阳性样本血清中ige浓度显著低于抗人il
‑
33中和性自身抗体阴性的哮喘患者样本。这些结果与抗人il
‑
33中和性自身抗体在体外作为中和抗体的功能一致,并表明抗人il
‑
33中和性自身抗体对哮喘有保护作用,不但可以降低病理性ii型细胞因子、ige水平,还抑制自身il
‑
33产生。
[0069]
人il
‑
33可以诱导小鼠肺部炎症、肺内炎细胞产生il
‑
5、il
‑
13等哮喘样改变[3],因此可以用来研究抗人il
‑
33中和性自身抗体是否可以有效的中和il
‑
33活性,并减轻人il
‑
33诱导的哮喘病理改变。将6周balb/c小鼠随机分为4个组,第一组为生理盐水对照组;第二组为il
‑
33重组蛋白(ril
‑
33),剂量为0.4μg/只;第三组为ril
‑
33+igg(2μg/只)对照组;第四组为ril
‑
33+抗人il
‑
33中和性自身抗体(2μg/只)组。通过滴鼻给药,ril
‑
33+抗人il
‑
33中和性自身抗体或对照igg先混合孵育30分钟后再滴鼻给药,3天后结束实验,检测结果如图8所示,其中图8中a为小鼠肺灌洗液(balf)中的淋巴细胞计数,图8中b为血清中il
‑
5的检测结果,图8中c为血清中il
‑
13的检测结果,图8中d为血清中tslp的检测结果。和对照组相比,抗人il
‑
33中和性自身抗体明显减少了il
‑
33诱发的呼吸道炎性淋巴细胞浸润(图8中a),抗人il
‑
33中和性自身抗体有效减少血清中il
‑
33诱生的炎性细胞因子il
‑
5、il
‑
13和tslp水平(图8中b
‑
d)。因此,抗人il
‑
33中和性自身抗体在体内具有很好的il
‑
33中和作用,可以有效的阻断il
‑
33诱导的肺炎和哮喘样病变,对哮喘具有预防和治疗作用。
[0070]
参考文献:
[0071]
1.holgate st,wenzel s,postma ds,weiss st,renz h,sly pd.asthma.nat rev dis primers.2015,1(1):15025.
[0072]
2.liew fy,girard jp,turnquist hr.interleukin
‑
33in health and disease.nat rev immunol.2016.16(11):676
‑
689.
[0073]
3.schmitz,j.,a.owyang,e.oldham,y.song,e.murphy,t.k.mcclanahan,g.zurawski,m.moshrefi,j.qin,x.li,et al il
‑
33,an interleukin
‑1‑
like cytokine that signals via the il
‑
1receptor
‑
related protein st2 and induces t helper type 2
‑
associated cytokines.immunity 2005.23:479
‑
490.
[0074]
4.kurowska
‑
stolarska m,kewin p,murphy g,russo rc,stolarski b,garcia cc,komai
‑
koma m,pitman n,li y,niedbala w,mckenzie an,teixeira mm,liew fy,xu d.il
‑
33induces antigen
‑
specific il
‑
5+t cells and promotes allergic
‑
induced airway inflammation independent of il
‑
4.j immunol.2008.181(7):4780
‑
90
[0075]
5.li d,guabiraba r,besnard ag,komai
‑
koma m,jabir ms,zhang l,graham gj,kurowska
‑
stolarska m,liew fy,mcsharry c,xu d.il
‑
33 promotes st2
‑
dependent lung fibrosis by the induction of alternatively activated macrophages and innate lymphoid cells in mice.j allergy clin immunol.2014.134(6):1422
‑
1432.e11.
[0076]
6.tiller t,meffre e,yurasov s,tsuiji m,nussenzweig mc,wardemann h.efficient generation of monoclonal antibodies from single human b cells by single cell rt
‑
pcr and expression vector cloning.j immunol methods.2008,329(1
‑
2):112
‑
124.
[0077]
7.tomimatsu k,shirahata s.antigen
‑
specific in vitro immunization:a source for human monoclonal antibodies.methods mol biol.2014.1060:297
‑
307.
[0078]
8.burbelo pd,goldman r,mattson tl。a simplified immunoprecipitation method for quantitatively measuring antibody responses in clinical sera samples by using mammalian
‑
produced renilla luciferase
‑
antigen fusion proteins.bmc biotechnol.2005.5:22.
[0079]
9.kuruvilla me,lee fe,lee gb.understanding asthma phenotypes,endotypes,and mechanisms of disease.clin rev allergy immunol.2019.56(2):219
‑
233.
[0080]
10.chung kf.diagnosis and management of severe asthma.semin respir crit care med.2018.39(1):91
‑
99.
[0081]
以上所揭露的仅为本技术较佳实施例而已,当然不能以此来限定本技术之权利范围,本领域普通技术人员可以理解实现上述实施例的全部或部分流程,并依本技术权利要求所作的等同变化,仍属于发明所涵盖的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1