一种Isaindigotone衍生物及其在制备抗肿瘤药物中的应用
一种isaindigotone衍生物及其在制备抗肿瘤药物中的应用
技术领域
1.本发明属于药物化学领域,具体涉及一种isaindigotone衍生物及其制备方法和在制备抗 癌药物中的应用。
背景技术:
2.胃癌治疗方案的选择主要是基于病程,出现的生物标志物,以及临床病征。胃癌早期患 者通常通过切除手术以治疗恶性肿瘤。手术类型取决于肿瘤浸润的位置和深度,包括内镜粘 膜切除术,食管远端切除术,胃次全切除术或全胃切除术。研究显示,相比于单纯手术切除, 二期和三期的胃癌患者接受辅助治疗后的生存率更高。目前,晚期胃癌的治疗主要是通过姑 息化疗改善症状。晚期胃癌化疗药物主要有紫杉醇类(紫杉醇和多西他赛)、氟尿嘧啶类(5
ꢀ‑
氟尿嘧啶、替吉奥、卡培他滨)、铂类(顺铂和奥沙利铂)、伊立替康、表柔沙星等,且多以 氟尿嘧啶联合铂类为一线化疗方案。
[0003][0004]
在过去的十多年中,伴随着诸如高通量筛选和组合化学这样的新型技术的出现,在新药 的探索的过程中,天然产物受到越来越广泛的关注。统计显示,从1940年到2002年间获批 的抗肿瘤药物,大约54%都是来自于天然产物或者受到相关化合物得到启示研究开发所得。 因此基于天然产物的药物开发具有广阔前景。
[0005]
pi3k/akt/mtor作为一条经典的抗凋亡信号转导通路,与细胞内诸如细胞增殖,迁移等多 种正常的生理活动密切相关。与其它肿瘤类似,胃癌中也存在着pi3k/akt/mtor通路异常。 综上所述,pi3k/akt/mtor通路在胃癌组织中的过度激活提示我们这条通路中的相关蛋白 可以作为抗肿瘤治疗的靶点。
[0006]
isaindigotone是从中药板蓝根中提取得到的一种喹唑啉酮衍生物,是由喹唑啉酮与苯亚 甲基连接而成。本发明合成了一类新的isaindigotone衍生物,所述isaindigotone衍生物具有 抗癌活性,能够靶向akt蛋白,对胃癌、结直肠癌、肝癌、胰腺癌等具有良好的抑制作用, 显著高于现有一线抗癌药物pt,在制备抗癌药物中具有广泛的应用空间。
技术实现要素:
[0007]
针对上述问题,本发明的目的在于提供一种新的isaindigotone衍生物,及其在制备抗癌 药物中的应用,具体包括以下内容:
[0008]
第一方面,本发明提供了一种isaindigotone衍生物或其药学上可接受的盐,其特征在于, 所述isaindigotone衍生物结构式如下式(i)所示:
[0009][0010]
其中,
[0011]
当所述n为1,所述r1和r2为氢时,所述r3和r4为氟、r5为氢,或所述r3和r5为氢、 r4为三氟甲氧基,或所述r3和r5为三氟甲基、r4为氢;
[0012]
当所述n为1,所述r1为氢,r2为氟时,所述r3、r4和r5为甲氧基,或所述r3和r4为氟、r5为氢,或r3和r5为三氟甲基、r4为氢;
[0013]
当所述n为1,所述r1和r2为氟时,所述r3和r5为氢、r4为三氟甲氧基,或所述r3和r5为三氟甲基、r4为氢;
[0014]
当所述n为1,所述r1为氟,r2为氢时,所述r3和r4为氟、r5为氢,或所述r3和r5为甲氧基、r4为羟基,或所述r5为氢、r3和r4形成1,3-二氧五环;
[0015]
当所述n为1,所述r1和r2为甲氧基时,所述r3和r4为氟、r5为氢,或所述r3和r5为氢、r4为氟,或所述r3和r5为氢、r4为三氟甲基,或所述r3为氢,r4和r5形成1,3-二 氧五环;
[0016]
当所述n为1,所述r1为甲氧基,r2为4-甲基哌嗪基时,所述r3和r5为氢、r4为三氟 甲基,或所述r3为氢、r4和r5为氟;
[0017]
当所述n为2,所述r1和r2为氢时,所述r3和r5为氢、r4为氟,或所述r3和r5为甲 氧基、r4为羟基;
[0018]
当所述n为2,所述r1为氟,r2为氢时,所述r3、r4和r5为甲氧基,或所述r3和r5为氢、r4为氟,或所述r5为氢、r3和r5形成1,3-二氧五环。
[0019]
第二方面,本发明提供了一种上述第一方面所述的isaindigotone衍生物或其药学上可接 受的盐在制备治疗癌症药物中的应用。
[0020]
优选地,所述癌症包括胃癌、结直肠癌、肝癌、胰腺癌。
[0021]
优选地,所述癌症为胃癌,所述isaindigotone衍生物包括以下所示化合物:
[0022][0023][0024]
优选地,所述isaindigotone衍生物为:
[0025][0026]
优选地,所述isaindigotone衍生物为:
[0027][0028]
优选地,所述癌症为胰腺癌,所述isaindigotone衍生物包括以下所示化合物:
[0029][0030][0031]
优选地,所述癌症为胰腺癌,所述isaindigotone衍生物为:
[0032][0033]
优选地,所述癌症为结肠癌,所述isaindigotone衍生物包括以下所示化合物:
[0034][0035]
优选地,所述isaindigotone衍生物的结构式为:
[0036][0037]
优选地,所述癌症为肝癌,所述isaindigotone衍生物的结构式如下所示:
[0038][0039]
优选地,所述的isaindigotone衍生物或其药学上可接受的盐,加入药学上可接受的辅料 制成药学上可接受的任一剂型。
[0040]
本发明的有益效果是:本发明首先提供了一类isaindigotone衍生物;其次,本发明通过 体外mtt抗肿瘤活性研究发现,所述isaindigotone衍生物对胃癌、结直肠癌、肝癌、胰腺癌 等多种癌症细胞均具有良好的抑制作用;尤其是所述isaindigotone衍生物能够显著抑制胃癌 细胞的增值,抑制胃癌细胞的活性,具有显著的治疗胃癌的效果,且其药效显著高于现有一 线抗癌药物pt,在制备抗癌药物中具有广泛的应用空间。
附图说明
[0041]
为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简 单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的 限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图 获得其他相关的附图。
[0042]
图1 isaindigotone衍生物的合成路线图;
[0043]
图2isaindigotone衍生物blg06对胃癌细胞体外抗增殖活性的影响结果;
[0044]
图3isaindigotone衍生物blg06对胃癌ags细胞形态的影响结果;
[0045]
图4isaindigotone衍生物blg06对胃癌ags细胞周期及凋亡的影响结果;
[0046]
图5isaindigotone衍生物blg06对线粒体(mmp)膜电位变化的影响结果;
[0047]
图6分子对接及蛋白质印迹实验结果;
[0048]
图7isaindigotone衍生物blg06抑制ags细胞迁移的结果。
具体实施方式
[0049]
为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
[0050]
以下实施例所用的人癌细胞系包括结直肠癌细胞系hct116、胃癌细胞系ags、胰腺癌细胞系panc-1、肝癌smmz-7721以及正常胃细胞系ges-1;所述hct116、ags、panc-1购自atcc(美国);所述smmz-7721和ges-1购自兰州大学药学院。除hct116、ags、smmz-7721细胞系在1640培养基(1640,solarbioinvitrogencorp.,beijing,china)中培养;panc-1和ges-1细胞系在高糖培养基(dmem,solarbioinvitrogencorp.,beijing,china)中培养;培养条件为:37℃、5%co2条件,所有细胞都补充有10%胎牛血清(fbs)、100u/ml青霉素和100mg/ml链霉素。
[0051]
实施例1isaindigotone衍生物的制备
[0052]
isaindigotone衍生物的合成路线如图1所示,合成的isaindigotone衍生物分别用blg01-22表示,合成的isaindigotone衍生物的结构式如下表1所示:
[0053]
(1)b1-b7的合成:在室温下,将45mlpocl3小心地添加到各种2-氨基苯甲酸(a1-5,19.30mmol,1eq)和吡咯烷-2酮或2-哌啶酮(38.60mmol,2eq)的混合溶液中;然后将混合物在110℃搅拌7h;减压除去pocl3后,将残余物倒入冰水中,然后加入naoh溶液使溶液呈碱性;混合物用3
×
50ml的ch2cl2萃取;合并的有机相用mgso4干燥,真空浓缩,然后通过快速柱纯化,用石油醚/etoac(4:1)洗脱,得到白色固体。
[0054]
(2)b8的合成:将催化量的na2co3加入到中间体b4(15.00mmol)和n-甲基哌嗪(4.00ml)的dmf(36.00ml)溶液中;然后将混合物在140℃搅拌2h;减压除去部分dmf后,将残渣倒入30.00ml水中,过滤,水洗,得到白色固体。
[0055]
(3)blg01-blg22的合成:将催化量的naoac加入到中间体b1-b8(10.00mmol)和不同取代的苯甲醛(c1-7,20.00mmol),acoh(70.00ml)溶液中;然后将混合物在115℃下搅拌6h;减压除去部分acoh后,将残余物倒入15.00ml冰冷的丙酮中,然后过滤并用丙酮洗涤,得到白色或黄色固体。
[0056]
得到的化合物分别用blg01-blg22表示,其中blg01-blg22的谱图数据如下所示:
[0057]
blg01:(e)-3-(3,4-difluorobenzylidene)-2,3-dihydropyrrolo[2,1-b]quinazolin-9(1h)-one;yield:69%;yellowsolid,m.p.218-220℃;1hnmr(400mhz,cdcl3)δ:8.29(d,j=7.9hz,1h),7.87
–
7.63(m,3h),7.45(m,1h),7.37(m,1h),7.27(m,2h),4.31(t,j=7.2hz,2h),3.26(t,j=7.4hz,2h).13cnmr(100mhz,cdcl3)δ:161.11,
155.03,151.66(d,j=13.0hz),149.54,149.19(d,j=12.8hz),134.32,132.56(d,j=2.8hz),128.37(d,j=2.3hz),127.34,126.44,126.41,120.95,118.12,117.94,117.92,117.74,44.00,25.34.ms-esim/z:calcdforc18h12f2n2o[m+h]+:311.0918;found:311.0985.
[0058]
blg02:(e)-3-(4-(trifluoromethoxy)benzylidene)-2,3-dihydropyrrolo[2,1-b]quinazolin-9(1h)-one;yield:73%;yellowsolid,m.p.174-175℃;1hnmr(400mhz,cdcl3)δ:8.29(d,j=8.0hz,1h),7.82(d,j=3.0hz,1h),7.75(d,j=4.1hz,2h),7.58(d,j=8.4hz,2h),7.44(m,1h),7.36
–
7.12(m,2h),4.30(t,j=7.2hz,2h),3.27(t,j=7.4,2h).13cnmr(100mhz,cdcl3)δ:161.15,155.19,149.59,149.26,134.29,134.10,132.48,131.10,128.97,127.33,126.43,126.34,121.12,120.95,44.00,25.44.ms-esim/z:calcdforc19h13f3n2o2[m+h]+:359.0929;found:359.0986.
[0059]
blg03:(e)-3-(3,5-bis(trifluoromethyl)benzylidene)-2,3-dihydropyrrolo[2,1-b]quinazolin-9(1h)-one;yield:76%;yellowsolid,m.p.318-320℃;1hnmr(400mhz,cdcl3)δ:8.33(d,j=8.0hz,1h),7.98(s,2h),7.93(s,1h),7.87(s,1h),7.78(d,j=2.1hz,2h),7.50(m,1h),4.36(t,j=7.1hz,2h),3.35(t,j=7.5hz,2h).13cnmr(100mhz,cdcl3)δ:161.05,137.46,135.82,134.46,132.58,132.24,129.03,129.01,127.57,127.18,126.81,126.51,122.06,121.73,121.11,44.01,25.46.ms-esim/z:calcdforc20h12f6n2o[m+h]+:411.0854;found:411.0877.
[0060]
blg04:(e)-6-fluoro-3-(3,4,5-trimethoxybenzylidene)-2,3-dihydropyrrolo[2,1-b]quinazolin-9(1h)-one;yield:85%;yellowsolid,m.p.212-214℃;1hnmr(400mhz,cdcl3)δ:8.28(dd,j=8.8,6.2hz,1h),7.77(d,j=2.9hz,1h),7.36(dd,j=9.9,2.5hz,1h),7.14(m,1h),6.80(s,2h),4.30(t,j=7.3hz,2h),3.92(d,j=2.4hz,9h),3.38(t,j=7.3hz,2h).13cnmr(100mhz,cdcl3)δ:160.54,156.77,153.38,139.40,131.54,130.85,130.14,128.96(d,j=10.7hz),117.58,114.87(d,j=8.4hz),114.68,112.36(d,j=21.7hz),112.07,107.41,61.01,56.30,44.07,25.42.ms-esim/z:calcdforc21h19fn2o4[m+h]+:383.1329;found:383.1378.
[0061]
blg05:(e)-3-(3,5-bis(trifluoromethyl)benzylidene)-6-fluoro-2,3-dihydropyrrolo[2,1-b]quinazolin-9(1h)-one;yield:80%;yellowsolid,m.p.208-209℃;1hnmr(400mhz,cdcl3)δ:8.31(dd,j=8.8,6.1hz,1h),7.98(s,2h),7.92(t,j=3.0hz,1h),7.88(s,1h),7.39(dd,j=9.7,2.5hz,1h),7.19(t,j=8.5hz,1h),4.35(t,j=7.1hz,2h),3.35(t,j=7.2hz,2h).13cnmr(100mhz,cdcl3)δ:167.85,165.32,160.33,155.61,151.66(d,j=13.1hz),137.27,135.48,132.45(d,j=33.6hz),129.57-128.55(m),127.86,124.41,122.23(d,j=4.3hz),121.70,117.82,115.51(d,j=23.7hz),112.75(d,j=22.0hz),44.06,25.43.ms-esim/z:calcdforc20h11f7n2o[m+h]+:429.0760;found:429.0565.
[0062]
blg06:(e)-3-(3,4-difluorobenzylidene)-6-fluoro-2,3-dihydropyrrolo[2,1-b]quinazolin-9(1h)-one;yield:83%;yellowsolid,m.p.243-245℃;1hnmr(400mhz,cdcl3)δ:8.31(dd,j=8.8,6.2hz,1h),7.77(d,j=2.6hz,1h),7.38(dd,j=9.7,2.5hz,1h),7.31(m,1h),7.26(m,1h),7.17(m,1h),4.31(t,j=7.3hz,2h),3.29(t,j=
7.3hz,2h).13 c nmr(100mhz,cdcl3)δ:160.45,158.60,156.27,151.84(d,j=13.6hz),151.65,1 29.09(d,j=4.5hz),128.96,126.53,126.47,118.12(d,j=18.8hz),117.98,117.75(d, j=9.9hz),115.24,115.01,112.66,112.44,44.04,25.34.ms-esi m/z:calcd for c18h11 f3n2o[m+h]+:329.0823;found:329.0700.
[0063]
blg07:(e)-6,7-difluoro-3-(4-(trifluoromethoxy)benzylidene)-2,3-dihydropyrrolo[2,1-b]quina zolin-9(1h)-one;yield:72%;yellow solid,m.p.167-169℃;1h nmr(400mhz,cdcl3) δ:8.04(dd,j=10.0,8.5hz,1h),7.81(t,j=2.9hz,1h),7.68-7.55(m,2h),7.51(d d,j=10.9,7.0hz,1h),7.31(d,j=8.3hz,2h),4.63-4.07(m,2h),3.30(t,j=7.3 hz,2h).13c nmr(100mhz,cdcl3)δ:159.78,156.27,155.98,149.44,133.84,131.92, 131.19,129.72,121.69,121.17,117.81,115.01,114.84,113.86,113.68,44.17,25.39.ms
‑ꢀ
esi m/z:calcd for c19h11f5n2o2[m+h]+:395.0741;found:395.0612.
[0064]
blg08:(e)-3-(3,5-bis(trifluoromethyl)benzylidene)-6,7-difluoro-2,3-dihydropyrrolo[2,1-b]qu inazolin-9(1h)-one;yield:79%;yellow solid,m.p.216-218℃;1h nmr(400mhz,cdcl 3)δ:1h nmr(400mhz,chloroform-d)δ8.06(dd,j=10.0,8.5hz,1h),7.98(s,2h), 7.89(s,1h),7.52(dd,j=10.8,7.0hz,1h),4.35(t,j=7.1hz,2h),3.36(t,j=7.3 hz,2h).13c nmr(100mhz,cdcl3)δ:159.66,156.26(d,j=14.8hz),155.15(d,j =2.5hz),153.70(d,j=14.6hz),150.92(d,j=14.4hz),148.41(d,j=14.4hz),14 7.23(d,j=9.7hz),137.20,135.25,132.48(d,j=33.6hz),129.06,127.86,124.40,122. 57-121.98(m),121.69,118.01(d,j=6.4hz),115.17(d,j=17.9hz),113.87(dd,j= 19.3,2.5hz),44.17,25.39.ms-esi m/z:calcd for c20h10f8n2o[m+h]+:447.0665;fo und:447.0503.
[0065]
blg09:(e)-7-fluoro-3-(4-hydroxy-3,5-dimethoxybenzylidene)-2,3-dihydropyrrolo[2,1-b]qui nazolin-9(1h)-one;yield:85%;yellow solid,m.p.243-245℃;1h nmr(400mhz,cdcl 3)δ:7.91(dd,j=8.5,3.0hz,1h),7.82-7.61(m,2h),7.45(m,1h),6.82(s,2h),4.3 0(t,j=7.4hz,2h),3.95(s,6h),3.47-3.21(m,2h).13c nmr(100mhz,cdcl3)δ: 161.69,160.56,159.23,155.27,147.20,146.46,136.29,131.11,129.29,128.64,127.03,12 2.79(d,j=24.2hz),121.90(d,j=8.6hz),111.29(d,j=23.7hz),107.10,56.39,44. 08,25.43.ms-esi m/z:calcd for c20h17fn2o4[m+h]+:369.1172;found:369.1040.
[0066]
blg10:(e)-3-(benzo[d][1,3]dioxol-5-ylmethylene)-7-fluoro-2,3-dihydropyrrolo[2,1-b]quinaz olin-9(1h)-one;yield:78%;yellow solid,m.p.288-290℃;1h nmr(400mhz,cdcl3)δ: 7.92(dd,j=8.5,3.0hz,1h),7.78-7.65(m,2h),7.59-7.39(m,2h),7.09(d,j=8. 5hz,1h),6.89(d,j=7.5hz,1h),6.04(s,2h),4.29(t,j=7.4hz,2h),3.34-3.20 (m,1h).13c nmr(100mhz,cdcl3)δ:160.53,148.32(d,j=20.7hz),130.57,129.4 0(d,j=8.2hz),129.01(d,j=7.3hz),125.40,123.67,122.90,111.29(d,j=23.6h z),110.05,109.01,108.80,108.04,107.73,101.57,101.01,56.05,44.08,25.51.ms-esi m/ z:calcd for c19h13fn2o3[m+h]+:337.0910;found:337.0950.
[0067]
blg11:(e)-3-(3,4-difluorobenzylidene)-7-fluoro-2,3-dihydropyrrolo[2,
esim/z:calcdforc21h17f3n2o3[m+h]+:403.1191;found:403.1145.
[0072]
blg16:(e)-3-(3,4-difluorobenzylidene)-7-fluoro-6-(4-methylpiperazin-1-yl)-2,3-dihydropyrrolo[2,1-b]quinazolin-9(1h)-one;yield:69%;yellowsolid,m.p.231-233℃;1hnmr(400mhz,cdcl3)δ:7.76(d,j=12.9hz,1h),7.61(d,j=3.1hz,1h),7.32-7.24(m,1h),7.23-7.12(m,2h),7.08(d,j=7.8hz,1h),4.20(t,j=7.1hz,2h),3.24(t,j=4.8hz,4h),3.17(d,j=9.8hz,2h),2.56(t,j=4.9hz,4h),2.31(s,3h).13cnmr(100mhz,cdcl3)δ:159.11,154.14(d,j=44.5hz),151.88,150.65(d,j=12.7hz),148.16(d,j=16.1hz),146.51,145.35(d,j=10.0hz),131.67,126.89,125.27,117.06,116.89,116.73,114.17(d,j=3.6hz),113.51(d,j=8.4hz),111.04(d,j=23.7hz),53.89,48.91(d,j=4.7hz),45.09,42.93,24.38.ms-esim/z:calcdforc23h21f3n4o[m+h]+:427.1667;found:427.1769.
[0073]
blg17:(e)-7-fluoro-6-(4-methylpiperazin-1-yl)-3-(4-(trifluoromethyl)benzylidene)-2,3-dihydropyrrolo[2,1-b]quinazolin-9(1h)-one;yield:78%;whitesolid,m.p.228-230℃;1hnmr(400mhz,cdcl3)δ:7.83
–
7.69(m,2h),7.65
–
7.49(m,4h),7.09(d,j=7.8hz,1h),4.21(t,j=7.1hz,2h),3.23(m,6h),2.56(t,j=4.8hz,4h),2.31(s,3h).13cnmr(100mhz,cdcl3)δ:159.07(d,j=3.2hz),154.42,153.82(d,j=2.2hz),151.94,146.49,145.37(d,j=10.1hz),137.82,133.38,129.40(d,j=32.8hz),128.66,127.43,124.76(q,j=3.8hz),114.24(d,j=3.6hz),113.57(d,j=8.5hz),111.06(d,j=23.8hz),53.89,48.91(d,j=4.7hz),45.08,42.94,24.61.ms-esim/z:calcdforc24h22f4n4o[m+h]+:459.1730;found:459.1257.
[0074]
blg18:(e)-6-(4-hydroxy-3,5-dimethoxybenzylidene)-6,7,8,9-tetrahydro-11h-pyrido[2,1-b]quinazolin-11-one;yield:79%;yellowsolid,m.p.226-227℃;1hnmr(400mhz,cdcl3)δ:8.36-8.14(m,1h),8.08(d,j=2.1hz,1h),7.71-7.52(m,2h),7.35(m,1h),6.68(s,2h),5.70(s,1h),4.25-4.03(m,2h),3.86(s,6h),2.91(t,j=6.6hz,2h),1.98(t,j=10.5hz,2h).13cnmr(100mhz,cdcl3)δ:161.14,150.95,146.60,145.86,134.80,134.46,133.11,127.16,126.64,126.19,125.66,125.03,119.03,106.39,55.40,41.06,24.99,21.12.ms-esim/z:calcdforc21h20n2o4[m+h]+:365.1423;found:365.1433.
[0075]
blg19:(e)-6-(4-fluorobenzylidene)-6,7,8,9-tetrahydro-11h-pyrido[2,1-b]quinazolin-11-one;yield:85%;yellowsolid,m.p.165-166℃;1hnmr(400mhz,cdcl3)δ:8.408.23(m,1h),8.18(d,j=2.2hz,1h),7.73(dd,j=7.0,1.7hz,2h),7.45(td,j=8.5,5.7hz,3h),7.12(t,j=8.7hz,2h),4.32-3.93(m,2h),3.03-2.71(m,2h),2.12-1.90(m,2h).13cnmr(100mhz,cdcl3)δ:163.65,162.12,151.63,147.51,134.19(d,j=4.6hz),132.37(d,j=3.4hz),131.80(d,j=8.1hz),129.84(d,j=1.7hz),127.30,126.68,126.24,120.17,115.61,115.40,42.19,25.71,22.06.ms-esim/z:calcdforc19h15fn2o[m+h]+:307.1168;found:307.1299.
[0076]
blg20:(e)-2-fluoro-6-(3,4,5-trimethoxybenzylidene)-6,7,8,9-tetrahydro-11h-pyrido[2,1-b]quinazolin-11-one;yield:82%;yellowsolid,m.p.164-166℃;1hnmr(400mhz,cdcl3)δ:8.14(d,j=2.2hz,1h),7.90(dd,j=8.5,
3.0hz,1h),7.72(dd,j=9.0,4.9hz,1h),7.46(d,j=3.0hz,1h),6.71(s,2h),4.29-4.07(m,2h),3.91(s,3h),3.90(s,6h),2.98(td,j=6.6,2.1hz,2h),2.05(t,j=6.2hz,2h).13cnmr(100mhz,cdcl3)δ:161.76,161.49,159.29,153.06,151.05(d,j=2.3hz),144.28,138.52,135.48,131.67,129.67(d,j=8.0hz),129.17,122.93(d,j=24.3hz),121.15(d,j=8.6hz),111.36(d,j=23.5hz),107.51,60.98,56.26,42.38,25.85,22.04.ms-esim/z:calcdforc22h21fn2o4[m+h]+:397.1485;found:397.1504.
[0077]
blg21:(e)-6-(benzo[d][1,3]dioxol-5-methylene)-2-fluoro-6,7,8,9-tetrahydro-11h-pyrido[2,1-b]quinazolin-11-one;yield:84%;yellowsolid,m.p.232-234℃;1hnmr(400mhz,cdcl3)δ:8.11(s,1h),7.89(dd,j=8.6,3.1hz,1h),7.75(d,j=7.9hz,1h),7.54-7.42(m,1h),7.01(d,j=8.9hz,2h),6.88(d,j=8.0hz,1h),6.02(s,2h),4.16(t,j=5.9hz,2h),3.07-2.84(m,2h),2.11-1.91(m,2h).13cnmr(100mhz,cdcl3)δ:161.73,161.43,159.26,151.45,147.82,147.78,135.54,130.27,129.57,129.47,125.20,122.96(d,j=24.3hz),121.04(d,j=8.7hz),111.38(d,j=23.5hz),109.81,108.45,101.39,42.24,25.88,22.02.ms-esim/z:calcdforc20h15fn2o3[m+h]+:351.1067;found:351.1123.
[0078]
blg22:(e)-2-fluoro-6-(4-fluorobenzylidene)-6,7,8,9-tetrahydro-11h-pyrido[2,1-b]quinazolin-11-one;yield:75%;yellowsolid,m.p.183-185℃;1hnmr(400mhz,cdcl3)δ:8.16(s,1h),7.90(dd,j=8.5,3.0hz,1h),7.72(dd,j=9.0,4.9hz,1h),7.51-7.41(m,3h),7.12(t,j=8.6hz,2h),4.20-4.12(m,2h),2.97-2.88(m,2h),2.11-1.91(m,2h).13cnmr(100mhz,cdcl3)δ:163.70,161.80,161.43(d,j=3.6hz),161.22,159.34,151.01(d,j=2.4hz),144.15,134.30,132.26(d,j=3.5hz),131.80(d,j=8.2hz),129.66(d,j=8.1hz),129.49,122.96(d,j=24.4hz),121.19(d,j=8.7hz),115.54(d,j=21.5hz),111.38(d,j=23.5hz),42.37,25.65,21.98.ms-esim/z:calcdforc19h14f2n2o[m+h]+:325.1074;found:325.1153.
[0079]
上述得到的isaindigotone衍生物blg01-22的结构式如下表1所示。
[0080]
表1isaindigotone衍生物的结构式
[0081]
[0082][0083]
实施例2 isaindigotone衍生物对不同人类癌细胞系的体外抗癌活性
[0084]
通过mtt法研究了22种isaindigotone衍生物对不同人类癌细胞系(包括ags、hct1 16、smmz-7721和panc-1)的体外抗癌活性,顺铂用作阳性对照。具体方法为:
[0085]
取不同癌细胞于96孔板(1
×
104个细胞/100μl)中培养,37℃预孵育12h,使其贴壁。 细胞与不同剂量的化合物孵育48h;处理后,每孔加入10μl的mtt溶液(5mg/ml), 37℃继续孵育4h;弃去培养基,每孔加入100μl的dmso,然后通过酶标仪(spectramax190,美国)
通过在波长490nm处读取每个孔的od值来确定衍生物的ic
50
值。
[0086]
isaindigotone衍生物和顺铂阳性对照对四种不同癌细胞48小时的ic
50
值见表2。结果表 明:
①
与其他癌细胞相比,胃癌细胞ags对大多数isaindigotone衍生物表现出更高的敏感性, ic
50
为1.96-44.50μm;尤其是化合物blg04、blg06显示出比isaindigotone本身更高的抑 制活性,其ic
50
分别为1.96μm、2.23μm、2.09μm;化合物blg18显示出与isaindigoton e相似的活性,ic
50
为6.79μm;
②
与isaindigotone相比,blg06在ags细胞中的抗癌活性 提高了近4倍,与顺铂相比,blg06对ags细胞的抗癌活性是顺铂的10倍;
③
与isaindigo tone相比,blg03、blg06、blg11、blg13、blg15、blg18、blg21对于胰腺癌细胞p anc-1也表现出显着的细胞毒性,其中blg06对胰腺癌细胞panc-1的ic
50
为9.94μm,活 性是isaindigotone的5倍;
④
与isaindigotone相比,blg06、blg06、blg18对于结直肠癌 细胞hct116也具有显著的抑制活性,其中blg18对结直肠癌细胞hct116的ic
50
为2.80 μm,其抑制活性为isaindigotone的20倍以上;对于肝癌细胞smmz-7721,大多数isaindigo tone衍生物显示出中等的细胞毒活性。
[0087]
综上所述,本发明所述isaindigotone衍生物对ags、hct116、smmz-7721和panc-1 癌细胞均具有一定的抑制活性。
[0088]
表2 isaindigotone衍生物blg01-22对各种肿瘤细胞的ic
50
(μm)
[0089]
[0090][0091]
实施例3 isaindigotone衍生物blg06对胃癌的抑制活性
[0092]
1.blg06的体外抗增殖活性
[0093]
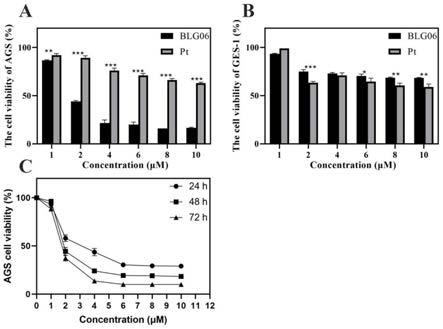
使用mtt法(同实施例1)测定在24h、48h和72h时,blg06对胃癌ags细胞系 和胃表皮细胞ges细胞系的抑制活性。
[0094]
结果如图2所示,与对照组相比,blg06对胃癌ags细胞具有显著的抑制作用,且胃 癌ags细胞活力以剂量和时间依赖性方式受到显着抑制;同时blg06对正常胃表皮细胞g es-1表现出良好的安全性。
[0095]
2.blg06对胃癌ags细胞形态的影响
[0096]
为了进一步确定生长抑制是否由细胞凋亡引起,使用hoechst 33258染色来可视化核形 态。具体方法为:
[0097]
将ags细胞接种在24孔板的腔室载玻片上,并用不同浓度的化合物blg06处理48h。 根据制造商的说明(solarbio life sciences,china),在室温下用4%多聚甲醛固定30min, 然后用pbs洗涤细胞3次,并与100:1稀释的hoechst 33258(10μg/ml)一起孵育在室温 下10min。再次洗涤载玻片并在荧光显微镜(zeiss,德国)下检查。
[0098]
结果如图3所示,荧光显微镜检查显示处理后的ags细胞表现出典型的形态变化,如染 色质凝聚和细胞收缩;该结果表明blg06能够诱导ags细胞凋亡。
[0099]
3.blg06对ags细胞周期的影响
[0100]
为了进一步确定blg06诱导细胞增殖抑制的潜在机制,将ags细胞用不同浓度的blg 06处理24h并用pi染色。用流式细胞术分析细胞周期分布。具体方法为:
[0101]
将ags细胞(7
×
105/孔)接种在6孔板中并用dmso或不同浓度的blg06处理。然后 收获细胞,用冷pbs洗涤,在4℃用70%乙醇固定并再次用pbs洗涤3次。之后,将细胞重 新悬
浮在100rnase a中,并在37℃下孵育30min,以用400μl碘化丙啶染色。最后通 过流式细胞仪(bd lsrfortessa,america)分析dna含量。
[0102]
结果如图4中a和b所示,各期ags细胞比例与对照组相比差异不大。说明,blg06 不能阻滞ags细胞周期。
[0103]
4.blg06对ags细胞凋亡的影响
[0104]
由于blg06引起ags的显着形态变化和高死亡率,进行annexin-v/pi染色以进一步确 定blg06是否可以诱导细胞凋亡。凋亡细胞中磷脂酰丝氨酸的易位使膜联蛋白v-fitc(一 种荧光素活性染料)能够与之结合。pi可以穿透破损的膜并与dna结合。因此,annexin-v /pi染色可以将活细胞与凋亡细胞和坏死细胞区分开来。具体方法为:
[0105]
ags细胞接种在六孔板上,并与化合物blg06(2.0μm、3.0μm、4.0μm和5.0μm) 一起孵育48h;然后将细胞悬浮在100μl稀释的结合缓冲液中,将细胞浓度调整为1
×
106细胞/ml,并加入5μl annexin-v-荧光素;在25℃下将混合物在黑暗中孵育5min后,加 入10μl碘化丙啶和400μl pbs;使用流式细胞仪(bd lsrfortessa,美国)进行测量。
[0106]
结果如图4中c和d所示,经blg06处理后,ags细胞早期凋亡的百分比从0.91%增 加到6.24%,晚期凋亡率从3.24%增加到30.40%,且早期凋亡细胞和晚期凋亡细胞的变异均 呈剂量依赖性。表明blg06能够诱导ags细胞凋亡。
[0107]
5.blg06对线粒体(mmp)膜电位变化的影响
[0108]
进一步研究了blg06对ags细胞中mmp的影响。具体方法为:线粒体膜电位的检测 是使用jc-10试剂盒(solarbio invitrogen corp.,北京,中国)测定。将ags细胞接种在2 4孔板的盖玻片上并孵育24h;将细胞用不同浓度的blg06(2.0μm、3.0μm、4.0μm和 5.0μm)再处理24h,然后用4%多聚甲醛固定;pbs洗涤3次后,jc-10 37℃染色20mi n;用羰基氰化物-3-氯苯腙(cccp,10.0μm)处理的细胞用作阳性对照;结果是通过激光 共聚焦荧光显微镜(zeiss,德国)获得的。
[0109]
结果如图5所示,cccp作为阳性对照,当ags细胞用不同浓度的blg06(2.0μm、3. 0μm、4.0μm和5.0μm)处理时,观察到mmp以剂量依赖性方式明显减少。实验结果表 明blg06诱导的ags细胞凋亡与线粒体介导的通路有关。
[0110]
6.分子对接
[0111]
为了进一步探索分子靶点,进行了分子对接以评估blg06是否是一种有效的pi3k/ak t/mtor抑制剂。对于akt蛋白,天冬氨酸292上的羧基阴离子与配体形成负相互作用。 由于其氨基阳离子,赖氨酸268与配体形成正相互作用。苏氨酸211和苏氨酸291、天冬酰 胺53和天冬酰胺54以及谷氨酰胺79作为极性氨基酸与配体形成强极性相互作用。这些对 接结果提供了对蛋白质-配体相互作用和进一步结构修饰以提高活性的重要依据。为了进一步 研究分子机制,我们通过蛋白质印迹分析检测了blg06对线粒体依赖性通路相关因子bax 和bcl-2以及凋亡效因子caspase-3激活的影响。具体方法为:
[0112]
细胞培养:细胞记数,接种,培养在六孔板中,长至100万个细胞后,取出,裂解,细 胞被收集后,加入8μl细胞裂解液,提取上清总蛋白液。使用bca法检测总蛋白浓度,后 变性蛋白样品,取相同质量的蛋白上样,sds-page胶电泳分离蛋白条带。根据目标蛋白计 算分子量,将相应位置的电泳胶条带切下,湿转法将蛋白条带转到pvdf膜上。
[0113]
配置tbst缓冲液:25mm nacl,100mm tris,0.2%tween-20,ph 7.4,用tbst 缓冲
液溶解的5%脱脂奶粉溶液(w/v)封闭pvdf膜。分别相应用一抗和二抗孵育pvdf膜, tbst缓冲液漂洗适当次数后,使用superecl plus超敏发光试剂盒显色成像。
[0114]
结果如图6所示,blg06处理48h后,bax和cleaved-caspase-3蛋白表达水平显着升高, bcl-2蛋白表达水平逐渐降低。表明blg06通过线粒体相关途径影响ags细胞的凋亡。
[0115]
7.blg06对pi3k/akt/mtor信号通路的影响
[0116]
为了进一步评估blg06是否影响pi3k/akt/mtor信号通路,据报道与细胞凋亡有关, 进行了蛋白质印迹分析以检查相关蛋白质的变化。akt的磷酸化水平是pi3k/akt/mtor信号 通路的重要标志之一,因此选择ags的blg06来测试其在2.00μm浓度下对akt磷酸化(s er 473)的抑制作用,持续48h。具体方法为:为了获得含有总蛋白的细胞裂解物,用rip a裂解液裂解ags细胞;使用bradford测定法定量蛋白质的浓度;将样品施加到10%sds
‑ꢀ
pafe(十二烷基硫酸钠-聚丙烯酰胺凝胶电泳)上,转移到pvde(聚偏二氟乙烯)膜上; 然后将膜浸入含有5%脱脂牛奶的tbst(tris缓冲盐水和吐温)中,轻轻搅拌1h,并在4℃ 下与一抗(gapdh#60004-ig,购自proteintech;akt#yt0185;p-akt#yp0006;mto r#yt2913,购自immunoway;pi3k#yp0176,购自affinity;bcl-2#bs-0032r、bax#bs
‑ꢀ
0127r、caspase-3#bs-0081r,购自bioss);之后,将膜与hrp标记的(辣根过氧化物酶) 二抗在室温下孵育2h,并在照相胶片上检测;最后,用imagej软件分析蛋白质的条带。
[0117]
结果如图6所示,blg06可以显着降低akt的磷酸化。此外,blg06下调ags细胞系 中pi3kcmtor蛋白的表达,这表明blg06能够影响pi3k/akt/mtor信号通路的功能,是 一种潜在的akt蛋白抑制剂。
[0118]
8.blg06抑制ags细胞迁移
[0119]
通过transwell迁移试验评估了blg06抑制ags细胞迁移的能力。具体方法为:为了分 析迁移活性,应用了具有8μm孔膜的transwell装置;将细胞以3
×
104个细胞/100μl的密 度培养并悬浮在无血清rpmi-1640培养基中;将细胞悬浮液接种到含有solarbio matrigel(8 μm孔径;corning)的装置的上室,然后接种600.0μl的20%fbs培养基;培养48h后, 分别用4%多聚甲醛固定细胞,并用0.1%结晶紫染色10min;使用光学显微镜对膜进行拍照。 结果如图7所示,与对照组相比,blg06能够显着减少迁移到腔室底层的细胞数量。表明b lg06可以阻止ags细胞的迁移。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1