2-苯氧乙胺基环己烷基磺酰胺化合物及其制备方法和应用
2
‑
苯氧乙胺基环己烷基磺酰胺化合物及其制备方法和应用
技术领域
1.本发明属于农用化学品领域,具体涉及n
‑
(2
‑
三氟甲基
‑4‑
氯苯基)
‑2‑
苯氧乙胺基环己烷基磺酰胺类化合物的合成和作为杀菌剂的应用。
背景技术:
2.磺酰胺类化合物是人类发现的第一个对细菌有选择作用的药物,其可以被系统地应用于细菌感染而引起的各种疾病治疗。磺胺类化合物在农药上具有杀菌、除草、杀虫等生物活性。而在杀菌剂领域,磺酰胺类的产品并不多见,主要的品种有磺菌胺(flusulfamide)、甲磺菌胺(tolnifanide)、氰霜唑(cyazofamid)等高效低毒的杀菌剂。2
‑
氧代环十二烷基磺酰胺对多种植物病原菌均有较好的抑制活性,以此为先导,对2
‑
氧代环烷基磺酰胺类化合物进行了深入研究,并开发出了候选杀菌剂品种环己磺菌胺(chesulfamide),用于防治番茄灰霉病(botrytis cinerea)及黄瓜叶斑病(corynesporacassiicola)。
[0003][0004]
一些含磺酰基的具有高效杀菌活性的新颖结构也相继被报道。2
‑
苯乙胺基环己烷基磺酰胺类化合物,即实验室自主合成的化合物syaup
‑
cn
‑
26(a)对番茄灰霉病菌具有很高的抑制活性。
[0005]
技术实现要素:
[0006]
本发明在上述研究的基础上,合成得到新的2
‑
苯氧乙胺基环己烷基磺酰胺系列化
合物,经生物活性测定结果表明所合成的化合物具有良好的杀菌活性。
[0007]
为了实现上述目的,本发明一方面提供一种2
‑
苯氧乙胺基环己烷基磺酰胺化合物,具有如下通式(1)所示的结构,
[0008][0009]
其中:r选h、烷基、单卤素、多卤素、苯氧基、三氟甲基、三氟甲氧基、2,2
‑
二甲基
‑
2,3
‑
二氢呋喃中的任意一种。
[0010]
更优选地,r选自以下基团中的任意一种:
[0011]
h、2
‑
f、3
‑
f、4
‑
f、2
‑
cl、3
‑
cl、3
‑
cl、2
‑
br、3
‑
br、4
‑
br、2
‑
ch3、3
‑
ch3、4
‑
ch3、2
‑
cf3、3
‑
cf3、4
‑
cf3、2
‑
och3、3
‑
och3、4
‑
och3、2
‑
t
‑
bu、4
‑
t
‑
bu、2
‑
ch2ch3、4
‑
ocf3、4
‑
oph、2,4
‑
cl2、2,4
‑
f2、3,4
‑
cl2、2,2
‑
二甲基
‑
2,3
‑
二氢呋喃;
[0012]
本发明另一方面提供一种2
‑
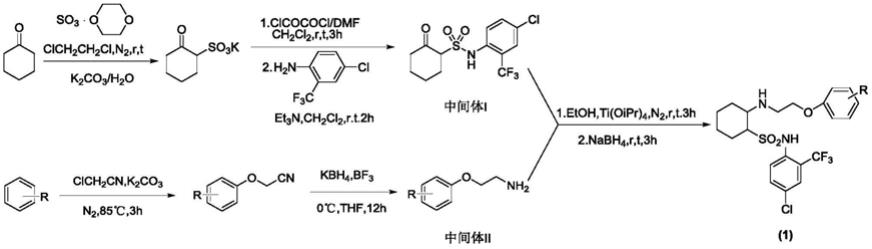
苯氧乙胺基环己烷基磺酰胺化合物的制备方法,合成路线为:
[0013][0014]
具体合成方法为:
[0015]
(1)环己酮、三氧化硫
·
二氧六环加合物、碳酸钾为原料,在室温下,氮气氛围中,制备得到2
‑
氧代环己烷基磺酸钾盐;在室温下2
‑
氧代环己烷基磺酸钾盐、无水二氯甲烷、n,n
‑
二甲基甲酰胺(dmf)、草酰氯反应生成2
‑
氧代环己烷基磺酰氯的二氯甲烷溶液,滴加到2
‑
三氟甲基
‑4‑
氯苯胺中,得到中间体(i)n
‑
(2
‑
三氟甲基
‑4‑
氯苯基)
‑2‑
氧代环己烷基磺酰胺;
[0016]
(2)氮气氛围中,以取代苯酚、碳酸钾、干燥的无水乙腈为原料,搅拌15min,再加入氯乙腈,85℃加热回流,反应3h,制备苯氧乙腈;在冰浴且排尽空气的三口瓶中,加入苯氧乙腈、硼氢化钾、四氢呋喃,搅拌均匀;然后加入三氟化硼乙醚溶液、冰浴搅拌反应12小时,制备中间体(ii)苯氧乙胺;
[0017]
(3)氮气氛围中,向n
‑
(2
‑
三氟甲基
‑4‑
氯苯基)
‑2‑
氧代环己烷基磺酰胺中加入无
水乙醇和钛酸四异丙酯、苯氧乙胺,室温下进行搅拌反应,待原料反应完全后,加入还原剂硼氢化钠继续反应,得到通式(1)所示化合物。
[0018]
本发明提供2
‑
苯氧乙胺基环己烷基磺酰胺化合物的其中一种用途是,用作农业杀菌剂,具体对油菜菌核、番茄灰霉、水稻纹枯、水稻稻瘟、禾谷镰刀、辣椒疫霉等病原真菌、卵菌有抑制作用,用于其病害的防治。
[0019]
本发明提供的2
‑
苯氧乙胺基环己烷基磺酰胺化合物对柑橘溃疡、水稻白叶枯、白菜软腐、西瓜果斑、枯草芽孢杆菌、大肠杆菌、铜绿假单胞菌等病原细菌有抑制作用,用于其病害的防治。
[0020]
本发明提供的2
‑
苯氧乙胺基环己烷基磺酰胺化合物的另一种用途是,用作农业除草剂,具体用于农田单子叶杂草和双子叶杂草的防治,特别是反枝苋、苘麻、稗草、马唐的防治。
[0021]
本发明的有益效果为:
[0022]
本发明提供的2
‑
苯氧乙胺基环己烷基磺酰胺化合物对油菜菌核、番茄灰霉、水稻纹枯、水稻稻瘟、禾谷镰刀、辣椒疫霉等病原菌有抑制作用,用于其病害的防治;对柑橘溃疡、水稻白叶枯、白菜软腐、西瓜果斑、枯草芽孢杆菌、大肠杆菌、铜绿假单胞菌等病原细菌有抑制作用,用于其病害的防治。此外,对反枝苋、苘麻、稗草、马唐等常见单子叶杂草和双子叶杂草亦具有抑制生长的作用。
具体实施方式
[0023]
为了使本领域技术人员更好地理解本发明的技术方案能予以实施,下面结合具体实施例对本发明作进一步说明,但所举实施例不作为对本发明的限定。
[0024]
以下各实施例中所述实验方法,如无特殊说明,均为常规方法;所涉及试剂和材料,如无特殊说明,均可在市场上购买得到。
[0025]
实施例1
[0026]
该通式范围内的化合物中间体i所示的n
‑
(2
‑
三氟甲基
‑4‑
氯苯基)
‑2‑
氧代环己烷基磺酰胺的制备,具体制备工艺流程如下所示:
[0027][0028]
具体制备过程为:连接合成反应实验装置,前期通入氮气以赶走反应瓶中的空气,保持氮气通入,向反应装置中通入氮气约5min后,室温下,将干燥的二氯甲烷200ml、2
‑
氧代环己烷基磺酸钾(0.115mol)、dmf(0.6ml)加入1000ml圆底烧瓶中,搅拌均匀,使原料充分混合均匀后,缓慢滴加草酰氯(0.115mol),在室温下搅拌反应2h;抽滤后滤液缓慢滴加到已用冰水浴降温的由2
‑
三氟甲基
‑4‑
氯苯胺(0.08mol)、三乙胺(0.15mol)以及110ml二氯甲烷组成的反应液中,滴加过程中反应温度控制在0~5℃;滴加完毕后自然升温,反应4h,此时反应液为橙色透明溶液,tlc监测[v(石油醚):v(乙酸乙酯)=1:1]反应进程,结果显示反应液
中无原料时停止反应,进行后处理操作;将反应液先后用75ml的3mol/l盐酸,50ml饱和碳酸氢钠,50ml蒸馏水洗涤;洗过的反应液用无水na2so4干燥3h,抽滤,滤液用旋转蒸发仪蒸干得粗产物,用丙酮+石油醚重结晶得白色固体中间体ⅰ。
[0029]
实施例2
[0030]
该通式范围内的化合物中间体ii的制备过程,具体制备工艺如下:
[0031][0032]
原料取代苯酚以3
‑
溴苯酚为例,化合物记为syaup
‑
zx9。具体制备过程为:氮气保护下,将3
‑
溴苯酚(28.9mmol)、碳酸钾(28.9mmol)、100ml干燥的无水乙腈加入250ml四口烧瓶中,搅拌15分钟,再加入3.35ml的氯乙腈,然后85℃加热回流,反应3小时,tlc监测[v(石油醚):v(乙酸乙酯)=3:1]反应进程,待原料反应完全后,停止反应;将反应液减压浓缩,随后水洗,干燥,抽滤,滤液减压浓缩,得到油状液体为苯氧基乙腈;再向置于冰浴内且排尽空气的带气球的密封的三口瓶中,加入硼氢化钾(72.3mmol),搅拌下加入3
‑
溴苯氧乙腈(28.9mmol),以及100ml四氢呋喃。然后滴加三氟化硼乙醚溶液(43.4mmol),滴加完毕后,继续冰浴1h,撤去冰浴,搅拌反应12h,tlc监测[v(石油醚):v(乙酸乙酯):v(甲醇)=10:10:3]反应进程;待原料反应完全后,停止反应;将液体抽滤去除固体,滤液减压浓缩,溶于40ml甲苯中,用6mol/l盐酸水溶液20ml
×
3萃取,合并盐酸水溶液,用氢氧化钠进行中和,调节其至ph=7,将中和后的水层用乙酸乙酯20ml
×
3萃取三次,并合乙酸乙酯后用无水硫酸钠干燥处理2h,抽滤,减压浓缩,得到中间体
ⅱ‑
9纯品。
[0033]
上述取代苯酚的取代基分别由h、2
‑
f、3
‑
f、4
‑
f、2
‑
cl、3
‑
cl、3
‑
cl、2
‑
br、4
‑
br、2
‑
ch3、3
‑
ch3、4
‑
ch3、2
‑
cf3、3
‑
cf3、4
‑
cf3、2
‑
och3、3
‑
och3、4
‑
och3、2
‑
t
‑
bu、4
‑
t
‑
bu、2
‑
ch2ch3、4
‑
ocf3、4
‑
oph、2,4
‑
cl2、2,4
‑
f2、3,4
‑
cl2、2,2
‑
二甲基
‑
2,3
‑
二氢呋喃取代,合成中间体
ⅱ‑
1~中间体
ⅱ‑
8,中间体
ⅱ‑
10~中间体
ⅱ‑
28。
[0034]
实施例3
[0035]
通式(1)所示的n
‑
(2
‑
三氟甲基
‑4‑
氯苯基)
‑2‑
(2
‑
(苯氧基乙基)氨基)环己烷磺酰胺的制备,其主要原料为实施例2合成的中间体
ⅱ‑
1~中间体
ⅱ‑
28,制成的该化合物编号以syaup
‑
zx1~syaup
‑
zx28记,具体制备工艺流程如下所示:
[0036][0037]
以n
‑
(4
‑
氯
‑2‑
(三氟甲基)苯基)
‑2‑
((2
‑
(3
‑
溴苯氧基)乙基)氨基)环己烷基磺酰胺(syaup
‑
zx9)的合成为例。室温下,将所有仪器均干燥处理,氮气保护条件下,向三颈烧瓶中加入100ml无水乙醇,1g的n
‑
(2
‑
三氟甲基
‑4‑
氯苯基)
‑2‑
环烷基磺酰胺(4.6mmol),2.06ml的钛酸四异丙酯(6.9mmol),搅拌15min,再滴加1g的3
‑
溴
‑
苯氧乙胺(4.6mmol),滴加
完毕后反应3h,之后向体系中加入0.35g硼氢化钠(9.3mmol),有气泡产生,再继续反应3h,tlc(v
石油醚
:v
乙酸乙酯
=1:1)监测反应进度,待反应物反应完毕后,向体系中加入由15ml氨水和15ml水组成的溶液(体积比1:1),搅拌10min,反应停止;将反应液抽滤,保留滤液,旋至近干,加入乙酸乙酯进行萃取,分别收集水相以及乙酸乙酯相,水相再用乙酸乙酯萃取2遍,合并乙酸乙酯相,加入适量无水硫酸钠干燥2h,抽滤,滤液旋干,得初产物;用硅胶色谱柱来进行分离,即得到所需的目标产物。这里r取代基的选择与发明内容对r的定义相同。
[0038]
实施例3制备得到的化合物syaup
‑
zx1~syaup
‑
zx28的理化数据如下表1所示;它们的1h nmr和ms数据如表2所示。
[0039]
表1化合物syaup
‑
zx1~syaup
‑
zx28的理化数据
[0040][0041]
表2化合物syaup
‑
zx1~syaup
‑
zx28的1h nmr和ms数据
[0042]
[0043][0044]
实施例4
[0045]
下面就以本发明提供的化合物为例,对这些化合物的杀菌活性进行具体测试。
[0046]
(一)化合物syaup
‑
zx1~syaup
‑
zx28对植物病原真菌和卵菌活性测定
[0047]
采用菌丝生长速率法测定化合物对多种植物病原菌的杀菌活性,具体方法如下:将样品化合物分别称重后用丙酮溶解,定容制备成浓度为5000mg/l试验用试剂,供活性测定使用;无菌状态下,取0.33ml的浓度为5000mg/l的药剂与33ml融化(60
±
5℃)的pda培养基混合均匀,制成浓度为50mg/l的含毒培养基33ml,然后均匀的将33ml的含毒培养基均匀的倒入3个直径为9cm的培养皿中,每皿11ml;采用啶酰菌胺、腐霉利作为对照药剂,设置丙酮溶剂为空白对照,普筛浓度为50mg/l,待皿中含毒培养基冷凝后,分别接入培养好的直径为0.5cm的病原菌菌块,置于26℃培养箱中培养;待其空白对照中的菌落充分生长后,以十字交叉法测量各处理的菌落直径,取其平均值;以校正后的空白对照和处理的菌落平均直径计算抑制率,采用菌丝生长速率法测定各化合物对核盘菌的抑制活性;经接种培养后,测量菌落直径,按计算式计算抑制率,并计算相应化合物的ec
50
值,每种化合物和对照药剂均设3次重复;经计算,化合物syaup
‑
zx1~syaup
‑
zx28对多种植物病原菌的杀菌活性如下表3所示。
[0048]
由表3可以看出,syaup
‑
zx系列化合物对多种植物病原真菌、卵菌均有一定的杀菌效果,表现出广谱性。但不同化合物对于同一植物病原菌表现出的活性效果差别较大,总体
来看syaup
‑
zx9表现出的杀菌效果较好。syaup
‑
zx9对番茄灰霉病菌的活性与实验室此前自主合成的化合物syaup
‑
cn26相当,但对其他真菌的活性均高于syaup
‑
cn26。对于水稻稻瘟病菌和禾谷镰刀病菌有7个化合物均高于syaup
‑
cn26,对于水稻纹枯病菌均几乎全部高于syaup
‑
cn6。本试验证明了本系列化合物的广谱杀菌活性。
[0049]
表3化合物syaup
‑
zx1~syaup
‑
zx28对多种植物病原菌的杀菌活性
[0050][0051][0052]
(二)化合物syaup
‑
zx1~syaup
‑
zx28对油菜菌核病菌的杀菌活性测定
[0053]
将化合物分别称重后用丙酮溶解,定容制备成浓度为5000mg/l试验用试剂,然后采用成倍稀释的方法,分别配置浓度为5000、1250、312.5、78、19.5mg/l的药液,供活性测定使用;无菌状态下,取0.33ml的浓度为5000mg/l的药剂与33ml融化(60
±
5℃)的pda培养基混合均匀,制成浓度为50mg/l的含毒培养基33ml,然后均匀的将33ml的含毒培养基均匀的倒入3个直径为9cm的培养皿中,每皿11ml;依次类推,配制浓度为50、12.5、3.125、0.78、
0.195mg/l共五个梯度的含毒培养基。
[0054]
采用多菌灵与啶酰菌胺,以及实验室此前自主合成的化合物syaup
‑
cn26为对照药剂,设置丙酮溶剂为空白对照,普筛浓度为50mg/l,梯度浓度为50、12.5、3.13、0.78、0.195mg/l。待皿中含毒培养基冷凝后,分别接入培养好的直径为0.5cm的病原菌菌块。置于28℃培养箱中培养。待其空白对照中的菌落充分生长后,以十字交叉法测量各处理的菌落直径,取其平均值。以校正后的空白对照和处理的菌落平均直径计算抑制率,采用菌丝生长速率法测定各化合物对灰霉病菌的抑制活性。经接种培养后,测量菌落直径,按下式计算抑制率,并计算相应化合物的ec
50
值,每种化合物和对照药剂均设3次重复。
[0055][0056]
采用油菜活体叶片法测定化合物的杀菌活性,具体方法如下:先准确称取20mg化合物,与15mg吐温
‑
20混匀后,用0.1ml的dmso溶解,再将其与7.5mg农乳500和30mg农乳600混合,溶解到0.4ml二甲基亚砜中,最后用二甲基亚砜补足至1ml,配制成含化合物质量分数为2%的乳油,用水稀释成质量浓度为200mg/l的供试药液试液。将多菌灵、啶酰菌胺、syaup
‑
cn26原药分别配制成2%乳油,并以此为对照药剂,以喷洒不含目标化合物的乳油溶液为空白对照;待油菜幼苗长至4片叶时,均匀喷施药液;待药液自然晾干后,在每片叶子中部接种直径为5mm的菌核病菌菌饼,置于智能人工气候箱内,在26
±
1℃、相对湿度90%以上及黑暗:光照=12h:12h条件下培养,待空白对照充分发病后测量病斑直径,以抑制率大小考察防治效果,每处理设5个重复;经计算,化合物syaup
‑
zx1~syaup
‑
zx28的对油菜菌核病菌的杀菌活性结果见表4和表5所示。
[0057]
由表4可以看出,在菌丝生长实验中药剂浓度50mg/l下,所有zx系列化合物对油菜菌核病菌均表现出一定的抑制活性,其中syaup
‑
zx4、syaup
‑
zx8、syaup
‑
zx9、syaup
‑
zx14、syaup
‑
zx15、syaup
‑
zx18、syaup
‑
zx22、syaup
‑
zx24、syaup
‑
zx25、syaup
‑
zx26抑制率都达到80%以上。syaup
‑
zx4以及syaup
‑
zx9的抑制率都高于90%。其中syaup
‑
zx9对油菜菌核病菌丝抑制率最好,达到了96.39%。且显著优于化合物syaup
‑
cn26。本次实验再次证明了此系列化合物的优异杀菌活性。
[0058]
在活体盆栽实验中,在油菜叶上接种油菜菌核病菌2天后,空白对照组出现较明显的发病现象,在油菜叶片上接种菌饼周围出现较大的病斑。而在用syaup
‑
zx系列化合物药液处理的油菜叶片上,一些叶片发病较轻甚至于没有发病,表现出化合物对于油菜菌核病菌较好的防治效果。总体来说,syaup
‑
zx系列化合物对油菜菌核病菌在活体上也表现出了较高的抑制活性。在所有合成的化合物中,有一半化合物对油菜菌核病菌的活体防效达到了70%以上,其中8个化合物syaup
‑
zx4、syaup
‑
zx8、syaup
‑
zx10、syaup
‑
zx11、syaup
‑
zx14、syaup
‑
zx15、syaup
‑
zx25、syaup
‑
zx28对其防治效果超过了80%,超过了对照药剂啶酰菌胺(防治效果80.17%)。化合物syaup
‑
zx9对油菜菌核病的活体防效更是高达95%以上,活性高于多菌灵以及啶酰菌胺。
[0059]
表4化合物syaup
‑
zx1~syaup
‑
zx28对油菜菌核病菌的杀菌活性
[0060][0061][0062]
由表5可以看出,syaup
‑
zx系列化合物的活性表现较好,有27个化合物的ec
50
值低于10.0μg/ml,其中12个化合物的ec
50
值低于对照药剂啶酰菌胺(3.01μg/ml)。化合物syaup
‑
zx9、syaup
‑
zx15、syaup
‑
zx22对油菜菌核病菌的活性表现特别优异,其ec
50
值低于2.0μg/ml,分别为0.94、1.71和1.33μg/ml。特别是化合物syaup
‑
zx9、syaup
‑
zx20、syaup
‑
zx25,其活性要优于对照药剂多菌灵(1.75μg/ml)。且显著优于化合物syaup
‑
cn26。本次实验再次证明了此系列化合物的优异杀菌活性。
[0063]
表5化合物syaup
‑
zx1~syaup
‑
zx28对菌核病菌的毒力
[0064][0065][0066]
(三)化合物syaup
‑
zx1~syaup
‑
zx28对多种病原细菌活性测定
[0067]
通过96孔细胞培养板法(比浊法)测定目标化合物对7种细菌的杀菌活性(见表6)。首先要活化菌株,将在超低温(
‑
80℃)环境下的保存在25%灭菌甘油中细菌,采用划线法在lb平板培养基进行活化,放置在黑暗环境中,温度控制在28℃下培养3d,等待产生单菌落,将其转入100ml的lb液体培养基中,密封后放入振荡摇床,控制温度在28℃,转速为180r/min条件下振荡培养48
‑
72h(不同细菌培养时间不同),使活化的菌种进入稳定生长期,即可进行下一步试验;取10ml进入稳定生长期的细菌菌液加入至100ml的lb液体培养基中,摇晃,使其混合均匀;使用多通道移液器,按照每孔196μl的细菌菌液量加入到96孔板中;再向细胞培养板每孔中加入4μl浓度为5000μg/ml的目标化合物溶液,使药液与孔内已有的带菌lb液体培养基均匀混合,配制成目标化合物在每孔中的浓度为100μg/ml;以磺胺嘧啶、硫酸链霉素为对照药剂、dmso作为溶剂对照、lb液体培养基为空白对照、只含有菌液的培养基为生长对照。每种化合物和对照均设3次重复。用封口膜封严,在28℃、180r/min环境中振荡培
养2d,直至本底对照孔内的菌液进入稳定生长期,即可开始调查;用紫外分光光度计,通过检测细胞培养板每孔中溶液的吸光度来评价化合物的杀菌效果,利用下面的公式计算抑制率:
[0068]
校正od值=含毒培养基od值-本底对照od值
[0069][0070]
由表6可以看出,syaup
‑
zx系列化合物对多种病原细菌均有一定的杀菌效果,总体来说zx25表现出的杀细菌效果较好,也具有较好的广谱性。目标化合物对白叶枯病菌具有优异的杀菌效果,化合物syaup
‑
zx4、syaup
‑
zx25的抑制率分别为88.66%、88.67%,优于对照药剂硫酸链霉素(79.30%)。目标化合物对柑橘溃疡病的活性表现较好,其中syaup
‑
zx2、syaup
‑
zx4、syaup
‑
zx25这三个化合物对柑橘溃疡病菌的抑制率分别为69.32%、73.76%和91.31%,特别是化合物zx25的抑制率为91.31%,高于对照药剂硫酸链霉素(抑制率为83.27%)。目标化合物对枯草芽孢杆菌病菌、白菜软腐病菌的抑制活性表现就一般。但不同化合物对于同一病原菌表现出的活性效果差别较大,总体来看化合物syaup
‑
zx25表现出的杀细菌效果较好。
[0071]
表6化合物syaup
‑
zx1~syaup
‑
zx28对多种病原细菌的杀细菌活性测定
[0072]
[0073][0074]
(四)化合物syaup
‑
zx1~syaup
‑
zx28的除草活性测定
[0075]
参照农药室内生物测定试验准则(农业部农药检定所,2008),将新化合物syaup
‑
zx1~syaup
‑
zx28分别配制成浓度为1000mg/l的丙酮溶液,吸取0.5ml药液加入铺有滤纸的6cm培养皿中,待丙酮挥发干后,加入5ml的0.05%吐温80水溶液,稀释得到100mg/l的水溶液,然后将刚刚萌发的种子整齐地排列在培养皿中,放在23~26℃的环境中培养,以0.05%吐温80水溶液为空白对照,每处理3个重复;3~6天后,分别测量单子叶杂草稗草、马唐(以等浓度乙草胺为对照药剂)和双子叶杂草反枝苋、苘麻(以等浓度莠去津为对照药剂)的芽长及根长,计算除草活性,公式如下:
[0076]
抑制率(%)=(空白对照长度
‑
处理长度)/空白对照长度
×
100
[0077]
经计算,化合物syaup
‑
zx1~syaup
‑
zx28的除草活性如下表7所示。
[0078]
表7化合物syaup
‑
zx1~syaup
‑
zx28除草活性
[0079]
[0080][0081]
注:“/”代表未进行此项试验
[0082]
由表7可以看出,syaup
‑
zx系列化合物对双子叶杂草(苘麻、反枝苋)的生长抑制率要明显优于对单子叶杂草(马唐、稗草)的抑制率。syaup
‑
zx系列化合物对双子叶杂草防效明显,多个化合物的生长抑制率高于80%,个别化合物达到95%以上,有进一步研究的价值。
[0083]
以上所述实施例仅是为充分说明本发明而所举的较佳的实施例,其保护范围不限于此。本技术领域的技术人员在本发明基础上所作的等同替代或变换,均在本发明的保护范围之内,本发明的保护范围以权利要求书为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1