一种含异恶唑啉的苯基吡啶类化合物及其用途的制作方法
1.本发明属农用除草剂领域,涉及一种取代苯基异恶唑啉化合物及其用途。
背景技术:
2.对于取代的联芳香基苯磺酰胺类化合物,报道的专利很多,例如wo9842700、 wo2001070736、wo2006065646、wo20081224614、wo2009148052、wo2009103440、 fr2727413、fr2749584、jp61050975等,主要应用于医药的研究。
3.us5783522提到了2-苯基吡啶化合物具有一定的除草活性,wo2004056785 中公开了苯并恶唑类化合物具有一定的除草活性。然而这些已知化合物对于杂草 的防除效果并不总是完全令人满意。本发明通式所示的化合物与现有技术是有显 著区别的,且均具有很好的除草活性。
技术实现要素:
4.本发明的目的在于提供一种结构新颖的除草化合物,这些化合物与现有技术 所提供的除草化合物相比,具有优异的除草活性,可用于有目的的防治有害植物。
5.为实现上述目的,本发明采用的技术方案为:
6.本发明提供一种取代苯基异恶唑啉化合物或其盐,如通式(i)所示:
[0007][0008]
式中:
[0009]
r1、r2、r3、r4、r5分别选自氢、卤素、cn、no2、c1-c4烷基、c1-c4卤代烷 基、c1-c4烷氧基或c1-c4卤代烷氧基;
[0010]
r5、r6、r7、r8分别选自氢、卤素或c1-c4烷基;
[0011]
r9、r
10
分别选自氢或c1-c4烷基;
[0012]r11
选自氢、c1-c4烷基或c-c4卤代烷基;
[0013]r12
选自co2r
13
、conhr
14
或ch2or
15
;
[0014]r13
、r
14
分别选自氢、c1-c4烷基、c1-c4卤代烷基、烯丙基、炔丙基、c1-c4 烷氧基c1-c3烷基、c1-c4烷羰基氧基c1-c4烷基、苄基、呋喃甲基或四氢呋喃 甲基;
[0015]r15
选自c1-c4烷基羰基、c1-c4卤代烷基羰基、c3-c6环烷基羰基、c1-c4 烷基碳酰基或c1-c4卤代烷基磺酰基。
[0016]
或其钠盐、钾盐或铜盐。
[0017]
本发明较为优选的化合物为,通式(i)中
[0018]
r1、r2、r3、r4、r5分别选自氢、卤素、c1-c4烷基或c1-c4卤代烷基;
[0019]
r5、r7分别选自氢、氯、氟或甲基;
[0020]
r6、r8分别选自氢;
[0021]
r9、r
10
分别选自氢或甲基;
[0022]r11
选自氢、甲基、乙基、三氟甲基或二氟甲基;
[0023]r12
选自co2r
13
、conhr
14
或ch2or
15
;
[0024]r13
、r
14
分别选自氢、甲基、乙基、正丙基、正丁基、异丙基、异丁基、叔丁 基、三氟乙基、烯丙基、炔丙基、甲氧基乙基、乙氧基乙基、甲基羰基氧基乙基 或四氢呋喃甲基;
[0025]r15
选自c1-c4烷基羰基、c3-c6环烷基羰基或c1-c4烷基磺酰基。
[0026]
或其钠盐或钾盐。
[0027]
本发明进一步优选的化合物为,通式(i)中
[0028]
r1、r2、r3、r4、r5分别选自氢、卤素、c1-c4烷基或c1-c4卤代烷基;
[0029]
r5、r7分别选自氢、氯或氟;
[0030]
r6、r8分别选自氢;
[0031]
r9、r
10
分别选自氢或甲基;
[0032]r11
选自氢、甲基或乙基;
[0033]r12
选自co2r
13
、conhr
14
或ch2or
15
;
[0034]r13
、r
14
分别选自甲基、乙基、正丙基、正丁基、异丙基、异丁基、叔丁基、 三氟乙基、烯丙基、炔丙基、甲氧基乙基、乙氧基乙基、甲基羰基氧基乙基或四 氢呋喃甲基;
[0035]r15
选自c1-c4烷基羰基、c3-c6环烷基羰基或c1-c4烷基磺酰基。
[0036]
或其钠盐或钾盐。
[0037]
本发明最为优选的化合物为,通式(i)中
[0038]
r1、r2、r3、r4、r5分别选自氢、氯、氟、甲基或三氟甲基;
[0039]
r5、r7分别选自氢、氯或氟;
[0040]
r6、r8分别选自氢;
[0041]
r9、r
10
分别选自氢;
[0042]r11
选自氢、甲基或乙基;
[0043]r12
选自co2r
13
、conhr
14
或ch2or
15
;
[0044]r13
、r
14
分别选自甲基、乙基、正丙基、正丁基、异丙基、异丁基、叔丁基、 三氟乙基、烯丙基、炔丙基、甲氧基乙基、乙氧基乙基、甲基羰基氧基乙基或四 氢呋喃甲基;
[0045]r15
选自c1-c4烷基羰基、环丙甲酰基或c1-c4烷基磺酰基。
[0046]
或其钠盐。
[0047]
上面给出的通式(i)化合物的定义中,汇集所用术语一般代表如下取代基:
[0048]
卤:指氟、氯、溴或碘。烷基:指直链或支链烷基。卤代烷基:直链或支链 烷基,在这些烷基上的氢原子部分或全部被卤原子所取代。烷氧基:直链或支链 烷基,经氧原子键连接到结构上。卤代烷氧基:直链或支链烷氧基上的氢原子部 分或全部被卤原子所取代。链烯基:直链或支链并可在任何位置上至少存在一个 碳碳双键。卤代链烯基:直链或支链链烯基上的氢原子部分或全部被卤原子所取 代。链炔基:直链或支链并可在任何位置上至少存在一个碳碳三键。卤代链炔基: 直链或支链链炔基上的氢原子部分或全部被卤原子所取代。环烷基:含三个或以 上碳原子的环状烷烃,例如环丙基、环丁基、环戊基等。烷基羰基:
烷基经羰基 连接到结构上,如ch3co-,ch3ch2co-。卤代烷基羰基:烷基羰基的烷基上的氢原 子可部分或全部被卤原子所取代,如cf3co-。烷氧基羰基:烷氧基经羰基连接到 结构上。如ch3oco-,ch3ch2oco-。卤代烷氧基羰基:烷氧基羰基的烷基上的氢原 子可部分或全部被卤原子所取代。如clch2ch2oco-。烷基磺酰基:直链或支链烷 基经磺酰基(-so
2-)连接到结构上,如甲基磺酰基。卤代烷基亚磺酰基:直链或 支链烷基亚磺酰基,其烷基上的氢原子可部分或全部被卤原子所取代。卤代烷基 磺酰基:直链或支链烷基磺酰基,其烷基上的氢原子可部分或全部被卤原子所取 代。烷基氨基:直链或支链烷基,经氮原子键连接到结构上。烷基酰基氨基:如 ch3conh-,ch3ch2conh-。烷基磺酰基氨基:如ch3so2nh-,ch3ch
2 so2nh-。
[0049]
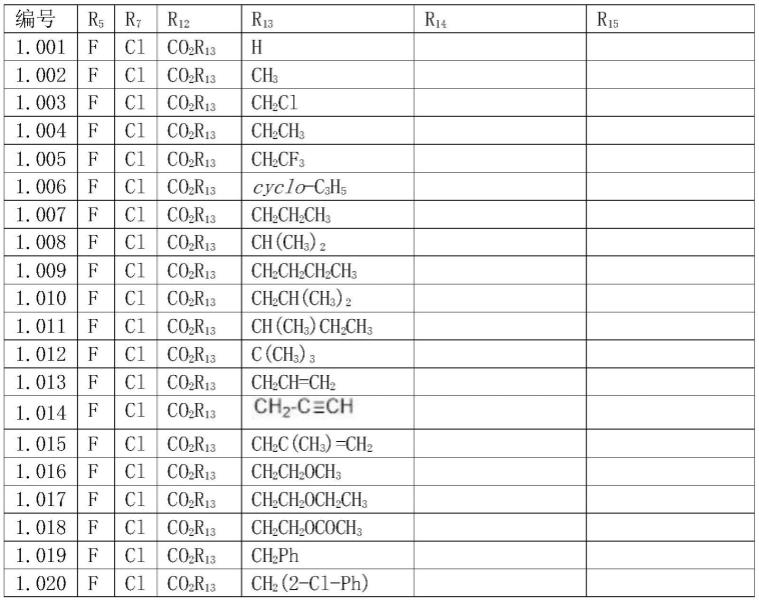
本发明中的部分化合物可以用下表中列出的具体化合物来说明,但本发明并 不仅限于这些化合物。当化合物r1=h、r2=h、r3=cf3、r4=h、r6=h、r8=h、r9=h、r
10
=h、 r
11
=ch3其他基团如表1所示,化合物编号为1.001-1.148。
[0050][0051]
表1
[0052]
[0053]
[0054]
[0055][0056]
通式(i)所示化合物,当表中的化合物r1=cf3、r2=h、r3=h、r4=h、r6=h、r8=h、 r9=h、r
10
=h、r
11
=ch3,r5、r7、r
12
、r
13
、r
14
、r
15
基团依次对应表1中的1.001-1.148,代 表化合物的编号为2.001-2.148。
[0057]
通式(i)所示化合物,当表中的化合物r1=h、r2=cf3、r3=h、r4=h、r6=h、r8=h、 r9=h、r
10
=h、r
11
=ch3,r5、r7、r
12
、r
13
、r
14
、r
15
基团依次对应表1中的1.001-1.148,代 表化
物的编号为15.001-15.148。
[0071]
通式(i)所示化合物,当表中的化合物r1=h、r2=h、r3=cf3、r4=h、r6=h、r8=h、 r9=h、r
10
=h、r
11
=h,r5、r7、r
12
、r
13
、r
14
、r
15
基团依次对应表1中的1.001-1.148,代表 化合物的编号为16.001-16.148。
[0072]
通式(i)所示化合物,当表中的化合物r1=h、r2=h、r3=cf3、r4=h、r6=h、r8=h、 r9=h、r
10
=h、r
11
=cf3,r5、r7、r
12
、r
13
、r
14
、r
15
基团依次对应表1中的1.001-1.148,代 表化合物的编号为17.001-17.148。
[0073]
通式(i)所示化合物,当表中的化合物r1=h、r2=h、r3=cf3、r4=h、r6=h、r8=h、 r9=h、r
10
=h、r
11
=ch2ch3,r5、r7、r
12
、r
13
、r
14
、r
15
基团依次对应表1中的1.001-1.148, 代表化合物的编号为18.001-18.148。
[0074]
本发明通式(i)化合物可用如下方法制备(除另有说明的外,各基团的定义 同前),但本发明并不仅限于这些制备方法。
[0075]
首先在过渡金属催化剂存在下、于惰性溶剂中卤代芳香化合物(vi)和芳香硼 酸或酯(v)反应得到(iv):
[0076][0077]
式中:hal是氯、溴或碘,r9和r
10
独立地为氢或c
1-c4烷基。过渡金属催化 剂可选用钯催化剂例如四(三苯基膦)-钯(0)等。溶剂可选自甲苯、1,2-二氯乙烷 或二氧六环等惰性溶剂。反应温度为80-120度。
[0078]
通式(vi所示的卤代芳香化合物有市售。
[0079]
通式(v)所示的芳香硼酸或酯化合物部分有市售,也可以由已知方法制得, 例如参见us5783522。
[0080]
化合物iv通过氧化还原反应,在氯铬酸吡啶等条件存在下得到化合物iii, 化合物iii可使用j.agric.food chem.2005,53,8639-8643或wo200609234 所述方法得到目标物i。
[0081]
以上制备方法可以获得通式(i)化合物的异构体混合物,如需得到纯异构体, 可采用常规方法如结晶或色谱法进行分离。
[0082]
本发明的通式(i)化合物可以有效控制稗草、狗尾草、异型莎草、水莎草、 马唐、苘麻、百日草、反枝苋、马齿苋、苍耳、决明等杂草,对小麦、水稻、玉 米、大豆和棉花的作物具有一定的安全性,在农业上可用作除草剂。因此本发明 的技术方案还包括通式(i)化合物或其盐作为除草剂的用途。
[0083]
本发明还提供了一种除草组合物,该组合物中含有通式(i)的化合物或其盐 作为活性组分以及农业上可接受的载体,组合物中通式(i)的化合物的重量百分 含量为0.1-99%。因此本发明的技术方案还包括该组合物作为除草剂的用途。
[0084]
本发明的组合物可以按照常规方法制备:将通式(i)的化合物与载体混合。 这种组合物中的活性组分可以含本发明的单一化合物或几种化合物的混合物。
[0085]
本发明组合物中的载体系满足下述条件的物质:它与活性成分配制后便于施 用于待处理的位点,例如可以是植物、种子或土壤;或者有利于贮存、运输或操 作。载体可以是固体或液体,包括通常为气体但已压缩成液体的物质,通常在配 制除草组合物中所用的载体均可使用。
[0086]
合适的固体载体包括天然和合成的粘土和硅酸盐,例如硅藻土、滑石、硅镁 土、硅酸铝(高岭土)、蒙脱石和云母;碳酸钙;硫酸钙;硫酸铵;合成的氧化硅 和合成硅酸钙或硅酸铝;元素如碳和硫;天然的和合成的树脂如苯并呋喃树脂, 聚氯乙烯和苯乙烯聚合物和共聚物;固体多氯苯酚;沥青;蜡如蜂蜡,石蜡。
[0087]
合适的液体载体包括水;醇如异丙醇和乙醇;酮如丙酮、甲基乙基酮、甲基 异丙基酮、环已基酮;醚;芳烃如苯、甲苯、二甲苯;石油馏分如煤油和矿物油; 氯代烃如四氯化碳、全氯乙烯和三氯乙烯。通常,这些液体的混合物也是合适的。
[0088]
除草组合物通常加工成浓缩物形式并以此用于运输,在施用之前由使用者将 其稀释。少量的表面活性剂载体的存在有助于稀释过程。这样,按照本发明的组 合物中至少有一种载体优选是表面活性剂。例如组合物可含有至少两种载体,其 中至少一种是表面活性剂。
[0089]
表面活性剂可以是乳化剂、分散剂或润湿剂;它可以是非离子的或离子的表 面活性剂。合适的表面活性剂的例子包括聚丙烯酸和木质素磺酸的钠盐或钙盐; 分子中含至少12个碳原子的脂肪酸或脂肪胺或酰胺与环氧乙烷和/或环氧丙烷的 缩合物。甘醇、山梨醇、蔗糖或季戊四醇脂肪酸酯及这些酯与环氧乙烷和/或环 氧丙烷的缩合物;脂肪醇或烷基苯酚如对辛基苯酚或对辛基甲苯酚与环氧乙烷 和/或环氧丙烷的缩合物;这些缩合产物的硫酸盐和磺酸盐;在分子中至少含有 10个碳原子的硫酸或磺酸酯的碱金属或碱土金属盐,优选钠盐,例如硫酸月桂酸 酯钠,硫酸仲烷基酯钠,磺化蓖麻油钠盐,磺酸烷基芳基酯钠,如十二烷基苯磺 酸钠盐。
[0090]
本发明的组合物的实例是gb/t 19378-2017所述的固体制剂及液体制剂,例 如粉剂、可湿性粉剂、水分散粒剂、乳油、水乳剂、悬浮剂、油悬浮剂等。可湿 性粉剂通常含25%,50%或75%重量活性成分,且通常除固体惰性载体之外,还含 有3-10%重量的分散剂,且若需要可加入0-10%重量的稳定剂和/或其它添加剂如 渗透剂或粘着剂。粉剂通常可成型为具有与可湿性粉剂相似的组成但没有分散剂 的粉剂浓缩剂,再进一步用固体载体稀释,
得到通常含0.5-10%重量活性组分的 组合物。粒剂通常制备成具有10至100目(1.676-0.152mm)大小,且可用成团或 注入技术制备。通常粒剂含0.5-75%重量的活性成分和0-10%重量添加剂如稳定 剂、表面活性剂、缓释改良剂。所谓的“可流动干粉”由具有相对高浓度活性成 分的相对小的颗粒组成。可乳化浓缩剂除溶剂外,当需要时通常含有共溶剂, 1-50%w/v活性成分,2-20%w/v乳化剂和0-20%w/v其他添加剂如稳定剂、渗透剂 和腐蚀抑制剂。悬浮剂通常含有10-75%重量的活性成分、0.5-15%重量的分散剂、0.1-10%重量的其它添加剂如消泡剂、腐蚀抑制剂、稳定剂、渗透剂和粘着剂。
[0091]
水分散剂和乳剂,例如通过用水稀释按照本发明的可湿性粉剂或浓缩物得到 的组合物,也列入本发明范围。所说的乳剂可具有油包水或水包油两个类型。
[0092]
通过在组合物中加入其他的一种或多种除草剂,使其能比单独的通式(i)化 合物具有更广谱的活性。此外,其他除草剂可对通式(i)化合物的除草活性具有 增效作用。
具体实施方式
[0093]
以下结合实例对本发明的具体实施方式做进一步说明,应当指出的是,此处 所描述的具体实施方式只是为了说明和解释本发明,并不局限于本发明。(除另 有注明外,所用原料均为市售)
[0094]
制备实施例
[0095]
实施例1化合物1.004的制备
[0096][0097]
(1)中间体1.004-a的制备
[0098]
将2,3-二氯-5-三氟甲基吡啶,钯碳、碳酸钾、三苯基磷、dmf加入三口瓶 中,升温至80度,滴加4-氯-2-氟-5-甲基苯硼酸的dmf溶液,tlc点板检测。 待原料不再转化,趁热过滤体系,除去催化剂,向体系加入水有产品析出,对固 体洗涤并用乙醇重结晶,即得中间体1.004-a。
[0099]
(2)中间体1.004-b的制备
[0100]
将中间体1.004a、pcc等物质量的加入乙腈中回流3小时,tlc监测反应。 反应结束
后,通过过滤除去pcc,柱层析后,可得目标产物,浅色固体。
[0101]
(3)中间体1.004-c的制备
[0102]
将中间体1.004-b溶于乙醇中,降温至0度,搅拌下滴加盐酸羟胺水溶液, 升至室温反应2h,tlc检测,反应完全后将体系倒入水中得到固体,过滤得到白 色固体。
[0103]
(4)目标物1.004的制备
[0104]
将中间体1.004-c溶于二氯甲烷中,降温至0-5度,加入甲代丙烯酸甲酯和 三乙胺保持0-5度反应1小时。依次用盐酸、饱和食盐水洗涤、无水硫酸钠干燥。 减压蒸馏,粗产品硅胶柱纯化,减压蒸馏得到目标物。1h nmr(300mhz,tms, cdcl3)δppm 1.30(t,3h),1.71(s,3h),3.34(d,1h),3.89(d,1h),4.27(q, 2h),7.36(d,1h),7.38(s,1h),7.82(d,1h),8.41(s,1h),8.86(s,1h).元 素分析结果:c,52.99;h:3.52;n,6.48(理论值c,52.98;h,3.51;n,6.50)。
[0105]
实施例2化合物1.001的制备
[0106]
将化合物1.004溶于乙醇溶液中,加入过量的氢氧化钠水溶液,室温搅拌4 小时。tlc监测反应完毕,倒入水中,用盐酸调节ph到3,过滤,干燥得固体, 乙醚洗涤数次,得产物。1h nmr(300mhz,tms,cdcl3)δppm 1.71(s,3h), 3.34(d,1h),3.89(d,1h),7.36(d,1h),7.38(s,1h),7.82(d,1h),8.86(s, 1h),9.18(s,1h).元素分析结果:c,50.72;h:2.75;n,6.94(理论值c,50.70; h,2.75;n,6.96)。
[0107]
实施例3化合物1.002的制备
[0108][0109]
(1)中间体1.001-a的制备
[0110]
将化合物1.001溶于二氯甲烷中,滴加入3倍量的草酰氯,室温搅拌4小时, tlc监测反应完毕,减压除溶剂,得到油状物1.001-a,未经提纯直接用于下一 步。
[0111]
(2)目标物1.002的制备
[0112]
将1.001-a溶于二氯甲烷中,小心加入1.5倍量的无水乙醇和3倍量的三乙 胺的混和物,保持在室温搅拌反应1小时,tlc监测反应完毕。减压节除溶剂, 柱层析分离得到浅色固体,即为目标产物。1h nmr(300mhz,tms,cdcl3)δppm 1.71(s,3h),3.39(d,1h),3.60(s,1h),3.90(d,1h),7.36(d,1h),7.38(s, 1h),7.82(d,1h),8.41(s,1h),8.86(s,1h).元素分析结果:c,54.12;h: 4.10;n,9.47(理论值c,54.12;h,4.09;n,9.47)。
[0113]
通过此方法,还可以制备化合物1.003-1.026,表征数据见后表。
[0114]
实施例4化合物1.034的制备
[0115][0116]
将中间体1.001-a溶于二氯甲烷中,小心加入1.5倍量的异丙胺和3倍量的 三乙胺的混和物,保持在室温搅拌反应1小时,tlc监测反应完毕。减压节除溶 剂,柱层析分离得到浅色固体,即为目标产物。1h nmr(300mhz,tms,cdcl3) δppm 1.18(m,6h),1.71(s,3h),3.39(d,1h),3.90(d,1h),4.05(m,1h), 7.36(d,1h),7.38(s,1h),7.82(d,1h),8.41(s,1h),
8.86(s,1h).元素 分析结果:c,54.12;h:4.10;n,9.47(理论值c,54.12;h,4.09;n,9.47)。
[0117]
通过此方法,还可以制备化合物1.027-1.052,表征数据见后表。
[0118]
实施例5化合物1.053的制备
[0119][0120]
将中间体1.004-c溶于dmf中,升温到30摄氏度,在该温度下分批加入1.5 倍量的ncs,形成浅黄色溶液,保持在该温度下反应1小时。降至室温后,加入 二氯甲烷,随后用1n盐酸洗2次,饱和食盐水洗2次,无水硫酸镁干燥,抽滤, 将二氯甲烷溶液降温到0度,滴加1.5倍量的甲代烯丙基醇和3倍量的三乙胺的 混和溶液,保持在该温度下反应1小时。依次用1n盐酸,食盐水洗,有机相用 无水硫酸镁干燥,浓缩后柱层析分离得到黄色固体。1h nmr(300mhz,tms,cdcl3) δppm 1.69(s,3h),3.39(d,1h),3.62(s,2h),3.90(d,1h),4.01(s,1h), 7.36(d,1h),7.38(s,1h),7.82(d,1h),8.41(s,1h),8.86(s,1h).元素 分析结果:c,52.52;h:3.39;n,7.21(理论值c,52.52;h,3.37;n,7.21)。
[0121]
实施例6化合物1.056的制备
[0122]
将化合物1.053溶于二氯甲烷中,小心加入1.5倍量的丙酰氯和3倍量的三 乙胺的混和物,保持在室温搅拌反应1小时,tlc监测反应完毕。减压节除溶剂, 柱层析分离得到浅色固体,即为目标产物。1h nmr(300mhz,tms,cdcl3)δppm 1.21(q,3h),1.69(s,3h),2.65(m,2h),3.39(d,1h),3.60(s,2h),3.90(d, 1h),7.36(d,1h),7.38(s,1h),7.82(d,1h),8.41(s,1h),8.86(s,1h).元 素分析结果:c,52.98;h:3.50;n,6.51(理论值c,52.98;h,3.51;n,6.50)。
[0123]
通过此方法,还可以制备化合物1.054-1.074,表征数据见后表。
[0124]
其它化合物可参照上述方法进行制备,部分化合物的表征数据见表19。
[0125]
表19:
[0126]
[0127]
[0128][0129]
制剂实施例
[0130]
(配方中活性组分折百后计量加入,所示百分数均为重量百分含量)
[0131]
实施例7:60%可湿性粉剂
[0132]
化合物1.004(含量97.2%)60%,十二烷基萘磺酸钠2%,木质素磺酸钠9%, 高岭土补足至100%;
[0133]
将化合物1.004、十二烷基萘磺酸钠、木质素磺酸钠及高岭土(均为固体) 混合在一起,在粉碎机中粉碎,直到颗粒达到标准。
[0134]
实施例8:35%乳油
[0135]
化合物14.004(含量98.4%)35%,亚磷酸10%,乙氧基化甘油三酸酯15%, 环已酮补足至100%;
[0136]
亚磷酸溶解在环已酮中,然后加入化合物14.004和乙氧基化甘油三酸酯,得 到透明的溶液。
[0137]
实施例9:30%悬浮液
[0138]
化合物14.067(含量96.4%)30%,十二烷基萘磺酸钠4%,半纤维素2%, 环氧丙烷8%,水补足至100%;
[0139]
将化合物14.067与应加水量的80%的水及十二烷基萘磺酸钠在球磨机中(1mm 珠)中一起粉碎。半纤维素和环氧丙烷溶解在其余20%的水中,然后搅拌加入上 述组分。
[0140]
实施例10:25%水乳剂
[0141]
化合物1.132(含量96.2%)25%,十二烷基醇聚乙二醇磷酸酯4%,乙氧基甘 油三酸酯2%,十二烷基苯磺酸钙1.5%,环氧甲乙烷环氧丙烷共聚物2.5%,环 己酮30%,烷基芳基馏分补足至100%;
[0142]
将化合物1.132溶解在80%的应加入溶剂量中(环己酮和烷基芳基馏分),然 后加入乳化剂(十二烷基醇聚乙二醇磷酸酯、乙氧基甘油三酸酯及十二烷基苯磺 酸钙)和分散剂(2.5份环氧甲乙烷环氧丙烷共聚物),将混合物彻底搅拌。混合 物在球磨机(1mm珠)中粉
碎,然后再加入其余20%的溶剂。
[0143]
生物活性测试实施例
[0144]
实施例11室内除草活性测定
[0145]
将定量的杂草种子分别播于直径为7cm的装有营养土的纸杯中,播后覆土 1cm,镇压、淋水后在温室培养,苗前处理于播种后24小时进行;苗后处理需出 苗后间苗、定植(禾本科杂草10-20株/杯,阔叶杂草2-4株/杯),待禾 本科杂草2-3叶期,阔叶杂草长至2真叶期,按试验设计剂量用作物喷雾机进 行茎叶喷雾处理(喷雾压力1.95kg/cm2,喷液量50ml/m2,履带速度1.48km/h)。 试验设3次重复。待药液自然风干后,置于温室内按常规方法管理,定期观察试 材的生长发育情况,并根据实际情况,于处理后定期目测调查供试药剂对杂草的 防除效果。
[0146]
防除效果分级标准:0为无效,100%为将杂草完全杀死或严重抑制。
[0147]
部分苗后测试结果如下(所有质量浓度均以有效成分计):在1000g a.i./hm2剂量下,化合物1.001、1.002、1.003、1.004、1.005、1.006、1.007、1.008、 1.013、1.014、1.019、1.022、1.025、1.026、1.030、1.034、1.053、1.056、 1.068、1.078、1.082、1.087、1.106、1.108、1.112、1.131、1.142、1.144、 2.004、3.022、4.056、5.004、6.004、7.004、8.099、10.004、10.032、11.012、 12.004、13.004、14.004、14.005、14.030、14.034、14.056、14.067、15.011、 16.120、17.004等,苗前、苗后处理对苘麻、狗尾草、稗草、百日草等均具有较 高的除草好活性,防效大于80%。
[0148]
在200g a.i./hm2剂量下,化合物1.001、1.002、1.003、1.004、1.005、 1.006、1.007、1.008、1.013、1.014、1.019、1.022、1.025、1.026、1.030、 1.034、1.053、1.056、1.087、1.106、1.108、1.142、1.144、2.004、5.004、 6.004、7.004、8.099、10.004、10.032、11.012、12.004、13.004、14.004、 14.005、14.030、14.034、14.056、14.067、15.011、16.120、17.004等,苗前、 苗后处理对苘麻、狗尾草、稗草、百日草等均具有较高的除草好活性,防效大于 70%。
[0149]
实施例12杀草谱试验
[0150]
本发明化合物14.004进行了杀草谱试验,同时与商品化品种苯嘧磺草胺、 41%草甘膦异丙胺盐进行了对照,结果见下表,测定方法同前所述。
[0151][0152][0153]
实施例13:田间防治杂草试验
[0154]
在广西南宁柑橘试验基地进行,试验时田间杂草处于2-4叶期。手动式喷雾 器,喷液量45公斤/亩。处理15天后,目测调查对阔叶杂草、禾本科杂草的防 效及总防效。
[0155]
田间试验药效计算方法如下:
[0156][0157]
结果如下:
[0158]
化合物剂量g(a.i./ha)阔叶杂草防效禾本科杂草防效总防效14.004300908586嘧磺草胺wg100458565
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1