一种3,5-二硝基苯甲酸的制备方法
一种3,5
‑
二硝基苯甲酸的制备方法
技术领域
1.本发明涉及化学合成技术领域。具体而言,涉及一种3,5
‑
二硝基苯甲酸的制备新方法。
技术背景
2.3,5
‑
二硝基苯甲酸是重要的有机合成中间体,在医药工业上可合成磺胺柯衣酸、泛影酸、替米沙坦等,在染料工业上可用于合成染料中间体3,5
‑
二氨基苯甲酸,在液晶工业上可用于合成液晶中间体3,5
‑
二氨基苯甲酸
‑4‑
联苯酯等,属于新兴的高附加值的精细化工产品(tetrahedron letters 2014,55,6878
‑
6881;染料与染色2012,49,38
‑
39;journal of molecular structure 2019,1198,126894)。目前3,5
‑
二硝基苯甲酸合成工艺主要有两种(应用化工,2013,42(6),1105
‑
1106;fluid phase equilib,2004,226,9
‑
13;cs255644;cn111253261a;天然气化工—c1化学与化工,2021,46,76
‑
80):(1)以苯甲酸为原料,浓硫酸和硝酸为硝化剂经硝化反应生成3,5
‑
二硝基苯甲酸;(2)以间硝基苯甲酸为原料,浓硫酸和硝酸为硝化剂,经硝化反应生成3,5
‑
二硝基苯甲酸。上述两种工艺都采用混酸进行硝化,为了达到理想的反应效果,通常在较高反应温度下,在脱水值较高的混酸下同时加大硝化剂配比进行硝化反应。尽管混酸的硝化能力强,反应速度快,必须指出,硝化是一强放热反应,硝酸又是强氧化剂,通过提高温度来加速反应,易导致多硝化和氧化副反应发生。目前的反应工艺都存在反应时间长、物料易积蓄、过程控制不稳定及反应釜持液量大等问题,且硝化合成3,5
‑
二硝基苯甲酸是强放热反应,反应温度不易控制,易产生“飞温”现象,导致氧化副反应多,收率不高等问题;而且上述工艺过程中混酸用量都比较大,增加了三废处理的负荷和原料成本,大量废酸不能良好的进行回收,易污染环境。因此,关于3,5
‑
二硝基苯甲酸的制备方法尚存在一定的不足,研究开发绿色、高效的3,5
‑
二硝基苯甲酸的制备方法具有十分重要的意义。
技术实现要素:
3.针对现有技术的不足,本发明的目的是提供一种3,5
‑
二硝基苯甲酸的制备新方法,通过金属改性介孔材料负载型胍盐离子液体催化间二硝基苯与二氧化碳发生羧基化反应来制备目标物。该方法操作简单、高效、反应收率和选择性好,不产生大量废酸,环境友好。
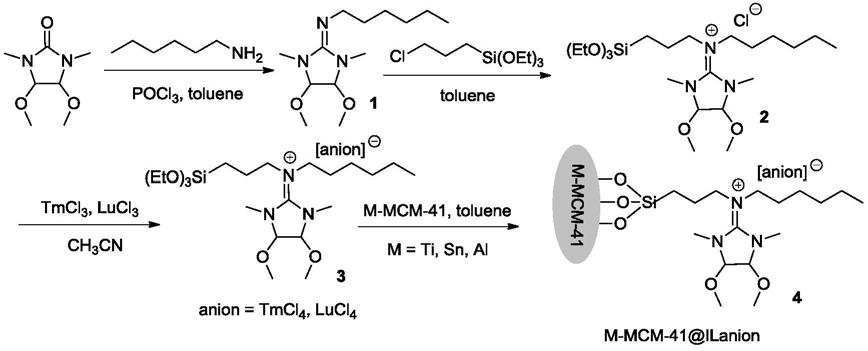
4.本发明所用的金属改性介孔材料负载型胍盐离子液体的化学反应原理和结构如下:
[0005][0006]
通式中离子液体阴离子anion可以是tmcl4,lucl4负离子。通式m
‑
mcm
‑
41@ilanion的催化剂的反应过程包括以下步骤:
[0007]
(1)4,5
‑
二甲氧基
‑
1,3
‑
二甲基咪唑烷
‑2‑
酮和三氯氧磷在甲苯溶剂中50
‑
65℃反应22
‑
26小时,加入正己胺继续反应16
‑
20小时,后加入质量分数20%naoh水溶液调ph至中性,用二氯甲烷萃取混合液,回收溶剂、干燥得中间体1;
[0008]
(2)中间体1与3
‑
氯丙基三乙氧基硅烷在甲苯溶剂中90
‑
110℃反应22
‑
24小时,回收溶剂、干燥得中间体2;
[0009]
(3)中间体2在乙腈溶剂中与含氯金属盐在60
‑
70℃反应20
‑
25小时,乙腈洗涤,干燥,得离子液体3;
[0010]
(4)离子液体3继续在甲苯溶剂中与金属改性介孔材料在90
‑
110℃反应20
‑
30小时后过滤,干燥,得金属改性介孔材料负载型胍盐离子液体催化剂。所述的催化剂具体优选包括ti
‑
mcm
‑
41@iltmcl4、sn
‑
mcm
‑
41@iltmcl4、al
‑
mcm
‑
41@iltmcl4、ti
‑
mcm
‑
41@illucl4、sn
‑
mcm
‑
41@illucl4、al
‑
mcm
‑
41@illucl4中的任意一种。
[0011]
步骤(1)、(2)、(3)、(4)中的溶剂包括甲苯和乙腈,反应过程中,所添加的溶剂均过量。
[0012]
步骤(1)中所述的4,5
‑
二甲氧基
‑
1,3
‑
二甲基咪唑烷
‑2‑
酮、三氯氧磷、正己胺的摩尔比为1:1
‑
1.5:1
‑
3,优选为1:1.2:2。
[0013]
步骤(2)中,中间体1与3
‑
氯丙基三乙氧基硅烷的摩尔比为1:1
‑
1.5,优选为1:1。
[0014]
步骤(3)中,所述的含氯金属盐为氯化铥或氯化镥;中间体2与含氯金属盐的摩尔比为1:1
‑
3,优选摩尔比为1:1
‑
1.5。
[0015]
步骤(4)中,所述的金属改性介孔材料为ti
‑
mcm
‑
41、sn
‑
mcm
‑
41、al
‑
mcm
‑
41;中间体3与金属改性介孔材料的质量比为0.4
‑
1.5:1,优选质量比为0.6
‑
1.2:1。
[0016]
本发明特征在于以间二硝基苯为原料,dmf为溶剂,经加入金属改性介孔材料负载型离子液体催化剂后,通入二氧化碳,在80~130℃温度下,提升二氧化碳压力并保持在指定压力,搅拌反应4~20小时即可制备得到3,5
‑
二硝基苯甲酸。
[0017]
本发明所用金属改性介孔材料负载型胍盐离子液体用量为间二硝基苯物料质量的5~50%,优选15~40%。
[0018]
本发明所述反应温度为80~130℃,优选100~120℃。
[0019]
本发明所述反应时间为4~20小时,优选8~14小时。
[0020]
本发明所述二氧化碳压力控制在0.5~5mpa,优选1.5~3.5mpa。
[0021]
本发明所述催化剂为金属改性介孔材料负载型胍盐离子液体ti
‑
mcm
‑
41@iltmcl4、sn
‑
mcm
‑
41@iltmcl4、al
‑
mcm
‑
41@iltmcl4、ti
‑
mcm
‑
41@illucl4、sn
‑
mcm
‑
41@illucl4、al
‑
mcm
‑
41@illucl4中的任意一种,优选ti
‑
mcm
‑
41@iltmcl4和sn
‑
mcm
‑
41@illucl4。
[0022]
本发明所述一种3,5
‑
二硝基苯甲酸的制备新方法,反应结束,将物料冷却,过量co2缓慢释放,催化剂在釜底,将含有产品3,5
‑
二硝基苯甲酸的上层液体过滤分离出。滤液蒸馏,粗产品经乙醇重结晶,干燥即可得到目标产物,回收的固体催化剂可不经处理即可进行重复使用,按比例投料进行下一批催化反应。
[0023]
本发明的催化反应原理如下:
[0024][0025]
依据本发明提供的制备3,5
‑
二硝基苯甲酸的方法,其关键技术是采用制备的金属改性介孔材料负载型胍盐离子液体催化间二硝基苯与二氧化碳发生羧基化反应得到3,5
‑
二硝基苯甲酸。
[0026]
本发明与现有催化反应技术相比,其优点为:(1)金属改性介孔材料负载型胍盐离子液体催化活性高,稳定性好,可方便的回收循环使用。(2)发明工艺原子经济性高达100%、反应过程绿色、反应效率高,无废酸产生。(3)整个反应体系为非均相催化,产物相和催化剂相易分离,反应过程简单,反应体系环境友好。
附图说明
[0027]
图1是实施例中制备得到的催化剂ti
‑
mcm
‑
41@iltmcl4和sn
‑
mcm
‑
41@illucl4的sem图。
[0028]
图2是实施例2中得到产品的液相色谱图。
具体实施方式
[0029]
下面通过实施例对本发明的内容作进一步的详细说明,但并不因此而限制本发明。
[0030]
实施例1
[0031]
实施方式的金属改性介孔材料负载型胍盐离子液体催化剂的制备方法,包括以下步骤:
[0032]
(1)4,5
‑
二甲氧基
‑
1,3
‑
二甲基咪唑烷
‑2‑
酮(0.25mol)和三氯氧磷(0.3mol)在甲苯(100ml)溶剂中60℃反应24小时,然后加入正己胺(0.5mol)后继续反应18小时,后加入质量分数20%naoh水溶液调ph至中性,用二氯甲烷(200ml)萃取混合液,回收溶剂、干燥得中间体1;
[0033]
(2)接着中间体1(0.15mol)与3
‑
氯丙基三乙氧基硅烷(0.15mol)在甲苯(120ml)中100℃反应24小时,回收溶剂、干燥得中间体2;
[0034]
(3)中间体2(0.1mol)在乙腈(150ml)溶剂中与氯化铥(0.1mol)或氯化镥(0.1mol)在65℃反应24小时,乙腈洗涤,干燥,得离子液体3;
[0035]
(4)离子液体3(8g)与金属改性介孔材料(10g)在甲苯(150ml)中110℃反应24小时,过滤,干燥得负载型离子液体催化剂4。依次为:ti
‑
mcm
‑
41@iltmcl4、sn
‑
mcm
‑
41@iltmcl4、al
‑
mcm
‑
41@iltmcl4、ti
‑
mcm
‑
41@illucl4、sn
‑
mcm
‑
41@illucl4、al
‑
mcm
‑
41@illucl4。
[0036][0037]
实施例2
[0038]
在不锈钢高压反应釜中加入间二硝基苯(10mmol),ti
‑
mcm
‑
41@iltmcl4(0.35g),dmf(20ml),然后将反应釜密封,通入二氧化碳以排除反应釜内的空气。保持二氧化碳压力在2.5mpa,110℃搅拌反应10小时。反应结束,将物料冷却,过量co2缓慢释放,催化剂在釜底,将含有产品的上层液体过滤分离出。滤液产物相回收溶剂,粗产物用乙醇进行重结晶,干燥即得到3,5
‑
二硝基苯甲酸,收率65%,含量96.4%(hplc见图2)。
[0039]
实施例3
[0040]
在不锈钢高压反应釜中加入间二硝基苯(10mmol),sn
‑
mcm
‑
41@iltmcl4(0.4g),dmf(20ml),然后将反应釜密封,通入二氧化碳以排除反应釜内的空气。保持二氧化碳压力在3.0mpa,120℃搅拌反应12小时。反应结束,将物料冷却,过量co2缓慢释放,催化剂在釜底,将含有产品的上层液体过滤分离出。滤液产物相回收溶剂,粗产物用乙醇进行重结晶,干燥即得到3,5
‑
二硝基苯甲酸,收率49%,hplc分析同实施例2,仅含量93.7%。
[0041]
实施例4
[0042]
在不锈钢高压反应釜中加入间二硝基苯(10mmol),al
‑
mcm
‑
41@iltmcl4(0.6g),dmf(20ml),然后将反应釜密封,通入二氧化碳以排除反应釜内的空气。保持二氧化碳压力在3.5mpa,120℃搅拌反应14小时。反应结束,将物料冷却,过量co2缓慢释放,催化剂在釜底,将含有产品的上层液体过滤分离出。滤液产物相回收溶剂,粗产物用乙醇进行重结晶,干燥即得到3,5
‑
二硝基苯甲酸,收率28%,hplc分析同实施例2,含量90.6%。
[0043]
实施例5
[0044]
在不锈钢高压反应釜中加入间二硝基苯(10mmol),ti
‑
mcm
‑
41@illucl4(0.5g),dmf(20ml),然后将反应釜密封,通入二氧化碳以排除反应釜内的空气。保持二氧化碳压力在3.0mpa,120℃搅拌反应14小时。反应结束,将物料冷却,过量co2缓慢释放,催化剂在釜底,将含有产品的上层液体过滤分离出。滤液产物相回收溶剂,粗产物用乙醇进行重结晶,
干燥即得到3,5
‑
二硝基苯甲酸,收率52%,hplc分析同实施例2,含量93.2%。
[0045]
实施例6
[0046]
在不锈钢高压反应釜中加入间二硝基苯(10mmol),sn
‑
mcm
‑
41@illucl4(0.45g),dmf(20ml),然后将反应釜密封,通入二氧化碳以排除反应釜内的空气。保持二氧化碳压力在3.0mpa,110℃搅拌反应12小时。反应结束,将物料冷却,过量co2缓慢释放,催化剂在釜底,将含有产品的上层液体过滤分离出。滤液产物相回收溶剂,粗产物用乙醇进行重结晶,干燥即得到3,5
‑
二硝基苯甲酸,收率60%,hplc分析同实施例2,含量94.8%。
[0047]
实施例7
[0048]
在不锈钢高压反应釜中加入间二硝基苯(10mmol),al
‑
mcm
‑
41@illucl4(0.65g),dmf(20ml),然后将反应釜密封,通入二氧化碳以排除反应釜内的空气。保持二氧化碳压力在3.5mpa,120℃搅拌反应14小时。反应结束,将物料冷却,过量co2缓慢释放,催化剂在釜底,将含有产品的上层液体过滤分离出。滤液产物相回收溶剂,粗产物用乙醇进行重结晶,干燥即得到3,5
‑
二硝基苯甲酸,收率31%,hplc分析同实施例2,含量92.0%。
[0049]
实施例8
[0050]
将实施例1中的催化剂回收,按实施例1中的各条件进行催化烷基化反应,重复使用回收催化剂4次,实验结果显示催化剂活性不减,目标产物收率58~64%,含量在94%以上。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1