异喹啉生物碱及其制备方法和应用与流程
1.本发明涉及医药技术领域,具体公开了异喹啉生物碱及其制备方法和应用。
背景技术:
2.据2020版《中国药典》记载:青风藤(sinomenii caulis)为防己科防己属植物青藤sinomenium acutum(thunb.)rehd.et wils.和毛青藤 sinomenium acutum(thunb.)rehd.et wils.var.cinereum rehd.et wils. 的干燥藤茎。青风藤性平,味苦、辛。归肝、脾经。具有祛风湿,通经络,利小便的功能。用于风湿痹痛,关节肿胀,麻痹瘙痒。现代药理学研究发现,青风藤具有镇痛、镇静、镇咳,抗炎,降压,免疫抑制,抗心律失常,抗心肌缺血、保护再灌注损伤,阻断神经节及神经肌肉传递,释放组胺,降低心肌的收缩性,抑制肾上腺素诱发的自律性;对胃肠道有兴奋作用,但也有轻度的胃肠不良反应等作用。青风藤化学成分研究发现其主含青藤碱、华青藤碱、尖防己碱、光千金藤碱、n
‑
去甲尖防己碱、双青藤碱等多种生物碱及消旋丁香树脂酚、乙酰齐墩果酸等成分。目前国内外学者对青风藤中异喹啉类生物碱抗肿瘤研究较少。
3.恶性肿瘤目前为威胁全人类健康的全球重大问题,据世界卫生组织统计,恶性肿瘤的总发病率在世界范围内呈逐年上升趋势。少数恶性肿瘤经积极防治已得到基本控制,如在欧美发达地区的宫颈癌发病率的上升趋势已有所遏制,然而,乳腺癌的发病率自上世纪70年代末持续上升。最新一期的中国癌症统计数据显示我国乳腺癌发病率在肿瘤登记地区已位居女性恶性肿瘤的第 1位。尽管近年有关乳腺癌的研究已取得不少成果,其诊治策略和方法也获得显著的进展,但仍有大约三分之一的乳腺癌患者死于转移性乳腺癌或其治疗的并发症。因此,寻找和开发一种针对乳腺癌的新的高效低毒治疗药物是我国抗肿瘤新药研发中亟待解决的重要问题。
技术实现要素:
4.针对上述问题,本发明主要为了解决现有异喹啉类生物碱化合物的一些缺失,以及弥补部分异喹啉类生物碱化合物的应用空白;同时针对青风藤提取异喹啉类生物碱化合物做进一步研究。
5.为了解决上述问题,本发明采用如下技术方案:
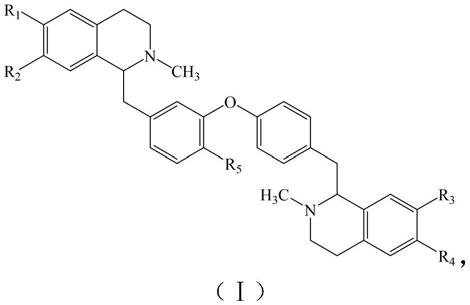
6.异喹啉类生物碱化合物,具有如下式ⅰ结构通式:
[0007][0008]
其中,r1、r2、r3、r4分别为下述之一
[0009]
‑
oh,
[0010]
‑
o(ch2)nr’,n为自然数,r’为卤代基或
‑
ch3;
[0011]
r5为
‑
h或
‑
oh。
[0012]
一些方式中,所述r’为
‑
ch3;0≤n≤10,优选的0≤n≤5。
[0013]
异喹啉类生物碱化合物的制备方法,包括下述步骤:
[0014]
提取:取干燥的青风藤原药材、粉碎、溶媒提取、合并提取液、用旋转蒸发仪减压除去溶媒、得青风藤提取物;
[0015]
萃取:用不同极性的溶媒对青风藤提取物进行萃取、合并萃取液、用旋转蒸发仪减压除去溶媒、得不同极性的萃取物;
[0016]
纯化:用柱色谱法对不同极性的萃取物进行分离纯化。
[0017]
一些方式中,提取步骤和萃取步骤中的溶媒分别至少包括水、无水乙醇、含水体积比为5~70%的乙醇、无水甲醇、含水体积比为5~70%的甲醇、环己烷、石油醚、乙酸乙酯、丙酮、含水体积比为5~70%的丙酮、正丁醇以及二氧化碳超临界流体中之一。
[0018]
一些方式中,提取步骤中的提取方法至少为渗漉法、浸渍法、煎煮法、回流提取法、连续回流提取法以及超临界流体提取法中任一。
[0019]
一些方式中,纯化步骤中的柱色谱法至少包括大孔树脂柱色谱法、硅胶柱色谱法、葡聚糖凝胶柱色谱法、反相柱色谱法、高效液相色谱法中之一;
[0020]
优选的,
[0021]
大孔树脂柱色谱法为:洗脱液为甲醇和水的混合液,洗脱方法为二者比例5:5~10:0依次梯度洗脱;
[0022]
硅胶柱色谱法为:硅胶粒度为100~200目,洗脱液为丙酮和乙酸乙酯的混合液,洗脱方法为二者比例5:1~1:1依次梯度洗脱;
[0023]
葡聚糖凝胶柱色谱法:洗脱液为三氯甲烷和甲醇的混合液,洗脱方法为二者比例2:1~1:2依次梯度洗脱;
[0024]
反相柱色谱法:洗脱液为甲醇和水的混合液,洗脱方法为二者比例7:3~ 10:0依次梯度洗脱;
[0025]
高效液相色谱法:洗脱液为甲醇或乙腈与水、磷酸及和三乙胺或二乙胺的混合液,洗脱方法为四组分的比例(4~6):(0~6):(0~0.01):(0.05~1),依次梯度洗脱。其中,四组分中,甲醇或乙腈择一,三乙胺或二乙胺择一;一些情况中,二乙胺与甲醇不同时使用。
[0026]
一些方式中,高效液相色谱法步骤为下述任一:
[0027]
a.高效液相色谱的洗脱液为甲醇、水、磷酸和三乙胺的混合液,洗脱方法为四者的比例4:6:0.01:0.01~9:1:0.01:0.01,依次梯度洗脱,
[0028]
b.高效液相色谱的洗脱液为乙腈、水和二乙胺的混合液,洗脱方法为三者的比例6:4:0.005~10:0:0.005,依次梯度洗脱,
[0029]
c.高效液相色谱的洗脱液为乙腈、水和三乙胺的混合液,洗脱方法为三者的比例5:5:0.01~9:1:0.01,依次梯度洗脱,
[0030]
d.高效液相色谱的洗脱液为乙腈、水、磷酸和三乙胺的混合液,洗脱方法为四者的比例5:5:0.01:0.01~10:0:0.01:0.01,依次梯度洗脱。
[0031]
异喹啉类生物碱化合物在制备抗肿瘤制剂中的应用。
[0032]
一些方式中,所述异喹啉类生物碱化合物为下述任一
[0033]
异喹啉类生物碱化合物为1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
[[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)
‑
甲苯氧基]苄基]
‑ꢀ
异喹啉,优选的,该化合物主要是在制备防治肺癌或乳腺癌药物中应用,
[0034]
1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑7‑
甲氧基
‑2‑
甲基
‑6‑
异喹啉,优选的,该化合物主要是在制备防治乳腺癌或肺癌药物中应用,
[0035]
1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑6‑
甲氧基
‑2‑
甲基
‑7‑
异喹啉,优选的,该化合物主要是在制备防治肝癌或乳腺癌药物中应用,
[0036]4‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]
‑2‑
[4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]苯氧基] 苯酚,优选的,该化合物主要是在制备防治肝癌或乳腺癌药物中应用。
[0037]
抑制肿瘤细胞增殖的药物,含有前述异喹啉类生物碱化合物;优选的,所述异喹啉类生物碱化合物至少为下述中之一
[0038]
异喹啉类生物碱化合物为1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
ꢀ‑1‑
[[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)
‑
甲苯氧基]苄基]
‑ꢀ
异喹啉,
[0039]
1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑7‑
甲氧基
‑2‑
甲基
‑6‑
异喹啉,
[0040]
1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑6‑
甲氧基
‑2‑
甲基
‑7‑
异喹啉,
[0041]4‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]
‑2‑
[4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]苯氧基] 苯酚。
[0042]
抗肿瘤的药物,含有前述异喹啉类生物碱化合物;
[0043]
优选的,
[0044]
所述异喹啉类生物碱化合物为异喹啉类生物碱化合物为1,2,3,4
‑
四氢
ꢀ‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
[[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)
‑
甲苯氧基]苄基]
‑
异喹啉,所述肿瘤为肺癌或乳腺癌;
[0045]
所述异喹啉类生物碱化合物为1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
ꢀ‑3‑
[4
‑
[(1,2,3,4
‑
四
氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基] 苯基]甲基]
‑7‑
甲氧基
‑2‑
甲基
‑6‑
异喹啉,所述肿瘤为乳腺癌或肺癌;
[0046]
所述异喹啉类生物碱化合物为1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
ꢀ‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基] 苯基]甲基]
‑6‑
甲氧基
‑2‑
甲基
‑7‑
异喹啉,所述肿瘤为肝癌或乳腺癌;
[0047]
所述异喹啉类生物碱化合物为4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
ꢀ‑1‑
异喹啉基]甲基]
‑2‑
[4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]苯氧基]苯酚,所述肿瘤为肝癌或乳腺癌。
[0048]
本发明的有益效果是:
[0049]
提供了新的异喹啉类生物碱化合物,同时开拓了其在肿瘤治疗中的应用,给出了一些新的肿瘤治疗方式,尤其针对其中部分癌症提供新的抑制药物;还进一步提供了通过青风藤来提取异喹啉类生物碱化合物的方法。
附图说明
[0050]
图1为实施例1中化合物核磁氢谱图、高效液相色谱图;
[0051]
图2为实施例2中化合物核磁氢谱图、高效液相色谱图;
[0052]
图3为实施例3中化合物核磁氢谱图、高效液相色谱图;
[0053]
图4为实施例4中化合物核磁氢谱图、高效液相色谱图;
[0054]
图5为异喹啉生物碱化合物的一种结构通式。
具体实施方式
[0055]
下面对本发明做进一步说明:
[0056]
异喹啉类生物碱化合物,具有如下结构通式:
[0057][0058]
其中,r1、r2、r3、r4分别为下述之一
[0059]
‑
oh,
[0060]
‑
o(ch2)nr’,n为自然数,r’为卤代基或
‑
ch3;
[0061]
r5为
‑
h或
‑
oh。
[0062]
一些方式中,所述r’为
‑
ch3,0≤n≤10,优选的0≤n≤5,且当r’为卤代基时,1≤n。
[0063]
异喹啉类生物碱化合物的制备方法,包括下述步骤:
[0064]
提取:取干燥的青风藤原药材、粉碎、溶媒提取、合并提取液、用旋转蒸发仪减压除去溶媒、得青风藤提取物;
[0065]
萃取:用不同极性的溶媒对青风藤提取物进行萃取、合并萃取液、用旋转蒸发仪减压除去溶媒、得不同极性的萃取物;
[0066]
纯化:用柱色谱法对不同极性的萃取物进行分离纯化。
[0067]
一些方式中,提取步骤和萃取步骤中的溶媒分别至少包括水、无水乙醇、含水体积比为5~70%的乙醇、无水甲醇、含水体积比为5~70%的甲醇、环己烷、石油醚、乙酸乙酯、丙酮、含水体积比为5~70%的丙酮、正丁醇以及二氧化碳超临界流体中之一。
[0068]
一些方式中,提取步骤中的提取方法至少为渗漉法、浸渍法、煎煮法、回流提取法、连续回流提取法以及超临界流体提取法中任一。
[0069]
一些方式中,纯化步骤中的柱色谱法至少包括大孔树脂柱色谱法、硅胶柱色谱法、葡聚糖凝胶柱色谱法、反相柱色谱法、高效液相色谱法中之一;
[0070]
优选的,
[0071]
大孔树脂柱色谱法为:洗脱液为甲醇和水的混合液,洗脱方法为二者比例5:5~10:0依次梯度洗脱;
[0072]
硅胶柱色谱法为:硅胶粒度为100~200目,洗脱液为丙酮和乙酸乙酯的混合液,洗脱方法为二者比例5:1~1:1依次梯度洗脱;
[0073]
葡聚糖凝胶柱色谱法:洗脱液为三氯甲烷和甲醇的混合液,洗脱方法为二者比例2:1~1:2依次梯度洗脱;
[0074]
反相柱色谱法:洗脱液为甲醇和水的混合液,洗脱方法为二者比例7:3~ 10:0依次梯度洗脱;
[0075]
高效液相色谱法:洗脱液为甲醇或乙腈与水、磷酸及和三乙胺或二乙胺的混合液,洗脱方法为四组分的比例(4~6):(0~6):(0~0.01):(0.05~1),依次梯度洗脱。其中,组分甲醇或乙腈、组分水、组分磷酸、组分三乙胺或二乙胺四组分中,甲醇或乙腈择一,三乙胺或二乙胺择一;一些情况中,二乙胺与甲醇不同时使用。
[0076]
一些方式中,高效液相色谱法步骤为下述任一:
[0077]
a.当提取的异喹啉类生物碱化合物主要为1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
ꢀ‑2‑
甲基
‑1‑
[[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)
‑
甲苯氧基]苄基]
‑
异喹啉时:高效液相色谱的洗脱液为甲醇、水、磷酸和三乙胺的混合液,洗脱方法为四者的比例4:6:0.01:0.01~9:1:0.01:0.01,依次梯度洗脱,梯度间隔不做特别限定,以能提取更高纯度异喹啉类生物碱为准;
[0078]
b.当提取的异喹啉类生物碱化合物主要为1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基] 苯基]甲基]
‑7‑
甲氧基
‑2‑
甲基
‑6‑
异喹啉时:高效液相色谱的洗脱液为乙腈、水和二乙胺的混合液,洗脱方法为三者的比例6:4:0.005~10:0:0.005,依次梯度洗脱,梯度间隔不做特别限定,以能提取更高纯度异喹啉类生物碱为准;
[0079]
c.当提取的异喹啉类生物碱化合物主要为1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
ꢀ‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基] 苯基]甲基]
‑6‑
甲氧基
‑2‑
甲基
‑7‑
异喹啉时:高效液相色谱的洗脱液为乙腈、水和三乙胺的混合液,洗脱方法为三者的比例5:5:0.01~9:1:0.01依次梯度洗脱,梯度间隔不做特别限定,以能提取更高纯度异喹啉类生物碱为准;
[0080]
d.当提取的异喹啉类生物碱化合物主要为4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]
‑2‑
[4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]苯氧基]苯酚时:高效液相色谱的洗脱液为乙腈、水、磷酸和三乙胺的混合液,洗脱方法为四者的比例5:5:0.01:0.01~ 10:0:0.01:0.01,依次梯度洗脱,梯度间隔不做特别限定,以能提取更高纯度异喹啉类生物碱为准。
[0081]
异喹啉类生物碱化合物在制备抗肿瘤制剂中的应用。
[0082]
一些方式中,所述异喹啉类生物碱化合物为下述任一
[0083]
异喹啉类生物碱化合物为1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
ꢀ‑1‑
[[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)
‑
甲苯氧基]苄基]
‑ꢀ
异喹啉,优选的,所述肿瘤为肺癌或乳腺癌,
[0084]
1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑7‑
甲氧基
‑2‑
甲基
‑6‑
异喹啉,优选的,所述肿瘤为乳腺癌或肺癌,
[0085]
1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑6‑
甲氧基
‑2‑
甲基
‑7‑
异喹啉,优选的,所述肿瘤为肝癌或乳腺癌,
[0086]4‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]
‑2‑
[4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]苯氧基] 苯酚,优选的,所述肿瘤为肝癌或乳腺癌。
[0087]
抑制肿瘤细胞增殖的药物,含有前述异喹啉类生物碱化合物;优选的,所述异喹啉类生物碱化合物至少为下述中之一
[0088]
异喹啉类生物碱化合物为1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
ꢀ‑1‑
[[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)
‑
甲苯氧基]苄基]
‑ꢀ
异喹啉,
[0089]
1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑7‑
甲氧基
‑2‑
甲基
‑6‑
异喹啉,
[0090]
1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑6‑
甲氧基
‑2‑
甲基
‑7‑
异喹啉,
[0091]4‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]
‑2‑
[4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]苯氧基] 苯酚。
[0092]
前文中所述“至少为下述之一”表示为下述一种或多种。
[0093]
抗肿瘤的药物,含有前述异喹啉类生物碱化合物;
[0094]
在一些如下具体情况中:
[0095]
所述异喹啉类生物碱化合物为异喹啉类生物碱化合物为1,2,3,4
‑
四氢
ꢀ‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
[[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)
‑
甲苯氧基]苄基]
‑
异喹啉,所述肿瘤为肺癌或乳腺癌;即,为治疗肺癌或乳腺癌的药物中含有该化合物。
[0096]
所述异喹啉类生物碱化合物为1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
ꢀ‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基] 苯基]甲基]
‑7‑
甲氧基
‑2‑
甲基
‑6‑
异喹啉,所述肿瘤为乳腺癌或肺癌;即,为治疗乳腺癌或肺癌的药物中含有该化合物。
[0097]
所述异喹啉类生物碱化合物为1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
ꢀ‑3‑
[4
‑
[(1,2,3,4
‑
四
氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基] 苯基]甲基]
‑6‑
甲氧基
‑2‑
甲基
‑7‑
异喹啉,所述肿瘤为肝癌或乳腺癌;即,为治疗肝癌或乳腺癌的药物中含有该化合物。
[0098]
所述异喹啉类生物碱化合物为4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
ꢀ‑1‑
异喹啉基]甲基]
‑2‑
[4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]苯氧基]苯酚,所述肿瘤为肝癌;即,为治疗肝癌或乳腺癌的药物中含有该化合物。
[0099]
实施例1
[0100]
本实施例提供化合物1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
[[(1,2,3,4
‑
四氢
ꢀ‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)
‑
甲苯氧基]苄基]
‑
异喹啉的制备方法及其抗肿瘤活性的测定方法和结果。
[0101]
其化学结构式为:
[0102][0103]
其提取分离纯化步骤为:
[0104]
s1、提取:青风藤粉碎后,用含水体积比10%的乙醇浸泡,热回流提取3 次,每次2小时,过滤,收集滤液并在减压条件下浓缩,得到浓缩液;
[0105]
s2、萃取:将上述浓缩液加0.5~1.5倍体积的水溶解后,用等体积的石油醚、乙酸乙酯、正丁醇依次萃取,收集不同极性萃取液并在减压条件下浓缩,得到浓缩液;
[0106]
s3、纯化:将s2所得乙酸乙酯萃取物依次通过大孔树脂柱色谱、硅胶柱色谱、葡聚糖凝胶柱色谱、反相柱色谱等进行反复纯化。
[0107]
所述s3中大孔柱色谱中,洗脱液为甲醇和水的混合液,洗脱方法为二者比例5:5~10:0依次梯度洗脱;
[0108]
所述s3中硅胶柱色谱中硅胶粒度为100~200目,洗脱液为丙酮和乙酸乙酯的混合液,洗脱方法为二者比例5:1~1:1依次梯度洗脱;
[0109]
所述s3中葡聚糖凝胶柱色谱的洗脱液为三氯甲烷和甲醇的混合液,洗脱方法为二者比例2:1~1:2依次梯度洗脱;
[0110]
所述s3中反相柱色谱的洗脱液为甲醇和水的混合液,洗脱方法为二者比例7:3~10:0依次梯度洗脱;
[0111]
所述s3中高效液相色谱的洗脱液为甲醇、水、磷酸和三乙胺的混合液,洗脱方法为四者的比例4:6:0.01:0.01~9:1:0.01:0.01,依次梯度洗脱。
[0112]
一具体方式为:
[0113]
溶样溶剂:80%甲醇水;
[0114]
洗脱方法:75%甲醇+25%水+0.1%磷酸+0.1%三乙胺,洗脱时长:20min, 75%甲醇+25%水逐步提升甲醇比例变为100%甲醇,洗脱时长:40min;
[0115]
流速:1.0ml/min;
[0116]
色谱柱:chromcore 120 c18,5μm,4.6*250mm;
[0117]
柱温:40℃。
[0118]
制得1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
[[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑ꢀ
甲基
‑1‑
异喹啉基)
‑
甲苯氧基]苄基]
‑
异喹啉,产品检测参考图1。在前述配比方案范围内均可制得目标产物。
[0119]
体外抗肿瘤活性实验方法:肿瘤细胞培养于含10%小牛血清、青霉素和链霉素培养液中,置37℃,5%co2培养箱中培养。取对数生长期细胞进行增殖抑制实验。用mtt法检测提取物对5种肿瘤细胞(人乳腺癌细胞 mda
‑
mb
‑
231、人宫颈癌细胞hela、人肝癌细胞hepg2、人前列腺癌细胞 pc
‑
3、人肺癌细胞a549)的增殖抑制作用,细胞活力数据见表1
‑
1。
[0120]
表1
‑
1:化合物1
‑
细胞活力(%)数据表
[0121][0122]
以提取物的浓度对肿瘤细胞生长抑制率作图,可得到量效曲线,计算抑制率。体外抗肿瘤活性实验结果:见表1
‑
2。
[0123]
表1
‑
2:1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
[[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
ꢀ‑2‑
甲基
‑1‑
异喹啉基)
‑
甲苯氧基]苄基]
‑
异喹啉对5种肿瘤细胞的抑制率
[0124][0125]
实施例2
[0126]
本实施例提供化合物1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑7‑
甲氧基
‑2‑
甲基
‑6‑
异喹啉的制备方法及其抗肿瘤活性的测定方法和结果。
[0127]
其化学结构式为:
[0128][0129]
其提取分离纯化步骤为:
[0130]
s1、提取:青风藤粉碎后,用含水体积比10%的乙醇浸泡,热回流提取3 次,每次2小时,过滤,收集滤液并在减压条件下浓缩,得到浓缩液;
[0131]
s2、萃取:将上述浓缩液加0.5~1.5倍体积的水溶解后,用等体积的石油醚、乙酸乙酯、正丁醇依次萃取,收集不同极性萃取液并在减压条件下浓缩,得到浓缩液;
[0132]
s3、纯化:将s2所得乙酸乙酯萃取物依次通过大孔树脂柱色谱、硅胶柱色谱、葡聚糖凝胶柱色谱、反相柱色谱等进行反复纯化。
[0133]
所述s3中大孔柱色谱中,洗脱液为甲醇和水的混合液,洗脱方法为二者比例5:5~10:0依次梯度洗脱;
[0134]
所述s3中硅胶柱色谱中硅胶粒度为100~200目,洗脱液为丙酮和乙酸乙酯的混合液,洗脱方法为二者比例5:1~1:1依次梯度洗脱;
[0135]
所述s3中葡聚糖凝胶柱色谱的洗脱液为三氯甲烷和甲醇的混合液,洗脱方法为二者比例2:1~1:2依次梯度洗脱;
[0136]
所述s3中反相柱色谱的洗脱液为甲醇和水的混合液,洗脱方法为二者比例7:3~10:0依次梯度洗脱;
[0137]
所述s3中高效液相色谱的洗脱液为乙腈、水和二乙胺的混合液,洗脱方法为三者的比例6:4:0.005~10:0:0.005,依次梯度洗脱。
[0138]
一具体方式为:
[0139]
溶样溶剂:70%乙腈水;
[0140]
洗脱剂:65%乙腈+35%水+0.05%二乙胺,洗脱时长:15min,65%乙腈+35%水逐步提升乙腈比例变为100%乙腈,洗脱时长:30min;
[0141]
流速:0.8ml/min;
[0142]
色谱柱:依利特sinachrom ods bp,5μm,250*4.6mm;
[0143]
柱温:40℃。
[0144]
制得1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
ꢀ‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑7‑
甲氧基
‑2‑
甲基
‑6‑
异喹啉,产品检测参考图2。在前述配比方案范围内均可制得目标产物。
[0145]
体外抗肿瘤活性实验方法:肿瘤细胞培养于含10%小牛血清、青霉素和链霉素培养液中,置37℃,5%co2培养箱中培养。取对数生长期细胞进行增殖抑制实验。用mtt法检测提取物对5种肿瘤细胞(人乳腺癌细胞mda
‑
mb
‑
231、人宫颈癌细胞hela、人肝癌细胞hepg2、人前列腺癌细胞pc
‑
3、人肺癌细胞 a549)的增殖抑制作用,细胞活力数据见表2
‑
1。
[0146]
表2
‑
1:化合物2
‑
细胞活力(%)数据表
[0147][0148][0149]
以提取物的浓度对肿瘤细胞生长抑制率作图,可得到量效曲线,计算抑制率。体外抗肿瘤活性实验结果:见表2
‑
2。
[0150]
表2
‑
2:1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑7‑
甲氧基
‑2‑
甲基
‑6‑
异喹啉对5种肿瘤细胞的抑制率
[0151][0152]
实施例3
[0153]
本实施例提供化合物1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑6‑
甲氧基
‑2‑ꢀ
甲基
‑7‑
异喹啉的制备方法及其抗肿瘤活性的测定方法和结果。
[0154]
其化学结构式为:
[0155][0156]
其提取分离纯化步骤为:
[0157]
s1、提取:青风藤粉碎后,用含水体积比10%的乙醇浸泡,热回流提取3 次,每次2小时,过滤,收集滤液并在减压条件下浓缩,得到浓缩液;
[0158]
s2、萃取:将上述浓缩液加0.5~1.5倍体积的水溶解后,用等体积的石油醚、乙酸乙酯、正丁醇依次萃取,收集不同极性萃取液并在减压条件下浓缩,得到浓缩液;
[0159]
s3、纯化:将s2所得乙酸乙酯萃取物依次通过大孔树脂柱色谱、硅胶柱色谱、葡聚糖凝胶柱色谱、反相柱色谱等进行反复纯化。
[0160]
所述s3中大孔柱色谱中,洗脱液为甲醇和水的混合液,洗脱方法为二者比例5:5~10:0依次梯度洗脱;
[0161]
所述s3中硅胶柱色谱中硅胶粒度为100~200目,洗脱液为丙酮和乙酸乙酯的混合液,洗脱方法为二者比例5:1~1:1依次梯度洗脱;
[0162]
所述s3中葡聚糖凝胶柱色谱的洗脱液为三氯甲烷和甲醇的混合液,洗脱方法为二者比例2:1~1:2依次梯度洗脱;
[0163]
所述s3中反相柱色谱的洗脱液为甲醇和水的混合液,洗脱方法为二者比例7:3~10:0依次梯度洗脱;
[0164]
所述s3中高效液相色谱的洗脱液为乙腈、水和三乙胺的混合液,洗脱方法为三者的比例5:5:0.01~9:1:0.01,依次梯度洗脱。
[0165]
一具体方式为:
[0166]
溶样溶剂:90%甲醇水;
[0167]
洗脱剂:
①
50%乙腈+50%水+0.1%三乙胺,洗脱时长:20min,
②
50%乙腈 +50%水逐步提升乙腈比例变为90%乙腈+10%水,洗脱时长:40min;
[0168]
流速:0.8ml/min;
[0169]
色谱柱:纳微unisil 5
‑
100 c18 ultra,250*4.6mm column;
[0170]
柱温:40℃。
[0171]
制得1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑6‑
甲氧基
‑2‑
甲基
‑7‑
异喹啉,产品检测参考图3。在前述配比方案范围内均可制得目标产物。
[0172]
体外抗肿瘤活性实验方法:肿瘤细胞培养于含10%小牛血清、青霉素和链霉素培养液中,置37℃,5%co2培养箱中培养。取对数生长期细胞进行增殖抑制实验。用mtt法检测提取物对5种肿瘤细胞(人乳腺癌细胞mda
‑
mb
‑
231、人宫颈癌细胞hela、人肝癌细胞hepg2、人前列腺癌细胞pc
‑
3、人肺癌细胞 a549)的增殖抑制作用,细胞活力数据见表3
‑
1。
[0173]
表3
‑
1:化合物3
‑
细胞活力(%)数据表
[0174][0175]
以提取物的浓度对肿瘤细胞生长抑制率作图,可得到量效曲线,计算抑制率。体外抗肿瘤活性实验结果:见表3
‑
2。
[0176]
表3
‑
2:1,2,3,4
‑
四氢
‑1‑
[[4
‑
羟基
‑3‑
[4
‑
[(1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基)甲基]苯氧基]苯基]甲基]
‑6‑
甲氧基
‑2‑
甲基
‑7‑
异喹啉对5种肿瘤细胞的抑制率
[0177][0178]
实施例4
[0179]
本实施例提供化合物4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]
‑2‑
[4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基] 苯氧基]苯酚的制备方法及其抗肿瘤活性的测定方法和结果。
[0180]
其化学结构式为:
[0181][0182]
其提取分离纯化步骤为:
[0183]
s1、提取:青风藤粉碎后,用含水体积比5%的乙醇浸泡,热回流提取3 次,每次2小时,过滤,收集滤液并在减压条件下浓缩,得到浓缩液;
[0184]
s2、萃取:将上述浓缩液加0.5~1.5倍体积的水溶解后,用等体积的石油醚、乙酸乙酯、正丁醇依次萃取,收集不同极性萃取液并在减压条件下浓缩,得到浓缩液;
[0185]
s3、纯化:将s2所得乙酸乙酯萃取物依次通过大孔树脂柱色谱、硅胶柱色谱、葡聚糖凝胶柱色谱、反相柱色谱等进行反复纯化。
[0186]
所述s3中大孔柱色谱中,洗脱液为甲醇和水的混合液,洗脱方法为二者比例5:5~10:0依次梯度洗脱;
[0187]
所述s3中硅胶柱色谱中硅胶粒度为100~200目,洗脱液为丙酮和乙酸乙酯的混合液,洗脱方法为二者比例5:1~1:1依次梯度洗脱;
[0188]
所述s3中葡聚糖凝胶柱色谱的洗脱液为三氯甲烷和甲醇的混合液,洗脱方法为二者比例2:1~1:2依次梯度洗脱;
[0189]
所述s3中反相柱色谱的洗脱液为甲醇和水的混合液,洗脱方法为二者比例7:3~10:0依次梯度洗脱;
[0190]
所述s3中高效液相色谱的洗脱液为乙腈、水、磷酸和三乙胺的混合液,洗脱方法为四者的比例5:5:0.01:0.01~10:0:0.01:0.01,依次梯度洗脱。
[0191]
一具体方式为:
[0192]
溶样溶剂:50%甲醇水;
[0193]
洗脱剂:
①
45%乙腈+55%水+0.1%磷酸+0.1%三乙胺,洗脱时长:20min,
②
45%乙腈+55%水逐步提升乙腈比例变为95%乙腈+5%水,洗脱时长:40min;
[0194]
流速:1.0ml/min;
[0195]
色谱柱:minxi teeh cg
‑
c18 5mic,250*4.6mm;
[0196]
柱温:40℃。
[0197]
制得4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]
‑2‑
[4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]苯氧基] 苯酚,产品检测参考图4。在前述配比方案范围内均可制得目标产物。
[0198]
体外抗肿瘤活性实验方法:肿瘤细胞培养于含10%小牛血清、青霉素和链霉素培养液中,置37℃,5%co2培养箱中培养。取对数生长期细胞进行增殖抑制实验。用mtt法检测提取物对5种肿瘤细胞(人乳腺癌细胞mda
‑
mb
‑
231、人宫颈癌细胞hela、人肝癌细胞hepg2、人前列腺癌细胞pc
‑
3、人肺癌细胞 a549)的增殖抑制作用,细胞活力数据见表4
‑
1。
[0199]
表4
‑
1:化合物4
‑
细胞活力(%)数据表
[0200][0201]
以提取物的浓度对肿瘤细胞生长抑制率作图,可得到量效曲线,计算抑制率。体外抗肿瘤活性实验结果:见表4
‑
2。
[0202]
表4
‑
2:4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]
‑2‑
[4
‑
[[1,2,3,4
‑
四氢
‑
6,7
‑
二甲氧基
‑2‑
甲基
‑1‑
异喹啉基]甲基]苯氧基] 苯酚对5种肿瘤细胞的抑制率
[0203][0204]
异喹啉类生物碱化合物还具有其他结构通式,当式ⅰ中r1
‑
r2均为
ꢀ‑
och2ch2ch3时,r3
‑
r4均为
‑
och2ch3,如下式ⅱ所示,其针对肿瘤细胞也具有相应的抑制作用。其中,r1
‑
r4的碳链长度也变化也同样具有相近的性质,均应在本发明保护范围中。
[0205][0206]
同时,式ⅰ中r1、r2均为
‑
och2ch2ch3,r3为
‑
och2cl,r4时为
‑
och2ch3,如下式ⅲ所示,其针对肿瘤细胞也具有相应的抑制作用。该化合可由式ⅱ化合物通过取代反应制备,在此仅列举了其中一个位置取代方式,其他位置的取代反应参考现有资料。
[0207][0208]
采用式ⅰ物质或其可预期同系物、取代物,凡是不影响对肿瘤细胞抑制作用的均应在本发明保护范围内。
[0209]
实验结果表明,本发明提供的一种青风藤中提取的异喹啉类生物碱抗肿瘤活性强,具有重要的经济效应。该异喹啉类生物碱可单独或联合使用,用于片剂、胶囊剂、颗粒剂、栓剂、丸剂、软膏剂、乳膏剂、喷雾剂、气雾剂、凝胶剂、散剂、糖浆剂、搽剂、涂剂、涂膜剂、酊剂、贴剂、贴膏剂、口服溶液剂、口服混悬剂、口服乳剂、膜剂、洗剂、冲洗剂、酒剂、膏药、茶剂等剂型。
[0210]
本领域的技术人员可以明确,在不脱离本发明的总体精神以及构思的情形下,可以做出对于以上实施例的各种变型。其均落入本发明的保护范围之内。本发明的保护方案以本发明所附的权利要求书为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1