一种特异性结合CD276的抗体或其抗原结合片段及其制备方法和应用与流程
一种特异性结合cd276的抗体或其抗原结合片段及其制备方法和应用
技术领域
1.本发明涉及生物免疫治疗技术领域,具体而言,涉及一种特异性结合cd276的抗体或其抗原结合片段及其制备方法和应用。
背景技术:
2.cd276,也称b7
‑
h3,是b7和cd28家族重要的免疫检查点成员,属于i型跨膜蛋白,胞外区包含两对相同的免疫球蛋白可变区和恒定区,胞内区很短,没有明确的信号基序。其mrna水平的表达较为广泛,但蛋白表达相对局限在静息的成纤维细胞、内皮细胞、成骨细胞、羊水干细胞等非免疫细胞,以及受诱导的抗原提呈细胞和nk细胞表面。
3.研究表明cd276在多种恶性肿瘤中表达均异常升高,包括脑胶质瘤、胰腺癌、卵巢癌、肺癌、肾癌、乳腺癌、前列腺癌、结直肠癌及其它肿瘤等。cd276在肿瘤细胞中表达升高后细胞黏连蛋白的粘附能力随之升高,导致肿瘤细胞的迁移和侵袭能力增强,表达水平与患者预后不良和临床转归差密切相关,推测其参与了肿瘤的免疫逃避。虽然其分子机制还不明确,但作为一种可能的免疫检查点分子,是一个有前景的肿瘤免疫治疗靶标。
4.嵌合抗原受体t细胞(chimeric antigen receptor
‑
t cell,car
‑
t)是一种针对肿瘤细胞表面特异性抗原的新型免疫治疗方法。现在,许多研究人员正在开发治疗实体瘤的car
‑
t细胞。
5.单链抗体作为car中重要的组成部分,目前传统上采用鼠源抗体,由于鼠抗的异质性会引起人抗鼠抗体反应(human anti
‑
mouse antibody reaction,hama),导致car
‑
t在循环系统中被很快清除,失去疗效。
6.鉴于此,特提出本发明。
技术实现要素:
7.本发明的目的在于提供一种特异性结合cd276的抗体或其抗原结合片段及其制备方法和应用。
8.本发明是这样实现的:第一方面,本发明实施例提供了一种特异性结合cd276的抗体或其抗原结合片段,所述抗体或其抗原结合片段至少包括以下重链可变区和轻链可变区中的一种;所述重链可变区至少包括hcdr1、hcdr2和hcdr3中的一种;所述hcdr1的序列如seq id no:1、2、或3所示,所述hcdr2的序列如seq id no:4、5、或6所示,所述hcdr3的序列如seq id no:7、8、9、或10所示;所述轻链可变区至少包括lcdr1、lcdr2和lcdr3中的一种;所述lcdr1的序列如seq id no:11、12、13、或14所示,所述lcdr2的序列如seq id no:15、或16所示,所述lcdr3的序列如seq id no:17、18、19、或20所示。
9.第二方面,本发明实施例提供了一种分离的核酸,其编码如前述实施例所述的特
异性结合cd276的抗体或其抗原结合片段。
10.第三方面,本发明实施例提供了一种载体,其包括如前述实施例所述的分离的核酸。
11.第四方面,本发明实施例提供了一种宿主细胞,其包括如前述实施例所述的载体。
12.第五方面,本发明实施例提供了一种特异性结合cd276的抗体或其抗原结合片段的制备方法,其包括培养如前述实施例所述的宿主细胞。
13.第六方面,本发明实施例提供了一种抗人cd276的嵌合抗原受体car,所述car包含可识别cd276抗原的抗原识别区、铰链区、跨膜区和胞内区;所述抗原识别区包括如前述实施例所述的特异性结合cd276的抗体或其抗原结合片段。
14.第七方面,本发明实施例提供了一种分离的核酸,其编码如前述实施例所述的抗人cd276的嵌合抗原受体car。
15.第八方面,本发明实施例提供了一种载体,其包括如前述实施例分离的核酸。
16.第九方面,本发明实施例提供了一种宿主细胞,其包括如前述实施例载体。
17.第十方面,本发明实施例提供了一种抗人cd276的嵌合抗原受体car的制备方法,其包括培养前述实施例宿主细胞。
18.第十一方面,本发明实施例提供了一种免疫效应细胞,其表达如前述实施例所述的特异性结合cd276的抗体或其抗原结合片段,或如前述实施例所述的抗人cd276的嵌合抗原受体car。
19.第十二方面,本发明实施例提供了一种免疫效应细胞的制备方法,其包括采用如前述实施例所述的分离的核酸或如前述实施例所述的载体感染免疫效应细胞。
20.第十三方面,本发明实施例提供了一种药物组合物,其包括:如前述实施例所述的特异性结合cd276的抗体或其抗原结合片段,或如前述实施例所述的分离的核酸,或如前述实施例所述的抗人cd276的嵌合抗原受体car、如前述实施例所述的分离的核酸,或如前述实施例所述的载体,或如前述实施例所述的免疫效应细胞。
21.第十四方面,本发明实施例提供了一种试剂在制备用于治疗或改善癌症的药物中的应用,所述试剂选自:如前述实施例所述的特异性结合cd276的抗体或其抗原结合片段、如前述实施例所述的分离的核酸、如前述实施例所述的载体、如前述实施例所述的宿主细胞、如前述实施例所述的特异性结合cd276的抗体或其抗原结合片段的制备方法制备获得的特异性结合cd276的抗体或其抗原结合片段、如前述实施例所述的抗人cd276的嵌合抗原受体car、如前述实施例所述的分离的核酸、如前述实施例所述的载体、如前述实施例所述的宿主细胞、如前述实施例所述的抗人cd276的嵌合抗原受体car的制备方法制备获得的抗人cd276的嵌合抗原受体car、如前述实施例所述的免疫效应细胞以及如前述实施例所述的免疫效应细胞的制备方法制备的免疫效应细胞中的至少一种。
22.本发明具有以下有益效果:本发明提供了一种特异性识别人cd276的全人源抗体,该抗体具有良好的安全性以及靶向cd276的治疗效果,且该抗体能够用于制备靶向cd276的免疫效应细胞,为与cd276表达相关的疾病提供了治疗或改善途径。
附图说明
23.为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。
24.图1为实施例1中重组人cd276
‑
avi
‑
his抗原蛋白的sds电泳图;图2为实施例1中重组人cd276
‑
avi
‑
his抗原蛋白质量鉴定图;图3为实施例2中使用octet k2仪器测定1c8、1h12、3c1和3e5解离常数;图4为实施例2中使用elisa测定cd276抗原与1c8、1h12、3c1和3e5 scfv片段的结合曲线;图5为实施例3中不同克隆cd276 car的示意图;图6为实施例4中不同克隆cd276 car
‑
t细胞的car表达阳性率;图7为实施例5中不同克隆cd276 car
‑
t细胞的cd107a表达;图8为实施例5中不同克隆cd276 car
‑
t细胞的infγ分泌;图9为实施例5中不同克隆cd276 car
‑
t细胞的il
‑
2分泌;图10为实施例5中不同克隆cd276 car
‑
t细胞对靶细胞的杀伤实验结果。
具体实施方式
25.为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。
26.首先,本发明实施例提供了一种特异性结合cd276的抗体或其抗原结合片段,所述抗体或其抗原结合片段至少包括以下重链可变区和轻链可变区中的一种;所述重链可变区至少包括hcdr1、hcdr2和hcdr3中的一种;所述hcdr1的序列如seq id no:1、2、或3所示,所述hcdr2的序列如seq id no:4、5、或6所示,所述hcdr3的序列如seq id no:7、8、9、或10所示;所述轻链可变区至少包括lcdr1、lcdr2和lcdr3中的一种;所述lcdr1的序列如seq id no:11、12、13、或14所示,所述lcdr2的序列如seq id no:15、或16所示,所述lcdr3的序列如seq id no:17、18、19、或20所示。
27.本文中的“抗体”与“免疫球蛋白”的定义可相互等同。
28.抗体的重链可变区和轻链可变区通常包括3个互补决定区cdr和4个骨架区fr。互补决定区之间通过骨架区连接,在识别抗体时,fr分子卷曲使cdr分子相互靠近。互补决定区为抗体或抗原结合片段与抗原的结合部位,因此,互补决定区的序列决定了抗体的特异性。本文中的“hcdr1”、“hcdr2”、“hcdr3”为重链可变区的3个互补决定区,“lcdr1”、“lcdr2”和“lcdr3”为轻链可变区的3个互补决定区。
29.本文中的“抗原结合片段”是指多肽片段,具有能够特异性靶向cd276的特性,其含有抗体重链可变区和/或轻链可变区的至少一个cdr;优选地,其可以含有重链可变区的hcdr1~3和/或轻链可变区的lcdr1~3。抗原结合片段可以通过多种技术制备,包括但不限于
将完整的抗体蛋白水解消化,以及由包含抗原结合片段的宿主细胞表达产生。
30.经一系列创造性劳动,本发明提供了上述靶向cd276的抗体或其抗原结合片段,所述抗体或其抗原结合片段具有良好的安全性和靶向性,能够特异性结合人cd276的胞外域,将包含该抗体或其抗原结合片段的编码序列的载体,用于感染免疫细胞,能够获得对表达cd276的肿瘤细胞具有显著杀伤能力的免疫效应细胞,该免疫效应细胞能够应用于治疗或改善cd276表达相关的疾病,从而为cd276阳性肿瘤的治疗奠定了基础。
31.在没有限定的情况下,抗体或其抗原结合片段的hcdr1、hcdr2、hcdr3、lcdr1、lcdr2和lcdr 3的序列可在上述范围内随机选择。
32.优选地,所述抗体或其抗原结合片段包括重链可变区和轻链可变区,其重链可变区和轻链可变区选自(a)~(d)项中的任意一种;(a)序列如seq id no:1所示的hcdr1、序列如seq id no:4所示的hcdr2、序列如seq id no:7所示的hcdr3以及序列如seq id no:11所示的lcdr1、序列如seq id no:15所示的lcdr2、序列如seq id no:17所示的lcdr3;(b)序列如seq id no:2所示的hcdr1、序列如seq id no:5所示的hcdr2、序列如seq id no:8所示的hcdr3以及序列如seq id no:12所示的lcdr1、序列如seq id no:15所示的lcdr2、序列如seq id no:18所示的lcdr3;(c)序列如seq id no:2所示的hcdr1、序列如seq id no:5所示的hcdr2、序列如seq id no:9所示的hcdr3以及序列如seq id no:13所示的lcdr1、序列如seq id no:15所示的lcdr2、序列如seq id no:19所示的lcdr3;(d)序列如seq id no:2所示的hcdr1、序列如seq id no:5所示的hcdr2、序列如seq id no:10所示的hcdr3以及序列如seq id no:14所示的lcdr1、序列如seq id no:16所示的lcdr2、序列如seq id no:20所示的lcdr3。
33.优选地,所述抗体或其抗原结合片段包括重链和轻链,所述重链可变区的氨基酸序列如seqidno:21、22、23和24中的任意一种所示;所述轻链可变区的氨基酸序列如seqidno:25、26、27和28中的任意一种所示。
34.可选地,所述抗体包括单克隆抗体、人源化抗体、嵌合抗体、双特异性抗体中的至少一种;所述抗原结合片段为fab、f(ab’)、f(ab’)2、fd、单链抗体scfv、二硫键连接的fv(sdfv)、或单域抗体中的至少一种。
35.在可选的实施方式中,所述抗体或其抗原结合片段是人源化的。
36.在可选的实施方式中,所述抗体还包括抗体恒定区;优选地,所述抗体恒定区选自:igg1、igg2、igg3、igg4、iga、igm、ige和igd中的任意一者的恒定区。
37.优选地,所述抗体恒定区的重链恒定区选自igg1、igg2、igg3、igg4中任意一者的重链恒定区,优选为igg4的重链恒定区;所述抗体恒定区的轻链恒定区为卡帕(κ)或拉姆达(λ),优选为卡帕。
38.本发明实施例还提供了一种分离的核酸,其编码如前述任意实施例所述的特异性结合cd276的抗体或其抗原结合片段。
39.本发明实施例还提供了一种载体,其包括如前述实施例所述的分离的核酸。
40.可选地,所述载体为表达载体或克隆载体。
41.可选地,所述载体为质粒载体。
42.本发明实施例还提供了一种宿主细胞,其包括前述实施例所述的分离的核酸或者前述实施例所述的载体。
43.可选地,所述宿主细胞库为原核细胞或真核细胞。可选地,所述原核细胞可以为大肠杆菌细胞,真核细胞具体可以为卵巢细胞。
44.本发明实施例还提供了一种特异性结合cd276的抗体或其抗原结合片段的制备方法,其包括培养如前述实施例所述的宿主细胞。
45.具体地,培养宿主细胞的条件是足以使得宿主细胞表达特异性结合cd276的抗体或其抗原结合片段的条件。
46.本发明实施例还提供了一种抗人cd276的嵌合抗原受体car,所述car包含可识别cd276抗原的抗原识别区、铰链区、跨膜区和胞内区;所述抗原识别区包括如前述任意实施例所述的特异性结合cd276的抗体或其抗原结合片段。
47.在没有限定的情况下,“抗原识别区”可以为单价的或多价的(如二价的或三价的)。抗原结合区可以是单特异性的或多特异性的(例如双特异性的)。双特异性可以是针对cd276和另一种抗原,也可以是针对cd276的两种不同表位。优选地,所述抗原识别区为单链抗体(一价或多价)。单链抗体scfv包括重链可变区和轻链可变区,重链可变区和轻链可变区通过linker(接头)连接而成的抗体。
48.优选地,scfv的重链可变区的氨基酸序列如seq id no:21,轻链可变区的氨基酸序列如seq id no:25;或重链可变区的氨基酸序列如seq id no:22,轻链可变区的氨基酸序列如seq id no:26;或重链可变区的氨基酸序列如seq id no:23,轻链可变区的氨基酸序列如seq id no:27;或重链可变区的氨基酸序列如seq id no:24,轻链可变区的氨基酸序列如seq id no:28所示。
49.在可选的实施方式中,scfv重链和轻链的连接方式为vh
‑
linker
‑
vl或vl
‑
linker
‑
vh。在一些实施例中,linker的序列可选用现有的接头序列,优选地,linker的序列可以为ggggsggggsggggs,也可以是(ggggs)n,其中n=1
‑
6,还可以为gstsgsgkpgsgegstkg。
50.优选地,所述car还包括前导信号肽序列。一般而言,信号肽是使多肽靶向细胞中的所需部位的肽序列。在一些实施方案中,信号肽使多肽靶向细胞的分泌通路,并且将允许多肽整合和锚定至脂双层。在一些实施方案中,信号肽为膜定位信号肽。优选地,所述前导肽序列来源于cd8的前导肽序列;更优选地,所述cd8前导肽序列具有seq id no:29所示的氨基酸序列。
51.本文中的“铰链区”、“跨膜区”和“胞内区”均可选自现有已知的car
‑
t技术中的铰链区、跨膜区和胞内区的序列。
52.嵌合抗原受体的铰链区位于胞外抗原结合区和跨膜区之间,铰链区是通常在蛋白质的两个域之间存在的氨基酸区段,并且可以允许蛋白质的柔性和两个域的彼此相对运动。铰链区可以是天然存在的蛋白质的铰链区或其部分。抗体(诸如igg、iga、igm、ige或igd抗体)的铰链区也可用于本文所述的嵌合抗原受体。非天然存在的肽也可用作本文所述的嵌合抗原受体的铰链区。在一些实施方案中,铰链区是肽接头。优选地,所述铰链区来源于cd8α。优选地,所述cd8α铰链区具有seq id no:30所示的氨基酸序列。
53.嵌合抗体受体的跨膜区可以形成α螺旋、多于一个α螺旋的复合物、β桶或能够跨域细胞磷脂双层的任何其它稳定结构。跨膜区可以是天然或合成来源的。跨膜区可源自cd3ε、cd4、cd5、cd8α、cd9、cd16、cd22、cd28、cd33、cd37、cd45、cd64、cd80、cd86、cd134、cd137、cd154、t细胞受体的α、β或ζ链。优选地,所述跨膜区来源于cd8α。优选地,所述cd8α跨膜区具有seq id no:31所示的氨基酸序列。
54.优选地,嵌合抗原受体的胞内区包含信号传导区和/或共刺激信号传导区。信号传导区和/或共刺激信号传导区的个数均可以为一个或多个。
55.胞内信号传导区负责表达嵌合抗原受体的免疫效应细胞的至少一种正常效应子功能的活化。例如,t细胞的效应子功能可以是细胞裂解活性或辅助活性,包括细胞因子的分泌。虽然通常可以利用整个胞内信号传导区,但是在很多情况下,使用整个链是不必要的。就使用胞内信号传导区的截短部分而言,只要其转导效应子功能信号,就可以使用这种截短部分代替完整链。因此,胞内信号传导区包括足以转导效应子功能信号的胞内信号传导区的任何截短形式。在一些实施方案中,信号传导区来源于cd3ζ、fcrγ (fcer1g)、fcrβ (fcε rib)、cd3γ、cd3δ、cd3ε、cd5、cd22、cd79a、cd79b和cd66d中的至少一种。优选地,所述胞内区来源于人cd3ζ胞内区。进一步地,所述人cd3ζ胞内区具有seq id no:32所示氨基酸序列。
56.在抗原特异性信号的刺激以外,很多免疫效应细胞还需要共刺激来促进细胞增殖、分化和存活,以及活化细胞的效应子功能。“共刺激信号传导区”可以是共刺激分子的胞质部分。术语“共刺激分子”是指免疫细胞(诸如t细胞)上的关联结合伴侣,该关联结合伴侣与共刺激配体特异性结合,从而由免疫细胞介导共刺激响应,诸如但不限于增殖和存活。共刺激信号传导区可源自card11,cd2,cd7,cd27,cd28,cd30,cd40,cd54,cd83,ox40,cd137, cd134,cd150,cd152,cd223,cd270,pd
‑
l2,pd
‑
l1,cd278,dap10,lat,nkd2c,slp76,trim,fcεriγ,myd88,和41bbl 中至少一种的胞内信号区。在一些实施方案中,共刺激信号传导区来源于4
‑
1bb。在一些实施方案中,4
‑
1bb共刺激信号传导区包含seq id no:33的氨基酸序列。
57.优选地,所述car的核苷酸序列如seq id no:34、35、36和 37中的任意一种所示。
58.本发明实施例提供了一种分离的核酸,其编码如前述任意实施例所述的抗人cd276的嵌合抗原受体car。
59.本发明实施例提供了一种载体,其包括如前述实施例所述的分离的核酸(编码如前述任意实施例所述的抗人cd276的嵌合抗原受体car的核酸)。载体可以为表达载体或克隆载体。在一些实施例中,载体为病毒载体。病毒载体包括但不限于腺病毒载体、腺相关病毒载体、慢病毒载体、逆转录病毒载体、牛痘载体、单纯疱疹病毒载体及其衍生物。
60.本发明实施例提供了一种宿主细胞,其包括如前述实施例所述的载体(含有编码如前述任意实施例所述的抗人cd276的嵌合抗原受体car的核酸的载体)。可选地,宿主细胞可以为原核细胞或真核细胞。优选为真核细胞,如哺乳动物细胞。
61.本发明实施例提供了一种抗人cd276的嵌合抗原受体car的制备方法,其包括培养如前述实施例所述的宿主细胞。
62.优选地,所述制备方法的培养条件足以使宿主细胞能够表达抗人cd276的嵌合抗原受体car。
63.本发明实施例提供了一种免疫效应细胞,其表达如前述任意实施例所述的特异性结合cd276的抗体或其抗原结合片段,或如前述任意实施例所述的抗人cd276的嵌合抗原受体car。
[0064]“免疫效应细胞”是可执行免疫效应功能的免疫细胞。在一些实施方案中,免疫效应细胞表达至少fcγriii并执行adcc效应子功能。介导adcc的免疫效应细胞的实例包括外周血单个核细胞(pbmc)、天然杀伤(nk)细胞、单核细胞、细胞毒性t细胞、中性粒细胞和嗜酸性粒细胞。
[0065]
优选地,所述免疫效应细胞选自:由多能干细胞或胚胎干细胞培养分化的免疫细胞、t淋巴细胞、nk细胞、外周血单个核细胞(pbmc)和造血干细胞中的至少一种。更优选地,所述免疫效应细胞为t淋巴细胞(同t细胞)。在一些实施方案中,t细胞可以为cd4+/ cd8
‑
、cd4
‑
/cd8+、cd4+/cd8+、cd4
‑
/cd8
‑
或它们的组合。在一些实施方案中,t细胞在表达嵌合抗原受体并结合至靶细胞时产生il
‑
2、ifn和/或tnf。在一些实施方案中,cd8+ t细胞在表达嵌合抗原受体并结合至靶细胞时裂解抗原特异性靶细胞。
[0066]
本发明实施例提供了如前述实施例所述的免疫效应细胞的制备方法,其包括采用如前述任意实施例所述的分离的核酸或如前述任意实施例所述的载体感染免疫效应细胞。
[0067]
本发明实施例通过将嵌合抗原受体引入免疫效应细胞(诸如t细胞)来制备经基因改造的免疫效应细胞。
[0068]
需要说明的是,将核酸或载体引入哺乳动物细胞的方法是本领域已知的,所述载体可以通过物理、化学或生物方法转入免疫效应细胞。用于将载体引入免疫效应细胞的物理方法包括磷酸钙沉淀、脂质体转染、粒子轰击、显微注射、电穿孔等等。用于将核酸或载体引入免疫效应细胞的化学手段包括胶体分散体系,诸如大分子复合物、纳米胶囊、微球体、珠粒和基于脂质的体系(包括水包油乳液、胶束、混合胶束和脂质体)。用作体外递送媒介物的示例性胶体体系是脂质体(例如人工膜囊泡)。用于将核酸或载体引入免疫效应细胞的生物方法包括使用dna和rna载体。病毒载体已成为将基因插入哺乳动物,例如人细胞的最广泛使用的方法。在一些实施方案中,转导的或转染的免疫效应细胞在引入核酸或载体之后离体繁殖。
[0069]
在一些实施方案中,所述制备还包括还包括进一步评估或筛选转导的或转染的免疫效应细胞以选择经改造的免疫效应细胞。
[0070]
本发明实施例提供了一种药物组合物,其包括:如前述任意实施例所述的特异性结合cd276的抗体或其抗原结合片段、如前述任意实施例所述的分离的核酸、如前述任意实施例所述的载体、如前述任意实施例所述的特异性结合cd276的抗体或其抗原结合片段的制备方法制备获得的特异性结合cd276的抗体或其抗原结合片段、如前述任意实施例所述的抗人cd276的嵌合抗原受体car、如前述任意实施例所述的分离的核酸、如前述任意实施例所述的抗人cd276的嵌合抗原受体car的制备方法制备获得的抗人cd276的嵌合抗原受体car、如前述任意实施例所述的免疫效应细胞以及如前述任意实施例所述的免疫效应细胞的制备方法制备的免疫效应细胞中的至少一种。
[0071]
在一些实施方案中,所述药物组合物还包括药学上可接受的载剂。
[0072]
药物组合物可以通过使具有所需纯度的活性药剂与任选的药学上可接受的载剂混合以冻干制剂或水溶液的形式制备。药学上可接受的载剂在所用的剂量和浓度下对接受
者是无毒的,可包括缓冲剂、抗氧化剂、防腐剂、等渗剂、稳定剂和表面活性剂中的至少一种。此外,为了使药物组合物可用于体内施用,它们必须是无菌的。可以通过无菌过滤膜过滤使药物组合物无菌。
[0073]
在一些实施方案中,药物组合物可以含有:细胞毒性剂、化学治疗剂、细胞因子、免疫抑制剂、生长抑制剂以及待治疗的具体适应症所需的活性药剂中的至少一种添加剂。添加剂的具体添加量可根据实际需要进行调整。
[0074]
本发明实施例还提供了试剂在制备用于治疗或改善癌症的药物中的应用,所述试剂选自:如前述任意实施例所述的特异性结合cd276的抗体或其抗原结合片段、如前述任意实施例所述的分离的核酸、如前述任意实施例所述的载体、如前述任意实施例所述的宿主细胞、如前述任意实施例所述的特异性结合cd276的抗体或其抗原结合片段的制备方法制备获得的特异性结合cd276的抗体或其抗原结合片段、如前述任意实施例所述的抗人cd276的嵌合抗原受体car、如前述任意实施例所述的抗人cd276的嵌合抗原受体car的制备方法制备获得的抗人cd276的嵌合抗原受体car、如前述任意实施例所述的免疫效应细胞以及如前述任意实施例所述的免疫效应细胞的制备方法制备的免疫效应细胞中的至少一种。
[0075]
优选地,所述治疗或改善癌症是指能够激发或提高癌症患者的免疫功能地药物。
[0076]
优选地,所述癌症为与cd276表达相关的癌症。
[0077]
本文中“与cd276表达相关的癌症”是指由cd276表达异常所直接或间接导致的疾病,通常是指由cd276过表达所导致的疾病。
[0078]
优选地,所述癌症选自脑胶质瘤、肾癌、卵巢癌、肺癌、胃癌、肝癌、肠癌、前列腺癌、胰腺癌和间皮癌中的至少一种。
[0079]
以下结合实施例对本发明的特征和性能作进一步的详细描述。
[0080]
实施例1:重组人cd276蛋白表达载体构建与真核表达。
[0081]
1 . cd276的29位至466位氨基酸区间的基因序列的合成及蛋白的表达载体的构建。
[0082]
将cd276的第29位至466位氨基酸序列(uniprot accession no:q5zpr3
‑
1)导入在线密码子优化工具(http://www.jcat.de/#opennewwindow),得到密码子优化后的核酸序列,然后通过化学合成的方式得到基因序列,同时在该基因序列的3’端添加avi
‑
tag和6
×
his
‑
tag的核酸序列,融合基因序列编码seq id no:39所示的氨基酸序列,seq id no:40所示的核苷酸酸序列。通过分子克隆,拼接产物用takara无缝克隆试剂盒克隆到pcdna3 .1(thermo)中,获得表达载体。
[0083]
22. 重组人cd276蛋白的表达、纯化及活性鉴定。
[0084]
以获得的表达载体转染293t细胞(atcc)5天后,收集培养上清,用akta explorer 100(ge)纯化重组人cd276蛋白。由于糖基化修饰等原因,重组人cd276蛋白经还原sds
‑
page电泳后通过考马斯亮蓝染色显示其大小约65千道尔顿左右,结果如图1所示。
[0085]
用商业化cd276鼠源抗体对重组人cd276蛋白进行elisa活性鉴定:在elisa板中2倍梯度稀释包被重组人cd276蛋白,第一个孔包被200ng,依次稀释2倍(100ul/well),4℃孵育过夜,次日200ul pbst清洗3次,加入1% bsa/pbs封闭1小时。去除封闭液,加入1:4000稀释的鼠抗人cd276抗体(每孔100ul),37℃孵育1小时。200ul pbst清洗3次后加入1:4000稀释的辣根过氧化物酶标记的羊抗鼠igg1抗体(每孔100ul),37℃孵育1小时。200ul pbst清
洗3次后加入100ul tmb显色液,37℃显色10分钟,加入100ul 1m盐酸终止显色,并读取od450,分析结果如图2和表1所示。
[0086]
表1分析结果 cd276ec50(ng/μl)15.12rsquare0.9946
[0087]
实施例2:抗人cd276人源抗体的制备。
[0088]
1. 构建人天然抗体噬菌体展示文库。
[0089]
采用两步法构建人天然抗体噬菌体展示文库,即分两步将人天然抗体的轻链基因和重链基因连接到噬菌体展示载体中。
[0090]
用人免疫球蛋白κ链可变区正向引物(vk
‑
mix
‑
f)和轻链恒定区反向引物(ck
‑
mix
‑
r)以人pbmc cdna为模板pcr扩增人免疫球蛋白κ链基因,pcr反应条件如下:98℃预变性1分钟后进入温度循环,98℃变性30秒,58℃退火30秒,72℃延伸1分钟,循环30次,72℃最终延伸10分钟。pcr产物经1%琼脂糖凝胶电泳后,用胶回收试剂盒(promega)回收750bp左右的κ链基因片段。κ链基因和噬菌体展示载体pcomb3z用nhei和sali dna内切酶(neb)进行双酶切,酶切后的κ链基因直接用胶回收试剂盒进行回收。而酶切后的pcomb3z载体经1%琼脂糖凝胶电泳后,用胶回收试剂盒(promega)回收5200bp载体片段。将κ链基因用t4 dna连接酶试剂盒(invitrogen)连接到pcomb3z载体中,连接产物用pcr回收试剂盒进行脱盐。将脱盐的连接产物电击转化tg1电转感受态细胞,得到κ文库,电击转化后的κ文库经过夜扩增,第二天用质粒大抽试剂盒(mn)抽取κ链文库质粒。
[0091]
使用人免疫球蛋白重链可变区正向引物(vh
‑
mix
‑
f)和igm ch1恒定区反向引物(igm
‑
ch1
‑
r)以人pbmc cdna为模板pcr扩增人免疫球蛋白igm fd(vh
‑
ch1)基因,pcr反应条件与上述相同。pcr产物经1%琼脂糖凝胶电泳后,用胶回收试剂盒(promega)回收750bp左右的fd基因片段。igm fd基因片段和κ链文库质粒用sfii dna内切酶进行单酶切,酶切后的igm fd基因直接用胶回收试剂盒进行回收。而酶切后的κ链文库经1%琼脂糖凝胶电泳后,用胶回收试剂盒(promega)回收4000bp载体片段。将igm fd基因用t4 dna连接酶试剂盒(invitrogen)连接到κ链文库中,连接产物用pcr回收试剂盒进行脱盐。将脱盐的连接产物电击转化tg1电转感受态细胞,得到人天然抗体fab噬菌体展示文库,电击转化后的抗体文库经过夜扩增,离心收集文库菌体,加终浓度20%甘油
‑
80度保存。
[0092]
取冻存的部分人天然抗体噬菌体展示文库接种到2yt培养集中,接种密度为0.1od,将菌液置于37℃、220rpm条件进行培养,大约1.5小时后,菌液密度达到0.6od,此时加入20倍于菌体数的m13ko7噬菌体静置30分钟侵染,然后30℃、220rpm培养过夜。第二天,10000
×
g离心菌液,收集培养上清,向培养上清中加入1/4体积的peg/nacl溶液(20% peg8000,2.5m nacl),混匀后冰浴1小时。冰浴结束后,8000
×
g离心10分钟收集沉淀,用pbs将沉淀重新溶解即得到人天然抗体噬菌体展示文库。
[0093]
2. 筛选cd276抗体。
[0094]
2.1 重组人cd276蛋白偶联到链霉亲和素磁珠。
[0095]
用生物素化试剂盒(易锦生物)按试剂盒说明书,将重组人cd276蛋白的avi
‑
tag进行生物素修饰,得到生物素化的cd276蛋白。取10ug上述生物素修饰的重组蛋白加入到经
pbs洗涤3次的100ul 链霉亲和素磁珠(dynabeads 280)中,置于旋转摇床上,速度18转每分钟,室温偶联30分钟,然后pbs洗涤3次。
[0096]
2.2 封闭噬菌体文库及磁珠。
[0097]
向0.5ml噬菌体文库中加入0.5ml 1% bsa/pbs,置于旋转摇床上,速度18转每分钟,室温旋转封闭1小时,这些噬菌体为input1。同时取100ul未偶联蛋白的dynabeads 280,pbs洗涤3次后,加入1ml 1% bsa/pbs,按上述条件旋转孵育1小时。另外向上述偶联cd276的磁珠中加入1ml 1% bsa/pbs按上述条件旋转封闭1小时。
[0098]
2.3 阴性淘选。
[0099]
为去除与磁珠相互作用的抗体,有必要进行阴性淘选。将经bsa封闭的噬菌体文库和未偶联抗原的磁珠混合,按上述条件旋转孵育1小时。孵育结束后将噬菌体磁珠混合物置于磁力架上,待磁珠都贴壁之后,将上清转移至新的ep管中。
[0100]
2.4 阳性淘选。
[0101]
将上述封闭后的偶联有cd276蛋白的磁珠加入到阴性淘选后的噬菌体上清中进行阳性淘选,按上述条件室温旋转孵育1小时。孵育结束后用1ml pbst(0.1% tween
‑
20 in pbs)洗涤磁珠,重复洗涤10次。洗涤结束后加入1ml 100mm甘氨酸(ph2.0),置于旋转摇床上速度设定18转每分钟,旋转洗脱10分钟。洗脱结束后将ep管置于磁力架上,待磁珠都贴壁后将洗脱液转移至新的ep管中。向洗脱液中加入0.2ml 1m tris
‑
hcl溶液(ph 8.0)进行中和。将中和后的洗脱液加入到30ml od600约为0.6的tg1菌液中静置侵染30分钟,然后加入20倍于菌体数的m13ko7噬菌体,静置侵染30分钟,最后加入100ml 2yt培养基及终浓度为100ug/ml的氨苄霉素和卡那霉素,30℃、220rpm培养过夜。第二天按上述收获噬菌体文库之方法收获噬菌体,此时得到的噬菌体为input2。
[0102]
2.5 重复阳性淘选。
[0103]
按上述淘选方法进行2次重复,即将input2进行下一轮阴性淘选和阳性淘选得到input3。不同之处在于input3进行淘选得到的洗脱液侵染tg1后,不加m13ko7,而是取10ul菌液进行梯度稀释,取103、104、105 三个稀释梯度个100ul菌液涂布2yt/amp平板,30℃培养过夜;剩余的菌液30℃、220rpm培养过夜。
[0104]
2.6 elisa筛选阳性抗体。
[0105]
用牙签随机挑取上述平板中的tg1单克隆到含600ul 2yt/amp的深孔板中,深孔板粘覆透气膜,37℃、220rpm培养3小时后,揭开透气膜,向孔内加入终浓度为1mm的iptg,30℃、220rpm培养过夜。elisa 板中包被重组人cd276蛋白,每孔100ng。次日,将深孔板4000rpm离心10分钟,去除孔内培养基保留菌体沉淀,每孔加入100ul tes溶液(20%蔗糖、0.1mm edta、50mm tris
‑
hcl,ph 8.0),震荡使菌体重新悬浮后冰浴30分钟,加入200ul超纯水震荡混匀,4000rpm离心10分钟,此时深孔板中的上清溶液即为含有抗体的周质腔提取物。用洗板机清洗elisa板三次,然后中加入200ul 1% bsa/pbs,37℃封闭1小时。去除elisa板中的封闭液,加入100ul上述周质腔提取物,37℃孵育1小时,用洗板机清洗3次,加入hrp
‑
conjugated
‑
protein
‑
l(辣根过氧化物酶标记的蛋白l)溶液,37℃孵育1小时,用洗板机清洗3次,加入100ul tmb显色液,37℃显色10分钟,加入100ul 1m盐酸终止。用酶标仪读取od450值,将读值高于背景值3倍的克隆进行桑格测序,获得抗体的基因序列。
[0106]
2.7 验证阳性克隆。
[0107]
根据测序结果,选取抗体cdr3氨基酸序列差异较大的克隆重新接种并诱导过夜,按上述elisa方法再次验证所选克隆能否结合cd276。最终得到1c8、1h12、3c1和3e5四条抗体序列。
[0108]
1c8的重链可变区氨基酸序列如seq id no:21所示,轻链可变区序列的氨基酸序列如seq id no:25所示。
[0109]
1h12的重链可变区氨基酸序列如seq id no:22所示,轻链可变区序列的氨基酸序列如seq id no:26所示。
[0110]
3c1的重链可变区氨基酸序列如seq id no:23所示,轻链可变区序列的氨基酸序列如seq id no:27所示。
[0111]
3e5的重链可变区氨基酸序列如seq id no:24所示,轻链可变区序列的氨基酸序列如seq id no:28所示。
[0112]
3. 解离速率常数koff排序。
[0113]
利用octet k2分子互作分析仪对上述步骤筛选到能结合重组人cd276蛋白的克隆周质腔提取物进行分析。使用200ul 100nm生物素化的重组人cd276蛋白进行sa探针固化,固化高度1nm。以周质腔提取液作为分析物,进行解离常数测定并排序,结果如图3和表2所示。
[0114]
表2解离常数名称responsekdis(1/s)kdiserrordissocr^23c10.81497.40e
‑
031.32e
‑
040.9871891h120.46291.02e
‑
021.90e
‑
040.9795833e50.47767.39e
‑
039.03e
‑
050.9939321c80.24361.50e
‑
023.87e
‑
040.948326
[0115]
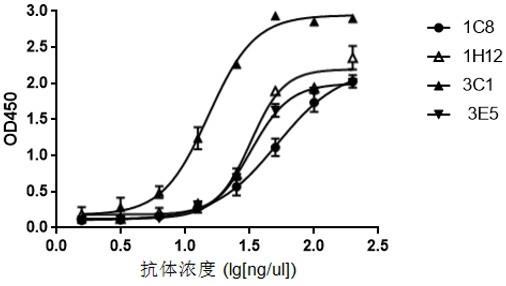
4. elisa测定重组人cd276 蛋白与1c8、1h12、3c1和3e5 scfv片段的结合曲线。
[0116]
分别构建1c8、1h12、3c1和3e5 scfv
‑
fc融合抗体并在真核细胞中的瞬转表达纯化,利用elisa来检测重组人cd276蛋白与上述4个scfv片段结合,elisa实验具体操作如下:酶标板中加入上文制备的重组人cd276蛋白100ng/孔,4℃包被过夜。pbs清洗三遍,加入1% bsa/pbs,200ul/孔,37℃封闭1小时。100ul pbs洗板后加入梯度稀释的上述4个scfv蛋白,37℃结合1小时。pbst清洗三遍,加入100ul 1:5000稀释的hrp
‑
山羊抗人igg(fab特异性的)37℃结合1小时。pbst清洗三遍,加入100ul/孔tmb显色液,37℃显色10分钟,加入100ul/孔elisa终止液,酶标仪读取od450数值,结果如图4和表3所示。
[0117]
表3检测结果 1c81h123c13e5ec5051.5832.1915.1232.14
[0118]
实施例3:含抗人cd276嵌合抗原受体元件的逆转录病毒原液制备。
[0119]
1. 靶向人cd276抗原的嵌合抗原受体的制备。
[0120]
基因合成或克隆含抗人cd276抗原的单链抗体scfv,铰链区、跨膜区和胞内信号段的嵌合抗原受体序列,其结构如图5所示。根据装载scfv和胞内信号的不同,将嵌合抗原受体分别命名为1c8
‑
bbz、1h12
‑
bbz、3c1
‑
bbz和3e5
‑
bbz,其核苷酸序列分别为seq id no:34、seq id no:35、seq id no:36和seq id no:37所示。同时选择文献报道的已知cd276鼠源抗
seqidno:14qsvssyvk
‑
cdr1
‑
4seqidno:15aasvk
‑
cdr2
‑
1seqidno:16dafvk
‑
cdr2
‑
2seqidno:17qqslsapltvk
‑
cdr3
‑
1seqidno:18qqsystppwtvk
‑
cdr3
‑
2seqidno:19qqtygnppwtvk
‑
cdr3
‑
3seqidno:20lhrsnwpplftvk
‑
cdr3
‑
4seqidno:21qvqlvesggglvqpggslrlscaasgftfgtyamswvrqapgkglewvsridgggsttnyadsvkgrftisrdnaknalylqmdslraedtamyyctratggtkhdywgqgtlvtvss1c8
‑
vhseqidno:22evqlvesggglvqpggslrlscaasgftfssyamswvrqapgkglewvsaisgsggstyyadsvkgrftisrdnskntlylqmnslraddtavyycaigihygfdywgqgtlvtvss1h12
‑
vhseqidno:23evqlvesggglvqpggslrlscaasgftfssyamswvrqapgkglewvsaisgsggstyyadsvkgrftisrdnsknslylqmnslgaedtavyycasisspddywgqgtlvtvss3c1
‑
vhseqidno:24qvqlvqsgaevkkpgssvkvsckasggtfsrfaiswvrqapgqglewmggiipifgtasyaqkfqgratitadeststaymelsslrsedtavyfcarghsgsytldywgqgtlvtvss3e5
‑
vhseqidno:25dvvmtqspsslsasvgdrvtitcrasqsvgiylnwyqqkpgkapklliyaasrlqsgvpsrfggsgsgtdftltisslqpedsatyycqqslsapltfgggtkveik1c8
‑
vkseqidno:26diqmtqspsslsasvgdrvtitcrasqsisfylnwyqqkpgkapklliyaasslqsgvpsrfggsgsgtdftltisslqpedfatyycqqsystppwtfgqgtkveik1h12
‑
vkseqidno:27diqmtqspsslsasvgdrvtiscrasqgigtflnwyqqkpgkvpkllihaasslqggvpsrfsgsgsgtdftltinslqredlatyycqqtygnppwtfgqgtkveik3c1
‑
vkseqidno:28qtpatlslspgeratlscrasqsagsqsvssylawyqqkpgqaprllindafnrapgiparfsgsgsgtdftltisslepedfavyyclhrsnwpplftfgggtkveik3e5
‑
vk
seqidno:29malpvtalllplalllhaarpcd8α信号肽seqidno:30tttpaprpptpaptiasqplslrpeacrpaaggavhtrgldfacdiycd8α铰链区seqidno:31iwaplagtcgvlllslvitlyccd8α跨膜区seqidno:32vkfsrsadapayqqgqnqlynelnlgrreeydvldkrrgrdpemggkprrknpqeglynelqkdkmaeayseigmkgerrrgkghdglyqglstatkdtydalhmqalpprcd3z胞质区seqidno:33rfsvvkrgrkkllyifkqpfmrpvqttqeedgcscrfpeeeeggcelr41bb胞质区
seqidno:34atggctctgcctgtgaccgccctgctgctgcctctggctctgctgctgcacgccgctcggcctgatgttgtgatgacacagtctccatcctccctgtctgcatctgtaggagacagagtcaccatcacttgccgggcaagtcagagtgttggcatctatttaaattggtatcagcagaaaccagggaaagcccctaagctcctgatctatgctgcatccagattgcaaagtggggtcccatcaaggttcggtggcagtggatctgggacagatttcactctcaccatcagcagtctgcaacctgaagattctgcaacttactactgtcaacagagtctcagtgcccctctcactttcggcggagggaccaaggtggagatcaagcgaggcggcggcggcagtggtggtggtggtagtggaggaggaggaagtcaggtgcagctggtggagtccgggggaggcttggtacagcctggggggtccctgagactctcctgtgcagcctctggattcacctttggcacctatgccatgagctgggtccgccaggctccagggaaggggctggagtgggtctcacgtattgatggtggtgggagcactacaaactacgcggactccgtgaagggccgattcaccatctccagagacaacgccaagaacgcgctgtatctgcaaatggacagtctgagagccgaggacacggctatgtattattgtacaagagcaacaggtggaacaaagcatgactactggggccagggaaccctggtcaccgtctcctcaactacaactccagcacccagaccccctacacctgctccaactatcgcaagtcagcccctgtcactgcgccctgaagcctgtcgccctgctgccgggggagctgtgcatactcggggactggactttgcctgtgatatctacatctgggcgcccttggccgggacttgtggggtccttctcctgtcactggttatcaccctttactgcaggttcagtgtcgtgaagagaggccggaagaagctgctgtacatcttcaagcagcctttcatgaggcccgtgcagactacccaggaggaagatggatgcagctgtagattccctgaagaggaggaaggaggctgtgagctgagagtgaagttctcccgaagcgcagatgccccagcctatcagcagggacagaatcagctgtacaacgagctgaacctgggaagacgggaggaatacgatgtgctggacaaaaggcggggcagagatcctgagatgggcggcaaaccaagacggaagaacccccaggaaggtctgtataatgagctgcagaaagacaagatggctgaggcctactcagaaatcgggatgaagggcgaaagaaggagaggaaaaggccacgacggactgtaccaggggctgagtacagcaacaaaagacacctatgacgctctgcacatgcaggctctgccaccaagatag1c8
‑
bbz
seqidno:35atggctctgcctgtgaccgccctgctgctgcctctggctctgctgctgcacgccgctcggcctgacatccagatgacccagtctccatcctccctgtctgcatctgtaggagacagagtcaccatcacttgccgggcaagtcagagcattagcttctatttaaattggtatcagcagaaaccagggaaagcccctaagctcctgatctatgctgcatccagtttgcaaagtggggtcccatcaaggttcggtggcagtggatctgggacagacttcaccctcaccatcagcagcctgcagcctgaagattttgcaacttactactgtcaacagagttacagtacccctccgtggacgttcggccaagggaccaaggtggaaatcaaacgaggcggcggcggcagtggtggtggtggtagtggaggaggaggaagtgaggtgcagctggtggagtctgggggaggcttggtacagcctggggggtccctgagactctcctgtgcagcctctggattcacctttagcagctatgccatgagctgggtccgccaggctccagggaaggggctggagtgggtctcagctattagtggtagtggtggtagcacatactacgcagactccgtgaagggccggttcaccatctccagagacaattccaagaacacgctgtatctgcaaatgaacagcctgagagccgacgacacggccgtatattactgtgcgattgggatccattacggctttgactactggggccagggaaccctggtcaccgtctcttcaactacaactccagcacccagaccccctacacctgctccaactatcgcaagtcagcccctgtcactgcgccctgaagcctgtcgccctgctgccgggggagctgtgcatactcggggactggactttgcctgtgatatctacatctgggcgcccttggccgggacttgtggggtccttctcctgtcactggttatcaccctttactgcaggttcagtgtcgtgaagagaggccggaagaagctgctgtacatcttcaagcagcctttcatgaggcccgtgcagactacccaggaggaagatggatgcagctgtagattccctgaagaggaggaaggaggctgtgagctgagagtgaagttctcccgaagcgcagatgccccagcctatcagcagggacagaatcagctgtacaacgagctgaacctgggaagacgggaggaatacgatgtgctggacaaaaggcggggcagagatcctgagatgggcggcaaaccaagacggaagaacccccaggaaggtctgtataatgagctgcagaaagacaagatggctgaggcctactcagaaatcgggatgaagggcgaaagaaggagaggaaaaggccacgacggactgtaccaggggctgagtacagcaacaaaagacacctatgacgctctgcacatgcaggctctgccaccaagatag1h12
‑
bbz
seqidno:36atggctctgcctgtgaccgccctgctgctgcctctggctctgctgctgcacgccgctcggcctgacatccagatgacccagtctccatcctccctgtctgcatctgttggagacagagtcaccatcagttgccgggcaagtcagggtattggtacttttttaaattggtaccagcagaagccagggaaagtccccaaacttctgatccatgctgcttccagtttgcaaggtggggtcccatcaaggttcagtgggagtggatctgggacagatttcactctcaccatcaacagcctgcaacgtgaagatcttgctacatactactgtcagcagacgtatggcaaccctccgtggacgttcggccaagggaccaaggtggagatcaaacgaggcggcggcggcagtggtggtggtggtagtggaggaggaggaagtgaggtgcagctggtggagtctgggggaggcttggtacagcctggggggtccctgagactctcctgtgcagcctctggattcacctttagcagctatgccatgagctgggtccgccaggctccagggaaggggctggagtgggtctcagctattagtggtagtggtggtagcacatactacgcagactccgtgaagggccggttcaccatctccagagacaattccaagaactcactgtatctgcaaatgaacagcctgggagccgaggacacggctgtgtattactgtgcatcaatctcctcccccgatgactactggggccagggaaccctggtcaccgtctcctcaactacaactccagcacccagaccccctacacctgctccaactatcgcaagtcagcccctgtcactgcgccctgaagcctgtcgccctgctgccgggggagctgtgcatactcggggactggactttgcctgtgatatctacatctgggcgcccttggccgggacttgtggggtccttctcctgtcactggttatcaccctttactgcaggttcagtgtcgtgaagagaggccggaagaagctgctgtacatcttcaagcagcctttcatgaggcccgtgcagactacccaggaggaagatggatgcagctgtagattccctgaagaggaggaaggaggctgtgagctgagagtgaagttctcccgaagcgcagatgccccagcctatcagcagggacagaatcagctgtacaacgagctgaacctgggaagacgggaggaatacgatgtgctggacaaaaggcggggcagagatcctgagatgggcggcaaaccaagacggaagaacccccaggaaggtctgtataatgagctgcagaaagacaagatggctgaggcctactcagaaatcgggatgaagggcgaaagaaggagaggaaaaggccacgacggactgtaccaggggctgagtacagcaacaaaagacacctatgacgctctgcacatgcaggctctgccaccaagatag3c1
‑
bbz
seqidno:37atggctctgcctgtgaccgccctgctgctgcctctggctctgctgctgcacgccgctcggcctgatattgtgatgacccagactccagccaccctgtctttgtctccaggggaaagagccaccctctcctgcagggccagtcagagcgctggcagtcaaagtgttagcagctacttagcctggtaccagcagaaacctggccaggctcccaggctcctcatcaatgatgcattcaacagggcccctggcatcccagccaggttcagtggcagtgggtctgggacagacttcactctcaccatcagcagcctagagcctgaagattttgcagtttattactgtctgcaccgtagcaactggcctcctttgttcactttcggcggggggaccaaggtggaaatcaaacgaggcggcggcggcagtggtggtggtggtagtggaggaggaggaagtcaggtgcagctggtgcagtctggggctgaggtgaagaagcctgggtcctcggtgaaggtctcctgcaaggcttctggaggcaccttcagcagatttgctatcagctgggtgcgacaggccccgggacaagggcttgagtggatgggagggatcatccctatctttggaacagcaagctacgcacagaagttccagggcagagccacgattaccgcggacgaatccacgagcacagcctacatggagctgagcagcctgagatctgaggacacggccgtgtatttctgtgcgagggggcatagtgggagctacacccttgactactggggccagggaaccctggtcaccgtctcctcaactacaactccagcacccagaccccctacacctgctccaactatcgcaagtcagcccctgtcactgcgccctgaagcctgtcgccctgctgccgggggagctgtgcatactcggggactggactttgcctgtgatatctacatctgggcgcccttggccgggacttgtggggtccttctcctgtcactggttatcaccctttactgcaggttcagtgtcgtgaagagaggccggaagaagctgctgtacatcttcaagcagcctttcatgaggcccgtgcagactacccaggaggaagatggatgcagctgtagattccctgaagaggaggaaggaggctgtgagctgagagtgaagttctcccgaagcgcagatgccccagcctatcagcagggacagaatcagctgtacaacgagctgaacctgggaagacgggaggaatacgatgtgctggacaaaaggcggggcagagatcctgagatgggcggcaaaccaagacggaagaacccccaggaaggtctgtataatgagctgcagaaagacaagatggctgaggcctactcagaaatcgggatgaagggcgaaagaaggagaggaaaaggccacgacggactgtaccaggggctgagtacagcaacaaaagacacctatgacgctctgcacatgcaggctctgccaccaagatag3e5
‑
bbz
seqidno:38atggctctgcctgtgaccgccctgctgctgcctctggctctgctgctgcacgccgctcggcctgatatcgtgatgacccagagccacaagttcatgagcaccagcatcggcgccagagtgagcatcacctgcaaggccagccaggacgtgaggaccgccgtggcctggtaccagcagaagcctggccagagccccaagctgctgatctacagcgccagctacagatacaccggcgtgcccgacagattcaccggcagcggcagcggcaccgacttcaccttcaccatcagcagcgtgcaggccgaggacctggccgtgtactactgccagcagcactacggcacccctccctggaccttcggcggcggcaccaagctggagatcaagggcggaggcggctccggcggcggcggctccggcggcggcggctccgaggtgcagctggtggagagcggcggcggcctggtgaagcccggcggcagcctgaagctgagctgcgaggccagcagattcaccttcagcagctacgccatgagctgggtgaggcagacccccgagaagagactggagtgggtggccgccatcagcggcggcggcaggtacacctactaccccgacagcatgaagggcaggttcaccatcagcagggacaacgccaagaacttcctgtacctgcagatgagctccctgagaagcgaggacaccgccatgtactactgcgccagacactacgacggctacctggactactggggccagggcaccaccctgaccgtgagcagcaccaggactacaactccagcacccagaccccctacacctgctccaactatcgcaagtcagcccctgtcactgcgccctgaagcctgtcgccctgctgccgggggagctgtgcatactcggggactggactttgcctgtgatatctacatctgggcgcccttggccgggacttgtggggtccttctcctgtcactggttatcaccctttactgcaggttcagtgtcgtgaagagaggccggaagaagctgctgtacatcttcaagcagcctttcatgaggcccgtgcagactacccaggaggaagatggatgcagctgtagattccctgaagaggaggaaggaggctgtgagctgagagtgaagttctcccgaagcgcagatgccccagcctatcagcagggacagaatcagctgtacaacgagctgaacctgggaagacgggaggaatacgatgtgctggacaaaaggcggggcagagatcctgagatgggcggcaaaccaagacggaagaacccccaggaaggtctgtataatgagctgcagaaagacaagatggctgaggcctactcagaaatcgggatgaagggcgaaagaaggagaggaaaaggccacgacggactgtaccaggggctgagtacagcaacaaaagacacctatgacgctctgcacatgcaggctctgccaccaagatag376.96
‑
bbz
seqidno:39levqvpedpvvalvgtdatlccsfspepgfslaqlnliwqltdtkqlvhsfaegqdqgsayanrtalfpdllaqgnaslrlqrvrvadegsftcfvsirdfgsaavslqvaapyskpsmtlepnkdlrpgdtvtitcssyqgypeaevfwqdgqgvpltgnvttsqmaneqglfdvhsilrvvlgangtysclvrnpvlqqdahssvtitpqrsptgavevqvpedpvvalvgtdatlrcsfspepgfslaqlnliwqltdtkqlvhsftegrdqgsayanrtalfpdllaqgnaslrlqrvrvadegsftcfvsirdfgsaavslqvaapyskpsmtlepnkdlrpgdtvtitcssyrgypeaevfwqdgqgvpltgnvttsqmaneqglfdvhsvlrvvlgangtysclvrnpvlqqdahgsvtitgqpmtfpasglndifeaqkiewhehhhhhh重组cd276蛋白氨基酸序列
seqidno:40ctggaggtgcaggtgcccgaggaccccgtggtggccctggtgggcaccgacgccaccctgtgctgcagcttcagccccgagcccggcttcagcctggcccagctgaacctgatctggcagctgaccgacaccaagcagctggtgcacagcttcgccgagggccaggaccagggcagcgcctacgccaaccgcaccgccctgttccccgacctgctggcccagggcaacgccagcctgcgcctgcagcgcgtgcgcgtggccgacgagggcagcttcacctgcttcgtgagcatccgcgacttcggcagcgccgccgtgagcctgcaggtggccgccccctacagcaagcccagcatgaccctggagcccaacaaggacctgcgccccggcgacaccgtgaccatcacctgcagcagctaccagggctaccccgaggccgaggtgttctggcaggacggccagggcgtgcccctgaccggcaacgtgaccaccagccagatggccaacgagcagggcctgttcgacgtgcacagcatcctgcgcgtggtgctgggcgccaacggcacctacagctgcctggtgcgcaaccccgtgctgcagcaggacgcccacagcagcgtgaccatcaccccccagcgcagccccaccggcgccgtggaggtgcaggtgcccgaggaccccgtggtggccctggtgggcaccgacgccaccctgcgctgcagcttcagccccgagcccggcttcagcctggcccagctgaacctgatctggcagctgaccgacaccaagcagctggtgcacagcttcaccgagggccgcgaccagggcagcgcctacgccaaccgcaccgccctgttccccgacctgctggcccagggcaacgccagcctgcgcctgcagcgcgtgcgcgtggccgacgagggcagcttcacctgcttcgtgagcatccgcgacttcggcagcgccgccgtgagcctgcaggtggccgccccctacagcaagcccagcatgaccctggagcccaacaaggacctgcgccccggcgacaccgtgaccatcacctgcagcagctaccgcggctaccccgaggccgaggtgttctggcaggacggccagggcgtgcccctgaccggcaacgtgaccaccagccagatggccaacgagcagggcctgttcgacgtgcacagcgtgctgcgcgtggtgctgggcgccaacggcacctacagctgcctggtgcgcaaccccgtgctgcagcaggacgcccacggcagcgtgaccatcaccggccagcccatgaccttccccgctagcggtctgaacgacatcttcgaggctcagaaaatcgaatggcacgaacatcatcaccatcaccat重组cd276蛋白核酸序列
[0125]
实施例4:cd276 car
‑
t细胞的制备和car阳性率测定1.pbmc分离与活化。
[0126]
采集志愿者外周血,用ficcol分离液分离获得pbmc,用含5% ab血清x
‑
vivo(lonza)培养基调整细胞密度为1x106/ml。预先用1ml含50ng/ml抗人cd3抗体(北京同立海元)和50ng/ml cd28抗体(北京同立海元)的包被液37℃ 2h孵育包被tc处理的6孔板,使用前除去包被液。将细胞以1ml/孔接种到已包被抗体的6孔板中,再加入100iu/ml的il2(北京双鹭),刺激培养48小时后病毒感染。
[0127]
2.病毒原液感染与培养。
[0128]
将活化后的t细胞调整为5x105/ml,在24孔板中分别加入1ml t细胞和1ml病毒原
液,每孔加1ul polybrene,32℃,2500rpm,离心1.5h。弃去上清液,每孔加入1ml t细胞培养基(含il
‑
2 100iu/ml)。将培养板置于37℃,5% co2培养箱中培养。感染后24h,转至6孔板,每天观察细胞的密度,适时补加含il
‑
2 100iu/ml的t细胞培养液,使t细胞的密度维持在1x106/ml左右,使细胞扩增。
[0129]
3.car阳性率检测。
[0130]
逆转录病毒感染的t淋巴细胞在病毒感染72h后检测car阳性率。针对含376.96、1c8、1h12、3c1和3e5克隆的嵌合抗原受体组和阴性未感染对照组nt,分别取1
×
106个细胞离心去除培养基,pbs洗细胞一次后100ul重悬置于流式上样管中(bd)。加入生物素
‑
标记的cd276抗原(1:400)四度孵育30分钟。pbs洗细胞一次后按推荐比例加入二抗brilliant violet 421链霉亲合素(biolegend)四度避光孵育30分钟。pbs洗细胞一次后200ul pbs重悬细胞并上机检测,car
‑
t阳性率流式分析结果如图6所示。
[0131]
实施例3:基于抗人cd276 car
‑
t细胞功能分析。
[0132]
1.抗人cd276 car
‑
t细胞cd107a表达分析。
[0133]
将含不同抗体克隆的car
‑
t细胞以及nt细胞分别与不同分组的靶细胞(cd276阳性表达的肾癌细胞系achn、肺癌细胞系a549和卵巢癌细胞系skov3)按1:1的效靶比(效应细胞和靶细胞均为3x105个)共孵育后,流式检测其cd107a表达情况来评价car
‑
t细胞在受到靶细胞刺激后的脱颗粒反应。将效应细胞和靶细胞混合置于37℃,5% co2培养箱中共孵育4小时后,流式检测各组样品中表达cd107a的细胞分别占cd3+细胞数的比例。cd107a表达的流式分析结果如图7所示。
[0134]
2.抗人cd276 car
‑
t细胞细胞因子分泌能力检测。
[0135]
将含不同抗体克隆的car
‑
t细胞以及nt细胞分别与不同分组的靶细胞(cd276阳性表达的细胞系achn、a549和skov3)按1:1的效靶比(效应细胞和靶细胞均为1x105个)共孵育24小时后,收集其上清,利用elisa(酶联免疫)方法检测ifn
‑
γ和il
‑
2的分泌情况。ifn
‑
γ检测采用bd ifn
‑
γ和il
‑
2试剂盒检测,实验步骤依据产品说明书进行。ifn
‑
γ分泌的检测结果如图8所示。il
‑
2分泌的检测结果如图9所示。
[0136]
3.抗人cd276 car
‑
t细胞毒性实验。
[0137]
car
‑
t杀伤毒性实验通过检测car
‑
t细胞体外对靶细胞的杀伤效果来评估car
‑
t细胞的体外功能。以不同效靶比(以3x104个靶细胞为基准,效靶比分别为20:1, 10:1, 5:1和2.5:1)将t细胞分别与稳定表达萤火虫荧光素酶的cd276阳性靶细胞achn
‑
luc
‑
gfp、a549
‑
luc
‑
gfp和skov3
‑
luc
‑
gfp,以及阴性靶细胞molm13
‑
luc
‑
gfp共同培养,同时设置靶细胞和未转染car元件t细胞混合的阴性对照组(nt)。过夜孵育后在培养体系中加入萤光素酶反应底物,检测荧光值,通过以下公式计算杀伤效率:杀伤效率=(1
‑
实验孔荧光值/对照孔荧光值)x100%。实验分组及分析结果如图10所示。
[0138]
以上结果表明,本发明专利提供的靶向cd276的car
‑
t细胞同对照鼠源car一样,都具有很强的免疫功能,表现为较优的cd107a表达、ifn
‑
γ和il
‑
2分泌以及对靶细胞的特异性杀伤功能。以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1