靶向人APC蛋白的多肽及其在制备药物中的应用
靶向人apc蛋白的多肽及其在制备药物中的应用
技术领域
1.本发明涉及生物医药领域,更具体地,本发明涉及靶向人apc蛋白的多肽及其在制备治疗结直肠癌和家族性腺瘤性息肉病的药物中的应用。
背景技术:
2.结直肠癌(colorectal carcinoma,crc)是人类常见的恶性肿瘤,亦是我国最常见的恶性肿瘤之一,其死亡率位居前列。根据国家癌症中心公布的最新数据,2015年我国新发的结直肠癌病例达38.76万人,约占全部恶性肿瘤发病的9.87%;而由结直肠癌导致的死亡病例达18.71万人,约占全部恶性肿瘤死亡的8%,造成了严重的社会负担。
3.结直肠癌主要分为散发性和家族性两种,绝大部分结直肠癌为散发性结直肠癌。家族性腺瘤性息肉病(familial adenomatous polyposis,fap)约占全部结直肠癌的1%。fap发病率大概是每30,000人群中可有1人患fap。典型的fap主要临床表现为:结肠及直肠遍布数目超过100个以上的腺瘤性息肉和微腺瘤。约90%的fap患者在30岁前可见息肉,且随着息肉体积和数量的增长导致大部分患者产生血便、排便习惯改变、腹痛及消瘦等症状。如不及早进行手术干预,fap发展为结直肠癌的概率为100%,癌变的平均年龄为40岁。
4.由于结直肠癌发病隐匿,早期诊断困难,多数结直肠癌患者在初诊时已出现淋巴转移或远处器官转移,是造成死亡的最主要原因之一。对于不可手术切除的晚期及复发性结直肠癌,以氟尿嘧啶+铂类为基础的化疗仍是主要的姑息治疗手段,且有效率低。近年来,虽然西妥昔单抗、贝伐单抗、曲妥珠单抗、阿帕替尼等靶向药物及免疫治疗在一定程度上提高了结直肠癌患者的生存预后,但仅有少部分患者获益。因此,亟需探索新的治疗策略和靶点让更多患者收益。
5.众所周知,结直肠癌的发生发展是一个多分子异常、多阶段进展的复杂过程。目前已公认:apc(adenomatous polyposis coli)基因突变导致其蛋白功能异常或其表达异常是结直肠癌“腺瘤-腺癌”恶性进展的关键引发步骤。其中,apc基因的胚系突变可导致fap;而体细胞性突变与80%以上的散发性结直肠腺瘤和结直肠癌的发生及预后有密切关系。并且apc基因研究早期阶段发现的小鼠动物模型同样确证了apc基因突变在fap和结直肠癌发病和进展中的驱动作用。
6.apc基因定位在5号染色体的q21-22区段,编码蛋白含有2843个氨基酸,蛋白质分子量达311.8kd并含有多个结构域。apc蛋白的经典作用是wnt信号转导通路中的关键负性调节因子。其与轴蛋白(axin)、gsk3β等组成复合物结合并抑制β-连环蛋白(β-catenin)的稳定性。95%apc的突变是导致其翻译提前终止,表达截断型apc蛋白的无义突变。这种截断型蛋白没有β-连环蛋白和轴蛋白的结合位点以及gsk3磷酸化位点,导致细胞内β-连环蛋白水平升高并促进肿瘤形成。另外,apc蛋白可通过与肌动蛋白及细胞黏附分子相关蛋白α-连环蛋白及β-连环蛋白等结合直接调控细胞的运动、黏附能力进而调节细胞的生长、分化及染色体稳定性。
7.多项研究发现,apc基因突变可导致细胞的黏附能力减弱并促进结直肠癌细胞转
移;过表达截断型apc蛋白可促进结直肠癌细胞的迁移能力,而抑制截断型apc蛋白或抑制其与相互作用的蛋白如asef结合可以显著降低结直肠癌细胞的迁移转移能力。这提示截断型apc蛋白不仅是导致了与β-连环蛋白、肌动蛋白等蛋白失去结合能力的功能缺失(loss-of-function)蛋白,同时很可能是获取新功能(gain-of-function)并发挥重要促癌调控作用的蛋白。因此,靶向截断型apc蛋白很可能是结直肠癌治疗的新策略和重要靶点。但目前尚无较强的系统性阻断截断型apc蛋白分子功能的研究及低毒性药物报道。
8.近年来,在抗肿瘤药物方面,靶向多肽因具有亲和力高、特异性强、毒副作用少及容易合成等特点,一直是肿瘤治疗领域的研究热点。多肽体积小、结构简单、但通常具有与天然蛋白/抗体类似的生物学功能。相比抗体识别、靶向多肽穿透性强、免疫原性低、易于化学合成与修饰、批次重复性高。目前尚无可靶向截断型apc蛋白的多肽研究报道。
9.因此,本领域亟需一种毒性副作用小、特异性强的靶向截断型apc蛋白的药物以用于治疗结直肠癌和家族性腺瘤性息肉病。
技术实现要素:
10.有鉴于此,本发明提供了一种毒性副作用小、特异性强的靶向截断型apc蛋白的多肽,从而有效抑制结直肠癌细胞的成瘤性和增殖能力。
11.本发明人系统回顾检索总结了截断型apc蛋白的报道,发现截断型apc蛋白是一种核浆穿梭蛋白。由于正常定位是蛋白发挥其生物学功能的重要前提条件,发明人根据影响apc蛋白定位的氨基酸位点,设计了多条可以特异性扰乱截断型apc蛋白出核或正常定位过程的多肽,从而抑制结直肠癌细胞的成瘤性和增殖能力。
12.因此,在第一方面,本发明提供了一种靶向人apc蛋白的多肽,所述多肽包含seq id no:1所示的人apc蛋白第68-74位的氨基酸序列(seq id no:7)并且其余氨基酸在存在的情况下与人apc蛋白的氨基酸序列完全匹配,所述多肽由7-25个氨基酸组成,优选由10-25个氨基酸组成,更优选由12-23个氨基酸组成。
13.在第二方面,本发明提供了一种融合多肽,所述多肽包含本发明第一方面所述的靶向人apc蛋白的多肽,以及跨膜肽。
14.在第三方面,本发明提供了一种药物组合物,所述药物组合物包含:(1)本发明第一方面所述的靶向人apc蛋白的多肽、或者本发明第二方面所述的融合多肽,以及(2)药学上可接受的载体。
15.在第四方面,本发明提供了本发明第一方面所述的靶向人apc蛋白的多肽、或者本发明第二方面所述的融合多肽在制备用于治疗结直肠癌、直结肠癌转移和/或家族性腺瘤性息肉病的药物中的用途,其中,所述结直肠癌、直结肠癌转移和/或家族性腺瘤性息肉病中存在有apc基因突变。
16.本发明的有益效果为:本发明提供了一种靶向人apc蛋白的多肽,该多肽可以扰乱截断型apc蛋白出核或正常定位过程,从而抑制结直肠癌细胞的成瘤性和增殖能力。本发明的多肽毒性副作用小、特异性强,因此可用于制备治疗直肠癌和/或家族性腺瘤性息肉病的发病和转移的药物。
附图说明
17.为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的实施方案。
18.图1显示了敲除内源性突变的apc基因可以显著抑制结肠癌细胞在裸鼠上的成瘤性和增殖能力。其中,图1a为通过crispr/cas9方法敲除肿瘤细胞sw480和dld-1细胞株中的apc基因的示意图;图1b为通过蛋白质印迹法检测的不同克隆的apc蛋白表达结果图;图1c示出了sw480细胞株在裸鼠中的形成的皮下瘤的大小和he染色切片;图1d示出了dld-1细胞株在裸鼠中的形成的皮下瘤的大小和he染色切片。nc:阴性对照;ko:敲除;c1、c2、c3和c4分别表示不同的经apc基因敲除的细胞株。
19.图2显示了发明人设计的多条靶向人apc蛋白的多肽(trunapc-neip1、trunapc-neip2、trunapc-neip3、trunapc-neip4、trunapc-neip5、trunapc-neip6)以及trunapc-neip1 mut(其中trunapc-neip1的亮氨酸突变为丙氨酸)的免疫荧光实验结果。nc:阴性对照。实验结果显示trunapc-neip 1可以导致截断型apc蛋白不能均匀分布在胞浆,而聚集在核周。而将trunapc-neip1中的亮氨酸突变为丙氨酸(trunapc-neip1 mut)则会明显减弱trunapc-neip 1的出核阻断功能。将trunapc-neip1氨基酸从两端缩短(序列trunapc-neip3至trunapc-neip5)则导致其阻断效果较trunapc-neip1减弱,而增加trunapc-neip 1两端的氨基酸长度(序列trunapc-neip6,apc蛋白的第58-80位氨基酸)并未提高其阻断效果。
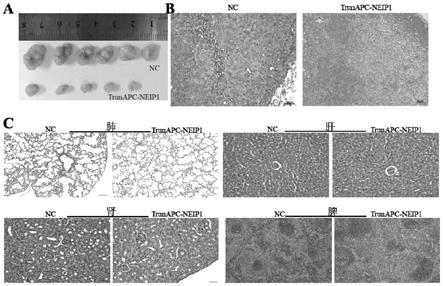
20.图3显示了尾静脉注射trunapc-neip1多肽对结肠癌细胞在裸鼠上的增殖能力的影响及多肽对裸鼠重要脏器的影响。其中,图3a示出了结直肠癌细胞的裸鼠模型中皮下瘤的大小;图3b为结直肠癌细胞的裸鼠模型中皮下瘤的he染色切片图;nc:阴性对照。图3c是小鼠重要脏器细胞(肺、肝、肾和脾)的he染色切片结果图。实验结果显示尾静脉注射trunapc-neip1多肽对小鼠重要脏器无明显损伤。
具体实施方式
21.下面将结合本发明的实施方案和附图,对本发明进行清楚、完整的描述。显然,所描述的实施方案仅仅是本发明的一部分实施方案,而不是全部的实施方案。基于本发明中的实施方案,本领域普通技术人员可以获得的所有其他实施方案,都属于本发明保护的范围。
22.如上所述,本发明旨在提供一种毒性副作用小、特异性强的靶向截断型apc蛋白的多肽,其可以有效抑制结直肠癌细胞的成瘤性和增殖能力,从而可用于制备治疗直肠癌和/或家族性腺瘤性息肉病的发病和转移的药物。
23.如背景技术部分所述,所谓“家族性腺瘤性息肉病”是指一种常染色体显性遗传性疾病,其临床病症主要表现为整个结直肠(大肠)布满大小不一的腺瘤。病人在出生时并无结直肠息肉,多在15岁前后出现息肉,初起时息肉为数不多,随着年龄增长而增多。可出现腹部不适、腹痛、大便带血或带黏液、大便次数增多等症状。fap患者的大肠息肉为腺瘤性息肉,属癌前病变,如不及时治疗,终将100%发生癌变。
24.结直肠的癌前损害通过原癌基因或抑癌基因的遗传学改变而发展为肿瘤,该过程为“腺瘤-腺癌”过程。apc基因是结直肠癌抑癌基因,但apc基因突变导致其蛋白功能异常或其表达异常是引发结直肠癌“腺瘤-腺癌”恶性进展的关键步骤。其中,apc基因的胚系突变可导致fap,而体细胞性突变驱动了大部分散发性结直肠腺瘤和结直肠癌的发生及恶性进展。
25.研究报道apc基因突变产生的截断型apc蛋白是一个核浆穿梭蛋白,用出核阻断剂来普霉素b(leptomycin b,lmb)处理后可显著抑制截断型apc蛋白的出核。由于正常定位是蛋白发挥其生物学功能的重要前提条件,发明人想通过阻断截断型apc蛋白出核,来达到阻断其生物学功能的目的。但发明人用lmb处理细胞时发现,该抑制剂的细胞毒性较大,且特异性不强,不利于开展动物体内实验和临床转化。因此,发明人根据影响apc蛋白定位的氨基酸位点,设计了多条可以特异性扰乱截断型apc蛋白出核或正常定位过程的多肽。
26.因此,在第一方面,本发明提供了一种靶向人apc蛋白的多肽,所述多肽包含人apc蛋白第68-74位的氨基酸序列(seq id no:7)与人apc蛋白的氨基酸序列完全匹配,所述多肽由7-25个氨基酸组成。
27.在一个优选的实施方案中,所述多肽由10-25个氨基酸组成。在一个更优选的实施方案中,所述多肽由12-23个氨基酸组成。
28.本说明书中的“靶向多肽”是指针对特定的生物靶标具有特异性亲和作用的肽分子。多肽由几个到几十个结构、性质、功能各异的氨基酸按照一定的顺序通过酰胺键连接而成。
29.发明人选取了多个包含人apc蛋白的部分氨基酸序列的多肽片段进行免疫荧光实验,所述多肽片段包括以下序列:
30.·
人apc蛋白(seq id no:1)第67-78位(trunapc-neip1)的氨基酸序列(seq id no:2);
31.·
人apc蛋白(seq id no:1)第164-175位(trunapc-neip2)的氨基酸序列(seq id no:4);
32.·
人apc蛋白(seq id no:1)第68-77位(trunapc-neip3)的氨基酸序列(seq id no:6);
33.·
人apc蛋白(seq id no:1)第70-77位(trunapc-neip4)的氨基酸序列(seq id no:8);
34.·
人apc蛋白(seq id no:1)第68-74位(trunapc-neip5)的氨基酸序列(seq id no:7);以及
35.·
人apc蛋白(seq id no:1)第58-80位(trunapc-neip6)的氨基酸序列(seq id no:9)。
36.发明人发现trunapc-neip1、trunapc-neip3、trunapc-neip4、trunapc-neip5、trunapc-neip6都可以导致截断型apc蛋白不能均匀分布在胞浆,而聚集在核周,其中trunapc-neip1和trunapc-neip6的效果最佳。此外,trunapc-neip1在两种动物模型中均可以显著抑制人结直肠癌细胞的增殖及小鼠肠道腺瘤的形成。经过多次实验,发明人发现并认为其中最为关键的是人apc蛋白的第68、69、72、75和77位的亮氨酸。并且多肽中其余的氨基酸在存在的情况下必须与人apc蛋白的氨基酸序列完全匹配,因为该多肽为阻断型多肽,
目的是阻断人apc蛋白该片段与结合分子的作用,该作用是序列依赖性的,若序列不匹配,则会影响阻断效果。
37.发明人发现多肽片段的大小最优选为12个氨基酸(即,trunapc-neip1),因为将trunapc-neip1氨基酸序列从两端缩短后会降低其出核阻断功能的效果,而增加trunapc-neip1的长度并未提高其效果但却增加了生成成本。此外,如果多肽片段过长,其生成时长和生成难度均会增加,并且可能会产生新的二级机构反而干扰其核心肽段的作用。
38.因此,在一个实施方案中,所述多肽由seq id no:2所示的氨基酸序列组成。
39.在第二方面,本发明提供了一种融合多肽,所述多肽包含本发明第一方面所述的靶向人apc蛋白的多肽,以及跨膜肽。
40.本说明书中的“跨膜肽”是指一类具有跨细胞膜转运功能的多肽。通过将治疗性多肽与跨膜肽相结合是提高治疗性多肽通过细胞膜的一种有效方法。
41.在一个具体实施方案中,所述跨膜肽可以为seq id no:3所示的跨膜肽。
42.本发明的多肽,包括融合多肽在内,可人工合成,也可先合成其编码基因,再进行生物表达得到。
43.在第三方面,本发明提供了一种药物组合物,所述药物组合物包含:(1)本发明第一方面所述的靶向人apc蛋白的多肽、或者本发明第二方面所述的融合多肽,以及(2)药学上可接受的载体。
44.在第四方面,本发明提供了本发明第一方面所述的靶向人apc蛋白的多肽、或者本发明第二方面所述的融合多肽在制备用于治疗结直肠癌、直结肠癌转移和/或家族性腺瘤性息肉病的药物中的用途,其中,所述结直肠癌和/或家族性腺瘤性息肉病中存在有apc基因突变。
45.在一个实施方案中,所述药物为注射制剂。
46.综上所述,本发明提供了一种靶向人apc蛋白的多肽,该多肽可以扰乱截断型apc蛋白出核或正常定位过程,从而抑制结直肠癌细胞的成瘤性和增殖能力。本发明的多肽毒性副作用小、特异性强,因此可用于制备治疗直肠癌和/或家族性腺瘤性息肉病的发病和转移的药物。
47.实施例
48.发明人首先选取两株apc基因突变且产生截断型apc的常用crc细胞系sw480和dld-1,通过crispr/cas9方法敲除结直肠癌细胞系sw480和dld-1内源性突变的apc基因,并建立稳定细胞株,然后进行裸鼠皮下瘤实验,以明确突变型apc基因及其产生的截断型apc蛋白的功能。
49.实施例1.突变型apc基因及其产生的截断型apc蛋白的功能
50.1)细胞:本实验中所用人结肠癌细胞系sw480及dld-1均购自美国模式培养物集存库(american type culture collection,atcc),使用含10%胎牛血清的rpmi1640培养基,于5%co2、37℃的恒温培养箱中培养。sw480及dld-1细胞均具有内源性apc基因突变(分别在第1338和1427位氨基酸处发生突变),并产生截断型apc蛋白。
51.2)crispr/cas9方法敲除apc基因:利用http://crispr.mit.edu/在线设计单导rna(single-guide rnas,sgrna),sgrna-1序列为:ccggcttccataagaacgga,sgrna-2序列为cgttcttatggaagccggga。经过酶切及连接,将此sgrna序列克隆入lenticrispr v2质粒
(52961,购自addgene),由此构建好用于敲除细胞中apc基因的敲除载体。图1a示出了sgrna-1和sgrna-2在apc基因上的作用位点。然后,用lipofectamine 2000(invitrogen)转染apc基因敲除载体及对照空载体进入sw480及dld-1细胞,用2μg/ml为终浓度的嘌呤霉素处理细胞两周。之后,将细胞转至96孔板进行单细胞培养,3周后提取单细胞培养的细胞,并用蛋白质印迹法检测apc蛋白的表达情况。
52.图1b通过蛋白质印迹法的检测结果。从该图中可以看出,无论是sw480细胞还是dld-1细胞,其阴性对照组(nc)均正常地表达出apc蛋白,而在四个基因敲除的细胞克隆中,未见apc蛋白的表达或apc蛋白的表达显著降低。选取apc基因被成功敲除的克隆继续扩大培养用于后续实验。
53.3)裸鼠皮下瘤实验:裸鼠购自北京维通利华公司,周龄为3-4周,雌雄不限,每组实验6只。扩大培养所需细胞,即转入空载的sw480和dld-1细胞及稳定敲除apc基因的单克隆株细胞,取对数生长期的细胞用0.25%胰酶消化,并用pbs洗两遍以去除含血清培养基。对所得细胞计数,用无血清培养基重悬细胞浓度至4
×
106个细胞/0.1ml,然后注射至裸鼠后肢背面的皮下。每周观察2-3次。三周后或若实验过程中发现肿瘤长径接近2cm,则脱臼处死小鼠,然后取出皮下瘤拍照,然后进行10%福尔马林固定、石蜡包埋、切片。
54.图1c为在裸鼠中注射肿瘤细胞sw480而形成的肿瘤的照片,以及相应的he染色切片的照片,图1d为在裸鼠中注射肿瘤细胞dld-1而形成的肿瘤的照片,以及相应的he染色切片的照片。从这些图中可以看出,在nc组中,即在没有敲除apc基因的细胞注射的裸鼠中,形成了体积相对较大的肿瘤;而在apc基因被敲除的情况下,形成的肿瘤体积大大下降,甚至肿瘤消失(在apc基因被敲除的dld-1细胞处理组中)。在he染色切片中,nc组呈现出大量增殖的细胞,而在基因敲除的sw480细胞处理组中,可以看到细胞增殖受到很大影响。
55.以上实验结果表明,敲除突变型apc基因,可显著抑制结直肠癌细胞在裸鼠中的成瘤性及增殖能力。
56.实施例2.靶向人apc蛋白的多肽的合成
57.通过实施例1的结果可以知晓,截断型apc蛋白会导致结直肠癌。因此,为寻找阻断截断型apc蛋白发挥作用的方法,发明人根据截断型apc蛋白是核浆穿梭蛋白的特性,想到通过抑制apc蛋白的出核来影响蛋白的生物学功能。
58.为此,发明人根据影响apc蛋白定位的氨基酸位点,设计了多条有可能特异性扰乱截断型apc蛋白出核或正常定位过程的多肽。
59.靶向人apc蛋白的多肽的序列如下:
60.trunapc-neip1:人apc蛋白的第67-78位氨基酸,序列为dllerlkelnld;
61.trunapc-neip2:人apc蛋白的164-175位氨基酸,序列为nltkridslplt;
62.trunapc-neip1 mut:将trunapc-neip1中的亮氨酸全部突变为丙氨酸,序列为daaerakeanad。
63.trunapc-neip3:人apc蛋白的第68-77位氨基酸,序列为llerlkelnl;
64.trunapc-neip4:人apc蛋白的第70-77位氨基酸,序列为erlkelnl;
65.trunapc-neip5:人apc蛋白的第68-74位氨基酸,序列为llerlke;
66.trunapc-neip6:人apc蛋白的第58-80位氨基酸,序列为eamassgqidllerlkelnldss
67.为了促进这些多肽进入到细胞内与apc蛋白相互作用,还在上述多肽的c端均添加了跨膜肽序列crgdkgpdc,并且将跨膜肽序列自身作为对照多肽(nc:阴性对照)。
68.上述多肽均由中国金斯瑞生物科技股份有限公司合成,测定其溶解性,合成纯度大于95%。第一次使用时:用dmso溶解多肽粉末至最大浓度,然后用生理盐水稀释至所需浓度。药物避免反复冻融,于-80℃冰箱保存。
69.实施例3.本发明多肽对截断型apc蛋白定位的影响
70.在本实施例中,通过免疫荧光观察多肽对截断型apc蛋白定位的影响。
71.取对数生长期状态良好的dld-1细胞,常规胰酶消化后铺板在共聚焦玻璃小皿中,按照细胞培养皿与共聚焦小皿的面积比例,计算所需铺板细胞数,目的是包装铺板后小皿的细胞密度《50%,从而有利于观察细胞形态。待细胞贴壁并恢复正常形态后,在常规培养基中加入多肽,终浓度为5μg/0.2ml。24小时后弃掉培养基,pbs洗脱后用4%多聚甲醛室温固定15分钟,弃掉固定剂后加入0.5%triton x-100,4℃破膜10分钟。后续按照常规免疫荧光的步骤封闭、孵育一抗、二抗、dapi染核及洗脱,加入适量50%甘油防止荧光淬灭。apc抗体购自abcam(ab16794),稀释比例为1:100。完成后即于激光共聚焦显微镜下观察并拍照。
72.图2示出了实验结果。从该图中可以发现:trunapc-neip2(第164-175位氨基酸)对截断型apc蛋白的定位几乎没有影响,截断型apc蛋白分布与对照组(nc)中分布非常相似,两者均广泛地分布在胞浆中,而trunapc-neip1(第67-78位氨基酸)却导致截断型apc蛋白凝集在核周,不能广泛分布在胞浆,说明该多肽可以有效地防止截断型apc蛋白出核;而亮氨酸突变为丙氨酸的trunapc-neip1 mut却失去了上述的防止出核功能。将trunapc-neip1氨基酸从两端缩短(序列trunapc-neip3至trunapc-neip5)则导致其阻断效果较trunapc-neip1减弱,而增加trunapc-neip1两端的氨基酸长度(trunapc-neip6序列,apc蛋白的第58-80位氨基酸)并未提高其阻断效果。因此,发明人认为trunapc-neip1对截断型apc蛋白定位有着显著影响,并且其中的亮氨酸可能起到重要作用。
73.实施例4.本发明多肽的抑癌作用
74.进一步地,通过dld-1细胞的裸鼠皮下瘤实验检测本发明多肽的抑癌效果。
75.采用购自北京维通利华公司的裸鼠,年龄为3周-4周,雌雄不限,每组实验6只。取无血清培养基重悬的dld-1细胞(浓度为4
×
106个细胞/0.1ml),注射至裸鼠后肢背面的皮下。待皮下瘤肉眼可见长出后,按照5mg/kg体重尾静脉注射c端添加了跨膜肽的trunapc-neip1或作为阴性对照的跨膜肽,浓度为75μg/200μl,每周两次,连续注射三周。每次注射前测量肿瘤的长短径。若实验过程中发现肿瘤长径大于2cm,即脱臼处死小鼠终止实验。处死小鼠后,取出皮下瘤及重要脏器,包括心、肝、肺、肾,进行大体组织拍照后及时10%福尔马林固定、石蜡包埋、切片。观察皮下瘤及重要脏器的he染色,看是否有重要脏器的损伤。
76.图3a为给具有皮下瘤的裸鼠中注射trunapc-neip1多肽后的肿瘤照片,图3b为相应的he染色切片的照片。在nc组中,即仅注射了跨膜肽的裸鼠中,形成了体积相对较大的肿瘤;而在注射trunapc-neip1多肽情况下,形成的肿瘤体积显著下降。在he染色切片中,nc组呈现出大量增殖的细胞,而在注射trunapc-neip1多肽的实验组中,可以看到细胞增殖受到很大影响。
77.以上实验结果表明,trunapc-neip1可明显抑制结直肠癌细胞的裸鼠皮下增殖能力,并且多肽的生物学毒性低。因此,本发明的多肽在制备用于治疗结直肠癌和家族性腺瘤
性息肉病的发生及转移的药物中,有很好的临床转化前景。
78.表1.序列表
79.80.
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1