一种全封闭无污染的数字化核酸检测芯片及检测方法
1.本发明属于微流控液滴数字聚合酶链式反应技术领域,具体属于一种全封闭无污染的数字化核酸检测芯片及检测方法。
背景技术:
2.随着医疗模式的转变和个体化用药的不断发展,医学检验界迫切地需要快速、精确的检测手段,分子检测则发挥出独特的优势。目前,分子检测技术主要有核酸分子杂交、聚合酶链式反应(pcr)和生物芯片技术等,分子检测产品主要应用在肿瘤、感染、遗传、产前筛查等临床各科的检测,以及体检中心、技术服务中心、第三方检测机构及微生物快速检测市场等方面,并在新型冠状病毒的检测中起到重要的作用。数字pcr(digital pcr,dpcr)技术是基于单分子pcr方法来进行计数的核酸定量,是一种核酸分子扩增及绝对定量的技术。基于液滴微流控技术的液滴数字pcr,由于具备:更容易提供小体积、高通量的微反应器等优点,受到广泛地关注。
3.微液滴数字pcr系统工作原理是:首先通过特殊的微液滴生成仪将待测样品均分到大量纳升级(直径为数微米到数百微米)的“油包水”微液滴中,微液滴的数量在百万级别。由于微液滴数量足够多,微液滴之间被油层相互隔离,因此每个微液滴相当于一个“微型反应器”,微液滴中只含有待测样品的dna单分子;然后,针对这些微液滴分别进行pcr扩增反应,并通过微液滴分析仪逐个对液滴的荧光信号进行检测,有荧光信号的微滴判读为1,没有荧光信号的微滴判读为0。最后,根据泊松分布原理及阳性微滴的个数与比例即可得出待测样品的目标dna分子数目,实现对核酸样本的绝对定量。微液滴样品荧光信号的判定依赖一个核心技术:微液滴荧光检测装置的设计和加工,利用激光激发微液滴内产物的荧光信号高低来区分阴性微液滴和阳性微液滴。
4.目前常见的仪器如bio
‑
rad qx200
tm
结合了油包水乳化微滴技术与微流体技术,借助微滴发生器,可将每个样品生成20000个均一的纳升级微滴,目的片段和背景序列在微滴中随机分布,每个微滴都是一个独立的反应器。在使用热循环仪进行pcr后,qx200微滴分析仪将逐个分析每个样品中的液滴。微滴被吸入后,在鞘液油的作用下依次通过一个双色光学检测系统。系统将计算阳性和阴性微滴的数量,从而以数字格式对靶dna进行绝对定量分析。
5.就数字pcr检测仪的微液滴观测而言,采用液滴阵列显微成像方式,可以清晰获取所有液滴的形态,降低非特异性扩增等干扰因素,提高检测结果的可靠性,但同时由于需要将生成的液滴进行转移、平铺,促使液滴转移、平铺的传统方式是利用一些如负压泵等外围驱动部件或驱动结构来产生负压或正压,而移液过程不仅增加了操作过程,耗费时间,同时还存在污染液滴的可能,最终导致结果的不准确性,因此设计制作一种可实现自动化全封闭无污染的一体化检测芯片及其系统显得尤为关键。
6.专利文献cn109536380a(一种核酸高灵敏检测的液滴微流控芯片及其使用方法)公开了一种核酸高灵敏检测的液滴微流控芯片及其使用方法,其发明进行功能区分隔,在
独立的区域内分别完成数字pcr的三环节,液滴制备,pcr扩增及平铺统计技术。由于其液滴制备、pcr扩增及平铺统计区域在同一平面内,因此芯片的面积较大,大大降低检测通量;其液滴制备过程在实践中较难实现,且不易控制生成液滴的尺寸;在扩增及转移部分的结构复杂,难以达到严格密封;对于油相要求较高,需要使用两种互不相溶且不影响后续反应和观测结果的油相,不仅增加了实验难度,而且增加了实验成本。
技术实现要素:
7.为了解决现有技术中存在的问题,本发明提供一种全封闭无污染的数字化核酸检测芯片及检测方法,解决目前液滴的移液操作复杂,耗费时间易产生交叉污染的问题。
8.为实现上述目的,本发明提供如下技术方案:一种全封闭无污染的数字化核酸检测芯片,包括芯片本体、第一穿刺针和第二穿刺针,所述芯片本体为透明材质,所述芯片本体上设有若干个进油通孔,进油通孔的出口连接进油槽,所述进油槽上连接有第一穿刺针的一端开口,第一穿刺针的另一端开口伸入试管中,所述试管用于接收进油通孔输送的油相,第二穿刺针的一端开口连接在芯片本体内腔中开设的进液槽内,所述进液槽的出口连接有平铺腔室,所述平铺腔室的底部平面处于水平方向,所述第二穿刺针的另一端开口伸入试管中;
9.第一穿刺针的另一端开口始终伸入试管中的油相内,在油相充满试管时,第二穿刺针的另一端开口接触油相的顶部液面。
10.进一步的,所述芯片本体包括依次层叠的第一芯片、第二芯片和第三芯片,所述第一芯片上的第一连接面用于连接第二芯片,第一连接面上开设有进油槽和进液槽,所述进油槽的一侧壁连通至进油通孔的侧壁,进油通孔贯通第二芯片和第三芯片,所述进油槽同轴连通有出油通孔,所述出油通孔贯通第二芯片和第三芯片,出油通孔和第一穿刺针过盈配合;所述进液槽的一侧壁连通有平滑流道,所述平滑流道的出口连通至平铺腔室,所述平滑流道的入口直径到出口直径由微液滴直径3~5倍逐渐减少,所述进液槽同轴连通有进液通孔,所述进液通孔贯通第二芯片和第三芯片,进液通孔和第二穿刺针过盈配合,所述平铺腔室的面积为试管中总微液滴单层平铺面积的1.2倍。
11.进一步的,所述第一芯片、第二芯片和第三芯片上还贯通有排气通孔,所述平铺腔室的末端连通至排气通孔的侧壁上,所述平铺腔室末端的直径小于微液滴的直径;
12.所述第三芯片的内腔中设有废液腔,所述废液腔的入口连通排气通孔的一端。
13.进一步的,所述第三芯片上的第二连接面用于连接试管,所述第二连接面上设有卡位薄壁,所述卡位薄壁用于卡合试管的试管上盖,所述进油通孔和出油通孔位于卡位薄壁围合的区域内,所述第二连接面上一体成型有帽盖,所述进油通孔和出油通孔上均同轴连接有帽盖,所述帽盖为凸起结构,所述帽盖与第一穿刺针和第二穿刺针均为过盈配合,所述帽盖和卡位薄壁均为硅胶材质。
14.进一步的,所述第一连接面上还一体化有平铺腔支撑柱,所述平铺腔支撑柱和第二芯片接触。
15.进一步的,由第二芯片到第一芯片方向,所述平铺腔室的高度为微液滴直径的0.5~2倍;
16.所述平滑流道的入口直径为1mm,所述平滑流道的出口直径为0.3mm,所述平滑流
道入口处的高度为0.3mm,平滑流道的出口处的高度为0.1mm。
17.进一步的,所述第一芯片上还一体化有若干个定位标记,所述定位标记位于相邻平铺腔室之间,同一平铺腔室之间相邻的定位标记的形状不一致。
18.进一步的,所述第一穿刺针和第二穿刺针为长穿刺针或短穿刺针,所述长穿刺针的开口距离试管开口的距离大于短穿刺针的开口到试管开口的距离;
19.所述长穿刺针和短穿刺针的一端开口均与第一连接面平齐,所述长穿刺针和短穿刺针的一端开口上均一体成型有凸台,凸台均顶压在第一芯片的壁面上。
20.进一步的,还包括供油装置和底部支座,所述供油装置的出口连接有橡皮管,所述橡皮管和进油通孔过盈配合;
21.所述底部支座上设有试管凹槽,所述试管凹槽用于放置试管,所述底部支座上还一体成型有支柱;
22.当芯片本体的底部放置底部支座时,支柱和芯片本体的底部壁面接触。
23.本发明还提供一种全封闭无污染的数字化核酸芯片的检测方法,包括以下步骤:
24.装有微液滴的试管固定在芯片本体上,第一穿刺针伸入试管内,进油通孔接入油相,油相经过进油通孔进入进油槽,进油槽内的油相经过第一穿刺针进入试管内,微液滴浮于油相的液面处;
25.待油相充满试管内腔时,油相的液面接触第二穿刺针,油相持续由第一穿刺针进入试管,油相液面上的微液滴被推入第二穿刺针,微液滴依次经过第二穿刺针、进液槽和平铺腔室,微液滴不断进入平铺腔室,逐步完成平铺,平铺完成后,将芯片本体移至光学检测平台进行检测;
26.经光学检测平台得到检测图像,对多个图像进行拼接和增强处理,得到原始核酸拷贝数及置信区间,完成数字化核酸芯片检测。
27.与现有技术相比,本发明至少具有以下有益效果:
28.本发明提供一种全封闭无污染的数字化核酸检测芯片,将透明材质作为芯片本体,便于实时观测,通过在芯片本体上开设进油通孔和进油槽以及第一穿刺针,实现油相进入带有微液滴的试管中,其中微液滴的密度小于油相的密度,微液滴会一直处于油相的液面处,因此,在油相充满试管时,油相持续充入试管中,油相液面上的微液滴会被被动推入第二穿刺针中,经过出液槽进入平铺腔室,从而在平铺腔室中进行平铺,随后进行光学检测操作即可获得扩增后液滴的荧光信息,本发明将pcr扩增与后续检测独立开来,降低芯片复杂性,避免检测环节对pcr扩增缓解的反应通量的制约,能够快速、有效地促使液滴平铺,无需两种油相,芯片耗材较少,成本较低,特别是一体化芯片在移液过程中避免了开盖操作可能带来的交叉污染风险,操作简单,耗时短,并且相比流式检测可以观测微液滴状态,提高检测成功率和时效性,同时也可应用于蛋白或核酸,如pcr\lamp\rpa反应等技术,满足不同应用场合的分析需求。
29.进一步的,平滑流道的入口直径到出口直径均匀减少,使得进液槽和平铺腔室能够平滑连接,保证液滴顺利进入流道,避免液滴在流道内的挤压碰撞而导致液滴融合,避免了微液滴破裂或者严重变形,保证了移液后微液滴的质量。
30.进一步的,贯通第一芯片、第二芯片和第三芯片的排气通孔,便于排出气体,利于微液滴平铺过程。
31.进一步的,卡位薄壁能够更加紧密连接试管,帽盖能够更加紧密连接第一穿刺针和第二穿刺针,起到卡位和密封的作用。
32.进一步的,平铺腔支撑柱能够对平铺腔体进行支撑,避免热压键合出现塌陷,保证液滴平铺效果。
33.进一步的,平滑流道的直径以及高度设计能够保证生成特定体积的液滴,如直径20um~200um的液滴,微液滴的体积可控,而且平铺腔室的高度为微液滴直径的0.5~2倍能够保证微液滴的平铺质量。
34.进一步的,在图像处理完成后,通过每个平铺腔室的定位标记能够将每个图片对应拼接,方便观测微液滴的平铺状态。
35.进一步的,长穿刺针和短穿刺针的凸台利于油相和微液滴沿着管道进入腔室,且结构简单,避免了复杂的结构和制造工艺。
36.进一步的,支柱能够对芯片本体进行支撑,保证芯片本体的水平,确保移液后微液滴的质量。
37.本发明还提供一种全封闭无污染的数字化核酸芯片的检测方法,采用一体化设计以实现微液滴平铺、成像分析的功能。微液滴在试管中完成pcr热循环扩增后,与本发明所述芯片组装配合使用,通过向芯片进油通孔压入油相,油相经第一穿刺针进入试管并使得试管中的微液滴在浮力作用下上浮,微液滴通过第二穿刺针进入到芯片的平铺腔室,进而流入平铺腔室实现液滴单层平铺,随后进行光学检测操作即可获得扩增后液滴的荧光信息,避免了开盖操作可能带来的交叉污染风险,操作简单。
附图说明
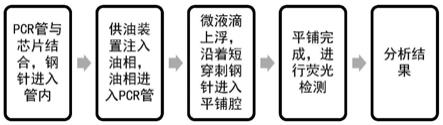
38.图1为本发明的整体流程示意图;
39.图2为本发明的整体结构示意图;
40.图3为芯片本体的结构示意图;
41.图4为第一芯片的仰视结构示意图;
42.图5为图4的c
‑
c剖视结构示意图;
43.图6为图5的h局部放大示意图;
44.图7为第二芯片的轴视结构示意图;
45.图8为第一穿刺针和第二穿刺针的结构示意图;
46.图9为第三芯片的仰视结构示意图;
47.图10为图9中b
‑
b剖视结构示意图;
48.图11为四联排的试管结构示意图;
49.图12为底部支座和试管的配合结构示意图;
50.图13为图12的d
‑
d剖视结构示意图;
51.图14为试管充入油相的过程图,图14a为试管的初始状态示意图,图14b为试管中油相充满的状态示意图,图14c为另一实施例中,试管的初始状态示意图,图14d为试管中油相充满的状态示意图;
52.图15为10
×
物镜镜头下的微液滴平铺的示意图;
53.图16为5
×
物镜镜头下的微液滴平铺的示意图。
54.附图中:1
‑
芯片本体,1100
‑
第一芯片,1110
‑
进油槽,1120
‑
进液槽,1130
‑
平滑流道,1140
‑
平滑流道出口,1150
‑
平铺腔室,1160
‑
定位标记,1170
‑
平铺腔支撑柱,1200
‑
第二芯片,1210
‑
进油通孔,1220
‑
出油通孔,1230
‑
进液通孔,1300
‑
第三芯片,1310
‑
帽盖,1320
‑
卡位薄壁,1330
‑
废液腔,1400
‑
排气通孔,1500
‑
定位销通孔,1600
‑
短穿刺针,1700
‑
长穿刺针,1800
‑
第一穿刺针,1900
‑
第二穿刺针,2
‑
试管上盖,3
‑
试管,4
‑
底部支座,401
‑
试管凹槽,402
‑
支柱,5
‑
供油装置。
具体实施方式
55.下面结合附图和具体实施方式对本发明作进一步的说明。
56.如图2和图3所示,本发明提供一种全封闭无污染的数字化核酸检测芯片,将pcr扩增与后续检测独立开来,降低芯片复杂性,避免检测环节对pcr扩增缓解的反应通量的制约,能够快速、有效地促使液滴平铺,无需两种油相,芯片耗材较少,成本较低,特别是一体化芯片在移液过程中避免了开盖操作可能带来的交叉污染风险,并且相比流式检测可以观测微液滴状态,提高检测成功率和时效性,同时也可应用于蛋白或核酸,如pcr\lamp\rpa反应等技术,满足不同应用场合的分析需求。
57.在本实施例中,一种全封闭无污染的数字化核酸检测芯片包括供油装置5、微液滴平铺与检测微流控的芯片本体1、装载有微液滴的试管3、固定试管3和支撑芯片的底部支座4四部分;其中芯片本体1包括进油通孔1210、进油槽1110、出油通孔1220、进液槽1120、与试管3配合的帽盖1310和卡位薄壁1320、平滑流道1130、平铺腔室1150、平铺腔支撑柱1170、排气通孔1400、废液腔1330等。其中,芯片本体1为透明材质,芯片本体1上设有若干个进油通孔1210,进油通孔1210的出口连接进油槽1110,进油槽1110上连接有第一穿刺针1800的一端开口,第一穿刺针1800的另一端开口伸入试管3中,试管3用于接收进油通孔1210输送的油相,第二穿刺针1900的一端开口连接在芯片本体1内腔中开设的进液槽1120内,进液槽1120的出口连接有平铺腔室1150,平铺腔室1150的底部平面处于水平方向,第二穿刺针1900的另一端开口伸入试管3中;
58.第一穿刺针1800的另一端开口始终伸入试管3中的油相内,在油相充满试管3时,第二穿刺针1900的另一端开口接触油相的顶部液面。
59.具体的,芯片本体1的透明材质为透明玻璃,也可采用聚甲基丙烯酸甲酯(pmma)或聚碳酸酯(pc)等高分子聚合物材料制作。芯片本体包括三层,分别为第一芯片1100、第二芯片1200和第三芯片1300,第一芯片1100、第二芯片1200和第三芯片1300依次层叠,其中,第一芯片1100与第二芯片1200由聚合物材料经注塑加工后热压键合而成,或由透明玻璃刻蚀制作,获得高精度的腔室和配合关系。
60.如图4、图5和图6所示,具体的,第一芯片1100通过第一连接面和第二芯片1200接触连接,第一连接面上开设有进油槽1110和进液槽1120,进油槽1110的一侧壁连通至进油通孔1210的侧壁,其中,进油通孔1210贯通第二芯片1200和第三芯片1300,进油槽1110同轴连通有出油通孔1220,出油通孔1220贯通第二芯片1200和第三芯片1300,出油通孔1220和第一穿刺针1800过盈配合;进液槽1120的一侧壁连通有平滑流道1130,平滑流道1130的出口连通至平铺腔室1150,平滑流道1130的入口直径到平滑流道出口1140直径由微液滴直径3~5倍均匀减少,进液槽1120同轴连通有进液通孔1230,进液通孔1230贯通第二芯片1200
和第三芯片1300,进液通孔1230和第二穿刺针1900过盈配合,平铺腔室1150的面积为试管3中总微液滴单层平铺面积的1.2倍。其中,进油槽1110、进液槽1120的体积可根据平铺腔室1150或阵列pcr反应腔室的大小进行调节。第一芯片1100上的进油槽1110的直径为3毫米,高度为0.3毫米的圆形腔室,进油通孔1210的宽度为1毫米,高度为0.3毫米,进液槽1120为直径3毫米,高度0.3毫米的圆形腔室,进液槽1120经平滑流道1130,平滑流道1130的高度从0.3毫米平缓减小到0.1毫米,宽度也由1毫米平缓减小到0.3毫米。进液槽1120与进入平铺腔室1150的平滑流道1130平滑连接,平滑流道1130的高度平滑减小,保证微液滴顺利进入平滑流道1130,避免液滴在平滑流道1130内的挤压碰撞而导致液滴融合,能够避免微液滴破裂或者严重变形,而且独特的平滑流道1130的设计,使本发明能够生成特定体积的微液滴,如直径20um~200um的微液滴。
61.进一步的,平铺腔室1150的高度为微液滴直径的0.5~2倍,优选地,高度为液滴直径的1.25倍,其中,平铺腔室1150的面积大于单层微液滴总面积的20%左右。
62.在本实施例中,平铺腔室1150上的末端连通至排气通孔1400的侧壁上,排气通孔1400贯通第一芯片1100、第二芯片1200和第三芯片1300,排气通孔1400用于排出气体,利于微液滴平铺过程。其中,平铺腔室1150的末端流道的宽度小于微液滴直径,流道末端连接排气通孔1400用于排气,利于平铺过程顺利进行。排气通孔1400入口与废液腔1330上端连接,其中,废液腔1330位于第三芯片1300的内腔中,第三芯片1300的下表面镂空,废液腔1330用于收集废液,避免污染环境,目的是为了释放收集平铺腔室1150中持续流入液体产生的压力,同时减少交叉污染。
63.如图7所示,在本实施例中,第二芯片1200上还开设有定位销通孔1500,定位销通孔1500贯通第一芯片1100、第二芯片1200和第三芯片1300,通过定位销通孔1500用于芯片本体1制造时精密配合。
64.具体的,第一连接面上还一体化有平铺腔支撑柱1170,平铺腔支撑柱1170和第二芯片1200接触,平铺腔支撑柱1170起到支撑平铺腔室1150的作用,避免热压键合出现塌陷,保证液滴平铺效果。
65.在本实施例中,相邻平铺腔室1150之间设有定位标记,定位标记1160和第一芯片1100一体成型,同一平铺腔室1150之间相邻的定位标记1160的形状不一致,例如长方形、三角形、圆形或正方形等,在得到每个平铺腔室1150的图像时,通过对齐每个定位标记1160实现图像的拼接,便于在图像处理时进行拼接操作。
66.如图9和图10所示,具体的,第三芯片1300设有第二连接面,第二连接面为靠近试管的第三芯片1300表面,第二连接面上设有卡位薄壁1320,卡位薄壁1320用于卡合在试管上盖2,起到严格卡位、密封的作用,进油通孔1210和出油通孔1220位于卡位薄壁1320围合的区域内,第二连接面上一体成型有帽盖1310,进油通孔1210和出油通孔1220上均同轴连接有帽盖1310,帽盖1310为凸起结构,第一穿刺针1800穿过进油通孔1210和帽盖1310然后穿透试管上盖2进入试管3内,第二穿刺针1900穿过出油通孔1220和帽盖1310然后穿透试管上盖2进入试管3内,其中,第一穿刺针1800和第二穿刺针1900通过帽盖1310固定,帽盖1310与第一穿刺针1800和第二穿刺针1900均为过盈配合,增加穿刺针和芯片本体1连接的稳定性,帽盖1310和卡位薄壁1320均为硅胶材质,利用硅胶形变达到过盈配合效果,从而实现压紧密封。
67.如图8所示,具体的,第一穿刺针1800和第二穿刺针1900为长穿刺针1700或短穿刺针1600,长穿刺针1700的开口距离试管3开口的距离大于短穿刺针1600的开口到试管3开口的距离;优选的,长穿刺针1700和短穿刺针1600的一端开口均与第一连接面平齐,长穿刺针1700和短穿刺针1600的一端开口上均一体成型有凸台,凸台均顶压在第一芯片1100的壁面上,利于油相和微液滴沿着管道进入腔室,且结构简单,避免了复杂的结构和制造工艺。在本实施例中,第一穿刺针1800为长穿刺针1700,第二穿刺针1900为短穿刺针1600,短穿刺针1600的上端与进液槽1120相连,通过第三芯片1300下端的帽盖1310结构增加配合的稳定性,短穿刺针1600的下端伸入试管3,其中,短穿刺针1600的下端要高于长穿刺针1700下端,初始状态下短穿刺针1600应该在乳液液面以上,以保证微液滴能顺利进入短穿刺针。
68.如图11和图12和图13所示,在本实施例中,试管3为标准pcr管,试管上盖2采用软硅胶材料制作,管体可直接采用0.2ml pcr八联管以降低耗材成本,试管3由底部支座4固定,其中上设有试管凹槽401,试管凹槽401用于放置试管3,所述底部支座4上还一体成型有支柱402,圆形的支柱402是为了支撑芯片本体1,防止因芯片倾斜影响观测,当芯片本体1的底部放置底部支座4时,支柱402和芯片本体1的底部壁面接触。
69.在本实施例中,还包括供油装置5,供油装置5的出口连接有出油导管,本实施例中,出油导管采用橡皮管,橡皮管和进油通孔1210过盈配合,防止油相泄露。
70.在本实施例中,穿刺针和出油导管和芯片本体1以及供油装置5以及试管3的连接处均能通过具有米字或十字缺口的硅胶塞进行密封,从而有效避免交叉污染。
71.本发明采用一体化设计以实现微液滴平铺、成像分析的功能。微液滴在pcr管中完成pcr热循环扩增后,与本发明所述芯片组装配合使用,通过向芯片进油口1210压入油相,油相经长穿刺钢针1700进入pcr管并使得pcr管中的微液滴在浮力作用下上浮,微液滴通过短穿刺钢针1600进入到芯片的平铺腔,进而流入平铺腔实现液滴单层平铺,随后进行光学检测操作即可获得扩增后液滴的荧光信息。
72.在本发明的另一实施例中,提供一种全封闭无污染的数字化核酸芯片的检测方法,包括以下步骤:
73.装有微液滴的试管3固定在芯片本体1上,第一穿刺针1800伸入试管3内,进油通孔1210接入油相,油相经过进油通孔1210进入进油槽1110,进油槽1110内的油相经过第一穿刺针1800进入试管3内,微液滴浮于油相的液面处;
74.待油相充满试管3内腔时,油相的液面接触第二穿刺针1900,油相持续由第一穿刺针1800进入试管3,油相液面上的微液滴被推入第二穿刺针1900,微液滴依次经过第二穿刺针1900、进液槽1120和平铺腔室1150,微液滴不断进入平铺腔室1150,逐步完成平铺,平铺完成后,将芯片本体1移至光学检测平台进行检测;
75.经光学检测平台得到检测图像,对多个图像进行拼接和增强处理,通过对明视场图像处理得到总的液滴数,对荧光视场图像处理得到阳性液滴数,识别液滴融合和破裂,剔除假阳性和假阴性液滴,进而通过泊松概率模型推导出原始核酸拷贝数及置信区间,完成数字化核酸芯片检测。
76.如图1和图14中的图14a以及图14b所示,第一穿刺针为长穿刺针,第二穿刺针为短穿刺针,具体的,第一步:装有微液滴的pcr试管通过pcr试管上盖与芯片本体的卡位薄壁结合固定,长、短穿刺钢针进入pcr管内部。
77.第二步:供油装置从进油导管注油,油相经过进油通孔、进油槽、出油通孔、长穿刺钢针进入pcr管内,控制流速。
78.第三步:由于微液滴的密度小于所加油相的密度,随着油相的不断流入,微液滴上浮,直至到达短穿刺钢针下端后,沿着短钢针进入芯片。
79.第四步:微液滴沿着短穿刺钢针、进液槽、平滑流道,沿着流道进入平铺腔,气体从末端的通气孔排出。
80.第五步:微液滴不断进入平铺腔,逐步完成平铺,平铺过程完成后,将芯片移至光学检测平台进行检测。
81.第六步:对图像进行拼接、增强等处理,得到分析结果。
82.如图14中的图14c和图14d所示,第一穿刺针为短穿刺针,第二穿刺针为长穿刺针,具体的,第一步:装有微液滴的pcr试管通过pcr试管上盖与芯片本体的卡位薄壁结合固定,长、短穿刺钢针进入pcr管内部。
83.第二步:供油装置从进油导管注油,油相经过进油通孔、进油槽、出油通孔、短穿刺钢针进入pcr管内,控制流速。
84.第三步:由于微液滴的密度小于所加油相的密度,随着油相的不断流入,微液滴上浮,直至到达长穿刺钢针开口处后,沿着长穿刺针进入芯片。
85.第四步:微液滴沿着长穿刺针、进液槽、平滑流道,沿着流道进入平铺腔,气体从末端的通气孔排出。
86.第五步:微液滴不断进入平铺腔,逐步完成平铺,平铺过程完成后,将芯片移至光学检测平台进行检测。
87.第六步:对图像进行拼接、增强等处理,得到分析结果。
88.如图15和16所示,说明通过本发明的管内制备液滴的装置可以生成均匀、形态良好的微液滴。
89.最后应说明的是:以上所述实施例,仅为本发明的具体实施方式,用以说明本发明的技术方案,而非对其限制,本发明的保护范围并不局限于此,尽管参照前述实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:任何熟悉本技术领域的技术人员在本发明揭露的技术范围内,其依然可以对前述实施例所记载的技术方案进行修改或可轻易想到变化,或者对其中部分技术特征进行等同替换;而这些修改、变化或者替换,并不使相应技术方案的本质脱离本发明实施例技术方案的精神和范围,都应涵盖在本发明的保护范围之内。因此,本发明的保护范围应以权利要求所述的保护范围为准。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1