一种2-花生四烯酸甘油一酯的制备方法
一种2
‑
花生四烯酸甘油一酯的制备方法
技术领域
1.本发明涉及甘油一酯的制备方法领域,具体涉及一种2
‑
花生四烯酸甘油一酯的制备方法。
背景技术:
2.甘油一酯(monoacylglycerols,mags)是一类同时含有亲水基团和疏水基团的化合物,是一种非离子型乳化剂,被广泛应用于食品、医药及相关行业中,每年全球mags乳化剂的产量约为15~19万吨,mags的物理化学和营养学性质与其脂肪酸组成,以及脂肪酸在甘油骨架上的酰化位置分布有关有关。含有长链多不饱和脂肪酸(常见的如epa、dha)的mags大多具有与其类似的生理活性,此外2
‑
甘油一酯(2
‑
monoacylglycerols,2
‑
mags)相比于1
‑
甘油一酯(1
‑
monoacylglycerols,1
‑
mags),可以直接被人体吸收,从而发挥其生理活性,但更不稳定,难以制备及储存高纯度产物。
[0003]2‑
花生四烯酸甘油一酯(2
‑
arachidonoylglycerol,2
‑
ag)是指sn
‑
2位为花生四烯酸(arachidonic acid,ara)的mags。研究发现,2
‑
ag是一种内源性脂质信号分子,在免疫系统、心血管系统及中枢神经系统中发挥着众多生理功能;在受到脑创伤、脑缺血以及促炎刺激时,2
‑
ag能够抑制大麻素受体所依赖的促炎细胞因子和细胞核因子
‑
b(nuclear factor
‑
b,nf
‑
b),从而起到保护神经元的作用;此外,多项研究表明了2
‑
ag还具有调节食欲、减轻疼痛、缓解炎症以及改善记忆等生理功能;因此,2
‑
ag具有潜在的药用价值,以期用于治疗肥胖症、慢性疼痛、焦虑症和抑郁症等,合成2
‑
ag或富含ara的2
‑
mags具有现实意义。
[0004]
尽管2
‑
ag的化学结构简单,但获得途径仍然有限,因为制备它的化学方法效率相当低;一方面,由于存在两个相邻的伯羟基官能团,sn
‑
2位的酰基甘油表现出高度的异构化倾向(酸、碱和热促进酰基的迁移),为其高纯度产物的合成、分离、储存等造成困难。另一方面,2
‑
ag特有的一个问题是花生四烯基部分对影响天然烯烃系统完整性的自氧化表现出明显的敏感性,因此限制了其制备的可用程序的数量;化学催化法是目前主要生产具有饱和脂肪酸的单甘脂的方法,具有低成本和短时的优势,但高温下易导致油的氧化,且不具备特异性,显然不满足制备高纯度2
‑
ag的要求。酶催化制备富含ara的甘油一酯具有高效、专一、反应条件温和、副产物少、重复利用酶等优点,将是应用于工业化生产的首选技术。
技术实现要素:
[0005]
本发明的目的是提供一种2
‑
花生四烯酸甘油一酯的制备方法,其具有利用绿色环保、高效的酶催化醇解法制备高纯度、高产量2
‑
ag的优点。
[0006]
本发明的上述技术目的是通过以下技术方案得以实现的:
[0007]
一种2
‑
花生四烯酸甘油一酯的制备方法,
[0008]
s1:将sn
‑
2位富含花生四烯酸的油脂和乙醇以摩尔比为1:20~1:100的比例下,在反应温度为20℃~50℃下进行混合;
[0009]
s2:将脂肪酶添加进入混合物进行酶促醇解反应,醇解反应体系水分活度为0.1~
0.50,通过磁力搅拌反应,反应时间1h~10h,得到粗产物;
[0010]
进一步设置:所述s2中粗产物还可以通过萃取法进行纯化,将粗产物以1:8~1:16(w/v)的比例与有机溶剂水溶液混合,再添加等体积的非极性溶剂进行萃取,分层后,取极性溶液层,去除有机溶剂和水后得到2
‑
花生四烯酸甘油一酯。
[0011]
进一步设置:所述纯化后的2
‑
花生四烯酸甘油一酯还可以通过结晶法进一步纯化,将得到的2
‑
花生四烯酸甘油一酯与溶剂以摩尔比为1:6~1:15比例混合后,在0℃以下结晶,结晶后收集滤液,得到2
‑
花生四烯酸甘油一酯。
[0012]
进一步设置:所述s1中sn
‑
2位富含花生四烯酸的油脂为花生四烯酸含量大于35%的脂质。
[0013]
进一步设置:所述s1步骤中sn
‑
2位富含花生四烯酸的油脂制备如下:将花生四烯酸和甘油以摩尔比为3:1以上的组成在脂肪酶作用下进行酶促反应,反应温度为50℃~80℃,反应体系压力在500pa以下进行反应,去除脂肪酶和未反应完的底物,得到sn
‑
2位富含花生四烯酸的合成脂质。
[0014]
进一步设置:所述s2步骤中醇解反应体系水分活度为0.1~0.25。
[0015]
进一步设置:所述溶剂为非极性溶剂,所述非极性溶剂包括己烷、乙醚、石油醚中的一种或多种。
[0016]
进一步设置:所述s2步骤中酶促醇解反应为2h~6h。
[0017]
进一步设置:所述脂肪酶包括南极假丝酵母(candida antarctica)、伯克霍尔德菌(burkaholderia cepacia)以及疏棉状嗜热丝孢菌(thermomyces lanuginose)为来源的脂肪酶。
[0018]
进一步设置:所述脂肪酶包括lipozyme 435、lipase cl“amano”im及lipase ps“amano”中的一种或多种。
[0019]
综上所述,本发明具有以下有益效果:
[0020]
1、本发明采用酶法醇解以制备sn
‑
2位花生四烯酸甘油一酯,绿色环保、短时高效;
[0021]
2、本发明采用富含花生四烯酸的油脂作为原料,可获得高纯度高产量的2
‑
花生四烯酸甘油一酯,纯度可达到65%~90%;
[0022]
3、本发明使用的酶法醇解反应体系实际上是通过控制水分活度,以提高酶活性并减少sn
‑
2位花生四烯酸发生酰基转移,从而保证2
‑
花生四烯酸甘油一酯的高纯度;
[0023]
4、本发明使用的酶法酯交换反应体系注重控制反应压力,以快速除去反应副产物,推进反应不断正向进行,保证较高的转酯率;
[0024]
5、本发明所用到的脂肪酶,可以重复再利用多次,显著降低生产成本,达到规模化生产要求。
附图说明
[0025]
下面结合附图对本发明进一步说明。
[0026]
图1为本发明酶促酯交换制备富花生四烯酸甘油三酯得到的液相色谱图(示差检测器),其中,a为对比例1的条件下反应产物的脂质组成,b为实施例4中取真空度为200pa条件下反应产物的脂质组成。
[0027]
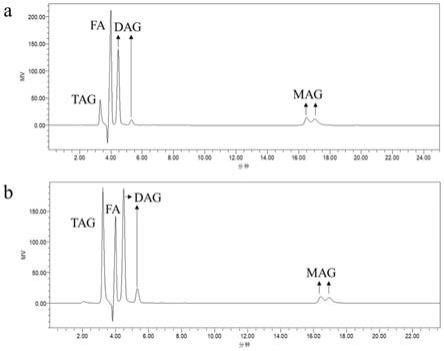
图2为本发明酶促醇解制备富花生四烯酸甘油三酯得到的液相色谱图(示差检测
器),其中,a为对比例4的条件下反应产物的脂质组成,b为实施例6中取最佳条件,加入lipozyme 435脂肪酶,酶添加量(相对于油脂的质量分数)为8%条件下反应产物的脂质组成。
具体实施方式
[0028]
下面结合附图对本发明的具体实施方式做进一步说明。
[0029]
本发明所采用的技术方案是:
[0030]
实施例1~5为酯交换制备富含花生四烯酸甘油三酯的实施例:
[0031]
实施例1:(选取酶的种类不同进行对比)
[0032]
在25ml锥形瓶中加入15mmol花生四烯酸乙酯和4mmol甘油,再加入脂肪酶,酶添加量(相对于脂肪酸乙酯的质量分数)为10%,待体系混合均匀,在55℃、200pa压力下进行酶促反应,磁力搅拌220r/min反应6h;反应结束后以4000r/min的转速离心取上清液,去除脂肪酶,经hplc
‑
rid检测得到反应粗产物中脂质组成,计算甘油三酯的得率,结果如表1所示。
[0033]
表1.酶促反应中不同酶的种类对甘油三酯得率的影响
[0034][0035]
实施例2:(底物不同摩尔比进行对比)
[0036]
在25ml锥形瓶中加入15mmol花生四烯酸乙酯和一定量的甘油,花生四烯酸乙酯和甘油为3:0.5~3:1再加入lipozyme 435脂肪酶(来源于candida antarctica),酶添加量(相对于脂肪酸乙酯的质量分数)为10%,待体系混合均匀,在55℃、200pa压力下进行酶促反应,磁力搅拌220r/min反应6h。反应结束后以4000r/min的转速离心取上清液,去除脂肪酶,经hplc
‑
rid检测得到反应粗产物中脂质组成,计算甘油三酯的得率,结果如表2所示。
[0037]
表2.酶促反应中不同底物摩尔比对甘油三酯得率的影响
[0038][0039]
实施例3:(根据温度不同进行对比)
[0040]
在25ml锥形瓶中加入15mmol花生四烯酸乙酯和4mmol甘油,再加入lipozyme 435脂肪酶(来源于candida antarctica),酶添加量(相对于脂肪酸乙酯的质量分数)为10%,待体系混合均匀,在50℃~80℃、200pa压力下进行酶促反应,进行酶促反应,磁力搅拌220r/min反应6h。反应结束后以4000r/min的转速离心取上清液,去除脂肪酶,经hplc
‑
rid检测得到反应粗产物中甘油酯组成,结果如表3所示。
[0041]
表3.酶促反应中不同温度对甘油三酯得率的影响
[0042]
反应温度/℃50556080甘油三酯得率90.81%94.34%95.16%96.13%
[0043]
实施例4:(根据反应压力不同进行对比)
[0044]
在25ml锥形瓶中加入16.4mmol花生四烯酸和4mmol甘油,再加入lipozyme 435脂肪酶(来源于candida antarctica),酶添加量(相对于脂肪酸的质量分数)为10%,待体系混合均匀,在55℃,在100pa~500pa压力下进行酶促反应,进行酶促反应,磁力搅拌220r/min反应6h。反应结束后以4000r/min的转速离心取上清液,去除脂肪酶,经hplc
‑
rid检测得到反应粗产物中甘油酯组成,结果如表4所示。
[0045]
表4.酶促反应中不同真空度对甘油三酯得率的影响
[0046]
真空度/pa100200300400500甘油三酯得率95.01%94.91%93.71%92.56%91.65%
[0047]
实施例5:(根据反应时间对比)
[0048]
在25ml锥形瓶中加入16.4mmol花生四烯酸和4mmol甘油,再加入lipozyme 435脂肪酶(来源于candida antarctica),酶添加量(相对于脂肪酸的质量分数)为10%,待体系混合均匀,在55℃,200pa压力下进行酶促反应,进行酶促反应,磁力搅拌220r/min反应1~10h。反应结束后以4000r/min的转速离心取上清液,去除脂肪酶。经hplc
‑
rid检测得到反应粗产物中甘油酯组成,结果如表5所示。
[0049]
表5.酶促反应中不同反应时间对甘油三酯得率的影响
[0050]
反应时间/h246810甘油三酯得率77.87%84.42%94.91%95.01%95.35%
[0051]
实施例6~10为酶法醇解制备2
‑
花生四烯酸甘油一酯的实施例:
[0052]
实施例6:(选取不同酶的种类)
[0053]
将原料(包括乙醇)与饱和硝酸镁溶液置于同一密闭容器中放置24h,调节水分活度为0.53。将2.2mmol来源于高山被孢霉的富花生四烯酸油与87mmol无水乙醇混合,加入不同的脂肪酶,酶添加量(相对于油脂的质量分数)为8%或15%,在35℃条件下进行醇解反应,磁力搅拌300r/min反应8h。反应结束后以4000r/min的转速离心取上清液,去除脂肪酶,35℃下旋转蒸发去除乙醇。经hplc
‑
rid检测并计算得到反应粗产物中2
‑
mag得率,结果如表6所示。
[0054]
表6.酶促醇解反应中不同酶的种类对粗产物2
‑
mag得率的影响
[0055][0056]
实施例7:(底物摩尔比不同)
[0057]
将原料(包括乙醇)与饱和硝酸镁溶液置于同一密闭容器中放置24h,调节水分活度为0.53。将2.2mmol来源于高山被孢霉的富花生四烯酸油与87mmol无水乙醇混合,加入脂肪酶lipozyme 435,酶添加量(相对于油脂的质量分数)为8%,在35℃条件下进行醇解反应,磁力搅拌300r/min反应8h。反应结束后以4000r/min的转速离心取上清液,去除脂肪酶,35℃下旋转蒸发去除乙醇,经hplc
‑
rid检测并计算得到反应粗产物中2
‑
mag得率,结果如表7所示。
[0058]
表7.醇解反应中不同底物摩尔比对粗产物2
‑
mag得率的影响
[0059][0060]
实施例8:(根据水分活度不同进行对比)
[0061]
将原料(包括乙醇)与饱和盐溶液(饱和氯化锂溶液、饱和氯化镁溶液、饱和硝酸镁溶液)置于同一密闭容器中放置24h,调节水分活度。将2.2mmol来源于高山被孢霉的富花生四烯酸油与87mmol无水乙醇混合,加入脂肪酶lipozyme tl im,酶添加量(相对于油脂的质量分数)为15%,在35℃条件下进行醇解反应,磁力搅拌300r/min反应8h。反应结束后以4000r/min的转速离心取上清液,去除脂肪酶,35℃下旋转蒸发去除乙醇。经hplc
‑
rid检测并计算得到反应粗产物中2
‑
mag得率,结果如表8所示。
[0062]
表8.醇解反应中不同水分活度对粗产物2
‑
mag得率的影响
[0063]
水分活度0.110.330.532
‑
mag含量81.45%80.46%82.48%
[0064]
实施例9:(根据反应温度不同进行对比)
[0065]
将原料(包括乙醇)与饱和氯化锂溶液置于同一密闭容器中放置24h,调节水分活度为0.11。将2.2mmol来源于高山被孢霉的富花生四烯酸油与87mmol无水乙醇混合,加入脂肪酶lipozyme 435,酶添加量(相对于油脂的质量分数)为8%,在20℃~50℃一定温度下进行醇解反应,磁力搅拌300r/min反应8h。反应结束后以4000r/min的转速离心取上清液,去除脂肪酶,35℃下旋转蒸发去除乙醇。经hplc
‑
rid检测并计算得到反应粗产物中2
‑
mag得率,结果如表9所示。
[0066]
表9.醇解反应中不同反应温度对粗产物2
‑
mag得率的影响
[0067]
反应温度/℃25303540452
‑
mag得率46.71%84.68%86.59%85.41%83.55%
[0068]
实施例10:(根据反应时间时间进行对比)
[0069]
将原料(包括乙醇)与饱和硝酸镁溶液置于同一密闭容器中放置24h,调节水分活度为0.53。将2.2mmol来源于高山被孢霉的富花生四烯酸油与87mmol无水乙醇混合,加入脂肪酶lipozyme tl im,酶添加量(相对于油脂的质量分数)为15%,在35℃条件下进行醇解反应,磁力搅拌300r/min反应1~10h时间。反应结束后以4000r/min的转速离心取上清液,去除脂肪酶,35℃下旋转蒸发去除乙醇。经hplc
‑
rid检测并计算得到反应粗产物中2
‑
mag得率,结果如表10所示。
[0070]
表10.醇解反应中不同反应时间对粗产物2
‑
mag得率的影响
[0071]
反应时间/h2468102
‑
mag得率30.12%51.87%60.48%82.48%72.45%
[0072]
实施例11~13为醇解反应及纯化制备2
‑
花生四烯酸甘油一酯的实施例:
[0073]
实施例11:(溶剂萃取)
[0074]
(1)酶法醇解制备2
‑
ag
[0075]
将原料(包括乙醇)与饱和硝酸镁溶液置于同一密闭容器中放置24h,调节水分活度为0.53。将2.2mmol来源于高山被孢霉的富花生四烯酸油与87mmol无水乙醇混合,加入脂肪酶lipozyme 435,酶添加量(相对于油脂的质量分数)为8%,在35℃条件下进行醇解反应,磁力搅拌300r/min反应8h。反应结束后以4000r/min的转速离心取上清液,去除脂肪酶,35℃下旋转蒸发去除乙醇。
[0076]
(2)溶剂萃取法分离纯化2
‑
ag
[0077]
向1g去除溶剂的粗产物中加入10ml有机溶剂
‑
水溶液和10ml正己烷,然后转移至分液漏斗中震荡分离。混合溶液分为两层,上层为正己烷相,包含极性较弱的甘油三酯、脂肪酸乙酯和甘油二酯;下层为含2
‑
ag的有机溶剂
‑
水相。收集下层并用正己烷清洗两次。40℃旋转蒸发去除溶剂,经hplc
‑
rid检测得到2
‑
mag含量,结果如表11所示。
[0078]
表11.不同的溶剂萃取条件下纯化产物的2
‑
mag含量
[0079][0080][0081]
实施例12:(溶剂萃取+低温结晶)
[0082]
(1)酶法醇解制备2
‑
ag
[0083]
将原料(包括乙醇)与饱和硝酸镁溶液置于同一密闭容器中放置24h,调节水分活度为0.53。将2.2mmol来源于高山被孢霉的富花生四烯酸油与87mmol无水乙醇混合,加入脂肪酶lipozyme 435,酶添加量(相对于油脂的质量分数)为8%,在35℃条件下进行醇解反应,磁力搅拌300r/min反应8h。反应结束后以4000r/min的转速离心取上清液,去除脂肪酶,35℃下旋转蒸发去除乙醇。
[0084]
(2)溶剂萃取法分离纯化2
‑
ag
[0085]
向1g去除溶剂的粗产物中加入15ml 85%甲醇
‑
水溶液和15ml正己烷,然后转移至分液漏斗中震荡分离。混合溶液分为两层,上层为正己烷相,包含极性较弱的甘油三酯、脂肪酸乙酯和甘油二酯;下层为含2
‑
ag的有机溶剂
‑
水相。收集下层并用正己烷清洗两次。40℃旋转蒸发去除溶剂。
[0086]
(3)低温结晶法分离纯化2
‑
ag
[0087]
将2g去除溶剂的产物溶于30ml正己烷(1:15,w/v),在不同温度下低温结晶10h,低温下抽滤得到结晶,如此重复结晶两次。经hplc
‑
rid检测得到2
‑
ag含量,结果如表12所示。
[0088]
表12.不同的结晶温度对低温结晶中纯化产物的2
‑
ag含量的影响
[0089]
结晶温度/℃0
‑
10
‑
20
‑
302
‑
ag含量55.37%58.48%67.17%73.26%
[0090]
实施例13:(溶剂萃取+低温结晶)
[0091]
(1)酶法醇解制备2
‑
ag
[0092]
如实施例12所述。
[0093]
(2)溶剂萃取法分离纯化2
‑
ag
[0094]
如实施例12所述。
[0095]
(3)低温结晶法分离纯化2
‑
ag
[0096]
将2g去除溶剂的产物溶于16ml非极性溶剂(1:8,w/v)中,在
‑
30℃下低温结晶10h,低温下抽滤得到结晶,如此重复结晶两次,经hplc
‑
rid检测得到2
‑
ag含量,结果如表13所示。
[0097]
表13.不同的非极性溶剂对低温结晶中纯化产物的2
‑
ag含量的影响
[0098]
非极性溶剂己烷乙醚石油醚2
‑
ag含量74.65%68.63%69.56%
[0099]
对比例1:(与实施例4对比)
[0100]
加入一定量lipase df im脂肪酶(来源于rhizopus oryzae),其他条件与实施例4一致。得到反应产物中甘油三酯得率28.27%。
[0101]
采用实施例4中真空度为200pa的条件,以花生四烯酸及甘油为原料,将使用lipozyme 435脂肪酶所得产物的甘油三酯得率与对比例1使用lipase df im脂肪酶作对比,见图1。其中,图1a为使用lipase df im脂肪酶反应得到的液相色谱图,图1b为使用lipozyme 435脂肪酶反应得到的液相色谱图。图1a的甘油三酯得率较低为28.27%;图1b的甘油三酯得率为94.91%。
[0102]
对比例2:(与实施例4对比)
[0103]
在常压下进行酶促酯交换反应,其他条件与实施例4一致,得到反应产物中甘油三酯得率43.82%。
[0104]
对比例3:(与实施例6对比)
[0105]
加入一定量lipozyme rm im脂肪酶(来源于rhizomucor miehei),其他条件与实施例6一致。得到反应粗产物中2
‑
mag得率8.74%。
[0106]
对比例4:(与实施例6对比)
[0107]
加入2ml丙酮作为溶剂,采用lipozyme 435脂肪酶,其他条件与实施例6一致。得到反应粗产物中2
‑
mag得率45.02%。
[0108]
采用实施例6中的最佳条件,加入lipozyme 435脂肪酶,酶添加量(相对于油脂的质量分数)为8%,以富花生四烯酸油及无水乙醇为原料,将无溶剂反应体系与对比例4加入2ml丙酮的有机溶剂体系作对比,见图2。其中,图2a为添加丙酮作溶剂反应得到的液相色谱图,图2b为不添加丙酮作溶剂反应得到的液相色谱图。图2a的2
‑
mag得率较低为45.02%;图2b的2
‑
mag得率较高为88.59%。
[0109]
对比例5:(与实施例8对比)
[0110]
将原料与饱和硫酸钾溶液置于同一密闭容器中放置24h,调节水分活度为0.97,其
他条件与实施例8一致。得到反应粗产物中2
‑
mag得率67.08%。
[0111]
对比例6:(与实施例9对比)
[0112]
在80℃下进行酶促醇解反应,其他条件与实施例9一致。得到反应粗产物中2
‑
mag得率54.16%。
[0113]
对比例7:(与实施例12对比)
[0114]
低温结晶中将2g去除溶剂的产物溶于乙醇(极性溶剂),其他条件与实施例12一致,得到纯化产物中2
‑
ag含量51.45%。
[0115]
以上是本发明的较佳实施例而已,并非对本发明作任何形式上的限制,凡是依据本发明的技术实质对以上实施例所做的任何简单修改、等同变化与修饰,均属于发明技术方案的范围内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1