一种AIE型三苯胺衍生物荧光探针及其制备方法和其在水合肼检测中的应用
一种aie型三苯胺衍生物荧光探针及其制备方法和其在水合肼检测中的应用
技术领域
1.本发明属于有机小分子生物荧光探针技术领域,具体涉及一种aie型三苯胺衍生物荧光探针、制备方法及其在水合肼检测中的应用。
背景技术:
2.众所周知,水合肼不仅因其易燃易爆的特性而成为导弹和火箭推进系统的推进剂,而且是化学、制药和农业中最重要的反应基础之一。其强大的还原能力还能通过扫氧,有效抑制给水、供热系统的热水锅炉的金属腐蚀。最重要的是,水合肼具有致癌和毒性,在其制造、运输、应用和处置过程中,即使微量泄漏也可能导致严重的环境污染和严重的健康风险,更糟糕的是,由于其水溶性良好,水合肼很容易通过皮肤和口腔接触和吸入,被生物系统吸收。作为一种神经毒素和诱变原,过量接触水合肼可能导致严重的器官损伤,包括肝、肾、肺、中枢神经系统和呼吸道感染等。因此,美国环境保护署(epa)建议将水合肼作为致癌物质的允许阈值定为10ppb(0.31μm)。由于水合肼的广泛存在和剧毒性,其精准、高灵敏及快速检测主要还是依靠荧光分析法。设计结构新颖的荧光探针分子,丰富其荧光成像方式并提高成像性能,已逐渐成为荧光成像技术发展过程中的热点与难点。
3.与传统的荧光探针相比,aie分子生物探针的简单设计和荧光开启特性提供了水介质中特异性分析物和生物过程的直接可视化,具有更高的灵敏度和更好的准确性。不同剂型和表面功能的aie点生物探针在量子点和小分子染料上表现出吸收率大、发光度高、生物相容性好、无随机闪烁、耐光漂白等先进特性,这些特性使肿瘤细胞检测、长期细胞示踪和肿瘤成像成为可能。最近的研究极大地扩展了aie荧光剂的生物应用范围,并为荧光生物探针的设计提供了新的策略。预计,aie生物探针的未来发展将将单光子或多光子荧光与其他形式(如磁共振成像)或功能(如治疗)相结合,以充分展示其作为新一代治疗诊断试剂的潜力。与此同时,分子生物学的发展将提供更特异性的生物受体,这将有助于开发具有高选择性和高灵敏度的下一代aie生物探针,用于分子传感和成像。近几年,对aie分子的研究取得了很大的进展,如硅杂环戊二烯及其衍生物、四苯基乙烯(tpe)衍生物以及其它具有aie现象的分子,在生物检测领域得到了广泛的应用。尽管如此,用于检测水合肼的aie型荧光探针仍很缺乏,这类探针亟待开发。
技术实现要素:
4.对目前可用于水合肼检测的aie型荧光探针缺乏的现状,本发明提供了一种aie型三苯胺衍生物荧光探针及其制备方法和应用。
5.为了实现上述发明目的,本发明采用以下技术方案:
6.一种aie型三苯胺衍生物荧光探针,其结构式如式ⅰ所示:
[0007][0008]
该荧光探针的化学名称为(z)
‑2‑
(4
‑
(((e)4
‑
(二甲胺基)苯亚甲基)氨基)苯)3
‑
(4
‑
(二苯胺)苯基)丙烯腈,分子式为c
36
h
30
n4。
[0009]
一种所述aie型三苯胺衍生物荧光探针的制备方法,该荧光探针的合成路线如下:
[0010][0011]
具体制备步骤如下:第一步,制备(e)
‑2‑
(4
‑
(4
‑
(二甲胺基)苯亚甲基)氨基)苯基)乙腈;第二步,制备4
‑
(二苯胺)苯甲醛;第三步,(e)
‑2‑
(4
‑
(4
‑
(二甲胺基)苯亚甲基)氨基)苯基)乙腈和4
‑
(二苯胺)苯甲醛在碱性环境下反应,制得所述荧光探针。
[0012]
所述的第一步的合成路线如下:
[0013][0014]
具体反应步骤如下:将4
‑
(二甲胺基)苯甲醛先溶解在乙醇中,搅拌反应,再加入2
‑
(4
‑
氨基)乙腈,加入醋酸溶液,加热回流,用薄层色谱法监测进程,待反应完成后冷却至室温,然后放冰箱静置一晚,有淡黄色晶体析出,抽滤,再用无水乙醚对沉淀进行洗涤,得到淡黄色固体(纯)产品(e)
‑2‑
(4
‑
(4
‑
(二甲胺基)苯亚甲基)氨基)苯基)乙腈。
[0015]
其中,4
‑
(二甲胺基)苯甲醛与2
‑
(4
‑
氨基)乙腈的物质的量比为0.8
‑
1;反应的ph值为4.5
‑
6.5;加热回流温度为75
‑
85℃。
[0016]
所述的第二步的合成路线如下:
[0017][0018]
具体反应步骤如下:将dmf加入到三颈烧瓶内,置于冰浴中,逐滴加入pocl3,在低温下搅拌,将温度增加到室温,然后,加入三苯胺,升温搅拌,冷却至室温,反应混合物缓慢倒入冰水浴中,用naoh中和,二氯甲烷萃取,合并有机相,有机相用无水mgso4干燥,过滤,浓缩有机层,用乙酸乙酯:石油醚=1:10(v/v)过柱,得到4
‑
(二苯胺)苯甲醛白色固体;
[0019]
其中,三苯胺、dmf及pocl3的物质的量比为1:1:1
‑
1:1.2:1.5;低温下搅拌的温度为
‑
10℃
‑
10℃;升温搅拌的时间为10h
‑
15h,具体的温度为40℃
‑
65℃。
[0020]
所述的第三步的具体步骤如下:
[0021]
将(e)
‑2‑
(4
‑
(4
‑
(二甲胺基)苯亚甲基)氨基)苯基)乙腈溶于有机溶剂中,然后加入4
‑
(二苯胺)苯甲醛,再加入碱,加热回流,搅拌2h,薄层色谱法点板跟踪至反应结束后,抽滤后得到橙色固体(z)
‑2‑
(4
‑
(((e)4
‑
(二甲胺基)苯亚甲基)氨基)苯)3
‑
(4
‑
(二苯胺)苯基)丙烯腈。
[0022]
所述有机溶剂选自甲苯、乙腈、二氯乙烷、二氯甲烷、n,n
‑
二甲基甲酰胺、四氯化碳、正己烷、四氢呋喃、甲醇或乙醇中的一种;所述的碱选自哌啶、氢氧化钠、碳酸氢钠、叔丁醇钾中的一种;加热回流温度为75
‑
85℃;(e)
‑2‑
(4
‑
(4
‑
(二甲胺基)苯亚甲基)氨基)苯基)乙腈、碱与4
‑
(二苯胺)苯甲醛的物质的量比为1:1:1
‑
1:1.2:1.5。
[0023]
上述制备方法中,反应结束后的后处理方式并无特别的限定,本领域技术人员可依据物料的理化性质,结合公知常识的分离手段,采用常规的物理分离手段来实现目标产物的分离,优选的技术方案为过滤法,更进一步优选,选用减压抽滤。
[0024]
上述制备方法中,通过薄层色谱法监测反应终点,反应时间无特别的限定。
[0025]
一种所述的aie型三苯胺衍生物荧光探针在水合肼检测中的应用。
[0026]
一种水合肼检测试剂,包括上述荧光探针。
[0027]
进一步地,所述水合肼检测试剂为体内水合肼检测试剂。
[0028]
该探针设计的初衷是想通过4
‑
(二甲胺基)苯甲醛中的醛基与2
‑
(4
‑
氨基)乙腈中的氨基通过希夫碱反应,形成c=n双键,提供可以用于水合肼检测的作用位点。
[0029]
检测原理如下,首先根据相关报道文献推测探针tpaa与n2h4发生相互作用时可能的反应机制是:在n2h4存在的情况下,tpaa的c=n键断裂,由此形成了一个含有氨基的化合物和具有醛基的化合物,该醛基化合物会继续与n2h4作用,得到另一种新化合物,其通过esi
‑
ms分析数据证实。
[0030]
有益效果:
[0031]
1、本发明首次提供了一种具有aie性能的三苯胺类化合物荧光探针,丰富了水合肼类荧光分子探针的种类,为有机分析和光化学提供了新型的探针分子,可广泛应用于荧光分析或检测领域。
[0032]
2、该新型荧光分子探针实现了对水合肼的高灵敏检测,其检测限为0.13μm。
[0033]
3、该荧光探针分子可以实现在hela细胞中对水合肼含量检测和成像研究。
附图说明
[0034]
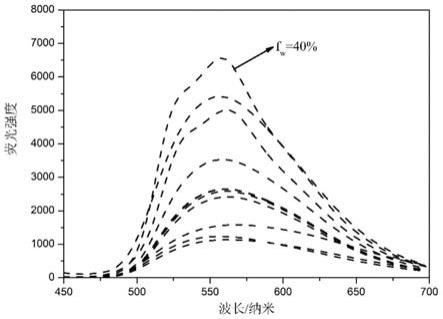
图1为探针分子tpaa在不同含水量的dmso
‑
h2o混合液中的荧光图。
[0035]
图2为探针分子tpaa在dmso溶液中紫外及荧光图及斯托克斯位移。
[0036]
图3为探针分子tpaa的dmso溶液对其他不同类型干扰物的荧光图。
[0037]
图4为探针分子tpaa的dmso溶液对不同浓度水合肼的荧光图。
[0038]
图5为探针分子tpaa的dmso溶液对水合肼检测动力学图。
[0039]
图6为探针分子tpaa检测n2h4的机理图。
[0040]
图7为探针分子tpaa与n2h4响应后终产物的液相质谱图。
[0041]
图8为探针分子tpaa在hela细胞中水合肼的成像图。图中的a1、b1、c1和d1是细胞的绿色通道和蓝色通道的叠加图,随着水合肼浓度的增加,叠加图的光强度增强,a2、b2、c2和d2是细胞的明场图。
具体实施方式
[0042]
下面结合附图和具体实施例对本发明作进一步详细说明,但不应理解为对本发明的限制。在不背离本发明精神和实质的情况下,对本发明方法、步骤或条件所作的修改或替
换,均属于本发明的范围。实施例中未注明具体条件的实验方法及未说明配方的试剂均为按照本领域常规条件。
[0043]
实施例1
[0044]
aie型三苯胺衍生物荧光探针的制备:
[0045]
第1步、化合物(e)
‑2‑
(4
‑
(4
‑
(二甲胺基)苯亚甲基)氨基)苯基)乙腈的制备
[0046][0047]
将4
‑
(二甲胺基)苯甲醛(0.4470g,3mmol)先溶解在15ml etoh中,搅拌反应,再加入2
‑
(4
‑
氨基)乙腈(0.4130g,3.5mmol)加热至80℃回流,用薄层色谱法监测进程反应完成后冷却至室温,放入冰箱过夜,有晶体析出,抽滤,得到淡黄色固体产品,产率:90.2%,0.7123g;纯度99%以上。(注:4
‑
(二甲胺基)苯甲醛和2
‑
(4
‑
氨基)乙腈购买于南京晴文生物科技有限公司。)
[0048]1h nmr(400mhz,chloroform
‑
d)δ8.32(s,1h),7.81(d,j=8.3hz,2h),7.36
‑
7.32(m,2h),7.23(d,j=8.1hz,2h),6.78
‑
6.74(m,2h),3.79(s,2h),3.09(s,6h)。
[0049]
第2步、化合物4
‑
(二苯胺)苯甲醛的制备
[0050][0051]
将7.75ml的dmf加入到三颈烧瓶内,置于冰浴中,9.5ml的pocl3逐滴加入,在0℃下搅拌40min,将温度增加到室温,然后,加入1g的三苯胺,反应在45℃下搅拌14h,冷却至室温,反应混合物缓慢倒入冰水浴中,用naoh中和,二氯甲烷萃取,合并有机相,有机相用无水mgso4干燥,过滤,浓缩有机层,用乙酸乙酯:石油醚=1:10(v/v)过柱,得到白色固体,产率:88.0%,0.98g;纯度99%以上。
[0052]1h nmr(400mhz,chloroform
‑
d)δ9.83(s,1h),7.73
‑
7.67(m,2h),7.40
‑
7.34(m,4h),7.22
‑
7.16(m,6h),7.06
‑
7.01(m,2h)。
[0053]
第三步、化合物(z)
‑2‑
(4
‑
(((e)4
‑
(二甲胺基)苯亚甲基)氨基)苯)3
‑
(4
‑
(二苯胺)苯基)丙烯腈的制备
[0054][0055]
将中间体(e)
‑2‑
(4
‑
(4
‑
(二甲胺基)苯亚甲基)氨基)苯基)乙腈(0.2634g,1mmol)溶于乙醇中,然后加入4
‑
(二苯胺)苯甲醛(0.2050g,0.75mmol),再加入1.2mmol叔丁醇钾,搅拌数小时,薄层色谱法点板跟踪至反应结束后,趁热抽滤后,用热乙醇洗涤,干燥得到橙色固体(z)
‑2‑
(4
‑
(((e)4
‑
(二甲胺基)苯亚甲基)氨基)苯)3
‑
(4
‑
(二苯胺)苯基)丙烯腈,产率:87.8%,0.3411g;纯度99%以上。
[0056]1h nmr(400mhz,dmso
‑
d6)δ8.48(s,1h),7.92(s,1h),7.87(d,j=9.0hz,2h),7.75(dd,j=14.5,8.8hz,4h),7.42
‑
7.37(m,4h),7.32(d,j=8.7hz,2h),7.20
‑
7.14(m,6h),6.97(d,j=8.9hz,2h),6.80(d,j=9.1hz,2h),3.03(s,6h).
13
c nmr(101mhz,dmso
‑
d6)δ
160.88,152.98,149.74,146.58,141.25,131.24,131.15,130.99,130.38,126.95,126.73,125.99,125.09,124.09,122.20,120.69,111.92.esi
‑
ms m/z:[probe]
+
calcd for c
36
h
30
n4519.25;found 519.2。
[0057]
下面对探针分子tpaa的荧光性质及其在水合肼检测中的应用进行进一步研究。
[0058]
实施例2探针分子tpaa在不同含水量的dmso
‑
h2o混合液中的荧光性能测试仪器:日立f7100型分子荧光光谱仪。
[0059]
实验方法为:将实施例1制得的探针分子tpaa溶解于dmso中得到1mm的探针母液,常温避光保存,用探针母液分别配制成0%、10%、20%、30%、40%、50%、60%、70%、80%、90%、98%含水量的dmso
‑
h2o混合液,浓度均为0.1mm。
[0060]
测量时分别移取1ml不同含水量的dmso
‑
h2o混合液到1cm比色皿中先后进行荧光光谱测试,如图1所示。随着含水率的增加,荧光强度逐渐增大。当含水量达到40%左右时,558nm处的荧光发射值最高。但随着水分的不断增加,荧光发射强度逐渐降低,是由于溶剂的极性随着含水量的增加而增加,刚性发光分子可以从局部发射(ie)态转移到扭曲分子电荷转移(tict)态。故选用40%含水量的探针溶液用于tpaa的后续测试。
[0061]
实施例3探针分子tpaa的紫外吸收光谱及荧光光谱性质测试
[0062]
测试仪器:pe 950s型紫外光谱仪,日立f7100型分子荧光光谱仪。
[0063]
实验方法为:将实施例1制得的探针分子tpaa溶解于dmso溶液中得到1mm的探针母液,常温保存,避光。实验测定中用dmso和h2o将溶液稀释成0.01mm的标准液进行测试。
[0064]
测量时移取3ml探针的dmso溶液到1cm比色皿中先后进行紫外吸收光谱及荧光光谱测试,如图2所示。结果表明:探针tpaa最强紫外吸收峰出现在420nm左右,荧光发射峰出现在537nm左右,斯托克位移达到117nm。这么大的斯托克位移,可以有效的克服因荧光自吸收而在生命体中难以应用的缺陷,实现探针在生命体中的应用。
[0065]
实施例4探针分子tpaa对其他干扰离子的荧光图
[0066]
测试仪器:日立f100型分子荧光光谱仪。
[0067]
实验方法为:将实施例1制得的探针分子tpaa溶解于dmso中得到1mm的探针母液,常温保存。取水合肼、四丁基氰化铵、znso4、agno3、co(no3)2、cuso4、fe2(so4)3、pbno3、nano2、nano3、kh2po4、nahso4、na2s、kcl、cacl2用二次水配置成0.01m母液。实验测定中将探针溶液稀释成10μm的标准溶液进行测试。
[0068]
测量时移取1ml探针的dmso溶液到1cm比色皿中分别滴加600μm的过氧化氢、四丁基氰化铵、naclo、na2s2o3、na2hpo4、mgso4、nano2、nahco3、nano3、kh2po4、k2co3、ch3coona、nahso3进行荧光测试。结果如图3所示。结果表明:探针tpaa对水合肼表现出明显的荧光增强现象,而对于一些生物体内常见的金属阳离子和酸根阴离子几乎没有什么影响,进一步说明探针tpaa具有优异的选择性,能够应用于生物体内。
[0069]
实施例5 tpaa的dmso溶液对水合肼的定量分析
[0070]
测试仪器:日立f7100型分子荧光光谱仪。
[0071]
实验方法为:将实施例1制得的探针分子tpaaa溶解于dmso中得到1mm的探针母液,常温保存。水合肼用二次水配置成0.01m母液,实验测定中将探针溶液稀释成1μm的标准溶液进行测试。
[0072]
采用标准加入法测试探针分子对水合肼的荧光响应,移取1ml的探针母液(10μm)
至比色皿中,每次加入1μl的水合肼检测荧光强度变化,水合肼含量加到600μm不再继续加入,如图4所示,随着水合肼含量的增加,在537nm处的荧光峰强度不断增强,因此,该探针对水合肼有较高的灵敏度,可用于生物体内微量水合肼的检测。
[0073]
实施例6探针分子tpaa在水合肼存在下的动力学实验
[0074]
测试仪器:日立f7100型分子荧光光谱仪。
[0075]
实验方法为:将实施例1制得的探针分子tpaa溶解于dmso中得到1mm的探针母液,常温保存。水合肼用二次水配置成0.01m母液。实验测定中将溶液稀释成10μm的标准溶液进行测试。
[0076]
移取1ml的探针母液(10μm)至比色皿中,设置荧光激发波长为420nm,分别测试探针,探针+水合肼溶液在不同的时间(0分钟、1分钟、2分钟、3分钟、5分钟、10分钟、15分钟、20分钟、25分钟)荧光强度的变化,如图5所示。实验结果表明,开始探针溶液的荧光强度随时间的增加而增强,探针+水合肼在20min内荧光强度达到最高值,后荧光强度趋于稳定,说明该探针响应迅速且稳定性较好。
[0077]
实施例7探针分子tpaa机理探究实验
[0078]
实验方法:首先根据相关报道文献推测探针tpaa与n2h4发生相互作用时可能的反应机制是:如图6在n2h4存在的情况下,tpaa的c=n键断裂,由此形成了一个含有氨基的化合物(1)和具有醛基的化合物(2),该醛基化合物会继续与n2h4作用,得到化合物(3),然后通过液相质谱esi
‑
ms分析数据证实(m/z:calculated for164.2和388.2;图7)。
[0079]
实施例8探针分子tpaa在hela细胞中对水合肼的成像研究。
[0080]
实验方法为:将实施例1制得的探针分子tpaa溶解于dmso中得到1mm的探针母液,常温保存。实验测定中用dmso和h2o将溶液稀释成0.01mm的标准液进行测试。
[0081]
为了证明探针在生物系统的实际应用,在共聚焦荧光显微镜下对细胞进行了在不同ph值下的生物荧光成像实验。将hela细胞接到培养皿中在37℃条件下培养24h,然后将tpaa标准液(10μm)加入到培养皿中,加入不同浓度的水合肼(50、100、150μm)继续孵育1小时后进行荧光成像,如图8所示。实验结果表明探针分子tpaa在随着水合肼浓度增加,荧光在不断增强。这些结果表明,探针tpaa可以作为检测细胞内水合肼的荧光标签进入细胞,因而具有在生物体内检测水合肼的潜力。
[0082]
需要说明的是,以上内容仅仅说明了本发明的技术思想,不能以此限定本发明的保护范围,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰均落入本发明权利要求书的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1