一种不饱和脂肪酸类化合物及其分离方法和应用
1.本发明涉及诺丽果化学领域,特别涉及一种不饱和脂肪酸类化合物及其分离方法和应用。
背景技术:
2.诺丽(morindacitrifolia)又名海巴戟,为茜草科(rubiaceae)海巴戟天属(morinda)的常绿灌木或小乔木,集中分布于热带、亚热带地区,在我国主要分布于海南岛、西沙群岛和台湾岛等地。《本草纲目》记载,“海巴戟”具有“扶正祛邪,滋阴补肾、壮阳,祛风湿、治冷宫不孕、治阳痿”之功。诺丽果是一种具有独特保健作用的聚花果,由其发酵产生的原汁(诺丽酵素)为广受欢迎的保健饮品,具有降三高(高血糖、高血压、高血脂)、抗肿瘤等功效。
3.研究报道诺丽果的化学成分主要为苯丙素(苷)类、黄酮(苷)类、二萜、三萜、环烯醚萜类、酚酸类等类型化合物,且都具有较好的生物活性。关于诺丽种子的化学成分研究报道较少。本发明旨在对诺丽种子化学成分研究,以期得到具有显著降血糖作用的新结构化合物,充分挖掘诺丽这一保健水果的药用价值。
4.专利cn202110344488.x不饱和脂肪酸类化合物及其制备方法和应用,从红背山麻杆中提取不饱和脂肪酸类化合物,该化合物具有加强神经细胞分化功能,没有说明本发明中不饱和脂肪酸类化合物对α
‑
葡萄糖苷酶的抑制作用。专利不饱和脂肪酸化合物及其制备方法和应用,该申请从从海洋真菌aspergillus sp.gdmcc 61218的发酵液中分离得到,这类不饱和脂肪酸化合物具有明显的抑制植物病原真菌活性,可用于制备抗植物病原真菌农药,该申请没有说明本发明中不饱和脂肪酸类化合物对α
‑
葡萄糖苷酶的抑制作用。因此本发明提出一种从诺丽果种子中提取得到具有抑制α
‑
葡萄糖苷酶作用的不饱和脂肪酸类化合物。
技术实现要素:
5.鉴以此,本发明提出一种新结构的不饱和脂肪酸类化合物,具有较好的α
‑
葡萄糖苷酶抑制作用,并提供目标化合物的分离方法。
6.本发明的技术方案是这样实现的:
7.包括以下步骤:
8.(1)将诺丽种子粉碎,制得诺丽种子粉末,加入石油醚超声提取,料液比为1kg:4~5l,提取次数为3~6次,提取时间为1~3h,合并提取液,将提取液减压浓缩制得浸膏;
9.(2)将步骤(1)制得的浸膏,使用硅胶柱洗脱分离,洗脱剂由石油醚和乙酸乙酯制得,制得洗脱组分1,即得fr.1~6组分;
10.(3)将fr.2组分先使用正相硅胶柱洗脱分离,洗脱剂由石油醚和乙酸乙酯制得,得到洗脱组分2,将洗脱组分2减压浓缩后,再经凝胶柱层析,洗脱剂为氯仿和甲醇混合液,得到洗脱组分3,将洗脱组分3减压浓缩后再经高效液相色谱仪制备,得到不饱和脂肪酸类化
合物i。
11.进一步的,步骤(1)中,所述超声频率为30~50khz,超声时间每次15
‑
30min。
12.进一步的,步骤(2)中,所述石油醚和乙酸乙酯的体积比为100~1:1。
13.进一步的,步骤(3)中,所述石油醚和乙酸乙酯的体积比为20~1:1,所述氯仿和甲醇体积比为5:1。
14.进一步的,步骤(3)中,所述凝胶柱型号为sephadex lh
‑
20。
15.进一步的,所述洗脱剂洗脱体积为3~6个柱体积。
16.进一步的,步骤(3)中,所述高效液相色谱仪的色谱条件为:色谱柱为c
18
(100
×
2.1mm,1.7μm),流速为2ml/min,流动相为体积比40:60的乙腈和水。
17.与现有技术相比,本发明的有益效果是:
18.本发明从诺丽种子中提取分离出不饱和脂肪酸类化合物i,具有良好的α
‑
葡萄糖苷酶抑制作用。进一步的,本发明通过极性溶剂浸提、溶剂梯度洗脱和液相色谱分离等多级分离提取方法,从诺丽种子中得到该不饱和脂肪酸类化合物。
附图说明
19.图1:化合物i的1h
‑
nmr谱(meod
‑
d4)
20.图2:化合物i的
13
c
‑
nmr谱(meod
‑
d4)
21.图3:化合物i的dept(135
°
)谱(meod
‑
d4)
22.图4:化合物i的1h
‑1h cosy谱(meod
‑
d4)
23.图5:化合物i的hsqc谱(meod
‑
d4)
24.图6:化合物i的hmbc谱(meod
‑
d4)
25.图7:化合物i的hresims谱
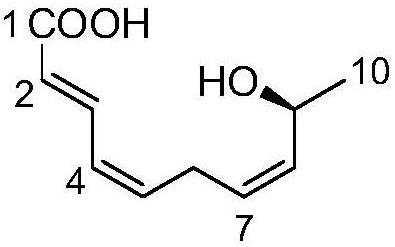
26.图8:化合物i结构图
具体实施方式
27.为了更好理解本发明技术内容,下面提供具体实施例,对本发明做进一步的说明。
28.本发明实施例所用的实验方法如无特殊说明,均为常规方法。
29.本发明实施例所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
30.实施例1诺丽果种子洗脱组分1的制备方法
31.(1)将诺丽种子粉碎,制得诺丽种子粉末,加入石油醚超声提取,超声频率为40khz,超声时间每次20min,料液比为1kg:4l,提取次数为4次,提取时间为2h,合并提取液,将提取液减压浓缩制得浸膏;
32.(2)称取50g步骤(1)制得的浸膏,使用硅胶柱洗脱分离,洗脱剂由石油醚和乙酸乙酯制得,依次采用石油醚和乙酸乙酯体积比为100:1、70:1、30:1、10:1、5:1、1:1进行洗脱,每个梯度收集3个柱体积,每个梯度得到一个组分,共得到6个组分,即组分1~6。
33.使用高效液相色谱仪检测含量,色谱条件为检测条件:
34.检测波长220nm;
35.色谱柱:waters c
18
(100
×
2.1mm,1.7μm);
36.进样体积:2μl;
37.流动相a:乙腈;流动相b:0.1%甲酸水;
38.洗脱梯度:(0~4min,5%~15%a;4.01~12min,15%~25%a;12.01~18min,25%~40%a;18.01~23min,40%~90%a;23.01~25min,90%~5%a)
39.体积比100:170:130:110:15:11:1含量(%)40.3743.1941.3139.1237.6135.13
40.实验结果表明,本发明中采用石油醚和乙酸乙酯体积比为70:1洗脱得到的不饱和脂肪酸类化合物含量最高。
41.实施例2诺丽果种子洗脱组分2的制备方法
42.将实施例1得到的洗脱组分2使用正相硅胶柱洗脱分离,洗脱剂由石油醚和乙酸乙酯制得,依次采用石油醚和乙酸乙酯体积比为100:1、70:1、30:1、10:1、5:1、1:1进行洗脱,收集各梯度洗脱组分进行检测。
43.检测条件同实施例1
44.体积比20:110:130:15:11:1含量(%)60.1365.1258.4253.1154.62
45.实验结果表明,本发明中使用正相硅胶柱层析,采用石油醚和乙酸乙酯体积比为10:1洗脱得到的不饱和脂肪酸类化合物含量最高。
46.实施例3诺丽果种子不饱和脂肪酸类化合物的制备方法
47.将实施例2得到的洗脱组分2进行减压浓缩,再经sephadex lh
‑
20凝胶柱层析,洗脱剂由体积比为1:1的氯仿和甲醇制得,洗脱量为4个柱体积,得到洗脱组分3,将洗脱组分3减压浓缩后再经高效液相色谱仪制备,色谱条件为:waters c
18
色谱柱,流速为2ml/min,流动相为体积比40:60的乙腈和水,得到不饱和脂肪酸类化合物i。
48.试验例1不饱和脂肪酸类化合物的结构鉴定
49.运用波谱(1h nmr,
13
c nmr,hsqc,hmbc,noesy)和ms等现代结构鉴定技术,确定实施例3不饱和脂肪酸类化合物i的化学结构。
50.结构鉴定数据如下:化合物i为无色油状物,易溶于甲醇。经高分辩质谱hresi(
‑
)ms(m/z181.0860[m
‑
h]
‑
,理论值181.0865)确定其分子式为c
10
h
14
o3;根据1h,
13
c及二维核磁共振数据确定其结构,骨架类型为不饱和脂肪酸。由于分子中只含有一个手性中心,经测定化合物i的旋光值为((c 0.10,meoh),对照文献数据,碳9位构型为s。因此,化合物鉴定为(s,2e,4z,7z)
‑9‑
羟基十碳
‑
2,4,7
‑
三烯酸[(s,2e,4z,7z)
‑9‑
hydroxydeca
‑
2,4,7
‑
trienoic acid],将其命名为moricitacid a,其1h和
13
cnmr数据归属见表1。
[0051]
表1.化合物i的1h
‑
nmr(400mhz)和
13
c
‑
nmr(100mhz)数据
[0052][0053]
经以上分析,确定化合物i结构,参见图8。
[0054]
试验例2药理活性实验
[0055]
实验材料:
[0056]
96孔板、恒温培养箱、酶标仪(elx800)、恒温振荡器、阿卡波糖(acarbose)、α
‑
葡萄糖苷酶、对硝基酚、对硝基苯
‑
α
‑
d
‑
葡萄糖苷
[0057]
实验方法:
[0058]
按要求配制好底物pnpg溶液,0.2mol/l的na2co3溶液,α
‑
葡萄糖苷酶的酶溶液,以阿卡波糖标准溶液为抑制剂。
[0059]
依次取已制备的50μl磷酸盐缓冲液(ph 6.8),20μl化合物i(终浓度分别为0.6,0.3,0.15,0.0725mg
·
ml
‑1),10μlα
‑
葡萄糖苷酶(1.0u
·
ml
‑1),20μl2.5mmol
·
l
‑1底物(对硝基苯基
‑
α
‑
d
‑
吡喃葡萄糖苷)溶液,混匀后在37℃下孵育15分钟,然后加入150μl na2co3溶液终止反应。供试品混合均匀后在405nm波长处测定吸光度(a)值,即在酶的作用下底物释放出的硝基酚量。平行测定3次,取平均值。按下式计算样品对α
‑
葡萄糖苷酶的抑制率:
[0060]
抑制率(%)=[1
‑
(a405nm sample
‑
a405nm blank)/a405nm control]
×
100
[0061]
式中,a405nm sample表示样品的a值,a405nm blank表示空白的a值(排除样品和酶的干扰),a405nm control表示排除样品干扰的a值。
[0062]
化合物的α
‑
葡萄糖苷酶抑制作用的结果如表2所示,从实验结果可知,化合物i表现出较好的α
‑
葡萄糖苷酶抑制效果,ic
50
为243μm。
[0063]
表2化合物i的α
‑
葡萄糖苷酶抑制活性
[0064]
化合物ic
50
/μmi243
a
acarbose135.4
[0065]
以上所述仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1