一种基于多肽Pep42构建的嵌合抗原受体免疫细胞制备及其应用
本发明属于免疫细胞治疗领域,具体涉及一种基于多肽pep42构建的嵌合抗原受体免疫细胞制备及其应用。
背景技术:
1、生物免疫治疗是一种新兴的,具有显著疗效的肿瘤治疗方法,是继手术、放疗、化疗后的第四大肿瘤治疗手段,它在不破坏机体免疫系统功能的前提下,通过特异性识别肿瘤细胞,进而消灭组织中的肿瘤细胞而实现治疗肿瘤的目的。免疫细胞疗法是生物免疫治疗中的一种重要类型,其中,又以过继免疫细胞治疗发展最为迅猛。嵌合抗原受体t细胞(chimeric antigen receptor-tcell,car-t)疗法是一种常见的过继免疫细胞疗法,该方法直接将可识别肿瘤抗原的基因片段(包括纳米抗体、单链抗体、细胞因子和配体等)与t细胞活化所需信号分子(包括cd3ζ链、cd28和4-1bb等共刺激分子)基因结合,构建成嵌合抗原受体(car),通过基因转导的方式导入并修饰t细胞,赋予t细胞识别肿瘤抗原并迅速活化杀伤肿瘤细胞的能力,能有效规避mhc的限制性。目前,car-t疗法在血液恶性肿瘤治疗方面取得了巨大成功,实体瘤治疗方面,存在car-t归巢难,肿瘤微环境抵抗和缺少肿瘤特异性或相关性抗原等问题,亟待解决。
2、内质网应激是细胞应对内质网蛋白积累产生的一种应答形式,可诱发未折叠蛋白反应(upr),即细胞通过减少蛋白质合成,促进蛋白质降解,增加内质网分子伴侣表达等方式缓解内质网压力,内质网应激持续时间过长或过强,超过细胞自身未折叠蛋白反应的调节能力,将会引起细胞代谢紊乱和凋亡等。肿瘤微环境中,由于缺氧、葡萄糖饥饿和酸中毒等不利因素的存在常引起内质网应激反应,肿瘤细胞通过激活未折叠蛋白反应来适应这些不利条件,避免死亡。葡萄糖调节蛋白78(grp78)又称bip蛋白,由hspa5基因编码,是内质网未折叠蛋白反应的关键分子。在内质网应激下,grp78可大量表达并促进蛋白质正确折叠,缓解内质网压力,具有极强的抗细胞凋亡能力。大量文献证明,grp78在肺癌、肝癌、结直肠癌等多种实体瘤细胞中表达上调,并部分转移到细胞膜表面参与pi3k/akt和jak2/stat3等信号通路的激活调控。grp78细胞膜转移的特性在正常细胞中很少见,提示csgrp78可作为cat-t治疗实体瘤的抗原,理论上具有很好的特异性和安全性。
3、因此,靶向csgrp78构建有效工作的car-t对实体瘤或其它csgrp78表达异常相关性疾病的治疗具有重要价值。
技术实现思路
1、本发明的目的是提供一种以基于环肽pep42构建的嵌合抗原受体免疫细胞及其制备和应用方法。
2、在本发明的第一方面,提供了一种嵌合抗原受体(car),其特征在于,所述的car含有一胞外结合域,所述的胞外结合域能够特异性地结合pep42受体,并且所述的胞外结合域具有环肽结构。
3、在另一优选例中,所述的环肽结构是基于小分子环肽pep42的环肽结构,并且特异性地结合pep42受体。
4、在另一优选例中,所述的car的胞外结合域除了含有针对pep42受体的具有环肽结构的第一胞外结构域之外,还包括针对额外靶点的第二胞外结构域。
5、在另一优选例中,所述的额外靶点为肿瘤特异性靶点。
6、在另一优选例中,所述的环肽结构位于胞外结合域的末端(即n端)或中间。
7、在另一优选例中,所述环肽结构的长度为12-15个氨基酸;较佳地13-15个氨基酸。
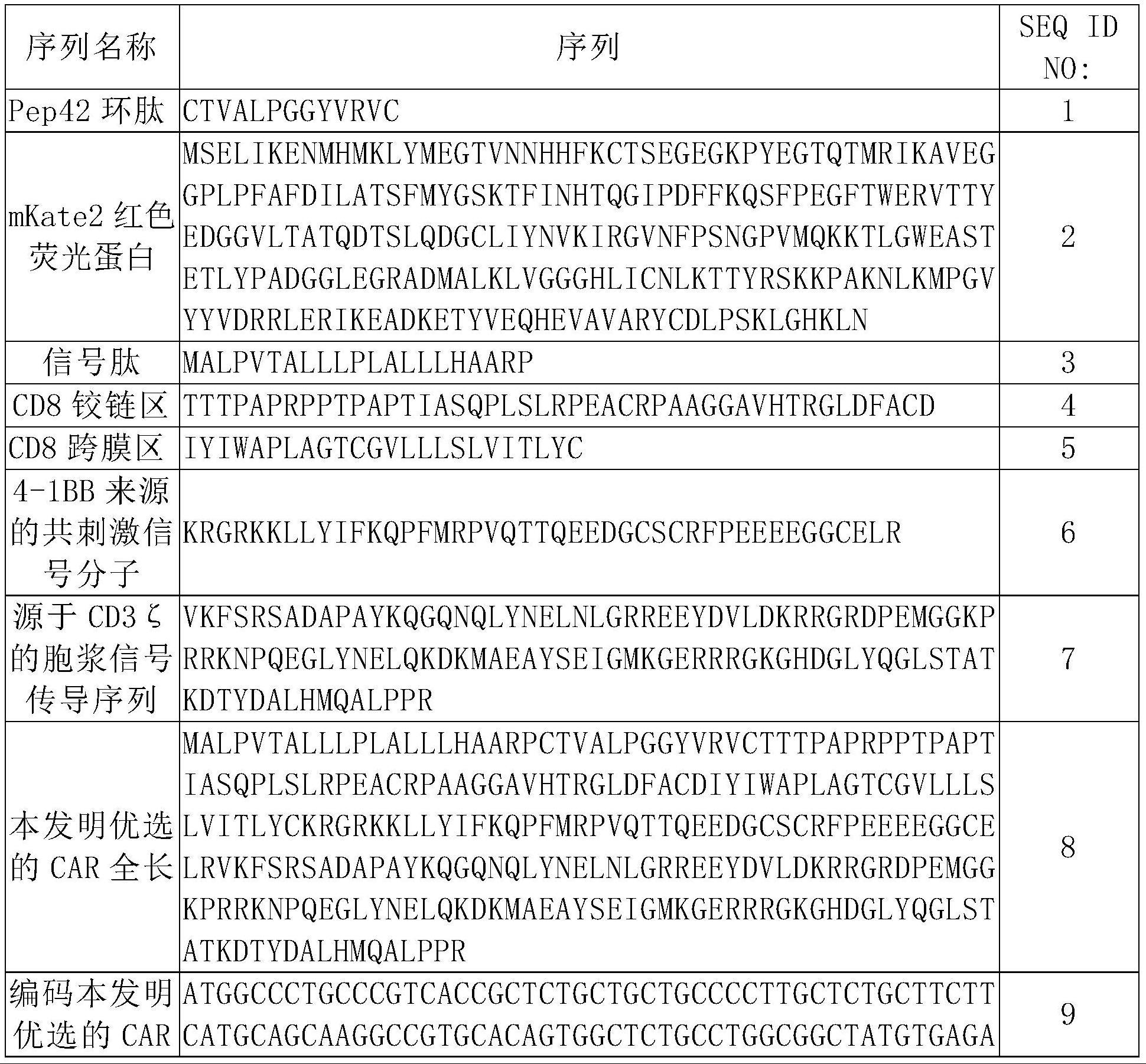
8、在另一优选例中,所述的环肽结构(或pep42肽段)具有如seq id no:1所示的氨基酸序列,或其氨基酸序列与seq id no:1的相同性≥85%,较佳地≥90%,更佳地≥93%,或与seq id no:1相比具有1、2或3个氨基酸的差异。
9、在另一优选例中,所述的pep42受体选自下组:细胞膜表面grp78(csgrp78)。
10、在另一优选例中,其特征在于,所述的胞外结合域包括pep42肽段,所述的pep42肽段具有如seq id no:1所示的氨基酸序列。
11、在另一优选例中,所述的胞外结合域具有如seq id no:1所示的氨基酸序列。
12、在另一优选例中,所述的pep42肽段与葡萄糖调节蛋白78(grp78)受体具有特异性结合。
13、在另一优选例中,所述的grp78是位于细胞膜表面(或膜结合)的grp78蛋白(csgrp78)。
14、在另一优选例中,所述的grp78蛋白来源于人或非人哺乳动物。
15、在另一优选例中,所述非人哺乳动物包括:啮齿动物(如大鼠、小鼠)、灵长动物(如猴);优选为灵长动物。
16、在另一优选例中,所述的grp78蛋白是人源的或猴源的。
17、在另一优选例中,所述的grp78蛋白是人源的。
18、在另一优选例中,所述的pep42具有如seq id no:1所示的氨基酸序列。
19、在另一优选例中,所述car的结构如下式i所示:
20、l-eb-h-tm-c-cd3ζ-rp (i)
21、式中,
22、各“-”独立地为连接肽或肽键;
23、l是无或信号肽序列;
24、eb是胞外结合域;
25、h是无或铰链区;
26、tm是跨膜结构域;
27、c是无或共刺激信号分子;
28、cd3ζ是源于cd3ζ的胞浆信号传导序列;
29、rp是无或报告蛋白。
30、在另一优选例中,所述的报告蛋白rp中还包括位于其n端的自剪切识别位点,优选地为t2a序列。
31、在另一优选例中,所述的报告蛋白rp为荧光蛋白。
32、在另一优选例中,所述的报告蛋白rp为mkate2红色荧光蛋白。
33、在另一优选例中,所述的mkate2红色荧光蛋白的氨基酸序列如seq id no:2所示。
34、在另一优选例中,所述的l是选自下组的蛋白的信号肽:cd8、cd28、gm-csf、cd4、cd137、或其组合。
35、在另一优选例中,所述的l是cd8来源的信号肽。
36、在另一优选例中,所述l的氨基酸序列如seq id no:3所示。
37、在另一优选例中,所述的h是选自下组的蛋白的铰链区:cd8、cd28、cd137、或其组合。
38、在另一优选例中,所述的h是cd8来源的铰链区。
39、在另一优选例中,所述h的氨基酸序列如seq id no:4所示。
40、在另一优选例中,所述的tm是为选自下组的蛋白的跨膜区:cd28、cd3epsilon、cd45、cd4、cd5、cd8、cd9、cd16、cd22、cd33、cd37、cd64、cd80、cd86、cd134、cd137、cd154、或其组合。
41、在另一优选例中,所述的tm是cd8来源的跨膜区。
42、在另一优选例中,所述tm的氨基酸序列如seq id no:5所示。
43、在另一优选例中,所述的c是选自下组的蛋白的共刺激信号分子:ox40、cd2、cd7、cd27、cd28、cd30、cd40、cd70、cd134、4-1bb(cd137)、pd1、dap10、cds、icam-1、lfa-1(cd11a/cd18)、icos(cd278)、nkg2d、gitr、tlr2,或其组合。
44、在另一优选例中,所述的c是4-1bb来源的共刺激信号分子。
45、在另一优选例中,所述c的氨基酸序列如seq id no:6所示。
46、在另一优选例中,所述的源于cd3ζ的胞浆信号传导序列的氨基酸序列如seq idno:7所示。
47、在另一优选例中,所述的嵌合抗原受体car的氨基酸序列如seq id no:8所示。
48、在本发明的第二方面,提供了一种核酸分子,所述核酸分子编码如本发明第一方面所述的嵌合抗原受体。
49、在本发明的第三方面,提供了一种载体,其特征在于,所述的载体含有如本发明第二方面所述的核酸分子。
50、在另一优选例中,所述的载体选自下组:dna、rna、质粒、慢病毒载体、腺病毒载体、逆转录病毒载体、转座子、或其组合。
51、在另一优选例中,所述载体为慢病毒载体。
52、在另一优选例中,所述载体选自下组:ptomo慢病毒载体、plenti、plvth、pljm1、phcmv、plbs.cag、phr、plv等。
53、在另一优选例中,所述的载体是ptomo慢病毒载体。
54、在另一优选例中,所述载体中还包括选自下组的:启动子、转录增强元件wpre、长末端重复序列ltr等。
55、在另一优选例中,所述载体包含如seq id no:9所示的核苷酸序列。
56、在本发明的第四方面,提供了一种宿主细胞,所述的宿主细胞含有如本发明第三方面所述的载体或染色体中整合有外源的如本发明第二方面所述的核酸分子或表达如本发明第一方面所述的car。
57、在本发明的第五方面,提供了一种工程化免疫细胞,所述的免疫细胞含有如本发明第三方面所述的载体或染色体中整合有外源的如本发明第二方面所述的核酸分子或表达如本发明第一方面所述的car。
58、在另一优选例中,所述的工程化免疫细胞选自下组:t细胞、nk细胞、nkt细胞,或巨噬细胞。
59、在另一优选例中,所述的工程化的免疫细胞是嵌合抗原受体t细胞(car-t细胞)或嵌合抗原受体nk细胞(car-nk细胞)。
60、在另一优选例中,所述的工程化免疫细胞是car-t细胞。
61、在本发明的第六方面,提供了一种制备如本发明第五方面所述的工程化免疫细胞的方法,包括以下步骤:将如本发明第二方面所述的核酸分子或如本发明第三方面所述的载体转导入免疫细胞内,从而获得所述工程化免疫细胞。
62、在另一优选例中,所述的方法还包括对获得的工程化免疫细胞进行功能和有效性检测的步骤。
63、在本发明的第七方面,提供了一种药物组合物,所述药物组合物含有如本发明第一方面所述的car、如本发明第二方面所述的核酸分子、如本发明第三方面所述的载体、如本发明第四方面所述的宿主细胞,和/或如本发明第五方面所述的工程化免疫细胞,以及药学上可接受的载体、稀释剂或赋形剂。
64、在另一优选例中,所述制剂为液态制剂。
65、在另一优选例中,所述制剂的剂型为注射剂。
66、在另一优选例中,所述制剂中所述工程化的免疫细胞的浓度为1×103-1×108个细胞/ml,较佳地1×104-1×107个细胞/ml。
67、在本发明的第八方面,提供了一种如本发明第一方面所述的car、如本发明第二方面所述的核酸分子、如本发明第三方面所述的载体、或如本发明第四方面所述的宿主细胞,和/或如本发明第五方面所述的工程化免疫细胞的用途,用于制备预防和/或治疗肿瘤药物或制剂。
68、在另一优选例中,所述的药物或制剂还用于预防和/或治疗其他pep42受体异常表达相关的疾病。
69、在另一优选例中,所述的pep42受体包括但不限于csgrp78等。
70、在另一优选例中,所述的其他pep42受体异常表达相关的疾病包括但不限于肿瘤、衰老、肥胖、心血管疾病、糖尿病、神经退行性疾病、感染性疾病等。
71、在另一优选例中,所述的其他pep42受体异常表达相关的疾病包括:csgrp78异常表达相关的疾病。
72、在另一优选例中,所述的pep42受体异常表达是指所述pep42受体过度表达。
73、在另一优选例中,所述pep42受体过度是指所述pep42受体表达量为正常生理状况下表达量的≥1.5倍,较佳地≥2倍,更佳地≥2.5倍。
74、在另一优选例中,所述的csgrp78异常表达相关的疾病包括:肿瘤、衰老、心血管疾病、肥胖等。
75、在另一优选例中,所述的疾病是csgrp78高表达(即csgrp78阳性)的恶性肿瘤。
76、在另一优选例中,所述肿瘤包括血液肿瘤和实体瘤。
77、在另一优选例中,所述血液肿瘤选自下组:急性髓细胞白血病(aml)、多发性骨髓瘤(mm)、慢性淋巴细胞白血病(cll)、急性淋巴白血病(all)、弥漫性大b细胞淋巴瘤(dlbcl)等,或其组合。
78、在另一优选例中,所述的实体瘤选自下组:乳腺癌、胃癌、肝胆癌、结直肠癌、膀胱癌、非小细胞肺癌、卵巢癌和食道癌、胶质细胞瘤、肺癌、胰腺癌、前列腺癌等,或其组合。
79、在本发明的第九方面,提供了一种如本发明第五方面所述的工程化免疫细胞、或如本发明第七方面所述的药物组合物的用途,用于预防和/或治疗癌症或肿瘤。
80、在本发明的第十方面,提供了一种治疗疾病的方法,包括给需要治疗的对象施用有效量的如本发明第五方面所述的工程化免疫细胞、或如本发明第七方面所述的药物组合物。
81、在另一优选例中,所述疾病为pep42受体异常表达相关的疾病。
82、在另一优选例中,所述疾病为癌症或肿瘤。
83、在另一优选例中,所述的工程化免疫细胞或药物组合物中所包含的car免疫细胞是来源于所述对象的细胞(自体细胞)。
84、在另一优选例中,所述的工程化免疫细胞或药物组合物中所包含的car免疫细胞是来源于健康个体的细胞(异体细胞)。
85、在另一优选例中,所述的方法可与其他治疗方法联合使用。
86、在另一优选例中,所述的其他治疗方法包括化疗、放疗、靶向治疗等方法。
87、应理解,在本发明范围内中,本发明的上述各技术特征和在下文(如实施例)中具体描述的各技术特征之间都可以互相组合,从而构成新的或优选的技术方案。限于篇幅,在此不再一一累述。
- 还没有人留言评论。精彩留言会获得点赞!