一种人冠状病毒HCoV-229E的MNP标记位点、引物组合物、试剂盒及其应用
一种人冠状病毒hcov-229e的mnp标记位点、引物组合物、试剂盒及其应用
技术领域
1.本发明实施例涉及生物技术领域,特别涉及一种人冠状病毒hcov-229e的mnp标记位点、引物组合物、试剂盒及其应用。
背景技术:
2.冠状病毒在系统分类上属冠状病毒属(coronavirus),基因组为线性单股正链的rna 病毒,是自然界广泛存在的一大类病毒。病毒有包膜,电子显微镜观察这些包膜上有形状类似日冕的棘突,故命名这类病毒为冠状病毒。冠状病毒通过呼吸道分泌物排出体外,经口液、喷嚏、接触传染,并通过空气飞沫传播。冠状病毒感染分布在全世界多个地区,并多次引起大流行。新冠肺炎的病原菌新型冠状病毒(2019-ncov或sars-cov-2,引发新型冠状病毒肺炎covid-19)是目前已知的第7种可以感染人的冠状病毒,其余6种分别是hcov-229e、hcov-oc43、hcov-nl63、hcov-hku1、sars-cov(引发重症急性呼吸综合征)和mers-cov(引发中东呼吸综合征)。hcov-229e是具有急性呼吸道症状的成年患者的常见和重要病原体,通常会导致较轻的流感样疾病。潜伏期范围为2-5d,主要在冬季流行,人群普遍易感,通过呼吸道飞沫传播。
3.现有的人冠状病毒检测技术主要通过病毒的分离鉴定,依赖于检测病原和抗体进行血清型鉴定、间接或直接免疫荧光法和检测遗传物质的分子检测技术,包括pcr、核苷酸杂交和测序技术。这些技术各有优势,但在时长、操作复杂度、检测通量、检测变异的准确性和灵敏度、成本等方面也存在一个或多个局限。比如病毒分离鉴定操作复杂、耗时长;血清型鉴定、间接或直接免疫荧光法容易出现交叉反应,导致检测不准确,且不能监测变异;pcr检测技术一次反应仅针对一种病毒的1到2个标记进行检测,效率低下,且容易由于病毒的变异导致检测失败。宏基因组测序技术是另一种检测人冠状病毒的技术,但其往往包括大量的宿主测序数据,对低病毒载量的样本进行检测时,尤其需要超深度的测序,导致高的成本。
4.因此,开发快速、准确的、一次性高通量的检测分型多种人冠状病毒的人冠状病毒检测分析方法对于人冠状病毒的检测和防疫都具有重要意义。
技术实现要素:
5.本发明目的是提供一种人冠状病毒hcov-229e的mnp标记位点、引物组合物、试剂盒及其应用,可以对人冠状病毒hcov-229e进行鉴定和变异检测,具有多靶标、高通量、高灵敏和精细分型的效果。
6.在本发明的第一方面,提供了一种人冠状病毒hcov-229e的mnp标记位点,所述mnp 标记位点是指在人冠状病毒hcov-229e基因组上筛选的物种特异的且在物种内部具有多个核苷酸多态性的基因组区域,包括人冠状病毒hcov-229e参考基因组nc_002645.1上的8 个标记。
7.说明书表1对其进行了进一步的说明,表1中标注的所述mnp标记位点的起始和终止位置是基于表1中mnp同一行对应的参考序列确定的。
8.在本发明的第二方面,提供了一种用于检测所述mnp标记位点的多重pcr引物组合物,所述多重pcr引物组合物包括8对引物,每个mnp标记位点的引物包括上引物和下引物,具体的引物核苷酸序列如seq id no.1~seq id no.16所示。说明书表1对其进行了进一步的说明。
9.在本发明的第三方面,提供了一种用于检测所述人冠状病毒hcov-229e mnp标记位点的检测试剂盒,所述试剂盒包括所述的引物组合物。
10.进一步地,所述试剂盒还包括多重pcr预混液。
11.以及上述标记、引物组合物和试剂盒在非疹断目的的人冠状病毒hcov-229e定性检测中的应用,在制备人冠状病毒hcov-229e定性检测产品中的应用。
12.在本发明的第四方面,提供了所述的人冠状病毒hcov-229e的mnp标记位点或者所述的多重pcr引物组合物或者所述的检测试剂盒在人冠状病毒hcov-229e的鉴定、dna 指纹数据库的构建、遗传变异检测中的应用。
13.以上所述的应用中,首先是获取待测样本的病毒总rna;利用商业化试剂盒对所述总 rna进行cdna合成;利用本发明的试剂盒对所述cdna和空白对照进行第一轮多重pcr 扩增,循环数不高于25个;对扩增产物进行纯化后,进行基于第二轮pcr扩增的样本标签和二代测序接头添加;对第二轮扩增产物纯化后定量;检测多个毒株时通过将第二轮扩增产物等量混合后进行高通量测序;测序结果比对到所述的人冠状病毒hcov-229e的参考序列上,获取在所述cdna中的检测序列数目和基因型数据。根据在所述cdna和所述空白对照获得的人冠状病毒测序序列数量和检出mnp标记位点的数目,对所述cdna的测序数据进行数据质量控制和数据分析,获得在所述样本中检出的人冠状病毒hcov-229e的mnp 标记位点数目、覆盖每个所述mnp标记位点的测序序列数目和所述mnp标记位点基因型数据。
14.当用于人冠状病毒hcov-229e鉴定时,根据在待测样品和空白对照中检出的人冠状病毒hcov-229e的测序序列数量和检出mnp位点的数目,进行质控后判定待测样品中是否含有人冠状病毒hcov-229e的核酸。其中,所述的质控方案和判定方法是以拷贝数已知的人冠状病毒hcov-229e的rna为检测样本,评估所述试剂盒检测人冠状病毒hcov-229e 的灵敏度、准确性和特异性,制定所述试剂盒检测人冠状病毒hcov-229e时的质控方案和判定方法。
15.当用于人冠状病毒hcov-229e遗传变异检测时,包括hcov-229e感染病例个体间和个体内部毒株的遗传变异检测。个体间毒株的遗传变异检测包括利用所述的试剂盒和方法,获得待比较个体所感染毒株在8个mnp标记位点的基因型数据。通过基因型比对,分析毒株间在所述8个mnp标记位点上的主基因型是否存在差异。若所比较毒株在至少一个mnp 标记位点的主基因型存在变异,则判定两者存在遗传变异。作为一种备选方案,也可以通过单重pcr对待比较毒株的8个标记分别进行扩增,然后对扩增产物进行sanger测序,获得序列后,对待比较毒株每个mnp标记位点的基因型进行比对。如果存在主基因型不一致的mnp标记位点,则待比较毒株之间存在变异。当检测个体所感染的毒株内部是否存在遗传变异时,则通过统计模型判定在个体内部检测到的毒株在所述的mnp标记位点是否检出主基因型以外的次基因型。若至少一个mnp标记位点存在次基因型,则判定所测毒株内部存在遗传变
异。
16.当用于构建人冠状病毒hcov-229e的mnp指纹数据库时,将从样本中鉴定的人冠状病毒hcov-229e的所述mnp标记位点的基因型数据,录入数据库文件,构成人冠状病毒 hcov-229e的mnp指纹数据库;每次鉴定不同的样本时,通过和所述人冠状病毒 hcov-229e的mnp指纹数据库比对,鉴定样本中的人冠状病毒hcov-229e是否和数据库中的毒株在所述mnp标记位点存在主基因型(在一个mnp标记位点具有超过50%测序片段支持的基因型)的差异,在至少1个mnp标记位点存在主基因型差异的人冠状病毒 hcov-229e即为新的变异类型,收录进mnp指纹数据库。
17.以上所述的应用中,当用于人冠状病毒hcov-229e分型检测时,是对待测样本中的人冠状病毒hcov-229e进行鉴定,获得每个所述mnp位点的基因型;收集网上公开的人冠状病毒hcov-229e的基因组序列和已构建的人冠状病毒hcov-229e mnp指纹数据库组成人冠状病毒hcov-229e参考序列库;将待测样本中人冠状病毒hcov-229e的基因型和所述人冠状病毒hcov-229e的参考序列库进行比对,筛选遗传上一致或最接近的毒株,获得待测样本中人冠状病毒hcov-229e的分型。根据同所述参考序列库的比对结果,鉴定样品中的人冠状病毒hcov-229e是已有的型还是新的变型,实现对人冠状病毒hcov-229e的精细分型。
18.本发明实施例中的一个或多个技术方案,至少具有如下技术效果或优点:
19.本发明提供了一种人冠状病毒hcov-229e的mnp标记位点、引物组合物、试剂盒及其应用,所提供的人冠状病毒hcov-229e的8个mnp标记位点和其引物组合,可进行多重pcr扩增,融合二代测序平台进行扩增产物的测序,满足对人冠状病毒hcov-229e进行高通量、高效率、高准确性和高灵敏度检测的需求,满足人冠状病毒hcov-229e标准的、可共享的指纹数据构建的要求;满足准确检测人冠状病毒hcov-229e感染病例个体间和个体内部毒株的遗传变异的需求。本发明在人冠状病毒hcov-229e领域属于首创,并未见相关文献报道。
附图说明
20.为了更清楚地说明本发明实施例中的技术方案,下面将对实施例描述中所需要使用的附图作一简单地介绍,显而易见地,下面描述中的附图是本发明实施例的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其它的附图。
21.图1为mnp标记位点多态性原理图;
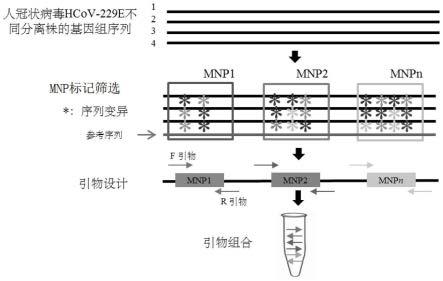
22.图2为人冠状病毒hcov-229e mnp标记位点的筛选和引物设计流程图;
23.图3为mnp标记位点的检测流程图。
具体实施方式
24.下文将结合具体实施方式和实施例,具体阐述本发明实施例,本发明实施例的优点和各种效果将由此更加清楚地呈现。本领域技术人员应理解,这些具体实施方式和实施例是用于说明本发明实施例,而非限制本发明实施例。
25.在整个说明书中,除非另有特别说明,本文使用的术语应理解为如本领域中通常所使用的含义。因此,除非另有定义,本文使用的所有技术和科学术语具有与本发明实施例所属领域技术人员的一般理解相同的含义。若存在矛盾,本说明书优先。
26.除非另有特别说明,本发明实施例中用到的各种原材料、试剂、仪器和设备等,均可通过市场购买得到或者可通过现有方法制备得到。
27.本技术实施例的技术方案为解决上述技术问题,总体思路如下:
28.筛选适用于检测群体生物的mnp标记位点作为检测目标。mnp标记位点是指在基因组上一段区域内由多个核苷酸引起的多态性标记。与ssr标记和snp标记相比,mnp标记位点具有以下优势:(1)等位基因丰富,单个mnp位点上有2n种等位基因,高于ssr和snp,适用于微生物这种典型的群体生物的检测;(2)物种区分能力强,只需要少量的mnp 标记位点就能实现物种鉴定,减少了检测错误率。检测mnp标记位点的mnp标记位点法融合超多重pcr和二代高通量测序技术,具有以下优势:(1)输出的是碱基序列,无需平行实验,可构建标准化的数据库进行共享;(2)高效率,利用样品dna条形码,突破测序样品数量的局限,可一次性对成百上千份样本的数万个mnp位点分型;(3)高灵敏度,利用多重pcr一次检测多个靶标,避免单个靶标扩增失败导致高的假阴性和低的灵敏度;(4) 高准确性,利用二代高通量测序仪对扩增产物测序数百次。
29.鉴于以上优点和特性,mnp标记位点及其检测技术mnp标记位点法可实现群体生物多等位基因型的分类与溯源,在病原微生物的鉴定、指纹数据库构建、遗传变异检测等方面都具有应用潜力。目前在微生物中,尚未有关于mnp标记位点的报道,也缺乏相应的技术。mnp标记位点法的开发、筛选和应用在植物中具有较好的应用基础。
30.因此,本发明开发了人冠状病毒hcov-229e的mnp标记位点,所述mnp标记位点为在人冠状病毒hcov-229e基因组上筛选的区分于其他物种且在物种内部具有多个核苷酸多态性的基因组区域,包括:以nc_002645.1为参考基因组的mnp-1~mnp-15的8个mnp 标记位点。
31.接着,本发明开发了用于检测所述人冠状病毒hcov-229e特异的mnp标记位点的多重pcr引物组合物,所述多重pcr引物组合物包括8对引物,所述8对引物的核苷酸序列如seq id no.1~seq id no.16所示。所述引物互相间不冲突,可以通过多重pcr进行高效的扩增;
32.所述多重pcr引物组合物可以用于检测人冠状病毒hcov-229e mnp标记位点的检测试剂盒。所述试剂盒能够稳定、灵敏地检测低至10拷贝/反应的hcov-229e。
33.本发明的重现性试验中每个样品不同文库间、不同建库批次间mnp标记位点主基因型的差异对数为0,重现率r=100%,准确率a=100%。
34.本发明的mnp标记位点和所述试剂盒在复杂模板中检测目标微生物具有高特异性。
35.下面将结合实施例、对比例及实验数据对本技术的一种人冠状病毒hcov-229e的mnp 标记位点、引物组合物、试剂盒及其应用进行详细说明。
36.实施例1、人冠状病毒hcov-229e mnp标记位点的筛选和多重pcr扩增引物的设计
37.s1、人冠状病毒hcov-229e mnp标记位点的筛选
38.基于网上公开的hcov-229e的547个、hcov-hku1的518个、hcov-nl63的913个、 hcov-oc43的1426个、mers-cov的1438、sars-cov-2的40855和sars-cov的44326 个基因组为参考序列,通过序列比对,和与ncbi数据库对比,获得15个hcov-229e特异的mnp标记位点。对于网上不存在基因组数据的物种,也可以通过高通量测序获得待检测微生物物种代表分离株的基因组序列信息,其中高通量测序可以是全基因组或简化基因组测序。为了保
证所筛选标记的多态性,一般使用至少10个遗传上具有代表性的分离株的基因组序列作为参考。
39.筛选的8个mnp标记位点如表1及如seq id no.1-seq id no.16所示:
40.表1所述mnp标记位点以及检测引物在参考序列上的起始位置
[0041][0042]
所述步骤s1具体包括:
[0043]
选择所述人冠状病毒hcov-229e的一个或多个代表株的基因组序列作为参考基因组,将所述基因组序列和所述参考基因组进行序列比对,获得所述人冠状病毒hcov-229e各毒株的单核苷酸多态性标记;
[0044]
在所述参考基因组上,以100-300bp为窗口,以1bp为步长进行窗口平移,筛选获得多个候选mnp标记位点区域,其中,所述候选mnp标记位点区域含有≥2个所述单核苷酸变异标记,且两端各30bp的序列上均不存在所述单核苷酸多态性标记;
[0045]
在所述候选多核苷酸多态性标记区域中筛选区分度dp≥0.2的区域作为mnp标记位点;其中,dp=d/t,t是在所述候选多核苷酸多态性标记区域中所有小种两两比较时的比较对数, d是在所述候选多核苷酸多态性标记区域中至少两个单核苷酸多态性差异的样品对数。
[0046]
作为一种可选的实施方式,在所述参考基因组上,以100-300bp为窗口进行筛选时,也可选用其他步长,本实施方式采用步长为1bp,有利于全面的筛选。
[0047]
s2、多重pcr扩增引物的设计
[0048]
通过引物设计软件设计所述mnp标记位点的多重pcr扩增引物,引物设计遵循引物间互不干扰,所有引物可以组合成引物池进行多重pcr扩增,即所有设计的引物可以在一个扩增反应中均正常扩增。
[0049]
s3、引物组合的检测效率评估
[0050]
使用湖北省疾控预防控制中心提供的拷贝数已知的人冠状病毒hcov-229e rna,
经商业化试剂盒反转录成cdna,加入到2ng/反应的人基因组dna中,制备成1000拷贝/反应的模板。使用所设计的引物组合,通过多重pcr结合二代测序的检测方法进行检测,构建 4个重复的检测文库。根据4个重复检测文库的测试结果,最终获得本发明提供的兼容性最好的8个mnp标记位点及其检测引物组合物,具体如表1以及seq id no.1-seq id no.16 所示。
[0051]
实施例2、所述mnp标记位点和引物鉴定人冠状病毒hcov-229e的性能评估和阈值设置
[0052]
1、mnp标记位点的检测
[0053]
本实施例中,将拷贝数已知的人冠状病毒hcov-229e核苷酸标准品经商业化试剂盒反转录成cdna后,加入到人基因组dna中,制备成1拷贝/反应、10拷贝/反应和100拷贝 /反应的人冠状病毒hcov-229e模拟样本,同时设置的等体积的无菌水作为空白对照。本实施例共计上述4个样本,每个样本每天构建3个重复文库,连续检测4天,即每个样本获得12组测序数据,具体如表2所示。根据在12次重复实验中,在空白对照和人冠状病毒 hcov-229e核苷酸标准品中检出的人冠状病毒hcov-229e的mnp标记位点的测序片段数和标记数,评估检测方法的重现性、准确性、灵敏度,制定质控体系污染和目标病原体检出的阈值和判定标准。
[0054]
mnp标记位点的检测流程如图3所示。
[0055]
表2-人冠状病毒hcov-229e的mnp标记位点法的检测灵敏度、稳定性分析
[0056][0057][0058]
如表2所示,在1拷贝/反应的12组数据中,能检出1-2个mnp位点,而在空白对照中部分也能检出1个位点;在10拷贝/反应的12组数据中,能稳定的检出至少6个mnp 标记位点,远远的高于空白对照中检出的mnp位点数目,表明所述试剂盒能够稳定、灵敏地检测低至10拷贝/反应的hcov-229e。
[0059]
2、mnp标记位点检测试剂盒检测人冠状病毒hcov-229e的重现性和准确性评估
[0060]
基于两次重复中,共同检出标记的基因型是否可重现,评估mnp标记位点检测方法检测人冠状病毒hcov-229e的重现性和准确性。具体地,对表2所示的100拷贝/反应样品的 12组数据分别进行两两比较,结果如表3所示,主基因型存在差异的mnp标记位点数目都为0;依据2次重复实验间可重现的基因型认为是准确的原则,准确率a=1-(1-r)/2=0.5+0.5r, r代表重现率,即主基因型可重现的标记数目占共有标记数目的比率。本项目重现性
试验中每个样品不同文库间、不同建库批次间mnp标记位点主基因型的差异对数为0,重现率r =100%,准确率a=100%。
[0061]
表3人冠状病毒hcov-229e mnp标记位点检出方法的重现性和准确率评估
[0062][0063]
3、mnp标记位点检测试剂盒检出人冠状病毒hcov-229e的阈值判定
[0064]
如表2所示,在1个拷贝/反应的样本中能检出比对到人冠状病毒hcov-229e的序列,至少覆盖2个mnp标记位点。而在部分空白对照中也检出了人冠状病毒hcov-229e的序列。由于mnp标记位点检测方法的极度灵敏,因此检测过中的数据污染容易导致假阳性的产生。因此本实例中制定如下质控方案。
[0065]
质控方案具体如下:
[0066]
1)测序数据量大于2.5百万碱基。测算依据是每个样品检测mnp标记位点的数目是8 个,一条测序片段的长度是300个碱基,所以当数据量大于2.5百万碱基时,大部分样品一次实验可以保证覆盖每个标记的测序片段数量达到1000倍,保证对每个mnp标记位点碱基序列的精准分析。
[0067]
2)根据测试样品中的人冠状病毒hcov-229e的信号指数s和空白对照中人冠状病毒 hcov-229e的噪音指数p判定污染是否可接受,其中:
[0068]
空白对照噪音指数p=nc/nc,其中nc和nc分别代表空白对照中,人冠状病毒hcov-229e 的测序片段的数量和总测序片段数量。
[0069]
测试样品的信号指数s=nt/nt,其中nt和nt分别代表测试样品中,人冠状病毒hcov-229e 的测序片段的数量和总测序片段数量。
[0070]
3)计算测试样品中mnp标记位点的检出率,指的是检出标记数和总设计标记数的比值。
[0071]
表4待测样品中人冠状病毒hcov-229e的信噪比
[0072][0073]
如表4所示,人冠状病毒hcov-229e在空白对照中的噪音指数平均值是0.04%,而在 1个拷贝的样品中的信号指数平均值是0.27%,1个拷贝的样品和空白对照的信噪比的平均值是6.75,因此,本发明规定当信噪比大于10倍时,可判定检测体系中的污染是可接受的。在10个拷贝的样品和空白对照的信噪比的平均值是68.3,在10拷贝/反应的12组数据中,能稳定的检出至少6个mnp标记位点,占总标记的75%。因此,在保证准确性的情况下,本标准规定人冠状病毒hcov-229e的信噪比判定阈值是34,即当样品中人冠状病毒 hcov-229e的信噪比大于34,且标记检出率大于等于37.5%时,判定样本中检出了人冠状病毒hcov-229e的核苷酸。基于所设置判定阈值,本发明所提供的试剂盒能准确、灵敏的检测到低至10拷贝/反应的人冠状病毒hcov-229e。
[0074]
4、mnp标记位点检测方法检测人冠状病毒hcov-229e的特异性评估
[0075]
人为的将人冠状病毒hcov-229e和人冠状病毒hcov-nl63、hcov-hku1、 hcov-oc43 sars-cov-2、以及人副流感病毒、偏肺病毒、人鼻病毒、流行性腮腺炎病毒、麻疹病毒、呼吸道合胞病毒、甲型流感病毒、乙型流感病毒、丙型流感病毒、禽流感病毒和寨卡病毒的rna混在一起,制备混合模板,以空白模板作为对照,采用本发明所提供的试剂盒对混合模板中的病原体进行检测,进行3个重复实验。结果在3次重复中,在混合模板中获得的测序序列都仅能特异的比对到hcov-229e的8个mnp位点。按照所述的质控方案和阈值进行判定后,在3个重复实验中都能特异的检出hcov-229e,表明mnp标记位点和所述试剂盒在复杂模板中检测目标微生物的高特异性。
[0076]
实施例3、人冠状病毒hcov-229e感染病例个体间毒株的遗传变异检测
[0077]
利用所述的试剂盒和mnp标记位点检测方法对对收集到的一个人冠状病毒 hcov-229e毒株不同时期繁殖的6份拷贝毒株进行检测,样本依次命名为s1-s6,每个mnp 标记位点的测序平均覆盖倍数达3000倍,每个毒株均可以检出全部8个mnp标记位点(表 5)。将6个毒株的指纹图谱进行两两比对,结果如表5所示,有2份(s-1,s-2)和同批次一起检测的4份人冠状病毒hcov-229e均存在部分标记的主基因型差异(表5),存在毒株间变异。
[0078]
所述的试剂盒通过检测mnp标记位点鉴定毒株间遗传变异的应用可以用于监测病毒的遗传变异,可以用于保证不同实验室相同命名人冠状病毒hcov-229e毒株的遗传一致性,从而保证研究结果的可比较性,这对于人冠状病毒hcov-229e的防疫监测、精准治疗和科学研究都具有重要意义。
[0079]
表5-1个冠状病毒hcov-229e毒株的6份拷贝样本的检测分析
[0080][0081][0082]
实施例4、人冠状病毒hcov-229e感染病例内部毒株的遗传变异检测
[0083]
人感染冠状病毒后,作为群体生物,人冠状病毒hcov-229e内部部分个体发生变异,导致复合感染。当变异的个体还未累积时,只占群体的极少部分,在对群体进行分子标记检测时,表现为低频率的主基因型外的次等位基因型。低频率的次等位基因型往往和技术错误混在一起,导致现有技术难以区分。本发明检测的是高多态性的mnp标记位点,基于多个错误同时发生的几率低于一个错误发生的几率,mnp标记位点的技术错误率显著低于现有的标记,比如snp标记。对复合感染检测的关键是判定在感染个体检测到的mnp位点的次等位基因型的真实性。
[0084]
本实施例次等位基因型的真实性评估按如下进行:首先按照以下规则排除具有链偏好性(在dna双链上覆盖的测序序列数的比值)的等位基因型:链偏好性大于10倍,或者与主等位基因型的链偏好性之差大于5倍。
[0085]
不存在链偏好性的基因型基于表6测序序列数目和比例判定其真实性。表6列出了基于binom.inv函数计算在α=99.9999%的概率保障下,e
max
(n=1)和e
max
(n≥2)分别为1.03%和0.0994%时,在各个标记中次等位基因型测序序列数目的临界值,只有次等位基因型的测序序列数目超过临界值时判定为真实的次等位基因型。当存在多个候选次等位基因时,对各候选等位基因型的p值进行多重校正,fdr《0.5%的候选等位基因判定是真实的次等位基因型。
[0086]
表6涉及到的参数e
max
(n=1)和e
max
(n≥2)指的是携带n个snp的错误等位基因的测序序列数占该标记总测序序列数的最高比例。e
max
(n=1)和e
max
(n≥2)分别为1.03%和0.0994%是根据在930个纯合mnp标记位点检测到的所有次等位基因型的频率获得。
[0087]
表6部分测序深度下进行判定次等位基因型的临界值
[0088][0089][0090]
按照上述参数,将表5中展示的基因型存在差异的两个毒株的核苷酸按照以下8个比例1/1000,3/1000,5/1000,7/1000,1/100,3/100,5/100,7/100混合,制备人工杂合样本,每个样本检测3次重复,获得共计24个测序数据。通过和所述两个毒株的mnp标记位点的基因型进行精准比对,在24个人工杂合样本中均检测到了存在杂合基因型的标记,说明了所开发的人冠状病毒hcov-229e的mnp标记位点检测方法在检测毒株群体内部低频遗传变异的适用性。
[0091]
实施例5、人冠状病毒hcov-229edna指纹数据库的构建
[0092]
利用常规ctab法、商业化试剂盒等方法提取用于构建人冠状病毒hcov-229edna指纹数据库的所有毒株或是样本的dna,采用琼脂糖凝胶和紫外分光光度计检测dna的质量。若所提取的dna在260nm与230nm处的吸光度值的比值大于2.0,260nm与280nm 吸光度值比值介于1.6与1.8之间,dna电泳主带明显,无明显降解和rna残留,则说明基因组dna达到相关的质量要求,可进行后续实验。
[0093]
将上述6个毒株的测序数据进行序列比对后获得每个毒株每个标记的主基因型,
形成每个毒株的mnp指纹图谱,两两比对后,将和其他毒株存在至少1个主基因型差异的指纹图谱录入数据库文件,形成人冠状病毒hcov-229e的mnp指纹数据库。通过将每次新的样本中检测获得的毒株的mnp指纹图谱同已构建的mnp指纹数据库进行比对,将主基因型存在差异的毒株的mnp指纹图谱所构建的mnp指纹数据库,实现数据库的共建共享和随时更新。所构建的mnp指纹数据库基于检测的毒株的基因序列,因此和所有的高通量测序数据兼容。
[0094]
实施例6、在人冠状病毒hcov-229e精细分型中的应用
[0095]
利用所述的引物组合和mnp标记位点检测方法对上述6份人冠状病毒hcov-229e毒株进行检测,获得了每个毒株mnp指纹图谱。将每个毒株的dna指纹图谱进行两两比对和与构建的指纹数据库进行比对,和已有指纹数据库相同的,定义为已有的变型,在至少一个mnp标记位点存在主基因型差异的,定义为新的变型,实现对人冠状病毒hcov-229e 的精细分型。对6份人冠状病毒hcov-229e样本的检测如表5所示,所检测的6份人冠状病毒hcov-229e被分为2种,有2份和其他4份在1个mnp标记位点的主基因型存在差异。因此,所述的方法对人冠状病毒hcov-229e的分辨率达到了单碱基的水平,可以实现对样本中人冠状病毒hcov-229e的精细分型。
[0096]
最后,还需要说明的是,术语“包括”、“包含”或者其任何其他变体意在涵盖非排他性的包含,从而使得包括一系列要素的过程、方法、物品或者设备不仅包括那些要素,而且还包括没有明确列出的其他要素,或者是还包括为这种过程、方法、物品或者设备所固有的要素。
[0097]
尽管已描述了本发明实施例的优选实施例,但本领域内的技术人员一旦得知了基本创造性概念,则可对这些实施例作出另外的变更和修改。所以,所附权利要求意欲解释为包括优选实施例以及落入本发明实施例范围的所有变更和修改。
[0098]
显然,本领域的技术人员可以对本发明实施例进行各种改动和变型而不脱离本发明实施例的精神和范围。这样,倘若本发明实施例的这些修改和变型属于本发明实施例权利要求及其等同技术的范围之内,则本发明实施例也意图包含这些改动和变型在内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1