一种棉花GhLAC4编码基因、棉花抗病模块miR397-LAC4及应用的制作方法
一种棉花ghlac4编码基因、棉花抗病模块mir397
‑
lac4及应用
技术领域
1.本发明涉及领域,特别是一种棉花ghlac4编码基因、棉花抗病模块mir397
‑
lac4及应用。
背景技术:
2.棉花是双子叶植物,是唯一由种子生产纤维的农作物,作为重要的纺织原料,棉花是全球范围内最重要的经济作物之一,也是我国重要的农产品之一。而棉花黄萎病的危害造成棉花产量和品质下降,曾多次在我国各主产棉区暴发成灾,年发生面积近300万hm2,年经济损失约12亿元,已成为我国棉花可持续发展面临的主要问题。棉花黄萎病是由轮枝菌(verticillium)引起的严重维管束病害;在我国主要病原菌为大丽轮枝菌,通过植株根部浸染,进入木质部导管中,在其中进行生长和繁殖,最终阻挡水分和矿物质运输,使叶片萎蔫,导致整株植物受损或死亡。当大丽轮枝菌侵入植物时,植物和病原菌接触,在表面形成可分泌效应蛋白的界面,由该界面将病原菌丝或效应蛋白从植物根部入侵并繁殖于维管组织中,在植物的蒸腾作用下,病原孢子和毒素在植株体内进行运输,从而造成植株发病。而且大丽轮枝菌的菌丝和微菌核在土壤和植株体内存活时间长、生理小种多且复杂等特点,使其产生的病害防治困难。虽然人们采取许多措施,包括化学农药施用、生物控制和栽培措施等防治方法来防治棉花黄萎病,但是,这些措施的防治效果并不理想。当前,普遍认为利用植物抗病基因进行抗病品种的选育是解决棉花黄萎病危害的重要手段,因此,分离和鉴定抗病基因并阐明其分子机制成为当前研究的一个主要方向。
3.木质素广泛存在于植物中,是细胞壁的重要组成部分;其重要功能主要包括木质部导管运输水分和矿物质营养和对病原菌及昆虫入侵的防御。木质素是植物的一种重要的次生代谢物的聚合物,主要由苯丙环路径和ja的合成代谢途径进行生物合成的,其最后一步关键反应是由植物漆酶决定。植物漆酶(lac)属于蓝铜氧化酶家族,一种多聚氧化还原酶,能够促进木质素单体聚合。在拟南芥中有17个漆酶基因,其中lac4、lac11、lac15和lac17具有木质素生物合成作用。相关研究验证了漆酶基因能够促进木质素单体聚合,影响植物的生长与发育。但是有关lac,尤其lac4,抗性研究及其机制仍然需要进一步探讨。
4.研究表明有些lac基因,包括4个与木质素合成相关的lac基因,能够被mir397调控植物木质素参与生物逆境的抗性。但是mir397与lac4一起参与木质素合成,但是有关其调控植物的抗病性功能和其机制尚未见报道。
技术实现要素:
5.本发明的目的是要解决现有技术中存在的不足,提供一种棉花ghlac4编码基因、棉花抗病模块mir397
‑
lac4及应用,棉花木质素的改变,减少棉花对大丽轮枝菌的敏感性,从而保护植物的生长发育。
6.为达到上述目的,本发明是按照以下技术方案实施的:
7.本发明的第一个目的是要提供一种棉花ghlac4编码基因,所述棉花ghlac4编码基
因为:
8.seq id no.2所示的蛋白质;
9.或将seq id no.2所示的蛋白质通过一个或多个氨基酸的替换、缺失或/和插入而衍生得到的仍具有ghlac4基因功能或活性的蛋白变体;
10.或seq id no.3所示的核苷酸;
11.或将seq id no.3所示的核苷酸通过一个或多个碱基的替换、缺失或/和插入而衍的序列变体。
12.进一步地,所述seq id n0.2所示氨基酸序列组成的蛋白质的氨基末端或羧基末端连接上如下标签:
13.标签残基序列poly
‑
arg5
‑
6个rrrrrpoly
‑
his2
‑
10个hhhhhhflag8个dykddddkstrep
‑
tag ii8个wshpqfekc
‑
myc10个eqkliseedl。
14.进一步地,所述seq id n0.2所示氨基酸序列通过将seq id n0.3所示碱基序列中缺失一个或几个氨基酸残基的密码子,和/或进行一个或几个碱基对的错义突变,和/或在其5’端和/或3’端连上标签的编码序列得到。
15.本发明的第二个目的是要提供一种的棉花ghlac4编码基因在培育抗黄萎病棉花中的应用。
16.本发明的第三个目的是要提供一种棉花抗病模块mir397
‑
lac4,包括ghr
‑
mir397基因和ghlac4编码基因,所述ghr
‑
mir397基因为seq id no.1所示的核苷酸。
17.本发明的第四个目的是要提供一种棉花抗病模块mir397
‑
lac4在培育抗黄萎病棉花中的应用。
18.与现有技术相比,本发明提供的ghlac4编码基因能够提高棉花抗黄萎病性能,提供的mir397
‑
lac4通过调控木质素合成途径基因和ja途径基因参与陆地棉对丽轮枝菌的抗性响应,进而增强棉花的抗黄萎病性能。
附图说明
19.图1为棉花与拟南芥lacs家族系统发育树分析对比图。
20.图2为ghr
‑
mir397和ghlac4在棉花不同组织器官的特异性表达分析图。
21.图3为大丽轮枝菌侵染棉花后ghr
‑
mir397和ghlac4在不同时间点的表达谱分析示意图。
22.图4为ghr
‑
mir397和ghlac4在烟草叶片gus染色分析示意图。
23.图5为棉花ghpds基因沉默分析示意图。
24.图6为棉花ghr
‑
mir397沉默和过表达植株表达分析示意图。
25.图7为棉花ghr
‑
mir397沉默和过表达植株及对照植株发病情况示意图。
26.图8为棉花ghr
‑
mir397沉默和过表达植株及对照植株病指统计示意图。
27.图9为棉花ghr
‑
mir397沉默和过表达植株及对照植株茎秆恢复培养示意图。
28.图10为棉花ghr
‑
mir397沉默和过表达植株及对照植株茎秆生物量示意图。
29.图11为棉花ghlac4基因沉默分析示意图。
30.图12为棉花ghlac4基因沉默植株和对照植株发病情况示意图。
31.图13为棉花ghlac4基因沉默植株和对照植株病指统计示意图。
32.图14为棉花ghlac4基因沉默植株和对照植株茎秆恢复培养示意图。
33.图15为棉花ghlac4基因沉默植株和对照植株茎秆生物量示意图。
34.图16为为棉花ghlac4基因沉默植株、对照植株、ghr
‑
mir397沉默和过表达植株木质素合成途径相关基因分析示意图。
35.图17为棉花ghlac4基因沉默植株、对照植株、ghr
‑
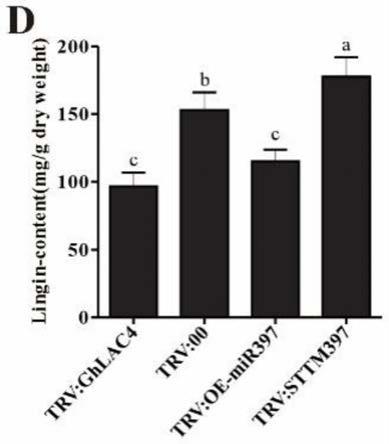
mir397沉默和过表达植株木质素含量分析示意图。
36.图18为棉花ghlac4基因沉默植株、对照植株、ghr
‑
mir397沉默和过表达植株木质部间苯三酚染色图。
37.图19为棉花ghlac4基因沉默植株、对照植株、ghr
‑
mir397沉默和过表达植株木质部间ma
ü
le染色图。
38.图20为棉花ghlac4基因沉默植株、对照植株、ghr
‑
mir397沉默和过表达植株木质素释放的主要g、s和h硫酸解单体的测定。
具体实施方式
39.为使本发明的目的、技术方案及优点更加清楚明白,以下结合实施例,对本发明进行进一步的详细说明。此处所描述的具体实施例仅用于解释本发明,并不用于限定发明。
40.首先对以下实施例所用的试剂、材料等的来源作说明:
41.有关试剂盒使用参照所购试剂盒的应用说明;所用限制性内切酶和其它工具酶均购自takara公司。
42.棉花材料为中棉所35,购自山西农业科学院棉花研究所种苗公司。烟草材料、大肠杆菌
‘
dh5α’感受态细胞和根癌农杆菌菌株
‘
gv3101’由植物基因组学国家重点实验室保存。黄萎病菌菌株(大丽轮枝菌,v.dahliae)
‘
v991’,由中国农业科学院植物保护研究所简桂良研究员馈赠。各种限制性内切酶及buffer购自takara公司。各类化学试剂、培养基、柱式植物总rna分离提取纯化试剂盒和植物dna提取试剂盒均购自北京擎科生物科技有限公司。质粒小量制备试剂盒(升级版离心柱型)购自北京擎科生物科技有限公司。taq dna聚合酶、dntps、taq buffer、t4 dna连接酶、pcr纯化回收试剂盒;pcr切胶回收试剂盒、克隆载体peasy
‑
t1试剂盒、easyscript one
‑
step gdna removel and cdna synthesis supermix试剂盒、transstart top green qpcr supermix试剂盒均购自北京全式金生物技术有限公司。表达载体pbi121为课题组保存备用。
43.实施例1
44.本实施例具体公开了棉花ghlac4编码基因的克隆和表达分析,其过程如下:
45.1.总rna的提取和cdna第一链的合成
46.经硫酸脱绒过的棉花种子浸泡在水中,放在37℃的培养箱过夜,次日,转移至培养盒中,保持种子湿润情况下黑暗处萌芽。取发芽一致的种子转至含hoagland’s营养液的培
养盒中,于28℃温室,光周期16h光照/8h黑暗培养箱中进行培养。棉花幼苗长出真叶后分别摘取棉花幼苗的根、茎和叶样品,使用柱式植物总rna分离提取纯化试剂盒提取棉花rna。cdna第一链的合成参照easyscript one
‑
step gdna removal and cdna synthesis supermix试剂盒说明进行。
47.2.棉花ghlac4基因克隆
48.根据拟南芥lac4序列在棉花基因组数据库(https://www.cottongen.org/)进行直系同源比对,找到与拟南芥lac4高保守性的直系同源基因,命名为ghlac4。根据ghlac4基因序列设计引物,引物为ghlac4
‑
f:5
’‑
gagaacacgggggactctagaatggagatggcaccatggattc
‑3’
;ghlac4
‑
r:5’ataagggactgaccacccggggatccgcacttggggaaatcacttgga
‑3’
。
49.本实验所有引物均由北京擎科生物科技有限公司合成。以棉花叶的cdna为模板进行pcr扩增,将pcr产物连接到t载体上进行测序,测序由北京擎科生物技术有限公司完成。结果表明获得的片段大小与预期的大小一致,该片段全长1671bp,包含了从atg开始tga结束完整的orf阅读框,编码了556个氨基酸,分子量为68.4kda,理论等电点为5.24(如seq id n0.2和seq id n0.3所示)。
50.3.ghlac4基因序列系统进化树构建
51.从棉花基因组数据库(https://www.cottongen.org/)和拟南芥数据库(https://www.arabidopsis.org/)中,选取82个陆地棉漆酶和17个拟南芥漆酶氨基酸序列,利用mega7.0程序进行系统进化树的构建,由图1我们可以看出,ghlac4与atlac4聚在一组,表明两者蛋白具有较高的亲缘关系。
52.4.ghlac4基因在不同组织和不同处理条件下的表达分析
53.4.1样品的采集与处理
54.大丽轮枝菌接种:将发好芽的棉花种子种植到水培培养盒中,置于光周期16h光照/8h黑暗、28℃的培养箱中进行培养,选取长势一致并具有两片真叶的棉苗进行不同处理。对棉株主根进行统一伤根处理后放到含有1
×
106conidia/ml孢子液中浸泡2h,然后再转到水培盒中,置于培养箱中继续培养。按照相应的时间点取棉株根样(0、1、2、3、5、7、10和12天),保存于
‑
80℃冰箱待用。
55.4.2quantitative real
‑
time rt
‑
pcr(qrt
‑
pcr)方法
56.利用qrt
‑
pcr方法,检测ghr
‑
mir397和ghlac4在棉花根、茎和叶中的表达情况及其病原菌和激素诱导后的表达情况。
57.扩增ghr
‑
mir397的引物为:mir397
‑
f:5
’‑
cgcgattgagtgcagcgtt
‑3’
;mir397
‑
r:5
’‑
agtgcagggtccgaggtatt
‑3’
。以棉花ub6作为内参基因,扩增引物为:ub6
‑
f:5
’‑
cggggacatccgataaaattggaac
‑3’
;ub6
‑
r:5
’‑
ggaccatttctcgatttgtgcgtg
‑3’
。qrt
‑
pcr所用的反应体系为20μl,以不同处理后的棉花样本cdna为模板,具体反应体系按照试剂盒使用说明进行配置。扩增条件为:95℃预变性2min,40个循环:95℃10s,58℃15s,72℃15s。以ub6基因为内参,生物学实验重复3次。生物学实验重复3次。扩增ghlac4的引物为:qghlac4
‑
f:5
’‑
gaccattccctgcttttcacc
‑3’
;qghlac4
‑
r:5
’‑
tgcttgtgtagttgaatggagc
‑3’
。以棉花ubq7作为内参基因,扩增引物为:ubq7
‑
f:5
’‑
gaaggcattccacctgaccaac
‑3’
;ubq7
‑
r:5
’‑
cttgaccttcttcttcttgtgcttg
‑3’
。qrt
‑
pcr所用的反应体系为20μl,以不同处理后的棉花样本cdna为模板,具体反应体系按照试剂盒使用说明进行配置。扩增条件为:95℃,5min;95
℃,10s;60℃,30s;72℃,30s;40个循环。生物学实验重复3次。基因的相对表达量通过2
–
δδct
方法计算。
58.4.3组织特异表达分析
59.抽取棉花的根、茎和叶器官的总rna,反转录成cdna,利用该cdna作为模板进行qrt
‑
pcr分析,结果表明ghr
‑
mir397和ghlac4基因在这些组织器官中均表达(图2),ghr
‑
mir397在根里的表达量较高,叶和子叶次之,茎中的表达量最低,ghlac4基因则相反,ghlac4在茎秆中相对表达较高,在根部表达最低。暗示这个两个基因的表达存在负相关关系,其模块功能可能存在组织特异性。
60.4.4大丽轮枝菌入侵对棉花ghr
‑
mir397和ghlac4诱导表达分析
61.为了分析ghr
‑
mir397和ghlac4基因是否参与棉花的抗病性,用大丽轮枝菌的孢子液对棉苗进行接菌,提取棉花根rna并反转录成cdna,利用该cdna作为模板,通过qrt
‑
pcr方法分析ghr
‑
mir397和ghlac4基因对大丽轮枝菌的响应,与对照mock相比接菌后ghr
‑
mir397的表达被抑制,分别在接菌的第2天和第7天明显被抑制表达,暗示着ghr
‑
mir397可能通过下调自身表达水平以提高靶标基因的表达水平积极参与陆地棉的抗病响应。而ghlac4的表达量在接菌1天后呈上升趋势,在接菌的第2天达到最高值,随后稍有下降(图3)。这与ghr
‑
mir397的接菌诱导表达量呈负相关关系,进一步的暗示着ghr
‑
mir397与ghlac4可能作为一个整体调控陆地棉的抗病性。
62.实施例2
63.本实施例具体公开了ghr
‑
mir397在转录后调控靶基因ghlac4,具体步骤如下:
64.1.构建pcambia1300
‑
mir397表达载体
65.用植物dna提取试剂盒提取棉花dna,以提取的dna为模板,正向和反向引物分别为(f:ggatacatgtacgtaacgcgtaatttacttttcaattgttccaaagg和r:tgcttcgaatcatcaatgcagctttgaatgaagaactctt)扩增ghr
‑
mir397前体基因,扩增条件为:95℃,5min;95℃,30s;60℃,30s;72℃,30s;35个循环。扩增产物插入表达载体pcambia1300,构建pcambia1300
‑
mir397表达载体。
66.2.构建pbi121
‑
ghlac4和pbi121
‑
ghlac4
mu
载体
67.使用棉花的cdna为模板,加入正向引物ghlac4
‑
f(gagaacacgggggactctagaatggagatggcaccatggattc),引物序列中引入xba i限制性酶切位点和反向引物ghlac4
‑
r(ataagggactgaccacccggggatccgcacttggggaaatcacttgga),引物序列中引入bamh i限制性酶切位点,扩增基因ghlac4。扩增条件为:95℃,5min;95℃,30s;60℃,30s;72℃,60s;35个循环。扩增产物插入表达载体pbi121,融合gus基因表达,构建pbi121
‑
ghlac4。设计突变正向引物lac4
mu
‑
f(tgcttcgaatcatcaatgcagctttgaatgaagaactctt),和反向引物lac4
mu
‑
r(gttcttcattcaaagctgcattgatgattcgaagcatgtac)引,扩增条件为:95℃,5min;95℃,30s;60℃,30s;72℃,60s;35个循环。扩增产物插入表达载体pbi121,融合gus基因表达,构建pbi121
‑
ghlac4
mu
载体。
68.3.农杆菌介导转化烟草叶片
69.将菌种接种到含有卡那霉素(50mg/ml)、庆大霉素(50mg/ml)和利福平(25mg/ml)的lb液体培养基中,28℃振荡培养过夜;室温4000r/min离心10min;弃上清,用mma(10mm mgcl2,10mm mes
‑
naoh,200μm acetosyringone;od600=1.0)缓冲液重悬菌体,调节菌液
od600=1.0,室温静置约2h;注射前将重悬菌液按照试验需要混合,用注射器的针头轻点烟草叶背面,然后由注射器注射直到叶片充分被重悬菌液浸润;注射后先置于暗室培养1天,再转移置培养箱培育2天可进行gus报告基因染色检测。
70.4.gus组织染色
71.剪取烟草叶片放入预冷的95%丙酮中,使丙酮浸满整个叶片,在冰上浸泡过夜。将浸泡好的叶片用pbs缓冲液润洗3
‑
4遍,再加入gus染色液,放在真空抽滤仪中,缓慢抽滤6min,使gus染色液充分浸入烟草叶片,置于37℃染色,随时观察颜色变化。待染色完成后,取出烟草叶片,分别用50%、75%、90%梯度酒精洗涤叶片。最后将叶片中浸泡在无水乙醇中直至叶片绿色完全褪去。
72.5.在本氏烟叶中瞬时表达ghr
‑
mir397调控其靶基因ghlac4
73.为进一步验证ghr
‑
mir397在体内切割靶标基因ghlac4,将过量表达ghr
‑
mir397载体与ghlac4和突变ghlac4(ghlac4
mu
)融合gus报告基因载体转化农杆菌,共注射烟草叶片瞬时表达,进行组织染色分析。如图4所示,单独注射ghlac4:gus和ghlac4
mu
:gus,gus报告基因均能表达,注射区域蓝色较深;当ghr
‑
mir397和ghlac4:gus共注射时,注射区域的蓝色不明显,表明ghr
‑
mir397抑制了ghlac4表达,从而使gus报告基因不能正常表达;而当ghr
‑
mir397与ghlac4
mu
:gus共注射时,注射区域蓝色明显,说明突变基因ghlac4mu不能被ghr
‑
mir397切割。这些结果都表明ghr
‑
mir397可以在ghlac4转录后切割mrna抑制其表达。
74.实施例3
75.为研究mir397
‑
lac4模块陆在地棉中的抗病功能,本实施例具体公开了ghr
‑
mir397和ghlac4基因沉默及过表达植株对大丽轮枝菌的抗性影响。
76.1.病毒诱导基因沉默(virus
‑
induced gene silencing,vigs)植株的培育
77.1.1病毒沉默载体trv:sttm397的构建
78.由北京擎科生物科技有限公司化学合成,sttm397(gaggatcctaactcacgtgaccgcaactacttgttgttgttgttatggtctaatttaaatatggtctaaagaagaagaattaactcacgtgaccgcaactacttggtaccctc),在sttm397合成片段的5’端和3’端分别加上酶切位点bamh i和kpni。将sttm397合成片段酶切,插入病毒载体pyl156,构建沉默载体trv:sttm397载体。
79.1.2病毒过表达载体trv:oe
‑
mir397的构建
80.以棉花dna为模板,使用正向引物mir397
‑
f(agaaggcctccatggggatccatccccggatggaagaaaca),引物序列中引入酶切位点bamh i(下划线部分)和反向引物mir397
‑
r(gagacgcgtgagctcggtaccaatttacttttcaattgttccaaagg),引物序列中引入酶切位点kpni(下划线部分),扩增条件为:95℃,5min;95℃,30s;60℃,30s;72℃,30s;42个循环。扩增产物插入病毒载体pyl156,构建过表达载体trv:oe
‑
mir397。
81.1.3病毒沉默载体trv:ghlac4的构建
82.病毒沉默表达载体pyl156由清华大学刘玉乐教授惠增。首先利用pcr技术克隆ghlac4基因的目的片段,扩增所用引物为lac4
‑
f:5
’‑
agaaggcctccatggggatccttgaatggagcaggcgga
‑3’
;lac4
‑
r:5
’‑
gagacgcgtgagctcggtacccgtcaaccccaccgaaaaa
‑3’
(下划线分别是bamh i和kpn i酶切位点)。用限制性内切酶bamh i和kpn i酶切pyl156载体和扩增产物,然后进行连接反应,将片段插入到pyl156载体的bamh i和kpn i位点之间构建成病毒沉默载体trv:ghlac4。将构建成功的病毒沉默载体trv:ghlac4转化大肠杆菌dh5α后,挑选阳性
克隆,进行bamh i和kpn i酶切以及测序鉴定,结果表明所获得的片段是所要克隆的ghlac4基因的目的片段。
83.1.4工程农杆菌的培养
84.将已构建正确的病毒沉默载体trv:ghlac4、辅助载体pyl192、阳性对照载体trv:pds(植物基因组学国家重点实验室保存)和阴性对照载体pyl156用电击法转化到农杆菌gv3101中,经卡那霉素(50mg/ml)、庆大霉素(50mg/ml)和利福平(25mg/ml)筛选,挑选阳性克隆,进行pcr和测序验证,结果表明病毒沉默载体trv:ghlac4、辅助载体pyl192、阳性对照载体trv:pds和阴性对照载体pyl156已经转入农杆菌gv3101。
85.1.5ghlac4基因沉默植株、ghr
‑
mir397沉默和过表达植株的培育
86.上述验证正确的工程农杆菌加到含有卡那霉素(50mg/ml)、庆大霉素(50mg/ml)和利福平(25mg/ml)的液体lb培养基中于28℃,200rpm过夜培养,培养液经离心后倒去上清,用mma(10mm mes,10mm mgcl2,200mm as)溶液重悬菌体,调节至终浓度od600为1.0,放到黑暗处静置2小时,然后将含有trv:ghlac4、trv:sttm397、trv:oe
‑
mir397、trv:pds和pyl156的农杆菌悬浮液分别与含pyl192的农杆菌悬浮液按1:1混合均匀备用。当棉花两片子叶完全展开后,可用于农杆菌注射侵染;先用针头在子叶背面点个不透孔,然后用1ml去掉针头的无菌注射器将菌液从子叶背面的伤口处注射进去,尽量使整片子叶全部被侵染,将注射后的植株放到黑暗处处理12h,然后放到光照培养箱进行培养。
87.2.ghr
‑
mir397负调控陆地棉对大丽轮枝菌的抗性
88.农杆菌转化棉株两周后,观察到阳性对照trv:pds植株新长出来的真叶出现白化表型,这表明同批次处理的其他基因也可能发生沉默(图5)。为进一步研究ghr
‑
mir397在陆地棉中的抗病功能,利用烟草脆裂病毒(tobacco rattle virus,trv)沉默系统和sttm(short tandem mimicry technology)技术构建沉默ghr
‑
mir397载体,转化农杆菌gv3101,注射棉花子叶,培育ghr
‑
mir397沉默植株(trv:sttm397)。stem
‑
loop rt
‑
qpcr结果显示,ghr
‑
mir397在trv:sttm397植株中的相对表达量比trv:00植株下降了约50%,sttm结构干涉明显,显著降低了ghr
‑
mir397在trv:sttm397植株中的表达(图6)。对这些植株进行接种大丽轮枝菌孢子液,在接菌第21天,与trv:00植株相比,ghr
‑
mir397沉默植株的病情较轻,叶片出现的萎蔫、黄化现象较少(图7);trv:sttm397植株的病情指数为42,显著低于对照组trv:00植株的65(图8);从这些棉株茎的秆剖秆横切面可以观察到trv:00植株比trv:sttm397植株的维管组织的褐化现象更为严重,暗示其可能有更多的大丽轮枝菌入侵到棉花内部;进一步的棉株茎秆的恢复培养及大丽轮枝菌dna生物量检测结果也表明(图9,图10),在trv:00植株中有更多的大丽轮枝菌入侵到棉株内部,导致其病变严重。同时,培育的过量表达ghr
‑
mir397植株(trv:oe
‑
mir397,图6)在接菌后,其叶片失水、退绿和落叶表型比trv:00植株更明显(图7),对大丽轮枝菌的抗性显著低于trv:00植株(图8)。这些结果表明,ghr
‑
mir397在陆地棉抵抗大丽轮枝菌的入侵过程中有重要的功能,沉默ghr
‑
mir397的表达能提高植株的抗病性,而过量表达ghr
‑
mir397会增加植株对大丽轮枝菌的敏感性。
89.3.ghnac100l沉默植株对大丽轮枝菌的抗性分析
90.为研究ghlac4在陆地棉中的抗病功能,利用trv沉默系统构建ghlac4沉默病毒载体,转化农杆菌gv3101,注射棉花子叶,培育了沉默lac4植株(trv:lac4,图11)。对trv:lac4植株和trv:00植株分别接种大丽轮枝菌孢子液,接菌第21天,ghlac4沉默植株的叶片的黄
化、萎蔫、失水现象更为严重(图12);其茎秆恢复培养实验中有更多的菌落(图13);其维管组织褐化现象也更严重;表明有更多的大丽轮枝菌菌丝进入ghlac4沉默植株的内部,这与棉株茎秆的大丽轮枝菌dna生物量检测结果一致(图14)。trv:lac4植株的病情指数为69,显著高于trv:00植株的42(图15)。这些结果表明沉默ghlac4会导致陆地棉对大丽轮枝菌的易感性。
91.实施例4
92.进一步,为了验证mir397
‑
lac4模块的抗病功能是与棉花的木质素合成和积累相关性,本实施例具体公开了mir397
‑
lac4模块对棉花的木质素的积累分析:
93.1棉花组织化学染色
94.1.1间苯三酚染色:样品取自ghlac4沉默植株、ghr
‑
mir397过表达植株、ghr
‑
mir397沉默植株和对照植株进行wiesner试剂染色。具体操作方法为:分别取棉株同等部位的茎杆进行徒手切片,厚度小于0.3cm。选完整性好且薄厚均匀的部位加入1%的间苯三酚溶液处理10min,去除间苯三酚溶液后,再加入18%hcl处理10min,直接在体式镜(dm2500,leica,germany)下观察和拍照。
95.1.2ma
ü
le染色:选取生长时期相同的植株,选取相同的节间,进行徒手切片;从中选取厚薄均匀的切片,5%kmno4染色10min;蒸馏水洗涤4
‑
5次,直到没有红色,10%盐酸处理10min;蒸馏水洗涤2次,25%的浓氨水侵染3min,然后封片保存,于体式镜(dm2500,leica,germany)下观察并拍照。
96.2.木质素含量和组分测定
97.木质素含量检测实验方法是用klason法。具体步骤如下:1、选取vigs处理后的棉花幼苗下胚轴,加入液氮研磨粉碎,取400mg样品置入50ml离心管,同时加入45ml甲醇,200rpm/min摇床振荡过夜。4000rpm/min离心10min,去除上清。2、加入45ml甲醇,200rpm/min振荡2h,4000rpm/min离心10min去上清。3、重复步骤2。4、将去除上清的样品于60
‑
80℃完全烘干,称取200mg(w1)样品至玻璃试管中。5、加入4ml72%浓硫酸30℃水浴1h。
98.木质素的组成是通过硫酸解法测定的,将大约20mg无抽提物样品与15ml混有8:75:1二氧六环/乙硫醇混合物中的mbf3乙醚混合。用气相色谱
‑
质谱(gc/ms)对木质素衍生单体进行了鉴定,并用gc对其进行了定量。
99.3.陆地棉mir397/lac4模块影响木质素的积累
100.为了研究ghlac4的抗病功能是否与植株的木质素合成和积累相关。首先,利用rt
‑
qpcr方法检测ghlac4沉默植株木质素合成途径相关基因,结果表明这些基因都下调表达,影响木质素的合成(图16)。其次,植株的木质素含量测定结果显示,ghlac4沉默植株的木质素含量显著减少(图17)。最后,对这些棉株的茎秆切片进行间苯三酚
‑
hcl和ma
ü
le染色分析,间苯三酚
‑
hcl染色结果显示trv:lac4l植株比trv:00植株着色浅,表明沉默ghlac4基因表达会减少木质素积累(图18);ma
ü
le染色分析显示,ghlac4沉默植株木质部被染成棕红色较深,而trv:00植株棕红色较浅或呈现黄褐色(图19),表明在trv:00植株中可能有较少的g
‑
木质素被合成。这些结果也暗示着ghlac4沉默植株由于其木质素含量的减少,对大丽轮枝菌的易感性增加。由于过量表达ghr
‑
mir397植株的抗病表型与ghlac4沉默植株一致,其木质素合成途径相关基因也下调表达(图16),且木质素含量减少(图17)。茎秆切片的间苯三酚
‑
hcl和ma
ü
le染色分析结果也表明过量表达ghr
‑
mir397会影响植株的木质素合成和积
累,g
‑
木质素合成被抑制。而沉默ghr
‑
mir397的表达则会上调植株的木质素合成相关基因表达(图16),增加木质素的积累,有较多的g
‑
木质素被合成,并增强植株的抗病性。同时通过gc/ms结果可知,沉默ghr
‑
mir397有更多的g
‑
木质素被合成,而沉默ghlac4和过表达ghr
‑
mir397则可能较少的g
‑
木质素被合成(图20)。
101.上述结果表明,棉花mir397
‑
lac4模块通过调控木质素合成途径基因和ja途径基因参与陆地棉对丽轮枝菌的抗性响应,能够增强棉花的抗黄萎病性能。
102.本发明的技术方案不限于上述具体实施例的限制,凡是根据本发明的技术方案做出的技术变形,均落入本发明的保护范围之内。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1