一种特异性识别TYGPVFMSL肽段的荧光PCR引物组及其应用的制作方法
一种特异性识别tygpvfmsl肽段的荧光pcr引物组及其应用
1.本发明要求申请号为202110685511.1,申请日为2021年06月21日,发明名称为“一种特异性识别tygpvfmsl肽段的荧光pcr引物组及其应用”的中国专利的优先权。
技术领域
2.本发明涉及基因工程技术领域,尤其涉及一种特异性识别tygpvfmsl肽段的荧光pcr引物组及其应用。
背景技术:
3.ebv是可以感染人类的疱疹病毒家族的一员。ebv感染与某些类型的癌症有关。这些因ebv病毒感染所导致的癌症患者有望在tcr-t细胞治疗中获益。
4.tcr-t细胞治疗是有望治疗实体肿瘤的新一代免疫细胞疗法。在tcr-t细胞治疗的过程中,需要不断监测被输注到病人体内的药用tcr-t细胞的生长和续存的情况。能实现此目的技术手段中,荧光定量pcr(qpcr)是检测灵敏度很高的技术手段。利用qpcr监测tcr-t细胞,需要针对tcr-t细胞的特定tcr基因序列设计qpcr引物。然而现有技术并未发现针对tcr基因序列所设计的qpcr引物组应用于检测tcr-t细胞在病人体内生长和续存状况中。
技术实现要素:
5.针对现有技术的缺陷,本发明的目的在于提供一种特异灵敏的追踪tcr-t细胞药物的引物组,尤其涉及一种特异性识别tygpvfmsl肽段的荧光pcr引物组及其应用。为了实现上述发明目的,本发明提供以下技术方案:
6.本发明提供了一种引物组,包括位点为l24-3、l24-5和l24-13 tcr引物对中的一种或几种。
7.作为优选,所述引物组依据hlaa24分型,ebv病毒抗原肽段tygpvfmsl的tcr设计。
8.作为优选,位点为l24-3的tcr引物对的序列如seq id no.1~2所示;
9.位点为l24-5的tcr引物对的序列如seq id no.3~4所示;
10.位点为l24-13的tcr引物对的序列如seq id no.5~6所示。
11.作为优选,位点为l24-3的tcr引物对的序列还如seq id no.8~9所示;
12.位点为l24-5的tcr引物对的序列还如seq id no.10~11所示;
13.位点为l24-13的tcr引物对的序列还如seq id no.12~13所示。
14.本发明还提供了所述的引物组在制备特异性检测hlaa24分型患者体内ebv病毒抗原肽段tygpvfmsl的tcr产品中的应用。
15.作为优选,所述产品为试剂盒产品。
16.作为优选,所述试剂盒为荧光定量pcr试剂盒。
17.本发明提供了一种特异性识别tygpvfmsl肽段的荧光pcr引物组及其应用,本发明的引物组依据hlaa2分型,ebv病毒抗原肽段tygpvfmsl的tcr设计得到的。将本技术的引物组制备成荧光定量pcr试剂盒,追踪患者体内tcr-t细胞药物时,能特异的检测到药物的灵
敏度为10个拷贝数的基因片段。
附图说明
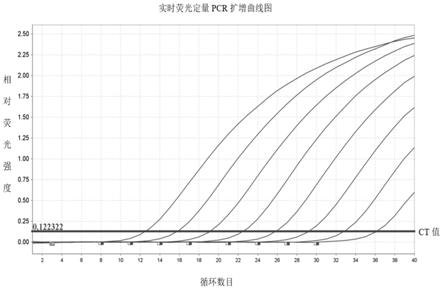
18.图1为l24-3位点质粒dna标准品的扩增曲线(从左到右质粒dna标准品的稀释度分别为108拷贝、107拷贝、106拷贝、105拷贝、104拷贝、103拷贝、102拷贝、101拷贝的基因片段)。
19.图2为l24-3位点质粒dna标准品扩增产物的电泳图(从左到右质粒dna标准品的稀释度分别108拷贝、107拷贝、106拷贝、105拷贝、104拷贝、103拷贝、102拷贝、101拷贝的基因片段)。
20.图3为l24-3位点质粒dna标准品的标准曲线图。
21.图4为l24-3位点的tcr-t细胞药的基因组dna的扩增曲线(从左到右,基因组dna的稀释度分别为原液、10倍稀释、100倍稀释、1000倍稀释、10000倍稀释)。
22.图5为l24-3位点的tcr-t细胞药的基因组dna扩增产物的电泳图(从左到右基因组dna的稀释度分别为原液、10倍稀释、100倍稀释、1000倍稀释、10000倍稀释)。
具体实施方式
23.在本发明中,位点为l24-3的tcr引物对的模板序列如seq id no.14所示;
24.位点为l24-5的tcr引物对的模板序列如seq id no.15所示;
25.位点为l24-13的tcr引物对的模板序列如seq id no.16所示。
26.本发明实施例中所述的tcr质粒标准品的构建方法为:
27.(1)将每个位点对应的tcr基因片段克隆至seq id no.7所示的质粒载体中,得到含有特定tcr基因片段的质粒载体;
28.(2)将含有特定tcr基因片段的质粒载体在大肠杆菌内扩增,提纯质粒dna,得到相应位点的tcr质粒标准品。
29.在本发明实施例中以l24-3位点为例设计方案,其余位点的检测方法与之相同。
30.在本发明实施例中所述的tcr-t细胞药的基因组dna为从相应的tcr-t药物细胞中提取的基因组dna。
31.下面结合实施例对本发明提供的技术方案进行详细的说明,但是不能把它们理解为对本发明保护范围的限定。
32.实施例1引物设计
33.依据hlaa24分型,ebv病毒抗原肽段tygpvfmsl的l24-3、l24-5和l24-13位点设计tcr引物对,得到的引物对的序列如seq id no.1~6和seq id no.8~13所示。
34.实施例2标准曲线建立
35.以tcr的l24-3位点为例设计方案。
36.取l24-3位点的质粒dna标准品的108个拷贝数稀释液、107个拷贝数稀释液、106个拷贝数稀释液、105个拷贝数稀释液、104个拷贝数稀释液、103个拷贝数稀释液、102个拷贝数稀释液、101个拷贝数稀释液,按照下述的反应体系和反应程序设置实时荧光pcr。
37.反应体系:pcr预混液10μl;正向引物0.4μl,引物浓度:10μm/μl;反向引物0.4μl,引物浓度:10μm/μl;rox reference dye(50
×
)0.2μl;tcr-t细胞药的基因组dna2μl,浓度50ng/μl,或tcr的质粒标准品dna2μl;nuclease-free water 7μl;总反应体系共20μl。
38.pcr反应程序:95℃,30s;(95℃,5s;60℃,20s)40个循环。设置参比荧光为rox,选择反应类型为sybr green reagents,选择荧光检测通道sybr,设置在60℃时采集荧光信号。
39.经实时荧光pcr扩增得到的l24-3位点质粒dna标准品的扩增曲线如图1所示。
40.将每个稀释度的质粒dna标准品的扩增产物进行琼脂糖凝胶电泳,结果如图2所示。
41.以扩增曲线的ct值为纵坐标,质粒dna标准品的log以10为底的基因片段拷贝数为横坐标建立标准曲线,标准曲线的结果如图3所示。标准曲线的方程式由计算机做线性拟合产生由于计算公式中的r2≥0.95,则证明本实施例的标准曲线有效。
42.实施例3灵敏度检测
43.将针对l24-3位点的tcr-t细胞药的基因组dna原液、10倍稀释液、100倍稀释液、1000倍稀释液、10000倍稀释液,根据实施例2实时荧光pcr的反应体系和程序进行扩增。得到针对l24-3位点的tcr-t细胞药的基因组dna的扩增曲线如图4所示。将扩增产物进行琼脂糖凝胶电泳,结果如图5所示。
44.将得到的每个稀释度的tcr-t细胞药的基因组dna的ct值代到实施例2的标准曲线中,可以计算得到每个稀释度的tcr-t细胞药的基因组dna的拷贝数。
45.经过计算,针对l24-3位点的tcr-t细胞药基因组dna原液的拷贝数为27423个拷贝,10倍稀释液的拷贝数为3064个拷贝、100倍稀释液的拷贝数为759个拷贝、1000倍稀释液的拷贝数为70个拷贝,10000倍稀释液的拷贝数为6个拷贝。由此可以得出,本实施例1得到的引物对于检测l24-3位点的tcr-t细胞药的最低检测限能达到6个拷贝,但由于标准曲线的最低值为10,因此将灵敏度设置为10。即,在实际应用中,引物在患者外周血样的基因组dna中的检灵敏度能达到10个拷贝的tcr基因片段。
46.将其余位点的引物按照本实施例3的灵敏度的检测方法检测相对应位点的tcr-t细胞药,所得到的灵敏度均能达到10个拷贝。
47.实施例4
48.按照seq id no.17所示的质粒载体设置l24-3、l24-5和l24-13位点对应的tcr基因片段,得到seq id no.18~20所示的基因片段,所述l24-3位点对应seq id no.18,l24-5位点对应seq id no.19,l24-13位点对应seq id no.20。利用这三个位点设计引物来检测相应位点的tcr-t细胞药物,同样能得到实施例1~3所述引物和效果。
49.由以上实施例可知,本发明提供了一种特异性识别tygpvfmsl肽段的荧光pcr引物组及其应用,本发明的引物组依据hlaa24分型,ebv病毒抗原肽段tygpvfmsl的tcr设计得到的。将本技术的引物组制备成荧光定量pcr试剂盒,追踪患者体内tcr-t细胞药物时的灵敏度能达到10个拷贝的tcr-t细胞药物。
50.以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1