一种氟芳烃氨基酸及其合成方法
1.本发明属于有机合成技术领域,涉及一种氟芳烃氨基酸及其合成方法。
背景技术:
2.非天然手性氨基酸(uaa)广泛用于化学和生物学的肽/蛋白质研究领域。这其中,含氟芳烃修饰的氨基酸引起了我们极大的关注。一方面芳环相互作用在蛋白质构象方面起着重要作用,另一方面氟代氨基酸已被证明能够有效稳定蛋白质结构并可用于研究酶动力学或蛋白质-蛋白质相互作用的识别基序(ref: j. med. chem.2018, 61, 1382; j. am. chem. soc. 2012, 134, 14890; chem. soc. rev. 2008, 37, 320.)。因此,开发通用且有效的合成方法来构建这些结构对于学术界和工业界都非常重要。因此,发展了一种从市售原材料中获得多样化的光学纯氟化氨基酸产物,具有十分重要的意义。
技术实现要素:
3.本发明的目的在于提供一种新型的氟芳烃氨基酸及其合成方法,是在镍催化下对氨基酸进行含氟芳烃修饰,以解决现有技术在合成该类化合物面临的官能团兼容性差或者需要繁琐的操作步骤等问题。
4.本发明一种氟芳烃氨基酸,其结构式为:,其中ar为苯环或吡啶环,fn表示在苯环或吡啶环任意位点取代的氟原子,n为1~5的整数。
5.本发明一种氟芳烃氨基酸的合成方法,以含氟苄基溴/氯和氨基酸锌试剂为原料,在非质子型溶剂及惰性气体中,镍催化剂催化下,于70~100℃(优选90℃)下反应2h,经分离纯化得到氟芳烃氨基酸;所述含氟苄基溴/氯的结构式为:,其中ar为苯环或吡啶环,fn表示在苯环或吡啶环任意位点取代的氟原子,n为1~5的整数,x为溴或氯。
6.所述氨基酸锌试剂的结构式为:。
7.所述含氟苄基溴/氯和氨基酸锌试剂的摩尔比为1:2。
8.所述镍催化剂为氯化镍、溴化镍、乙酰丙酮镍、1,3-双(二苯基膦丙烷)二氯化镍、三环己基膦二氯化镍,优选溴化镍;所述镍催化剂的加入量为含氟苄基溴/氯摩尔量的0.1%~10%;优选加入量为2.5%。
9.所述非质子型溶剂为环醚类或酰胺类溶剂,包括n-甲基吡咯烷酮(nmp)、四氢呋喃(thf)或二氧杂环己烷(dioxane),优选n-甲基吡咯烷酮。
10.本发明可以通过多种方法进行分离纯化,包括:重结晶、柱层析等。以上纯化方法均为本领域的常规方法,例如,进行重结晶时,可采用极性溶剂与非极性溶剂的混合溶剂,
优选为乙酸乙酯-石油醚,乙醇-石油醚混合溶剂。使用柱层析时,所用的展开剂采用混合溶剂,例如二氯甲烷-石油醚或乙酸乙酯-石油醚的混合溶剂等。
11.本发明的反应可在配体存在或无配体条件(优选无配体条件)进行,配体可选用ruphos或1,10-phen。
12.合成路线如下:,式中: x为溴或氯,ar为苯环或吡啶环,fn表示在苯环或吡啶环任意位点取代的氟原子,n为1~5的整数。
13.本发明的有益效果:(1)本发明在镍催化下对氨基酸进行含氟芳烃修饰,操作简便,反应条件温和,反应迅速,产率高,且所选用的原料和催化剂都来自于廉价的工业原料,十分经济、便捷,适合大规模的生产。(2)本发明具有十分优异的官能团兼容性以及反应多样性,一些用常规方法难以合成的氨基酸衍生物,用本方法都能高效的合成。(3)本发明合成的产物在生物医药有着十分重要的应用,并且所得的产物可以通过简单的转化得到多种的衍生物。
14.术语:本发明术语“芳烃”指具有芳香性的烃类,一般是指分子中含有苯环的化合物。广义的芳香烃应包括非苯芳烃,如吡啶、吡咯、呋喃等。
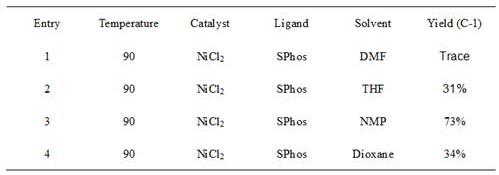
15.术语“含氟芳烃”指芳环上的氢原子被氟原子取代后的基团,例如4-氟苯基、2,3-二氟苯基、2,3,4,5,6-五氟苯基等或类似基团。
16.术语“氨基酸”指同一分子结构中既含有碱性氨基又含有酸性羧基的有机化合物。
具体实施方式
17.实施例1向25 ml的反应管中,分别加入0.7 mg(0.005 mmol)氯化镍,4.1 mg(0.01 mmol)sphos,氩气置换三次后分别加入2 ml溶剂nmp,注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.3
ꢀµ
l(0.2 mmol,1当量)化合物a-1,在90 ℃下搅拌2小时后,得化合物c-1,产率如表1(氟谱产率)。1h nmr (400 mhz, cdcl3) δ 7.04
ꢀ–ꢀ
6.98 (m, 1h), 6.91
ꢀ–ꢀ
6.84 (m, 1h), 5.09 (d, j = 8.4 hz, 1h), 4.36
ꢀ–ꢀ
4.31 (m, 1h), 3.73 (s, 3h), 2.64 (t, j = 8.0 hz, 2h), 2.16
ꢀ–ꢀ
2.07 (m, 1h), 1.93
ꢀ–ꢀ
1.83 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
120.10
ꢀ–ꢀ‑
120.14 (m, 1f),
ꢀ‑
136.61
ꢀ–ꢀ‑
136.71 (m, 1f),
ꢀ‑
143.14
ꢀ–ꢀ‑
143.28 (m, 1f). c-1为新化合物。
18.实施例2将溶剂nmp替换为dmf,其余皆同实施例1。
19.实施例3将溶剂nmp替换为thf,其余皆同实施例1。
20.实施例4将溶剂nmp替换为dioxane,其余皆同实施例1。
21.实施例1-4的反应条件及产率如下表:表1从表中可以看出以n-甲基吡咯烷酮为溶剂产率较高。
22.实施例5向25 ml的反应管中,分别加入4.1 mg(0.01 mmol)sphos,及(0.005 mmol)催化剂nibr2,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.3
ꢀµ
l(0.2 mmol,1当量)化合物a-1,在90 ℃下搅拌2小时后,得化合物c-1,产率如表2(氟谱产率)。1h nmr (400 mhz, cdcl3) δ 7.04
ꢀ–ꢀ
6.98 (m, 1h), 6.91
ꢀ–ꢀ
6.84 (m, 1h), 5.09 (d, j = 8.4 hz, 1h), 4.36
ꢀ–ꢀ
4.31 (m, 1h), 3.73 (s, 3h), 2.64 (t, j = 8.0 hz, 2h), 2.16
ꢀ–ꢀ
2.07 (m, 1h), 1.93
ꢀ–ꢀ
1.83 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
120.10
ꢀ–ꢀ‑
120.14 (m, 1f),
ꢀ‑
136.61
ꢀ–ꢀ‑
136.71 (m, 1f),
ꢀ‑
143.14
ꢀ–ꢀ‑
143.28 (m, 1f). c-1为新化合物。
23.实施例6将催化剂nibr2替换为ni(acac)2,其余皆同实施例5。
24.实施例7将催化剂nibr2替换为nicl2(dppp),其余皆同实施例5。
25.实施例8将催化剂nibr2替换为nicl2(dppp),其余皆同实施例5。
26.实施例5-8的反应条件及产率如下表:表2
实施例9向25 ml的反应管中,分别加入1.1 mg(0.005 mmol)溴化镍,4.1 mg(0.01 mmol)sphos,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.3
ꢀµ
l(0.2 mmol,1当量)化合物a-1,在温度70℃下搅拌2小时后,得化合物c-1,产率如表3(氟谱产率)。1h nmr (400 mhz, cdcl3) δ 7.04
ꢀ–ꢀ
6.98 (m, 1h), 6.91
ꢀ–ꢀ
6.84 (m, 1h), 5.09 (d, j = 8.4 hz, 1h), 4.36
ꢀ–ꢀ
4.31 (m, 1h), 3.73 (s, 3h), 2.64 (t, j = 8.0 hz, 2h), 2.16
ꢀ–ꢀ
2.07 (m, 1h), 1.93
ꢀ–ꢀ
1.83 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
120.10
ꢀ–ꢀ‑
120.14 (m, 1f),
ꢀ‑
136.61
ꢀ–ꢀ‑
136.71 (m, 1f),
ꢀ‑
143.14
ꢀ–ꢀ‑
143.28 (m, 1f). c-1为新化合物。
27.实施例10将温度70℃替换为80℃,其余皆同实施例9。
28.实施例11将温度70℃替换为100℃,其余皆同实施例9。
29.实施例9-11的反应条件及产率如下表:表3实施例12向25 ml的反应管中,加入(0.01 mmol)配体ruphos,1.1 mg(0.005 mmol)溴化镍,
氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.3
ꢀµ
l(0.2 mmol,1当量)化合物a-1,在90 ℃下搅拌2小时后,得化合物c-1,产率如表4(氟谱产率)。1h nmr (400 mhz, cdcl3) δ 7.04
ꢀ–ꢀ
6.98 (m, 1h), 6.91
ꢀ–ꢀ
6.84 (m, 1h), 5.09 (d, j = 8.4 hz, 1h), 4.36
ꢀ–ꢀ
4.31 (m, 1h), 3.73 (s, 3h), 2.64 (t, j = 8.0 hz, 2h), 2.16
ꢀ–ꢀ
2.07 (m, 1h), 1.93
ꢀ–ꢀ
1.83 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
120.10
ꢀ–ꢀ‑
120.14 (m, 1f),
ꢀ‑
136.61
ꢀ–ꢀ‑
136.71 (m, 1f),
ꢀ‑
143.14
ꢀ–ꢀ‑
143.28 (m, 1f). c-1为新化合物。
30.实施例13将配体ruphos替换为catacxium,其余皆同实施例12。
31.实施例14将配体ruphos替换为1,10-phen,其余皆同实施例12。
32.实施例15将配体ruphos替换为无配体存在,其余皆同实施例12。
33.实施例12-15的反应条件及产率如下表:表4实施例16向25 ml的反应管中,加入催化剂溴化镍(5% 当量,0.010 mmol),氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.3
ꢀµ
l(0.2 mmol,1当量)化合物a-1,在90 ℃下搅拌2小时后,得化合物c-1,产率如下(氟谱产率)。1h nmr (400 mhz, cdcl3) δ 7.04
ꢀ–ꢀ
6.98 (m, 1h), 6.91
ꢀ–ꢀ
6.84 (m, 1h), 5.09 (d, j = 8.4 hz, 1h), 4.36
ꢀ–ꢀ
4.31 (m, 1h), 3.73 (s, 3h), 2.64 (t, j = 8.0 hz, 2h), 2.16
ꢀ–ꢀ
2.07 (m, 1h), 1.93
ꢀ–ꢀ
1.83 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
120.10
ꢀ–ꢀ‑
120.14 (m, 1f),
ꢀ‑
136.61
ꢀ–ꢀ‑
136.71 (m, 1f),
ꢀ‑
143.14
ꢀ–ꢀ‑
143.28 (m, 1f). c-1为新化合物。
34.实施例17将催化剂溴化镍(5% 当量,0.010 mmol)替换为催化剂溴化镍(10% 当量,0.020 mmol),其余皆同实施例16。
35.实施例18将催化剂溴化镍(5% 当量,0.010 mmol)替换为不加催化剂溴化镍,其余皆同实施例16。
36.实施例16-18的反应条件及产率如下表:表5实施例19向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.3
ꢀµ
l(0.2 mmol,1当量)化合物a-2,在90 ℃下搅拌2小时后,得化合物c-2,产率为66%。1h nmr (400 mhz, cdcl3) δ 6.90
ꢀ–ꢀ
6.87 (m, 2h), 5.10 (d, j = 8.4 hz, 1h), 4.36
ꢀ–ꢀ
4.31 (m, 1h), 3.73 (s, 3h), 2.69 (t, j = 7.8 hz, 2h), 2.17
ꢀ–ꢀ
2.08 (m, 1h), 1.94
ꢀ–ꢀ
1.85 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
137.83
ꢀ–ꢀ‑
137.93 (m, 1f),
ꢀ‑
139.63
ꢀ–ꢀ‑
139.70 (m, 1f),
ꢀ‑
161.36
ꢀ–ꢀ‑
161.48 (m, 1f). c-2为新化合物。
37.实施例20向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.6
ꢀµ
l(0.2 mmol,1当量)化合物a-3,在90 ℃下搅拌2小时后,得化合物c-3,产率为72%。1h nmr (400 mhz, cdcl3) δ 6.83
ꢀ–ꢀ
6.76 (m, 2h), 5.10 (d, j = 8.0 hz, 1h), 4.35
ꢀ–ꢀ
4.30 (m, 1h), 3.74 (s, 3h), 2.66
ꢀ–ꢀ
2.55 (m, 2h), 2.15
ꢀ–ꢀ
2.04 (m, 1h), 1.92
ꢀ–ꢀ
1.83 (m, 1h), 1.44 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
135.37
ꢀ–ꢀ‑
135.44 (m, 2f),
ꢀ‑
164.59
ꢀ–ꢀ‑
164.70 (m, 1f). c-3为新化合物。
38.实施例21
向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.3
ꢀµ
l(0.2 mmol,1当量)化合物a-4,在90 ℃下搅拌2小时后,得化合物c-4,产率为52%。1h nmr (400 mhz, cdcl3) δ 7.02
ꢀ–ꢀ
6.94 (m, 1h), 6.81
ꢀ–ꢀ
6.75 (m, 1h), 5.12 (d, j = 8.4 hz, 1h), 4.40
ꢀ–ꢀ
4.35 (m, 1h), 3.73 (s, 3h), 2.82
ꢀ–ꢀ
2.68 (m, 2h), 2.21
ꢀ–ꢀ
2.12 (m, 1h), 1.95
ꢀ–ꢀ
1.85 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
121.63
ꢀ–ꢀ‑
121.71 (m, 1f),
ꢀ‑
139.42
ꢀ–ꢀ‑
139.50 (m, 1f),
ꢀ‑
143.24
ꢀ–ꢀ‑
143.37 (m, 1f). c-4为新化合物。
39.实施例22向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,51.4 mg(0.2 mmol,1当量)化合物a-5,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,在90 ℃下搅拌2小时后,得化合物c-5,产率为51%。1h nmr (400 mhz, cdcl3) δ 5.12 (d, j = 8.4 hz, 1h), 4.38
ꢀ–ꢀ
4.33 (m, 1h), 3.74 (s, 3h), 2.83
ꢀ–ꢀ
2.68 (m, 2h), 2.23 (s, 3h), 2.19
ꢀ–ꢀ
2.13 (m, 1h), 1.93
ꢀ–ꢀ
1.84 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
114.58 (dd, j = 22.2 hz, 13.2 hz, 2f),
ꢀ‑
146.35 (dd, j = 22.2 hz, 12.8 hz, 2f). c-5为新化合物。
40.实施例23向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.9
ꢀµ
l(0.2 mmol,1当量)化合物a-6,在90 ℃下搅拌2小时后,得化合物c-6,产率为60%。1h nmr (400 mhz, cdcl3) δ 6.86
ꢀ–ꢀ
6.79 (m, 1h), 5.16 (d, j = 8.4 hz, 1h), 4.35
ꢀ–ꢀ
4.30 (m, 1h), 3.73 (s, 3h), 2.67 (t, j = 8.0 hz, 2h), 2.16
ꢀ–ꢀ
2.07 (m, 1h), 1.92
ꢀ–ꢀ
1.83 (m, 1h), 1.43 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
139.85
ꢀ–ꢀ‑
139.97 (m, 1f),
ꢀ‑
143.82
ꢀ–ꢀ‑
143.92 (m, 1f),
ꢀ‑
156.04 (t, j = 20.3 hz, 1f),
ꢀ‑
158.55
ꢀ–ꢀ‑
158.68 (m, 1f). c-6为新化合物。
41.实施例24
向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,30.2
ꢀµ
l(0.2 mmol,1当量)化合物a-7,在90 ℃下搅拌2小时后,得化合物c-7,产率为51%。1h nmr (400 mhz, cdcl3) δ 5.12 (d, j = 8.0 hz, 1h), 4.39
ꢀ–ꢀ
4.34 (m, 1h), 3.75 (s, 3h), 2.84
ꢀ–ꢀ
2.68 (m, 2h), 2.21
ꢀ–ꢀ
2.12 (m, 1h), 1.93
ꢀ–ꢀ
1.83 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
144.10 (dd, j = 21.8 hz, 7.1 hz, 2f),
ꢀ‑
157.17 (t, j = 20.7 hz, 1f),
ꢀ‑
162.58 (td, j = 21.4 hz, 7.5 hz, 2f). c-7为新化合物。
42.实施例25向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.0
ꢀµ
l(0.2 mmol,1当量)化合物a-8,在90 ℃下搅拌2小时后,得化合物c-8,产率为80%。1h nmr (400 mhz, cdcl3) δ 6.72
ꢀ–ꢀ
6.67 (m, 2h), 6.66
ꢀ–ꢀ
6.60 (m, 1h), 5.12 (d, j = 8.4 hz, 1h), 4.37
ꢀ–ꢀ
4.31 (m, 1h), 3.73 (s, 3h), 2.71
ꢀ–ꢀ
2.59 (m, 2h), 2.18
ꢀ–ꢀ
2.07 (m, 1h), 1.95
ꢀ–ꢀ
1.85 (m, 1h), 1.44 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
110.36 (t, j = 8.1 hz, 2f). c-8为新化合物。
43.实施例26向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,25.6
ꢀµ
l(0.2 mmol,1当量)化合物a-9,在90 ℃下搅拌2小时后,得化合物c-9,产率为74%。1h nmr (400 mhz, cdcl3) δ 7.09
ꢀ–ꢀ
7.02 (m, 1h), 7.00
ꢀ–ꢀ
6.95 (m, 1h), 6.89
ꢀ–ꢀ
6.86 (m, 1h), 5.07 (d, j = 6.0 hz, 1h), 4.36
ꢀ–ꢀ
4.31 (m, 1h), 3.73 (s, 3h), 2.65
ꢀ–ꢀ
2.61 (m, 2h), 2.16
ꢀ–ꢀ
2.07 (m, 1h), 1.94
ꢀ–ꢀ
1.84 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
138.13
ꢀ–ꢀ‑
138.24 (m, 1f),
ꢀ‑
141.78
ꢀ–ꢀ‑
141.84 (m, 1f). c-9为新化合物。
44.实施例27
向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,25.4
ꢀµ
l(0.2 mmol,1当量)化合物a-10,在90 ℃下搅拌2小时后,得化合物c-10,产率为67%。1h nmr (400 mhz, cdcl3) δ 7.16
ꢀ–ꢀ
7.10 (m, 1h), 6.81
ꢀ–ꢀ
6.73 (m, 2h), 5.11 (d, j = 8.8 hz, 1h), 4.36
ꢀ–ꢀ
4.30 (m, 1h), 3.71 (s, 3h), 2.66 (t, j = 7.8 hz, 2h), 2.15
ꢀ–ꢀ
2.06 (m, 1h), 1.93
ꢀ–ꢀ
1.84 (m, 1h), 1.44 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
113.14 (s, 1f),
ꢀ‑
114.43 (s, 1f). c-10为新化合物。
45.实施例28向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,41.4 mg(0.2 mmol,1当量)化合物a-11,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,在90 ℃下搅拌2小时后,得化合物c-11,产率为49%。1h nmr (400 mhz, cdcl3) δ 7.18
ꢀ–ꢀ
7.10 (m, 1h), 6.85
ꢀ–ꢀ
6.80 (m, 2h), 5.12 (d, j = 7.2 hz, 1h), 4.40
ꢀ–ꢀ
4.34 (m, 1h), 3.70 (s, 3h), 2.79
ꢀ–ꢀ
2.66 (m, 2h), 2.17
ꢀ–ꢀ
2.10 (m, 1h), 1.95
ꢀ–ꢀ
1.85 (m, 1h), 1.46 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
116.05 (t, j = 6.2 hz, 2f). c-11为新化合物。
46.实施例29向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,25.4
ꢀµ
l(0.2 mmol,1当量)化合物a-12,在90 ℃下搅拌2小时后,得化合物c-12,产率为79%。1h nmr (400 mhz, cdcl3) δ 7.04
ꢀ–ꢀ
6.97 (m, 2h), 6.96
ꢀ–ꢀ
6.92 (m, 1h), 5.10 (d, j = 8.4 hz, 1h), 4.38
ꢀ–ꢀ
4.33 (m, 1h), 3.72 (s, 3h), 2.73 (t, j = 7.8 hz, 2h), 2.20
ꢀ–ꢀ
2.11 (m, 1h), 1.97
ꢀ–ꢀ
1.88 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
139.25
ꢀ–ꢀ‑
139.34 (m, 1f),
ꢀ‑
144.49
ꢀ–ꢀ‑
144.57 (m, 1f). c-12为新化合物。
47.实施例30
8.4 hz, 1h), 4.36
ꢀ–ꢀ
4.30 (m, 1h), 3.72 (s, 3h), 2.65
ꢀ–ꢀ
2.60 (m, 2h), 2.15
ꢀ–ꢀ
2.06 (m, 1h), 1.93
ꢀ–ꢀ
1.84 (m, 1h), 1.44 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
119.46
ꢀ–ꢀ‑
119.50 (m, 1f). c-16为新化合物。
51.实施例34向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.0
ꢀµ
l(0.2 mmol,1当量)化合物a-17,在90 ℃下搅拌2小时后,得化合物c-17,产率为74%。1h nmr (400 mhz, cdcl3) δ 7.73 (q, j = 8.4 hz, 1h), 6.76 (dd, j = 8.0 hz, 2.8 hz, 1h), 5.14 (d, j = 8.4 hz, 1h), 4.34
ꢀ–ꢀ
4.29 (m, 1h), 3.72 (s, 3h), 2.68 (t, j = 7.8 hz, 2h), 2.17
ꢀ–ꢀ
2.08 (m, 1h), 1.95
ꢀ–ꢀ
1.86 (m, 1h), 1.44 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
71.76 (t, j = 9.8 hz, 1f),
ꢀ‑
72.46 (t, j = 10.7 hz, 1f). c-17为新化合物。
52.实施例35向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.0
ꢀµ
l(0.2 mmol,1当量)化合物a-18,在90 ℃下搅拌2小时后,得化合物c-18,产率为73%。1h nmr (400 mhz, cdcl3) δ 7.83 (d, j = 4.8 hz, 1h), 7.03 (t, j = 4.8 hz, 1h), 5.22 (d, j = 8.4 hz, 1h), 4.37
ꢀ–ꢀ
4.31 (m, 1h), 3.71 (s, 3h), 2.76 (t, j = 7.8 hz, 2h), 2.21
ꢀ–ꢀ
2.13 (m, 1h), 1.98
ꢀ–ꢀ
1.89 (m, 1h), 1.41 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
88.82 (d, j = 26.7 hz, 1f),
ꢀ‑
146.68 (dd, j = 27.1 hz, 4.5 hz, 1f). c-18为新化合物。
53.实施例36向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,24.0
ꢀµ
l(0.2 mmol,1当量)化合物a-19,在90 ℃下搅拌2小时后,得化合物c-19,产率为74%。1h nmr (400 mhz, cdcl3) δ 8.03 (s, 1h), 7.61 (t, j = 7.8 hz, 1h), 6.86 (d, j = 6.8 hz, 1h), 5.13 (d, j = 7.6 hz, 1h), 4.36
ꢀ–ꢀ
4.32 (m, 1h), 3.72 (s, 3h), 2.70
ꢀ–ꢀ
2.65 (m, 2h), 2.17
ꢀ–ꢀ
2.08 (m, 1h), 1.96
ꢀ–ꢀ
1.86 (m, 1h), 1.44 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
71.69 (s, 1f). c-19为新化合物。
54.实施例37向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,21.4
ꢀµ
l(0.2 mmol,1当量)化合物a-20,在90 ℃下搅拌2小时后,得化合物c-1,产率为67%。1h nmr (400 mhz, cdcl3) δ 7.04
ꢀ–ꢀ
6.98 (m, 1h), 6.91
ꢀ–ꢀ
6.84 (m, 1h), 5.09 (d, j = 8.4 hz, 1h), 4.36
ꢀ–ꢀ
4.31 (m, 1h), 3.73 (s, 3h), 2.64 (t, j = 8.0 hz, 2h), 2.16
ꢀ–ꢀ
2.07 (m, 1h), 1.93
ꢀ–ꢀ
1.83 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
120.10
ꢀ–ꢀ‑
120.14 (m, 1f),
ꢀ‑
136.61
ꢀ–ꢀ‑
136.71 (m, 1f),
ꢀ‑
143.14
ꢀ–ꢀ‑
143.28 (m, 1f). c-1为新化合物。
55.实施例38向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,26.0
ꢀµ
l(0.2 mmol,1当量)化合物a-21,在90 ℃下搅拌2小时后,得化合物c-3,产率为68%。1h nmr (400 mhz, cdcl3) δ 6.83
ꢀ–ꢀ
6.76 (m, 2h), 5.10 (d, j = 8.0 hz, 1h), 4.35
ꢀ–ꢀ
4.30 (m, 1h), 3.74 (s, 3h), 2.66
ꢀ–ꢀ
2.55 (m, 2h), 2.15
ꢀ–ꢀ
2.04 (m, 1h), 1.92
ꢀ–ꢀ
1.83 (m, 1h), 1.44 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
135.37
ꢀ–ꢀ‑
135.44 (m, 2f),
ꢀ‑
164.59
ꢀ–ꢀ‑
164.70 (m, 1f). c-3为新化合物。
56.实施例39向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,25.1
ꢀµ
l(0.2 mmol,1当量)化合物a-22,在90 ℃下搅拌2小时后,得化合物c-8,产率为77%。1h nmr (400 mhz, cdcl3) δ 6.72
ꢀ–ꢀ
6.67 (m, 2h), 6.66
ꢀ–ꢀ
6.60 (m, 1h), 5.12 (d, j = 8.4 hz, 1h), 4.37
ꢀ–ꢀ
4.31 (m, 1h), 3.73 (s, 3h), 2.71
ꢀ–ꢀ
2.59 (m, 2h), 2.18
ꢀ–ꢀ
2.07 (m, 1h), 1.95
ꢀ–ꢀ
1.85 (m, 1h), 1.44 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
110.36 (t, j = 8.1 hz, 2f). c-8为新化合物。
57.实施例40
向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-1,25.1
ꢀµ
l(0.2 mmol,1当量)化合物a-23,在90 ℃下搅拌2小时后,得化合物c-9,产率为71%。1h nmr (400 mhz, cdcl3) δ 7.09
ꢀ–ꢀ
7.02 (m, 1h), 7.00
ꢀ–ꢀ
6.95 (m, 1h), 6.89
ꢀ–ꢀ
6.86 (m, 1h), 5.07 (d, j = 6.0 hz, 1h), 4.36
ꢀ–ꢀ
4.31 (m, 1h), 3.73 (s, 3h), 2.65
ꢀ–ꢀ
2.61 (m, 2h), 2.16
ꢀ–ꢀ
2.07 (m, 1h), 1.94
ꢀ–ꢀ
1.84 (m, 1h), 1.45 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
138.13
ꢀ–ꢀ‑
138.24 (m, 1f),
ꢀ‑
141.78
ꢀ–ꢀ‑
141.84 (m, 1f). c-9为新化合物。
58.实施例41向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-2,26.6
ꢀµ
l(0.2 mmol,1当量)化合物a-3,在90 ℃下搅拌2小时后,得化合物c-3d,产率为79%(>99% ee)。1h nmr (400 mhz, cdcl3) δ 6.81
ꢀ–ꢀ
6.77 (m, 2h), 5.10 (d, j = 8.8 hz, 1h), 4.35
ꢀ–ꢀ
4.30 (m, 1h), 3.74 (s, 3h), 2.64
ꢀ–ꢀ
2.59 (m, 2h), 2.15
ꢀ–ꢀ
2.06 (m, 1h), 1.92
ꢀ–ꢀ
1.83 (m, 1h), 1.44 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
134.81
ꢀ–ꢀ‑
134.89 (m, 2f),
ꢀ‑
164.03
ꢀ–ꢀ‑
164.15 (m, 1f). c-3d为新化合物。
59.实施例42向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-3,26.6
ꢀµ
l(0.2 mmol,1当量)化合物a-3,在90 ℃下搅拌2小时后,得化合物c-3l,产率为75%(>99% ee)。1h nmr (400 mhz, cdcl3) δ 6.81
ꢀ–ꢀ
6.77 (m, 2h), 5.10 (d, j = 8.4 hz, 1h), 4.35
ꢀ–ꢀ
4.30 (m, 1h), 3.74 (s, 3h), 2.64
ꢀ–ꢀ
2.59 (m, 2h), 2.15
ꢀ–ꢀ
2.06 (m, 1h), 1.92
ꢀ–ꢀ
1.83 (m, 1h), 1.44 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
135.87
ꢀ–ꢀ‑
135.95 (m, 2f),
ꢀ‑
165.09
ꢀ–ꢀ‑
165.22 (m, 1f). c-3l为新化合物。
60.实施例43
向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-2,25.7
ꢀµ
l(0.2 mmol,1当量)化合物a-13,在90 ℃下搅拌2小时后,得化合物c-13d,产率为77%(>99% ee)。1h nmr (400 mhz, cdcl3) δ 6.97
ꢀ–ꢀ
6.92 (m, 1h), 6.90
ꢀ–ꢀ
6.81 (m, 2h), 5.13 (d, j = 8.8 hz, 1h), 4.38
ꢀ–ꢀ
4.32 (m, 1h), 3.72 (s, 3h), 2.67 (t, j = 8.0 hz, 2h), 2.18
ꢀ–ꢀ
2.09 (m, 1h), 1.95
ꢀ–ꢀ
1.86 (m, 1h), 1.44 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
119.33
ꢀ–ꢀ‑
119.41 (m, 1f),
ꢀ‑
124.77
ꢀ–ꢀ‑
124.84 (m, 1f). c-13d为新化合物。
61.实施例44向25 ml的反应管中,加入1.1 mg(0.005 mmol)溴化镍,氩气置换三次后加入2 ml n-甲基吡咯烷酮(nmp),注射0.4 ml(0.4 mmol,1m)锌试剂b-3,25.7
ꢀµ
l(0.2 mmol,1当量)化合物a-13,在90 ℃下搅拌2小时后,得化合物c-13l,产率为73%(>99% ee)。1h nmr (400 mhz, cdcl3) δ 6.97
ꢀ–ꢀ
6.91 (m, 1h), 6.90
ꢀ–ꢀ
6.81 (m, 2h), 5.14 (d, j = 8.4 hz, 1h), 4.37
ꢀ–ꢀ
4.34 (m, 1h), 3.72 (s, 3h), 2.67 (t, j = 8.0 hz, 2h), 2.18
ꢀ–ꢀ
2.09 (m, 1h), 1.95
ꢀ–ꢀ
1.86 (m, 1h), 1.44 (s, 9h). 19
f nmr (376 mhz, cdcl3) δ
ꢀ‑
119.33
ꢀ–ꢀ‑
119.41 (m, 1f),
ꢀ‑
124.79
ꢀ–ꢀ‑
124.84 (m, 1f). c-13l为新化合物。
62.上述实施例1~实施例44合成的化合物c-1、化合物c-2、化合物c-3、化合物c-4、化合物c-5、化合物c-6、化合物c-7、化合物c-8、化合物c-9、化合物c-10、化合物c-11、化合物c-12、化合物c-13、化合物c-14、化合物c-15、化合物c-16、化合物c-17、化合物c-18、化合物c-19、化合物c-3d、化合物c-3l、化合物c-13d、化合物c-13l都是新化合物,在医药、农药、材料学中有着潜在的作用。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1