十三肽衍生物及其制备方法和应用
本发明属于生物医药领域,涉及十三肽衍生物及其制备方法和应用。
背景技术:
1、近年来由于多种因素导致的愈发严重的细菌耐药问题,如“超级细菌”的出现,使得细菌耐药性和耐药菌感染成为当前全球抗感染治疗和抗菌药物研发领域面临的巨大挑战。
2、2017年who发布首份急需研发新抗生素的重点病原体清单,其中1类重点包括:碳青霉烯耐药鲍曼不动杆菌(crab)、铜绿假单胞菌(crpa)和肠杆菌科细菌(cre)。这些“超级细菌”均为革兰阴性耐药菌。目前临床上用于治疗革兰阴性耐药感染的有效药物并不多,多粘菌素类药物往往作为“最后一道防线”使用。近些年已经在肺炎克雷伯杆菌和大肠埃希菌中发现了多粘菌素的抗性基因mcr-1,多粘菌素在临床上的作用也受到了挑战。开发新的抗革兰阴性耐药菌药物或其先导化合物极具紧迫性。
技术实现思路
1、本发明的目的是提供十三肽衍生物及其制备方法和应用。
2、本发明提供一株多粘类芽孢杆菌,即多粘类芽孢杆菌(paenibacillus polymyxa)cpcc 101223,已于2021年07月08日保藏于中国微生物菌种保藏管理委员会普通微生物中心(简称cgmcc,地址为:北京市朝阳区北辰西路1号院3号,中国科学院微生物研究所),保藏登记号为cgmcc no.22854。
3、本发明还提供了通式化合物的制备方法,包括如下步骤:发酵培养多粘类芽孢杆菌cpcc 101223,得到通式化合物。
4、具体的,所述制备方法包括如下步骤:用培养基发酵培养多粘类芽孢杆菌cpcc101223,得到发酵产物,从所述发酵产物中得到所述通式化合物。
5、所述培养基具体可为微生物培养基。
6、所述培养基具体可为发酵培养基。
7、用培养基发酵培养多粘类芽孢杆菌cpcc 101223的方法具体包括如下步骤:
8、(1)将多粘类芽孢杆菌cpcc 101223接种发酵培养基中,振荡培养;
9、(2)完成步骤(1)后,在体系中加入大孔吸附树脂,振荡培养,得到发酵产物。
10、用培养基发酵培养多粘类芽孢杆菌cpcc 101223的方法具体包括如下步骤:
11、(1)将多粘类芽孢杆菌cpcc 101223接种至发酵培养基中,振荡培养20h;
12、(2)完成步骤(1)后,在体系中加入大孔吸附树脂,振荡培养4h,得到发酵产物。
13、用培养基发酵培养多粘类芽孢杆菌cpcc 101223的方法具体包括如下步骤:
14、(1)将100ml多粘类芽孢杆菌cpcc 101223种子液接种至1l发酵培养基中,振荡培养20h;
15、(2)完成步骤(1)后,在体系中加入100ml大孔吸附树脂,振荡培养4h,得到发酵产物。
16、用培养基发酵培养多粘类芽孢杆菌cpcc 101223的方法具体包括如下步骤:
17、(1)将100ml多粘类芽孢杆菌cpcc 101223种子液接种至1l发酵培养基中,30℃、200r/min振荡培养20h;
18、(2)完成步骤(1)后,在体系中加入100ml大孔吸附树脂,30℃、200r/min振荡培养4h,得到发酵产物。
19、以上任一所述种子液的制备方法,包括如下步骤:挑取多粘类芽孢杆菌cpcc101223单菌落,接种至种子培养基中,振荡培养,得到种子液。
20、以上任一所述种子液的制备方法,包括如下步骤:挑取多粘类芽孢杆菌cpcc101223单菌落,接种至种子培养基中,振荡培养16h,得到种子液。
21、以上任一所述种子液的制备方法,包括如下步骤:挑取多粘类芽孢杆菌cpcc101223单菌落,接种至100ml种子培养基中,30℃、200r/min振荡培养16h,得到种子液。
22、种子培养基(tsb培养基):含胰蛋白胨15g/l、大豆蛋白胨5g/l、氯化钠5g/l,余量为水;ph为7.0-7.4。
23、发酵培养基:含玉米粉30g/l、可溶性淀粉10g/l、酵母粉1g/l、硫酸铵5g/l、碳酸钙10g/l,余量为水;ph为7.0-7.4。
24、从所述发酵产物中得到所述通式化合物的方法包括如下步骤:
25、(1)取所述发酵产物,收集大孔吸附树脂并将其转移至层析柱中,然后依次用去离子水、40%异丙醇水溶液、80%异丙醇水溶液洗脱层析柱,收集80%异丙醇水溶液进行洗脱时的过柱后洗脱液。
26、(2)取步骤(1)收获的过柱后洗脱液,进行固体上样并进行色谱分离纯化,获得fr.4和/或fr.5;
27、(3)取步骤(2)获得的fr.4,进行固体上样并进行色谱分离纯化,获得fr.4-4和/或fr.4-5和/或fr.4-6和/或fr.4-7和/或fr.4-8和/或fr.4-10和/或fr.4-11和/或fr.4-12和/或fr.4-13;
28、(4)取fr.5和/或fr.4-4和/或fr.4-5和/或fr.4-6和/或fr.4-7和/或fr.4-8和/或fr.4-10和/或fr.4-11和/或fr.4-12和/或fr.4-13,通过液相色谱分离纯化获得所述通式化合物。
29、从所述发酵产物中得到所述通式化合物的方法的所述步骤(1)为:取24l所述发酵产物,收集大孔吸附树脂并将其转移至层析柱中(柱体积2l),然后依次用10l去离子水、20l40%异丙醇水溶液、30l 80%异丙醇水溶液洗脱层析柱,收集80%异丙醇水溶液进行洗脱时的过柱后洗脱液。
30、步骤(1)中,所述洗脱的流速为2倍柱体积/h。
31、从所述发酵产物中得到所述通式化合物的方法的所述步骤(2)为:取步骤(1)收集的过柱后洗脱液,浓缩,然后加入溶胀后的ymc ods-aq-hg填料拌匀,然后浓缩蒸干,得到固体样品;将固体样品填充至样品柱,然后连接色谱柱,用色谱仪进行分离纯化。
32、从所述发酵产物中得到所述通式化合物的方法的所述步骤(2)为:取步骤(1)收集的过柱后洗脱液,采用旋转蒸发仪浓缩至100ml,然后加入10ml溶胀后的ymc ods-aq-hg填料拌匀,然后浓缩蒸干,得到固体样品;将固体样品填充至样品柱,然后连接色谱柱,用色谱仪进行分离纯化。
33、从所述发酵产物中得到所述通式化合物的方法的所述步骤(2)中,色谱柱为flashspherical c18 20-35μm 100a 120g。
34、从所述发酵产物中得到所述通式化合物的方法的所述步骤(2)中,色谱仪为美国teledyne isco公司combiflash rf200制备型色谱仪。
35、从所述发酵产物中得到所述通式化合物的方法的所述步骤(2)中,洗脱程序为:0-20min,流动相由20%流动相b和80%流动相a组成;20-35min,流动相b占流动相的体积分数由20%线性上升至40%,相应的流动相a占流动相的体积分数由80%线性下降至60%;35-70min,流动相由40%流动相b和60%流动相a组成。
36、从所述发酵产物中得到所述通式化合物的方法的所述步骤(2)中,洗脱程序为:0-20min,流动相由20%流动相b和80%流动相a组成;20-35min,流动相b占流动相的体积分数由20%线性上升至40%,相应的流动相a占流动相的体积分数由80%线性下降至60%;35-70min,流动相由40%流动相b和60%流动相a组成;70-100min,流动相b占流动相的体积分数由40%线性上升至100%,相应的流动相a占流动相的体积分数由60%线性下降至0%;100-120min,流动相全部为流动相b。
37、流动相a:由三氟乙酸和水组成,三氟乙酸浓度为0.05%;流动相b:由三氟乙酸和乙腈组成,三氟乙酸浓度为0.05%。
38、从所述发酵产物中得到所述通式化合物的方法的所述步骤(2)中,流动相流速为20ml/min。
39、从所述发酵产物中得到所述通式化合物的方法的所述步骤(2)中,检测波长为210nm。
40、收集流份,每个流份即对应一个洗脱峰的过柱后溶液,获得如下流份:fr.4和/或fr.5。
41、fr.4对应保留时间tr 25-40min的洗脱峰;fr.5对应tr 40-45min的洗脱峰。
42、从所述发酵产物中得到所述通式化合物的方法的所述步骤(3)为:取fr.4,浓缩,然后加入溶胀后的ymc ods-aq-hg填料,然后蒸干,得到固体样品;将固体样品填充至样品柱,然后连接色谱柱,用色谱仪进行分离纯化。
43、从所述发酵产物中得到所述通式化合物的方法的所述步骤(3)为:取300ml的fr.4,采用旋转蒸发仪浓缩至10ml,然后加入5ml溶胀后的ymc ods-aq-hg填料,然后蒸干,得到固体样品;将固体样品填充至样品柱,然后连接色谱柱,用色谱仪进行分离纯化。
44、从所述发酵产物中得到所述通式化合物的方法的所述步骤(3)中,色谱柱为flashspherical c18 20-35μm 100a 120g。
45、从所述发酵产物中得到所述通式化合物的方法的所述步骤(3)中,色谱仪为美国teledyne isco公司combiflash rf200制备型色谱仪。
46、从所述发酵产物中得到所述通式化合物的方法的所述步骤(3)中,洗脱程序为:0-40min,流动相由20%流动相b和80%流动相a组成;40-60min,流动相b占流动相的体积分数由20%线性上升至40%,相应的流动相a占流动相的体积分数由80%线性下降至60%;60-90min,流动相由40%流动相b和60%流动相a组成;90-120min,流动相b占流动相的体积分数由40%线性上升至100%,相应的流动相a占流动相的体积分数由60%线性下降至0%。
47、从所述发酵产物中得到所述通式化合物的方法的所述步骤(3)中,洗脱程序为:0-40min,流动相由20%流动相b和80%流动相a组成;40-60min,流动相b占流动相的体积分数由20%线性上升至40%,相应的流动相a占流动相的体积分数由80%线性下降至60%;60-90min,流动相由40%流动相b和60%流动相a组成;90-120min,流动相b占流动相的体积分数由40%线性上升至100%,相应的流动相a占流动相的体积分数由60%线性下降至0%;120-140min,流动相全部为流动相b。
48、流动相a:由三氟乙酸和水组成,三氟乙酸浓度为0.15%;流动相b:由三氟乙酸和乙腈组成,三氟乙酸浓度为0.15%。
49、从所述发酵产物中得到所述通式化合物的方法的所述步骤(3)中,流动相流速为20ml/min。
50、从所述发酵产物中得到所述通式化合物的方法的所述步骤(3)中,检测波长为210nm。
51、收集流份,每个流份即对应一个洗脱峰的过柱后溶液,获得如下流份:fr.4-4和/或fr.4-5和/或fr.4-6和/或fr.4-7和/或fr.4-8和/或fr.4-10和/或fr.4-11和/或fr.4-12和/或fr.4-13。
52、fr.4-4对应保留时间tr 27-30min的洗脱峰。fr.4-5对应保留时间tr 30-46min的洗脱峰。fr.4-6对应保留时间tr 46-68min的洗脱峰。fr.4-7对应保留时间tr 68-72min的洗脱峰。fr.4-8对应保留时间tr72-74min的洗脱峰。fr.4-10对应保留时间tr 78-85min的洗脱峰。fr.4-11对应保留时间tr85-92min的洗脱峰。fr.4-12对应保留时间tr 92-102min的洗脱峰。fr.4-13对应保留时间tr102-110min的洗脱峰。
53、从所述发酵产物中得到所述通式化合物的方法的所述步骤(4)中,色谱仪为岛津lc-20液相色谱仪(lc-20ad)。
54、从所述发酵产物中得到所述通式化合物的方法的所述步骤(4)中,色谱柱为ymc-pack ods-aq,10mm*250mm,孔径5μm。
55、从所述发酵产物中得到所述通式化合物的方法的所述步骤(4)中,流动相流速为4ml/min。
56、从所述发酵产物中得到所述通式化合物的方法的所述步骤(4)中,检测波长为210nm。
57、取fr.5和/或fr.4-4和/或fr.4-5和/或fr.4-6和/或fr.4-7和/或fr.4-8和/或fr.4-10和/或fr.4-11和/或fr.4-12和/或fr.4-13,浓缩蒸干,用40%乙腈水溶液溶解,即为浓缩液。
58、上样fr.4-4的浓缩液(具体上样量可为3ml);流动相由三氟乙酸、乙腈和水组成,三氟乙酸的浓度为0.15%,乙腈的浓度为31%;收集峰值对应的保留时间为8.21min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物1。
59、上样fr.4-5的浓缩液(具体上样量可为3ml);流动相由三氟乙酸、乙腈和水组成,三氟乙酸的浓度为0.15%,乙腈的浓度为33%;收集峰值对应的保留时间为8.37min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物2。
60、上样fr.4-5的浓缩液(具体上样量可为3ml);流动相由三氟乙酸、乙腈和水组成,三氟乙酸的浓度为0.15%,乙腈的浓度为33%;收集峰值对应的保留时间为9.24min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物3。
61、上样fr.4-5的浓缩液(具体上样量可为3ml);流动相由三氟乙酸、乙腈和水组成,三氟乙酸的浓度为0.15%,乙腈的浓度为33%;收集峰值对应的保留时间为8.37min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物2;收集峰值对应的保留时间为9.24min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物3。
62、上样fr.4-6的浓缩液(具体上样量可为3ml);流动相由三氟乙酸、乙腈和水组成,三氟乙酸的浓度为0.15%,乙腈的浓度为34%;收集峰值对应的保留时间为9.54min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物4。
63、上样fr.4-7的浓缩液(具体上样量可为3ml);流动相由三氟乙酸、乙腈和水组成,三氟乙酸的浓度为0.15%,乙腈的浓度为35%;收集峰值对应的保留时间为9.76min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物5。
64、上样fr.4-8的浓缩液(具体上样量可为3ml);流动相由三氟乙酸、乙腈和水组成,三氟乙酸的浓度为0.15%,乙腈的浓度为39%;收集峰值对应的保留时间为7.83min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物6。
65、上样fr.4-10的浓缩液(具体上样量可为3ml);流动相由三氟乙酸、乙腈和水组成,三氟乙酸的浓度为0.15%,乙腈的浓度为40%;收集峰值对应的保留时间为8.11min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物7。
66、上样fr.4-11的浓缩液(具体上样量可为2ml);流动相由三氟乙酸、乙腈和水组成,三氟乙酸的浓度为0.15%,乙腈的浓度为40%;收集峰值对应的保留时间为8.41min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物8。
67、上样fr.4-12的浓缩液(具体上样量可为2ml);流动相由三氟乙酸、乙腈和水组成,三氟乙酸的浓度为0.15%,乙腈的浓度为40%;收集峰值对应的保留时间为8.92min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物9。
68、上样fr.4-13的浓缩液(具体上样量可为2ml);流动相由三氟乙酸、乙腈和水组成,三氟乙酸的浓度为0.15%,乙腈的浓度为41%;收集峰值对应的保留时间为9.82min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物10。
69、上样fr.5的浓缩液(具体上样量可为2ml);流动相由三氟乙酸、乙腈和水组成,三氟乙酸的浓度为0.15%,乙腈的浓度为42%;收集峰值对应的保留时间为10.37min的洗脱峰对应的过柱后洗脱液,采用旋转蒸发仪浓缩,然后冷冻干燥,得到化合物11。
70、以上%,如无特殊说明均指的是体积百分含量。
71、以上任一所述大孔吸附树脂为非极性大孔吸附树脂。
72、以上任一所述大孔吸附树脂为diaion hp20大孔吸附树脂。
73、以上任一所述大孔吸附树脂满足如下指标中的任意一种或任意组合:水含量(%)为55-65,湿视密度(g/l-r)为680,孔体积(ml/g)为1.3,比表面积(m2/g)为590,好频度半径为290,粒度分布(≥0.25mm)≥90%,有效粒径(mm)≥0.25,均一系数≤1.6,使用温度(℃)≤130。
74、本发明还提供了通式的化合物。
75、本发明还保护多粘类芽孢杆菌cpcc 101223在制备通式化合物中的应用。
76、本发明还保护通式的化合物或其药学上可接受的盐在制备细菌抑制剂中的应用。
77、本发明还保护细菌抑制剂,其含有通式化合物或其药学上可接受的盐。
78、本发明还保护多粘类芽孢杆菌cpcc 101223的培养物,是将多粘类芽孢杆菌cpcc101223进行培养得到的物质。所述进行培养具体可为采用培养基进行培养。所述培养基具体可为微生物培养基。所述培养基具体可为发酵培养基。所述发酵培养基培养基具体可为上述发酵培养基。所述培养物具体可为上述用培养基发酵培养多粘类芽孢杆菌cpcc101223得到的发酵产物。
79、本发明还保护多粘类芽孢杆菌cpcc 101223或/和多粘类芽孢杆菌cpcc 101223的培养物在制备细菌抑制剂中的应用。
80、本发明还保护一种细菌抑制剂,其含有多粘类芽孢杆菌cpcc 101223或/和多粘类芽孢杆菌cpcc 101223的培养物。
81、本发明还保护一种细菌抑制剂的制备方法,包括如下步骤:将多粘类芽孢杆菌cpcc 101223或/和多粘类芽孢杆菌cpcc 101223的培养物作为细菌抑制剂的成分,得到所述细菌抑制剂。
82、以上任一所述通式化合物为如下通式的化合物:
83、x1-x2-dab-gly-ser-trp-ser-dab-dab-x3-glu-val-x4-ala;
84、x1为3-羟基-6-甲基辛酸、6-甲基庚酸、6-甲基辛酸,3-羟基-8-甲基壬酸、3-羟基癸酸或3-羟基-8-甲基癸酸;
85、x2为gly或val;
86、x3为val、ile或trp;
87、x4为val或ile。
88、具体的,所述通式化合物可为化合物7或化合物9或化合物11或化合物10或化合物8或化合物4或化合物5或化合物6或化合物1或化合物2或化合物3。
89、所述化合物1,x1为3-羟基-6-甲基辛酸,x2为gly,x3为val,x4为val。
90、所述化合物2,x1为6-甲基庚酸,x2为gly,x3为val,x4为val。
91、所述化合物3,x1为6-甲基庚酸,x2为gly,x3为ile,x4为val。
92、所述化合物4,x1为6-甲基辛酸,x2为gly,x3为val,x4为val。
93、所述化合物5,x1为6-甲基辛酸,x2为gly,x3为ile,x4为val。
94、所述化合物6,x1为6-甲基辛酸,x2为gly,x3为val,x4为ile。
95、所述化合物7,x1为3-羟基-8-甲基壬酸,x2为val,x3为trp,x4为val。
96、所述化合物8,x1为3-羟基癸酸,x2为val,x3为trp,x4为val。
97、所述化合物9,x1为3-羟基-8-甲基壬酸,x2为val,x3为trp,x4为ile。
98、所述化合物10,x1为3-羟基-8-甲基癸酸,x2为val,x3为trp,x4为ile。
99、所述化合物11,x1为3-羟基-8-甲基癸酸,x2为val,x3为trp,x4为val。
100、gly、val、ile、trp均为氨基酸。
101、gly为甘氨酸。val为缬氨酸。ile为异亮氨酸。trp为色氨酸。
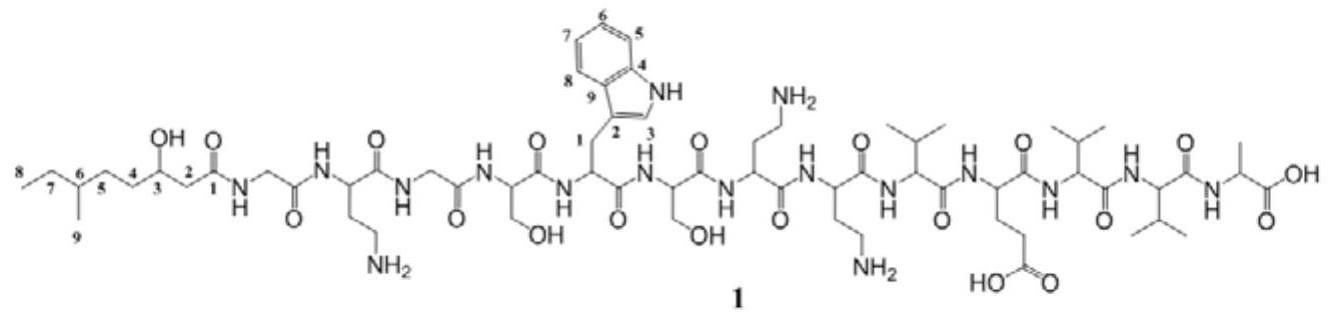
102、所述化合物1的结构式如下:
103、
104、所述化合物2的结构式如下:
105、
106、所述化合物3的结构式如下:
107、
108、所述化合物4的结构式如下:
109、
110、所述化合物5的结构式如下:
111、
112、所述化合物6的结构式如下:
113、
114、所述化合物7的结构式如下:
115、
116、所述化合物8的结构式如下:
117、
118、所述化合物9的结构式如下:
119、
120、所述化合物10的结构式如下:
121、
122、所述化合物11的结构式如下:
123、
124、以上任一所述细菌可为革兰阴性菌或革兰阳性菌。
125、所述革兰阴性菌包括但不限于:大肠埃希菌、肺炎克雷伯杆菌、丁香假单胞菌、鲍曼不动杆菌、阴沟肠杆菌、产气肠杆菌、弗劳地枸橼酸菌、雷极普鲁菲登杆菌、嗜麦芽假单孢菌或福氏志贺菌。
126、所述革兰阳性菌包括但不限于:金黄色葡萄球菌或屎肠球菌。
127、以上任一所述细菌具体可为表5中记载的各个细菌。
128、以上任一所述细菌可为敏感菌也可为耐药菌。
129、所述耐药可为如下任意一种或任意组合:甲氧西林耐药、万古霉素耐药、超广谱β-内酰胺酶引起的耐药、新德里金属-β-内酰胺酶1引起的耐药、多粘菌素耐药基因引起的耐药。
130、上文中,所述细菌抑制剂,除含有所述通式的化合物或其药学上可接受的盐外,还可含有适宜的载体或赋形剂。这里的载体材料包括但不限于水溶性载体材料(如聚乙二醇、聚乙烯吡咯烷酮、有机酸等)、难溶性载体材料(如乙基纤维素、胆固醇硬脂酸酯等)、肠溶性载体材料(如醋酸纤维素酞酸酯和羧甲乙纤维素等)。其中优选的是水溶性载体材料。使用这些材料可以制成多种剂型,包括但不限于片剂、胶囊、滴丸、气雾剂、丸剂、粉剂、溶液剂、混悬剂、乳剂、颗粒剂、脂质体、透皮剂、口含片、栓剂、冻干粉针剂等。可以是普通制剂、缓释制剂、控释制剂及各种微粒给药系统。为了将单位给药剂型制成片剂,可以广泛使用本领域公知的各种载体。关于载体的例子是,例如稀释剂与吸收剂,如淀粉、糊精、硫酸钙、乳糖、甘露醇、蔗糖、氯化钠、葡萄糖、尿素、碳酸钙、白陶土、微晶纤维素、硅酸铝等;湿润剂与粘合剂,如水、甘油、聚乙二醇、乙醇、丙醇、淀粉浆、糊精、糖浆、蜂蜜、葡萄糖溶液、阿拉伯胶浆、明胶浆、羧甲基纤维素钠、紫胶、甲基纤维素、磷酸钾、聚乙烯吡咯烷酮等;崩解剂,例如干燥淀粉、海藻酸盐、琼脂粉、褐藻淀粉、碳酸氢钠与枸橼酸、碳酸钙、聚氧乙烯、山梨糖醇脂肪酸酯、十二烷基磺酸钠、甲基纤维素、乙基纤维素等;崩解抑制剂,例如蔗糖、三硬脂酸甘油酯、可可脂、氢化油等;吸收促进剂,例如季铵盐、十二烷基硫酸钠等;润滑剂,例如滑石粉、二氧化硅、玉米淀粉、硬脂酸盐、硼酸、液体石蜡、聚乙二醇等。还可以将片剂进一步制成包衣片,例如糖包衣片、薄膜包衣片、肠溶包衣片,或双层片和多层片。为了将单位给药剂型制成丸剂,可以广泛使用本领域公知的各种载体。关于载体的例子是,例如稀释剂与吸收剂,如葡萄糖、乳糖、淀粉、可可脂、氢化植物油、聚乙烯吡咯烷酮、gelucire、高岭土、滑石粉等;粘合剂如阿拉伯胶、黄蓍胶、明胶、乙醇、蜂蜜、液糖、米糊或面糊等;崩解剂,如琼脂粉、干燥淀粉、海藻酸盐、十二烷基磺酸钠、甲基纤维素、乙基纤维素等。为了将单位给药剂型制成栓剂,可以广泛使用本领域公知的各种载体。关于载体的例子是,例如聚乙二醇、卵磷脂、可可脂、高级醇、高级醇的酯、明胶、半合成甘油酯等。为了将单位给药剂型制成注射用制剂,如溶液剂、乳剂、冻干粉针剂和混悬剂,可以使用本领域常用的所有稀释剂,例如,水、乙醇、聚乙二醇、1,3-丙二醇、乙氧基化的异硬脂醇、多氧化的异硬脂醇、聚氧乙烯山梨醇脂肪酸酯等。另外,为了制备等渗注射液,可以向注射用制剂中添加适量的氯化钠、葡萄糖或甘油,此外,还可以添加常规的助溶剂、缓冲剂、ph调节剂等。此外,如需要,也可以向药物制剂中添加着色剂、防腐剂、香料、矫味剂、甜味剂或其它材料。使用上述剂型可以经注射给药,包括皮下注射、静脉注射、肌肉注射和腔内注射等;腔道给药,如经直肠和阴道;呼吸道给药,如经鼻腔;粘膜给药。
131、本发明分离获得了多粘类芽孢杆菌(paenibacillus polymyxa)cpcc 101223,并从其发酵产物中获得了11个十三肽类新产物,具有较好的抗菌活性(包括革兰阳性菌和革兰阴性菌),特别具有抗革兰阴性耐药菌活性。化合物1-11的结构差异显著影响了其抗菌活性。本发明化合物来源与多粘类芽孢杆菌,制备工艺简单,具有较好的抗革兰阴性耐药菌活性,为阐明十三肽抗菌活性的构效关系提供了理论基础,适宜于抗革兰阴性耐药菌先导化合物研究或制备抗革兰阴性耐药菌药物。
- 还没有人留言评论。精彩留言会获得点赞!