病原微生物宏基因组定量检测的内标分子、试剂盒以及方法与流程
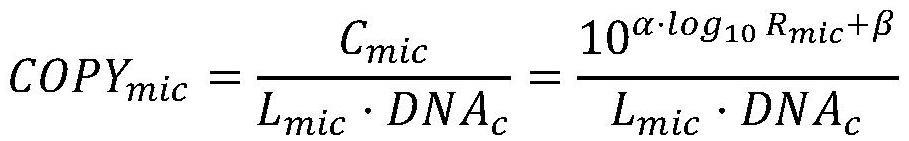
本发明涉及生物医药领域,特别是涉及病原微生物宏基因组定量检测的内标分子、试剂盒以及方法。
背景技术:
1、宏基因组(metagenome)(也称微生物环境基因组microbial environmentalgenome)。是由handelsam等1998年提出的新名词,定义为“the genomes ot the totalmicrobilta found in nature”,即生物环境中所有微小生物遗传物质的总和。目前宏基因组测序已经得到广泛的应用,如研究某种微生物的多样性(钟勇,基于宏基因组测序的扶桑绵粉蚧内共生菌多样性研究【j】pingyang customs,2020,29(4):273-278)、基于宏基因组测序研究环境中菌群的影响(郑微,宏基因组测序技术分析原发性肝癌患者肠道菌群特征【j】首都医科大学附属北京佑安医院临检中心,1674-1358.2021.03.002)、感染性疾病诊断中的应用(liu wei-ping,xia hui,tao zhi-yong.the use of metagenomic sequencingtechnology to diagnose infectious diseases[j]bengbu medical college,2021may;16(5):614-618)等。
2、呼吸道大部分微生物为常驻菌,只有达到一定丰度后才会有致病的风险,所以在呼吸道感染检测中除了定性检测外,定量也是指导医生准确诊断的重要指标。在宏基因组测序技术中,由于人源背景的影响,目前无法对样本中的微生物进行定量,因此实现宏基因组对病原微生物的定量具有重要的意义。目前对样本中微生物进行定量的方法主要有以下几种:
3、实时荧光定量pcr(rt-pcr):该方法是在pcr反应体系中加入与目的基因特异性结合的荧光探针,利用荧光信号累计实时监测整个pcr进程,最后通过扩增循环数与荧光信号的关系计算出目的基因的初始模板量。该方法特异性好,灵敏度高且可以定量计算出目的基因的量。目前应用于样本中抗原含量的定量,细菌丰度的研究,临床诊断的应用等。但是只能单一的对一种目的基因进行检测,无法确定目标基因的序列,并且只能检测已知目的基因以及可能漏检变异后的目标基因。
4、微滴式数字pcr(ddpcr):该方法是将含有核酸分子的pcr反应体系“分割”成数量众多的、纳升级的反应单元,核酸分子在每个反应单元中随机分布,每个反应单元中包含0、1或者多个目标核酸分子,然后进行pcr扩增反应,pcr扩增结束后,对每个反应单元的荧光信号进行计数统计和分析,通过泊松分布和阳性个数比例计算出目标基因的初始量。该方法具有rt-pcr的优点,并且可以对单核苷酸多态性、稀有突变和拷贝数变异进行分析。目前应用于器官移植物损伤评估,样本中病原微生物分子诊断,运用滴荧光振幅与扩增子大小之间的关系测定未知可扩增dna分子的绝对浓度和长度。但是同样无法对样本内的全部微生物的所有基因进行分析,并且无法测出目的基因的序列。
5、全面检测、无偏好性的宏基因组二代测序(mngs)在传染病诊断方面具有强大的优势,因为不需要特殊探针和靶向引物,从而有助于快速检测病原体。随着成本和时间的持续减少,mngs越来越多地用于临床诊断。宏基因组测序由于ngs中无偏倚性和高通量的特点,能对特定环境样本中的所有微生物进行基因分析,在急难危重感染性疾病的病原检测分析中起到有重要应用。但在正常流程中宏基因组测序无法对所检测的病原微生物进行定量。
6、cn202010383456.6公开了一种基于内参进行宏基因组病原定量检测的方法和装置,其通过在宏基因组检测过程中加入1种特定序列的内参,与样本同时进行提取、建库、上机测序以及信息分析,通过理论模型公式与内参序列的检出情况评估待测样本中人源核酸含量,再通过人源核酸含量评估病原核酸含量,可达到相对定量的效果。
7、鉴于上述方法的局限性以及市场的需要,本发明设计多段dna序列,与所测样本的序列均不同,在不影响样本的情况下参与文库构建步骤,最终通过测序及通过生物信息系统进行统计,绘制一条微生物的投入量与序列数关系的曲线,准确计算出样本中微生物的含量。
技术实现思路
1、基于此,本发明的目的之一在于提供用于病原微生物宏基因组定量检测的内标分子,该内标分子可以用于宏基因组的准确定量检测,且使检测方法简单化。
2、实现上述目的的技术方案包括如下。
3、用于病原微生物宏基因组定量检测的内标分子,其按照以下原理设计得到:包括至少6条核酸序列,每条序列的长度在1000±200bp范围内,
4、每条序列组成为自然界中唯一序列,
5、每条序列的gc含量在35%-70%范围内,
6、每条序列无微卫星序列,
7、每条序列连续相同碱基序列数小于4;
8、且在使用时,所述内标分子包括至少3组,每组含有至少2条内标核酸序列,
9、每组的核酸序列的总量至少存在2倍重量以上的差距。
10、在其中一些实施例中,所述内标分子的序列长度优选为1000±50bp,优选为1000±50bp,gc含量优选为45-55%。
11、在其中一些实施例中,所述内标分子3-10组,优选有4-6组,或者具体为3,4,5,6,7,8,9,10组等。
12、在其中一些实施例中,每组含有2-5条上述核酸序列,更优选为每组设有3条上述核酸序列。
13、在其中一些实施例中,使用时,组与组之间的核酸序列的总量具有依次的5倍以上的梯度递进,包括5-10倍,8-20倍,10-100倍,等等。
14、在其中一些实施例中,组与组之间的核酸序列在使用时的总量具有依次的8-12倍的梯度递进,更优选为依次的10倍的梯度递进。
15、在其中一些实施例中,每组内的每种不同核酸序列的含量(重量)相同或可忽略的微小差距。
16、在其中一些实施例中,所述内标分子包括seq id no.1-seq id no.15序列。
17、优选地,在其中一些实施例中,所述内标分子分成五组,优选地,所述五组中序列组成分别为组1:seq id no.1-seq id no.3;组2:seq id no.4-seq id no.6;组3:seq idno.7-seq id no.9;组4:seq id no.10-seq id no.12;组5:seq id no.13-seq id no.15。
18、在其中一些实施例中,上述组1至组5之间的核酸分子的总量为依次8-12倍的梯度递进,更优选为依次10倍的梯度递进。
19、在其中一些实施例中,5组中所述内标分子的用量分别为,组1为1ng,组2为0.1ng,组3为0.01ng,组4为0.001ng,组5为0.0001ng。在实际应用上,上述用量数据会有正常的误差,但依然在本发明的保护范围中。
20、本发明的另一目的提供一种病原微生物宏基因组定量检测试剂盒。
21、所述病原微生物宏基因组定量检测试剂盒,包括有上述内标分子,或者制备上述内标分子的试剂。
22、在其中一些实施例中,所述制备上述内标分子的试剂包括用以扩增内标分子的扩增引物。
23、在其中一些实施例中,优选为所述内标分子的包括seq id no.1-seq id no.15序列中的至少9条,进一步,其所述扩增引物根据分组,分别选自如seq id no.16-seq idno.45所示。
24、本发明的另一目的是提供一种病原微生物宏基因组定量检测方法。
25、包括以下技术方案。
26、一种病原微生物宏基因组定量检测方法,包括步骤如下:
27、1)获得在待检测样本;
28、2)对待检测样本进行dna提取,得到dna样本,或进行样本的dna提取,得到dna样本,再进行逆转录,得到rna样本;
29、3)对得到的dna样本或rna样本加入上述内标分子(即各组核酸序列的混合液),进行宏基因组文库构建;
30、4)进行测序和对测序结果的生物信息分析,得到病原微生物以及15种内标分子的种水平靶标检出数。
31、5)根据不同梯度的内标分子的靶标检出数的对数对应的投入量的对数绘制标准曲线,得到线性公式。
32、6)把病原微生物的种水平靶标检出数的对数代入线性公式中,得到的结果进行公式换算得到病原微生物的理论拷贝数。
33、本发明的另一目的是提供一种病原微生物宏基因组定量检测的标准曲线的建立方法,包括步骤如下:
34、1)获得核酸样本;
35、2)加入预混好的上述内标分子于核酸样本中,进行宏基因组文库构建;所述内标分子包括至少3组,组与组之间的内标分子的核酸总量具有梯度递进关系;
36、3)通过高通量测序与生信流程得到至少3个梯度的内标分子的检出序列数;对至少3个梯度的内标分子对应的序列检出数与投入量取对数;
37、使用y=ax+b这个线性模型,x等于取对数后的内标序列检出数,y等于取对数后的内标投入量,将至少3个梯度的内标数据拟合成一条平滑的曲线;通过该曲线得到一条反映不同梯度时投入量与序列数关系的线性公式:
38、log10 cis=α·log10 ris+β
39、根据病原微生物与内标的相关性得到病原微生物的投入量与序列数关系的线性公式:
40、log10 cmic=α·log10 rmic+β
41、根据拷贝数计算公式可换算得到:
42、
43、其中cis:内标的投入量;cmic:核酸样本中待测微生物的投入量(含量);ris:内标的序列检出数;rmic:待测微生物的种水平靶标检出数;copymic为核酸样本中待测微生物的拷贝数;lmic:核酸样本的待测微生物的基因组长度(bp);dnac:每ng下dna的质量。
44、在其中一些实施例中,所述内标分子为5组。
45、在其中一些实施例中,组与组之间所述梯度递进关系依次为8-12倍,优选为10倍。
46、在其中一些实施例中,病原微生物为侵犯人体,引起感染甚至传染病的微生物,或称病原体。包括朊毒体、真菌、细菌、螺旋体、支原体、立克次体、衣原体、病毒。其来源于呼吸道,或者消化道等部位。
47、本发明所述检测方法,创造性地设计了多组混合的、浓度呈梯度变化的特定的内标分子,相对qpcr与ddpcr的检测过程,只需在进行宏基因组测序时加入多组混合的、浓度呈梯度变化的特定的内标分子就可进行准确定量,不需要额外进行qpcr与ddpcr的操作,简化实验操作。本发明所述检测方法的所述内标分子配制好后操作流程简单,不受投入量的限制,后续生物信息分析系统配套设置好内标分析流程后可省略人工计算的步骤。无需在宏基因组测序后再对病原微生物进行定量,直接可以通过测序结果后的生物信息分析中得到结果,减少珍贵的临床样本的损耗。
48、根据发明人前期测试结果,本发明病原微生物宏基因组定量检测结果与ddpcr结果无显著差异。可以很好地作为临床样本微生物的定量,无靶标特异性要求,能同时对临床样本的绝大部分微生物进行准确定量。
- 还没有人留言评论。精彩留言会获得点赞!