一种细胞外RNA文库的构建方法及其应用与流程
一种细胞外rna文库的构建方法及其应用
技术领域
1.本发明涉及高通量测序以及文库构建技术领域,尤其是涉及一种细胞外rna文库的构建方法及其应用。
背景技术:
2.细胞外rna(extracellular rna,exrna)最早在血浆和血清中被发现,由于细胞外间隙以及体液中存在rna酶,exrna的发现并没有引起科学界的关注,当时人们普遍认为exrna无法稳定存在。直到2006年和2007年,两项开创性的工作分别证明rna存在于微囊泡(microvesicles)和外泌体(exosomes)中,这些rna可以被分泌到细胞外,作为信号分子影响受体细胞的行为。这个过程既可以发生在邻近的细胞之间,又能进行长距离的调控。这两项工作揭开了exrna研究的序幕,也为探索细胞间的信号转导开辟了新的视角。随后,exrna被发现存在于几乎所有的生物体液(body fluids)中,包括血液、唾液、尿液、母乳、脑脊液、羊水、腹水、胆汁以及胸腔积液中。高通量测序的结果也表明,除了mrna以外,exrna还包含多种非编码的rna类型,如mirna、pirna、tsrna、lncrna、核仁小rna等等。exrna的广谱存在以及多样性提示我们,其很可能参与了重要的生物学过程,调控正常的生长发育以及癌症和疾病的发生,exrna对于人类的健康或有着重大的意义和影响。
3.经典cdna文库构建通常先提取总rna,然后通过去除总rna的rrna,或者是用oligo(dt)捕获poly(a)+rna,加入随机引物逆转录,cdna产物然后转化为合适长度的双链dna,链接到平台特异的测序接头。最广泛使用的技术是使用rna片段、oligo dt随机引物(random hexamer引物),在合成第二链的时候添加dutp;在加接头之后,含尿嘧啶的第二链会在pcr的过程中通过高保真度的dna聚合酶被去除,或者被酶促降解,以达到链特异性。
4.具体来说,现有技术有着以下的局限性:1)需要先提取出总rna(total rna);2)需要的模板量较多,一般总rna都在1μg以上;3)需要多次用不同的酶处理有限的样品,需要经过反复的纯化,会损失很多有用的信息,特别是少量样品中的低丰度信息,很大程度上会影响结果的准确性。
5.鉴于此,特提出本发明。
技术实现要素:
6.本发明的目的在于提供一种专门针对细胞外rna的建库和检测方法及其应用,不需要提取rna,直接裂解生物体液后用带barcode磁珠捕获rna,实现高效、快速获得多种类型的文库,尤其在样本稀缺的情况下,有效实现样本的多种体液中的细胞外rna测序。
7.本发明提供的技术方案如下:
8.一种细胞外rna文库的构建方法,包括以下步骤:
9.(a)裂解体液样本;
10.(b)加入含有标签序列的磁珠捕获所述体液样本中的rna;
11.(c)逆转录;
12.(d)以第一链cdna为模板,合成第二链cdna;
13.(e)获得的第二链cdna经去核糖体rna后进行pcr富集获得全转录组检测文库。
14.在一个实施方案中,使用裂解液裂解体液样本,所述裂解液主要包含以下成分:80~120mm的tris-hcl;体积浓度0.8%~1.2%的lids;450~550mm的licl;以及7.5~15mm的dtt,质量体积分数4-6%的ficoll。
15.在本发明中,质量体积分数%是指溶质质量相对于溶液体积的百分比,通常1%(m/v)一般指固体溶于液体的,1g固体溶于100ml水中。
16.在一个实施方案中,步骤(b)中,含有标签序列的磁珠包括5’通用接头序列-barcode-ttttttttttttttttnnnnn+n-3’、、5’通用接头序列-barcode-ttttttttttttttttvn-3’、5’通用接头序列-barcode-nnnnnn/spc6/、5’通用接头序列-barcode-基因特异性引物中的一种或多种。
17.在一个实施方案中,步骤(c)中,逆转录引物中添加碱基修饰;优选地,所述碱基修饰包括3’lna、3’c6 spacer、3’spacer 18中的一种或多种。
18.在一个实施方案中,步骤(d)中,合成第二链cdna的体系中还包含二链随机引物和dna聚合酶,用带有通用序列的二链随机引物延伸第二链cdna;
19.优选地,所述dna聚合酶为klenow dna聚合酶。
20.在一个实施方案中,所述步骤(e)中,pcr扩增体系中,采用的扩增引物包括引物组:p5 fr引物和p7 rf引物;其中,p5fr引物的序列包括磁珠上的一段通用引物序列;p7 rf的序列包括逆转录引物的通用引物序列。
21.在一个实施方案中,所述体液包括血液、唾液、尿液、母乳、脑脊液、羊水、腹水、胆汁以及胸腔积液中的一种或多种。
22.本发明还提供了所述构建方法获得的细胞外rna检测文库。
23.本发明还提供了一种生物体液中细胞外rna的检测方法,将所述的构建方法获得的检测文库用于高通量测序,获得细胞外rna检测结果。
24.本发明还提供了一种所述的细胞外rna文库的构建方法或所述的细胞外rna检测文库在细胞外rna高通量测序中的应用。
25.有益效果:
26.(1)本发明提供的方法适合捕获多种生物体液(包括但不限于血清、血浆、脑脊液、胚胎培养液、唾液、尿液)中的细胞外rna(exrna)并进行文库构建。
27.(2)本发明是专门针对细胞外rna的检测,不需要提取rna;本发明不需要通过特异性磁珠捕获mrna的3’端的poly a尾巴,可直接裂解生物体液后用带barcode序列的磁珠捕获rna。
28.(3)本发明实现高效、快速获得多种类型的文库,尤其在样本稀缺的情况下,有效实现样本的多种体液中的细胞外rna捕获,能够在基础研究、临床诊断和药物研发等领域进行广泛应用。
附图说明
29.为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的
附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
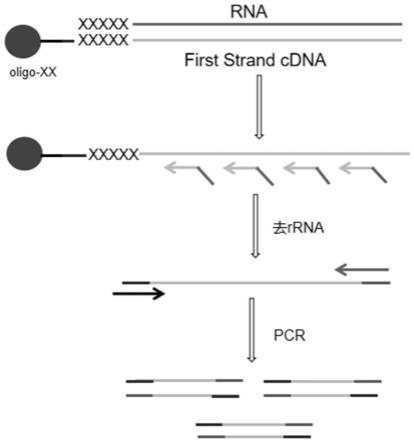
30.图1为本发明实施例提供的细胞外rna检测流程示意图;
31.图2为本发明实施例提供的基因体(genebody)的覆盖谱图;
32.图3为本发明实施例提供的基因表达箱线分布图;
33.图4为本发明实施例提供的精子样本1(jz1)的文库质控峰图;
34.图5为本发明实施例提供的精子样本2(jz2)的文库质控峰图;
35.图6为本发明实施例提供的脑脊液768样本(nao768)的文库质控峰图;
36.图7为本发明实施例提供的血浆768样本(xuejiang768)的文库质控峰图;
37.图8为本发明实施例提供的peitai16样本(胚胎培养液16)的文库质控峰图;
38.图9为本发明实施例提供的peitai16ii样本(胚胎培养液16ii)的文库质控峰图。
具体实施方式
39.下面将结合实施例对本发明的技术方案进行清楚、完整地描述,显然,所描述的实施例是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
40.除非特别说明,本发明采用的试剂、方法和设备为本技术领域常规试剂、方法和设备。除非特别说明,以下实施例所用试剂和材料均为市购。未注明具体条件的实验方法,通常按照常规条件,或制造厂商所建议条件实施。
41.实施例
42.本发明提供了一种生物体液中的细胞外rna检测方法,图1示出了本发明细胞外rna检测的流程示意图。
43.本发明的方法包括以下步骤:
44.1、裂解样本
45.(1)配制裂解液组分
[0046][0047][0048]
(2)将裂解液加入到体液样本中,催打混合均匀后,在金属浴中按照以下程序反应:
[0049]
温度时间25℃10min
[0050]
2、捕获样本的rna
[0051]
加入带标签序列磁珠,吹打混匀后25℃孵育15分钟,37℃孵育15分钟。
[0052]
带标签序列磁珠的标签序列为:
[0053][0054]
备注:+n表示最后一随机碱基带有lna修饰;/spc6/表示3`最后一随机碱基带c6 spacer修饰。
[0055]
3、逆转录
[0056]
用6
×
ssc漂洗两次后,加入以下逆转录(rt)反应试剂,按照下表配反应体系:
[0057][0058][0059]
轻弹管壁混匀,短暂离心收集37℃,60分钟。
[0060]
4、第二链cdna的合成
[0061]
以一链cdna模板,用带有通用序列的随机引物延伸二链cdna,随机引物的序列为:tctttccctacacgacgctcttccgatctnnnnn+n(seq id no.4),+n表示最后一随机碱基带有lna修饰。
[0062]
(1)按照下表配制二链cdna反应体系:
[0063]
组分体积neb buffer 22μl二链随机引物1μldntp1μlklenow1μl
d-(+)-trehalose(d-(+)-海藻糖)6ull-carnitine(左旋肉碱)3ulh2o至20μl
[0064]
配置完成后,轻弹管壁混匀,短暂离心收集样本。
[0065]
按照以下程序反应:
[0066]
温度时间25℃10min37℃15min45℃10min55℃10min4℃hold
[0067]
5、去除核糖体rna
[0068]
向二链cdna产物中加入1μl去rrna探针,吹打混匀后,按照以下程序反应:
[0069]
温度时间75℃2min70℃2min65℃2min60℃2min55℃2min37℃5min25℃5min
[0070]
6、pcr扩增
[0071]
获得二链cdna经去核糖体rna后,进行pcr富集。
[0072]
按照下表配置反应体系:
[0073]
组分体积cdna合成产物11.5μl2
×
hifi pcr mix12.5μlp5 forword primer0.5μlp7 reverse primer0.5μltotal25μl
[0074]
其中,p5 forword primer(p5fp引物):
[0075]
aatgatacggcgaccaccgagatctacactctttccctacacgacgctcttccgatct(seq id no.5);
[0076]
p7 reverse primer(p7rp引物):
[0077]
caagcagaagacggcatacgagat-index-gtgactggagttcagacgtgtgctcttccgatct(seq id no.6)。
[0078]
配置完成后,震荡混匀,短暂离心收集样本。
[0079]
按照以下程序反应:
[0080][0081][0082]
pcr反应产物用1
×
磁珠纯化,23μl水洗脱。
[0083]
7、qsep100全自动核酸蛋白分析系统检测文库主峰大小
[0084]
qsep100全自动核酸蛋白分析系统检测文库主峰在350-400bp左右,符合理论大小,如图4-图9所示。
[0085]
8.实验结果分析:
[0086]
1.基因组比对
[0087]
测序获得的序列数据经过质量控制以后,采用hisat2软件[1]与相应物种的基因组进行比对,基因组比对率是衡量数据质量的一个标准。本方法基因组比对率50-90%,数据为良好。
[0088]
表1基因组比对数据统计
[0089][0090]
all reads:总参与比对序列,即质量控制以后的测序序列;
[0091]
mapped reads:即总参与比对序列中能够比对到基因组上的测序序列;
[0092]
mapping rate:基因组比对率,即测序序列比对到基因组占总测序过滤后序列的比值;
[0093]
unique mapping:总参与比对序列中能够在基因组上只有唯一比对位置的序列;
[0094]
unique mapping rate:唯一位置比对率,即唯一位置比对序列占从测序过滤后序列的比值。
[0095]
2.质量控制
[0096]
质量控制对于保证rna-seq高质量且适合随后分析是至关重要的,我们使用rseqc评估rna-seq记过质量。将所有转录本缩放到100nt,并计算每个核苷酸覆盖的reads数,最后计算出一个沿gene body的覆盖图谱,从结果图2中可以看到gene body的覆盖从5'-3'比较均一。
[0097]
3.表达量计算
[0098]
基因表达(gene expression)是进行转录组测序研究的基础。
[0099]
根据基因组比对结果文件,利用htseq-count
[2]
计算基因的表达量,fpkm(fragments per kilo base million reads)用来进行标准化,结果分布见图3。
[0100]
根据基因组比对结果文件,利用htseq-count
[2]
计算基因的表达量,fpkm(fragments per kilo base million reads)用来进行标准化,所有基因的表达量fpkm结果分布图如图3所示,fpkm分布的中位数位于1以上(对应图中对数转换的坐标值0),fpkm大于0.01一般认为基因有表达,表明该方法可以检测到绝大部分基因。
[0101]
参考文献:
[0102]
[1]kim d,langmead b,et al.hisat:a fast spliced aligner with low memory requirements.nature methods,2015,12(4):357-360.
[0103]
[2]anders s,pyl p t,huber w.htseq-a python framework to work with high-throughput sequencing data.bioinformatics,2015,31(2):166-9.
[0104]
综上所述,本方法特别适用于细胞外rna的情况,能获得良好的数据,有效实现各种体液样本、外泌体或珍贵临床样本的转录组测序在基础研究、临床诊断和药物研发等邻域的广泛应用。
[0105]
最后应说明的是:以上各实施例仅用以说明本发明的技术方案,而非对其限制;尽管参照前述各实施例对本发明进行了详细的说明,本领域的普通技术人员应当理解:其依然可以对前述各实施例所记载的技术方案进行修改,或者对其中部分或者全部技术特征进行等同替换;而这些修改或者替换,并不使相应技术方案的本质脱离本发明各实施例技术方案的范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1