一种金刚烷三苯胺的合成工艺的制作方法
1.本发明属于化工合成领域,特别涉及一种金刚烷三苯胺的合成工艺。
背景技术:
2.电致发光(electroluminescence),又可称电场发光,简称el,是通过加在两电极的电压产生电场,被电场激发的电子碰击发光中心,而引致电子在能级间的跃迁、变化、复合导致发光的一种物理现象。近年来,有机电致发光器件(oled,organicelectroluminescent device)作为新一代显示技术逐渐进入人们的视野。oled是一种由多层有机薄膜结构形成的电致发光器件,其中的有机薄膜是利用蒸镀或旋涂工艺在基板上形成的有机发光材料的膜。与传统的显示技术相比,其在电压特性、发光亮度、发光效率、色质、响应速度以及观赏视角等方面极具优势,并且成本低,因此拥有广阔的市场前景。
3.金刚烷三苯胺是oled领域类重要的中间体,国内外客户所使用的电子传输材料,空穴阻挡材料等一系列具体有机分子结构均有其结构部分,特别是近几年来,国内厂商寻求国产化过程中,有更多包含其结构的不同种类的材料迫切需要该中间体的工业化生产。
4.目前,对于该化合物的合成方法未有合成方案报道过,仅有两篇韩国专利cn 111146349 a和cn 107148408 b属于同一家韩国公司对其结构的应用做了报道,主要是以此化合物或者该化合物中的中间体为原料,制备一系列的光电材料,都表现出优异的性能。然而该化合物特殊的分子结构导致对于它的研究和报道确少之又少。
5.因此,有必要设计一条能够符合工业化生产,满足经济适用性和符合市场需求的环境友好的金刚烷三苯胺的合成工艺。
技术实现要素:
6.本发明提供了一种金刚烷三苯胺的合成工艺,其目的是为了解决现有技术中金刚烷三苯胺的合成工艺缺少,不能工业化生产,不能满足oled市场日益增加的需求的问题。
7.为了达到上述目的,本发明的实施例提供了一种金刚烷三苯胺的合成工艺,所述合成工艺包括如下步骤:
8.1)取式1金刚烷醇、苯酚加入二氯乙烷溶剂中,再滴加浓硫酸反应得到式2的金刚烷苯酚
[0009][0010]
2)将所述金刚烷苯酚、三乙胺加入二氯乙烷溶剂中反应,反应完毕再滴加三氟甲磺酸酐反应得到式3的金刚烷苯基三氟甲磺酸酯
氯苯胺与催化剂pd(dppf)cl2摩尔比为1:0.002。
[0028]
进一步的,所述金刚烷苯基三氟甲磺酸酯与4-氨基-3-苯基苯硼酯摩尔比为1:1.1-1.5,所述金刚烷苯基三氟甲磺酸酯与催化剂pd(pph3)2cl2摩尔比为1:0.0005-0.02。
[0029]
更进一步的,所述金刚烷苯基三氟甲磺酸酯与4-氨基-3-苯基苯硼酯摩尔比为1:1.3,所述金刚烷苯基三氟甲磺酸酯与催化剂pd(pph3)2cl2摩尔比为1:0.005。
[0030]
进一步的,所述金刚烷三苯胺的液相纯度达99.9%以上。
[0031]
本发明的上述方案有如下的有益效果:
[0032]
1)本发明的上述方案所述的合成工艺具有经济适用性、符合市场需求,环境友好且适合工业化生产。
[0033]
2)本发明的方法原料易得、操作简单,收率较高,已实现百公斤级生产,且得到产品的高纯度、品质达99.9%以上。
附图说明
[0034]
图1是本发明的实施例1的金刚烷苯酚的1h nmr;
[0035]
图2是本发明的实施例1的金刚烷苯基三氟甲磺酸酯的1h nmr;
[0036]
图3是本发明的实施例1的2-苯基-4-氯苯胺的1h nmr;
[0037]
图4是本发明的实施例1的4-氨基-3-苯基苯硼酯的1h nmr;
[0038]
图5是本发明的实施例1的金刚烷三苯胺的1h nmr;
[0039]
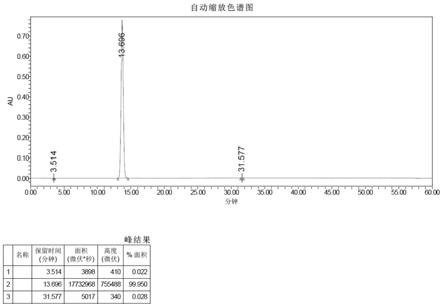
图6是本发明的实施例1的金刚烷三苯胺的液相谱图。
具体实施方式
[0040]
为使本发明要解决的技术问题、技术方案和优点更加清楚,下面将结合附图及具体实施例进行详细描述。
[0041]
本发明针对现有的问题,提供了一种金刚烷三苯胺的合成工艺。
[0042]
本发明实施例中金刚烷三苯胺的合成路线如下:
[0043][0044]
实施例1
[0045]
一种金刚烷三苯胺的合成方法,步骤如下:
[0046]
1)在1l的三口烧瓶中加入金刚烷醇150g,1.2-二氯乙烷500ml,在室温下搅拌,加入苯酚97.83g,并在冰水浴下冷却到0℃,再向反应体系中缓慢滴加浓硫酸116ml,维持体系温度在0℃左右,滴加完毕后,在0℃下继续搅拌30min,将反应温度升至室温,继续反应18h。通过液相监测反应完全后停止反应。静置分层,分去浓硫酸层,用碱水溶液调节ph至中性或弱碱性,静置分液,有机层浓缩至有大量固体析出,加入大量热水打浆30min后,热抽滤得到
金刚烷苯酚,烘干得到白色固体195g,收率86.67%。ms(ei):m/z 228.15,1h nmr如图1所述;
[0047]
2)在1l的三口烧瓶中加入金刚烷苯酚195g,1.2-二氯乙烷500ml和三乙胺154ml,在室温下搅拌溶解呈澄清透明状态,并在冰水浴下降温至0℃,再向反应体系中缓慢滴加三氟甲磺酸酐172ml,维持体系温度在0℃左右,滴加完毕后,移至室温反应30min。通过tlc点板监测反应完全后,将反应液倒入水中,静置分液,水洗两次分液,浓缩有机层,可得到金刚烷苯基三氟甲磺酸酯,无色油状液体267g,收率86.75%。ms(ei):m/z 360.10,1h nmr如图2所述;
[0048]
3)在3l的三口烧瓶中加入2-溴-4-氯苯胺300g,甲苯1000ml,乙醇200ml,碳酸钾600g和水200ml,加入苯硼酸212.6g和pd(pph3)
4 3.36g,氮气保护,升温至95℃下反应。通过tlc点板监测反应完全后,先分去水相,热水洗两次,分液浓缩有机相,加入石油醚结晶,鼓风烘干得到灰色晶体235g,收率79.41%,ms(ei):m/z 203.01,1h nmr如图3所述;
[0049]
4)在3l的单口烧瓶中加入2-苯基-4-氯苯胺235g,联硼酸频那醇酯351.61g,乙酸钾339g,pd(dppf)cl
2 1.68g,1,4-二氧六环1.3l,氮气保护,升温至95℃回流反应。通过tlc点板监测反应完全。反应液抽滤后旋干有机相,用二氯乙烷溶解后水洗两次,浓缩干有机相加入石油醚打浆至大量产物析出,抽滤得到灰色粉末状固体290g,收率85.14%,ms(ei):m/z 295.17,1h nmr如图4所述;
[0050]
5)在3l的单口烧瓶中加入金刚烷苯基三氟甲磺酸酯267g,4-氨基-3-苯基苯硼酯285g,pd(pph3)2cl
2 2.6g,加入307.7g碳酸钾和300ml水,并加入1.5l甲苯,升温至95℃回流反应,通过tlc点板监测反应完全,静置分去水相,热水洗涤两次后,有机相加入活性炭脱色后,抽滤浓缩甲苯,加入乙醇结晶降温至20℃抽滤得到固体,重复甲苯乙醇结晶三次后得到粉白色固体,烘干称重为210g,收率74.68%,ms(ei):m/z 379.10,1h nmr如图5所述,液相谱图如图6所示。
[0051]
实施例2
[0052]
一种金刚烷三苯胺的合成方法,步骤如下:
[0053]
1)在1000l的反应釜中加入1.2-二氯乙烷500l,搅拌下加入融化的苯酚97.83kg,加入完毕后通入冰盐水降温至0℃左右,加入固体金刚烷醇150kg,并在冰盐浴下冷却到零℃,再向反应体系中缓慢加入浓硫酸115.5l,维持体系温度在0℃左右。滴加完毕后继续通冰盐水保温30min,后通循环水使其恢复至25℃反应,通过液相监测反应完全,反应完全后停止反应,静置1h分层,分去浓硫酸层,用液碱调节ph至中性或者弱碱性,静置分液,用水500l洗两次。将有机层蒸除300l,大量固体析出加入热水400l,保温80℃1h,热抽滤得到黄白色固体,烘干减重得到200kg粗品,收率88.90%;
[0054]
2)在1000l的反应釜中加入1.2-二氯乙烷400l,金刚烷苯酚200kg和三乙胺150.36l,在室温下搅拌溶解呈澄清透明状态,通冰盐水降温至0℃,再向反应釜中缓慢滴加三氟甲磺酸酐177l,维持体系温度在0℃左右,滴加完毕后,关闭冰盐水,升至室温反应2h。液相监测反应完全后,在反应釜中加入300l水洗涤三次,蒸汽蒸有机层浓缩干可得到金刚烷苯基三氟甲磺酸酯,淡红色油状液体285kg,收率90.28%;
[0055]
3)在3000l的反应釜中加入2-溴-4-氯苯胺300kg,甲苯1000l,乙醇200l,碳酸钾600kg和水200l,加入苯硼酸212.6kg和pd(pph3)43.36kg,持续通氮气,保持95℃下反应。液
相点板监测反应完全后,静置先分去水相,用80℃热水500l洗两次,浓缩有机相,加入石油醚结晶,抽滤离心,鼓风烘干得到灰色晶体245kg,收率82.79%;
[0056]
4)在3000l的反应釜中加入1,4-二氧六环1000l,2-苯基-4-氯苯胺245kg,联硼酸频那醇酯367kg,乙酸钾354kg,,氮气鼓泡半小时后加入pd(dppf)cl21.76kg,升温至95℃回流反应。液相监测反应完全。趁热放料抽滤,后将有机相蒸干,用二氯乙烷溶解后水洗两次,蒸汽蒸干有机相后加入石油醚打浆至大量产物析出,抽滤得到产物310kg,收率约为87.30%;
[0057]
5)在3000l的反应釜中加入金刚烷苯基三氟甲磺酸酯285kg,加入327.88kg碳酸钾和560l水,并加入1000l甲苯,加入硼酯304kg和pd(pph3)2cl22.78kg,升温至95℃反应,保持95℃回流反应,液相监测反应完全,静置分去水相,热水洗涤两次后,有机相加入5kg活性炭脱色后,抽滤浓缩甲苯,加入乙醇结晶降温至20℃抽滤得到固体,重复甲苯乙醇结晶三次后得到粉白色固体,烘干称重为245kg,收率81.6%,测试液相纯度为99.95%。
[0058]
对比例1
[0059]
将实施例1步骤5)中的催化剂pd(pph3)2cl2替换成pd(pph3)4,其他步骤均相同,具体如下:
[0060]
在3l的单口烧瓶中加入金刚烷苯基三氟甲磺酸酯267g,4-氨基-3-苯基苯硼酯285g,pd(pph3)
4 4.2g,加入307.7g碳酸钾和300ml水,并加入1.5l甲苯,升温至95℃回流反应,同样时间下通过tlc点板监测反应原料剩余较多,静置分去水相,热水洗涤两次后,硅胶负载柱层析分离,得到产品称重为55g,收率19.56%。
[0061]
对比例2
[0062]
将实施例1步骤5)中的碱碳酸钾替换成磷酸钾,其他步骤均相同,具体如下:
[0063]
在3l的单口烧瓶中加入金刚烷苯基三氟甲磺酸酯267g,4-氨基-3-苯基苯硼酯285g,pd(pph3)2cl
2 2.6g,加入471.2g磷酸钾和300ml水,并加入1.5l甲苯,升温至95℃回流反应,同样时间下通过tlc点板监测反应原料剩余较多,静置分去水相,热水洗涤两次后,硅胶负载柱层析分离,得到产品称重为165g,收率58.68%。
[0064]
对比例3
[0065]
将实施例1步骤5)中的溶剂甲苯替换成1,4-二氧六环,其他步骤均相同,具体如下:
[0066]
在3l的单口烧瓶中加入金刚烷苯基三氟甲磺酸酯267g,4-氨基-3-苯基苯硼酯285g,pd(pph3)2cl
2 2.6g,加入307.7g碳酸钾和300ml水,并加入1.5l1,4-二氧六环,升温至95℃回流反应,同样时间下通过tlc点板监测反应原料剩余较多,静置分去水相,热水洗涤两次后,硅胶负载柱层析分离,得到产品称重为190g,收率67.57%。
[0067]
对比例4
[0068]
将实施例1步骤5)中的金刚烷苯基三氟甲磺酸酯与4-氨基-3-苯基苯硼酯摩尔比由1:1.3改为1:1,其他步骤均相同,具体如下:
[0069]
在3l的单口烧瓶中加入金刚烷苯基三氟甲磺酸酯267g,4-氨基-3-苯基苯硼酯218.69g,pd(pph3)2cl
2 2.6g,加入307.7g碳酸钾和300ml水,并加入1.5l甲苯,升温至95℃回流反应,同样时间下通过tlc点板监测反应原料剩余较多,静置分去水相,热水洗涤两次后,硅胶负载柱层析分离,得到产品称重为150g,收率53.34%。
[0070]
对比例5
[0071]
将实施例1步骤5)中的金刚烷苯基三氟甲磺酸酯与催化剂pd(pph3)2cl2摩尔比由1:0.005改为1:0.0003,其他步骤相同,具体如下:
[0072]
在3l的单口烧瓶中加入金刚烷苯基三氟甲磺酸酯267g,4-氨基-3-苯基苯硼酯285g,pd(pph3)2cl
2 0.16g,加入307.7g碳酸钾和300ml水,并加入1.5l甲苯,升温至95℃回流反应,同样时间下通过tlc点板监测反应原料剩余较多,静置分去水相,热水洗涤两次后,硅胶负载柱层析分离,得到产品称重为70g,收率24.89%。
[0073]
表1实施例1与各对比例的反应条件和收率表
[0074]
合成方案反应条件收率%实施例11.3倍4-氨基-3-苯基苯硼酯
ꢀꢀ
0.005倍pd(pph3)2cl2ꢀꢀꢀ
碳酸钾
ꢀꢀꢀꢀ
甲苯74.68对比例11.3倍4-氨基-3-苯基苯硼酯
ꢀꢀ
0.005倍pd(pph3)4ꢀꢀꢀꢀꢀ
碳酸钾
ꢀꢀꢀꢀ
甲苯19.56对比例21.3倍4-氨基-3-苯基苯硼酯
ꢀꢀ
0.005倍pd(pph3)2cl2ꢀꢀꢀ
磷酸钾
ꢀꢀꢀꢀ
甲苯58.68对比例31.3倍4-氨基-3-苯基苯硼酯
ꢀꢀ
0.005倍pd(pph3)2cl2ꢀꢀꢀ
碳酸钾
ꢀꢀꢀꢀ
1,4-二氧六环67.57对比例41倍4-氨基-3-苯基苯硼酯
ꢀꢀ
0.005倍pd(pph3)2cl2ꢀꢀꢀ
碳酸钾
ꢀꢀꢀꢀ
甲苯53.34对比例51.3倍4-氨基-3-苯基苯硼酯
ꢀꢀ
0.0003倍pd(pph3)2cl2ꢀꢀꢀ
碳酸钾
ꢀꢀꢀ
甲苯24.89
[0075]
从表1中可以看出,对比例1比较于实施例1,改变催化剂,其收率仅为19.56%;对比例2比较于实施例1,改变碱,其收率降低16%;对比例3比较于实施例1,改变溶剂,其收率降低7.11%;对比例4相比于实施例1,降低了4-氨基-3-苯基苯硼酯的用量,其收率降低21.34%;对比例5相比于实施例1,降低了催化剂的用量,其收率仅为24.89%;
[0076]
综上所述,通过上述设置不同条件进行反应,包括更换催化剂,改变碱,更换溶剂,改变物料的比例用量,所得到的中间产物收率效果来看,按本文中优选方式合成方案是最佳的,同时本文还按照该方案进行工业化生产,也得到了较高的收率,生产成本低廉,操作简单且得到产品品质极高。
[0077]
以上所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明所述原理的前提下,还可以作出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1