自由基聚合引发剂、组合物、固化物及固化物的制造方法与流程
1.本发明涉及感度及保存稳定性优异的自由基聚合引发剂。
背景技术:
2.作为感光性组合物,已知有在具有烯键式不饱和键的聚合性化合物中加有光聚合引发剂的光固化性组合物。这样的光固化性组合物由于能够通过照射能量射线(光)而固化,因此被用于光固化性油墨、感光性印刷版、各种光致抗蚀剂等。
3.作为上述感光性组合物中使用的光聚合引发剂,在下述专利文献1~7中提出了使用肟酯化合物。
4.现有技术文献
5.专利文献
6.专利文献1:美国专利申请公开第2004/170924号说明书
7.专利文献2:美国专利申请公开第2007/270522号说明书
8.专利文献3:美国专利申请公开第2009/292039号说明书
9.专利文献4:美国专利申请公开第2011/129778号说明书
10.专利文献5:ep2407456a1
11.专利文献6:ep2433927a1
12.专利文献7:日本特表2013-543875号公报
技术实现要素:
13.然而,在使用专利文献1~7中记载的肟酯化合物作为自由基聚合引发剂的情况下,存在有时感度不稳定这样的不良情况。
14.本发明是鉴于上述问题而进行的,主要目的是提供感度的稳定性优异的自由基聚合引发剂。
15.本发明人们为了解决上述课题而进行了深入研究,结果发现:包含肟酯化合物和规定量的酸成分的自由基聚合引发剂成为感度的稳定性优异的物质,从而完成本发明。
16.即,本发明为一种自由基聚合引发剂,其是包含下述通式(a)所表示的化合物和酸成分的自由基聚合引发剂,上述酸成分的含量在上述通式(a)所表示的化合物及上述酸成分的合计中为1ppm以上且400ppm以下。
17.[化学式1]
[0018][0019]
(式中,a表示碳原子数为6~20的芳香族环基,
[0020]r31
表示下述通式(1)所表示的基团,
[0021]r32
表示除上述通式(1)以外的自由基产生基、通过除上述通式(1)以外的自由基产生基将基团中的氢原子取代而得到的碳原子数为1~20的无取代或具有取代基的脂肪族烃基、通过除上述通式(1)以外的自由基产生基将基团中的氢原子取代而得到的碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、通过除上述通式(1)以外的自由基产生基将基团中的氢原子取代而得到的碳原子数为2~20的无取代或具有取代基的含杂环基团、或上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自下述组i中的二价的基团取代而得到的基团,
[0022]r33
表示卤素原子、硝基、氰基、-or
34
、-cor
34
、-ocor
34
、-coor
34
、-sr
34
、-sor
34
、-so2r
34
、-nr
35r36
、-nr
35
cor
36
、-conr
35r36
、碳原子数为1~20的无取代或具有取代基的脂肪族烃基、碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、碳原子数为2~20的无取代或具有取代基的含杂环基团、或上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自下述组i中的二价的基团取代而得到的基团,
[0023]r34
、r
35
及r
36
分别独立地表示氢原子、碳原子数为1~20的无取代或具有取代基的脂肪族烃基、碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、或碳原子数为2~20的无取代或具有取代基的含杂环基团、或上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自下述组i中的二价的基团取代而得到的基团,在r
34
、r
35
或r
36
存在多个的情况下,它们可以相同,也可以不同,
[0024]
将上述具有取代基的脂肪族烃基、上述具有取代基的含芳香族烃环的基团及上述具有取代基的含杂环基团中的1个以上的氢原子取代的取代基为卤素原子、氰基、硝基、羟基、硫醇基或-cooh,
[0025]
a表示1~20的整数,
[0026]
b表示0~20的整数,
[0027]
c表示0~20的整数,
[0028]
a、b及c的合计为20以下。)
[0029]
[化学式2]
[0030][0031]
(式中,r1表示碳原子数为1~20的无取代或具有取代基的脂肪族烃基、碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、或碳原子数为2~20的无取代或具有取代基的含杂环基团、或上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自下述组i中的二价的基团取代而得到的基团,
[0032]
r2表示氢原子、卤素原子、硝基、氰基、碳原子数为1~20的无取代或具有取代基的脂肪族烃基、碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、或碳原子数为2~20的无取代或具有取代基的含杂环基团、或上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自下述组i中的二价的基团取代而得到的
基团,
[0033]
将上述具有取代基的脂肪族烃基、上述具有取代基的含芳香族烃环的基团及上述具有取代基的含杂环基团中的1个以上的氢原子取代的取代基为卤素原子、氰基、硝基、羟基、硫醇基或-cooh,
[0034]
n表示0或1,
[0035]
*表示键合部位。)
[0036]
组i:-o-、-coo-、-oco-、-co-、-co-co-、-co-co-o-、-cs-、-s-、-so-、-so
2-、-nr
40-、-nr
40-co-、-co-nr
40-、-nr
40-coo-、-oco-nr
40-或-sir
40r41-。
[0037]r40
及r
41
分别独立地表示氢原子或碳原子数为1~20的无取代的脂肪族烃基,在r
40
或r
41
存在多个的情况下,它们可以相同,也可以不同。
[0038]
本发明的自由基聚合引发剂通过包含上述结构的化合物和规定量的酸成分,成为感度的稳定性优异的物质。
[0039]
在本发明中,上述酸成分优选为有机酸。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0040]
在本发明中,上述通式(a)所表示的化合物优选为下述式(a1)所表示的化合物。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0041]
[化学式3]
[0042][0043]
(式中,r
11
、r
12
、r
13
、r
14
、r
15
、r
16
及r
17
分别独立地为氢原子、上述通式(a)中的r
31
所表示的基团、上述通式(a)中的r
32
所表示的基团或上述通式(a)中的r
33
所表示的基团,r
11
与r
12
、r
12
与r
13
、r
14
与r
15
、r
15
与r
16
或r
16
与r
17
也可以互相键合而形成环,
[0044]r11
、r
12
、r
13
、r
14
、r
15
、r
16
及r
17
中的至少1个为上述通式(a)中的r
31
所表示的基团。)
[0045]
在上述通式(a1)中,r
11
优选为上述通式(a)中的r
31
。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0046]
在上述通式(a1)中,r
13
及r
16
中的1个以上优选为上述通式(a)中的r
33
。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0047]
在上述通式(a1)中,r
13
为上述通式(a)中的r
33
,用于的r
13
的r
33
优选为碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团或上述含芳香族烃环的基团中的1个以上的亚甲基被选自上述组i中的二价的基团取代而得到的基团。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0048]
在本发明中,上述通式(a)所表示的化合物的含量在上述自由基聚合引发剂100质量份中优选为90质量份以上。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0049]
本发明为一种组合物,其包含上述自由基聚合引发剂和自由基聚合性化合物。
[0050]
本发明的组合物通过包含上述自由基聚合引发剂,成为感度的稳定性优异的组合物。
[0051]
本发明为上述组合物的固化物。
[0052]
本发明的固化物由于使用上述组合物,因此变得容易调整固化物的耐久性等。
[0053]
本发明为一种固化物的制造方法,其具有将上述组合物中的自由基聚合性化合物彼此聚合的聚合工序。
[0054]
根据本发明的固化物的制造方法,由于在聚合工序中使用上述组合物,因此能够容易地得到所期望的耐久性等的固化物。
具体实施方式
[0055]
本发明涉及自由基聚合引发剂、组合物、固化物及固化物的制造方法。
[0056]
以下,对本发明的自由基聚合引发剂、组合物、固化物及固化物的制造方法进行详细说明。
[0057]
a.自由基聚合引发剂
[0058]
首先,对本发明的自由基聚合引发剂进行说明。
[0059]
本发明的自由基聚合引发剂的特征在于,其是包含下述通式(a)所表示的化合物(化合物a)和酸成分的自由基聚合引发剂,上述酸成分的含量在上述通式(a)所表示的化合物及上述酸成分的合计中为1ppm以上且400ppm以下。
[0060]
[化学式4]
[0061][0062]
(式中,a表示碳原子数为6~20的芳香族环基,
[0063]r31
表示下述通式(1)所表示的基团,
[0064]r32
表示除上述通式(1)以外的自由基产生基、通过除上述通式(1)以外的自由基产生基将基团中的氢原子取代而得到的碳原子数为1~20的无取代或具有取代基的脂肪族烃基、通过除上述通式(1)以外的自由基产生基将基团中的氢原子取代而得到的碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、通过除上述通式(1)以外的自由基产生基将基团中的氢原子取代而得到的碳原子数为2~20的无取代或具有取代基的含杂环基团、或上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自下述组i中的二价的基团取代而得到的基团,
[0065]r33
表示卤素原子、硝基、氰基、-or
34
、-cor
34
、-ocor
34
、-coor
34
、-sr
34
、-sor
34
、-so2r
34
、-nr
35r36
、-nr
35
cor
36
、-conr
35r36
、碳原子数为1~20的无取代或具有取代基的脂肪族烃基、碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、碳原子数为2~20的无取代或具有取代基的含杂环基团、或上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自下述组i中的二价的基团取代而得到的基团,
[0066]r34
、r
35
及r
36
分别独立地表示氢原子、碳原子数为1~20的无取代或具有取代基的
脂肪族烃基、碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、或碳原子数为2~20的无取代或具有取代基的含杂环基团、或上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自下述组i中的二价的基团取代而得到的基团,在r
34
、r
35
或r
36
存在多个的情况下,它们可以相同,也可以不同,
[0067]
将上述具有取代基的脂肪族烃基、上述具有取代基的含芳香族烃环的基团及上述具有取代基的含杂环基团中的1个以上的氢原子取代的取代基为卤素原子、氰基、硝基、羟基、硫醇基或-cooh,
[0068]
a表示1~20的整数,
[0069]
b表示0~20的整数,
[0070]
c表示0~20的整数,
[0071]
a、b及c的合计为20以下。)
[0072]
[化学式5]
[0073][0074]
(式中,r1表示碳原子数为1~20的无取代或具有取代基的脂肪族烃基、碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、或碳原子数为2~20的无取代或具有取代基的含杂环基团、或上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自下述组i中的二价的基团取代而得到的基团,
[0075]
r2表示氢原子、卤素原子、硝基、氰基、碳原子数为1~20的无取代或具有取代基的脂肪族烃基、碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、或碳原子数为2~20的无取代或具有取代基的含杂环基团、或上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自下述组i中的二价的基团取代而得到的基团,
[0076]
将上述具有取代基的脂肪族烃基、上述具有取代基的含芳香族烃环的基团及上述具有取代基的含杂环基团中的1个以上的氢原子取代的取代基为卤素原子、氰基、硝基、羟基、硫醇基或-cooh,
[0077]
n表示0或1,
[0078]
*表示键合部位。)
[0079]
组i:-o-、-coo-、-oco-、-co-、-co-co-、-co-co-o-、-cs-、-s-、-so-、-so
2-、-nr
’‑
、-nr
’‑
co-、-co-nr
’‑
、-nr
’‑
coo-、-oco-nr
’‑
或-sir’r
”‑
。
[0080]
r’及r”分别独立地表示氢原子或碳原子数为1~20的无取代的脂肪族烃基,在r’或r”存在多个的情况下,它们可以相同,也可以不同。
[0081]
这里,关于本发明的自由基聚合引发剂通过包含上述化合物a、以及规定量的酸成分而发挥上述的效果的理由,如以下那样推测。
[0082]
上述自由基聚合引发剂中,通过与化合物a一起并用的酸成分的含量为规定量,能够抑制在保管时上述通式(1)所表示的基团通过酸成分而分解。其结果是,上述自由基聚合
引发剂变得能够在所期望的时机产生规定量的自由基,成为感度的稳定性优异的物质。
[0083]
此外,上述自由基聚合引发剂通过包含上述化合物a、以及规定的量的酸成分,从而与固化性组合物的各成分的溶解速度提高,变得容易制备固化性组合物。
[0084]
本发明的自由基聚合引发剂包含化合物a和酸成分。
[0085]
以下,对本发明的自由基聚合引发剂的各成分进行详细说明。
[0086]
1.化合物a
[0087]
上述化合物a具有上述通式(1)所表示的基团即肟酯基,具体而言,r
31
为上述通式(1)所表示的基团。
[0088]
作为上述通式(a)及上述通式(1)中的卤素原子,可列举出氟原子、氯原子、溴原子、碘原子等。
[0089]
上述通式(a)及上述通式(1)中的碳原子数为1~20的脂肪族烃基为不含芳香族烃环及杂环的烃基,也可以具有取代基。所谓具有取代基的脂肪族烃基是脂肪族烃基中的1个以上的氢原子被取代基取代而得到的结构的基团。
[0090]
作为无取代的脂肪族烃基,例如可列举出碳原子数为1~20的烷基、碳原子数为2~20的烯基、碳原子数为3~20的环烷基、碳原子数为4~20的环烷基烷基。此外,作为具有取代基的上述脂肪族烃基,可列举出上述无取代的脂肪族烃基中的1个以上的氢原子被取代基取代而得到的基团等,作为该取代基,可列举出卤素原子、氰基、硝基、羟基、硫醇基或-cooh等。
[0091]
上述碳原子数为1~20的烷基可以为直链状,也可以为支链状。作为直链的烷基,可列举出甲基、乙基、丙基、丁基、异戊基、叔戊基、己基、庚基及辛基。作为支链的烷基,可列举出异丙基、仲丁基、叔丁基、异丁基、异戊基、叔戊基、2-己基、3-己基、2-庚基、3-庚基、异庚基、叔庚基、异辛基、叔辛基、2-乙基己基、壬基、异壬基、癸基、十二烷基、十三烷基、十四烷基、十五烷基、十六烷基、十七烷基、十八烷基等。
[0092]
上述碳原子数为2~20的烯基可以为直链状,也可以为支链状。此外,可以是在末端具有不饱和键的末端烯基,也可以是在内部具有不饱和键的内部烯基。作为末端烯基,例如可列举出乙烯基、烯丙基、2-甲基-2-丙烯基、3-丁烯基、4-戊烯基及5-己烯基等。作为内部烯基,例如可列举出2-丁烯基、3-戊烯基、2-己烯基、3-己烯基、2-庚烯基、3-庚烯基、4-庚烯基、3-辛烯基、3-壬烯基、4-癸烯基、3-十一碳烯基、4-十二碳烯基及4,8,12-十四碳三烯基烯丙基等。
[0093]
作为上述碳原子数为3~20的环烷基,可列举出碳原子数为3~20的饱和单环式烷基、碳原子数为3~20的饱和多环式烷基、及这些基团的环中的1个以上的氢原子被烷基取代而得到的碳原子数为4~20的基团。作为上述饱和单环式烷基,例如可列举出环丙基、环丁基、环戊基、环己基、环庚基、环辛基、环壬基及环癸基等。作为上述饱和多环式烷基,可列举出金刚烷基、十氢萘基、八氢戊搭烯基及二环[1.1.1]戊烷基等。作为将饱和单环式或饱和多环式烷基的环中的氢原子取代的烷基,可列举出作为上述碳原子数为1~20的烷基所例示的基团。作为饱和多环式烷基的环中的1个以上的氢原子被烷基取代而得到的基团,例如可列举出冰片基等。
[0094]
上述碳原子数为4~20的环烷基烷基是指烷基的氢原子被环烷基取代而得到的碳原子数为4~20的基团。环烷基烷基中的环烷基可以为单环,也可以为多环。作为环烷基为
单环的碳原子数为4~20的环烷基烷基,例如可列举出环丙基甲基、2-环丁基乙基、3-环戊基丙基、4-环己基丁基、环庚基甲基、环辛基甲基、2-环壬基乙基及2-环癸基乙基等。作为环烷基为多环的碳原子数为4~20的环烷基烷基,可列举出3-3-金刚烷基丙基及十氢萘基丙基等。
[0095]
上述通式(a)及上述通式(1)中的碳原子数为6~20的含芳香族烃环的基团为包含芳香族烃环且不含杂环的烃基,可以具有脂肪族烃基,也可以具有取代基。具有取代基的含芳香族烃环的基团是含芳香族烃环的基团中的1个以上的氢原子被取代基取代而得到的结构的基团。
[0096]
作为无取代的含芳香族烃环的基团,例如可列举出碳原子数为6~20的芳基、碳原子数为7~20的芳基烷基。此外,作为具有取代基的上述含芳香族烃环的基团,可列举出上述无取代的含芳香族烃环的基团中的1个以上的氢原子被取代基取代而得到的基团等,作为该取代基,可列举出卤素原子、氰基、硝基、羟基、硫醇基或-cooh等。
[0097]
上述碳原子数为6~20的芳基可以为单环结构,也可以为稠环结构,进而,也可以是2个芳香族烃环连接而得到的芳基。
[0098]
作为2个芳香族烃环连接而得到的芳基,可以是2个单环结构的芳香族烃环连接而得到的芳基,也可以是单环结构的芳香族烃环与稠环结构的芳香族烃环连接而得到的芳基,还可以是稠环结构的芳香族烃环与稠环结构的芳香族烃环连接而得到的芳基。
[0099]
作为连接2个芳香族烃环的连接基,只要是能够设为作为芳基整体具有芳香族性的芳基的连接基即可,可列举出单键、硫醚基(-s-)及羰基等。作为单环结构的芳基,例如可列举出苯基、甲苯基、二甲苯基、乙基苯基、2,4,6-三甲基苯基等。作为稠环结构的芳基,例如可列举出萘基、蒽基、菲基及芘基等。作为2个单环结构的芳香族烃环连接而得到的芳基,例如可列举出联苯、二苯基硫醚、苯甲酰基苯基等。
[0100]
上述碳原子数为7~20的芳基烷基是指烷基中的1个以上氢原子被芳基取代而得到的基团。作为碳原子数为7~20的芳基烷基,例如可列举出苄基、芴基、茚基、9-芴基甲基、α-甲基苄基、α,α-二甲基苄基、苯基乙基及萘基丙基等。
[0101]
上述通式(a)及上述通式(1)中的碳原子数为2~20的含杂环基团是包含杂环的烃基,可以具有含芳香族烃环的基团,也可以具有脂肪族烃基,还可以具有取代基。具有取代基的含杂环基团是含杂环基团中的1个以上的氢原子被取代基取代而得到的结构的基团。
[0102]
作为无取代的含杂环基团,可列举出吡啶基、喹啉基、噻唑基、四氢呋喃基、二氧杂戊环基、四氢吡喃基、吗啉基呋喃基、甲基噻吩基、己基噻吩基、苯并噻吩基、吡咯基、吡咯烷基、咪唑基、咪唑烷基、咪唑啉基、吡唑基、吡唑烷基、哌啶基、哌嗪基、嘧啶基、呋喃基、噻嗯基、苯并噁唑-2-基、噻唑基、异噻唑基、噁唑基、异噁唑基、吗啉基等杂环基、以及烷基的1个以上氢原子被杂环取代而得到的基团等。此外,作为具有取代基的上述含杂环基团,可列举出上述无取代的上述含杂环基团中的1个以上的氢原子被取代基取代而得到的基团等,作为该取代基,可列举出卤素原子、氰基、硝基、羟基、硫醇基或-cooh等。
[0103]
进而,无取代的含杂环基团可以是杂环与单环结构的芳香族烃环连接而得到的基团,也可以是杂环与稠环结构的芳香族烃环连接而得到的基团。作为连接2个芳香族烃环的连接基,可列举出单键及羰基等。作为杂环与单环结构的芳香族烃环连接而得到的含杂环基团,可列举出苯并噻吩等。
[0104]
上述通式(a)及上述通式(1)中的上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自上述组i中的二价的基团取代而得到的基团不具有多个二价的基团相邻的结构。多个二价的基团可以相同,也可以不同。
[0105]
在本发明中,基团的碳原子数在基团中的氢原子被取代基取代的情况下,规定该取代后的基团的碳原子数。例如,在碳原子数为1~20的烷基的氢原子被取代基取代而得到的基团的情况下,碳原子数为1~20是指氢原子被取代之后的碳原子数,而不是指氢原子被取代之前的碳原子数。
[0106]
此外,在本发明中,对于所限定的碳原子数的基团中的亚甲基被二价的基团取代而得到的基团的碳原子数,规定该取代后的基的碳原子数。例如,在碳原子数为1~20的烷基中的亚甲基被二价的基团取代而得到的基团的情况下,碳原子数为1~20是指亚甲基被二价的基团取代之后的碳原子数,而不是指取代之前的碳原子数。
[0107]
上述通式(a)中的a所表示的碳原子数为6~20的芳香族环基(以下,有时称为芳香族环基a。)是指含有芳香族环的碳原子数为6~20的结构,至少含有芳香族烃环及芳香族杂环中的任一者。
[0108]
此外,碳原子数为6~20的芳香族环基a的“碳原子数为6~20”是指形成芳香族环基中所含的芳香族环的环骨架的碳原子数。此外,在芳香族环基具有连接结构的情况下,是指形成芳香族环的环骨架的碳原子的合计数。例如,甲苯基、吲哚环基、二苯基硫醚基分别相当于碳原子数为6、8、12的芳香族环基。
[0109]
此外,芳香族环基a中所含的芳香族环可以为单环结构,也可以为多环结构。在为多环结构的情况下,可以是稠环结构,也可以是单环结构的芳香族环与单环结构的芳香族环连接而得到的多环结构,也可以是单环结构的芳香族环与稠环结构的芳香族环连接而得到的多环结构,还可以是稠环结构的芳香族环与稠环结构的芳香族环连接而得到的结构等的芳香族环彼此连接而得到的连接结构。
[0110]
作为连接芳香族环与芳香族环的连接基,只要是能够制成作为芳基整体具有芳香族性的多环结构的连接基即可,可列举出单键、硫醚基(-s-)及羰基等。
[0111]
在本发明中,芳香族环基a优选为多环结构。这是因为上述自由基聚合引发剂能够更有效地发挥感度的稳定性优异的效果。
[0112]
上述芳香族烃环是指不含杂环且含有芳香族烃环的结构,例如可列举出环丁二烯环、苯环、环辛四烯环、[14]轮烯环、[18]-轮烯环、萘环、蒽环等单环结构或稠环结构、三苯基胺结构、二苯基硫醚结构及芴环等连接结构等。
[0113]
在本发明中,上述芳香族烃环优选为多环结构,其中,优选为连接结构、稠环结构。
[0114]
作为连接结构,优选为连接基为硫醚基的二苯基硫醚结构。这是因为上述自由基聚合引发剂能够更有效地发挥感度的稳定性优异的效果。
[0115]
作为稠环结构,只要是2个以上的环结构稠合而得到的结构即可,优选为2个以上且4个以下的环结构稠合而得到的结构,优选为2个以上且3个以下的环结构稠合而得到的结构,特别优选为3个环结构稠合而得到的结构,其中特别优选为芴环。这是因为上述自由基聚合引发剂能够更有效地发挥感度的稳定性优异的效果。
[0116]
上述芳香族杂环是指含有芳香族杂环的结构,例如可列举出呋喃环、噻吩环、吡咯环、吡唑环、咪唑环、吡啶环、哒嗪环、嘧啶环、吡嗪环、咔唑环、及吲哚环等单环结构或稠环
结构等。
[0117]
在本发明中,上述芳香族杂环优选为多环结构,其中,优选为稠环结构。这是因为上述自由基聚合引发剂能够更有效地发挥感度的稳定性优异的效果。
[0118]
作为稠环结构,只要是2个以上的环结构稠合而得到的结构即可,优选为2个以上且4个以下的环结构稠合而得到的结构,优选为2个以上且3个以下的环结构稠合而得到的结构,优选为2个环结构稠合而得到的结构。这是因为上述自由基聚合引发剂能够更有效地发挥感度的稳定性优异的效果。
[0119]
作为2个环结构稠合而得到的结构,优选为吲哚环。这是因为上述自由基聚合引发剂能够更有效地发挥感度的稳定性优异的效果。
[0120]
作为3个环结构稠合而得到的结构,优选为咔唑环。这是因为上述自由基聚合引发剂能够更有效地发挥感度的稳定性优异的效果。
[0121]
通式(a)中,a表示1~19的整数,在a为2以上的整数的情况下,多个存在的r
31
可以相同,也可以不同。
[0122]
通式(a)中,b表示0~19的整数,在b为2以上的整数的情况下,多个存在的r
32
可以相同,也可以不同。
[0123]
通式(a)中,c表示0~19的整数,在c为2以上的整数的情况下,多个存在的r
33
可以相同,也可以不同。
[0124]
通式(a)中,a+b+c为20以下。其中,a+b+c将芳香族环基a中可键合的数设定为上限。
[0125]
a只要是可得到所期望的感度的稳定性的数即可,优选为1~3,优选为1~2,优选为1。这是因为通过a为上述的范围,上述自由基聚合引发剂能够有效地发挥感度的稳定性优异的效果。
[0126]
b只要是可得到所期望的感度的稳定性的数即可,优选为0~3,优选为0~2,优选为0~1。这是因为通过b为上述的范围,上述自由基聚合引发剂能够有效地发挥感度的稳定性优异的效果。
[0127]
c只要是可得到所期望的感度的稳定性的数即可,优选为0~3,优选为0~2,优选为0~1。这是因为通过c为上述的范围,上述自由基聚合引发剂能够有效地发挥感度的稳定性优异的效果。
[0128]
上述通式(1)所表示的基团是与上述芳香族环基a键合的基团,是将与构成芳香族环基中的芳香族环的环结构的原子键合的氢原子取代而键合的基团。
[0129]
作为上述通式(1)中使用的r1,优选为碳原子数为1~20的无取代或具有取代基的脂肪族烃基、或上述脂肪族烃基的基团中的1个以上的亚甲基被上述组i所表示的基团取代而得到的基团,更优选为碳原子数为1~20的无取代的脂肪族烃基、或上述脂肪族烃基的基团中的1个以上的亚甲基被上述组i所表示的基团取代而得到的基团,特别优选为碳原子数为1~20的无取代的脂肪族烃基。这是因为通过r1为上述的基团,上述自由基聚合引发剂能够有效地发挥感度的稳定性优异的效果。
[0130]
作为上述r1中使用的碳原子数为1~20的无取代的脂肪族烃基,优选为碳原子数为1~20的直链或支链的烷基,更优选为碳原子数为2~10的直链或支链的烷基,进一步优选为碳原子数为4~8的直链或支链的烷基,特别优选为碳原子数为4~8的直链的烷基。这
是因为上述自由基聚合引发剂能够有效地发挥感度的稳定性优异的效果。
[0131]
作为上述通式(1)中使用的r2,优选为碳原子数为1~20的无取代的脂肪族烃基,更优选为碳原子数为1~20的直链或支链的烷基,进一步优选为碳原子数为1~10的直链或支链的烷基,特别优选为碳原子数为1~3的直链的烷基。这是因为上述自由基聚合引发剂能够有效地发挥感度的稳定性优异的效果。
[0132]
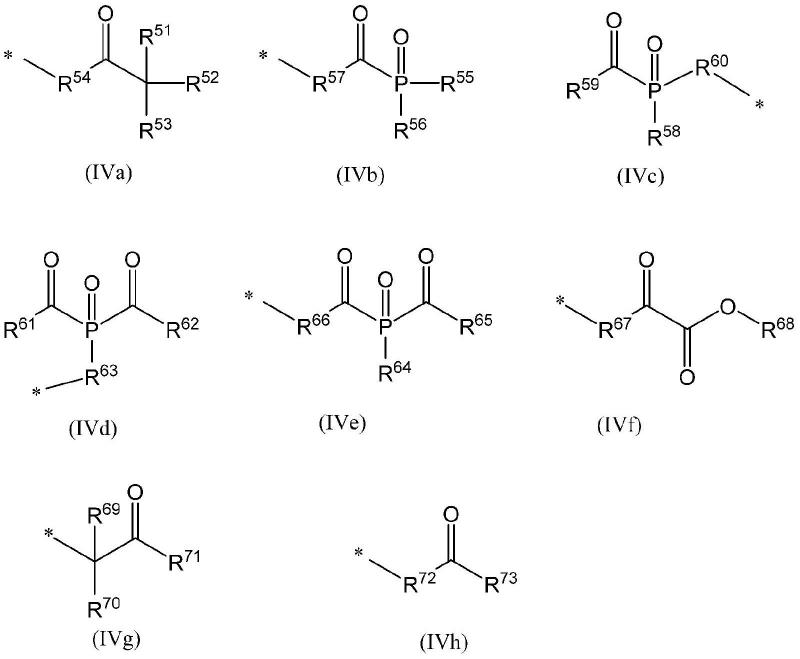
上述通式(a)中的除上述通式(1)以外的自由基产生基是指不具有肟酯基的自由基产生基,例如可列举出下述通式(iva)、(ivb)、(ivc)、(ivd)、(ive)、(ivf)、(ivg)及(ivh)所表示的基团。
[0133]
除上述通式(1)以外的自由基产生基是与上述芳香族环基a键合的基团,是将与构成芳香族环基中的芳香族环的环结构的原子键合的氢原子取代而键合的基团。
[0134]
[化学式6]
[0135][0136]
(式中,r
51
表示or
81
、nr
82r83
或碳原子数为2~20的无取代或具有取代基的含杂环基团,
[0137]r52
及r
53
分别独立地表示r
81
或or
81
,r
52
与r
53
也可以键合而形成环,
[0138]r55
、r
56
、r
58
、r
59
、r
61
、r
62
、r
64
、r
65
、r
71
及r
73
表示碳原子数为6~20的无取代或具有取代基的芳基,
[0139]r54
、r
57
、r
60
、r
63
、r
66
、r
67
及r
72
分别独立地表示碳原子数为6~20的无取代或具有取代基的亚芳基或单键,
[0140]r68
表示碳原子数为1~20的无取代或具有取代基的烃基,
[0141]r69
及r
70
分别独立地表示r
81
或or
81
,
[0142]r81
、r
82
及r
83
分别独立地表示氢原子或碳原子数为1~20的无取代或具有取代基的
烃基,
[0143]
*表示键合点。)
[0144]
作为上述通式(iva)、(ivb)、(ivc)、(ivd)、(ive)、(ivf)、(ivg)及(ivh)中使用的碳原子数为1~20的烃基,可列举出碳原子数为1~20的脂肪族烃基、碳原子数为6~20的含芳香族烃环的基团。
[0145]
作为上述通式(iva)、(ivb)、(ivc)、(ivd)、(ive)、(ivf)、(ivg)及(ivh)中使用的碳原子数为6~20的亚芳基,可列举出从碳原子数为6~20的芳基中除去1个氢原子而得到的二价的基团。
[0146]
作为上述通式(iva)、(ivb)、(ivc)、(ivd)、(ive)、(ivf)、(ivg)及(ivh)中使用的r
52
与r
53
键合而形成的环,可以是单环,也可以是稠环。作为单环,例如可列举出环戊烷、环己烷及环戊烯等单环的环烷烃、苯等单环的芳香族环、吡咯烷、吡咯、哌嗪、吗啉、硫代吗啉、四氢吡啶、内酯环及内酰胺环等单环的杂环。作为稠环,可列举出萘及蒽等。
[0147]
关于上述通式(iva)、(ivb)、(ivc)、(ivd)、(ive)、(ivf)、(ivg)及(ivh)中使用的碳原子数为1~20的脂肪族烃基、碳原子数为6~20的含芳香族烃环的基团、碳原子数为6~20的芳基、碳原子数为2~20的含杂环基团,可以设定为与通式(a)及上述通式(1)中使用的基团同样。
[0148]
此外,在具有取代基的含杂环基团、具有取代基的芳基、具有取代基的亚芳基、具有取代基的烃基中,作为取代含杂环基团、芳基、亚芳基及烃基中的1个以上的氢原子的取代基,可列举出卤素原子、氰基、硝基、羟基、硫醇基或-cooh等。
[0149]
在本发明中,上述化合物a优选为下述通式(a1)及(a2)所表示的化合物,更优选为下述通式(a1)所表示的化合物。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0150]
[化学式7]
[0151][0152]
(式中,r
11
、r
12
、r
13
、r
14
、r
15
、r
16
及r
17
分别独立地为氢原子、上述通式(a)中的r
31
所表示的基团、上述通式(a)中的r
32
所表示的基团或上述通式(a)中的r
33
所表示的基团,r
11
与r
12
、r
12
与r
13
、r
14
与r
15
、r
15
与r
16
或r
16
与r
17
也可以互相键合而形成环,
[0153]r11
、r
12
、r
13
、r
14
、r
15
、r
16
及r
17
中的至少1个为上述通式(a)中的r
31
所表示的基团。)
[0154]r11
与r
12
、r
12
与r
13
、r
14
与r
15
、r
15
与r
16
或r
16
与r
17
互相键合而形成的环可以为单环,也可以为稠环。作为单环,例如可列举出环戊烷、环己烷及环戊烯等单环的环烷烃、苯等单环的芳香族环、吡咯烷、吡咯、哌嗪、吗啉、硫代吗啉、四氢吡啶、内酯环及内酰胺环等单环的杂环。作为稠环,可列举出萘及蒽等。
[0155]
[化学式8]
[0156][0157]
(式中,r
21
、r
22
、r
23
、r
24
、r
25
、r
26
、r
27
及r
28
分别独立地为氢原子、上述通式(a)中的r
31
所表示的基团、上述通式(a)中的r
32
所表示的基团或上述通式(a)中的r
33
所表示的基团,r
21
与r
22
、r
22
与r
23
、r
23
与r
24
、r
25
与r
26
、r
26
与r
27
或r
27
与r
28
也可以互相键合而形成环,
[0158]
x1为单键、无键合、氧原子、硫原子、硒原子、cr
41r42
、co、nr
43
或pr
44
,
[0159]
x2为氧原子、硫原子、硒原子、cr
41r42
、co、nr
43
或pr
44
,
[0160]r41
、r
42
、r
43
及r
44
分别独立地为氢原子、上述通式(a)中的r
31
所表示的基团、上述通式(a)中的r
32
所表示的基团或上述通式(a)中的r
33
所表示的基团。)
[0161]
作为r
21
与r
22
、r
22
与r
23
、r
23
与r
24
、r
25
与r
26
、r
26
与r
27
或r
27
与r
28
互相键合而形成的环,可以设定为与作为上述的通式(a1)中r
11
与r
12
等键合而形成的环所例示的环同样。
[0162]
在本发明中,上述通式(a1)中的r
11
优选为上述通式(a)中的r
31
。即,上述通式(a1)中的r
11
优选为上述通式(1)所表示的基团。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0163]
此外,上述通式(a1)中的r
13
及r
16
的1个以上优选为上述通式(a)中的r
33
。即,上述通式(a1)中的r
13
及r
16
的1个以上表示卤素原子、硝基、氰基、-or
34
、-cor
34
、-ocor
34
、-coor
34
、-sr
34
、-sor
34
、-so2r
34
、-nr
35r36
、-nr
35
cor
36
、-conr
35r36
、碳原子数为1~20的无取代或具有取代基的脂肪族烃基、碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、碳原子数为2~20的无取代或具有取代基的含杂环基团、或上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自下述组i中的二价的基团取代而得到的基团,r
34
、r
35
及r
36
分别独立地表示氢原子、碳原子数为1~20的无取代或具有取代基的脂肪族烃基、碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、或碳原子数为2~20的无取代或具有取代基的含杂环基团、或上述脂肪族烃基、上述含芳香族烃环的基团或上述含杂环基团中的1个以上的亚甲基被选自下述组i中的二价的基团取代而得到的基团,在r
34
、r
35
或r
36
存在多个的情况下,它们可以相同,也可以不同,取代上述具有取代基的脂肪族烃基、上述具有取代基的含芳香族烃环的基团及上述具有取代基的含杂环基团中的1个以上的氢原子的取代基优选为卤素原子、氰基、硝基、羟基、硫醇基或-cooh。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0164]
在本发明中,r
13
优选为上述通式(a)中的r
33
,其中,用于r
13
的r
33
优选为碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团、或上述含芳香族烃环的基团中的1个以上的亚甲基被选自上述组i中的二价的基团取代而得到的基团。这是因为通过r
13
为上述结构,上述自由基聚合引发剂成为感度的稳定性更优异的自由基聚合引发剂。
[0165]
作为r
13
中使用的碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团中的“含芳香族烃环的基团”,优选单环结构或芳香族烃环连接而得到的结构的碳原子数为6~20的芳基,更优选芳香族烃环连接而得到的结构的碳原子数为12~18的芳基,特别优选
芳香族烃环连接而得到的结构的碳原子数为12~15的芳基,其中特别优选芳香族烃环通过羰基连接而得到的结构的碳原子数为12~15的芳基。这是因为通过r
13
为上述结构,上述自由基聚合引发剂成为感度的稳定性更优异的自由基聚合引发剂。
[0166]r16
可以是氢原子或上述通式(a)中的r
33
的任一者,优选为氢原子或碳原子数为1~20的无取代或具有取代基的脂肪族烃基,其中,更优选为氢原子或碳原子数为1~10的无取代的烷基,特别优选为氢原子或碳原子数为1~3的无取代的烷基,其中特别优选为氢原子。这是因为通过r
16
为上述结构,上述自由基聚合引发剂成为感度的稳定性更优异的自由基聚合引发剂。
[0167]
在r
11
、r
13
及r
16
为上述的基团的情况下,r
12
、r
14
、r
15
及r
17
可以为氢原子或上述通式(a)中的r
33
的任一者,优选为氢原子或碳原子数为1~20的无取代或具有取代基的脂肪族烃基,其中,更优选为氢原子或碳原子数为1~10的无取代的烷基,特别优选为氢原子或碳原子数为1~3的无取代的烷基,其中特别优选为氢原子。这是因为通过r
12
、r
14
、r
15
及r
17
为上述结构,上述自由基聚合引发剂成为感度的稳定性更优异的自由基聚合引发剂。
[0168]
在本发明中,进一步优选上述通式(a1)中的r
11
为上述通式(1)所表示的基团,r
13
为r
33
,用于r
13
的r
33
为碳原子数为6~20的无取代或具有取代基的含芳香族烃环的基团或上述含芳香族烃环的基团中的1个以上的亚甲基被选自上述组i中的二价的基团取代而得到的基团,r
12
、r
14
、r
15
、r
16
及r
17
为氢原子。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0169]
作为上述通式(a1)所表示的化合物的优选的具体例子,例如可列举出国际公开第2015/152153号等中例示的化合物。
[0170]
作为上述通式(a2)所表示的化合物中的优选的化合物,例如可列举出下述通式(a21)、(a22)及(a23)所表示的化合物。
[0171]
[化学式9]
[0172][0173]
(式中,r
21
、r
22
、r
23
、r
24
、r
25
、r
26
、r
27
、r
28
、r
41
、r
42
及r
43
与上述通式(a2)相同。)
[0174]
作为上述通式(a2)所表示的化合物,可以使用国际公开第2008/078678号、日本特开2011-132215号公报等中记载的化合物。
[0175]
上述通式(a)所表示的化合物可以通过国际公开第2015/152153号、国际公开第2008/078678号及日本特开2011-132215号公报等中记载的公知的方法来制造。
[0176]
例如,上述通式(a1)所表示的化合物(化合物a1)中上述通式(1)中的n为0的化合物可以按照下述《例1》中所示的反应式,通过以下的方法来制造。具体而言,通过使酮体1与卤化物反应来得到酮体2,通过使酮体2与盐酸羟胺反应来得到肟化合物3。接着,通过使酸酐4、酰氯4’或羧酸盐4”与该肟化合物3反应,能够制造上述化合物a1。
[0177]
上述通式(1)中的n为1的化合物a1也可以依据n为0的化合物a1,按照下述《例2》中所示的反应式来制造。
[0178]
[化学式10]
[0179]
《例1》
[0180][0181]
(式中,r
11
、r
12
、r
13
、r
14
、r
15
、r
16
及r
17
与上述通式(a1)相同。)
[0182]
[化学式11]
[0183]
《例2》
[0184][0185]
(式中,r
11
、r
12
、r
13
、r
14
、r
15
、r
16
及r
17
与上述通式(a1)相同。)
[0186]
作为上述化合物a的含量,在上述自由基聚合引发剂100质量份中,优选为70质量份以上,更优选为80质量份以上,特别优选为90质量份以上。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0187]
作为上述化合物a的含量,在上述自由基聚合引发剂的固体成分100质量份中,优选为70质量份以上,更优选为80质量份以上,特别优选为90质量份以上。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0188]
需要说明的是,固体成分是指除溶剂(水及有机溶剂)以外的全部的成分的合计。
[0189]
2.酸成分
[0190]
上述酸成分是作为除上述化合物a以外的成分而包含的成分,能够供给质子(h
+
)。
[0191]
因此,作为上述化合物a具有羧基等酸性基的化合物不包含在上述酸成分中。
[0192]
作为这样的酸成分,可以使用具有碳原子的有机酸、不具有碳原子的无机酸中的任一者。
[0193]
在本发明中,上述酸成分优选为有机酸。这是因为通过上述酸成分的种类为上述种类,上述自由基聚合引发剂成为感度的稳定性更优异的自由基聚合引发剂。
[0194]
酸成分的规定度可以如乙酸那样为1当量,也可以如草酸那样为2当量以上。
[0195]
在本发明中,酸成分的当量度优选为1以上且3以下,优选为1以上且2以下,优选为1。这是因为通过当量度为上述的范围,自由基聚合引发剂成为感度的稳定性更优异的自由
基聚合引发剂。
[0196]
上述酸成分的分子量优选250以下,更优选200以下,特别优选50以上且100以下。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0197]
作为上述酸成分的酸基,优选羧基、磺酸基、磷酸基、硝酸基及硼酸基,特别优选羧基。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0198]
作为有机酸的例子,可列举出甲酸、乙酸、丙酸、丁酸、乳酸等碳原子数为1~18的脂肪族单羧酸;草酸、丙二酸、琥珀酸、富马酸、马来酸、己二酸等碳原子数为1~12的脂肪族二羧酸;苯甲酸、邻苯二甲酸、间苯二甲酸、对苯二甲酸、水杨酸等芳香族羧酸;甲磺酸、对甲苯磺酸、十二烷基苯磺酸、三氟甲磺酸等碳原子数为1~20的磺酸等。
[0199]
作为无机酸的例子,可列举出盐酸、氢溴酸、硫酸、亚硫酸、磷酸、亚磷酸、多磷酸、硝酸、硼酸、高氯酸等。
[0200]
在本发明中,上述有机酸更优选为碳原子数为1~18的脂肪族单羧酸、碳原子数为1~12的脂肪族二羧酸,其中,更优选为碳原子数为1~18的脂肪族单羧酸,特别更优选为碳原子数为1~10的脂肪族单羧酸,其中特别更优选为碳原子数为1~5的脂肪族单羧酸,其中特别更优选为碳原子数为2~4的脂肪族单羧酸,其中特别优选为乙酸。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0201]
上述有机酸及无机酸可以单独使用1种,也可以将2种以上并用。
[0202]
上述酸成分的含量在上述化合物a及上述酸成分的合计中为1ppm以上且400ppm以下,其中更优选3ppm以上且200ppm以下,特别优选5ppm以上且30ppm以下。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0203]
需要说明的是,酸成分的含量为质量基准。
[0204]
此外,酸成分的含量可以通过离子色谱法来获得。
[0205]
上述酸成分的含量在上述自由基聚合引发剂中,优选1ppm以上且400ppm以下,更优选3ppm以上且200ppm以下,特别优选5ppm以上且30ppm以下。这是因为上述自由基聚合引发剂成为感度的稳定性更优异的物质。
[0206]
需要说明的是,酸成分的含量为质量基准。
[0207]
3.溶剂
[0208]
上述自由基聚合引发剂包含化合物a及酸成分,根据需要可以包含溶剂。
[0209]
上述溶剂是在常温(25℃)大气压下为液状、可分散或溶解化合物a及酸成分以及后述的其他成分的溶剂。因此,即使是在常温(25℃)大气压下为液状,上述化合物a及酸成分也不包括在溶剂内。
[0210]
作为溶剂,可列举出后述的“b.组合物”的“3.溶剂”中记载的水及有机溶剂。
[0211]
作为上述溶剂的含量,只要是可得到所期望的感度的稳定性的含量即可,在自由基聚合引发剂100质量份中,可以设定为1质量份以上且99质量份以下。
[0212]
上述自由基聚合引发剂只要是可得到所期望的感度的稳定性,则可以根据需要包含水。
[0213]
上述水的含量在化合物a、酸成分及水的合计中,优选为5质量%以下,其中,优选为1质量%以下,特别优选为0.5质量%以下,优选为0.1质量%以下。这是因为通过水的含量为上述的范围内,自由基聚合引发剂成为感度的稳定性更优异的自由基聚合引发剂。
[0214]
此外,关于水的含量的下限,只要是可得到所期望的感度的稳定性则没有特别限定,但从自由基聚合引发剂的制备容易性、保管容易性等观点出发,可以设定为0.01质量%以上。
[0215]
需要说明的是,关于水的含量,可以使用卡尔
·
费休(karl fischer)法来测定。
[0216]
4.其他的成分
[0217]
上述自由基聚合引发剂包含化合物a及酸成分,可以包含溶剂,但根据需要也可以包含其他的成分。
[0218]
作为这样的其他的成分,可列举出后述的“b.组合物”的“4.其他的成分”的项中记载的成分等。
[0219]
作为其他的成分,作为产生自由基的化合物,可以包含具有除化合物a以外的结构的化合物。
[0220]
5.自由基聚合引发剂
[0221]
上述自由基聚合引发剂是产生自由基的物质。
[0222]
由上述自由基聚合引发剂产生自由基的方法只要是对于自由基产生剂一般所使用的方法即可,具体而言,可列举出照射能量射线的方法、加热处理的方法、同时或依次进行这些方法的方法等。即,上述自由基聚合引发剂可以是通过能量射线照射而产生自由基的光自由基聚合引发剂,也可以是通过加热处理而产生自由基的热自由基聚合引发剂。
[0223]
作为上述能量射线,可列举出g射线(436nm)、h射线(405nm)、i射线(365nm)、可见光线、紫外线、远紫外线、x射线及带电粒子线等。
[0224]
在本发明中,自由基产生所使用的能量射线优选为在波长200nm以上且450nm的范围中在波长300nm以上且400nm以下的范围内具有极大光谱的射线,更优选为在波长340nm以上且380nm以下的范围内具有极大光谱的射线。这是因为能够由上述自由基聚合引发剂有效地产生自由基。
[0225]
作为上述能量射线的光源,可列举出低压汞灯、中压汞灯、高压汞灯、超高压汞灯、氙灯、金属卤素灯、电子射线照射装置、x射线照射装置、激光器(氩激光器、色素激光器、氮激光器、发光二极管(led)、氦镉激光器等)。
[0226]
关于上述能量射线的曝光量,只要是能够产生期望量的自由基的曝光量则没有特别限制,可以根据上述化合物a的用途等而适当决定。上述曝光量优选为5mj/cm2以上且2000mj/cm2以下。这是因为能够由上述自由基聚合引发剂有效地产生自由基。
[0227]
作为上述加热处理中的加热温度,例如优选为70℃以上且450℃以下,更优选为150℃以上且300℃以下。此外,作为加热处理中的加热时间,例如优选为1分钟以上且100分钟以下。这是因为能够由上述自由基聚合引发剂有效地产生自由基。
[0228]
上述自由基聚合引发剂的形状可以为粉末状,也可以为颗粒状。在形状为颗粒状的情况下,作为其制造方法,例如可列举出使用挤出机等将上述化合物a、酸成分及其他的成分混合后成型为颗粒状的方法。上述自由基聚合引发剂的形状也可以是上述化合物a及酸成分分散或溶解于溶剂中而得到的溶液状。
[0229]
作为上述自由基聚合引发剂的用途,例如可列举出包含自由基聚合性化合物的固化性组合物。
[0230]
作为上述固化性组合物的用途,例如可以用于光固化性涂料或清漆、光固化性粘
接剂、印刷基板、或彩色电视机、pc监视器、便携信息终端、数码相机等彩色显示的液晶显示元件中的滤色器、等离子体显示面板用的电极材料、粉末涂敷、印刷油墨、印刷版、粘接剂、牙科用组合物、凝胶涂层、电子工程学用的光致抗蚀剂、电镀抗蚀剂、蚀刻抗蚀剂、液状及干燥膜这两者、阻焊剂、用于制造各种显示用途用的滤色器或在等离子体显示面板、电气发光显示装置、及lcd的制造工序中用于形成结构的抗蚀剂、用于封入电气及电子部件的组合物、磁记录材料、微小机械部件、波导、光学开关、镀覆用掩模、蚀刻掩模、彩色试验体系、玻璃纤维电缆涂敷、丝网印刷用模版、用于通过立体光刻来制造三维物体的材料、全息照相记录用材料、图像记录材料、微细电子电路、脱色材料、用于图像记录材料的脱色材料、使用微胶囊的图像记录材料用的脱色材料、印刷布线板用光致抗蚀剂材料、uv及可见激光直接图像系用的光致抗蚀剂材料、在印刷电路基板的逐次叠层中的电介质层的形成中使用的光致抗蚀剂材料或保护膜等各种用途,对其用途没有特别限制。
[0231]
此外,作为上述固化性组合物的用途,还可列举出有机电致发光(有机el)显示器、量子点(qd)显示器、微发光二极管(μled)显示器中使用的滤色器、间隔壁材、绝缘膜等光学构件形成用组合物。
[0232]
作为上述固化性组合物的用途,还可列举出聚合性液晶涂敷组合物、导电性糊剂、uv固化性油墨等各种固化性油墨组合物。
[0233]
作为上述固化性组合物的用途,还可列举出半导体封装中使用的阻焊剂、电路形成用抗蚀剂、凸块用抗蚀剂等各种用途的电子基板电路中的绝缘性构件形成用组合物。
[0234]
b.组合物
[0235]
接着,对本发明的组合物进行说明。
[0236]
本发明的组合物的特征在于,其包含上述的自由基聚合引发剂和自由基聚合性化合物。
[0237]
本发明的组合物通过包含上述自由基聚合引发剂,成为感度的稳定性优异的组合物。
[0238]
1.自由基聚合引发剂
[0239]
作为本发明的组合物中的上述自由基聚合引发剂的含量,只要是相对于组合物能够赋予所期望的固化性等的含量则没有特别限定。
[0240]
本发明的组合物中的上述自由基聚合引发剂的含量例如在组合物的固体成分100质量份中,可以设定为0.001质量份以上且低于30质量份,优选为0.005质量份以上且10质量份以下。这是因为上述组合物成为感度的稳定性更优异的组合物。
[0241]
需要说明的是,固体成分包含除溶剂以外的全部的成分。
[0242]
作为上述自由基聚合引发剂的含量,相对于自由基聚合性化合物100质量份,优选0.1质量份以上且50质量份以下,更优选1质量份以上且30质量份以下,特别优选5质量份以上且20质量份以下。这是因为上述组合物成为感度的稳定性更优异的组合物。
[0243]
需要说明的是,关于上述的自由基聚合引发剂,与“a.自由基聚合引发剂”的项中记载的内容同样。
[0244]
2.自由基聚合性化合物
[0245]
上述自由基聚合性化合物只要是能够自由基聚合的化合物即可,例如可列举出具有丙烯酸基、甲基丙烯酸基、乙烯基等烯键式不饱和双键的化合物。
[0246]
上述自由基聚合性化合物是具有1个以上自由基聚合性基的化合物,可以是具有1个自由基聚合性基的单官能化合物或具有2个以上自由基聚合性基的多官能化合物中的任一者。
[0247]
上述自由基聚合性化合物可以是具有酸值的化合物或不具有酸值的化合物中的任一者。
[0248]
作为上述具有酸值的化合物,例如可列举出甲基丙烯酸、丙烯酸等具有羧基等的丙烯酸酯化合物、甲基丙烯酸酯化合物等。
[0249]
作为上述具有酸值的化合物,还可列举出包含具有羧基的结构单元及具有烯键式不饱和基的结构单元的聚合物。
[0250]
作为上述不具有酸值的化合物,可列举出氨基甲酸酯丙烯酸酯树脂、氨基甲酸酯甲基丙烯酸酯树脂、环氧丙烯酸酯树脂、环氧甲基丙烯酸酯树脂、丙烯酸-2-羟基乙酯、甲基丙烯酸-2-羟基乙酯等不具有羧基等的丙烯酸酯化合物、甲基丙烯酸酯化合物。
[0251]
上述自由基聚合性化合物可以单独或将2种以上混合而使用。例如,作为自由基聚合性化合物,可以将具有烯键式不饱和基且具有酸值的化合物与具有烯键式不饱和基且不具有酸值的化合物组合而使用。
[0252]
在将2种以上自由基聚合性化合物混合而使用的情况下,可以将它们预先共聚而制成共聚物来使用。
[0253]
作为这样的自由基聚合性化合物等,更具体而言,可列举出日本特开2016-176009号公报中记载的自由基聚合性化合物、国际公开2019/088055号中记载的具有自由基聚合性基的聚合性化合物等。
[0254]
作为包含具有羧基的结构单元及具有烯键式不饱和基的结构单元的聚合物,例如也可以使用日本特开2016-151744号公报中记载的[a]作为包含具有羧基的结构单元的聚合物的包含具有(甲基)丙烯酰基的结构单元作为具有交联性基的结构单元(a2)的聚合物、国际公开2019/088055号中记载的(2)具有亲水性基的聚合物中包含具有甲基丙烯酰基或丙烯酰基的结构单元作为结构单元(u2)的聚合物等。
[0255]
上述自由基聚合性化合物的含量只要是可得到所期望的固化物的含量则没有特别限定,例如在组合物的固体成分100质量份中,可以设定为1质量份以上且50质量份以下,优选为5质量份以上且40质量份以下,更优选为8质量份以上且30质量份以下,特别优选为10质量份以上且20质量份以下。这是因为上述组合物成为固化性优异的组合物。
[0256]
3.溶剂
[0257]
上述组合物除了包含上述自由基聚合引发剂及自由基聚合性化合物以外,还可以包含溶剂。
[0258]
上述溶剂在常温(25℃)大气压下为液状,可分散或溶解自由基聚合引发剂及自由基聚合性化合物及后述的其他的成分。因此,即使是在常温(25℃)大气压下为液状,上述自由基聚合引发剂、自由基聚合性化合物也不包括在溶剂内。
[0259]
作为上述溶剂,可以使用水、有机溶剂中的任一者。
[0260]
在本发明中,上述溶剂优选为有机溶剂。这是因为上述自由基聚合引发剂、自由基聚合性化合物的溶解或分散容易。
[0261]
作为上述有机溶剂,可列举出碳酸亚丙酯、碳酸二乙酯等碳酸酯类;丙酮、2-庚酮
等酮类;乙二醇单甲基醚乙酸酯、乙二醇单乙基醚乙酸酯、丙二醇-1-单甲基醚-2-乙酸酯、二丙二醇单甲基醚乙酸酯、3-甲氧基丁基醚乙酸酯、乙氧基乙基醚丙酸酯等醚酯类;乙二醇、丙二醇、丙二醇单乙酸酯、二丙二醇等多元醇类;二噁烷那样的环式醚类;甲酸乙酯、3-甲基-3-甲氧基丁基乙酸酯等酯类;甲苯、二甲苯等芳香族烃类;γ-己内酯、δ-己内酯等内酯类等。
[0262]
在本发明中,上述有机溶剂优选包含醚酯类。这是因为容易制成分散稳定性优异的组合物。
[0263]
上述溶剂的含量在上述组合物100质量份中,可以设定为1质量份以上且99质量份以下。
[0264]
4.其他
[0265]
上述组合物除了包含上述自由基聚合引发剂、自由基聚合性化合物及溶剂以外,还可以根据需要包含其他的成分。
[0266]
作为上述其他的成分,可列举出聚合性化合物、具有亲水性基的聚合物、着色剂、无机化合物、具有亲水性基的聚合物以外的其他的有机聚合物、链转移剂、敏化剂、表面活性剂、硅烷偶联剂、三聚氰胺、着色剂、使无机化合物等分散的分散剂等。
[0267]
作为上述其他的成分,可列举出国际公开2019/088055号中作为其他的成分而记载的成分。
[0268]
作为具有亲水性基的聚合物,也可以使用在日本特开2005-234362号公报中记载的作为(a1)不饱和羧酸和/或不饱和羧酸酐、(a2)含环氧基的不饱和化合物及(a3)其他的不饱和化合物的共聚物的〔a〕共聚物、日本特开2016-151744号公报中记载的[a]包含具有羧基的结构单元的聚合物、国际公开2019/088055号中记载的(2)具有亲水性基的聚合物中不含具有甲基丙烯酰基或丙烯酰基等自由基聚合性基的结构单元的聚合物等。
[0269]
上述添加剂的含量根据其使用目的而适当选择,没有特别限制,但例如相对于组合物的固体成分100质量份可以设定为合计50质量份以下,优选为30质量份以下。
[0270]
4.组合物
[0271]
作为上述组合物的制造方法,只要是能够将上述各成分按照成为所期望的含量的方式混合的方法即可,可以使用公知的混合方法。
[0272]
作为上述组合物的用途,例如可以作为通过光照射而固化的光固化性组合物来使用。作为具体的用途,与上述“a.自由基聚合引发剂”的项中记载的内容同样。
[0273]
c.固化物
[0274]
接着,对本发明的固化物进行说明。
[0275]
本发明的固化物为上述的组合物的固化物。
[0276]
本发明的固化物由于使用上述的组合物,因此成为耐久性等的调整容易的固化物。
[0277]
需要说明的是,关于上述的组合物,与上述“b.组合物”的项中记载的内容同样。
[0278]
关于上述固化物的用途,与上述“a.自由基聚合引发剂”的项中记载的内容同样。
[0279]
作为上述固化物的制造方法,只要是能够按照成为所期望的形状的方式形成上述组合物的固化物的方法则没有特别限定。
[0280]
作为这样的制造方法,例如可列举出后述的“d.固化物的制造方法”的项中记载的
制造方法。
[0281]
d.固化物的制造方法
[0282]
接着,对本发明的固化物的制造方法进行说明。
[0283]
本发明的固化物的制造方法的特征在于,其具有将上述的组合物中的自由基聚合性化合物彼此聚合的聚合工序。
[0284]
本发明的固化物的制造方法由于在聚合工序中使用上述的组合物,因此能够容易地得到所期望的耐久性等的固化物。
[0285]
1.聚合工序
[0286]
本发明中的聚合工序是将上述的组合物固化的工序。
[0287]
作为将上述组合物固化的方法,只要是能够将自由基聚合性化合物彼此聚合而使其固化的方法即可,可列举出由上述自由基聚合引发剂产生自由基的方法。
[0288]
作为由上述自由基聚合引发剂产生自由基的方法,只要是能够由上述自由基聚合引发剂产生期望量的自由基的方法即可,例如可列举出照射能量射线的方法、进行加热处理的方法及同时或依次进行它们的方法。关于这样的照射能量射线的方法、加热处理的方法等,可列举出与上述“a.自由基聚合引发剂”的项中记载的方法同样的方法。
[0289]
在本工序中,上述产生自由基的方法优选包含照射能量射线的方法。这是因为能够由上述自由基聚合引发剂有效地产生自由基,能够将自由基聚合性化合物有效地固化。
[0290]
需要说明的是,关于上述组合物,与上述“b.组合物”的项中记载的内容同样。
[0291]
2.其他的工序
[0292]
本发明的固化物的制造方法除了包含上述聚合工序以外,还可以根据需要包含其他的工序。
[0293]
作为上述其他的工序,可列举出在上述聚合工序后将组合物的涂膜中的未聚合部分除去而得到图案状固化物的显影工序、在上述聚合工序后将固化物进行加热处理的后烘烤工序、在上述聚合工序前将组合物进行加热处理而除去上述组合物中的溶剂的预烘烤工序、在上述聚合工序前形成上述组合物的涂膜的工序等。
[0294]
在本发明中,上述其他的工序优选具有后烘烤工序。这是因为能够将由上述自由基聚合引发剂产生的自由基有效地扩散,其结果是,变得容易形成自由基聚合性化合物的聚合充分进行而得到的固化物。
[0295]
作为上述显影工序中的除去未聚合部分的方法,例如可列举出将碱显影液等显影液涂布于未聚合部分的方法。
[0296]
作为上述碱显影液,可以使用四甲基氢氧化铵(tmah)水溶液、氢氧化钾水溶液、碳酸钾水溶液等一般作为碱显影液而使用的溶液。
[0297]
此外,作为显影液,可以使用丙二醇单甲基醚乙酸酯(pegmea)、环己酮等一般作为溶剂显影液而使用的溶液。
[0298]
作为使用了上述显影液的显影方法,只要是能够使想要显影的部位与显影液接触的方法即可,可以使用喷淋法、喷雾法、浸渍法等公知的方法。
[0299]
作为上述显影工序的实施时机,只要是上述固化工序后即可。
[0300]
上述后烘烤工序中的加热条件只要是能够提高通过固化工序而得到的固化物的强度等的条件即可,例如可以设定为200℃以上且250℃以下且20分钟~90分钟。
[0301]
作为上述预烘烤工序中的加热条件,只要是能够除去组合物中的溶剂的条件即可,例如可以设定为70℃以上且150℃以下且30秒~300秒钟。
[0302]
作为在上述形成涂膜的工序中涂布组合物的方法,可以使用旋转涂布机、辊涂机、棒涂机、模涂机、帘式涂布机、各种印刷、浸渍等公知的方法。
[0303]
上述涂膜可以形成于基材上。
[0304]
作为上述基材,可以根据固化物的用途等而适当设定,可列举出包含钠玻璃、石英玻璃、半导体基板、布线基板、金属、纸、塑料等的基材。
[0305]
此外,上述固化物可以在基材上形成后从基材剥离而使用,也可以从基材转印到其他的被粘物而使用。
[0306]
3.其他
[0307]
关于通过上述制造方法而制造的固化物及用途等,与上述“c.固化物”的项中记载的内容同样。
[0308]
本发明并不限定于上述实施方式。上述实施方式为例示,具有与本发明的权利要求书中记载的技术思想实质上同一构成、发挥同样的作用效果的方式不管是任何方式,都包含在本发明的技术范围内。
[0309]
实施例
[0310]
以下,列举出实施例及比较例对本发明更详细地进行说明,但本发明并不限定于这些实施例等。
[0311]
[制造例1~7]
[0312]
通过国际公开第2015/152153号中记载的方法,作为化合物a合成了在下文中所示的化合物no.1、no.3、no.5、no.71、no.73、no.77及no.131。将1h-nmr测定结果示于表1中。
[0313]
[化学式12]
[0314][0315]
表1
[0316][0317]
[制造例8~62]
[0318]
通过国际公开第2015/152153号中记载的方法,作为化合物a合成了下文中所示的化合物a-1~a-55。将1h-nmr测定结果示于表2中。
[0319]
[化学式13]
[0320][0321]
[化学式14]
[0322][0323]
[化学式15]
[0324][0325]
[化学式16]
[0326][0327]
[化学式17]
[0328][0329]
表2
[0330][0331]
[制造例63]蓝色颜料分散液的制造
[0332]
将作为分散剂的disper byk-161(12.5质量份;byk-chemie japan制)及作为着色
剂的颜料蓝15:6(15质量份)使用珠磨机分散到pgmea(72.5质量份)中而制造了蓝色颜料分散液。
[0333]
[实施例1~67、比较例1~8]
[0334]
对于制造例1~62中制造的化合物a,按照成为表4~6中所示的配方的方式进行酸成分的调整,制备了自由基聚合引发剂。酸成分的含量通过离子色谱法来定量。
[0335]
1.化合物a的保存稳定性评价
[0336]
将实施例及比较例中制备的自由基聚合引发剂与空气一起密封到螺旋管中,然后在60℃下保管1周,通过高效液相色谱法来分析保管前后的纯度,从而算出分解率,通过下述基准来评价稳定性。将结果示于表4~6中。
[0337]
+:分解率低于1%
[0338]
-:分解率为1%以上
[0339]
需要说明的是,分解率是(“保管前的自由基聚合引发剂中的化合物a的含有质量”-“保管后的自由基聚合引发剂中的化合物a的含有质量”)/“保管前的自由基聚合引发剂中的化合物a的含有质量
”×
100(%)所表示的值。
[0340]
分解率越小,可以判断保存稳定性越优异。
[0341]
2.感度的稳定性评价
[0342]
使用实施例及比较例中制备的自由基聚合引发剂,按照表3中所示的配方将各成分混合而制备组合物。表3的数值表示质量份。
[0343]
表中的各成分如下所述。
[0344]
a-1:实施例1~67、比较例1~8中制备的自由基聚合引发剂
[0345]
b-1:spc-3000(具有亲水性基的聚合物;昭和电工社制、固体成分42.7%、pgmea溶液)
[0346]
c-1:kayarad dpha(聚合性化合物(多官能丙烯酸酯);日本化药社制)
[0347]
d-1:蓝色颜料分散液(制造例9中制造的蓝色颜料分散液)
[0348]
e-1:kbe-403(偶联剂、信越化学株式会社制)
[0349]
f-1:丙二醇-1-单甲基醚-2-乙酸酯(溶剂)
[0350]
表3
[0351]
成分质量份a-11.9b-2100.0c-112.6d-1120.1e-11.7f-1186.0合计422.3
[0352]
在玻璃基板上旋涂各组合物,使用热板,在90℃下进行120秒钟预烘烤后,在23℃下进行60秒钟冷却。之后,使用超高压汞灯介由光掩模(掩模开口30μm)进行了曝光(曝光间隙为100μm、曝光量为40mj/cm2)。作为显影液使用0.04质量%koh水溶液进行显影后,充分进行水洗,使用洁净烘箱在230℃下进行20分钟后烘烤,使图案定影。用电子显微镜观察所
得到的图案,测定与掩模开口相对应的部分的线宽。
[0353]
对于使用刚制备后的自由基聚合引发剂的情况、和使用与空气一起密封到螺旋管中后在60℃下保管1周后的自由基聚合引发剂的情况,通过下述基准来进行感度评价。将结果示于表2~4中。
[0354]
+:在保管前后没有差异(线宽的变化率为
±
10%以下)
[0355]-:在保管前后有差异(线宽的变化率超过
±
10%)
[0356]
需要说明的是,保管前后的线宽的变化越小,则可以判断感度的稳定性越优异。
[0357]
此外,确认实施例的自由基聚合引发剂在与评价中使用的组合物的各成分混合时能够容易地均匀溶解或均匀分散。
[0358]
3.水分量测定
[0359]
使用卡尔
·
费休水分计来测定实施例及比较例中制备的自由基聚合引发剂中的水分量(质量%)。将结果示于表4~6中。
[0360]
需要说明的是,表中记载的水分量(质量%)表示化合物a、酸成分及水的合计中的水的含量。
[0361]
4.化合物a的溶解性评价
[0362]
量取0.4g实施例及比较例中制备的自由基聚合引发剂、9.6g的pgmea到螺旋管中,在温度为25度的环境下,一边用搅拌器搅拌一边通过目视来确认溶解的时间,通过下述基准来评价溶解性。将结果示于表7中。
[0363]
+:溶解时间低于20秒
[0364]
-:溶解时间为20秒以上
[0365]
表4
[0366][0367]
表5
[0368][0369]
表6
[0370][0371]
表7
[0372][0373]
由表4~7中所示的结果可以确认:实施例的自由基聚合引发剂的感度的稳定性优异。此外,实施例的自由基聚合引发剂的保存稳定性也优异,在溶剂中的溶解性也良好。
[0374]
产业上的可利用性
[0375]
根据本发明,能够提供感度的稳定性优异的自由基聚合引发剂。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1