一种丙泊酚传感器的制作方法
一种丙泊酚传感器
1.本发明一般地涉及检测和定量溶液中的静脉麻醉剂丙泊酚的方法、系统和装置。
2.丙泊酚(2,6-二异丙基苯酚)是一种用于诱导和维持麻醉的静脉药物。
[0003][0004]
它具有良好的特性,包括快速诱导和较短的半衰期;因此,在近30年来,它一直是最常用的静脉麻醉剂。
[0005]
全身麻醉中最常见的做法是在诱导阶段使用静脉麻醉剂,诸如丙泊酚,而在维持阶段使用挥发性麻醉剂。然而,也有可能在诱导和维持阶段都使用丙泊酚,这个过程被称为全静脉麻醉(tiva)。越来越多的证据表明,与传统的挥发性麻醉相比,tiva的优势包括:减少短期副作用,减少认知影响,有可能提高癌症病人的长期生存率,并且大大减少对环境的影响。
[0006]
尽管有这些众多的优势,但传统的挥发性麻醉仍然占了给予全身麻醉的绝大部分。更多利用tiva的主要障碍是缺乏合适的方法对接受麻醉的病人的血液丙泊酚浓度进行连续、实时监测。
[0007]
检测和定量丙泊酚的成熟技术包括高效液相色谱法(hplc),它与各种测量技术结合使用,其中最常见的是荧光检测。尽管hplc可能是一种普遍的技术,但由于它依赖于笨重和昂贵的设备,因此不太适合床旁应用。此外,hplc只提供不连续的,而不是连续的测量。它还需要复杂而耗时的样品预处理方法。
[0008]
质谱法是检测和定量生物样品中丙泊酚的另一种常用技术,与气相色谱法或液相色谱法结合使用。就hplc而言,在分析全血、血清或血浆中的丙泊酚时,要通过溶剂或固相萃取从样品中提取丙泊酚。就hplc而言,质谱技术的主要缺点是需要昂贵和笨重的设备,而且缺乏连续监测的能力。一个特别的缺点是需要漫长的分析和样品准备过程。
[0009]
已经对监测呼出气体中的丙泊酚进行了研究。然而,由于对血液丙泊酚浓度和呼出气体浓度之间的关系并不完全了解,目前还不清楚这种方法是否适用于病人监测。
[0010]
有报道称在尿液中检测出丙泊酚。然而,由于从给药到药物或其代谢物出现在尿液中的时间差很大,这种方法将不适用于全麻期间的实时丙泊酚监测。全血、血清或血浆代表了这种应用中最实用的生物体液。
[0011]
本发明旨在为丙泊酚的检测和/或定量提供改进或与之相关的改进。
[0012]
本发明的各方面和实施例涉及丙泊酚监测。
[0013]
一些方面和实施例提供、涉及或包括丙泊酚的例如使用血气分析器的不连续测量。
[0014]
一些方面和实施例提供、涉及或包括丙泊酚的直接测量,例如直接电化学测量。
[0015]
一些方面和实施例提供、涉及或包括实时丙泊酚监测。
[0016]
一些方面和实施例提供、涉及或包括床旁丙泊酚监测。
[0017]
本发明的一个方面提供了一种实时的、床旁、血液丙泊酚浓度测量传感器和/或测量系统。
[0018]
一些方面和实施例涉及对全身麻醉病人的丙泊酚血液浓度的床旁监测。这可以包括使用血气分析仪。
[0019]
一些方面和实施例提供、涉及或包括固相检测技术。
[0020]
一些方面和实施例涉及一种溶液相丙泊酚检测技术及其在实时丙泊酚监测中的应用。
[0021]
全身麻醉期间提供血液丙泊酚浓度的床旁和/或实时监测的目的对任何潜在的丙泊酚传感技术提出了一些要求。例如,任何方法都必须能够在足够窄的时间窗口内返回结果,以提供对麻醉师或其他医疗专业人员有实际用途的信息。这是诸如hplc和质谱等方法的一个主要原因,这些方法最好情况下产生结果的时间是大约几十分钟,对这种应用的效用有限。由于同样的原因,任何需要进行非简单的样品预处理的方法都可能不适合,因此,能够在生理条件下运行的传感器比那些不能够在生理条件下运行的传感器(例如基于吉布斯反应的光学技术,这需要碱性条件)更适合。
[0022]
为了用于外科手术场景中的病人监测,任何传感器系统都需要能够在外科手术,可能是8小时或更长时间的持续时间中产生稳定的结果。此外,已经证明丙泊酚会随着时间的推移在血浆和血细胞膜之间缓慢地重新分布,这意味着收集和测量样品之间的时间需要严格控制。照此,任何监测丙泊酚的技术(包括实时监测)都必须适合于自动化,只需进行最低限度的样品处理。
[0023]
可以经由丙泊酚的氧化作用通过电化学方法检测丙泊酚。电化学方法由于它们高灵敏度和易于自动化的潜力而具有吸引力,但在特异性方面具有重大挑战。此外,氧化反应会产生自由基,这些自由基会发生进一步的反应,在电极表面产生聚合物分子,这个过程被称为电聚合。这些聚合物不溶于水且不导电,因此会导致严重的电极污染(也被称为电极钝化)。因此,直接对丙泊酚进行电化学检测目前在实际应用中并不实用,因为任何丙泊酚传感器都需要在长达数小时的时间内产生稳定的电流。
[0024]
在全身麻醉期间,丙泊酚很可能与其他药物共同使用,因此,任何丙泊酚传感器都必须具有足够的特异性。特异性是电化学方法的一个特殊挑战,因为丙泊酚被电化学氧化的电位窗口与许多潜在的干扰化合物的电活性窗口相对应。
[0025]
该传感器可以是酶促的。
[0026]
本发明还提供了一种用于检测丙泊酚的基于酶的电化学传感器。
[0027]
可以提供一种基于酶的丙泊酚传感器,其例如通过将丙泊酚转化为能够经由简单电化学进行检测的醌/醌醇氧化还原对,避免了电极污染的问题。
[0028]
传感器可以包括电池,例如电极电池。
[0029]
例如,一些实施例可以包括直接固定在电极上的酶。
[0030]
例如,一些实施例包括工作电极、对电极和参比电极。
[0031]
例如,电极可以包括双电极电池(具有一个工作电极和组合的参比/对电极)或三
电极电池(具有工作电极、对电极和参比电极)。
[0032]
例如,电池可以有两种或三种类型的电极,例如工作电极、组合的参比和对电极、参比电极或对电极。在电池中,每种类型的电极可以有多个。
[0033]
一些实施例可以在单个电池内包括多个工作电极。
[0034]
一些实施例可以包括传感器设备上的多个电池。
[0035]
一些实施例可以包括两个、三个或更多的电极电池。
[0036]
传感器可以包括多个电极电池。这些电池可以是“用电线连接的”或以其他方式连接在一起的,也可以是独立的。
[0037]
对电极可以由包括但不限于碳、金、铂、银或银/氯化银等材料制成。
[0038]
参比电极可以由包括但不限于银和银/氯化银的材料制成。
[0039]
工作电极可以由包括但不限于碳、金、铂、银、铜、铝或氧化铟锡等材料制成。例如,工作电极可以不经处理,或以如下方式用纳米材料进行功能化处理。
[0040]
例如,工作电极可以是宏观尺度(》100μm)、微观尺度(1-100μm)或纳米尺度(《1μm),并且可以包括单个电极或多个电极的阵列,或者要么阵列的所有成员共享同一个对电极,要么阵列的每个成员都有一个相关联的独立对电极。
[0041]
电极可以使用任何适当的技术制造,诸如丝网印刷或精密加工技术,包括但不限于光刻法、蚀刻技术或化学气相沉积。
[0042]
电极可以是平面的,或采取纳米条状电极的形式,利用可以由包括但不限于:二氧化硅、氮化硅或聚对二甲基苯等材料制作的钝化层。
[0043]
电极可以包括多孔熔块材料,如碳质或类似材料。这些电极可以作为库仑电化学电池起作用。
[0044]
一些方面和实施例使用“传感器冗余”来提供更可靠的传感器。可以取样和比较来自独立电极的信号。异常值被丢弃,以确保一个电极的故障不会过度影响结果。
[0045]
关于电极功能化,例如,可以将薄膜直接沉积到工作电极表面。可替换地,在沉积之前,表面可以用纳米材料进行功能化,以提高传感器的性能。
[0046]
工作电极能够用单层纳米颗粒进行功能化,示例包括但不限于:氧化铁纳米颗粒、金纳米颗粒、银纳米颗粒、铂纳米颗粒、铜纳米颗粒、氧化锌纳米颗粒、氧化镍纳米颗粒、氧化铜纳米颗粒、碳纳米颗粒、铜纳米线、碳纳米管或石墨烯纳米片。
[0047]
工作电极可以用两层或多层不同的纳米颗粒进行功能化,示例包括但不限于:氧化铁纳米颗粒、金纳米颗粒、银纳米颗粒、铂纳米颗粒、铜纳米颗粒、氧化锌纳米颗粒、氧化镍纳米颗粒、氧化铜纳米颗粒、碳纳米颗粒、铜纳米线、碳纳米管或石墨烯纳米片。
[0048]
工作电极可以用单层纳米材料复合材料进行功能化,示例包括但不限于:用金属纳米颗粒(潜在的金属包括但不限于金、银、铂或其合金)功能化的碳纳米管,或以下两种或多种材料的任何组合:碳纳米管、石墨烯纳米片、金纳米颗粒、银纳米颗粒、铂纳米颗粒、铜纳米颗粒、氧化锌纳米颗粒、氧化镍纳米颗粒、氧化铜纳米颗粒或铜纳米线。
[0049]
工作电极可以通过等离子体增强的化学气相沉积法用垂直排列的碳纳米管进行功能化。然后这些纳米管可以被封装在绝缘材料诸如环氧树脂或二氧化硅中,以产生纳米电极阵列。
[0050]
传感器可以基于细胞色素p450酶组的一个或多个成员。
[0051]
细胞色素p450(cytochromes p450)是一组亚铁血红素—硫醇盐单氧酶。在肝微粒体中,这个酶参与nadph依赖的电子传递途径。
[0052]
在一个实施例中,提供了一种基于酶细胞色素p450 2b6的电化学丙泊酚传感器。细胞色素p450 2b6属于一组肝脏药物代谢细胞色素。
[0053]
传感器可以基于电极,诸如丝网印刷电极。
[0054]
在一个实施例中,表达酶细胞色素p450 2b6的失活酵母细胞与金纳米颗粒一起被固定在丝网印刷电极的表面上的壳聚糖膜内。在辅因子nadp
+
的存在下,该酶将丙泊酚转化为能够使用简单的电化学进行检测和定量的醌/醌醇氧化还原对。这种方法避免了电化学丙泊酚传感器中普遍存在的电极污染问题。
[0055]
目前已知人类有18个cypp450的超级家族,43个亚家族,包含57个基因和59个假基因。这些酶主要在肝脏中表达,负责异物代谢。丙泊酚的芳香羟基化主要由cyp2c9和cyp2b6介导,也有研究提出了cyp2a6、cyp2c8、cyp2c18、cyp2c19和cyp1a2等其他异构体。90%的丙泊酚在肝脏中代谢(smits,annaert and allegaert,2017)。
[0056]
cyp2b6和cyp2c9多态性已经显示出对前药和个体变量的显著代谢作用。cyp2b6*6等位基因和cyp2c9*2等位基因与ugt1a9和ugt1a6。
[0057]
一种或多种酶异构体(例如cyp2c9和cyp2b6)可以独立使用或一起使用,即如同在人类肝脏内可能出现的情况。这种酶元素的组合可以例如形成一种三明治方法。
[0058]
在一些实施例中,传感器将电化学传感、cyp p450和纳米材料结合起来。
[0059]
cyp酶缺乏特异性,有可能造成问题。然而,2b6是一种不混杂的酶。此外,在一些实施例中,2b6的作用不是直接测量的;因此,潜在的干扰化合物是该酶的底物是不够的
‑‑
它必须被转化为电化学活性分子。此外,任何潜在的干扰物必须在被测量的电位下或附近具有电化学活性,才能引起任何问题(一个恰当示例是布洛芬,它含有苯环,但不是2b6的底物,但是是一个更高的电位下具有电化学活性,因此不会引起问题)。最后,任何潜在的干扰物必须以足够高的数量存在,才能真正造成问题。例如,吗啡在某些实施例中测量的电位下实际上是有电化学活性的,但它与丙泊酚的相对浓度意味着它不能被检测到,所以这不是问题。
[0060]
一些方面和实施例是基于这样一个原则:它们不使用电极和cyp酶之间的直接电子转移。相反,通过使用间接方法(经由nadph)和电化学检测反应产物,本发明可以避免cyp酶的非特异性引起的潜在问题。
[0061]
一些实施例可以包括传感器调节器。例如,变量例如ph值和温度可以作为传感器调节器。据报道,丙泊酚在苯环上发生羟基取代物(-oh),然后当ph值为酸性(《6.5)且溶液中带正电荷时,丙泊酚会发生解离。
[0062]
一些实施例使用重组人cyp以及在失活的、透性化的酵母细胞内表达的p450。例如,cypexpresstm,它是一种由特定的、未修改的重组人cyp、p450氧化还原酶辅因子和抗氧化剂组成的被封装在半渗透性的外壳中的产品。
[0063]
一些实施例使用重组人酶。其他实施例使用合成替代品。
[0064]
一些实施例使用:酵母细胞和/或哺乳动物细胞和/或细菌细胞和/或合成细胞。
[0065]
包括细胞色素p450 2b6(cyp2b6)、cyp2c9、cyp2c19或cyp2e1的酶可以在失活的、透性化的酵母细胞内表达。
[0066]
cyp酶活性需要辅酶诸如细胞色素p450还原酶,以及辅因子诸如nadh或nadph的存在,以帮助电子转移。这一直是开发cyp酶生物传感器的障碍,直到开发出将电子直接传递到含有铁原卟啉ix(haem)的酶的活性部位的“无媒介物”或直接生物传感器。直接将酶固定在电极表面已经被证明可以直接测量cyp的活性。一系列的电极表面材料已经被报道为cyp生物传感器的基底,包括金、石墨和氧化铟锡(schneider,2013)。最近,已经报道应用纳米结构诸如金纳米球、碳纳米管和石墨烯,以通过增加电荷转移来提高酶生物传感器的灵敏度(preethichandra,2019)。以前的工作都没有研究过应用金属氧化物纳米颗粒来开发直接生物传感器,也没有用这种方法评估cyp 2b6的使用。
[0067]
目前还没有关于使用cyp2b6或任何其他cyp酶检测丙泊酚的报道。
[0068]
一些实施例是基于在电极表面固定cyp2b6酶,以提供灵敏、实时的丙泊酚测量。
[0069]
一些实施例使用表达cyp2b6酶的细胞。
[0070]
例如,可以使用表达单一cyp酶的酵母细胞、多种不同类型的表达不同cyp酶的酵母细胞的混合物,
‑‑
或表达多种cyp酶的酵母细胞来制备传感器。
[0071]
酵母细胞可以被固定在聚合物薄膜中的工作电极表面上。这个膜可以由包括但不限于以下项的聚合物制成:壳聚糖、聚丙烯酰胺、聚吡咯、nafion或pedot。
[0072]
壳聚糖可以被选作固定化的方法,因为它数量丰富,具有生物相容性,并且具有高度的多孔性。
[0073]
添加金纳米颗粒可以用于进一步提高酶的稳定性。
[0074]
为了改善薄膜的传感特性,可以将纳米颗粒与酵母细胞一起纳入其中。这种纳米颗粒的示例包括但不限于:金纳米颗粒、银纳米颗粒、铂纳米颗粒、铜纳米颗粒、氧化锌纳米颗粒、氧化镍纳米颗粒、氧化铜纳米颗粒、碳纳米颗粒、碳纳米管、石墨烯纳米片,或其任何组合。
[0075]
该薄膜也可以涂覆有单层或多层的聚合膜材料。这类材料的示例包括但不限于:聚乙烯、nafion、特氟龙和纤维素。
[0076]
根据本发明形成的传感器可以证明以下一项或多项:
[0077]-检测极限为100ng/ml,低至1ng/ml、0.1ng/ml或0.01ng/ml(例如49ng/ml)
[0078]-线性范围为0-1.4μg/ml
[0079]-在一分钟内对丙泊酚浓度的变化做出反应。
[0080]
另一个方面提供了一种避免了电极污染的问题的基于酶的电化学丙泊酚传感器。
[0081]
本发明还提供了一种用于实时监测全身麻醉期间的血液丙泊酚浓度的溶液相丙泊酚检测系统,其包括实时的、床旁、血液丙泊酚浓度测量传感器和分析物回收系统,允许连续、实时监测丙泊酚而无需抽血。
[0082]
分析物回收系统可以包括分子交换装置,诸如微透析探针。
[0083]
一些实施例利用微透析作为取样方法,因为它能够自动、连续,并且通过适当的传感器,允许实时在线监测。此外,这种技术涉及到将关注的分析物(例如丙泊酚)沿着浓度梯度从血液到由薄的半透膜隔开的灌注液,意味着只对药物的游离部分进行采样。这使得它更适用于监测药理相关的药物浓度。因此,这对分析方法提出了更高的要求,因为通常只有药物总浓度的2%(游离部分)可供测量。因此,同等的分析范围对于麻醉来说是0.04-0.1mg/l,对于镇静来说是0.01-0.3mg/l,即假设使用微透析法的药物回收效率为100%,则
范围为0.01-0.1mg/l,或10-100μg/l,(ng/ml)。然而,由于监测的目标是实时的,所以需要高的微透析灌注流速,这典型地意味着较低的回收率,并不是不常见的1-10%,意味着目标范围可能低至0.1-1μg/l(ng/ml)。
[0084]
一些实施例提供或涉及一种能够被用于基于微透析的采样系统的选择性丙泊酚生物传感器。
[0085]
另一个方面提供了一种丙泊酚生物传感器。还提供了一种包括这种生物传感器的床旁、实时血液丙泊酚浓度测量传感器。
[0086]
传感器可以被集成到技术中,以实现自动和连续测量。
[0087]
例如,丙泊酚传感器可以以两种方式使用:作为连接到微透析设备的在线传感器(如已经讨论过的);或作为独立的传感器,包括在生化分析仪诸如血气分析仪中。
[0088]
在第一种方法中,即在线传感器,在细胞内排列电极可能是有利的,以这种方式在以连续流动的方式使用时提高性能。参比电极和/或对电极可以与流动方向对齐。
[0089]
传感器可以通过采用任何适当的电化学测量技术来检测分析物,包括但不限于:安培法、循环伏安法、微分脉冲伏安法、方波伏安法和库仑法。
[0090]
在一些实施例中,提供了一种通过将丙泊酚转化为能够经由简单电化学检测的醌/醌醇氧化还原对,避免电极污染问题的基于酶的丙泊酚传感器。
[0091]
例如,该传感器可以在大约60秒内对丙泊酚浓度的变化作出反应,其检测极限约为49ng/ml,线性响应约为0至1.4μg/ml。
[0092]
根据本发明的原理形成的传感器、方法和系统能够提出一个为全身麻醉病人提供有效的床旁、实时监测丙泊酚的血液浓度的装置的重要的步骤。
[0093]
另一个方面提供了一种基于细胞色素p450 2b6酶的电化学丙泊酚传感器。
[0094]
例如,该酶可以在失活的酵母细胞(或本文中所述的其他细胞)内表达。
[0095]
在一些实施例中,例如,酵母细胞依次被固定在丝网印刷电极的表面上的含有例如金纳米颗粒的壳聚糖薄膜内。
[0096]
传感器中电化学反应的顺序可以是:还原发生在氧化之前。
[0097]
该传感器可以包括测量2,6-二异丙基醌还原电流的单传感器。
[0098]
一些实施例使用两个传感器,相对于灌注液的流动顺序,第一个测量2,6-二异丙基醌的还原电流,第二个测量2,6-二异丙基醌醇的氧化电流。
[0099]
连续的传感器可以在单个设备上共存,或在依次的两个独立的设备上。
[0100]
本发明的一个实施例提供了一种基于被固定在用碳纳米管/氧化石墨烯/氧化铁纳米颗粒纳米复合材料功能化的石墨丝网印刷电极的壳聚糖膜内的表达细胞色素p450 2b6的失活酵母细胞的丙泊酚传感器。在相关辅因子的存在下,该酶催化丙泊酚转化为醌/醌醇氧化还原对,允许对丙泊酚的简单电化学检测,而不会造成电极污染。这种传感器的检测极限为7ng/ml,能够检测血清类溶液中的丙泊酚,并且在丙泊酚的治疗范围内表现出线性响应。该传感器已经被证明对一些常见的围手术期药物具有良好的选择性,并且被表明在储存至少一周后仍然稳定。
[0101]
下面通过举例的方式,在以下编号的段落中列出了另外的方面和实施例。
[0102]
1.一种基于酶的电化学丙泊酚传感器,该传感器是基于细胞色素p450 2b6酶的。
[0103]
2.如段落1中所述的传感器,其中该传感器是基于电极的。
[0104]
3.如段落2中所述的传感器,其中该传感器是基于丝网印刷电极的。
[0105]
4.如任一前述段落中所述的传感器,其包括表达细胞色素p450 2b6的失活的透性化酵母细胞。
[0106]
5.如任一前述段落中所述的传感器,其包括与金纳米颗粒一起被固定在丝网印刷电极的表面上的壳聚糖膜内的表达酶细胞色素p450 2b6酶的失活酵母细胞。
[0107]
6.如任一前述段落中所述的传感器,该传感器被集成到技术中,以实现自动和连续测量。
[0108]
7.一种包括如段落1至5中任一所述的传感器的床旁、实时血液丙泊酚浓度测量传感器。
[0109]
8.一种用于实时监测全身麻醉期间的血液丙泊酚浓度的溶液相丙泊酚检测系统,其包括实时的、床旁、血液丙泊酚浓度测量传感器和分析物回收系统,允许连续、实时监测丙泊酚而无需抽血。
[0110]
9.如段落8中所述的系统,其中该分析物回收系统包括分子交换装置。
[0111]
10.如段落8或9中所述的系统,其中该分析物回收系统包括微透析探针。
[0112]
11.一种血液丙泊酚浓度测量传感器。
[0113]
12.一种如段落1所述的传感器,其提供不连续的丙泊酚测量。
[0114]
13.如段落1或2中所述的传感器,其形成血气分析仪的一部分。
[0115]
14.一种如段落1所述的传感器,其提供丙泊酚的直接电化学测量。
[0116]
15.如任一前述段落中所述的传感器,其中该传感器是酶促的。
[0117]
16.一种用于检测丙泊酚的基于酶的电化学传感器。
[0118]
17.如任一前述段落中所述的传感器,其中该传感器是基于细胞色素p450酶组的一个或多个成员的。
[0119]
18.如任一前述段落中所述的传感器,其中该传感器是基于细胞色素p450 2b6酶的。
[0120]
19.如段落15至18中任一所述的传感器,其中酶的作用将丙泊酚转化为醌/醌醇氧化还原对。
[0121]
20.一种用于在全身麻醉期间对血液丙泊酚浓度进行床旁测量的丙泊酚检测系统,其包括具有固相、酶法丙泊酚浓度测量传感器的血气分析仪。
[0122]
21.一种用于实时监测全身麻醉期间的血液丙泊酚浓度的固相丙泊酚检测系统,其包括实时的、床旁、血液丙泊酚浓度测量传感器和分析物回收系统,允许连续、实时监测丙泊酚而无需抽血。
[0123]
22.如段落11中所述的系统,其中该分析物回收系统包括分子交换装置。
[0124]
23.如段落21或22中所述的系统,其中该分析物回收系统包括微透析探针。
[0125]
24.一种丙泊酚生物传感器。
[0126]
25.如任一前述段落中所述的传感器或系统,其包括工作电极、对电极和参比电极。
[0127]
26.如任一前述段落中所述的传感器或系统,其涉及具有氧化还原步骤的电化学反应,其中氧化发生在还原之前。
[0128]
27.一种基于细胞色素p450 2b6酶的电化学丙泊酚传感器。
[0129]
28.如段落27中所述的传感器,其中该酶在失活的酵母细胞内表达。
[0130]
29.如段落28中所述的传感器,其中酵母细胞依次被固定在丝网印刷电极表面上的含有金纳米颗粒的壳聚糖薄膜内。
[0131]
30.如段落27至29中任一所述的传感器,其中在电化学反应的顺序中,还原发生在氧化之前。
[0132]
31.如段落27至30中任一所述的传感器,其包括测量2,6-二异丙基醌还原电流的单传感器。
[0133]
32.如段落27至30中任一所述的传感器,其包括两个传感器,相对于灌注液的流动顺序,第一个测量2,6-二异丙基醌的还原电流,第二个测量2,6-二异丙基醌醇的氧化电流。
[0134]
33.如段落32中所述的传感器,其中顺序传感器共同位于单个设备上或依次位于两个独立的设备上。
[0135]
34.一种包括cyp酶的血液丙泊酚酶生物传感器,在电极和cyp酶之间不存在直接电子转移的情况下进行传感,使用经由nadph的间接方法,并且通过电化学检测反应产物。
[0136]
35.一种用于基于tiva麻醉的实时血液丙泊酚监测系统。
[0137]
36.一种用于基于tiva麻醉的血液丙泊酚监测系统。
[0138]
37.一种用于临床的实时、连续的丙泊酚检测器。
[0139]
本发明的不同方面和实施例可以单独使用或一起使用。
[0140]
所附独立权利要求和从属权利要求陈述了本发明的另外的特别和优选的方面。从属权利要求的特征可以适当与独立权利要求的特征结合,并且可以结合不同于权利要求中所陈述的那些特征。
[0141]
附图示出了本发明的方面和实施例的示例。
[0142]
在下面描述中,所有定向术语,例如上、下、前、后、径向、轴向,都与附图相关,并且不应被解释为对本发明或其与封闭件的连接的限制。
[0143]
下面充分详细地描述了示例实施例,以使本领域普通技术人员能够具化和实施本文中所描述的系统和过程。重要的是,实施例能够以许多替换的形式来提供,并且不应该被解释为受限于本文中所陈述的示例。
[0144]
因此,尽管实施例能够以各种方式进行修改和采取各种替换形式,但是其具体实施例在附图中示出并且作为示例在下文中进行了详细描述。这无意限制所公开的特定形式。相反,应包括落入所附权利要求范围内的所有修改、等同物和替代形式。在整个附图和适用地方的详细描述中,示例实施例的元件始终通过相同的附图标记来表示。
[0145]
本文中用于描述实施例的术语并不旨在限制范围。冠词“一”和“该”是具有一个指示物的单数形式,但是在本文中使用单数形式不应排除存在多个指示物。换言之,单数形式提及的元件可以有一个或多个,除非上下文另外明确指出。将进一步理解的是,当在本文中使用时,术语“包括”列举所阐明的特征、项目、步骤、操作、元件和/或部件的存在,但不排除一个或多个其他特征、项目、步骤、操作、元素、部件和/或其组的存在或添加。
[0146]
除非另有定义,否则本文所用的所有术语(包括技术术语和科学术语)都应按照本领域的惯例进行理解。还要理解的是,除非在本文中明确地定义,否则通用用法的术语也应按照相关领域的惯例进行理解,而不是理想化或过度形式化的含义。
[0147]
图1示出了丙泊酚和磷丙泊酚的代谢途径。虚线箭头代表次要途径,两种代谢物都
能够进行葡萄糖醛酸苷和硫酸盐的共轭。sult:磺基转移酶;ugt:udp:葡萄糖醛酸转移酶;aldh:醛脱氢酶;alp:碱性磷酸酶;nqo1:心肌黄酶;cyp:细胞色素p450。
[0148]
描述了一种基于细胞色素p450 2b6酶的电化学丙泊酚传感器。
[0149]
一些实施例将cyp2b6酶固定在电极表面,以提供灵敏、实时的丙泊酚测量。在氧气存在的情况下,丙泊酚发生羟基化反应,以形成通过两个单电子还原步骤在酶的活性部位催化的2,6-二异丙基-1,4-醌和2,6-二异丙基-1,4-醌醇的氧化还原对(图2-改编自shioya等人,2011)。酶活性将从电极上吸取电子,从而产生与丙泊酚浓度成比例的测量电流。因此,不需要辅因子。
[0150]
试图以这种方式将细胞色素p450 2b6固定在电极中,为此任何可归因于酶的电化学信号迅速减少,以至于它们不再能从噪声底线中辨别出来。最终得出结论,这是由于细胞色素p450 2b6固有的不稳定性造成的酶变性。为了提高酶的稳定性,尝试了许多不同的固定化技术,包括nhs/edc连接、重氮连接、多层膜、导电聚合物薄膜和壳聚糖薄膜,但都有些不成功。因此,间接检测可能比直接方法更受青睐。一种这样的间接方法利用cypexpress,即含有重组人cyp2b6的失活酵母细胞,这些细胞依次被固定在丝网印刷电极表面上的含有金纳米颗粒的壳聚糖薄膜内。在辅因子nadp
+
的存在下,该酶将丙泊酚转化为醌/醌醇氧化还原对。这种氧化还原对能够通过电化学方法检测,而不会导致电极污染,因此能够简单、直接和快速地测量丙泊酚的浓度。壳聚糖被选作固定化的方法,因为它数量丰富,具有生物相容性,并且具有高度的多孔性。添加金纳米颗粒可以用于进一步提高酶的稳定性(zhao,2011;gherardi,2019)。
[0151]
在一些实施例中,酶在失活酵母细胞内表达,失活酵母细胞依次被固定在丝网印刷电极表面上的含有金纳米颗粒的壳聚糖薄膜内。细胞色素p450 2b6是负责在人体内代谢丙泊酚的主要酶之一。在辅因子nadp
+
存在下,该酶会将丙泊酚转化为醌/醌醇氧化还原对(图3
‑‑
细胞色素p450 2b6将丙泊酚转化为醌/醌醇氧化还原对的反应机制。nadp
+
作为酶反应的电子源,电极用于检测反应产物。改编自shioya等人,2011)。nadp
+
作为电子源,允许酶催化丙泊酚的转化。与直接电化学氧化不同,以这种方式转化丙泊酚不会导致聚合,因此不会造成电极污染。由此产生的氧化还原对能够通过电化学方法检测,因此能够简单和快速地测量丙泊酚的浓度。壳聚糖被选作固定化的方法,因为它数量丰富,具有生物相容性和高度的多孔性。加入金纳米颗粒是为了帮助电极和失活的酵母细胞之间的电子转移。在这个实施例中,传感器在大约0-1.4μg/ml的范围内具有非限制性的线性反应,检测极限大约为49ng/ml。
[0152]
在一个实施例中,cypexpress/金纳米颗粒/壳聚糖薄膜的制备方法是将cypexpress悬浮液(25mg/ml的磷酸盐缓冲液,ph为7)、金纳米颗粒悬浮液和1%的壳聚糖溶液(1%的乙酸)按体积比1:1:2混合,滴涂1μl到电极表面并且使其干燥。使用的电极是由直径1mm的石墨工作电极、石墨对电极和银/氯化银假参比电极组成的丝网印刷的三电极电池。
[0153]
在一些实施例中,电化学反应的顺序(即先正后负)对传感器是很重要的,即已经发现还原必须发生在氧化之前。设备可以包括测量2,6-二异丙基醌的还原电流的单传感器或相对于灌注液的流动顺序,第一个测量2,6-二异丙基醌的还原电流,第二个测量2,6-二异丙基醌醇的氧化电流的两个传感器。这些连续传感器可以在单个设备上共存,或依次在
两个独立的设备上。顺序测量可以提供对干扰化合物更好的区分,因为虽然其他化合物在两个电压(正或负)中的一个下可能具有电活性,但它们在两个电压下都具有电活性的可能性较小。此外,在氧化峰的负电压附近的干扰化合物通常较少。
[0154]
材料和方法
[0155]
材料
[0156]
所有材料均由sigma-aldrich提供并且按规定使用。将β-烟酰胺腺嘌呤二核苷酸磷酸钠盐水合物(nadp
+
)和d-葡萄糖6-磷酸二钾盐水合物(g6p)溶于10mm磷酸盐缓冲盐水(pbs),ph为7.4,制成溶液,其中各自的浓度为50μg/ml。除非另有说明,这是在章节2.4中描述的电化学测量的测试溶液。2,6-二异丙基苯酚(97%)在二甲亚砜(99%)中稀释,制成10mm的储备溶液。进一步用nadp
+
/g6p溶液稀释这个储备溶液,产生如本文所述描述的测试所需的不同浓度的丙泊酚溶液。
[0157]
仪器设备
[0158]
这些实验中使用的丝网印刷电极是从bvt技术公司购买的。它们构成由直径1mm的石墨工作电极、石墨对电极和银/氯化银(ag/agcl)假参比电极组成的三电极电池。所有的测量都是使用palmsens emstat3恒电位仪进行的。
[0159]
电极制备
[0160]
通过将电极浸泡在10mm k3[fe(cn)6],1m kno3溶液中进行预处理,并且在-0.6和+0.8v之间以100mv/s的扫描速率进行循环伏安测试,共进行了10次循环。
[0161]
金纳米颗粒是使用标准的柠檬酸钠还原技术生产的。简而言之,将10mg氯化金水合物(haucl4)(99.995%)溶于20ml去离子水,并且在磁力搅拌下达到沸点。将二水合柠檬酸三钠(99%)溶于去离子水,制成2.5%(w/v)的溶液,并将1ml的这个溶液加入到haucl4溶液中,将混合物在沸点保持5-10分钟,直到其颜色变为深红色,然后让其冷却到室温。
[0162]
cypexpress 2b6(失活的、透性化的酵母,表达细胞色素p450 2b6)以25mg/ml的浓度悬浮于磷酸盐缓冲液(ph为7)中。这个悬浮液与金纳米颗粒溶液和1%(w/v)的壳聚糖溶液(1%的乙酸)以体积比1:1:2进行混合。将1μl的这个混合物滴涂在丝网印刷电极的工作电极上,并且在4℃下晾干。干燥后,将电极在室温下浸泡在10mm的pbs中30分钟,然后重新干燥并且储存在4℃直到使用。
[0163]
电化学测量
[0164]
循环伏安法测量是通过在功能化电极上沉积50μl的不同浓度的丙泊酚溶液,并且以100mv/s的速率在-0.8和+1.0v之间循环使用。
[0165]
将功能化电极浸入20ml的50μg/ml的nadp
+
和g6p溶液(10mm的pbs)中,并且在+0.5v时测量电流,从而进行计时电流法测量。用磁力搅拌器搅拌该溶液,每隔一定时间向该溶液注入60μl的1mm的丙泊酚溶液。
[0166]
对照测量是通过在不含nadp
+
或g6p的pbs溶液中如上所述进行计时电流法测量,并且每隔一定时间注入20μl的1mm丙泊酚溶液。这些实验使用同一电极进行了三次。在每次运行之间,用10mm的pbs冲洗电极,干燥并且在4℃下储存过夜。
[0167]
结果和讨论
[0168]
不同丙泊酚浓度的循环伏安法(图4-丙泊酚浓度溶液的循环伏安图:a)0.18,b)0.89,c)1.78,d)2.67,e)3.57和f)4.47μg/ml,所有溶液都含有50μg/ml的nadp
+
和g6p,10mm
的pbs。扫描速率为100mv/s。电位是相对于ag/agcl。)示出了大约在+0.6v和-0.25v的浓度依赖性峰值。这种行为是对醌/醌醇氧化还原对的预期(quan等人,2007),峰值分别对应于2,6-二异丙基醌的还原和2,6-二异丙基醌醇的氧化。这告诉我们,酵母细胞内的酶正在按预期将丙泊酚转化为其产物。
[0169]
已经发现,醌醇的氧化只发生在醌的还原之后。仅仅在-0.2v下进行监测将不会提供任何信号。
[0170]
将传感器浸泡在含有50μg/ml的nadp
+
和葡萄糖-6-磷酸的10mm pbs溶液并且在+0.6v下执行安培法以评估传感器的性能。每隔一定时间用1mm的丙泊酚溶液(10mm pbs,10%二甲亚砜)对该溶液进行加注。
[0171]
图5
–
a:连续注入丙泊酚溶液后,功能化电极的计时电流反应。电位是+0.5v对ag/agcl。溶液为10mm pbs,含有50μg/ml nadp
+
和50μg/ml g6p。b:平台电流的平均值对丙泊酚浓度。误差条代表三个标准差。已经应用了基线校正。
[0172]
计时电流法测量显示,每次加入丙泊酚溶液后,电流明显增加(图5a)。反应很快速,在大约60秒内达到平台,并且在整个实验中保持稳定。将平均平台电流相对丙泊酚浓度作点图(图5b)示出,该传感器在0.25-4μg/ml的治疗范围内对不同的丙泊酚浓度产生明显的反应(langmaier等人,2011)。反应是线性的
‑‑
在0和1.4μg/ml之间,灵敏度是4.2na/μg/ml/mm2,检测限是49ng/ml,远低于治疗范围的下限。
[0173]
检出限(lod)使用下式计算:lod=(3.3
×
σ
low
)/梯度,其中σ
low
是低丙泊酚浓度下的标准偏差。
[0174]
图6a:在没有nadp
+
和g6p的情况下,连续几天在同一电极的第一、第二和第三次重复中,电极对连续注入丙泊酚溶液的计时电流响应。电位是+0.5v对ag/agcl,溶液是10mm的pbs。b:平台电流的平均值对丙泊酚浓度。误差条代表三个标准差。
[0175]
图6a示出了在没有nadp
+
和g6p的情况下进行的计时电流法测量的结果。加入丙泊酚后电流的增加是丙泊酚直接电化学氧化的结果,在没有nadp
+
和g6p的情况下,丙泊酚不会被酶所转化。在第一次运行中可以看到,在第四次注入丙泊酚后(相当于大约0.7μg/ml的浓度),有一个明显的电流随时间下降的趋势,这表明电极污染了。
[0176]
这在图6b中更加明显,可以看到电流响应在大约1μg/ml的丙泊酚时趋于平稳,一个在如上所述的传感器的线性范围内很舒适的值。在连续几天使用同一电极执行的重复测量示出了类似的响应,但灵敏度明显降低。电极的第三次运行的灵敏度是第一次运行的22%。这些结果明显证明了丙泊酚氧化造成的电极污染,而在nadp
+
和g6p的存在下,丙泊酚被酶转化,则不会发生污染。在添加nadp
+
和g6p的情况下执行的类似实验结果是,传感器在第三次运行时显示的灵敏度大约为第一次运行时的95%(未示出)。
[0177]
为了提高传感器的性能,电极表面可以用纳米复合材料进行功能化。已经研究了各种材料,但最有希望的用金属氧化物纳米颗粒,是特别是氧化铜纳米颗粒(cuonp)和氧化铁纳米颗粒(feonp)修饰的结合碳纳米管(cnt)和氧化石墨烯(go)的纳米复合材料。
[0178]
图7a示出了根据本发明形成的并且包括工作电极、对电极和参比电极的传感器。
[0179]
如图7b所示,参比电极和/或对电极可以与流动方向对齐。
[0180]
图8至图17示出了本发明的另外的实施例。
[0181]
图8是用纳米复合材料对电极表面进行功能化的图解。
[0182]
平面碳电极具有包含金纳米颗粒和表达单一cyp酶的单一类型酵母细胞的薄膜。三电极电池具有宏观尺度工作电极。
[0183]
图9-平面金电极,用单层碳纳米管进行功能化,薄膜上含有表达单一cyp酶的单一类型的酵母细胞。三电极电池具有由微阵列组成的工作电极。
[0184]
图10-平面铂电极,用金纳米颗粒功能化的碳纳米管的复合层进行功能化处理,薄膜包含银纳米颗粒和两种类型的酵母细胞,每种细胞都表达一种cyp酶。双电极电池具有宏观尺度工作电极和组合的对/参比电极。
[0185]
图11-平面碳电极,用两层不同纳米材料进行功能化,薄膜上包含金纳米颗粒和表达多种cyp酶的单一类型的酵母细胞。三电极电池具有宏观尺度工作电极。
[0186]
图12-平面铂电极,用单层碳纳米管进行功能化,薄膜上含有氧化铜纳米颗粒和表达单一cyp酶的单一类型的酵母细胞。具有多个微尺度工作电极的多电极装置,每个电极都有表达不同cyp酶的酵母,每个电极都有相关联的对电极并且共享一个共同的参比电极(三电极电池)。
[0187]
图13-平面铂电极,用垂直排列的部分封装在环氧树脂中的碳纳米管进行功能化,以形成纳米电极阵列。薄膜包含金纳米颗粒和表达单一cyp酶的单一类型酵母细胞。三电极电池具有由纳米电极阵列组成的工作电极。
[0188]
图14-纳米条状电极,具有氮化硅钝化层,具有包含铂纳米颗粒和表达单一cyp酶的单一类型的酵母细胞的薄膜。具有纳米条状工作电极的三电极电池。
[0189]
图15-涂有碳纳米管导电网络和氮化硅钝化层的金纳米条状电极。薄膜包含金纳米颗粒和表达单一cyp酶的单一类型酵母细胞。具有纳米条状工作电极的三电极电池。
[0190]
图16-平面碳电极,具有包含金纳米颗粒和表达单一cyp酶的单一类型酵母细胞的薄膜。该薄膜上涂有纤维素膜。三电极电池具有宏观尺度工作电极。
[0191]
图17-平面碳电极,用单层碳纳米管进行功能化,薄膜上含有金纳米颗粒和表达单一cyp酶的单一类型的酵母细胞。该薄膜上涂布有由一层聚乙烯和一层nafion组成的双层膜。三电极电池具有宏观尺度工作电极。
[0192]
使用前面描述的相同的安培测量法来评估纳米复合材料功能化的传感器的性能。
[0193]
表1示出了每种变体纳米复合材料的灵敏度和检测限。
[0194]
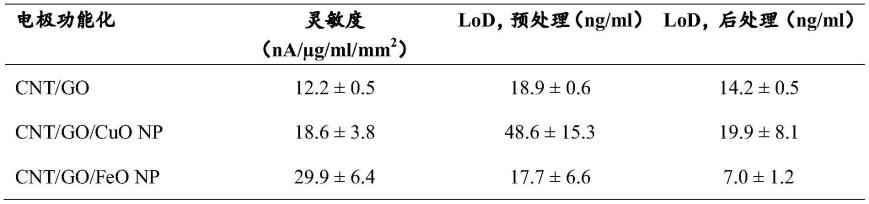
表1示出了cnt/go、cnt/go/cuonp和cnt/go/feonp电极的多次重复的平均灵敏度和检测限(lod)(每个示例显示在error!reference source not found.中)。正如已经讨论过的,使用金属氧化物纳米颗粒修饰的氧化石墨烯制备的电极与使用非修饰的氧化石墨烯制备的电极相比,显示出明显的灵敏度增加,其中feo纳米颗粒的改进最大。然而,cnt/go/cuonp的lod比cnt/go的lod要高,这一事实可以归因于噪声的增加。然而,cnt/go/feonp电极的lod是7.0
±
1.2,大约是cnt/go电极的一半,这是一个重大的改进。在以前的出版物[ref]中,表明了由本文中描述的在裸碳丝网印刷电极上的这种类型的酶薄膜组成的传感器的lod为49ng/ml。因此,可以看出,这些碳纳米复合材料功能化电极为丙泊酚的检测提供了显著的灵敏度改进,其中碳纳米管和氧化铁纳米颗粒修饰的氧化石墨烯的复合材料提供了最大的改进。
[0195][0196]
表1-用各种不同的纳米材料功能化的电极的灵敏度和检测限。
[0197][0198]
表2-用纳米复合材料功能化的传感器的灵敏度和检测限。
[0199]
与非功能化电极相比,纳米复合材料功能化的电极呈现出明显的改善,其中cnt/go/feonp复合材料的改善最大。这种性能的改善是增加表面积、改善电子转移和纳米复合材料的催化作用的结合的结果。滑动平均滤波器(有十秒仓)被应用于电流响应,作为降低噪音的方法,为检测极限提供了额外的改善。
[0200]
图18:a)对于i)cnt/go,ii)cnt/go/cuonp,和iii)cnt/go/feonp功能化的传感器,传感器对连续注入丙泊酚溶液的安培响应,b)对产生的丙泊酚浓度的平台电流平均值。电位是+0.5v对丝网印刷ag/agcl。溶液为10mm pbs,含有50μg/ml nadp
+
和50μg/ml g6p。误差条代表三个标准差。已经应用了基线校正和滑动平均滤波器。
[0201]
图18a示出了用cnt/go(i)、cnt/go/cuonp(ii)和cnt/go/feonp(iii)功能化的电极在增加丙泊酚浓度(每五分钟注入一次丙泊酚溶液)时的安培测量结果。图18b示出了平均平台电流与产生的丙泊酚浓度的关系。可以看出,所有三个传感器都随着丙泊酚浓度的增加而产生明显的电流增加。这些反应很快速,在大约一分钟内发生,并且在整个实验中保持稳定。在所有情况下,电流响应在所调查的范围内相对于丙泊酚浓度呈线性关系。
[0202]
cnt
–
碳纳米管
[0203]
cuonp
–
氧化铜纳米颗粒
[0204]
feonp
–
氧化铁纳米颗粒
[0205]
go
–
氧化石墨烯
[0206]
使用金属氧化物修饰的氧化石墨烯制备的电极的灵敏度似乎比使用非修饰的氧化石墨烯制备的传感器的灵敏度要高得多。如前所述,循环伏安法的结果并不表明通过包括金属氧化物纳米颗粒实现了表面积或电子转移方面的改进,这表明不敏感性的改进是由于金属氧化物纳米颗粒的催化特性。
[0207]
与非功能化电极相比,纳米复合材料功能化的电极呈现出明显的改善,其中cnt/go/feonp复合材料的改善最大。这种性能的改善是增加表面积、改善电子转移和纳米复合材料的催化作用的结合的结果。滑动平均滤波器(有十秒仓)被应用于电流响应,作为降低噪音的方法,为检测极限提供了额外的改善。
[0208]
图19:a)对于cnt/go/feonp功能化的传感器对连续注入血清样溶液的丙泊酚溶液的安培响应,b)对产生的丙泊酚浓度的平台电流平均值。电位是+0.5v对丝网印刷ag/agcl。溶液为10mm pbs,含有50μg/ml nadp
+
和50μg/ml g6p。误差条代表三个标准差。已经应用了基线校正。
[0209]
为了评价传感器在更接近生理条件下的性能,准备了包含5wt%的牛血清白蛋白(bsa)、137mm的nacl、2.7mm的kcl和10mm的磷酸盐缓冲液(ph为7.4)的溶液,此外还有50μg/ml的nadp
+
和葡萄糖-6-磷酸。这些溶液被认为是“血清样的”,因为它们具有生理盐度(opoku-okrah,2015)、ph(1985)和白蛋白浓度(kim,2020)。在这些溶液中,传感器在丙泊酚的治疗范围内(1-10μg/ml)产生线性电流反应(rengenthal,1999)。灵敏度为3.1
±
0.2na/μg/ml/mm2,检测极限为143
±
27ng/ml(图20)。灵敏度较低,检测限也高于在pbs中获得的检测限,这是可以预期的,因为大部分丙泊酚将与白蛋白结合,如前所述,因此传感器只检测游离部分。然而,这个检测限仍然舒适地低于治疗范围的下限。
[0210]
图20:在制造1、2、5和7天后测试cnt/go/feonp传感器对丙泊酚浓度的电流响应。
[0211]
这些纳米复合材料传感器已经被证明在制造后储存七天内都能产生一致的结果(图20),所观察到的灵敏度和检测限的少量变化是由设备间的变化造成的。在制造和测试之间,传感器被储存在4℃。目前正在进行更长期的货架期测试(在几个月的时间里)。
[0212]
为了评估传感器对潜在干扰围手术期药物的特异性,如前所述的进行安培测量,每隔一定时间注入各种不同药物(图21)。该传感器对常见的围手术期药物没有产生明显的反应:利多卡因(altermatt,2012)、布洛芬(rainsford,2009)、吗啡(pinky,2020)、咪达唑仑(wong,1991)、苯磺酸顺阿曲库铵溶液(guo,2017)和芬太尼(peng,1999)。每种药物都以适当的浓度注入,以产生与最终丙泊酚浓度具有相同的近似比例的最终浓度,作为它们的预期治疗范围(regenthal,1999)。
[0213]
图22:cnt/go/feonp/酶功能化的电极在连续注入a:利多卡因溶液(i-iii;分别为0.23、0.47和0.70μg/ml)、布洛芬溶液(iv-vi;分别为0.21、0.41和0.62μg/ml)、吗啡溶液(vii-ix;分别为0.0028、0.0057和0.0085μg/ml)和丙泊酚溶液(x-xii;分别为0.18、0.35和0.53μg/ml)b:咪达唑仑溶液(i-iii;分别为0.0033、0.0065和0.0097μg/ml)、苯磺酸顺阿曲库铵溶液(iv-vi;分别为0.12、0.25和0.37μg/ml),芬太尼溶液(vii-ix;分别为0.0018、0.0035和0.0053μg/ml)和丙泊酚溶液(x-xii;分别为0.18、0.35和0.53μg/ml)。电位是+0.5v对丝网印刷ag/agcl。溶液为10mm pbs,含有50μg/ml nadp
+
和50μg/ml g6p。
[0214]
一个确实会导致干扰的潜在围手术期药物是常用的抗炎药物扑热息痛(colsoul,2019),因为它和丙泊酚之间的化学结构相似。对减轻这种潜在干扰的各种尝试进行了研究,包括nafion膜和分子印迹聚合物。一个是与扑热息痛可以在比丙泊酚或酶促反应产物更低的电位下被氧化有关。这可以从图22中看出,该图示出了用cnt/go/feonp纳米复合材料功能化的电极(但没有酶薄膜)在+0.25v下连续注入丙泊酚和扑热息痛溶液的安培测量。很明显,在这个电位下,电极对扑热息痛产生反应,但对丙泊酚不产生反应,这允许在较低电位下的第二个电极有可能选择性地测量扑热息痛的浓度,然后可以从最终信号中减去。可以使用双电位方法来说明潜在的扑热息痛干扰。
[0215]
图22:cnt/go/feonp功能化的电极(无酶薄膜)在+0.25v下连续注入丙泊酚(黑色)和扑热息痛(红色)溶液进行安培测量的电流响应。
[0216]
纳米颗粒合成
[0217]
金属氧化物纳米颗粒使用jamzad等人的方法合成的。
[0218]
月桂叶提取物的制备方法是用研钵和研杵将20g干月桂叶研磨成粉末。然后将粉末状的月桂叶加入到200ml的去离子水中,在90℃下搅拌10分钟。所得的溶液被过滤,然后离心以去除任何剩余的植物材料。这种月桂叶提取物溶液储存在4℃备用,并且在四个星期内使用。
[0219]
对于氧化铜和氧化铁修饰的氧化石墨烯(go),将go以1mg/ml的浓度添加到0.1m的金属盐溶液(fecl3或cucl2)中,并且超声处理30分钟,使go分散开。将这个分散液按1:1的比例加入月桂叶提取物溶液中,在室温下放置一夜,使金属氧化物纳米颗粒形成。
[0220]
然后将金属氧化物纳米颗粒修饰的氧化石墨烯以5000rpm的速度离心15分钟从溶液中提取出来,并且通过重新悬浮在去离子水中和重新离心三次来进行清洗。然后将金属氧化物纳米颗粒修饰的氧化石墨烯再次悬浮在去离子水中,加入到mwcnt中,将混合物超声处理1小时,产生具有2mg/ml的mwcnt和1mg/ml的go的分散液。然后用去离子水将该分散液稀释到0.1mg/ml的mwcnt和0.05mg/ml的go的浓度。
[0221]
电极功能化
[0222]
将mwcnt/go/monp分散液超声处理1小时,以确保最大程度的分散。然后将1μl分散液滴在spe的工作电极上,让其蒸发,再滴涂1μl分散液,并且以同样的方式进行干燥。然后用去离子水冲洗电极,以去除任何未结合的纳米材料。
[0223]
酶薄膜的制备已在前面描述过。简而言之,cypexpress 2b6以25mg/ml的浓度悬浮在磷酸盐缓冲液(ph为7)中,这个悬浮液与金纳米颗粒溶液和1%的壳聚糖溶液(1%的乙酸)按体积比1:1:2进行混合。将1μl的这个混合物沉积spe的we上,并且在4℃下静止干燥。干燥后,将电极浸泡在10mm的pbs中30分钟,然后在室温下的空气中干燥。功能化的电极储存在4℃直到使用。
[0224]
结果
[0225]
图23-示例a:基线校正,和b:通过滑动平均滤波器进行平滑处理。插图-63和64分钟之间的部分的放大。
[0226]
为了抵消这种类型的传感器常见的漂移和噪声的影响,应用了一些简单的信号处理。首先,基线校正是通过对第一次注入丙泊酚溶液前5分钟的电流响应进行线性拟合,并且校正所有数据,使其相对于这个基线进行测量。这方面的一个示例显示在图23a中,其中原始数据由实线示出,计算的基线由虚线示出。传感器的漂移从基线的轻微下降趋势中得到证明。
[0227]
其次,通过对当前数据应用滑动平均滤波器,以10秒为仓尺寸进行平滑处理。仓尺寸根据平滑程度和诱发的时间滞后之间的合理折衷决定。这方面的一个示例显示在图23b中,其中原始数据(由黑线示出)和平滑数据(由蓝线示出)一起被绘制出来。滤波器对噪声的减少是很明显的。
[0228]
虽然本文已经参考附图详细公开了本发明的说明性实施例,但是应该理解,本发明不限于所示的确切实施例,并且本领域技术人员能够在不偏离本发明的范围的情况下在其中实现各种改变和修改。
[0229]
参考文献
[0230]
cussonneau,x.,de smet,e.,lantsoght,k.,salvi,j.-p.,2007,j.pharma.biomed.anal.(药学与生物医学分析杂志),44,680-682.
[0231]
vishwananthan,k.,stewart,j.,t.,1999,j.chromatogr.relat.technol.(色谱与相关技术杂志),22,923-931.
[0232]
hikiji,w.,kudo,k.,usumoto,y.,tsuji,a.,ikeda,n.,2010,j.anal.toxicol.(分析毒理学杂志),34,389-393.
[0233]
lee,s.y.,parl,n.-h.,jeong,e.-k.,wi,j.-w.,kim,c.-j.,kim,j.y.,in,m.k.,hong,j.,2012,j.chromatogr.b(色谱学杂志b),900,1-10.
[0234]
liu,b.,pettigrew,d.m.,bates,s.,laitenberger,p.g.,troughton,g.,2012,j.clin.monit.comput.(临床监测与计算杂志),26,29-36.
[0235]
diao,j.,wang,t.,li,l.,2019,royal soc.open sci.(皇家学会开放科学),6,181753.
[0236]
anon.(2016)insights into cyp2b6-mediated drug-drug interactions(cyp2b6介导的药物之间相互作用研究).acta pharmaceutica sinica.b[online](药剂学学报b【线上】).6(5),pp.413-425.
[0237]
ouchi,k.and sugiyama,k.(2015)required propofol dose for anesthesia and time to emerge are affected by the use of antiepileptics:prospective cohort study(麻醉所需的丙泊酚剂量和出现的时间受使用抗癫痫药的影响:前瞻性队列研究).bmc anesthesiology[online](bmc麻醉学杂志【线上】).15(1),pp.34.
[0238]
smits,a.,annaert,p.and allegaert,k.(2017)biomarkers of propofol metabolism in neonates:the quest beyond ontogeny.[online].(新生儿丙泊酚代谢的生物标志物:超越个体发育的探索【线上】)
[0239]
dinis-oliveira,r.j.(2018)metabolic profiles of propofol and fospropofol:clinical and forensic interpretative aspects(丙泊酚和磷丙泊酚的代谢概况:临床和法医的解释方面).biomed research international[online](国际生物医学研究【线上】).2018pp.6852857-16.
[0240]
altermatt,f r等,evaluation of the effect of intravenous lidocaine on propofol requirements during total intravenous anaesthesia as measured by bispectral index(用双频谱指数衡量静脉注射利多卡因对全静脉麻醉期间丙泊酚需求的影响评价).br.j.anaesth.(英国麻醉学杂志),2012年06月;108(6):979-983.
[0241]
o and jacobsen,s,ph lablility in serum during equilibriam dialysis(平衡透析过程中血清中的ph变化).br.j.clin.pharmac.(英国临床药理学杂志),1985年07月;20:85-88.
[0242]
colsoul,m-l等,long-term stability of an infusion containing paracetamol,alizapride,ketorolac and tramadol in glass bottles at 5
±
3℃(含有扑热息痛、阿立必利、酮咯酸和曲马多的输液在5
±
3℃的玻璃瓶中的长期稳定性).eur.j.hosp.pharm.(欧洲医院药学杂志),2019年06月;27:e74-e78.
[0243]
cussonneau,x等,a rapid and simple hplc method for the analysis of propofol in biological fluids(用于分析生物体液中丙泊酚的快速简单的hplc方法),
j.of pharm.biomed.anal.(药学与生物医学分析杂志),2007年11月;44:680-682.
[0244]
eisenried,a等,determination of total and unbound propofol in patients during intensive care sedation by ultrafiltration and lc-ms/ms(用超滤和lc-ms/ms测定重症监护镇静过程中患者体内总丙泊酚含量和游离丙泊酚含量).j pharm biomed anal.(药学与生物医学分析杂志),2016年07月15日;126:148-55.
[0245]
fan,s-z等,propofol concentration monitoring in plasma or whole blood by gas chromatography and high-performance liquid chromatography(气相色谱法和高效液相色谱法监测血浆或全血中的丙泊酚浓度).anesth.analg.(麻醉与镇痛),1995年07月;81(1):175-8.
[0246]
gherardi,f等,immobilized enzymes on gold nanoparticles:from enhanced stability to cleaning of heritage textiles(金纳米颗粒上的固定化酶:从增强稳定性到清洁文物纺织品).acs app.bio mater.(acs应用生物材料杂志),2019年10月;2:5136-5143.
[0247]
guo,j等,pharmacokinetics and pharamcodynamics of cisatracurium in patients undergoing surgery with two henodilution methods(两种血液稀释方法下手术患者的顺阿曲库铵的药代动力学和药效动力学).j.clin.anesth.(临床麻醉杂志),2017年05月;38:75-80.
[0248]
kim,j w等,serum albumin and beta-amyloid deposition in the human brain(血清白蛋白和人脑中的β-淀粉样蛋白沉积).neurology(神经病学),2020年07月;95:e815-e826.
[0249]
kwak,j-h等,determination of propofol glucuronide from hair sample by using mixed mode anion exchange cartridge and liquid chromatography tandem mass spectrometry(混合模式阴离子交换柱和液相色谱串联质谱法测定毛发样本中的丙泊酚葡萄糖醛酸苷).j chromatogr.(色谱学杂志),2016年03月;1015-1016:209-213.
[0250]
liu,b等,performance evaluation of a whole blood propofol analyser(全血丙泊酚分析仪的性能评估).jclin.monit.comput.(临床监测与计算杂志),2012年02月;26(1):29-36.
[0251]
mazoit,j x and samii k,binding of propofol to blood components:implications for pharmacokinetics and for pharmacodynamics(丙泊酚与血液成分的结合:对药代动力学和药效动力学的影响).br.j.clin.pharmacol.(英国临床药理学杂志),1999年01月;47(1):35-42.
[0252]
miekisch,w.等,assessment of propofol concentrations in human breath and blood by means of hs-spme-gc-ms(通过hs-spme-gc-ms评估人体呼吸和血液中的丙泊酚浓度).clin chim acta.(临床化学学报)2008年09月;395(1-2):32-7.
[0253]
opoku-okrah,c等,changes in potassium and sodium concentrations in stored blood.(储存血液中的钾和钠浓度的变化),pan african medical j.(泛非医学杂志),2015年03月;20:236.
[0254]
peng,p w h等,a review of the use of fentanyl analgesia in the management of acute pain in adults(芬太尼镇痛在成人急性疼痛治疗中的应用回顾)
of phenolic compounds(电解酚类化合物时电极污染的建模分析).electrochimica acta(电化学学报),2013年01月;94:259
–
268.
[0267]
zhao,s等,a gold nanoparticle-mediated enzyme bioreactor for inhibitor screening by capillary electrophoresis(用毛细管电泳法筛选抑制剂的金纳米颗粒介导的酶生物反应器).anal.biochem.(分析生物化学),2011年04月;411(1):88-93.
[0268]
cn102262082b,optical fiber sensor-molecular imprinting online detection method for detecting propofol in biological samples and optical fiber sensor-molecular imprinting online detection device.filed(光纤传感分子印迹在线检测生物样品中异丙酚的方法和光纤传感分子印迹在线检测装置)2011-07-12.
[0269]
m.jamzad and m.k.bidkorpeh,"green synthesis of iron oxide nanoparticles by the aqueous extract of laurus nobilis l.leaves and evaluation of the antimicrobial activity,(用月桂叶的水提取物绿色合成氧化铁纳米颗粒并评价其抗菌活性)"journal of nanostructures in chemistry(化学纳米结构装置),vol.10,pp.193-201,2020.
[0270]
s.fakhari,m.jamzad and h.k.fard,"green synthesis of zinc oxide nanoparticles:a comparison(氧化锌纳米颗粒的绿色合成比较),"green chemistry letters and reviews(绿色化学快报与评论),vol.12,no.1,pp.19-24,2019.
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1