用于核酸的快速检测和绝对量化的基于数字CRISPR的方法
本发明涉及用于检测和定量样品中的靶核酸的基于数字crispr的方法、用于此类方法的试剂盒以及用于检测受试者中疾病的存在和/或严重程度的方法。
背景技术:
1、通常将dna和rna用作检测靶标,以指示生物实体的存在。从生物医学研究到临床诊断再到环境保护等各个领域都需要核酸量化技术。广泛使用的rt-qpcr作为covid-19诊断的金标准在速度和灵敏度方面具有优势,但是需要精确的热循环和高pcr效率。经由rt-qpcr的量化依赖于外部标准或参考物质的使用,并且结果可以是可变的,即使在经过培训的实验室中仍报道了20%-30%的可变性[sedlak,r.h.和jerome,k.r.diagnosticmicrobiology and infectious disease 75:1-4(2013)]。因此,具有改善的精密度和准确度的绝对量化方法对于病毒研究至关重要。
2、数字pcr被越来越多地用作核酸绝对量化的高度准确且灵敏的方法[salipante,s.j.和jerome,k.r.clinical chemistry 66:117-123(2020);sedlak,r.h.和jerome,k.r.diagnostic microbiology and infectious disease 75:1-4(2013)]。在数字pcr反应中,将pcr混合物分离为数千个单独的反应,导致每个分区中存在零个或一个核酸靶分子。在对每个分区进行独立的pcr扩增和终点荧光检测之后,基于阳性分区的比例确定样品的拷贝数。由于独立地进行每个分区中的pcr反应,因此通过数字pcr进行的绝对量化更精确、对抑制剂的耐受性更高、并且克服了扩增效率差[whale,a.s.等人nucleic acidsresearch 40:e82-e82(2012)]。基于数字pcr的病毒检测的灵敏度和精密度已经在例如sars-cov-2感染的患者样品的定量检测和病毒载量分析中得到证明,其中检测限(lod)为约2拷贝/反应,并且与rt-pcr相比,假阴性和假阳性较少[alteri,c.等人plos one 15:e0236311(2020);liu,x.等人emerging microbes&infections 9:1175-1179(2020);suo,t.等人emerging microbes&infections 9(1):1259-1268(2020);yu,f.等人clinicalinfectious diseases 71:793-798(2020)]。除了在病毒诊断中的应用外,数字pcr还成功地用于病毒研究的其他领域(包括sars-cov-2的空气动力学传播的研究)以及用于通过鼻咽拭子-qpcr测试量化病毒阴性患者的肺组织中残余sars-cov-2载量[liu,y.等人nature582:557-560(2020);yao,x.-h.等人cell research 30:541-543(2020)]。然而,数字pcr的主要缺点是,由于在热循环期间有效的分区间热传递的1-2℃/s升降温速率,因此需要相对较长的反应时间(约4小时),相比之下,qpcr则需要1小时。因此,减少数字pcr的反应时间对于能够在快速病毒检测中采用所述技术是至关重要的。
3、在病毒检测中也使用了等温扩增方法,其在恒定温度下扩增核酸靶分子,从而减少反应时间。这些方法包括采用重组酶聚合酶扩增(rpa)或环介导的等温扩增(lamp)的方法[notomi,t.等人nucleic acids research 28:e63-e63(2000);piepenburg,o.等人plosbiology 4:e204(2006);tomita,n.等人nature protocols 3:877-882(2008)]。最近,已经开发了使用rna指导的crispr/cas系统的创新诊断方法来检测核酸。在rna指导的crispr/cas系统中,利用cas效应子(如cas12a、cas12b和cas13a)的“附带切割活性”:一旦cas蛋白发现并切割其特定的dna/rna靶标,它就会结合并降解其他非特异性dna/rna寡核苷酸,如荧光标记的报告基因寡核苷酸[chen,j.s.等人science 360:436-439(2018);gootenberg,j.s.等人science 356:438-442(2017);li,s.y.等人cell discovery 4:20(2018)]。通过将rpa或lamp介导的靶分子的等温扩增与crispr/cas生物传感系统相结合,诸如sherlock和detectr的方法已经成功证明了临床样品中的登革病毒、人乳头瘤病毒以及sars-cov-2的检测[broughton,j.p.等人nature biotechnology(2020);ding,x.等人naturecommunications 11:4711(2020);gootenberg,j.s.等人science 356:438-442(2017);li,s.y.等人cell discovery 4:20(2018)]。然而,由于基于crispr的方法不是定量的并且需要在扩增与检测步骤之间进行多次操作,因此仍然需要定量、快速且稳健的病毒检测方法。
4、需要一种改进的分子平台以实现对核酸和其他靶分子的快速、可视化和模块化检测以及量化。
技术实现思路
1、本发明提供了一种核酸检测和量化系统,所述核酸检测和量化系统包括:crispr系统,其包含效应蛋白和一种或多种被设计为与相应靶分子结合的指导rna;基于核酸的掩蔽构建体;样品分配步骤,其将所述样品细分至多个区室中;以及任选地,用于扩增样品中的靶分子的核酸扩增试剂。此方法将定量数字pcr、快速等温扩增和特异性crispr检测的优点组合在一锅式反应系统中,所述一锅式反应系统将单独的反应分配至高密度芯片中的多个小区室中。在这项研究中,我们展示了一种数字crispr方法(也称为快速数字crispr方法,radica),所述方法允许在一小时内在恒定温度下对核酸进行绝对量化。我们使用含有sars-cov-2的n(核蛋白)基因的dna验证了此方法,并且显示r2值>0.99的线性信号与输入响应(signal-to-input response)。我们将我们的数字crispr检测系统与传统的数字pcr方法进行了进一步比较,并且显示使用数字crispr系统的优越速度(1h相比于4h),同时显示出与传统数字pcr的灵敏度和准确度可比较的灵敏度和准确度。此外,我们成功地将数字crispr用于对来自人b细胞的爱泼斯坦-巴尔病毒、人腺病毒和单纯疱疹病毒的绝对量化(r2值>0.98)以及在一个反应中对若干个靶标的多重检测。总之,我们快速且灵敏的数字crispr方法允许核酸的准确检测和绝对量化。
2、在第一方面,提供了一种用于检测和定量样品中的靶核酸的方法,所述方法包括:
3、a)形成混合物,所述混合物包含:样品核酸;
4、用于扩增一种或多种靶核酸序列的等温扩增反应试剂;
5、cas12a、cas12b、cas13b或cas14效应子或其衍生物;
6、含有dna靶向序列并且被设计为与所述cas效应子形成复合物的至少一种指导多核苷酸;以及
7、含有非靶序列的基于核酸的掩蔽构建体,
8、b)将所述混合物分配至多个区室中;
9、c)将所分配的混合物在用于等温扩增以及cas效应子切割所扩增的dna链的温度下孵育,
10、其中所述cas效应子展现出附带核酸酶活性,并且一旦被所述靶序列激活则切割所述基于核酸的掩蔽构建体的非靶序列;以及
11、d)检测来自切割所述非靶序列的信号,从而检测所述样品中的一种或多种靶序列,以及
12、e)基于阳性与阴性区室的比例的泊松分布确定所述靶核酸的拷贝数。
13、在一些实施方案中,所述cas效应子是cas12a或cas12b。
14、在一些实施方案中,所述方法用于检测和/或量化样品中的病原体、基因表达、基因拷贝数变异或外来因子。
15、在一些实施方案中,所述至少一种指导多核苷酸是crrna。
16、在一些实施方案中,所述扩增选自基于核酸序列的扩增、重组酶聚合酶扩增、环介导的等温扩增、链置换扩增、核酸外切酶ill辅助信号扩增、杂交链反应、解旋酶依赖性扩增、等温环链置换聚合、多重置换扩增、基于引发酶的全基因组扩增、滚环扩增和全基因组扩增。
17、在一些实施方案中,与cas12a偶联的扩增选自重组酶聚合酶扩增、链置换扩增、滚环扩增和多重置换扩增。
18、在一些实施方案中,与cas12b偶联的扩增选自环介导的等温扩增、解旋酶依赖性扩增、链置换扩增和滚环扩增。
19、在一些实施方案中,与cas13偶联的扩增选自基于核酸序列的扩增、重组酶聚合酶扩增和链置换扩增。
20、在一些实施方案中,与cas14偶联的扩增选自重组酶聚合酶扩增、链置换扩增和滚环扩增。
21、在一些实施方案中,所述等温扩增是重组酶聚合酶扩增或环介导的等温扩增。
22、在一些实施方案中,所述掩蔽构建体抑制可检测阳性信号的产生直到被裂解,或者掩蔽可检测阳性信号直到所述掩蔽构建体被裂解。
23、在一些实施方案中,所述掩蔽构建体包含淬灭的荧光核酸探针,如ssdna探针、dsdna或rna探针。
24、在一些实施方案中,所述靶标是dna或rna。
25、在一些实施方案中,所述靶标是病毒dna或rna。
26、在一些实施方案中,所述病毒是sars-cov-2病毒、人腺病毒(hadv)、单纯疱疹病毒(hsv)或爱泼斯坦-巴尔病毒(ebv)。
27、在一些实施方案中,所述分配是基于微流体的、基于液滴的或基于膜的,优选基于芯片的。
28、在一些实施方案中,将所述混合物分配至至少1,000个区室,优选至少10,000个区室中。
29、在一些实施方案中,所述指导物具有包含与所述一种或多种靶序列的错配的序列。
30、在一些实施方案中,所述错配位于所述指导序列中单核苷酸变异的上游或下游。
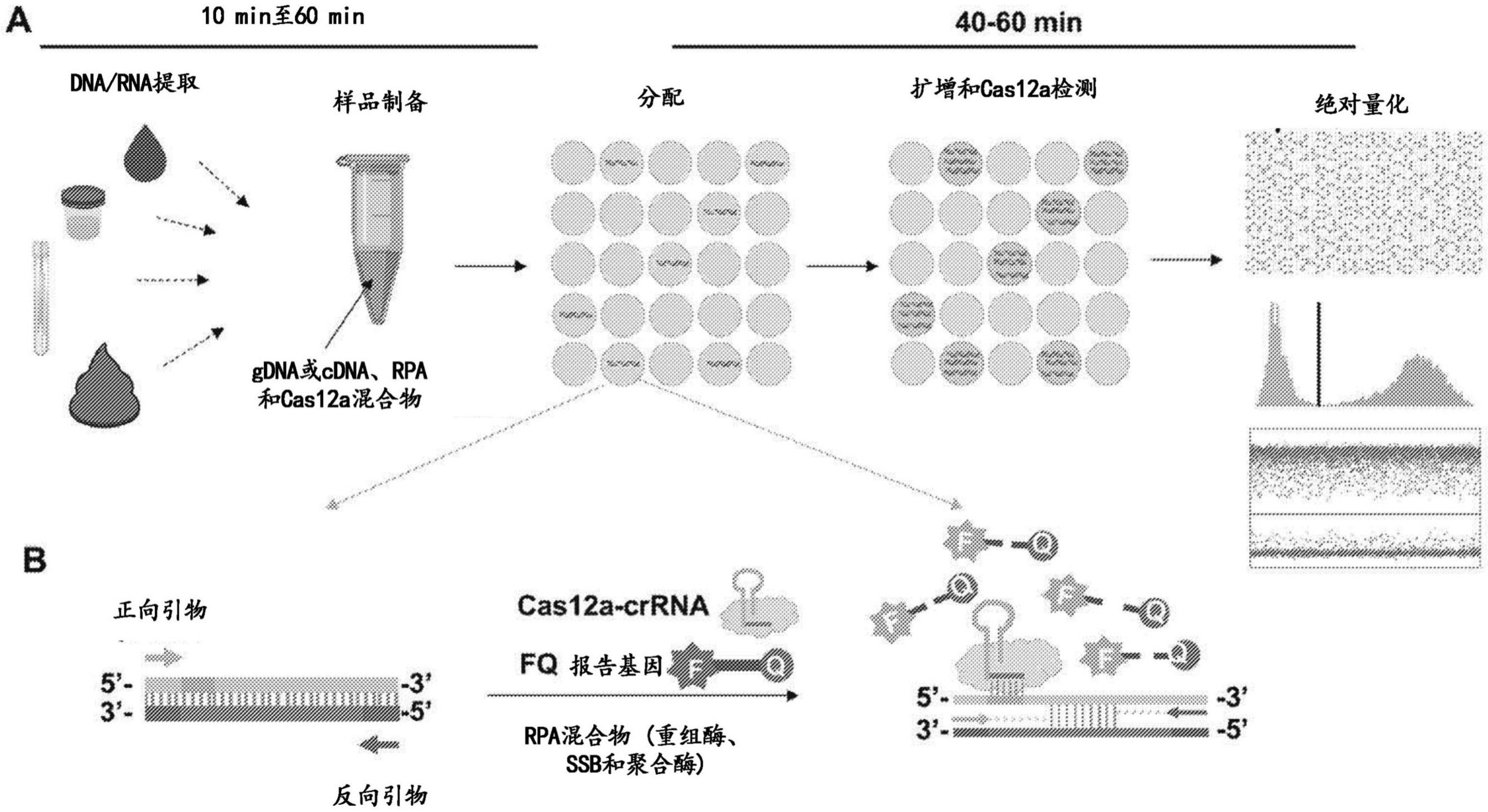
31、在一些实施方案中,所述等温扩增是重组酶聚合酶扩增(rpa)。根据本发明的重组酶聚合酶扩增radica的示意图示于图1中。
32、在一些实施方案中,在c)步骤中,所述rpa反应是在42℃下。
33、在一些实施方案中,所述cas效应子是cas12a。在一些实施方案中,所述cas12a同源物来自毛螺科细菌(lachnospiraceae bacterium)nd2006(lbcas12a)。
34、发现在步骤c)中在42℃下使用cas12a,40min孵育足以进行定性检测,并且60min孵育足以进行定量检测(实施例3)。
35、在一些实施方案中,所述等温扩增是热启动lamp或rt-lamp反应。
36、在一些实施方案中,在步骤c)中,所述热启动rt-lamp反应是在60℃下。
37、在一些实施方案中,所述cas效应子是cas12b,其已经显示为与高灵敏度的一锅式rt-lamp反应相容。根据本发明的热启动radica的示意图示于图24中。
38、在一些实施方案中,所述cas效应子是来自酸性脂环酸芽孢杆菌(alicyclobacillus acidiphilus)的cas12b(aapcas12b)。
39、在一些实施方案中,将warmstart rtx逆转录酶、warmstart dna聚合酶和cas12b/crrna组合。在一些实施方案中,使用bst 2.0warmstart dna聚合酶。
40、在一些实施方案中,所述基于核酸的掩蔽构建体是包含5个胸腺嘧啶(t)碱基的淬灭的荧光报告基因。有利地,此掩蔽构建体显示高信噪比和反应速率。
41、在一些实施方案中,将牛磺酸添加至反应混合物中以改善反应动力学。
42、在一些实施方案中,40min孵育足以进行定性检测并且60min孵育足以通过热启动radica进行定量检测。
43、在一些实施方案中,所述等温扩增反应是多重反应。
44、在一些实施方案中,所述多重反应检测靶核酸和人核酸(dna)对照。
45、在一些实施方案中,所述多重反应检测野生型靶核酸及其变体或突变体。例如,多重反应用于检测野生型sars-cov-2n(或其他)基因及其sars-cov-2突变变体。如实施例17和实施例18以及图45-图48所例示的,所述反应可以包括用于检测野生型靶核酸及其至少一种变体的多重引物。
46、在一些实施方案中,所述靶核酸是sars-cov-2、hadv、hsv或爱泼斯坦-巴尔病毒核酸;
47、所述等温扩增是:
48、a)重组酶聚合酶扩增;所述cas效应子是cas12a;或
49、b)lamp或rt-lamp;所述cas效应子是cas12b;
50、所述至少一种指导多核苷酸是crrna;
51、将所述混合物分配至至少1,000个区室,优选至少10,000个区室中,并且其是基于芯片的;并且所述掩蔽构建体包含淬灭的荧光ssdna探针。
52、在一些实施方案中,所述扩增反应是热启动的。
53、在第二方面,提供了一种用于检测受试者中疾病的存在和/或严重程度的方法,所述方法包括以下步骤:
54、a)形成混合物,所述混合物包含:来自所述受试者的含有核酸的样品;
55、用于扩增一种或多种靶疾病核酸序列的等温扩增反应试剂;
56、cas12a、cas12b、cas13b或cas14效应子或其变体;
57、含有dna靶向序列并且被设计为与所述cas效应子形成复合物的至少一种指导多核苷酸;以及
58、含有非靶序列的基于核酸的掩蔽构建体,
59、b)将所述混合物分配至区室中;
60、c)将所分配的混合物在用于等温扩增以及cas效应子切割所扩增的dna链的温度下孵育,
61、其中所述cas效应子展现出附带核酸酶活性,并且一旦被所述靶序列激活则切割所述基于核酸的掩蔽构建体的非靶序列;
62、d)检测来自切割所述非靶序列的信号,从而检测所述样品中的一种或多种靶序列;
63、e)基于阳性与阴性区室的比例的泊松分布确定所述靶核酸的拷贝数,并且将所述数目与对照值进行比较;
64、其中阳性区室指示所述受试者中疾病的存在,并且其中所述靶核酸的拷贝数指示所述受试者中所述疾病的严重程度。
65、在一些实施方案中,所述疾病是病原体感染。
66、在一些实施方案中,所述疾病是病毒感染。
67、在一些实施方案中,所述cas效应子是cas12a和/或cas12b。
68、在一些实施方案中,所述方法用于检测和/或量化病原体、基因表达或基因拷贝数变异。
69、在一些实施方案中,所述至少一种指导多核苷酸是crrna。
70、在一些实施方案中,所述扩增选自基于核酸序列的扩增、重组酶聚合酶扩增、环介导的等温扩增、链置换扩增、核酸外切酶ill辅助信号扩增、杂交链反应、解旋酶依赖性扩增、等温环链置换聚合、多重置换扩增、基于引发酶的全基因组扩增、滚环扩增和全基因组扩增。
71、在一些实施方案中,所述等温扩增是重组酶聚合酶扩增或环介导的等温扩增。
72、在一些实施方案中,所述掩蔽构建体抑制可检测阳性信号的产生直到被裂解,或者掩蔽可检测阳性信号直到所述掩蔽构建体被裂解。
73、在一些实施方案中,所述掩蔽构建体包含淬灭的荧光核酸探针。
74、在一些实施方案中,所述靶标是dna或rna。
75、在一些实施方案中,所述靶标是病毒dna或rna。
76、在一些实施方案中,所述病毒是sars-cov-2、人腺病毒(hadv)、单纯疱疹病毒(hsv)或爱泼斯坦-巴尔病毒。
77、在一些实施方案中,所述分配是基于微流体的、基于液滴的或基于膜的,优选基于芯片的。
78、在一些实施方案中,将所述混合物分配至至少1,000个区室中。
79、在一些实施方案中,所述等温扩增是热启动rt-lamp反应。
80、在一些实施方案中,所述等温扩增反应是多重反应。
81、在一些实施方案中,所述方法进一步包括施用对所述受试者的疾病严重程度有效的治疗。
82、在第三方面,提供了一种定量样品中的靶核酸的试剂盒,所述试剂盒包含:
83、a)用于扩增一种或多种靶核酸序列的等温扩增反应试剂;
84、b)cas12a、cas12b、cas13b或cas14效应子或其变体;
85、c)含有dna靶向序列并且被设计为与所述cas效应子形成复合物的至少一种指导多核苷酸;
86、d)含有非靶序列的基于核酸的掩蔽构建体,以及
87、e)分配装置或基底。
88、在试剂盒的一些实施方案中,所述靶核酸是sars-cov-2、人腺病毒(hadv)、单纯疱疹病毒(hsv)或爱泼斯坦-巴尔病毒核酸;所述等温扩增反应试剂是:
89、a)重组酶聚合酶扩增反应试剂;所述cas效应子是cas12a;或
90、b)热启动rt-lamp扩增反应试剂;所述cas效应子是cas12b;
91、所述至少一种指导多核苷酸是crrna;所述分配装置或基底包含至少1,000个区室并且是基于芯片的;并且所述基于核酸的掩蔽构建体包含至少一个淬灭的荧光ssdna探针。
92、在一些实施方案中,所述分配装置或基底包含至少10,000个区室。
- 还没有人留言评论。精彩留言会获得点赞!