用以抑制发炎缓解牙龈肿痛改善口腔菌群平衡的唾液乳杆菌菌株ZK-88的制作方法
用以抑制发炎缓解牙龈肿痛改善口腔菌群平衡的唾液乳杆菌菌株zk-88
技术领域
1.本发明属于工业微生物技术领域,特别涉及一种唾液乳杆菌zk-88及其应用。
背景技术:
2.唾液乳杆菌,是革兰氏染色阳性杆菌,不生成孢子,不具触酶、氧化酶及运动性,在好氧及厌氧环境均能生长,属于兼性异质发酸性菌株,葡糖代谢时不产生气体。
3.研究表明,唾液乳杆菌在t帮助型活化调节细胞(cd4+/cd25+cells)、t抑制/毒杀活化细胞(cd8+/cd25+cells)与自然杀手细胞(cd16+/cd+cells)的表现有显著的增加,il-12与ifn-γ亦呈现显著增加,说明唾液乳杆菌可诱导专一性的免疫反应而改善先天性与后天性免疫反应。
4.鉴于双歧杆菌的重要作用,新菌株的获得对新药物、新功能食品等的研发是至关重要的。
技术实现要素:
5.基于上述技术问题,本发明的主要目的在于提供一株唾液乳杆菌(lactobacillus salivarius)zk-88,该菌株对多种革兰氏阴性致病菌和革兰氏阳性致病菌具有抑制作用。
6.本发明的目的可以通过以下技术方案实现:一株唾液乳杆菌(lactobacillus salivarius)zk-88,其已于2021年10月28日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏编号为cgmcc no.23682,保藏地址为北京市朝阳区北辰西路1号院3号。
7.所述的唾液乳杆菌(lactobacillus salivarius)zk-88在制备保健食品或者抗革兰氏阴性致病菌的药物中的应用。
8.在其中一些实施例中,所述革兰氏阴性致病菌为大肠杆菌。
9.在其中一些实施例中,所述革兰氏阴性致病菌为具核梭杆菌。
10.在其中一些实施例中,所述革兰氏阴性致病菌为牙龈卟啉单胞菌。
11.所述的动物唾液乳杆菌(lactobacillus salivarius)zk-88在制备保健品或者抗革兰氏阳性致病菌的药物中的应用。
12.在其中一些实施例中,所述革兰氏阳性致病菌为金黄色葡萄球菌。
13.在其中一些实施例中,所述药物包含唾液乳杆菌(bifidobacterium animalis)zk-88以及药学上可以接受的辅料。
14.在其中一些实施例中,所述辅料包含填充剂、崩解剂、润滑剂、润湿剂、助悬剂和矫味剂中的一种或者多种。
15.在其中一些实施例中,所述药物的剂型为片剂、胶囊剂、粉剂、丸剂、颗粒剂或者溶液剂。
16.在其中一些实施例中,所述保健食品为饼干、糕点、饮料、口服液、冲剂、饮料、液体
乳类或者奶粉。
17.一种药物或者保健食品,所述的药物或者保健食品包含所述的唾液乳杆菌(lactobacillus salivarius)zk-88或/和其代谢物。
18.相对于传统技术,本发明具有以下有益效果:本发明提供一株唾液乳杆菌(lactobacillus salivarius)zk-88,该菌株对牙龈卟啉单胞菌等革兰氏阴性致病菌以及金黄色葡萄球菌等革兰氏阳性致病菌具有明显抑制作用,能够用于制备预防/治疗针对这些致病菌感染的抗菌药物,也适用于制备改善这些致病菌感染情况的药品,或者是保健品。
附图说明
19.为了更清楚地说明本发明具体实施方式或现有技术中的技术方案,下面将对具体实施方式或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图是本发明的一些实施方式,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
20.图1为本发明一个实施例中各处理组脂肪细胞油红染色结果图;图2为本发明一个实施例中各处理组胆碱水解酶活性检测图;图3为本发明一个实施例中各处理组大鼠体重统计图;图4为本发明一个实施例中各组大鼠的牙周指数;图5为本发明一个实施例中各处理组血液炎症因子检测结果图;图6为本发明一个实施例中各处理组牙槽骨3d光学扫描图;图7为本发明一个实施例中肠道微生物16rrna测序结果图(粪便样本);图8为本发明一个实施例中大鼠粪便微生物聚类图;图9为本发明一个实施例中大鼠龈沟液微生物16rrna测序结果图;图10为本发明一个实施例中大鼠龈沟液微生物聚类图。
21.本发明提供的唾液乳杆菌(lactobacillus salivarius),命名为唾液乳杆菌lactobacillus salivarius。该菌株已于2021年10月28日保藏于中国微生物菌种保藏管理委员会普通微生物中心,地址:北京市朝阳区北辰西路1号院3号,保藏编号为cgmcc no.23682,邮政编码为100101;该菌株于2021年10月28日由保藏中心收到并登记入册,经保藏中心于2021年10月28日检测为存活菌株。
具体实施方式
22.为了便于理解本发明,下面将对本发明进行更详细的描述。但是,应当理解,本发明可以以许多不同的形式来实现,并不限于本文所描述的实施方式或实施例。相反地,提供这些实施方式或实施例的目的是使对本发明的公开内容的理解更加透彻全面。
23.除非另有定义,本文所使用的所有的技术和科学术语与属于本发明的技术领域的技术人员通常理解的含义相同。本文中在本发明的说明书中所使用的术语只是为了描述具体的实施方式或实施例的目的,不是旨在于限制本发明。本文所使用的术语“和/或”的可选范围包括两个或两个以上相关所列项目中任一个,也包括相关所列项目的任意的和所有的组合,所述任意的和所有的组合包括任意的两个相关所列项目、任意的更多个相关所列项
目、或者全部相关所列项目的组合。
24.除非另外说明或存在矛盾之处,本文中使用的术语或短语具有以下含义:本文所使用的术语“和/或”、“或/和”、“及/或”的可选范围包括两个或两个以上相关所列项目中任一个项目,也包括相关所列项目的任意的和所有的组合,所述任意的和所有的组合包括任意的两个相关所列项目、任意的更多个相关所列项目、或者全部相关所列项目的组合。
25.本文中,“优选”仅为描述效果更好的实施方式或实施例,应当理解,并不构成对本发明保护范围的限制。
26.本发明中,“第一方面”、“第二方面”、“第三方面”等仅用于描述目的,不能理解为指示或暗示相对重要性或数量,也不能理解为隐含指明所指示的技术特征的重要性或数量。
27.本发明中,以开放式描述的技术特征中,包括所列举特征组成的封闭式技术方案,也包括包含所列举特征的开放式技术方案。
28.本发明中,涉及到数值区间,如无特别说明,则包括数值区间的两个端点。
29.本发明中涉及的百分比含量,如无特别说明,对于固相-液相混合和固相-固相混合均指质量百分比,对于液相-液相混合指体积百分比。
30.本发明中涉及的百分比浓度,如无特别说明,均指终浓度。所述终浓度,指添加成分在添加该成分后的体系中的占比。
31.本发明中的温度参数,如无特别限定,既允许为恒温处理,也允许在一定温度区间内进行处理。所述的恒温处理允许温度在仪器控制的精度范围内进行波动。
32.第一方面,本发明提供一株唾液乳杆菌(lactobacillus salivarius)zk-88,其已于2021年10月28日保藏于中国微生物菌种保藏管理委员会普通微生物中心,保藏编号为cgmcc no.23682,保藏地址为北京市朝阳区北辰西路1号院3号。
33.第二方面,本发明提供所述的唾液乳杆菌(lactobacillus salivarius)zk-88在制备保健品或者抗革兰氏阴性致病菌的药物中的应用。
34.本发明中,所述革兰氏阴性致病菌可以为,包括但不限于:大肠杆菌具核梭杆菌、牙龈卟啉单胞菌。例如:所述革兰氏阴性致病菌为牙龈卟啉单胞菌,则所述唾液乳杆菌(lactobacillus salivarius)zk-88可用于制备牙龈卟啉单胞菌感染所致的牙周炎的药物,该药物可以降低机体血液中的炎症因子含量。
35.本发明中,所述药物包含动物唾液乳杆菌(lactobacillus salivarius)zk-88以及药学上可以接受的辅料。
36.本发明中,所述辅料可以选自,包括但不限于:填充剂、崩解剂、润滑剂、润湿剂、助悬剂和矫味剂。
37.本发明中,所述药物的剂型为片剂、胶囊剂、粉剂、丸剂、颗粒剂或者溶液剂。
38.本发明中,所述保健食品可以为,包括但不限于:饼干、糕点、饮料、口服液、冲剂、饮料、液体乳类或者奶粉。
39.第三方面,本发明提供所述的唾液乳杆菌(lactobacillus salivarius)zk-88在制备保健食品或者抗革兰氏阳性致病菌的药物中的应用。
40.本发明中,所述革兰氏阳性致病菌可以为,包括但不限于:金黄色葡萄球菌。
41.本发明中,所述药物包含唾液乳杆菌(lactobacillus salivarius)zk-88以及药学上可以接受的辅料。
42.本发明中,所述辅料可以选自,包括但不限于:填充剂、崩解剂、润滑剂、润湿剂、助悬剂和矫味剂。
43.本发明中,所述药物的剂型为片剂、胶囊剂、粉剂、丸剂、颗粒剂或者溶液剂。
44.本发明中,所述保健食品可以为,包括但不限于:饼干、糕点、饮料、口服液、冲剂、饮料、液体乳类或者奶粉。
45.本发明中,所述保健食品亦称功能性食品,一个特定的食品种类。它具有调节人体功能的作用,但不以治疗疾病为目的,适于特定人群食用。本发明所述的保健食品是指声称具有特定保健功能或者以补充维生素、矿物质为目的的食品,即适宜于特定人群食用,具有调节机体功能,不以治疗疾病为目的,并且对人体不产生任何急性、亚急性或者慢性危害的食品。
46.第四方面,本发明提供一种药物或者保健食品,所述的药物或者保健食品包含所述的唾液乳杆菌(lactobacillus salivarius)zk-88或/和其代谢物。
47.第五方面,本发明还提供一种益生菌组合物,所述益生菌组合物包含所述唾液乳杆菌(lactobacillus salivarius)zk-88以及其他益生菌。
48.本发明中,所述其他益生菌可以选自,包括但不限于:动物双歧杆菌、唾液链球菌、植物乳杆菌。其他益生菌可以是一种,也可以是益生菌中的多种。其中,所述唾液乳杆菌可以选用,包括但不限于:双歧杆菌(bifidobacterium animalis)zk-77。本发明提供的动物双歧杆菌(bifidobacterium animalis)zk-77,分类命名为动物双歧杆菌bifidobacterium animalis。该菌株已于2021年10月28日保藏于中国微生物菌种保藏管理委员会普通微生物中心,地址:北京市朝阳区北辰西路1号院3号,保藏编号为cgmcc no.23681,邮政编码为100101;该菌株于2021年10月28日由保藏中心收到并登记入册,经保藏中心于2021年10月28日检测为存活菌株。
49.下述实施例中所述试验方法,如无特别说明,均为常规方法;所述试剂和生物材料,如无特别说明,均可从商业途径获得。
50.下述实施例中,所述百分含量如无特别说明,均为质量百分含量。
实施例
51.一、菌株分离及鉴定1、方法取人口腔冲洗液样品100μl,并梯度稀释至10-1-10-4
倍,制备稀释液;以含溴甲酚紫的mrs培养基为选择性培养基,在平板涂布所述稀释液,用于分离乳杆菌;以含莫匹罗星锂盐的mrs培养基为选择性培养基,在平板上涂布所述稀释液,用于分离双歧杆菌;涂布的平板置于37℃,厌氧过夜培养,挑取单菌落纯化,并16s鉴定保种。
52.16s鉴定:采用通用引物27f(seq id no.1:agagtttgatcctggctcag)和1492r(seq id no.2:tacggctaccttgttacgactt),产生16s pcr片段,提交擎科生物公司测序(正向)。针
对动物双歧杆菌和唾液乳杆菌,测序使用的通用引物相同,扩增的目的片段为代表不同菌株种属特异性的基因片段,测序后和菌种库基因序列比对后,可确定细菌种属。
53.2、结果表1、两株菌的ncbi比对结果唾液乳杆菌zk-88的16s测序结果如seq id no.3所示:tatgctctgctatgatgcaagtcgacgaaactttcttacaccgaatgcttgcattcaccgtaagaagttgagtggcggacgggtgagtaacacgtgggtaacctgcctaaaagaaggggataacacttggaaacaggtgctaataccgtatatctctaaggatcgcatgatccttagatgaaagatggttctgctatcgcttttagatggacccgcggcgtattaactagttggtggggtaacggcctaccaaggtgatgatacgtagccgaactgagaggttgatcggccacattgggactgagacacggcccaaactcctacgggaggcagcagtagggaatcttccacaatggacgcaagtctgatggagcaacgccgcgtgagtgaagaaggtcttcggatcgtaaaactctgttgttagagaagaacacgagtgagagtaactgttcattcgatgacggtatctaaccagcaagtcacggctaactacgtgccagcagccgcggtaatacgtaggtggcaagcgttgtccggatttattgggcgtaaagggaacgcaggcggtcttttaagtctgatgtgaaagccttcggcttaaccggagtagtgcattggaaactggaagacttgagtgcagaagaggagagtggaactccatgtgtagcggtgaaatgcgtagatatatggaagaacaccagtggcgaaagcggctctctggtctgtaactgacgctgaggttcgaaagcgtgggtagcaaacaggattagataccctggtagtccacgccgtaaacgatgaatgctaggtgttggagggtttccgcccttcagtgccgcagctaacgcaataagcattccgcctggggagtacgaccgcaaggttgaaactcaaaggaattgacgggggcccgcacaagcggtggagcatgtggttaattcgaagcacgcgaagaccttaccaggcttgactcctttgacccctaaaaattaggtttcccttcgggacaagtgacagtggtgatggctgcctcactcgggccggaatgtgggtaagtccgaacaacgaaccttgttgcattgcagattaattgggacctggcaaatgccgggcaaccggagaagggggacactcagtcttgccc动物双歧杆菌zk-77的测序结果如seq id no.4所示:aatgcgctgctacctgcagtcgaacgggatccctggcagcttgctgtcggggtgagagtggcgaacgggtgagtaatgcgtgaccaacctgccctgtgcaccggaatagctcctggaaacgggtggtaataccggatgctccgctccatcgcatggtggggtgggaaatgcttttgcggcatgggatggggtcgcgtcctatcagcttgttggcggggtgatggcccaccaaggcgttgacgggtagccggcctgagagggtgaccggccacattgggactgagatacggcccagactcctacgggaggcagcagtggggaatattgcacaatgggcgcaagcctgatgcagcgacgccgcgtgcgggatggaggccttcgggttgtaaaccgcttttgttcaagggcaaggcacggtttcggccgtgttgagtggattgttcgaataagcaccggctaactacgtgccagcagccgcggtaatacgtagggtgcgagcgttatccggatttattgggcgtaaagggctcgtaggcggttcgtcgcgtccggtgtgaaagtccatcgcctaacggtggatctgcgccgggtacgggcgggctggagtgcggtaggggagactggaattcccggtgtaacggtggaatgtgtagatatcgggaagaacaccaatggcgaaggcaggtctctgggccgtcactgacgctgaggagcgaaagcgtggggagcgaacaggattagataccctggtagtccacgccgtaaacggtggatgctggatgtggggccctttccacgggtcccgtgtcggagccaacgcgttaagcatcccgcctggggagtacggccgcaaggctaaaactcaaagaaattgacgggggcccgcacaagcggcggagcatgcggattattcgatgcacgcgaagaccttacctgggcttgaatgtgccagatcgcgtggagaccggttcccttcggggccgttccaggtggtgctggccgcctcagtcgtgcgggaatgtgggtaagtccgcacgagccaccctcgcgctgttgcagcggta
二、耐胆酸、胆碱检测1、方法分别配置ph2.0(胆酸)的mrs培养基和含0.3%(w/v)胆碱盐的mrs培养基,将菌株母液以5%接种量分别接种于mrs培养基、ph2.0(胆酸)的mrs培养基和含0.3%(w/v)胆碱盐的mrs培养基中,处理2h后平板计数。同时,还以唾液链球菌k12作为对照菌株。
54.其中:接种于mrs培养基的处理对应“对照”,接种于ph2.0(胆酸)的mrs培养基的处理对应“ph2.0(胆酸)”,接种于含0.3%(w/v)胆碱盐的mrs培养基的处理对应“0.3%胆碱盐”。
55.2、结果不同菌株对应的不同处理的平板计数结果见下表。
56.表2三、产小分子脂肪酸能力检测1、方法(1)菌株母液制备:动物双歧杆菌zk-77的菌液制备:菌种1%(v/w)接种于新鲜mrs培养基37℃,厌氧过夜培养。
57.唾液乳杆菌zk-88的菌液制备:菌种1%(v/w)接种于新鲜mrs培养基37℃,厌氧过夜培养。
58.(2)样品处理:取1ml菌株菌液,5000r/min,离心10min,留取上清。
59.(3)色谱柱:7890a-5975c气相色谱-质谱联用仪、vf-waxms(30m
×
0.25mm
×
0.25
µ
m)毛细管色谱柱。
60.(4)进样方式:顶空进样,恒温炉温度70℃,样品流路温度90℃,传输线温度110℃,样品瓶加压气压160.0kpa,样品瓶恒温时间10min,样品瓶加压时间1min,gc循环时间22min。
61.(5)gc操作:程序升温,初始温度100℃,以5℃/min升至150℃后,升温至240℃并保持3min;进样口温度230℃,辅助温度240℃,四级杆温度150℃,离子源温度230℃,进样量1
µ
l,进样方式:不分流进样,载气:高纯氮气(》99.999%),载气流速:2ml/min。
62.2、结果动物双歧杆菌zk-77和唾液乳杆菌zk-88的产乙酸、丙酸和丁酸的情况如下表所示。
63.表3
四、菌株抗生素抗性检测1、方法双层平板法检测候选菌株对抗生素的抗性。双层平板的下层为1.5%(w/v)的琼脂营养培养基,双层平板的上层用0.5%(w/v)的软琼脂培养基,与菌株菌液(制备参照“三、产小分子脂肪酸能力检测”)100:1(v:v)混匀。待平板固化和表面干燥后,放入商品化抗生素药敏片(tet,cm,fz,amp,ery,na,rif,gen和neo)过夜培养,根据抑菌圈大小,观察益生菌对抗生素的抗性。同时还设置了唾液链球菌k12对照菌株组。
64.其中:tet对应四环素,cm对应氯霉素,fz对应,amp对应氨苄霉素,ery对应红霉素,na表示空值,无抗生素处理,rif对应利福平,gen对应庆大霉素和neo对应新霉素。
65.2、结果表4五、菌株凝血试验检测1、方法(1)配置krt缓冲溶液(nacl 7.5g,kcl 0.383g,mgso4
·
7h2o 0.318g,cacl2 0.305g,用盐酸调ph 7.4,加水至1l)。
66.(2)将新鲜羊血红细胞用pbs缓冲溶液清洗一次,3000rpm,5min离心,10%(w/v)终浓度重悬于krt缓冲液。
67.(3)菌株过夜培养液在krt缓冲液中2倍梯度稀释,分别制备2倍、4倍、6倍、8倍的稀释液;过夜培养液的制备参照“三、产小分子脂肪酸能力检测”。
68.(4)25
µ
l羊血红细胞加入梯度稀释的菌悬液(25
µ
l),室温放置2h后检测凝聚现象。
69.同时还设置了唾液链球菌k12对照菌株组。
70.2、结果动物双歧杆菌zk-77和唾液乳杆菌zk-88菌株的凝血试验检测结果见下表。
71.表5六、菌株拮抗检测1、方法双层平板法检测菌株对病原菌株的拮抗作用。双层平板下层为1.5%(w/v)的琼脂营养培养基,双层平板上层用0.5%(w/v)的软琼脂培养基,菌液与软琼脂培养基体积比1:100混匀、过夜培养。待平板固化和表面干燥后,用1ml枪头打孔,接种菌株菌苔,根据抑菌圈大小,观察菌株对病原菌(大肠杆菌、金黄色葡萄球菌、绿脓杆菌、具核梭杆菌、白色念珠菌、牙龈卟啉菌)的抑制作用。菌液的制备参照“三、产小分子脂肪酸能力检测”。
72.2、结果动物双歧杆菌zk-77和唾液乳杆菌zk-88对各病原菌的抑菌圈统计见下表。
73.表6七、脂肪细胞实验1、方法(1)细胞分化诱导当细胞汇合率为70%-80%时,按照atcc
®
cl-173
™
产品说明书中提供的与传代培养相关的说明,通过胰蛋白酶消化收获细胞。将细胞接种到前脂肪细胞扩增培养基中,生长48小时,或直到培养物达到100%融合为止。再孵育48小时后,从每个孔中移出前脂肪细胞扩增培养基,并添加相同体积的分化培养基。同时按灭活菌液与分化培养基体积比1:1000的比例,加入灭活菌液(以不添加任何菌株的菌液为对照)。菌液的制备参照“三、产小分子脂肪酸能力检测”,沸水浴30min热灭活。
74.在分化培养基中孵育48小时,用脂肪细胞维持培养基替换分化培养基,每48小时更换一次脂肪细胞维持培养基。诱导后6天到10天之间,通过油红染色观察脂质滴形成,红色越多,表明油滴越多。
75.其中,染色的步骤包括:脂肪细胞以pbs缓冲液冲洗2次,置于4%甲醛固定20min,弃掉,pbs洗1次-2次,油红o染液0.5h-1h,60%异丙醇快速漂洗3s,pbs洗2编-3遍,显微镜观察。
76.前脂肪细胞扩增培养基:90%(w/v)dmem,10%(w/v)小牛血清;分化培养基:90%(w/v)dmem,10%(w/v)胎牛血清(fbs),1.0μm地塞米松,0.5mm甲基异丁基黄嘌呤(ibmx),10μg/ml胰岛素;脂肪细胞维持培养基:90%(w/v)dmem,10%(w/v)胎牛血清,10μg/ml胰岛素。
77.油红染色液配置:1g油红溶于200ml异丙醇中,混匀后搅拌溶解,配成储存液。4℃避光保存。临用时3:2与蒸馏水配置原液,静置一会后过滤,滤纸片,此工作液不能保留超过1h-2h。
78.60%异丙醇的配方:100%异丙醇60ml加蒸馏水40ml,4℃保存。
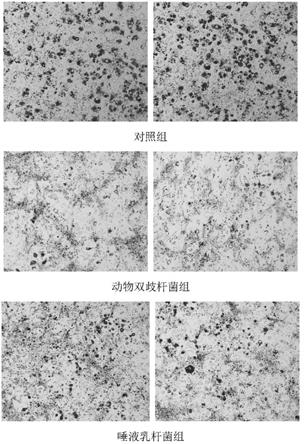
79.染色结果见图1。图1中,每组图片的左图和右图对应重复实验结果,颜色越深表明分化程度越高。
80.八、胆碱水解酶活性检测(bsh)1、方法新鲜培养液0.5μl滴加到mrs培养基和含0.5%(w/w)tdca (胆碱盐)的mrs培养基中,37℃过夜培养,观察菌落周围沉淀圈的形成。其中,+:沉淀圈直径<1.5cm;++:沉淀圈直径≥1.7cm;-:无沉淀圈。培养液的制备参照参照“三、产小分子脂肪酸能力检测”。
81.2、结果结果见图2。编号为cb29y5的动物双歧杆菌zk-77,酶活结果:++,见图2上图。编号为cb13m2的唾液乳杆菌zk-88,酶活结果:—,见图2下图。
82.九、动物实验(一)牙周炎模型构建及菌株效果验证1、材料动物:健康6周龄雄性sd大鼠。
83.菌种:牙龈卟啉单胞菌(w83)、编号为cb29y5的动物双歧杆菌zk-77、编号为cb13m2的唾液乳杆菌zk-88、唾液链球菌k12。
84.试剂:10%(w/v)水合氯醛溶液、1%(w/v)肝素溶液、2%(w/v)羧甲基纤维素溶液、4%(w/v)多聚甲醛溶液、10%(w/v)edta、生理盐水、pbs缓冲液。
85.工具:注射器、自制开口器、止血钳、金柄持针器、镊子、手术剪、体重秤、泡沫板、线手套、手术刀片和刀柄、牙周探针、4-0可吸收结扎丝线、灌胃针、大鼠固定器。
86.仪器:流式分析仪、ct扫描仪、离心机、超净台、coy厌氧培养箱。
87.2、牙周炎模型的建立spf级sd大鼠21只,体重180
±
20g,活动良好,无牙周病,大鼠腹腔注射10%水合氯醛300mg/kg麻醉后,选择双侧上颌第二磨牙用4-0可吸收医用丝线结扎于牙颈部,结扎丝线尽量放入龈沟内,遇结扎丝线脱落需要重新结扎。结扎后,每隔一天全口涂抹包裹于2%羧甲基纤维素钠溶液中的牙龈卟啉单胞菌(od 0.8-1),用高糖饲料(keyesdiet 2000)喂养,建
模第1、3、5、7、14、21、28天观察探针指数(pdd)、探诊出血指数(bop)、松动指数,4周后随机取一只建模大鼠和一只空白对照处死,测定血液中il-6浓度和tnf-α浓度,取上颌,在x射线观察牙槽骨吸收情况,取牙周组织固定,做病理切片,观察牙周组织病理变化,确定建模成功。
88.3、牙周炎治疗(1)菌株饲喂1)按照5%(v/w)的接种量分别接种编号为cb29y5的动物双歧杆菌zk-77、编号为cb13m2的唾液乳杆菌zk-88、唾液链球菌k12,于mrs培养基中37℃培养12h以上,制备菌液。
89.2)取100ml培养好的菌液离心,去上清,pbs缓冲液洗涤后,将菌重悬于100ml生理盐水中制备菌悬液,每隔三天更换饮水、用菌悬液饲喂大鼠。
90.其中,模型组3只,动物双歧杆菌组3只,唾液乳杆菌3只,唾液链球菌组 3只,空白对照组(即健康组)3只。
91.(2)饲料饲喂前两周饲喂高糖饲料,后面更换普通饲料。
92.4、结果(统计各组的平均值)图3为各组大鼠的体重统计图。由图可知,相对于模型组,cb29y5动物双歧杆菌和cb13m2唾液乳杆菌的处理有助于大鼠体重提升。
93.图4为各组大鼠的牙周指数。由图可知,相对于模型组,cb29y5动物双歧杆菌和cb13m2唾液乳杆菌的处理有效降低大鼠牙周指数。
94.图5为各组大鼠的血液炎症指标。由图可知,相对于模型组,cb29y5动物双歧杆菌能降低血液炎症因子il-6、il-10、mcp-1、ifn-γ和tfn,cb13m2唾液乳杆菌能降低血液炎症因子il-6、il-10、mcp-1、ifn-γ、tfn和il-12p70。
95.图6为牙槽骨3d光学扫描结果。统计大鼠牙根分叉出牙槽骨吸收情况:接种牙嘌呤单胞菌后,牙槽骨吸收情况明显变坏,益生菌干预能改善这一情况。
96.(二)益生菌对肠道等微生物的影响1、方法分别收集各组大鼠的粪便、龈沟冲洗液送测序公司进行16s rrna测序。
97.2、结果结果见图7、图8、图9和图10。
98.图7为肠道微生物16s rrna测序结果(粪便样本)。根据图7可知编号为cb29y5的动物双歧杆菌zk-77和编号为cb13m2的唾液乳杆菌zk-88的对大鼠肠道菌群多样性没有影响。
99.图8为大鼠粪便微生物聚类图,图中,b. ygy:牙嘌呤单胞菌 p. g w83+动物双歧杆菌b. a cb29y5,c.ygy:空白对照,l.ygy:牙嘌呤单胞菌p. g w83+唾液乳杆菌l.s cb13m2,p.ygy:牙嘌呤单胞菌p.g w83,s.ygy:牙嘌呤单胞菌p.g w83+唾液链球菌s.s k12(商业菌株)。根据图8可知编号为cb29y5的动物双歧杆菌zk-77和编号为cb13m2的唾液乳杆菌zk-88的对大鼠肠道菌群多样性没有影响。
100.图9为龈沟液微生物16s rrna测序结果(多样性无明显差异)。根据图9可知编号为cb29y5的动物双歧杆菌zk-77和编号为cb13m2的唾液乳杆菌zk-88的对大鼠口腔菌群多样性没有影响。
101.图10为大鼠龈沟液微生物聚类图。b.ygy:牙嘌呤单胞菌 p. g w83+动物双歧杆菌 b.acb29y5,c.ygy:空白对照,l.ygy:牙嘌呤单胞菌p.g w83+唾液乳杆菌l.s cb13m2,p.ygy:牙嘌呤单胞菌p. g w83,s.ygy:牙嘌呤单胞菌 p.g w83+唾液链球菌s. s k12(商业菌株)。根据图10可知编号为cb29y5的动物双歧杆菌zk-77和编号为cb13m2的唾液乳杆菌zk-88的对大鼠肠道菌群多样性没有影响。
102.以上所述实施例仅表达了本发明的几种实施方式,便于具体和详细地理解本发明的技术方案,但并不能因此而理解为对发明专利保护范围的限制。应当指出的是,对于本领域的普通技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改进,这些都属于本发明的保护范围。应当理解,本领域技术人员在本发明提供的技术方案的基础上,通过合乎逻辑的分析、推理或者有限的试验得到的技术方案,均在本发明所述附权利要求的保护范围内。因此,本发明专利的保护范围应以所附权利要求的内容为准,说明书及附图可以用于解释权利要求的内容。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1