一种单一调控机械特性的酸响应纳米凝胶的方法及用途
1.本发明涉及高分子材料制备方法及用途,特别涉及一种单一调控机械特性的酸响应纳米凝胶的方法与用途。
背景技术:
2.纳米载药系统如脂质体、胶束和聚合物纳米颗粒等常被用于提升药物的稳定性、溶解性,可通过增强的渗透和截留(epr)效应改善药代动力学参数、提高药物在病灶的积累能力并促进药物在靶部位的递送,在临床抗肿瘤应用中具有广阔的前景。例如,目前上市的纳米药物包括和等已被批准用于卵巢癌、乳腺癌、胰腺癌和白血病等癌症治疗。然而,这些纳米药物由于稳定性差、药物释放慢等原因难以达到理想的治疗效果。
3.理想的纳米药物应该具备长循环、有效的肿瘤积累、深度的肿瘤渗透、高效的细胞内化和快速药物释放等能力。研究表明,纳米粒子在体内递送各个阶段的效率取决于其物理化学性质,如大小、形状、组成、表面电荷和疏水性等,进而影响纳米药物的治疗效果。近年来,研究发现通过调节纳米颗粒的机械特性可以增强抗肿瘤药物体内递送效率,并已成功应用于多种肿瘤模型的治疗中。常用的改变颗粒机械硬度的方法如:增加颗粒外壁厚度、改变材料以及更换表面成分等,然而这些方法在改变纳米颗粒机械硬度的同时也会影响颗粒的表面特性、形貌及其他物理性质,难以达到单一调控药用载体的机械特性的目的,因此无法得到系统且具有普遍性的结论。为此设计一种在保证其他理化性质一致的同时单一改变颗粒机械特性的体系,用于研究硬度对药用载体在体内递送效果的影响具有重要意义。
4.水溶性聚合物通过交联方式形成的具有网状结构的纳米凝胶颗粒生物相容性好、修饰位点丰富、且可通过改变交联密度来控制其机械特性。凝胶的制备过程中常使用小分子交联剂、催化剂等添加剂,会造成凝胶中小分子残留、生物相容性差等缺点。
技术实现要素:
5.发明目的:本发明的目的是提供单一调控机械特性的酸响应纳米凝胶的方法。
6.本发明的另一目的是提供所述单一调控机械特性的酸响应纳米凝胶的用途。
7.技术方案:所述单一调控纳米凝胶机械特性的方法,不同比例的乙烯基醚丙烯酸酯及其衍生物与聚乙烯醇(pva)富含的羟基键通过酸响应型缩醛键连接,利用自身的化学交联反应制备出具有不同交联密度的纳米凝胶,在增加颗粒内部复杂程度的同时不改变其表面性质,实现对颗粒机械特性的单一调控。
8.本设计涉及两种体系,其一是将通过缩醛键连接不同比例丙烯酸酯的聚乙烯醇在紫外光作用下发生自由基反应交联形成纳米凝胶,另外是聚乙烯醇上修饰不同比例的巯基与聚乙烯醇上修饰的双键在碱性条件下发生迈克尔加成的自身交联,提出了两种单一调控机械特性的酸响应纳米凝胶体系。
9.进一步地,所述的聚乙烯醇分子量为8~100kda。
10.进一步地,所述聚乙烯醇接枝的乙烯基醚丙烯酸酯选自如下所示结构的化合物:
11.其中,n=2~5,r选自h或ch3。
12.进一步地,所述聚乙烯醇通过缩醛键连接的丙烯酸酯的比例为0.5%~8%。
13.进一步地,所述聚乙烯醇上修饰的巯基是通过接枝双巯基化合物实现的,如下所示结构的化合物:
[0014]14.其中,n=2~4;m=2~4;x=5~12。
[0015]
进一步地,所述聚乙烯醇上修饰的巯基官能团的比例为0.5%~8%。
[0016]
进一步地,所述自由基反应是聚乙烯醇上通过缩醛键连接的丙烯酸酯所提供丙烯双键,在紫外光和光引发剂的作用下发生碳碳双键之间的自由基反应。
[0017]
进一步地,所述迈克尔加成反应是聚乙烯醇上通过缩醛键连接的丙烯酸酯的双键被巯基修饰后,与聚乙烯醇-缩醛丙烯酸酯的碳碳双键在碱性条件下发生迈克尔加成反应。
[0018]
进一步地,所述不同机械特性的酸响应纳米凝胶体系是指将一系列缩醛键连接的聚乙烯醇(pva)衍生物在无交联剂条件下,利用两种自身的化学交联反应制备出具有不同交联密度的纳米凝胶,在增加颗粒内部复杂程度的同时不改变其表面性质,得到两种可单一调控纳米凝胶机械特性的体系。
[0019]
本发明是通过改变聚乙烯醇接枝小分子的比例,再利用自身的化学交联反应制备出具有不同交联密度的纳米凝胶。该体系制备的纳米凝胶载药体系在肿瘤酸性环境下,缩醛键会发生水解断裂,实现药物的靶向递送。
[0020]
该可调控机械特性酸响应纳米凝胶具有独特的酸响应三维交联网状结构,既保证了其高稳定性且在肿瘤部位酸性环境下可响应性解交联并释放药物,可广泛用于肿瘤的靶向治疗。
[0021]
本发明合成一系列缩醛键连接的聚乙烯醇衍生物,在不添加额外小分子交联剂情况下,利用自身的化学交联反应制备出具有不同交联密度的纳米凝胶,在增加颗粒内部复杂程度的同时不改变其表面性质,实现对颗粒机械特性的调控,为解决单一调控颗粒硬度的难题提供了关键思路。同时该纳米凝胶载药体系因缩醛键的存在,在肿瘤酸性环境下会发生裂解,实现药物的可控释放,为设计智能的肿瘤靶向治疗药用载体提供了重要的研究思路。
[0022]
有益效果:本发明与现有技术相比,具有如下优势:
[0023]
1、本发明的纳米凝胶可通过改变交联密度来实现对纳米颗粒机械性能的单一调控,可用于系统研究纳米颗粒机械性能对药物包载及释放、细胞内吞、体内循环、肿瘤富集和渗透等的影响,对于研究纳米颗粒与生物体相互作用机制具有重要的意义。
[0024]
2、该药物载体制备简单,反应温和,结构明确,无需额外添加交联剂,具有良好的
生物相容性。
[0025]
3、该纳米凝胶体系既保证了其高稳定性且在肿瘤部位酸性环境下可响应性解交联并释放药物,从而产生高效肿瘤治疗效果,在药物控制释放领域具有巨大的应用前景。
附图说明
[0026]
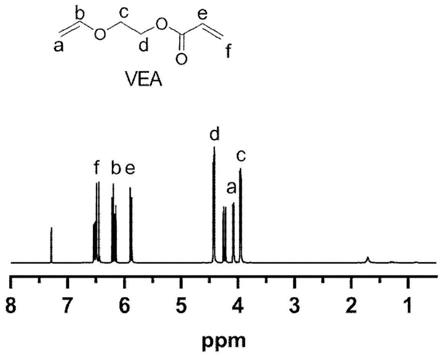
图1为实施例1中乙烯基醚丙烯酸酯(vea)的氢核磁图谱;
[0027]
图2为实施例1中聚乙烯醇-缩醛丙烯酸酯(pva-vea)的氢核磁谱图;
[0028]
图3为实施例2中巯基修饰的聚乙烯醇-缩醛丙烯酸酯(pva-vea-sh)的氢核磁谱图;
[0029]
图4为实施例4所得聚合物纳米凝胶pva-vea在不同酸性(ph5.0,ph7.4)条件下的粒径变化结果图;
[0030]
图5为实施例6所得两批不同交联度纳米凝胶对mcf-7肿瘤细胞的细胞毒性结果图。
具体实施方式
[0031]
实施例1合成酸敏感聚合物聚乙烯醇-缩醛丙烯酸酯(pva-vea)
[0032]
(1)合成小分子乙烯基乙醚丙烯酸酯(vea)
[0033][0034]
将乙二醇单乙烯基醚(80ml,0.908mol)溶于1200ml的二氯甲烷中,加入三乙胺(tea,160.4ml,1.20mol),随后在冰浴下缓慢滴加丙烯酰氯(90ml,1.088mol),滴加结束后,常温反应8h。反应结束后,过滤,用碳酸钠水溶液萃取两次,取有机相,用硫酸镁干燥后,过滤,旋蒸浓缩,最后经减压蒸馏得到无色有刺激气味液体乙烯基乙醚丙烯酸酯。产率:63.2%。氢核磁图谱如图1所示。
[0035]
(2)合成不同接枝率的酸敏感聚合物聚乙烯醇-缩醛-丙烯酸酯(pva-vea)
[0036][0037]
在氮气保护下,将聚乙烯醇pva(2.00g,25.5mmol的羟基)溶于50ml的无水二甲亚砜中,加入pva中羟基的30%、40%、66.67%、80%量的乙烯基乙醚丙烯酸酯,并加入催化量的ptsa,室温反应6h。反应结束后,加入300μl三乙胺(tea)终止反应。所得溶液经甲醇透析,减压蒸发浓缩,冰乙醚沉淀和冷冻真空干燥得到产物,核磁图谱如图2所示,对6-6.5ppm处双键氢特征峰积分,可确定pva上所接vea的比例分别为2%、4%和6%。
[0038]
实施例2合成巯基修饰的聚乙烯醇-缩醛-丙烯酸酯(pva-vea-sh)
[0039]
将200mg pva-vea溶解至2ml甲醇中,在氮气保护下,将pva-vea中双键二十倍当量的3,6-二氧杂-1,8-辛烷二硫醇(oc)溶解至1ml甲醇中,滴加30μl三乙胺,最后将pva-vea的甲醇溶液滴加至oc甲醇溶液中,常温密闭搅拌过夜,所得反应液经减压浓缩,乙醚沉淀和真空干燥得到产物,核磁图谱如图3所示,双键特征峰(6-6.5ppm)的消失,说明巯基将双键完
全取代。
[0040]
实施例3紫外交联法制备不同交联程度的纳米凝胶(pva-vea)
[0041]
(1)pva-vea
2%
纳米凝胶采用反向纳米沉淀法制备。在氮气保护条件下将200μl pva-vea
2%
(10mg/ml)水溶液,低温缓慢滴至10ml快速搅拌的丙酮中,随后加入5%聚合物质量的光引发剂i2959,紫外光照三十分钟后,加入4ml高纯水,经旋蒸和透析后得到0.5mg/ml的pva-vea
2%
纳米凝胶水溶液。动态光散射仪测得纳米凝胶平均粒径为159.09nm,粒径分布指数为0.09,平均zeta电位为-19.5mv。
[0042]
(2)pva-vea
4%
纳米凝胶采用反向纳米沉淀法制备。在氮气保护条件下将200μl pva-vea
4%
(10mg/ml)水溶液,低温缓慢滴至10ml快速搅拌的丙酮中,随后加入5%聚合物质量的光引发剂i2959,紫外光照三十分钟后,加入4ml高纯水,经旋蒸和透析后得到0.5mg/ml的pva-vea
4%
纳米凝胶水溶液。动态光散射仪测得纳米凝胶平均粒径为153.23nm,粒径分布指数为0.08,平均zeta电位为-22.5mv。
[0043]
(3)pva-vea
6%
纳米凝胶采用反向纳米沉淀法制备。在氮气保护条件下将200μl pva-vea
6%
(10mg/ml)水溶液,低温缓慢滴至10ml快速搅拌的丙酮中,随后加入5%聚合物质量的光引发剂i2959,紫外光照三十分钟后,加入4ml高纯水,经旋蒸和透析后得到0.5mg/ml的pva-vea
6%
纳米凝胶水溶液。动态光散射仪测得纳米凝胶平均粒径为159.99nm,粒径分布指数为0.04,平均zeta电位为-20.5mv。由表1可知,聚合物分子接枝不同比例丙烯酸酯基团在紫外作用下发生自由基交联反应制备得到不同交联密度的纳米颗粒,而纳米颗粒的尺寸(150nm左右)和表面电荷(-20mv左右)并未发生明显改变,说明这种通过改变内部复杂结构实现对颗粒的机械特性单一调控的方式是可行的。
[0044]
表1.紫外交联法制备的纳米凝胶的表征a[0045][0046]a纳米凝胶最终浓度为0.5mg/ml。
[0047]b平均粒径(nm)和粒径分布在25℃条件下通过动态光散射仪测定。
[0048]
实施例4迈克尔加成法制备不同交联密度的纳米凝胶(pva-vea-sh)
[0049]
(1)pva-vea
2%-sh
2%
纳米凝胶采用反向纳米沉淀法制备。将100μl pva-vea
2%
(10mg/ml)水溶液与100μl pva-vea
2%-sh
2%
(10mg/ml)水溶液涡旋混匀,在氮气保护条件下低温缓慢滴至10ml快速搅拌的丙酮中,之后加入5μl三乙胺(tea),静置反应12h。反应结束后加入10μl巯基乙醇(0.15g/ml)终止反应,静置30min后加入4ml高纯水,经旋蒸和透析后得到0.5mg/ml的pva-vea
2%-sh
2%
纳米凝胶水溶液。动态光散射仪测得纳米凝胶平均粒径为177.09nm,粒径分布指数为0.09,平均zeta电位为-1.8mv。
[0050]
(2)pva-vea
4%-sh
4%
纳米凝胶采用反向纳米沉淀法制备。将100μl pva-vea
4%
(10mg/ml)水溶液与100μl pva-vea
4%-sh
4%
(10mg/ml)水溶液涡旋混匀,在氮气保护条件下低温缓慢滴至10ml快速搅拌的丙酮中,之后加入5μl三乙胺(tea),静置反应12h。反应结束
后加入10μl巯基乙醇(0.15g/ml)终止反应,静置30min后加入4ml高纯水,经旋蒸和透析后得到0.5mg/ml的pva-vea
4%-sh
4%
纳米凝胶水溶液。动态光散射仪测得纳米凝胶平均粒径为171.44nm,粒径分布指数为0.08,平均zeta电位为-1.1mv。
[0051]
(3)pva-vea
6%-sh
6%
纳米凝胶采用反向纳米沉淀法制备。将100μl pva-vea
6%
(10mg/ml)水溶液与100μl pva-vea
6%-sh
6%
(10mg/ml)水溶液涡旋混匀,在氮气保护条件下低温缓慢滴至10ml快速搅拌的丙酮中,之后加入5μl三乙胺(tea),静置反应12h。反应结束后加入10μl巯基乙醇(0.15g/ml)终止反应,静置30min后加入4ml高纯水,经旋蒸和透析后得到0.5mg/ml的pva-vea
6%-sh
6%
纳米凝胶水溶液。动态光散射仪测得纳米凝胶平均粒径为168.52nm,粒径分布指数为0.04,平均zeta电位为-2.5mv。由表2可知,接枝不同比例巯基的聚合物与接枝不同比例丙烯酸酯聚合物在碱性条件下发生迈克尔加成反应得到具有不同交联密度的纳米凝胶,而纳米凝胶的尺寸(170nm左右)和表面电荷(-1.8mv左右)并未发生明显变化,说明这种通过改变内部复杂结构实现对颗粒的机械特性单一调控的方式是可行的。
[0052]
表2.迈克尔加成反应法制备的纳米凝胶的表征c[0053][0054]c纳米凝胶最终浓度为0.5mg/ml。
[0055]d平均粒径(nm)和粒径分布在25℃条件下通过动态光散射仪测定。
[0056]
实施例5酸性条件下使聚合物纳米凝胶(pva-vea)解交联
[0057]
分别准备两份聚合物纳米凝胶溶液(pva-vea
6%
,1ml,0.5mg/ml)并加入到玻璃样品池中,向其中一个样品池中加入一定量盐酸溶液使胶束溶液最终ph为5.0,另一个样品池中加入等量ph7.4磷酸盐缓冲溶液使胶束溶液最终ph为7.4,然后玻璃样品池用橡胶塞封住,并置于37℃恒温摇床(200rpm)中,在选定时间和37℃条件下,通过动态激光光散射(dls)来监测纳米凝胶的粒径变化。图4为聚合物纳米凝胶(pva-vea
6%
)在不同ph条件下放置不同时间的粒径变化图。结果表明,在ph7.4条件下,纳米凝胶在放置12小时后粒径没有发生明显变化,而在ph5.0条件下放置6小时纳米凝胶粒径明显变大,出现了两个大粒径峰,说明纳米凝胶发生了部分解交联和溶胀。
[0058]
实施例6两种交联方法制备的不同交联度纳米凝胶(pva-vea/pva-vea-sh)对mcf-7细胞毒性测试
[0059]
纳米凝胶在mcf-7细胞中的毒性通过mtt法测定。首先将100μl细胞的dmem悬浮液(dmem培养基中含10%胎牛血清、100iu/ml青霉素和100g/ml链霉素)铺于96孔培养板中,并置于37℃,5%二氧化碳条件下培养12h使单层细胞的覆盖率达到70~80%。然后向每孔中加入10μl不同浓度的纳米凝胶的水溶液。待继续培养24h后,向每孔中加入10μl 3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐(mtt)的pbs溶液(5mg/ml),并放入培养箱继续培养4h以使mtt与活细胞作用。随后移除含有mtt的培养液,向每孔中加入150μl dmso以溶解活细
胞与mtt产生的紫色甲瓒结晶,并使用酶标仪(spectramaxi3x)测定每个孔在570nm处的紫外吸收。细胞相对存活率通过与只有空白细胞的对照孔在570nm处的吸收相比得到。实验数据均是平行三组得到的。
[0060]
细胞存活率(%)=(od570样品/od570对照)
×
100%
[0061]
图5为两批不同交联度纳米凝胶(pva-vea/pva-vea-sh)对mcf-7细胞毒性结果图。结果表明:两种交联方法制备的不同交联度的纳米凝胶在设置浓度下对细胞都几乎没有毒性,说明本设计中制备的纳米凝胶体系具有良好的生物相容性,可用作药用载体的研究。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1