Wee1的大环类抑制剂的制作方法
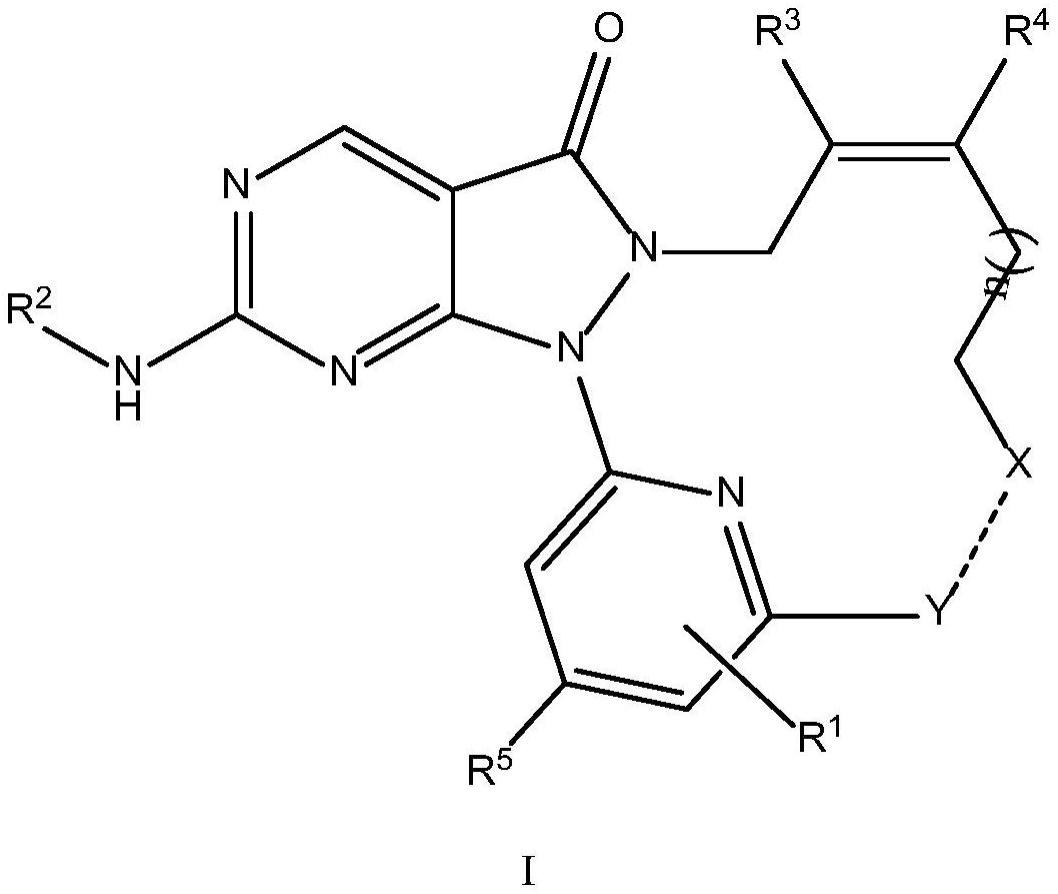
本发明涉及一种wee1的大环类抑制剂、及其制备方法、药物组合物及应用。
背景技术:
1、wee1(wee1 g2检测点激酶;基因编号:7465)是丝氨酸/苏氨酸蛋白激酶家族中的一员,可直接磷酸化细胞周期蛋白依赖性激酶1(cdk1),磷酸化位点为cdk1的酪氨酸15残基,该位点是一个抑制性磷酸化位点,对cdk1活性起消极调节作用。g2检测点的激活主要是通过抑制有丝分裂,促进细胞周期蛋白b-cdk1复合物。正常细胞在g1逮捕期内对损伤的dna进行修复,然而癌细胞g1-s检测点常常缺失,需要依靠g2-m检测点的功能来进行dna修复。例如,p53缺陷肿瘤细胞缺乏g1检测点的功能,因而依赖g2检测点作为细胞周期停滞对dna损伤进行应答反应。dna受损后,g2检测点阻止受损细胞进入有丝分裂,进而保护其免受有丝分裂灾难及细胞凋亡。wee1是g2检测点功能发挥中必不可少的因素。通过wee1抑制剂来废除g2检测点可能选择性的使p53缺陷性癌细胞对dna损伤敏感,避免对周围正常组织产生影响。wee1也调节s期的cdk活性,阻止正常的s期进程中dna损伤的诱导。此外,wee1在同源重组(hr)修复中起积极调解作用,同源重组修复是dna双链断裂修复的重要路径。
2、wee1在多种癌症类型中高度表达,包括肝细胞癌,乳腺癌,宫颈癌,肺癌,鳞状细胞癌,桥内弥漫性脑胶质瘤[dipg],胶质母细胞瘤,成神经管细胞瘤,白血病,黑色素瘤和卵巢癌。wee1的高表达已经在一些癌症中被报道,以响应升高的复制压力,并且已经与肿瘤进展和无病存活率差相关联。而在非小细胞肺癌中,缺乏wee1表达与预后不良相关。这些研究表明,缺乏wee1表达的癌症易于发生遗传畸变,并且可能对dna损伤性药物的敏感性增加,用这些药剂治疗可能诱导wee1的表达。相比之下,表达wee1的肿瘤细胞可能更依赖于完整的g2-m检查点得以存活和进行有丝分裂。因此,抑制wee1激酶活性可能使依赖于功能性g2-m检查点的癌症对dna损伤疗法更敏感.
3、虽然wee1激酶活性对肿瘤细胞的信号传导中起着至关重要的作用。迄今为止,已经进入到临床研究wee1小分子抑制剂却很少,因此需要进一步开发wee1小分子抑制剂,以满足临床未满足的用药需求。
技术实现思路
1、本发明的目的在于提供如式i所示的化合物、其异构体或其药学上可接受的盐:
2、
3、其中,
4、r1和r5独立选自氢、卤素、羟基、氰基、硝基、巯基、-nrarb、-oc(o)ra、-oc(o)ora、-oc(o)nrarb、-c(o)ora、-c(o)ra、-c(o)nrarb、-nhc(o)ra、-nhc(o)ora、-nhc(o)nrarb、-nhs(o)2ra、-nhc(=nh)ra、-nhc(=nh)nrarb、-s(o)ra、-s(o)2ra、-s(o)2nrarb、-nhs(o)2nrarb、c1-c6烷基、(c1-c6烷基)-o-、(c1-c6烷基)-s-、c2-c6炔基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基,所述c1-c6烷基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基本身或作为另一基团的一部分任选地被卤素、氰基、羟基、-nrarb、c1-c3烷基或c1-c3烷基氧基取代;
5、或者,r1和r5与其相互连接碳原子形成a环,所述a环为取代或未取代的c3-15环烷基、3-15元杂环烷基,c6-c12芳基、5-12元杂芳基,所述a环可被氢、卤素、羟基、氰基、硝基、巯基、-nrarb、c1-c6烷基、(c1-c6烷基)-o-、(c1-c6烷基)-s-、c2-c6炔基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基取代,所述c1-c6烷基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基本身或作为另一基团的一部分任选地被卤素、氰基、羟基、-nrarb、c1-c3烷基或c1-c3烷基氧基取代;
6、r2为c6-c12芳基、5-12元杂芳基、c3-c8环烷基或4-14元杂环烷基,其中所述基团任选地被卤素、羟基、氰基、硝基、巯基、-nrarb、-oc(o)ra、-oc(o)ora、-oc(o)nrarb、-c(o)ora、-c(o)ra、-c(o)nrarb、-nhc(o)ra、-nhc(o)ora、-nhc(o)nrarb、-nhs(o)2ra、-nhc(=nh)ra、-nhc(=nh)nrarb、-s(o)ra、-s(o)2ra、-s(o)2nrarb、-nhs(o)2nrarb、c1-c6烷基、(c1-c6烷基)-o-、(c1-c6烷基)-s-、c2-c6炔基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基取代,所述c1-c6烷基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基本身或作为另一基团的一部分任选地被卤素、氰基、羟基、-nrarb、c1-c3烷基或c1-c3烷基氧基取代;
7、r3和r4分别独立地选自h、卤素、羟基、氰基、氨基或c1-c3烷基,所述c1-c3烷基任选被卤素、羟基或氨基取代;
8、选自:或-g-,其中g是5-10元杂环基或5-10元杂芳基,所述基团任选地被卤素、羟基、氰基、硝基、巯基、-nrarb、-oc(o)ra、-oc(o)ora、-oc(o)nrarb、-c(o)ora、-c(o)ra、-c(o)nrarb、-nhc(o)ra、-nhc(o)ora、-nhc(o)nrarb、-nhs(o)2ra、-nhc(=nh)ra、-nhc(=nh)nrarb、-s(o)ra、-s(o)2ra、-s(o)2nrarb、-nhs(o)2nrarb、c1-c6烷基、(c1-c6烷基)-o-、(c1-c6烷基)-s-、c2-c6炔基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基取代,其中所述c1-c6烷基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基本身或作为另一基团的一部分任选地被卤素、氰基、羟基、-nrarb、c1-c3烷基或c1-c3烷基氧基取代;
9、n为0~2的整数;
10、ra和rb各自独立地任选自氢、c1-c6烷基、卤代c1-c6烷基、c3-c8环烷基、3-8元杂环烷基、苯基、5-10元杂芳基、3-8元杂环烷基c1-c6烷基、c3-8环烷基c1-c6烷基、苯基c1-c6烷基或5-10元杂芳基c1-6烷基。
11、在本发明优选的实施方案中,式i所示的化合物进一步如式ii-1或式ii-2所述:
12、
13、m1、m2、m3、m4和m5各自独立地选自n、o或c;
14、------为单键或双键;
15、r6和r7各自独立选自氢、卤素、羟基、氰基、硝基、巯基、-nrarb、-oc(o)ra、-oc(o)ora、-oc(o)nrarb、-c(o)ora、-c(o)ra、-c(o)nrarb、-nhc(o)ra、-nhc(o)ora、-nhc(o)nrarb、-nhs(o)2ra、-nhc(=nh)ra、-nhc(=nh)nrarb、-s(o)ra、-s(o)2ra、-s(o)2nrarb、-nhs(o)2nrarb、c1-c6烷基、c1-c6卤代烷基、(c1-c6烷基)-o-、(c1-c6烷基)-s-、c2-c6炔基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基,所述c1-c6烷基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基本身或作为另一基团的一部分任选地被卤素、氰基、羟基、-nrarb、c1-c3烷基或c1-c3烷基氧基取代;
16、m为0、1、2或3;
17、p选自0或1;
18、r1、r2、r3、r4、r5、n、ra和rb如通式i所述。
19、在一些实施方案中,r2选自苯基、其中所述基团任选地被卤素、羟基、氰基、硝基、巯基、-nrarb、-oc(o)ra、-oc(o)ora、-oc(o)nrarb、-c(o)ora、-c(o)ra、-c(o)nrarb、-nhc(o)ra、-nhc(o)ora、-nhc(o)nrarb、-nhs(o)2ra、-nhc(=nh)ra、-nhc(=nh)nrarb、-s(o)ra、-s(o)2ra、-s(o)2nrarb、-nhs(o)2nrarb、c1-c6烷基、(c1-c6烷基)-o-、(c1-c6烷基)-s-、c2-c6炔基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基取代,所述c1-c6烷基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基本身或作为另一基团的一部分任选地被卤素、氰基、羟基、-nrarb、c1-c3烷基或c1-c3烷基氧基取代。
20、在一些实施方案中,r2选自苯基、其中所述基团任选地被卤素、羟基、氰基、硝基、巯基、-nrarb、-oc(o)ra、-oc(o)ora、-oc(o)nrarb、-c(o)ora、-c(o)ra、-c(o)nrarb、-nhc(o)ra、-nhc(o)ora、-nhc(o)nrarb、-nhs(o)2ra、-nhc(=nh)ra、-nhc(=nh)nrarb、-s(o)ra、-s(o)2ra、-s(o)2nrarb、-nhs(o)2nrarb、c1-c6烷基、(c1-c6烷基)-o-、(c1-c6烷基)-s-、c2-c6炔基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基取代,所述c1-c6烷基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基本身或作为另一基团的一部分任选地被卤素、氰基、羟基、-nrarb、c1-c3烷基或c1-c3烷基氧基取代。
21、在一些实施方案中,r2选自苯基、其中所述基团任选地被甲基、
22、在一些实施方案中,r2为
23、在一些典型的实施方案中,r2为
24、在本发明优选的实施方案中,所示的化合物进一步如式iii-1或式iii-2所述
25、
26、r8选自h、卤素、羟基、氰基、氨基或c1-c3烷基。
27、在一些实施方案中,r3和r4分别独立地选自h、卤素、羟基、氰基、氨基或c1-c3烷基。
28、在一些典型的实施方案中,r3和r4分别独立地选自h、氟、氯或甲基。
29、在一些典型的实施方案中,r3和r4分别选自h。
30、在一些实施方案中,选自:其中,r6选自氢或c1-c6烷基,所述c1-c6烷基本身或作为另一基团的一部分任选地被卤素、氰基、羟基、-nrarb、c1-c3烷基或c1-c3烷基氧基取代;在一些典型的实施方案中,r6选自氢、甲基、乙基或异丙基。
31、在一些典型的实施方案中,选自:
32、在一些典型的实施方案中,选自:
33、在一些实施方案中,选自其中r7选自氢、羟基、氰基、c1-c6烷基,所述c1-c6烷基本身或作为另一基团的一部分任选地被卤素、氰基、羟基、-nrarb、c1-c3烷基或c1-c3烷基氧基取代;在一些典型的实施方案中,r7选自甲基、乙基、异丙基、氰基或三氟甲基。
34、在一些实施方案中,选自
35、在一些实施方案中,选自
36、在一些典型的实施方案中,选自
37、在一些实施方案中,r1和r5独立选自氢、卤素、羟基、氰基、硝基、巯基、-nrarb、c1-c6烷基、(c1-c6烷基)-o-、(c1-c6烷基)-s-、c2-c6炔基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基,所述c1-c6烷基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基本身或作为另一基团的一部分任选地被卤素、氰基、羟基、-nrarb、c1-c3烷基或c1-c3烷基氧基取代;或者,r1和r5与其相互连接碳原子形成苯环,所述苯环可被氢、卤素、羟基、氰基、硝基、巯基、-nrarb、c1-c6烷基、(c1-c6烷基)-o-、(c1-c6烷基)-s-、c2-c6炔基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基,所述c1-c6烷基、c2-c6烯基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基本身或作为另一基团的一部分任选地被卤素、氰基、羟基、-nrarb、c1-c3烷基或c1-c3烷基氧基取代。
38、在一些实施方案中,r1和r5独立选自氢、卤素、羟基、氰基、硝基、巯基、-nrarb、c1-c6烷基;或者r1和r5与其相互连接碳原子形成苯环,所述苯环可被氢、卤素、-nrarb、羟基、氰基或c1-c6烷基取代。
39、在一些实施方案中,r1选自氢、c1-c6烷基或卤素。
40、在一些实施方案中,r1选自氢、甲基或氟。
41、在一些实施方案中,r1和r5与其相互连接碳原子形成苯环。
42、在一些实施方案中,n为0或1。
43、另一方面,本发明提供下列化合物或其药学上可接受的盐:
44、
45、在一些实施方案中,本发明的式i、ii-1、ii-2、iii-1或iii-2所示化合物上的氢任选地被氘取代。
46、在一些实施方案中,本发明还提供一种制备所述化合物的方法,包括但不限于以下步骤:
47、
48、z选自卤素,优选氟、氯、溴或碘;r1、r2、r3、r4、r5和n如前所述。
49、另一方面,本发明提供一种制备式(i)化合物的方法,包括但不限于以下合成方案:
50、合成方案1:
51、
52、式1-1化合物与式1-2化合物在碱性条件下反应得式1-3化合物;式1-3化合物在酸性条件下脱保护基得式1-4化合物;式1-4化合物在碱性条件下进行环合反应得式1-5化合物。
53、合成方案2:
54、
55、r1和r5的定义如前所述;rc选自c1-c6烷基、c6-c12芳基、c3-c10环烷基、3-12元杂环烷基或5-12元杂芳基,所述基团任选地被卤素、氰基、羟基、-nrarb、c1-c3烷基或c1-c3烷基氧基取代;x选自氯、溴和碘;q选自1或2。
56、式2-1化合物与式2-2化合物在碱性条件下反应得式2-3化合物;式2-3化合物与式2-4化合物在碱性条件下反应得式2-5化合物;式2-5化合物与式1-5化合物反应得到式2-6化合物;式2-6化合物进行环合反应得式2-7化合物;式2-7化合物与4-(4-甲基哌嗪-1-基)苯胺反应得式2-8化合物。
57、合成方案3:
58、
59、式3-1化合物进行氧化得到式3-2化合物;式3-2化合物进行溴代得式3-3化合物;式3-3化合物水解得到式3-4化合物;式3-4化合物与式3-5化合物在碱性条件下反应得式3-6化合物;式3-6化合物与式1-5化合物反应得到式3-7化合物;式3-7化合物进行环合反应得式3-8化合物;式3-8化合物与4-(4-甲基哌嗪-1-基)苯胺反应得式3-9化合物。
60、合成方案4:
61、
62、式4-1化合物与水合肼反应得式4-2化合物;式4-2化合物与1,1-二甲氧基-n,n-二甲基甲胺反应得式4-3化合物;式4-3化合物与丁-3-烯基-1-胺进行环合得式4-4化合物;式4-4化合物与式1-5化合物反应得到式4-5化合物;式4-5化合物进行环合反应得式4-6化合物;式4-6化合物与4-(4-甲基哌嗪-1-基)苯胺反应得式4-7化合物。
63、合成方案5:
64、
65、式5-1化合物与4-溴-1-丁烯反应得式5-2化合物;式5-2化合物与硼酸三异丙酯在碱性条件下反应得式5-3化合物;式5-3化合物与2,6-二溴吡啶反应得式5-4化合物;式5-4化合物与式1-5化合物反应得到式5-5化合物;式5-5化合物进行环合反应得式5-6化合物;式5-6化合物与4-(4-甲基哌嗪-1-基)苯胺反应得式5-7化合物。
66、合成方案6:
67、
68、式6-1化合物与4-溴-1-丁烯在碱性条件下反应得式6-2化合物;式6-2化合物与6-溴吡啶甲醛进行环合反应得式6-3化合物;式6-3化合物与式1-5化合物反应得到式6-4化合物;式6-4化合物进行环合反应得式6-5化合物;式6-5化合物与4-(4-甲基哌嗪-1-基)苯胺反应得式6-6化合物。
69、合成方案7:
70、
71、rd选自h,溴,甲基;re选自h,甲基,三氟甲基。
72、式7-1化合物在甲醇钠,甲醇和氯化铵存在下反应得式7-2化合物;式7-2化合物与式7-3化合物进行环合反应得式7-4化合物;式7-4化合物与4-溴-1-丁烯反应得式7-5化合物;式7-5化合物与式1-5化合物反应得到式7-6化合物;式7-6化合物进行环合反应得式7-7化合物;式7-7化合物与4-(4-甲基哌嗪-1-基)苯胺反应得式7-8化合物。
73、在一些实施方案中,本发明还提供了一种药物组合物,其包括治疗有效量的活性组分以及药学上可接受的辅料;所述活性组分包括如式i、ii-1、ii-2、iii-1或iii-2所示化合物、其异构体、前药、稳定的同位素衍生物和药学上可接受的盐中的一种或多种。
74、在一些实施方案中,所述药物组合物中,所述活性组分还可包括癌症、病毒感染或自身免疫疾病的其它治疗剂。
75、在一些实施方案中,所述其他种类的治疗剂包括微管蛋白抑制剂、烷化剂、拓扑酶抑制剂、铂类化合物、抗生素、抗代谢类药物、激素和激素类药物、靶向治疗药物、免疫治疗剂和干扰素中的一种或多种。
76、在一些实施方案中,所述药物组合物中,所述药学上可接受的辅料可包括药学上可接受的载体、稀释剂和/或赋形剂。
77、在一些实施方案中,本发明还提供了如式i、ii-1、ii-2、iii-1或iii-2所示化合物、其异构体、前药、稳定的同位素衍生物或药学上可接受的盐,或所述药物组合物在制备wee1抑制剂中的应用。
78、在一些实施方案中,本发明还提供了如式i、ii-1、ii-2、iii-1或iii-2所示化合物、其异构体、前药、稳定的同位素衍生物或药学上可接受的盐,或所述药物组合物在制备癌症的化学疗法或放射性疗法的增敏剂中的应用。其中,所述化学疗法或放射线疗法的增敏剂是指在癌症治疗领域中个,通过与放射线疗法和/或使用抗癌剂的化学疗法组合使用,相加地或协同地提高这些放射线疗法和/或化学疗法的治疗效果的药物
79、在一些实施方案中,本发明还提供了如式i、ii-1、ii-2、iii-1或iii-2所示化合物、其异构体、前药、稳定的同位素衍生物或药学上可接受的盐,或所述药物组合物在制备治疗和/或缓解由wee1介导的相关疾病的药物中的应用;本发明优选提供了如式i、ii-1、ii-2、iii-1或iii-2所示化合物、其异构体、前药、稳定的同位素衍生物或药学上可接受的盐,或所述药物组合物在制备治疗和/或预防由wee1介导的相关疾病的药物中的应用。
80、在一些实施方案中,所述的wee1介导的相关疾病包括癌症、代谢性疾病、免疫性疾病;优选地,所述癌症包括肺癌、胃癌、乳腺癌、膀胱癌、胰腺癌、直肠癌、肝癌、血癌、卵巢癌、结肠癌、皮肤癌和头颈癌,所述代谢性疾病包括糖尿病、高血脂、肥胖和冠心病,所述免疫性疾病包括风湿性关节炎、红斑狼疮和银屑病。
81、在一些实施方案中,所述疾病包括肿瘤和非肿瘤性疾病。所述疾病优选为癌症。
82、在一些实施方案中,本发明优选用所述如式i、ii-1、ii-2、iii-1或iii-2所示化合物、其异构体、前药、稳定的同位素衍生物或药学上可接受的盐,或所述药物组合物在制备治疗和/或缓解癌症药物中的应用。
83、在一些实施方案中,本发明还进一步提供了所述如式i、ii-1、ii-2、iii-1或iii-2所示化合物、其异构体、前药、稳定的同位素衍生物或药学上可接受的盐,或所述药物组合物还可和一种或多种其它种类的治疗剂和/或治疗方法联合用于治疗和/或缓解由wee1介导的相关疾病,所述的疾病优选为癌症。
84、相关定义
85、除非有特定说明,下列用在说明书和权利要求书中的术语具有下述含义:
86、术语“任选”或“任选地”是指随后描述的事件或情况可能发生或可能不发生,该描述包括发生所述事件或情况和不发生所述事件或情况。
87、中的是指化学键连接处。当双环或多环中出现且连接位置不确定的情况下,表示连接位点仅限于所在的单环上的任意原子,只要原子价容许。例如,表示连接位点位于该环中任意原子,且需满足原子价键的要求。
88、单波线与双波线均是指化学键连接处,两者具有相同的化学意义,如无特殊说明,与的区别仅在于区分连接的位置或顺序。
89、------为单键或双键。
90、本文中的数字范围,是指给定范围中的各个整数。例如,“c1-c6”是指该基团可具有1个碳原子、2个碳原子、3个碳原子、4个碳原子、5个碳原子或6个碳原子。
91、术语“被取代”是指特定基团上的任意一个或多个氢原子被取代基取代,只要特定基团的价态是正常的并且取代后的化合物是稳定的。例如,“被卤素取代”是指特定基团上的任意一个或多个氢原子被卤素取代,只要特定基团的价态是正常的并且取代后的化合物是稳定的。
92、术语“烷基”是指包含1-20个碳原子的饱和直链或支链烃基,优选1-10个碳原子,更优选1-8,1-6,1-4,或1-3个碳原子,烷基的代表性例子包括但不限于:甲基、乙基、正丙基、异丙基、正丁基、仲丁基、叔丁基、异丁基、戊基、己基、庚基、辛基、壬基、癸基、4,4-二甲基戊基、2,2,4-三甲基戊基、十一烷基、十二烷基,及它们的各种异构体等。
93、术语“环烷基”是指包含3-20个碳原子的饱和或部分不饱和(包含1或2个双键)的单环或多环基团。“单环环烷基”优选3-10元单环烷基,更优选3-8元单环烷基,例如:环丙基、环丁基、环戊基、环己基、环庚基、环辛基、环癸基、环十二烷基、环己烯基。“多环环烷基”包括“桥环基”、“稠合环烷基”和“螺环烷基”,“桥环基”的代表性例子包括但不限于:冰片基、双环[2.2.1]庚烯基、双环[3.1.1]庚烷基、双环[2.2.1]庚烷基、双环[2.2.2]辛烷基、双环[3.2.2]壬烷基、双环[3.3.1]壬烷基、双环[4.2.1]壬烷基和金刚烷基等。“稠合环烷基”包含稠合到苯基、环烷基、或杂芳基上的环烷基环,稠合环烷基包括但不限于:苯并环丁烯、2,3-二氢-1-h-茚、2,3-环戊烯并吡啶、5,6-二氢-4h-环戊基[b]噻吩、十氢萘等。“螺环烷基”是指两个单环环烷基共用一个碳原子形成的双环基团,螺环烷基包括但不限于:螺[2,5]辛基、螺[2,4]庚基、螺[4,5]癸基等。所述多环环烷基优选包含7~12个碳原子。单环环烷基或多环环烷基可以通过环上任意的1个或2个碳原子链接到母体分子上。
94、述语“杂环基”意指稳定的含杂原子或杂原子团的单环、双环或三环,它们可以是饱和的、部分不饱和的或不饱和的(芳族的),它们包含碳原子和1、2、3或4个独立地选自n、0和s的环杂原子,其中上述任意杂环可以稠合到一个苯环上形成双环。氮和硫杂原子可任选被氧化(即no和s(0)p,p是1或2)。氮原子可以是被取代的或未取代的。该杂环可以附着到任何杂原子或碳原子的侧基上从而形成稳定的结构。如果产生的化合物是稳定的,本文所述的杂环可以发生碳位或氮位上的取代。杂环中的氮原子任选地被季铵化。
95、术语“杂环烷基”指由碳原子以及选自氮、氧或硫等杂原子组成的饱和或部分不饱和(包含1或2个双键)的非芳香环状基团,此环状基团可为单环或多环基团,在本发明中,杂环烷基中杂原子个数优选1、2、3或4,杂环烷基中的氮、碳或硫原子可任选地被氧化。氮原子可任选进一步被其他基团取代而形成叔胺或季铵盐。“单环杂环烷基”优选3-10元单环杂环烷基,更优选3-8元单环杂环烷基。例如:氮丙啶基、四氢呋喃-2-基、吗啉-4-基、硫代吗啉-4-基、硫代吗啉-s-氧化物-4-基、哌啶-1-基、n-烷基哌啶-4-基、吡咯烷-1-基、n-烷基吡咯烷-2-基、哌嗪-1-基、4-烷基哌嗪-1-基等。“多环杂环烷基”包括“稠合杂环烷基”、“螺杂环基”和“桥杂环烷基”。“稠合杂环烷基”包含稠合到苯基、环烷基、杂环烷基或杂芳基的单环杂环烷基环,稠合杂环烷基包括但不限于:2,3-二氢苯并呋喃基、1,3-二氢异苯并呋喃基、二氢吲哚基、2,3-二氢苯并[b]噻吩基、二氢苯并哌喃基、1,2,3,4-四氢喹啉基等。“螺杂环基”是指两个杂环烷基或一个环烷基和一个杂环烷基共用一个碳原子形成的双环基团,螺杂环基包括但不限于:5-氮杂[2.5]辛基、4-氮杂[2.5]辛基、4-氮杂[2.4]庚基等,所述多环杂环烷基优选7-15元,更优选7-12元。单环杂环烷基和多环杂环烷基可以通过环上任意的1个或2个环原子链接到母体分子上。上述环原子特指组成环骨架的碳原子和/或氮原子。
96、术语“芳基”是指任何稳定的6-20元单环或多环芳香族基团,例如:苯基、萘基、四氢萘基、2,3-二氢化茚基、或联苯基等。
97、术语“杂芳基”是指至少1个环上的碳原子被选自氮、氧或硫的杂原子置换所形成的芳香环基团,其可为5-7元单环结构或7-20稠合环结构,优选5-6元单环杂芳基和8-10元稠环杂芳基。在本发明中,杂原子个数优选1、2或3,包括:吡啶基、嘧啶基、哌嗪基、哒嗪-3(2h)-酮基、呋喃基、噻吩基、噻唑基、吡咯基、咪唑基、吡唑基、噁唑基、异噁唑基、1,2,5-噁二唑基、1,2,4-噁二唑基、1,3,4-噁二唑基、1,3,4-噻二唑、1,2,4-三氮唑基、1,2,3-三氮唑基、四氮唑基、吲唑基、异吲唑基、吲哚基、异吲哚基、苯并呋喃基、苯并噻吩基、苯并[d][1,3]二氧戊环基、苯并噻唑基、苯并噁唑基、喹啉基、异喹啉基、异喹啉酮基、喹唑啉基、4-羟基噻吩并[3,2-c]吡啶基、4,5-二氢-4-氧代呋喃[3,2]吡啶基、4-羟基-5-氮杂吲哚基、呋喃[2,3-c]并吡啶-7(6h)-酮基、噻吩[2,3-c]并吡啶-7(6h)-酮基、1,2,3,4-四氢吡咯并[1,2-a]吡嗪等。
98、术语“卤素”表示氟、氯、溴或碘。
99、术语“卤代c1-c6烷基”是指被卤素任意取代的c1-c6烷基。
100、本发明所述“室温”是指15-30℃。
101、所述的同位素取代衍生物包括:式i中任意的氢原子被1-5个氘原子取代得到的同位素取代衍生物、式i中任意的碳原子被1-3个碳14原子取代得到的同位素取代衍生物或式i中任意的氧原子被1-3个氧18原子取代得到的同位素取代衍生物。
102、所述的“前药”是指化合物在体内代谢后转换成原始活性化合物。代表性地讲,前药为非活性物质,或者比活性母体化合物活性小,但可以提供方便的操作、给药或者改善代谢特性。
103、所述的“药学上可接受的盐”是指保留了特定化合物的游离酸和碱的生物学效力而没有生物学不良作用的盐。例如酸(包括有机酸和无机酸)加成盐或碱加成盐(包括有机碱和无机碱)。
104、本发明的药学上可接受的盐可由含有酸根或碱基的母体化合物通过常规化学方法合成。一般情况下,这样的盐的制备方法是:在水或有机溶剂或两者的混合物中,经由游离酸或碱形式的这些化合物与化学计量的适当的碱或酸反应来制备。
105、术语“药学上可接受的载体”是指对机体无明显刺激作用,而且不会损害该活性化合物的生物活性及性能的那些载体。包括但不限于国家食品药品监督管理局许可的可用于人或动物的任何稀释剂、崩解剂、粘合剂、助流剂、润湿剂。
106、权利要求书和说明书中所使用的简称其含义如下:
107、m:mol/l;
108、mm:mmol/l;
109、μm:μmol/l;
110、nm:nmol/l;
111、lcms:液相色谱-质谱联用技术
- 还没有人留言评论。精彩留言会获得点赞!