一种用于免疫细胞改造的截短型gRNA、基因编辑系统、免疫细胞及应用
本发明属于基因修饰领域,具体涉及一种用于免疫细胞改造的截短型grna、基因编辑系统、免疫细胞及应用。
背景技术:
1、目前car-t细胞治疗技术,以及新兴的car-nk、tcr-t及car-m等细胞治疗技术,在恶性肿瘤的治疗中展示出了强大的治疗效果。这些免疫细胞识别肿瘤靶标所依靠的是免疫细胞上面装载的嵌合抗原受体(chimeric antigen receptor,car)或tcr受体等。这些人工装载受体的特异性通常是由胞外的抗体结构域部分所决定的,这些抗体虽然赋予了免疫细胞良好的靶向性,同样也带来了其它一系列问题,例如,提高了免疫细胞的异源性,导致输入病人体内的免疫细胞被快速清除;或者由于抗体自身的特性,如scfv抗体之间的相互交联特性,导致免疫细胞产生较高的本底激活而快速发生功能耗竭。这就要求我们采用新的技术来替代传统抗体的应用,从而避开这些传统抗体所产生的弊端。
技术实现思路
1、本发明的目的是提供一种用于免疫细胞改造的截短型grna,可实现靶基因的建库或功能干扰,从而达到改良免疫细胞功能的目的。
2、本发明的第二个目的是提供一种用于免疫细胞改造的基因编辑系统。
3、本发明的第三个目的是提供一种利用上述基因编辑系统对免疫细胞改造得到的改造免疫细胞。
4、本发明的第四个目的是提供上述截短型grna、基因编辑系统、改造免疫细胞的应用。
5、为了实现以上目的,本发明所采用的技术方案是:
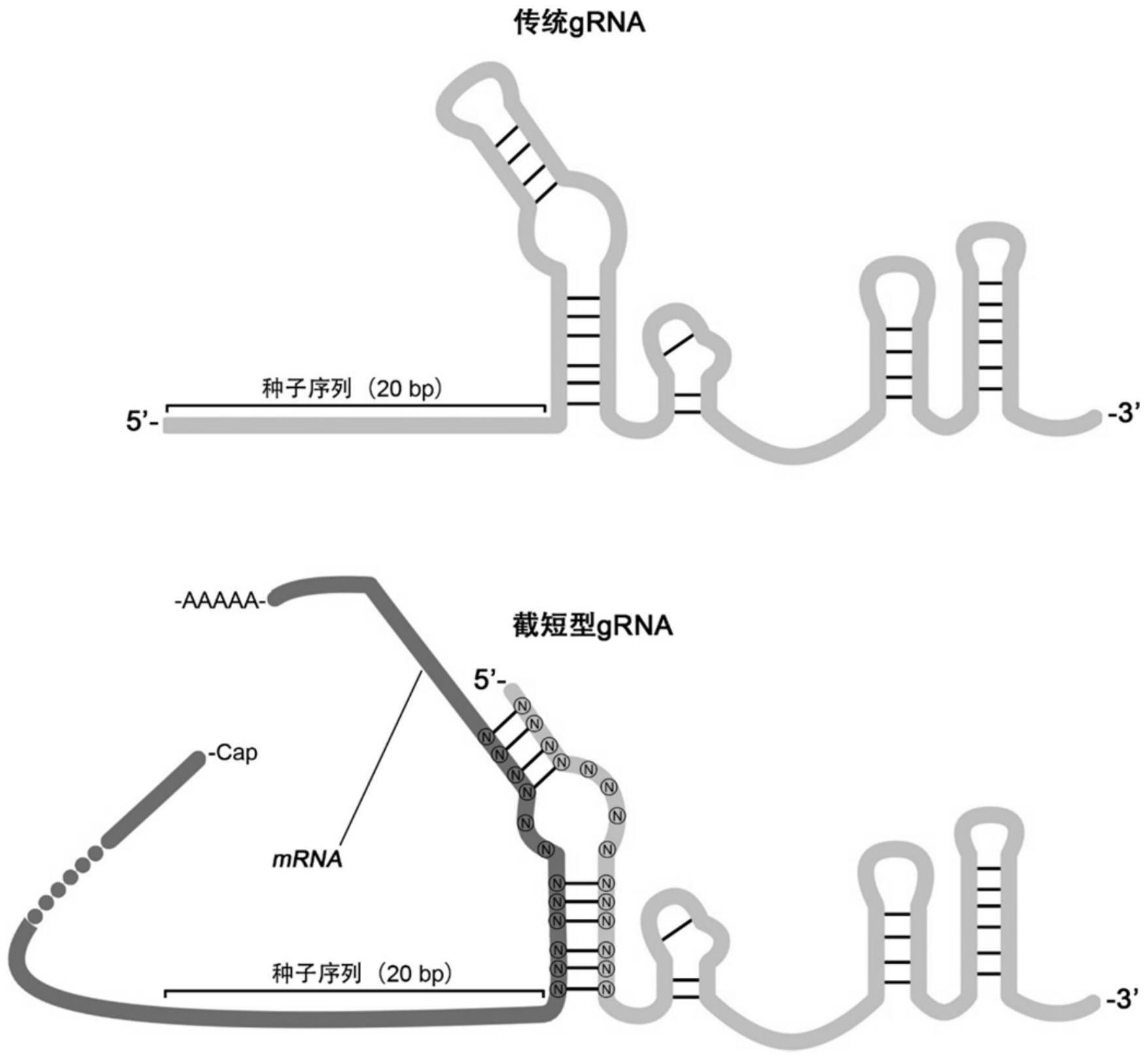
6、一种用于免疫细胞改造的截短型grna,所述截短型grna为改进型tracrrna,不含crrna,所述改进型tracrrna是将tracrrna 5’端原本识别crrna的区域序列,修改为靶标基因识别序列;所述改进型tracrrna在靶细胞内通过所述靶标基因识别序列与靶标基因的mrna相结合,在靶细胞内自组装,形成结构完整且具有引导功能的grna。
7、传统的grna引导的碱基编辑器可以有效造成grna识别区及毗邻区域的突变,但是grna与靶标识别主要依靠5′端的20bp引导序列,然而这20bp引导序列中仅有2bp的突变就会造成96%的grna引导功能丧失。
8、目前在真核细胞中普遍使用的grna是由原核生物表达的两段rna,即crrna和tracrrna通过gaaa四个核苷酸连接而成。本发明提供的用于免疫细胞改造的截短型grna,不再直接表达完整的grna序列,而是只表达grna的tracrrna部分(即截短型grna,简称grnaδ),并且将grnaδ的5′端与crrna相互补的序列(约14bp)修改为能够与基因指定区域右边的序列相互识别的序列。
9、当grnaδ与目标基因的mrna结合之后,真核细胞中也有相应的rna酶对grnaδ:mrna进行切割加工,最终得到完整的自组装grna,由于这种设计能够使grna的种子序列(seed region)始终来自于靶基因的待突变区,并且待突变区突变之后grna种子序列也能够相应的发生变化,从而使这种自组装grna始终靶向自身的种子序列来源区,并在靶基因待突变区产生持续的突变,从而实现靶基因的持续突变或建库。
10、本发明提供的上述改进型的grna表达策略,改进后的方案能够使基因指定区域产生持续突变,并且不会影响grna继续导向基因指定区域。上述自组装grna同时也体现出自靶向grna(self-targeting grna)的特点。
11、优选地,所述靶标基因为nkg2d受体胞外域基因,所述截短型grna的基因序列选自seq id no:1第248至393位、seq id no:2第248至393位、seq id no:3第248至393位中的一种或两种或三种。
12、优选地,所述靶标基因为nkg2d受体胞内区基因,所述截短型grna的基因序列选自seq id no:4第248至393位、seq id no:5第248至393位中的一种或两种。
13、针对多个靶标的同时改造,可实现靶基因位点的泛突变,从而进一步优化靶基因的建库或功能干扰效果。
14、一种用于免疫细胞改造的基因编辑系统,包括上述截短型grna以及碱基编辑器。
15、碱基编辑器在截短型grna或具有grna类似结构和引导功能的rna片段引导下,能够在grna所靶向的基因区域产生广泛的基因突变,最终导致相应基因功能的改变。利用上述基因编辑系统可建立大容量天然受体突变库,结合现有筛选技术,如磁珠分选、流式分选或高通量测序等,可通过一次建库筛选到靶向不同肿瘤抗原的天然受体突变体。
16、优选地,所述碱基编辑器选自第一碱基编辑器或第一碱基编辑器的突变体,所述第一碱基编辑器选自be3、abe7.10、abe8e、abe8s、ectada、mada、hadar2、hadat2、aid、apobec3g、apobec1、cda1中的一种或两种以上组合。
17、优选地,所述碱基编辑器的核苷酸序列如seq id no:6所示。
18、一种改造免疫细胞,其是利用上述基因编辑系统对免疫细胞进行改造得到。
19、利用上述基因编辑系统改造得到的改造免疫细胞,使被靶向的受体序列发生改变或其识别的配体发生转换,或者使被靶向的受体的胞内抑制性信号丧失功能。经过这种方法改造的免疫细胞能够有效识别肿瘤细胞,并且免疫细胞对肿瘤细胞的杀伤效果明显得到提升。
20、优选地,所述免疫细胞选自nk细胞、t细胞、nkt细胞、巨噬细胞、粒细胞、dc细胞中的一种。
21、进一步优选地,所述免疫细胞选自nk-92细胞并将所述nk-92细胞上nkg2d受体72位氨基酸由丙氨酸ala突变为苏氨酸thr。在改造nk-92细胞nkg2d受体的时候,我们还发现了nk-92细胞的nkg2d受体72位氨基酸是ala,nkg2d(72ala)会影响nkg2d受体在nk-92细胞上的表达量,以及减弱nk-92的杀伤效果。因此我们通过碱基编辑器使nkg2d(72ala)突变为nkg2d(72thr),可增强nk-92的抗肿瘤效果。并在此基础上进行nkg2d突变改造。
22、上述截短型grna、基因编辑系统、改造免疫细胞在制备肿瘤治疗试剂、建立免疫细胞文库中的应用。
23、利用本发明的上述方式,可方便建立大容量、多样性免疫细胞文库,更有利于获得所期望的免疫细胞性能。
24、利用本发明的上述方式,可克服现有car-t、car-nk、tcr-t及car-m等细胞治疗技术的不足,从而进一步优化肿瘤治疗效果。
技术特征:
1.一种用于免疫细胞改造的截短型grna,其特征在于,所述截短型grna为改进型tracrrna,不含crrna,所述改进型tracrrna是将tracrrna 5’端原本识别crrna的区域序列,修改为靶标基因识别序列;所述改进型tracrrna在靶细胞内通过所述靶标基因识别序列与靶标基因的mrna相结合,在靶细胞内自组装,形成结构完整且具有引导功能的grna。
2.如权利要求1所述的用于免疫细胞改造的截短型grna,其特征在于,所述靶标基因为nkg2d受体胞外域基因,所述截短型grna的基因序列选自seq id no:1第248至393位、seqid no:2第248至393位、seq id no:3第248至393位中的一种或两种或三种。
3.如权利要求1或2所述的用于免疫细胞改造的截短型grna,其特征在于,所述靶标基因为nkg2d受体胞内区基因,所述截短型grna的基因序列选自seq id no:4第248至393位、seq id no:5第248至393位中的一种或两种。
4.一种用于免疫细胞改造的基因编辑系统,其特征在于,包括权利要求1~3中任一项所述的截短型grna以及碱基编辑器。
5.如权利要求4所述的用于免疫细胞改造的基因编辑系统,其特征在于,所述碱基编辑器选自第一碱基编辑器或第一碱基编辑器的突变体,所述第一碱基编辑器选自be3、abe7.10、abe8e、abe8s、ectada、mada、hadar2、hadat2、aid、apobec3g、apobec1、cda1中的一种或两种以上组合。
6.如权利要求4所述的用于免疫细胞改造的基因编辑系统,其特征在于,所述碱基编辑器的核苷酸序列如seq id no:6所示。
7.一种改造免疫细胞,其特征在于,其是利用权利要求4~6中任一项所述的基因编辑系统对免疫细胞进行改造得到。
8.如权利要求7所述的改造免疫细胞,其特征在于,所述免疫细胞选自nk细胞、t细胞、nkt细胞、巨噬细胞、粒细胞、dc细胞中的一种。
9.如权利要求8所述的改造免疫细胞,其特征在于,所述免疫细胞选自nk-92细胞并将所述nk-92细胞上nkg2d受体72位氨基酸由丙氨酸ala突变为苏氨酸thr。
10.如权利要求1~3中任一项所述的截短型grna、权利要求4~6中任一项所述的基因编辑系统、权利要求7~9中任一项所述的改造免疫细胞在制备肿瘤治疗试剂、建立免疫细胞文库中的应用。
技术总结
本发明属于基因修饰领域,具体涉及一种用于免疫细胞改造的截短型gRNA、基因编辑系统、免疫细胞及应用。该截短型gRNA为改进型tracrRNA,不含crRNA,所述改进型tracrRNA是将tracrRNA 5’端原本识别crRNA的区域序列,修改为靶标基因识别序列;所述改进型tracrRNA在靶细胞内通过所述靶标基因识别序列与靶标基因的mRNA相结合,在靶细胞内自组装,形成结构完整且具有引导功能的gRNA。本发明提供的上述改进型的gRNA表达策略,改进后的方案能够使基因指定区域产生持续突变,并且不会影响gRNA继续导向基因指定区域。
技术研发人员:牛志远,郭长江,支灵通,朱武凌,罗志霞,孙朋洋,陈冠旭,靳心如,宁琳薇
受保护的技术使用者:新乡医学院
技术研发日:
技术公布日:2024/1/16
- 还没有人留言评论。精彩留言会获得点赞!